Эта заявка заявляет преимущество продолженной заявки US №60/556571, «Способы производства ксилита», зарегистрированной 26 марта 2004 года, которая включена сюда посредством ссылки во всей полноте.
Область техники, к которой относится изобретение
Настоящее изобретение относится к способам производства ксилита. В частности, изобретение предоставляет способы производства ксилита, включающие окислительное декарбоксилирование соединений.
Уровень техники
Ксилит является встречающимся в природе пятиуглеродным сладким спиртом, присутствующим во многих фруктах и овощах и продуцируемым в человеческом теле в ходе нормального метаболизма. Ксилит является также важным промышленным продуктом и широко применяется в производстве кондитерских изделий, включая бессахарную жевательную резинку, дыхательные пастилки и сухие твердые конфеты, а также в продуктах для профилактики заболеваний полости рта, продуктах для улучшения самочувствия, фармацевтических продуктах и т.п.
Определенные свойства ксилита делают его привлекательным подсластителем или заменителем сахара в различных случаях, особенно при производстве подслащенных продуктов питания. Например, ксилит нетоксичен и обладает приблизительно такой же сладостью, как сахароза, при меньшей энергетической ценности, составляющей около 2,4 ккал/г. Ксилит метаболизируется независимо от глюкозы и может без риска употребляться лицами с не-инсулиновым диабетом, обладает низким гликемическим индексом и, как показано, обладает антикетогенным действием при диабете. Кристаллы ксилита растворяются с поглощением тепла и создают ощущение прохлады при растворении во рту. Считается, что ксилит является кариостатиком и даже антикариогеном, и считается, что он не используется микрофлорой рта, производящей бляшки. Действительно, применение ксилита вместо сахарозы связывают с уменьшением кариеса зубов. В целом, ксилит является предпочитаемым подсластителем.
Ксилит обычно получают способами, применяющими различное природное сырье, особенно материалы, содержащие ксилан. Ксилит можно получать множеством способов, включая гидрирование ксилозы, полученной из гидролизата гемицеллюлозы (ксилана или арабиноксилана), как раскрыто в патентах US №№2989569, 3558725 и 4008285.
Каталитическое гидрирование D-ксилозы в гидролизатах гемицеллюлозы остается первостепенным промышленным источником ксилита. Промышленное производство D-ксилозы в первую очередь осуществляется посредством гидролиза гемицеллюлозы (ксиланов и арабиноксиланов). Однако многие из этих способов производства ксилита дороги и требуют много времени, и был предложен ряд альтернативных способов синтеза ксилита. Такие способы включают различные синтетические химические процессы, применение микроорганизмов и такие способы, как ферментация. Однако, несмотря на эти результаты, есть потребность производить ксилит таким способом, который отличается низкой стоимостью и выходом высокоочищенного продукта. Снижение количества отбросов (потерь) при его производстве также желательно. Ввиду расширения применения ксилита, в частности благодаря его свойствам как подсластителя и терапевтическим эффектам, имеется постоянная потребность в способах производства ксилита.
Раскрытие изобретения
Предоставлены способы производства ксилита, включающие окислительное декарбоксилирование реагента субстрата. Предпочтительно окислительное декарбоксилирование производят одним из двух способов. В первом осуществлении окислительное декарбоксилирование производят электрохимическим способом, предпочтительно, таким как анодное окислительное декарбоксилирование реагента субстрата. Во втором осуществлении окислительное декарбоксилирование реагента субстрата проводят посредством одной или более химических реакций.
Большое разнообразие реагентов субстратов можно применять для осуществления способов производства ксилита. Реагент субстрат может быть исходным материалом для реакции окислительного декарбоксилирования или может быть получен из любого подходящего материала предшественника. Предпочтительными материалами предшественника являются уроновые кислоты, включающие структуру фуранозного или пиранозного цикла. В некоторых аспектах осуществлений один или более материал предшественника может претерпевать одну или более химическую реакцию, такую как реакции окисления, реакции восстановления или реакции гидролиза для получения подходящего реагента субстрата.
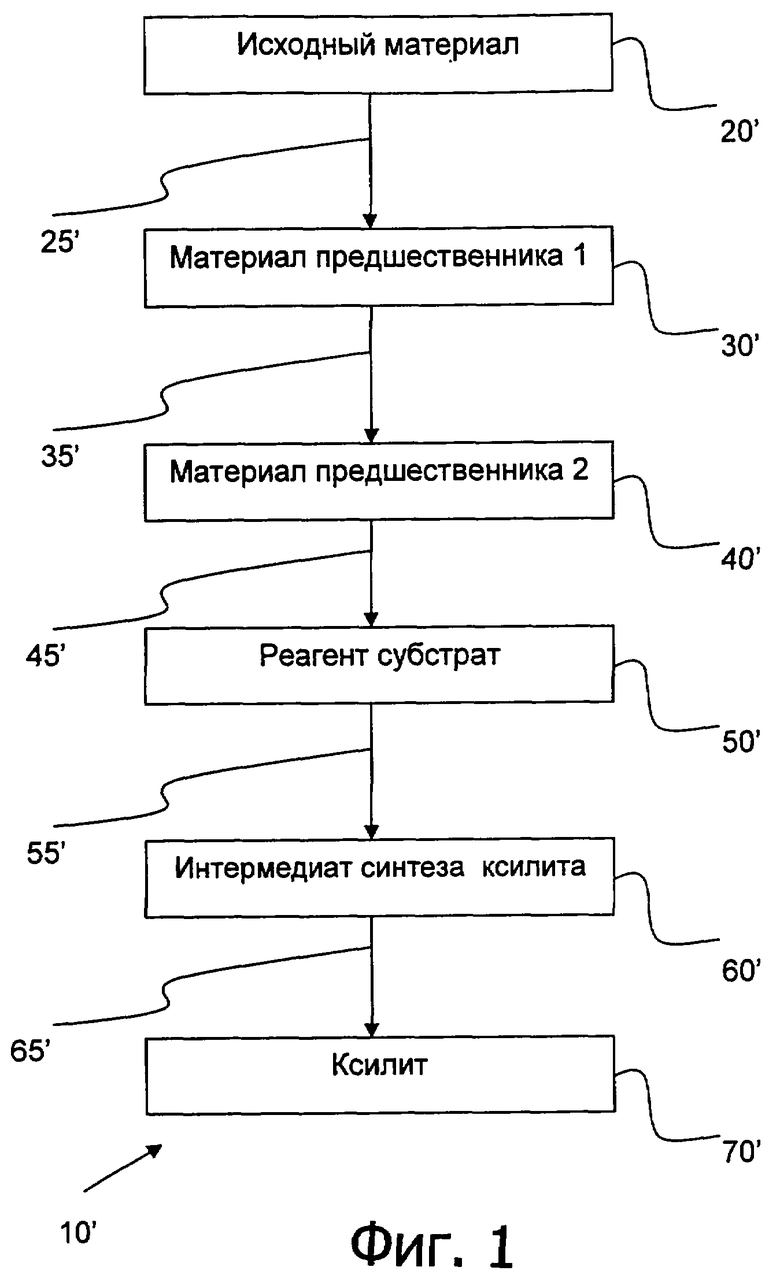
На фиг.1 показана основная реакционная схема 10' для производства ксилита по некоторым осуществлениям. Реакционная схема 10' включает этапы предоставления реагента субстрата 50', включающего звено уроновой кислоты, и окислительного декарбоксилирования реагента субстрата 55'. Подходящие реагенты субстраты включают содержащие уроновую кислоту реагенты субстраты, которые претерпевают нужную реакцию декарбоксилирования при определенных реакционных условиях. В одном осуществлении способ получения ксилита включает этапы предоставления реагента субстрата 50', включающего остаток уроновой кислоты и окислительное декарбоксилирование 55' реагента субстрата посредством электрохимического окислительного декарбоксилирования подходящего реагента субстрата. Предпочтительно реагент субстрат включает звено уроновой кислоты со структурой пиранозного или фуранозного цикла. В альтернативном осуществлении способ получения ксилита включает этапы предоставления реагента субстрата 50', включающего остаток уроновой кислоты, и окислительное декарбоксилирование 55' реагента субстрата посредством химического окислительного декарбоксилирования подходящего реагента субстрата. Предпочтительно реагент субстрат второго осуществления включает звено L-гулоновой кислоты.
На этапе 55' окислительного декарбоксилирования получается интермедиат синтеза ксилита соединение 60' или альтернативно получается ксилит или другое соединение, применимое для получения ксилита. Можно производить различные интермедиаты синтеза ксилита, и интермедиаты синтеза ксилита, полученные по первому осуществлению, могут быть такими же или отличаться от интермедиатов синтеза ксилита, произведенных способами второго осуществления. Реагентом субстратом может быть 50', предоставленный в качестве исходного материала, или он может быть получен из одного или более материалов предшественника.
На фиг.1 способ получения ксилита 10' далее включает этапы: предоставление исходного материала 20', химической модификации 25' исходного материала 20' для получения первого материала предшественника 30', химической модификации 35' первого предшествующего материала 30' для получения второго материала предшественника 40' и химической модификации 45' второго материала предшественника 40' для получения реагента субстрата 50'. Интермедиат синтеза ксилита 60' химически модифицируют 65' для производства продукта реакции, включающего ксилит 70'. Предпочтительно продукт реакции включает ксилит с выходом не менее 20% теоретического выхода ксилита. Химическая модификация исходного материала, материала предшественника или интермедиата синтеза ксилита может обозначать любую подходящую реакцию или серию реакций, которая модифицирует химическую структуру материала, включая реакции окисления, реакции восстановления, гидролиза или реакции конденсации.
В одном предпочтительном аспекте первого осуществления способ производства ксилита включает этап электрохимического окислительного декарбоксилирования реагента субстрата D-глюкуроновой кислоты, реагента субстрата D-фруктофуранозилуроновой кислоты или реагента субстрата L-гулоновой кислоты для производства интермедиата синтеза ксилита. Предпочтительно, способ включает этап окислительного декарбоксилирования реагента субстрата посредством анодного декарбоксилирования, где реагент субстрат выбирают из группы, состоящей из гликозида, олигосахарида, полисахарида, 1-фосфата или гликозил-фторида соли D-глюкуроновой кислоты. На этапе окислительного декарбоксилирования производится интермедиат синтеза ксилита. Интермедиат синтеза ксилита является, предпочтительно, диальдегидной или дикарбонильной структурой, которую, предпочтительно, далее восстанавливают с помощью катализатора гидрирования и газообразного водорода с выходом продукта, включающего ксилит.
В одном предпочтительном аспекте второго осуществления способ производства ксилита включает этап окислительного декарбоксилирования реагента субстрата D-глюкуроновой кислоты для получения диальдегидного интермедиата синтеза ксилита, такого как D-ксило-пент-1,5-диоза. Этап окислительного декарбоксилирования производит первый интермедиат синтеза ксилита, предпочтительно, диальдегидную или дикарбонильную структуру. В другом предпочтительном аспекте второго осуществления способ производства ксилита включает этап окислительного декарбоксилирования реагента субстрата L-гулоновой кислоты для получения интермедиата синтеза ксилита, такого как L-ксилоза, для получения второго интермедиата синтеза ксилита, предпочтительно, диальдегидной или дикарбоновой структуры. Предпочтительно, во всех аспектах второго осуществления интермедиаты синтеза ксилита далее химически модифицируют, например, посредством реакций восстановления/дегидрирования, для получения продукта реакции, включающего ксилит.
Краткое описание чертежей
На фигуре 1 показан основной реакционный процесс синтеза ксилита.
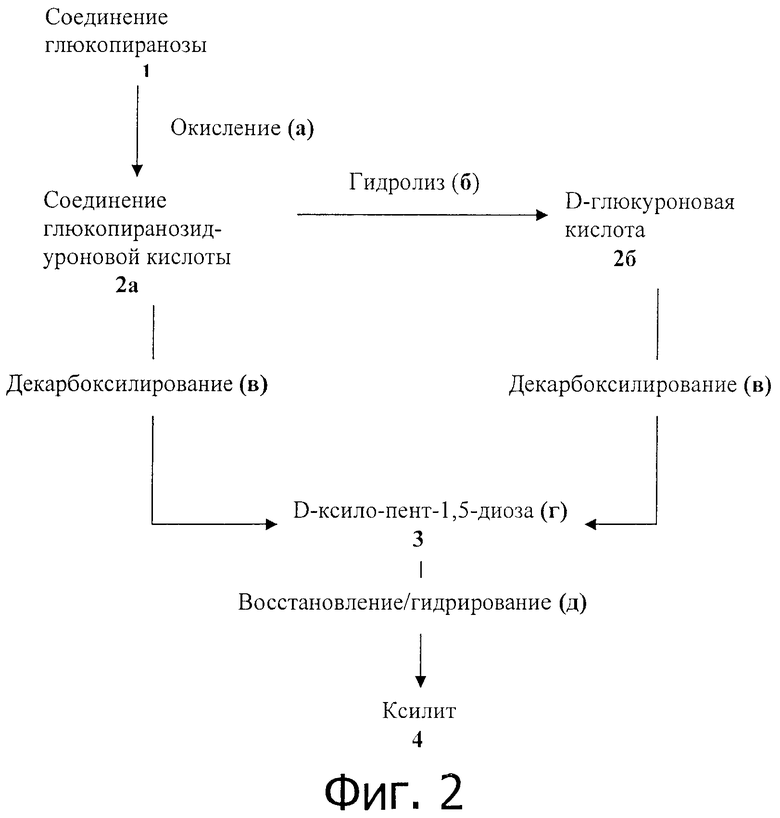
На фигуре 2 показаны два реакционные процесса синтеза ксилита, включающие электрохимическое окислительное декарбоксилирование.
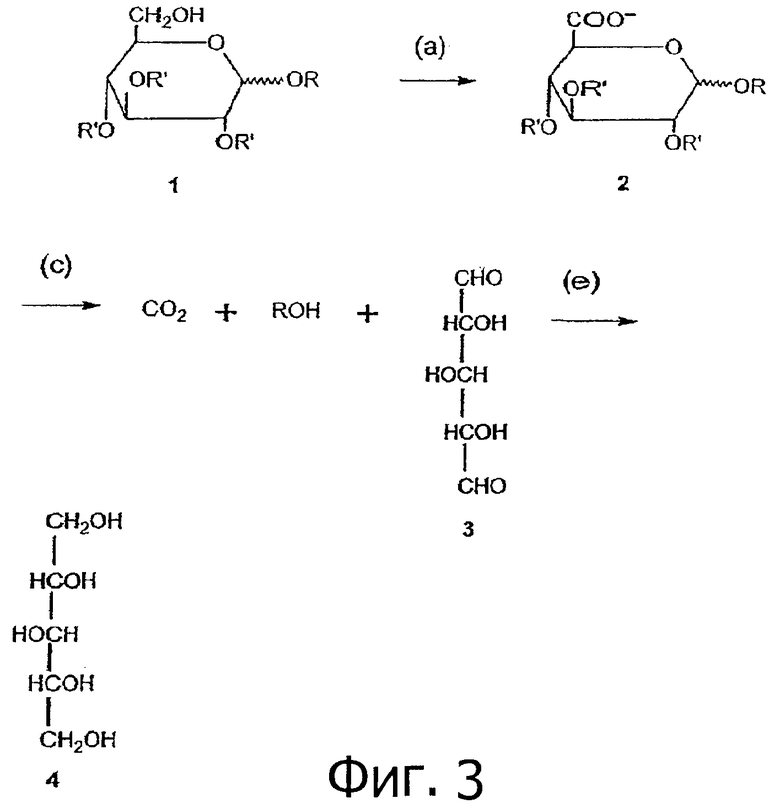
На фигуре 3 показана схема реакций по способу с фигуры 2.
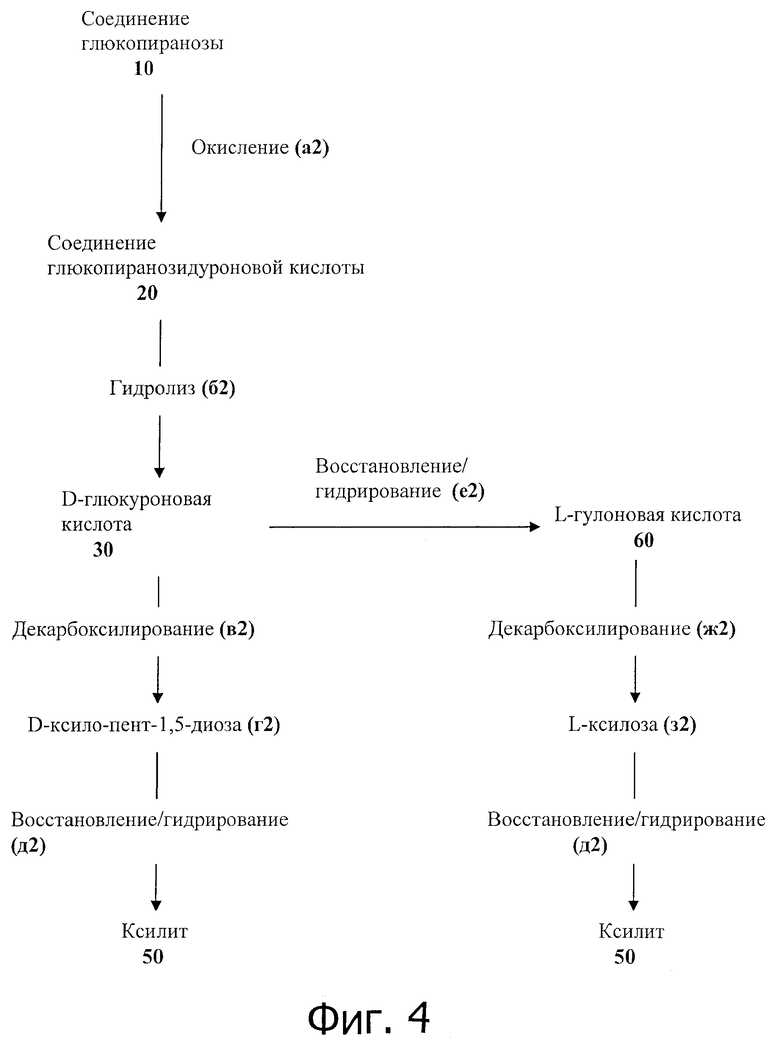
На фигуре 4 показаны два реакционные процесса синтеза ксилита, включающие процессы химического окислительного декарбоксилирования.
На фигуре 5 показана схема реакций по первому способу с фигуры 4.
На фигуре 6 показана схема реакций по второму способу с фигуры 4.
Осуществление изобретения
Термины «около, приблизительно» или «значительно», применимые по отношению к количеству, относятся к вариациям названного количества, которые равны названному количеству, например, количество, которое незначительно отличается от названного количества для той цели или функции, для которой оно предназначено. Вариация количества или взаимосвязь, модифицированная терминами «около» или «значительно», включают вариации на базе основных указаний, содержащихся в описанных и прочитанных рядовым специалистом в данной области техники.
Ссылки на «соединение D-фруктуронофуранозила (кислоты)» и «соединение D-глюкуронопиранозила (кислоты)», как применяется здесь, включает гликозиды, полимеры или олигомеры и производные и соли вышеперечисленных, если не оговорено другое.
Ссылка на «соединение D-глюкуроновой кислоты» как применяют здесь, включает гликозиды, их полимеры или олигомеры предпочтительно с защищенной восстановительной группой на конце и производные и соли вышеперечисленных.
Ссылка на «соединение глюкопиранозы», как применено здесь, включает гликозиды, полимеры или олигомеры α(альфа)-, β(бета)- и α,β(альфа, бета)-глюкопиранозы и производные и соли вышеперечисленных.
Ссылка на «соединение фруктофуранозы», как применено здесь, включает гликозиды, полимеры или олигомеры α(альфа)-, β(бета)- и α,β(альфа, бета)-фруктофуранозы и производные и соли вышеперечисленных.
Ссылка на «соединение глюкопиранозидуроновой кислоты», как применяют здесь, включает гликозиды, полимеры или олигомеры α(альфа)-, β(бета)- и α,β(альфа, бета)-глюкопиранозидуроновой кислоты и производные и соли вышеперечисленных.
Термин «исходный материал» относится к химическому веществу, которое исходно предоставляется в способе получения ксилита, до реакции окислительного декарбоксилирования. Исходный материал может быть химически модифицирован для получения материала предшественника или он может быть реагентом субстратом реакции окислительного декарбоксилирования.
Термин «материал предшественника» относится к продукту химической модификации исходного материала или продукту химической модификации другого материала предшественника.
Термин «реагент субстрат» относится к химическому веществу, которое претерпевает окислительное декарбоксилирование для получения интермедиата синтеза ксилита или продукта синтеза ксилита. В некоторых аспектах, исходный материал бывает также реагентом субстратом. «Реагент субстрат уроновая кислота» является реагентом субстратом, который включает не менее одного остатка уроновой кислоты.
Термин «соединение уроновой кислоты», как применяют здесь, относится к соединению, включающему уроновую кислоту, включая определенные гликозиды, их полимеры или олигомеры, а также их соответствующие соли. Соединение уроновой кислоты или производные и соли вышеперечисленных предпочтительно способны к превращению в диальдегидные интермедиаты синтеза ксилита или их производные и соли.
Синтез ксилита, включающий электрохимическое окислительное декарбоксилирование
В первом осуществлении, схематически представленном на фиг.2, способы получения ксилита включают этап окислительного декарбоксилирования, проводимый электрохимическим способом предпочтительно посредством окислительного декарбоксилирования реагента субстрата. Применение электрохимического декарбоксилирования при синтезе ксилита имеет много преимуществ. В частности, в процесс вовлечено мало химических реагентов и реакция способна быть весьма избирательной, так что часто проще очищать продукт. Более того, обычно очень мало отходов, пренебрежимое количество побочных продуктов и обычно расход реагентов минимален в процессе электрохимического декарбоксилирования.
Соединение глюкопиранозы (1) применяют в качестве исходного материала для обоих процессов, показанных на фиг.2, хотя любой исходный материал, который можно превратить в подходящий реагент субстрат, можно применять в качестве исходного материала или материала предшественника. Соединение глюкопиранозы (1) можно окислить (а) до соединения глюкопиранозидуроновой кислоты (2а) любым подходящим способом с окислительной реакцией для образования предпочтительного реагента субстрата. Исходный материал или материал предшественника могут включать любую D-глюкуронопиранозильную группу без замещения у кислорода в 6-ой позиции, или D-фруктуронофуранозильную группу без замещения у кислорода в цикле. Реагентом субстратом (2а) является предпочтительно соль D-глюкуроновой кислоты или ее гликозида, олигомера или полимера либо в виде природного материала, либо полученный в реакции окисления (а). Реагент субстрат (2а) при необходимости можно предоставлять в форме натриевой, калиевой, аммонийной, кальциевой и/или магниевой соли.
Реакцию окисления (а) материала предшественника (1) до реагента субстрата можно проводить способами, известными в данной области техники, включая, но не ограничиваясь этим, окисление воздухом/О2 на таком катализаторе, как платина, стабильные нитроксильные радикалы (например, TEMPO с регенерацией), окисление ионами переходных металлов с электрохимической регенерацией и электрохимически. Подходящие реакции окисления (а) для применения с целью окисления соединений D-глюкопиранозила до соединений D-глюкуронопиранозила описаны в следующих литературных источниках, которые включены сюда посредством ссылки во всей полноте: K.Heyns et al, "Selective catalytic oxidation of carbohydrates, employing platinum catalysts," Advances in Carbohydrate Chemistry and Biochemistry, 17, 169-221 (1962); Т.Yamada et al., Air oxidation of cyclodextrin with a platinum catalyst," Journal of Applied Glycoscience, 47, 21-26 (2006); P.L.Bragd et al., "Selective oxidation of carbohydrates by 4-AcNH-TEMPO/peracid systems," Carbohydrate Polymers, 49, 397-406 (2002); K.Yasuda et al., "The simultaneous use of immobilized reagents for the one-pot conversion of alcohols to carboxylic acids," Journal of the Chemical Society, Perkin Transactions, 1, 1024-1025 (2002).
D-глюкопиранозидуроновая кислота (2а) может применяться как реагент субстрат, который претерпевает электрохимическое декарбоксилирование (в) с образованием интермедиата синтеза ксилита (3). В противном случае глюкопиранозидуроновая кислота (2а) может применяться как материал предшественника, который претерпевает гидролиз (б) с образованием реагента субстрата D-глюкуроновой кислоты (2б). Гидролиз (б) соединения D-глюкопиранозидуроновой кислоты можно проводить, применяя α- и/или β-глюкуронозидазу (или смесь обеих) или кислоту при нагревании для освобождения D-глюкуроновой кислоты. Глюкуроновую кислоту можно отделять от любого неионного сахарида с помощью ионообменной хроматографии или электродиализа. В любом реакционном способе карбоксильная часть реагента субстрата (например, соединение глюкопиранозидуроновой кислоты (2а) или реагент субстрат D-глюкуроновая кислота (2б) претерпевает электрохимическое декарбоксилирование (в) с образованием интермедиата синтеза ксилита (3). Интермедиат синтеза ксилита, полученный обоими способами, показанный на фиг.2, включает D-ксило-пент-1,5-диозу (г). Предпочтительно интермедиат синтеза ксилита (3) является диальдегидным интермедиатом синтеза ксилита.
Подходящие реагенты субстраты для проведения этапа электрохимического окислительного декарбоксилирования (в) реагента субстрата предпочтительно содержат уроновую кислоту, которая предпочтительно находится в виде пиранозной или фуранозной циклической структуры. Реагент субстрат может быть углеводородной (органической, карбоновой) кислотой, такой как альдоновая или сахариновая кислота, хотя реагенты субстраты, включающие уроновую кислоту, предпочтительны. Точнее, реагент субстрат предпочтительно включает химическую часть, выбранную из группы, состоящей из гликозида, олигосахарида, полисахарида, 1-фосфата или гликозил-фторида соли D-глюкуроновой кислоты и D-фруктуронофуранозила (кислоты). Примеры предпочтительных реагентов субстратов показаны на фиг.2 как соединение глюкопиранозидуроновой кислоты (2а) или соединение D-глюкуроновой кислоты (2б).
Этап окислительного декарбоксилирования реагента субстрата (в) предпочтительно проводят с помощью электрохимического окислительного декарбоксилирования реагента субстрата. Реагент субстрат находится предпочтительно в своей ионизованной форме (например, соль) либо в виде свободного соединения, либо связанного через гликозидную связь со спиртом или другой молекулой. Подходящей реакцией окислительного декарбоксилирования (в) для получения интермедиата синтеза ксилита (3) является реакция окислительного декарбоксилирования, такая как реакция Хофера-Места (Hofer, Moest, Annalen, 1902, 828, 284). Реакция Хофера-Места описана, например, у Kruis, Schanzer, Z. physikal. Chem., 1942, 191, A, 301, Neuberg (Biochemische Zeitschrift 7 (1908) 537). Декарбоксилирование D-глюконовой кислоты до D-арабинозы было исследовано как экономически важная реакция и были разработаны проточные реакторы с постоянным потоком. Следующие литературные источники включены сюда посредством ссылки во всей полноте: Pergola et al., Electrochimica Acta 39 (1994) 1415; Pezzatini et al., Electroanalysis 4 (1992) 129; Vallieres and Matlosz, J. Electrochem. Society 146 (1999) 2933.
Аппарат (установка) для декарбоксилирования реагента субстрата предпочтительно включает электрохимическую ячейку. Реакцию анодного окислительного декарбоксилирования (в) можно проводить с помощью электрохимической ячейки. Анод электрохимической ячейки можно изготовить из любого подходящего материала, но предпочтительно из спектрально-чистого графита, пиролитического углерода, графита, пропитанного воском, стекловидного углерода, диспергированного графита, диспергированного углеродного материала, углеродной ткани, кокса или платины в виде упакованной основы (bed), разжиженной основы или пористого анода. Патент US №950366, включенный посредством ссылки во всей полноте, раскрывает установку для декарбоксилирования D-глюконовой кислоты с выходом D-арабинозы, которую можно применять для проведения реакции окислительного декарбоксилирования (в). Электрохимическая ячейка предпочтительно включает анод электрохимической ячейки, где, как считается, происходит реакция окислительного декарбоксилирования (в). Площадь поверхности анода предпочтительно большая и может быть изготовлена из многих углеродных материалов, платины или других металлов. Контакт между исходным материалом и анодом вызывает декарбоксилирование, которое приводит к освобождению двуокиси углерода и образованию интермедиата синтеза ксилита (3). Предпочтительно электрохимическая ячейка далее включает катод, так что внутри электрохимической ячейки может проходить реакция.
Считается, что электрохимическое окислительное декарбоксилирование имеет место, когда раствор, включающий реагент субстрат, контактирует с анодом электрохимической ячейки, к которой приложен потенциал. Не вдаваясь в теорию, можно сказать, что окислительное декарбоксилирование соединения глюкопиранозидуроновой кислоты приводит к образованию карбокатиона (иона карбония) у углерода 5, который стабилизируется в виде иона карбоксония (включая атом кислорода цикла). Добавление иона гидроксила или молекулы воды к такому интермедиату может образовывать полуацеталь, который в водном окружении раскрывается, образуя альдегид (углерод 5) и полуацеталь при углероде 1. Последний распадается до альдегида, образуя диальдегид.
Другие примеры способов электрохимического окисления описаны в следующих источниках, которые включены сюда посредством ссылки во всей полноте: Schuurman et al., Studies in Surface Science and Catalysis, 72 (1992) 43; Applied Catalysis A: General 89 (1992) 31, 47 и ссылки в нем; P.L.Bragd, A.C.Besemer, H. van Bekkum, Carbohydrate Polymers 49 (2002) 397-406); Matsuoka et al., Fuel Cells 2 (2002) 35.
Осуществление электрохимического декарбоксилирования (в) реагента субстрата, такого как глюкопиранозидуроновая кислота (2а) или D-глюкуроновая кислота (2б), дает интермедиат синтеза ксилита (3), такой как D-ксило-пент-1,5-диоза (г). Одна или более последующая химическая модификация интермедиата синтеза ксилита (3), такая как реакция восстановления-гидрирования (д), приводит к смеси продуктов, включающей ксилит (4). Неионный интермедиат синтеза ксилита (3) можно отделять от непрореагировавшего исходного материала (2), например, посредством анионообменной хроматографии или электродиализа. Восстановление интермедиата синтеза ксилита (3) можно проводить любым подходящим способом, известным в уровне техники, включая, но не ограничиваясь этим каталитическое гидрирование. Эффективные катализаторы включают рутений и никель. В частности, можно применять рутениевый катализатор на носителе и никель Рэнея. В одном аспекте интермедиат синтеза ксилит (3) можно восстанавливать водородом с рутением (патентная заявка WO №2004052813, включенная сюда полностью посредством ссылки), никелем (патент US №4008285, включенный сюда полностью посредством ссылки) или с другим известным катализатором гидрирования для получения ксилита (4). Гидрирование обычно проводят при температурах между приблизительно 70°С и приблизительно 150°С и давлении Н2 между приблизительно 0,1 и приблизительно 10 МПа. В противоположность этому можно применять электрохимическое восстановление (Taylor, Chemical and Metallurgical Engineering, v.44 (1937) 588, включенная сюда полностью посредством ссылки). Восстановление интермедиата, полученного декарбоксилированием D-фруктуронофуранозила (кислоты), дает смесь ксилита и D-арабинитола. Ксилит можно собрать с помощью кристаллизации (De Faveri et al., J. Food Engineering 61 (2004) 407, включенная сюда посредством ссылки полностью).
На фиг.3 приведена детальная схема химических реакций для различных химических соединений, которые можно применять в способах производства ксилита по реакционным схемам на фиг.2. Исходный материал или материал предшественника (1) может быть любым подходящим соединением, которое можно химически изменить с образованием реагента субстрата (2), который претерпевает электрохимическое окислительное декарбоксилирование (в). Как отмечалось выше, подходящий исходный материал или материал предшественника может включать любую D-глюкуронопиранозильную группу или D-фруктуронофуранозильную группу без замещения у кислорода в 6-ой позиции. Исходный материал (1) или материал предшественника (если приложимо), который превращается в реагент субстрат, является предпочтительно солью D-глюкуроновой кислоты (1 на фиг.2) или гликозидом, олигомером или полимером вышеперечисленных либо природного происхождения, либо полученный посредством окисления. Двумя примерами подходящих природных материалов, применимых в качестве материала предшественника или исходного материала, являются глюуоран (gluuoran) и глюкуронан (полимер глюкуроновой кислоты природного происхождения). Другие подходящие соединения исходного материала (1) включают глюкозиды (R = алкильная или арильная группа), соединения с остатками D-глюкопиранозила, соединенными гликозидной связью, такие как мальто- или целлюло-олиго- или полисахариды (R и/или одна из R' групп = остаток D-глюкопиранозила, другая R' группа = Н), D-глюкопиранозил-фосфат (R = фосфат), D-глюкопиранозил-фторид (OR=F) или сахароза (R = остаток D-фруктофуранозила). Исходный материал (1) может иметь либо альфа-, либо бета-конфигурацию при атоме углерода номер 1. С другой стороны, олиго- или полисахариды, включающие остатки D-фруктофуранозила, соединенные по типу 2,1, могут также служить исходным материалом. В другом аспекте соль соединения, содержащего D-фруктофуранозил или его олигомер или полимер с 2,1-связями, полученный окислением фруктана с 2,1-связями или полученных из него олигомеров также может служить реагентом субстратом в последовательности реакций.
На фиг.3 исходный материал (1) переводят в подходящий реагент субстрат (2), как описано выше относительно реакционных схем на фиг.2. У реагента субстрата (2) агликон гликозида (R) является предпочтительно химическим звеном, выбранным из группы, состоящей из алкильного или арильного спирта, сахара и остатка глюкопирануронозила (олиго- или полиглюкуроновой кислоты) или подобной защитной группе у углерода 1 остатка глюкуронопиранозила. Оставшиеся этапы схемы химических реакций на фиг.3, включая окислительное декарбоксилирование (в) для получения соединения интермедиата синтеза ксилита (3) и реакция гидрирования (д) для получения продукта ксилита (4), проводят, как описано в реакционных схемах, показанных на фиг.2. Предпочтительно реагент субстрат является уроновой кислотой и интермедиат синтеза ксилита (3) является диальдегидным интермедиатом синтеза ксилита.
В первом предпочтительном аспекте первого осуществления способ производства ксилита включает следующие этапы: предоставление исходного материала, содержащего D-глюкопиранозил, окисление исходного материала, содержащего D-глюкопиранозил, любым подходящим способом для образования реагента субстрата, включающего остаток D-глюкуронопиранозила, электрохимическое декарбоксилирование реагента субстрата, включающего остаток D-глюкуронопиранозила, для образования интермедиата синтеза ксилита; восстановление и гидрирование интермедиата синтеза ксилита любым подходящим способом для производства ксилита. Предпочтительно окислительное декарбоксилирование проводят посредством анодного электрохимического процесса. Также предпочтительно, чтобы интермедиат синтеза ксилита был неионным соединением. В одном аспекте интермедиат ксилита является D-ксило-пент-1,5-диозой.
В другом предпочтительном аспекте первого осуществления способ получения ксилита включает следующие этапы: предоставление исходного материала, содержащего D-глюкопиранозил, окисление исходного материала, содержащего D-глюкопиранозил, любым подходящим способом для образования материала предшественника, включающего остаток D-глюкуронопиранозила, гидролиз материала предшественника, включающего остаток D-глюкуронопиранозила, любым подходящим способом для образования реагента субстрата, включающего остаток D-глюкуроновой кислоты, электрохимическое декарбоксилирование реагента субстрата, содержащего остаток D-глюкуроновой кислоты, с образованием интермедиата синтеза ксилита; восстановление и гидрирование интермедиата синтеза ксилита любым подходящим способом для производства ксилита. Предпочтительно, окислительное декарбоксилирование проводят посредством анодного электрохимического процесса. Также предпочтительно, чтобы интермедиат синтеза ксилита был неионным соединением. В одном аспекте интермедиат ксилита является D-ксило-пент-1,5-диозой.
В третьем предпочтительном аспекте первого осуществления способ получения ксилита включает следующие этапы: предоставление исходного материала, содержащего D-фруктуронофуранозил без замещения по кислороду в шестой позиции, окисление исходного материала, содержащего D-фруктофуранозил, любым подходящим способом для образования реагента субстрата, включающего остаток D-фруктуронофуранозила, гидролиз материала предшественника, включающего остаток D-фруктуронофуранозила, и окислительное декарбоксилирование материала предшественника, содержащего остаток D-фруктуронофуранозила, для производства ксилита. Предпочтительно окислительное декарбоксилирование проводят посредством анодного электрохимического процесса.
В то время как предпочтительные аспекты первого осуществления представлены по отношению к частным молекулярным структурам, многие другие реагенты субстраты, материалы предшественника и исходные материалы также рассматриваются. Например, электрохимическое окислительное декарбоксилирование можно приложить к любому соединению, включающему остаток уроновой кислоты для производства других материалов предшественника. Остатки D-фруктофуранозилуроната, соединенные по типу 2,1, такие как можно получить посредством окисления первичной спиртовой группы (углерод-6 инулина, инулиновых олигосахаридов или других фруктанов с 2,1-связями) таким же образом, что окисляют соединения, содержащие остатки D-глюкопиранозила, могут претерпевать такие же фундаментальные (основные) последовательности реакций, ведущие к карбокации (иону карбония) фурана. Последующее добавление гидроксила и раскрытие цикла и освобождение дают интермедиат, который можно восстановить до смеси ксилита и L-арабинитола. Изомеризация L-арабинитола приводит к смеси эпимеров алдитола, среди которых имеется ксилит (патенты US №№5714602 и 6458570, оба из которых включены сюда посредством ссылки). Ксилит можно также получать биохимически из других пентитолов (патент ЕР №421882, патенты US №№6303353 и 6340582, патент Японии №2004024140).
В одном аспекте первого осуществления способ получения ксилита включает следующие этапы: предоставление исходного материала, содержащего D-фруктуронофуранозил без замещения по кислороду в 6-ой позиции, окисление исходного материала, содержащего D-фруктуронофуранозил, любым подходящим способом для образования соединения D-фруктуронофуранозила, декарбоксилирование материала предшественника с получением интермедиата синтеза ксилита и D-арабинитола и восстановление предшественника ксилита для получения ксилита вместе с D-арабинитолом. Предпочтительно окислительное декарбоксилирование проводят посредством анодного электрохимического процесса.
Синтез ксилита, включающий химическое окислительное декарбоксилирование
Во втором осуществлении, показанном схематически на фиг.4, процессы получения ксилита включают этап окислительного декарбоксилирования, проводимого посредством одной или более химической реакции. Можно применять различные химические реакции для проведения окислительного декарбоксилирования реагента субстрата по второму осуществлению.
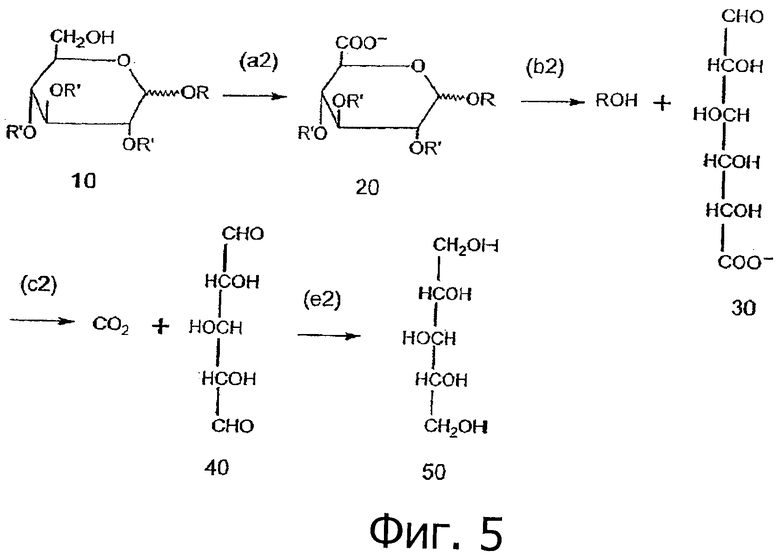
Способы получения ксилита, включающие применение химических реакций для проведения этапа декарбоксилирования, схематически показаны на фиг.4. Фиг.4 представляет два альтернативные процесса производства ксилита второго осуществления. В первом аспекте ксилит производят из реагента субстрата D-глюкуроновой кислоты (30), который претерпевает химическое декарбоксилирование (в2). Во втором аспекте ксилит получают из реагента субстрата L-гулоновой кислоты (60), который претерпевает химическое декарбоксилирование (ж2) с образованием интермедиата синтеза ксилита. Полученный интермедиат синтеза ксилита зависит от того, какой реагент субстрат применяли. В первом аспекте в качестве интермедиата синтеза ксилита (40) производят D-ксило-пент-1,5-диозу (г2). Во втором аспекте в качестве интермедиата синтеза ксилита (70) получают L-ксилозу (з2). Интермедиаты синтеза ксилита (40), (70) можно восстанавливать реакцией гидрирования (д2).
Любой подходящий исходный материал можно превращать в реагент субстрат, который может применяться в качестве реагента субстрата или материала предшественника. Соединение глюкопиранозы (10) показано как исходный материал для процессов на фиг.4. Исходный материал можно окислять (а2) до соединения глюкопиранозидуроновой кислоты (20) посредством любой подходящей окислительной реакции, как описано относительно способов синтеза ксилита первого осуществления, для образования материала предшественника или реагента субстрата. Реакция окисления (а2) материала предшественника (10) до материала предшественника глюкопиранозидуроновой кислоты (20) можно осуществлять способами, известными в данной области техники, включая, но не ограничиваясь этим окисление воздухом/О2 на катализаторе, таком как платина, устойчивые радикалы нитроксила (например, TEMPO с регенерацией) окисление ионами переходных металлов с электрохимической регенерацией и электрохимически. Подходящие реакции окисления (а2) для применения при окислении соединений D-глюкопиранозила до остатков D-глюкуронопиранозила описаны в следующих источниках, которые включены сюда посредством ссылки во всей полноте: К.Heyns et al, "Selective catalytic oxidation of carbohydrates, employing platinum catalysts," Advances in Carbohydrate Chemistry and Biochemistry, 17, 169-221 (1962); Т.Yamada et al., Air oxidation of cyclodextrin with a platinum catalyst," Journal of Applied Glycoscience, 47, 21-26 (2006); P.L.Bragd et al., "Selective oxidation of carbohydrates by 4-AcNH-TEMPO/peracid systems," Carbohydrate Polymers, 49, 397-406 (2002); K.Yasuda et al., "The simultaneous use of immobilized reagents for the one-pot conversion of alcohols to carboxylic acids," Journal of the Chemical Society, Perkin Transactions, 1, 1024-1025 (2002).
Глюкопиранозидуроновая кислота (20) может применяться как материал предшественника, который можно превращать в реагент субстрат или другой материал предшественника. Глюкопиранозидуроновую кислоту (20) можно переводить в D-глюкуроновую кислоту (30) посредством гидролиза (62) материала предшественника глюкопиранозидуроновой кислоты (20). Гидролиз (62) материала предшественника глюкопиранозидуроновой кислоты (20) можно проводить любым пригодным способом, как например, с помощью фермента, такого как α- и/или β-глюкуронозидаза, или с помощью кислоты при нагревании. Глюкуроновую кислоту (30) можно отделять от неионных сахаридов с помощью ионообменной хроматографии.
D-глюкуроновая кислота (30) может служить реагентом субстратом и претерпевать химическое декарбоксилирование (в2). В противном случае D-глюкуроновая кислота (30) предпочтительно служит материалом предшественника, который далее восстанавливают (е2) посредством подходящей реакции дегидрирования с образованием реагента субстрата L-гулоновой кислоты (60). Реагент субстрат D-глюкуроновую кислоту (30) можно восстановить способом, известным в данной области техники. Подходящие реакции гидрирования включают применение водорода и катализатора гидрирования, например, как описано выше для восстановления (д2) интермедиата синтеза ксилита (4) на фиг.2.
Реагент субстрат D-гулоновая кислота (30) может претерпевать соответствующий тип химического окислительного декарбоксилирования (в2) с выходом первого интермедиата синтеза ксилита (40) D-ксило-пент-1,5-диозы (г2). Сходным образом реагент субстрат L-гулоновая кислота (60) может претерпевать любой подходящий тип окислительного декарбоксилирования (ж2) с выходом второго интермедиата синтеза ксилита (д2) (L-ксилозы). Реакции окислительного декарбоксилирования обычно приводят к освобождению двуокиси углерода и образованию интермедиатов синтеза ксилита, таких как D-ксило-пент-1,5-диоза (г2) или L-ксилоза (ж2). Эти неионные интермедиаты синтеза ксилита (40) и (70) можно отделить от непрореагировавшего исходного материала с помощью анионообменной хроматографии.
Окислительное декарбоксилирование (в2) (ж2) можно проводить с реагентом субстратом (30), применяя различные химические реакции. Примеры подходящих способов окислительного декарбоксилирования включают, не ограничиваясь этим, один или более из следующих: применение иона переходного металла как катализатора с первичным окисляющим агентом, применение гипохлорита/хлорноватистой кислоты, фотохимические реакции Гофера-Места и применение надкритической воды.
В одном аспекте химическое окислительное декарбоксилирование проводят с применением гипохлорита/хлорноватистой кислоты. Предпочтительно химическое окислительное декарбоксилирование проводят с реагентом субстратом, включающим α-гидрокси кислоту, таким как D-глюкуроновая кислота или L-гулоновая кислота. Амиды сахарных кислот также можно декарбоксилировать гипохлоритом (деградация Хоффмана). Деградацию Хоффмана также можно применять для декарбоксилирования глюкуронозидов. Дальнейшие детали по окислительному декарбоксилированию углеводородов с применением гипохлорита/хлорноватистой кислоты находятся у R.L.Whistler et al., "Preparation of D-arabinose and D-glucose with hypochlorite", J. Amer. Chem. Soc., 81, 46397 (1981), которая включена сюда посредством ссылки.
Химическое окислительное декарбоксилирование можно также проводить с применением надкритической воды, например, как описано у V.DiTullio et al., "Supercritical water refining of petroleum residues and simultaneous hydrolysis-decarboxylation of waste glycerides, fats and proteins", PCT International Application Publication No. WO 2002/74881 (Int'l filing date September 26, 2002) (Chemical Abstracts 137, 265376 (2002)), которая включена сюда посредством ссылки полностью.
В другом аспекте химическое окислительное декарбоксилирование проводят с применением в качестве катализаторов ионов переходных металлов, таких как: Fe(III), Cu(II), Ru(III), Co(II), Mn (III), Ag(I), Bi(III)/Bi(0) и их комплексов с первичными окисляющими агентами, такими как перекись водорода, гипохлорит, гипохлорит/бромид, гипобромит, двуокись хлора, кислород, озон, пероксинитрит, персульфат или бром для регенерации катализатора.
Предпочтительно способ производства ксилита включает проведение окислительного декарбоксилирования с применением в качестве катализатора ионов переходного металла меди, такого как Cu(II), в сочетании с подходящим первичным окислителем. Например, можно проводить деградацию по Руффу, предпочтительно применяя ионы меди, а не железа для деградации по Руффу кислых сахаров. Декарбоксилирование с помощью Cu(I)/кислорода алифатических и (α)-гидроксикислот в органических растворителях может применяться в одном аспекте. В другом аспекте соли Cu(III) и йодной кислоты (периодат) и теллуровой кислоты (теллурат) можно применять для декарбоксилирования (α)-гидроксикислот с выходом альдегидов и кетонов. Деградация по Руффу описана у W.Pigman et al., "The Carbohydrates", АР, New-York, 2nd Ed., v. IA (1972), v. IB (1980), части которой, относящиеся к окислительному декарбоксилированию углеводородов, включены сюда посредством ссылки.
Химическое окислительное декарбоксилирование можно также проводить с применением катализатора Ru(III) в сочетании с подходящим первичным окислителем, описанным выше, например, как описано в Y.R.Rao et al., "Kinetics of ruthenium (III)-catalyzed oxidative decarboxylation of some aliphatic acids by cerie sulfate", Proc. Natl. Symposium on Catalysis, 4th, 341-346 (Chemical Abstracts 94, 46397 (1981)), которая включена сюда посредством ссылки.
Альтернативно химическое окислительное декарбоксилирование можно проводить с применением соединения Ce(IV), например, декарбоксилирование D-глюконовой кислоты с выходом D-арабинозы. Ацетат свинца(IV) также можно применять в реакциях декарбоксилирования, например, для избирательного расщепления глюкуронозидных связей, как известно в данной области техники.
Различные подходящие ионы переходных металлов можно применять для декарбоксилирования (α)-гидроксикислот, следуя механизму декарбоксилирования по Гоферу-Месту. Например, реакции химического декарбоксилирования могут быть также реакциями декарбоксилирования в стиле Колбе/Гофер-Места, проводимых с применением одного или более из следующих: Pb(IV), Ag(II), Mn(III), Co(III), Ce(IV) или Th(III). Другие примеры включают применение одного или более соединений, включающих ионы Ni(II) или Ti(IV) в деградации по Руффу. Другие соединения, применимые для окислительного декарбоксилирования, включают соединения, включающие одно или более из следующих: Au(III), Pt(IV), Ir(IV), Ag(II) и Hg(II), как известно в данной области техники. Для декарбоксилирования соединений пиранозы предпочтительные способы окислительного декарбоксилирования включают способы деградации Хоффмана и способы, включающие применение соединений, содержащих Pb(TV).
Фотохимические варианты реакции Гофера-Места также можно применять для окислительного декарбоксилирования. Фотоокислительные варианты реакции задействуют окись титана (к которой могут добавляться Fe, Cu, Ag или другие ионы металлов) или железо(III)-порфириновые комплексы. Дальнейшие детали этих способов фотохимического окислительного декарбоксилирования находятся в следующих источниках, которые включены сюда полностью: J.M.Hermann et al, "Photocatalytic degradation of aqueous hydroxyl-butandioic acid (malic acid) in contact with powdered and support titania in water," Catalysis Today, 54, 131-141 (1999); P.Hanson et al., "The mechanisms of the photo-decarboxylation of alkyl-and arylmethyl-carboxylates using visible light and iron (III) tetra(2-N-methylphyridyl) porphrin pentachloride in aqueous solution," Journal of the Chemical Society, Perkin Transactions, 2, 2653-2568 (1998).
Обратимся опять к фиг.4, где первый интермедиат синтеза ксилита (40), показанный как D-ксило-пент-1,5-диоза (г2), или второй интермедиат синтеза ксилита (70), показанный как L-ксилоза (з2), можно восстановить (д2) с помощью водорода и катализатора гидрирования для получения ксилита (50). Восстановление (д2) можно проводить с помощью любой подходящей реакции, такой как рутениевый или никелевый катализ. Например, восстановление (д2) может быть реакцией гидрирования, проведенной с водородом и рутением (см. патентную заявку WO №2004052813, включенную сюда посредством ссылки), никеля (патент US №4008285, включенную сюда посредством ссылки) или другие катализаторы гидрирования, известные в области техники, для получения ксилита (50). В одном аспекте гидрирование можно проводить при температурах между 70°С и 150°С и при давлении между 0,1 и 10 МПа H2. Альтернативно, можно применять электрохимическое восстановление (Taylor, Chemical and Metallurgical Engineering, v.44 (1937) 588, которая включена сюда посредством ссылки). В одном аспекте интермедиат синтеза ксилита (40) D-ксило-пент-1,5-диозу (г2) и/или интермедиат синтеза ксилита (70) L-ксилозу (ж2) можно восстанавливать водородом и рутением.
После восстановления (ж2) ксилит (50) можно получить из конечного продукта кристаллизацией, например, как описано у De Faveri et al., J. Food Engineering 61 (2004) 407, которая включена сюда посредством ссылки полностью. L-ксилозу (70) можно отделить от непрореагировавших солей L-гулоновой кислоты с помощью анионообменной хроматографии. Ксилит можно отделить от L-гулоновой и D-глюкуроновой кислот любым пригодным способом, включая ионообменную хроматографию. В одном особенно предпочтительном аспекте L-гулоновую кислоту в ионизованной солевой форме окисляют с выходом L-ксилозы и декарбоксилируют D-глюкуроновую кислоту с выходом диальдегида, причем оба эти продукта можно восстановить для получения ксилита.
На фиг.5 представлена последовательность реакций, описанных на фиг.4, когда исходным материалом (10) является звено α-D-глюкопиранозила, связанное гликозидной связью, или родственные соединения и реагентом субстратом является D-глюкуроновая кислота (30). На фиг.5 исходный материал (10) окисляется (а2) до материала предшественника (20) (например, соединения глюкопиранозидуроновой кислоты), который гидролизуется (62) до реагента субстрата D-глюкуроновой кислоты (30). Химическое окислительное декарбоксилирование (в2) реагента субстрата D-глюкуроновой кислоты (30) приводит к интермедиату синтеза ксилита диальдегиду (40), который можно восстановить до ксилита (50). Предпочтительно интермедиат синтеза ксилита (40) является диальдегидом.
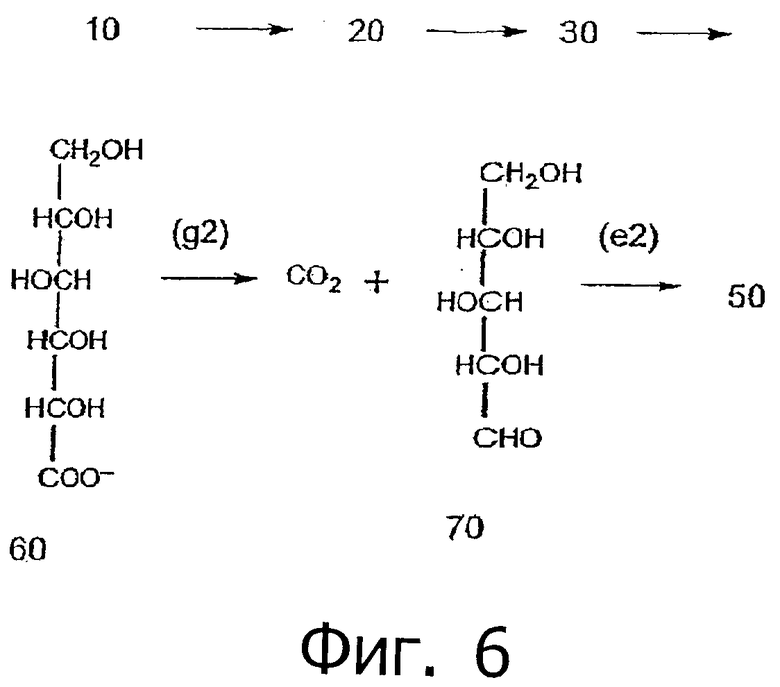
Фиг.6 представляет последовательность реакций фиг.4, когда соединение D-глюкуроновой кислоты (30) является материалом предшественника, который восстанавливается (е2) до L-гулоновой кислоты (60). L-гулоновая кислота (60) претерпевает декарбоксилирование для получения интермедиата синтеза ксилита L- ксилозы (70), которую можно восстановить (д2) до ксилита (50).
Предпочтительно соединение D-глюкуроновой кислоты (30) является солью, включающей натриевую, калиевую, аммонийную, кальциевую и/или магниевую соли олиго- или поли(глюкуроновой кислоты) (степень полимеризации 2 или выше). Точнее, соединение D-глюкуроновой кислоты (30) может быть солью D-глюкуроновой кислоты, алкилом или арилом D-глюкуронопиранозида, D-глюкуронопиранозил-1-фосфата и глюкуронопиранозил-фторида. Реагент субстрат (30) также может быть соединением D-фруктуронофуранозила, при необходимости, включающим натриевую, калиевую, аммонийную, кальциевую и/или магниевую соли окисленного инулина или другого фруктана со связью 2,1. Соль L-гулоновой кислоты (60) предпочтительно включает не менее одной группы, состоящей из натриевой, калиевой, аммонийной, кальциевой и/или магниевой соли L-гулоновой кислоты.
Со ссылкой на фиг.5 и 6, исходный материал (10) или материал предшественника могут быть соединением, которое включает глюкозиды (R= алкильная или арильная группа), другие соединения с остатками D-глюкопираноза, соединенные гликозидными связями, такие как мальто- или целлюло-олиго- или полисахариды (R и/или одна из R' групп = α-D-глюкопиранозил, другая R' группа = Н), D-глюкопиранозил-фосфат (R= фосфат), D-глюкопиранозил-фторид (OR=F) или сахароза (R=звено D-фруктофуранозила). Гидроксиалкильная группа (OR) у первого углерода исходного материала (10) может находиться либо в α-, либо в β-конфигурации. При необходимости исходный материал (10) может быть природным глюкуронаном или сахарозой, окисленной для включения остатка D-глюкуроновой кислоты. Исходный материал может быть также получен окислением алкил-глюкозида, D-глюкозо-1-фосфата или D-глюкопиранозил-фторида до соответствующего соединения, содержащего D-глюкуроновую кислоту; крахмала, декстрина, мальтодекстрина или других производных крахмала до соединений, включающих множественные остатки D-глюкуроновой кислоты, окислением целлюлозы или целлодекстрина до соединений, включающих множественные остатки D-глюкуроновой кислоты; сахарозы с получением остатка глюкуроновой кислоты. Исходный материал может быть также глюкуронаном естественного происхождения.
Реагент субстрат (20) на фиг.5 является предпочтительно D-глюкуроновой кислотой или гликозидом, олигомером или полимером вышеперечисленных или родственным соединением либо в виде природного материала, либо полученным с помощью окисления. Реагент субстрат (60) на фиг.6 является предпочтительно соединением L-гулоновой кислоты. Интермедиат синтеза ксилита (40) на фиг.5 (после окислительного декарбоксилирования D-глюкуроновой кислоты и гликозидов или родственных им соединений) или интермедиат синтеза ксилита (60) на фиг.6 (после окислительного декарбоксилирования D-глюкуроновой кислоты) можно восстановить (д2) с выходом ксилита (50). Восстановление (д2) можно проводить любым пригодным способом, включая таковые, описанные в отношении этапа (д) восстановления интермедиата синтеза ксилита на фиг.2 первого осуществления.
В одном аспекте второго осуществления способ получения ксилита включает следующие этапы: предоставление исходного материала, содержащего D-глюкопиранозил, окисление исходного материала, содержащего D-глюкопиранозил, любым пригодным способом для образования материала первого предшественника, включающего звено D-глюкуронопиранозила, гидролиз первого материала предшественника любым подходящим способом для образования второго материала предшественника, включающего D-глюкуроновую кислоту, восстановление и гидрирование второго материала предшественника любым подходящим способом с образованием реагента субстрата, включающего L-гулоновую кислоту, окислительное декарбоксилирование реагента субстрата, включающего L-гулоновую кислоту, для получения интермедиата синтеза ксилита, восстановление и гидрирование интермедиата синтеза ксилита любым подходящим способом для производства ксилита. Предпочтительно интермедиатом синтеза ксилита является L-ксилоза.
Альтернативный аспект второго осуществления предоставляет способ получения ксилита, включающий следующие этапы: предоставление исходного материала, содержащего D-глюкопиранозил, окисление исходного материала, содержащего D-глюкопиранозил, любым пригодным способом для образования материала предшественника, включающего звено D-глюкуронопиранозила, гидролиз материала предшественника, включающего звено D-глюкуронопиранозила, любым подходящим способом для образования реагента субстрата, включающего D-глюкуроновую кислоту, окислительное декарбоксилирование реагента субстрата, включающего D-глюкуроновую кислоту, для получения интермедиата синтеза ксилита, восстановление и гидрирование интермедиата синтеза ксилита любым подходящим способом для производства ксилита. В этом аспекте интермедиатом синтеза ксилита обычно является D-ксило-пент-1,5-диоза.
Другой аспект второго осуществления предоставляет способ получения ксилита, включающий следующие этапы: предоставление исходного материала, содержащего D-глюкопиранозил, окисление исходного материала, содержащего D-глюкопиранозил, любым пригодным способом для образования материала предшественника, включающего звено D-глюкопиранозидуроновой кислоты, гидролиз материала предшественника, включающего звено D-глюкопиранозидуроновой кислоты, любым подходящим способом для образования реагента субстрата, включающего D-глюкуроновую кислоту, окислительное декарбоксилирование реагента субстрата, включающего D-глюкуроновую кислоту, для получения интермедиата синтеза ксилита, восстановление и гидрирование интермедиата синтеза ксилита любым подходящим способом для производства ксилита. В этом аспекте интермедиатом обычно является D-ксило-пент-1,5-диоза.
Способы производства ксилита дают выход приблизительно 20, 30, 40, 50, 60, 70, 80, 85, 90, 95 или до 100% от теоретического выхода, более предпочтительно, не менее приблизительно 40%, не менее приблизительно 60%, не менее приблизительно 80% или предпочтительно не менее приблизительно 95% теоретического выхода.
Предпочтительно также, что способы производства ксилита потребляют не менее приблизительно 20, 30, 40, 50, 60, 70, 80, 85, 90, 95 или до 100% исходного материала в молярном отношении и более предпочтительно, потребляют не менее приблизительно 50%, не менее приблизительно 60%, не менее приблизительно 70%, не менее приблизительно 80%, не менее приблизительно 90%, не менее приблизительно 95% или более исходного материала в молярном отношении. В некоторых осуществлениях непрореагировавший исходный материал используют заново посредством применения непрореагировавшего исходного материала в качестве исходного материала для новой реакции, материала предшественника или реагента субстрата.
Иллюстративные сочетания аспектов осуществлений описаны ниже. В отношении способов синтеза ксилита первого осуществления особенно предпочтительно электрохимическое окислительное декарбоксилирование реагента субстрата, включающего структуру пиранозного или фуранозного цикла. В одном аспекте реагенты субстраты окислительного декарбоксилирования являются соединениями, включающими D-глюкуронопиранозильную группу без химического замещения у кислорода в 6-ой позиции пиранозного цикла. В другом аспекте реагенты субстраты для окислительного декарбоксилирования являются веществами, включающими D-фруктуронофуранозильную группу без химического замещения у кислорода фуранозильного цикла. В отношении способов синтеза ксилита второго осуществления предпочтительны реакции, включающие этапы гидролиза соединения, включающего D-глюкуронопиранозильное звено, освобождающие свободную D-глюкуроновую кислоту и последующее восстановление до L-гулоновой кислоты. Восстановление с ионами металлов в качестве катализаторов, особенно меди (например, деградация по Руффу), предпочтительно для восстановления D-глюкуроновой кислоты в L-гулоновую кислоту. Несколько отдельных иллюстративных сочетаний аспектов первого и второго осуществления приведены ниже.
В первом иллюстративном аспекте способ производства ксилита включает один или более из следующих этапов:
а) декарбоксилирование D-глюкуронового соединения электрохимически для получения диальдегида как интермедиата синтеза ксилита,
б) гидрирование интермедиата синтеза ксилита в присутствии катализатора для производства ксилита,
в) при необходимости отделение интермедиата синтеза ксилита от непрореагировавшей соли уроновой кислоты или гликозида, их олигомеров или полимеров и родственных соединений,
г) при необходимости повторное использование любого непрореагировавшего исходного материала на этапе а).
Во втором иллюстративном аспекте способ производства ксилита включает один или более из следующих этапов:
а) декарбоксилирование соли D-фруктуронофуранозильной кислоты или гликозида, его олигомера или полимера электрохимически для получения дикарбонильного интермедиата синтеза ксилита,
б) гидрирование интермедиата синтеза ксилита в присутствии катализатора для получения смеси ксилита и D-арабинитола,
в) при необходимости отделение интермедиата от непрореагировавшей соли D-фруктуронофуранозильной кислоты или гликозида, их олигомеров или полимеров; или
г) при необходимости далее включающий повторное использование оставшегося исходного материала на этапе а).
В третьем иллюстративном аспекте способ производства ксилита включает один или более из следующих этапов:
а) декарбоксилирование соли D-гулоновой кислоты электрохимически для получения L-ксилозы,
б) гидрирование L-ксилозы в присутствии катализатора для производства ксилита,
в) при необходимости отделение L-ксилозы или ксилита от непрореагировавшей соли L-гулоновой кислоты,
г) при необходимости повторное использование любого непрореагировавшего исходного материала на этапе а).
В четвертом иллюстративном аспекте способ производства ксилита включает этап растворения соли уроновой кислоты или ее гликозида в подходящем смешивающемся с водой растворителе, таком как вода, метанол, этанол, диоксан или ацетонитрил.
В пятом иллюстративном аспекте способ производства ксилита включает этап электрохимического декарбоксилирования. Предпочтительно окислительное декарбоксилирование происходит внутри электрохимической ячейки на аноде. Более предпочтительно анод включает спектрально чистый графит, пиролитический углерод, графит, пропитанный воском, стекловидный углерод, диспергированный графит, диспергированные углеродные материалы, углеродная ткань, кокс или платина в виде упакованной основы, разжиженной основы или пористого анода. Предпочтительно также, что реакция восстановления происходит на катоде в электрохимической ячейке.
В шестом иллюстративном аспекте способ получения ксилита включает этап каталитического гидрирования/восстановления, при необходимости проводимый с применением рутения, никеля Рэнея или других катализаторов гидрирования.
В седьмом иллюстративном аспекте способ получения ксилита включает один или более из следующих этапов:
а) восстановление D-глюкуроновой кислоты до L-гулоновой кислоты,
б) декарбоксилирование соли L-гулоновой кислоты для получения L-ксилозы,
в) гидрирование L-ксилозы в присутствии катализатора гидрирования для производства ксилита, при необходимости применяя рутений, никель или другие катализаторы гидрирования,
г) при необходимости отделение L-ксилозы от непрореагировавшей L-гулоновой кислоты; или
д) при необходимости повторное использование L-гулоната на этапе б).
L-Гулоновая кислота при необходимости может предоставляться в форме натриевой, калиевой, аммонийной, кальциевой и/или магниевой соли.
В восьмом иллюстративном аспекте способ производства ксилита включает проведение этапа химического окислительного декарбоксилирования одним или более из следующих путей:
а) применение катализа ионами переходных металлов, такими как: Fe(III), Cu(II), Ru(III), Co(II), Mn(III), Ag(I) или Bi(III)/Bi(0);
б) применение комплексов переходных металлов;
в) применение первичного окислителя, такого как перекись водорода, гипохлорит/хлорноватистая кислота, гипобромит/бромноватистая кислота, гипохлорит/бромид, двуокись хлора, кислород/воздух, озон, пероксинитрит или персульфат;
г) применение фотоокислительного декарбоксилирования, совершаемого с окисью титана, двуокисью титана с добавлением (присадкой) Fe, Cu, Ag или других ионов металлов, или окиси титана с присадкой из комплекса Fe(III)-порфирин или других комплексов с ионами металлов; или
д) применение гипохлорита/хлорноватистой кислоты или гипобромита/бромноватистой кислоты.
В девятом иллюстративном аспекте способ производства ксилита включает проведение одного или более из следующих этапов:
а) гидролиз соединения, содержащего звено D-глюкуроновой кислоты,
б) декарбоксилирование соли D-глюкуроновой кислоты для получения диальдегидного интермедиата синтеза ксилита, и
в) гидрирование интермедиата синтеза ксилита в присутствии катализатора для производства ксилита,
г) при необходимости отделение интермедиата синтеза ксилита от непрореагировавшей соли уроновой кислоты,
д) при необходимости повторное использование оставшегося исходного материала на этапе б).
ПРИМЕРЫ
Следующие примеры только иллюстративны и их не следует понимать как ограничивающие, поскольку дальнейшие модификации раскрытых осуществлений будут очевидны для специалистов в данной области техники ввиду данных указаний. Все эти модификации считаются охваченными областью приложения осуществлений, раскрытых здесь.
Пример 1:
Электрохимическое декарбоксилирование соли D-глюкуроната моногидрата для получения ксилита
Глюкуронат натрия одноводный (2,69 г, 0,0115 моль) растворяют в 43 мл смеси метанол/вода (46,2 вес.%). Раствор подвергают электролизу в односекционной ячейке с графитовым анодом при постоянном напряжении 9,99 В течение 4,31 ватт-часов. Раствор электролита затем доводят до 110 мл смесью этанол/вода (50%) и гидрируют посредством добавления никеля Рэнея и пропускания газа водорода при 1 атм при 50°С. Получающийся гидрированный сироп содержит 0,87 г ксилита (50% от теоретического выхода) и 1,10 г L-гулоната натрия (42% исходного материала в молярном отношении).
Теоретический выход или «% от теоретического выхода» рассчитывают следующим образом:
Во-первых, определяют следующие молекулярные веса:
а) D-глюкуронат натрия моногидрат 235
б) метил-β-D-глюкуронат натрия 231
в) L-гулонат натрия 219
г) ксилит 152
Далее производят расчет следующим образом: 2,69 г исходного материала составляет 0,0114 моля и теоретический выход ксилита составляет 0,0114×152, т.е. 1,74 г. Реальный выход составляет 0,87 г, что составляет 50% теоретического выхода.
Пример 2:
Электрохимическое декарбоксилирование соли алкил-β-D-глюкуронозида для получения ксилита
Метил-β-D-глюкуронозид натрия (2,52 г, 0,0103 моль) растворяют в 39 мл воды. Раствор подвергают электролизу в односекционной ячейке с графитовым анодом при постоянном напряжении 9,99 вольт в течение 8,49 ватт-часов. Раствор электролита затем доводят до 110 мл смесью этанол/вода (50%) и гидрируют посредством добавления никеля Рэнея и пропускания газа водорода при 1 атм при 50°С. Получающийся гидрированный сироп содержит 0,70 г ксилита (42% от теоретического выхода).
Пример 3:
Электрохимическое декарбоксилирование соли L-гулоната для получения ксилита
L-гулонат натрия (2,67 г, 0,01222 моль) растворяют в 43 мл смеси метанол-вода (46,2 вес.%). Раствор подвергают электролизу в односекционной ячейке с графитовым анодом при постоянном напряжении 9,99 В в течение 5,32 ватт-часов. Раствор электролита затем доводят до 110 мл смесью этанол/вода (50%) и гидрируют посредством добавления никеля Рэнея и пропускания газа водорода при 1 атм при 50°С. Получающийся гидрированный сироп содержит 0,87 г ксилита (47% от теоретического выхода) и 1,10 г L-гулоната натрия (41% исходного материала, в молярном отношении).
Пример 4:
Cu(II) - декарбоксилирование соли L-гулоната для получения ксилита
L-Гулонат натрия (2,25 г, 0,0100 моль) растворяют в 17 мл воды и добавляют 35 мг сульфата меди пятиводного. рН раствора поднимают до 7,0 с помощью гидроокиси натрия (2М). По ходу реакции постоянно добавляют 1,2 мл 30%-ной перекиси водорода. Значение рН поддерживают при 7,0, добавляя гидроокись натрия (2М). Через 13 мин температура составляет 44°С и медь выпадает в осадок в виде оранжевой суспензии. Реакционный раствор фильтруют и затем доводят до 110 мл 50%-ой смесью этанол/вода, и гидрируют посредством добавления никеля Рэнея и пропускания газа водорода при 1 атм при 50°С. Получающийся гидрированный сироп содержит 0,91 г ксилита (58% от теоретического выхода) и 0,72 г L-гулоната натрия (32% исходного материала в молярном отношении).
Пример 5:
Декарбоксилирование соли L-гулоната с помощью хлорноватистой кислоты для получения ксилита
L-гулонат натрия (0,244 г, 1,12×10-3 моль) растворяют в 15 мл воды и поднимают температуру до 50°С. Добавляют 1,5 мл 13%-ного раствора гипохлорита натрия. Добавляют 2М хлорноватистую кислоту для понижения рН до 5,0. Реакцию держат при 50°С и поддерживают рН при 5,0, добавляя 2М гидроокись натрия. Через 19 мин реакционную смесь доводят до 110 мл 50%-ой смесью этанол/вода и гидрируют посредством добавления никеля Рэнея и пропускания газа водорода при 1 атм при 50°С. Получающийся гидрированный сироп содержит 0,16 г ксилита (95% от теоретического выхода) и 0,004 г L-гулоната натрия (2% исходного материала в молярном отношении).
Поскольку описаны различные осуществления изобретения, для рядовых специалистов в данной области техники будет очевидно, что другие осуществления и реализации возможны внутри области приложения изобретения. Соответственно изобретение ограничено только областью притязаний, отраженных в формуле изобретения, и их эквивалентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ОДНОВРЕМЕННОГО ЭЛЕКТРОЛИТИЧЕСКОГО ДЕКАРБОКСИЛИРОВАНИЯ И ВОССТАНОВЛЕНИЯ САХАРОВ | 2014 |
|
RU2694908C2 |
| СПОСОБЫ ЭЛЕКТРОЛИТИЧЕСКОГО ДЕКАРБОКСИЛИРОВАНИЯ САХАРОВ | 2014 |
|
RU2686850C2 |
| СПОСОБЫ ЭЛЕКТРОЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ЭРИТРОЗЫ ИЛИ ЭРИТРИТОЛА | 2006 |
|
RU2433211C2 |
| ЭПИМЕРИЗОВАННЫЕ ПРОИЗВОДНЫЕ ПОЛИСАХАРИДА К5 С ВЫСОКОЙ СТЕПЕНЬЮ СУЛЬФАТИРОВАНИЯ | 2003 |
|
RU2333222C2 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-3-АМИНОМЕТИЛ-5-МЕТИЛГЕКСАНОВОЙ КИСЛОТЫ (ПРЕГАБАЛИНА) | 2013 |
|
RU2544859C1 |
| СПОСОБ ПОЛУЧЕНИЯ КСИЛИТА | 1993 |
|
RU2142999C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАЦЕМИЧЕСКОГО НЕБИВОЛОЛА | 2006 |
|
RU2392277C2 |
| КОМПОЗИЦИЯ СВЯЗУЮЩЕГО НА ОСНОВЕ ОЛИГОМЕРНЫХ СЛОЖНЫХ ЭФИРОВ, ЕЕ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ ДЛЯ СВЯЗЫВАНИЯ ОРГАНИЧЕСКИХ ИЛИ МИНЕРАЛЬНЫХ ВОЛОКОН | 2019 |
|
RU2789703C2 |
| НОВЫЕ ПЕНТАСАХАРИДЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1999 |
|
RU2193040C2 |
| УРОНОВАЯ КИСЛОТА И ПРОБИОТИКИ | 2006 |
|
RU2419445C2 |
Настоящее изобретение относится к вариантам способа получения ксилита, который широко применяется в производстве кондитерских изделий, а также в продуктах для профилактики заболевания полости рта, продуктах для улучшения самочувствия, фармацевтических продуктах и т.п. Один из вариантов способа включает электрохимическое окислительное декарбоксилирование соединения уроновой кислоты, включающее фуранозный или пиранозный цикл для получения интермедиата синтеза ксилита и гидрирование интермедиата синтеза ксилита для получения ксилита. Еще один из вариантов способа включает гидролиз соединения D-глюкуроновой кислоты, декарбоксилирование соединения D-глюкуроновой кислоты для получения диальдегидного интермедиата синтеза ксилита и гидрирование интермедиата синтеза ксилита в присутствии катализатора гидрирования для получения ксилита. Предлагаемое изобретение позволяет экономичным способом получить ксилит с высоким выходом при минимальном количестве потерь. 9 н. и 11 з.п. ф-лы, 6 ил.
1. Способ производства ксилита, включающий этапы:
а) электрохимическое окислительное декарбоксилирование соединения уроновой кислоты для получения интермедиата синтеза ксилита и
б) гидрирование интермедиата синтеза ксилита для получения ксилита.
2. Способ по п.1, где соединение уроновой кислоты включает фуранозный или пиранозный цикл.
3. Способ производства ксилита, включающий этапы:
а) восстановление D-глюкуроновой кислоты до L-гулоновой кислоты,
б) электрохимическое окислительное декарбоксилирование L-гулоновой кислоты для получения L-ксилозы и
в) гидрирование L-ксилозы для получения ксилита.
4. Способ по п.3, дополнительно включающий этап повторного применения оставшейся L-гулоновой кислоты.
5. Способ получения ксилита, включающий следующие этапы:
а) гидролиз соединения D-глюкуроновой кислоты,
б) декарбоксилирование соединения D-глюкуроновой кислоты для получения диальдегидного интермедиата синтеза ксилита,
в) гидрирование интермедиата синтеза ксилита в присутствии катализатора гидрирования для получения ксилита.
6. Способ по п.5, дополнительно включающий этап отделения интермедиата синтеза ксилита от непрореагировавшего соединения D-глюкуроновой кислоты.
7. Способ получения ксилита, включающий этапы:
а) предоставление материала, содержащего D-глюкопиранозил,
б) окисление материала, содержащего D-глюкопиранозил, с образованием материала предшественника, содержащего звено D-глюкуронопиранозила,
в) гидролиз материала предшественника, содержащего звено D-глюкуронопиранозила, для образования реагента субстрата, содержащего D-глюкуроновую кислоту,
г) окислительное декарбоксилирование реагента субстрата, включающего D-глюкуроновую кислоту, для получения интермедиата синтеза ксилита и
д) восстановление/гидрирование интермедиата синтеза ксилита для получения ксилита.
8. Способ получения ксилита, включающий этапы:
а) предоставление материала, содержащего D-фруктуронофуранозил, незамещенный по позиции кислорода цикла,
б) окисление материала, содержащего D-фруктуронофуранозил, с образованием материала предшественника, включающего звено D-фруктуронофуранозила,
в) гидролиз материала предшественника, содержащего звено D-фруктуронофуранозила, и
г) электрохимическое окислительное декарбоксилирование материала предшественника, содержащего звено D-фруктуронофуранозила, для получения ксилита.
9. Способ получения ксилита, включающий этапы:
а) электрохимическое декарбоксилирование соединения D-глюкуроновой кислоты для получения интермедиата синтеза ксилита и
б) гидрирование интермедиата синтеза ксилита в присутствии катализатора для получения ксилита.
10. Способ по п.9, дополнительно включающий этап отделения интермедиата синтеза ксилита от непрореагировавшего соединения D-глюкуроновой кислоты.
11. Способ по п.9, дополнительно включающий этапы: повторное применение непрореагировавшего соединения D-глюкуроновой кислоты и электрохимическое декарбоксилирование непрореагировавшего соединения D-глюкуроновой кислоты.
12. Способ производства ксилита, включающий этапы:
а) электрохимическое декарбоксилирование соединения уроновой кислоты для получения дикарбонильного интермедиата синтеза ксилита и
б) гидрирование дикарбонильного интермедиата синтеза ксилита в присутствии катализатора.
13. Способ по п.12, дополнительно включающий отделение интермедиата синтеза ксилита от непрореагировавшего соединения уроновой кислоты.
14. Способ по п.13, дополнительно включающий этап повторного применения оставшегося соединения уроновой кислоты.
15. Способ получения ксилита, включающий этапы:
а) электрохимическое декарбоксилирование соли L-гулоновой кислоты для получения L -ксилозы и
б) гидрирование L-ксилозы в присутствии катализатора для получения ксилита.
16. Способ по п.15, дополнительно включающий этап отделения L-ксилозы от непрореагировавшей соли L-гулоновой кислоты.
17. Способ по п.15, дополнительно включающий повторное использование любой непрореагировавшей соли L-гулоновой кислоты.
18. Способ по п.1, где соединение уроновой кислоты растворено в смешивающемся с водой растворителе, выбранном из группы, состоящей из воды, метанола, этанола, диоксана и ацетонитрила.
19. Способ получения ксилита, включающий этапы:
а) предоставление исходного материала, содержащего D-глюкопиранозил,
б) окисление исходного материала, содержащего D-глюкопиранозил, с образованием материала предшественника, включающего звено D-глюкопиранозила,
в) электрохимическое декарбоксилирование материала предшественника, содержащего звено D- глюкопиранозила, для получения предшественника ксилита,
г) восстановление/гидрогенирование предшественника ксилита для получения ксилита.
20. Способ по п.19, в котором исходный материал, содержащий D-глюкопиранозил, содержит алкокси-группу на С-1 углероде.
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| US 5714602 A, 03.02.1998 | |||
| US 4066711 A, 03.01.1978 | |||
| US 4075406 A, 21.02.1978 | |||
| US 3784408 A, 08.01.1974 | |||
| СПОСОБ ПОЛУЧЕНИЯ КСИЛИТА | 1997 |
|
RU2176996C2 |
Авторы
Даты
2010-05-10—Публикация
2005-03-25—Подача