ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к новому соединению K04-0144, в т.ч. к любому из соединений K04-0144A, K04-0144B и K04-0144C, которые демонстрируют противомикробное действие в отношении различных бактерий, включая метициллин-устойчивые Staphylococcus aureus (MRSA), а также к соединению K04-0144D, которое демонстрирует увеличение анти-MRSA активности в комбинации с β-лактамовыми антибиотиками, и, кроме того, к способу получения указанных соединений.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Staphylococcus aureus являются индигенными грам-положительными бактериями, живущими на различных поверхностях организма, например на коже и поверхности желудочно-кишечного тракта человека и животных, и безвредны для здоровых людей, но в случае нарушения иммунитета, как например у пациентов после хирургической операции, новорожденных детей и стариков, эти микроорганизмы вызывают различные тяжелые инфекционные заболевания от инфекций мягких тканей кожи, например, гнойных состояний, сопровождающих резаные раны или проникающие раны, до пневмонии, перитонита, сепсиса, менингита и, кроме того, пищевого отравления, шокового синдрома и энтерита, вызванного энтеротоксином и токсином-1 синдрома токсического шока. Указанные заболевания являются тяжелыми заболеваниями, которыми не следует пренебрегать, и в худшем случае они могут явитьсяпричиной смерти. В последнее время метициллин-устойчивый Staphylococcus aureus (MRSA) признан социальной проблемой, вследствие того, что он является микроорганизмом, вызывающим инфекции в больницах. Данный патогенный микроорганизм устойчив к различным лекарственным средствам, таким как β-лактамовые антибиотики, вследствие чего в настоящее время для лечения инфекций MRSA применяют ванкомицин, т.е. антибиотик гликопептидного ряда, и арбекацин, т.е. антибиотик аминогликозидного ряда. Известны другие антибиотики, разработанные в последнее время, как например, смесь хинупристин-далфопристин и оксазолидиноновый антибиотик линезолид.
Известно, что применяемые в настоящее время в качестве эффективных антибиотиков против MRSA ванкомицин и арбекацин, проявляют побочные действия, такие как нарушения слуха, вызванные расстройством восьмого черепного нерва. Далее, гликопептидные антибиотики вызывают побочные эффекты, такие как шок, нефротоксичность и «синдром красного человека», и при применении в клинике, необходимо осторожное введение, например, наблюдение за уровнем препарата в крови. Помимо MRSA, обладающих мультилекарственной устойчивостью, сообщалось о бактериях с низкой чувствительностью к основному лечебному средству - ванкомицину. Следовательно, необходимо выявление новых антибиотиков и разработка новых способов лечения. В настоящее время в качестве нового способа лечения ведется разработка комбинированной терапии с применением β-лактамовых антибиотиков или β-лактамовых антибиотиков и других антибиотиков, имеющих отличающийся характер действия (Hiromi Hasegawa et al. “Science of antibiotic administration”, pp. 264-273, 1998). Далее, сообщается о веществах, которые сами по себе не проявляют противомикробной активности, но восстанавливают или усиливают эффективность β-лактамовых антибиотиков. Например, могут быть упомянуты чайный экстракт или его активные фракции (полифенольные соединения), раскрытые в опубликованном японском переводе международной публикации согласно PCT заявки на патент Hei 9-509677 или (PCT/JP2006/305625).
Проблема, которую предполагалось решить с помощью настоящего изобретения:
В свете описанной ситуации, важно разработать новые антибиотики с новой структурой, демонстрирующие антибактериальную активность против MRSA. Далее, ожидается, что препараты, усиливающие активность β-лактамовых антибиотиков против MRSA, снизят уровень дозировки β-лактамовых антибиотиков и уменьшат частоту появления устойчивых бактерий в результате уменьшения периода введения препарата. Далее, в то же время ожидается преодоление устойчивости к лекарственным препаратам, за счет комбинирования двух лекарственных средств с различным характером действия.
Задача, на решение которой направлено настоящее изобретение, заключается в разработке новых терапевтических препаратов против MRSA-инфекций и инфекционных заболеваний, вызванных микроорганизмами с мультилекарственной устойчивостью, в т.ч. устойчивых к β-лактамовым антибиотикам.
Средства для решения проблемы
Авторы настоящего изобретения провели обширные исследования соединений, проявляющих противомикробную активность против MRSA или соединений, улучшающих активность β-лактамовых антибиотиков, направленные на метаболиты, вырабатываемые микроорганизмами, и обнаружили, что вещества, демонстрирующие целевые виды активности, вырабатывались в культуральной жидкости штамма Streptomyces K04-0144, который недавно был выделен из почвы. Затем, соединения, демонстрирующие целевую активность, были выделены из культуральной массы и очищены, после чего могли бы быть получены три типа анти-MRSA антибиотиков и соединение, усиливающее активность β-лактамовых антибиотиков. Поскольку вещества с подобной химической структурой не были известны ранее, анти-MRSA антибиотики были названы соединением K04-0144A, соединением K04-0144B и соединением K04-0144C, а действующее вещество, усиливающее активность β-лактамовых антибиотиков, было названо соединением K04-0144D. Кроме того, все эти соединения в совокупности были названы соединением K04-0144.
В соответствии с этими данными работа над настоящим изобретением была завершена и изобретение относится к соединению K04-0144, включающему любое из следующих соединений:
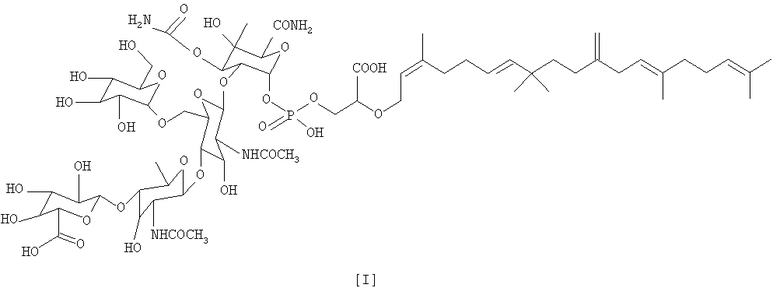
соединение K04-0144A, имеющее следующую формулу (I):
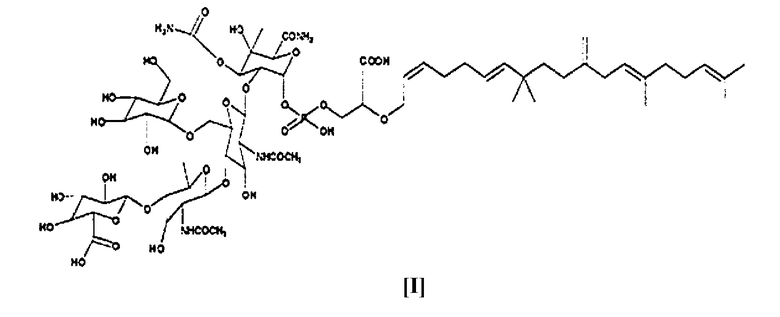
соединение K04-0144B, имеющее следующую формулу (II):
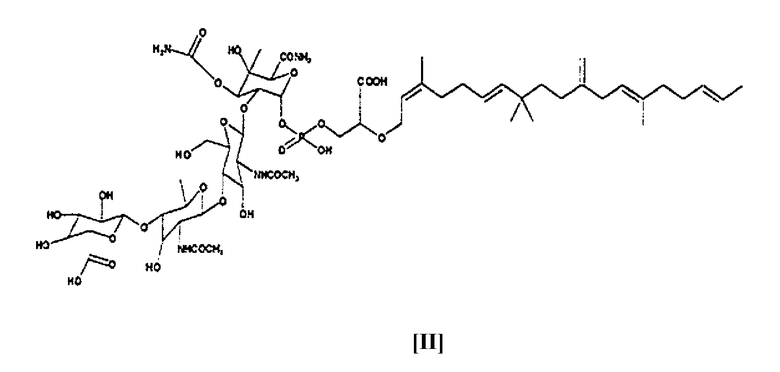
соединение K04-0144C, имеющее следующую формулу (III):
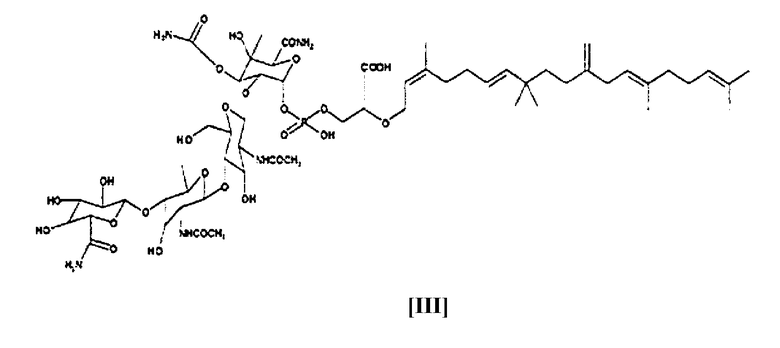
и
соединение K04-0144D, имеющее следующую формулу (IV):
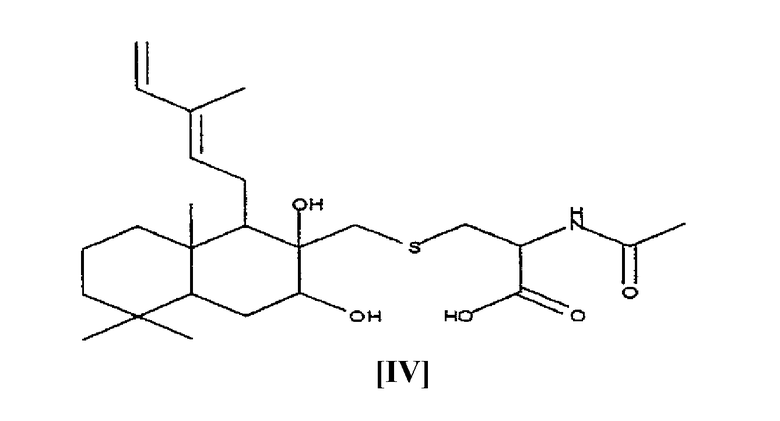
Далее, настоящее изобретение относится к способу получения нового соединения K04-0144, включающему культивирование микроорганизмов, принадлежащих к роду Streptomyces и обладающих способностью вырабатывать в среде соединение K04-0144, накопление соединения K04-0144 в культуральной среде и выделение соединения K04-0144 из культуральной массы.
Кроме того, настоящее изобретение относится к микроорганизмам Streptomyces sp. K04-0144 (NITE BP-107).
Штамм, примененный для получения нового соединения K04-0144, представленного формулами (I),(II),(III) и (IV) выше по тексту, может быть упомянут как пример такого штамма, как Streptomyces sp. K04-0144, который был недавно изолирован авторами настоящего изобретения из почвы Ishigaki-island, Okinawa Pref., Japan.
Таксономические свойства данного штамма являются следующими.
(I) Морфологические свойства
Вегетативные мицелии демонстрируют хороший рост на различных средах из агара и не наблюдается фрагментации. Воздушные мицелии хорошо растут на агаре с экстрактом дрожжей-экстрактом солода и глицерин-аспарагиновом агаре, и имеют цвет от белого до серого. При наблюдении под микроскопом на воздушных мицелиях видны цепи из 20 или более спор, и их формы являются спиральными. Споры представляют собой цилиндры размером примерно 1,0×1,0 мкм. Поверхность спор является гладкой. Склероции, спорангии и зооспоры не наблюдаются.
(II) Характеристики на различных средах
Культуральные свойства описываемого штамма, которые наблюдали в соответствии со способом E.B.Shirling и D.Gottlieb (International Journal of Systematic Bacteriology, 16: 313, 1966), показаны в следующей таблице. Цвет определен по соответствию стандартному цвету, с применением Color Harmony Manual, 4th Ed. (Container Corp. of America, Chicago, 1958) и отображен названием цвета и его кодом в круглых скобках. Приведенные данные, если не указано конкретно, являются результатами наблюдений при 27°C в течение 2 недель на различных средах.
бледно-желтый (1ca)
серые «Темная чаща» (2ih)
нет названия (24 Ѕ ml)
серый «темная чаща» (2ih)
темно-оливковый серый (1ml)
бледно-желтый (1ca)
(при 21-23°C)
простая желатиновая среда
Незначительно потребляются: L-арабиноза, D-ксилоза, раффиноза, D-фруктоза, сахароза
(IV) Хемотаксономические свойства
Диаминопимелиновая кислота клеточной стенки относится к LL типу и основными менахинонами являются MK-9(H6) и MK-9(H8).
(V) Заключение
Таксономические свойства описываемого штамма можно суммировать следующим образом. Диаминопимелиновая кислота в клеточной стенке относится к LL-типу и основными менахинонами являются MK-9(H6) и MK-9(H8). Формой цепочки спор является спираль с образованием длинной цепочки спор, и поверхность споры является гладкой. Цвет вегетативных мицелиев является коричневым. Цвет воздушной массы меняется от белого до серого. Не наблюдается образования пигмента меланина.
На основании этих данных можно считать, что данный штамм относится к роду Streptomyces, согласно Bergey's Manual of Systematic Bacteriology, vol.4, 1989.
Международное депонирование микроорганизма
Описываемый штамм был депонирован как Streptomyces sp.K04-0144 на основе Будапештского договора о международном признании депонирования микроорганизмов для целей процедуры выдачи патентов в Депозитарии микроорганизмов национального института технологии и патентной экспертизы (NPMD) Международного административного агентства, 1-5-8 Kazusa-kamatari, Kisarazu-shi, Chiba-ken, 292-0818 Japan. Датой депонирования является 30 июня 2005, и инвентарный номер NITE BP-107.
Физико-химические свойства:
Ниже по тексту заявки приведены физико-химические свойства соединения K04-0144 по настоящему изобретению.
1. Соединение K04-0144A
(1) Внешний вид: белый порошок
(2) Молекулярная формула: C64H103N4O33P
Отр. ИЭР-МС ВР (Масс-спектроскопия с ионизацией электрораспылением высокого разрешения) (m/z) [M-H]-:
Вычислено: 1485,6206
Экспериментальное значение: 1485,6164
(3) Молекулярная масса: 1487
Отр. ИЭР-МС (m/z) [M-H]-: наблюдалось значение 1485.
(4) спектр УФ: в метаноле, фиг.1, конечное поглощение
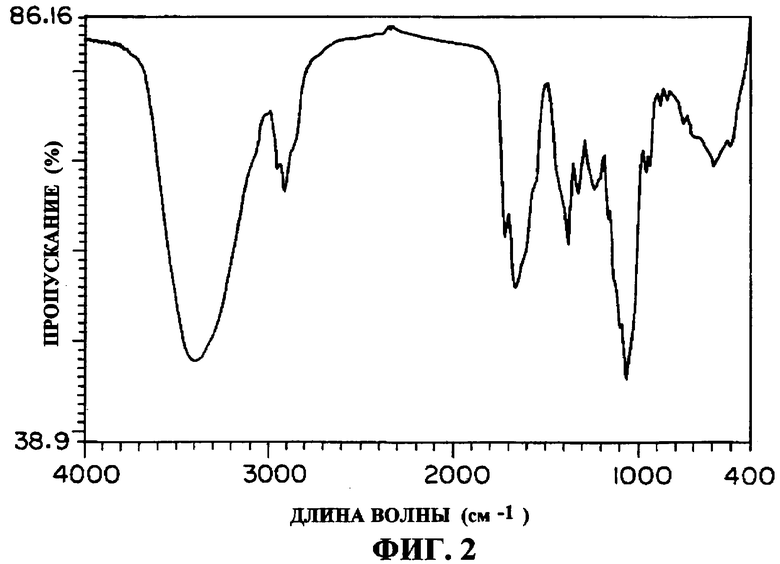
(5) ИК-спектр: KBr, фиг.2, наблюдались специфические полосы поглощения с νmax при 3299, 2960, 1722, 1673, 1068 см-1.
(6) Удельное вращение: [α]D 24=+6,7° (c=0,1 MeOH)
(7) Растворимость в растворителях:
растворимо в метаноле, воде и ДМСО
нерастворимо в ацетоне, хлороформе и гексане.
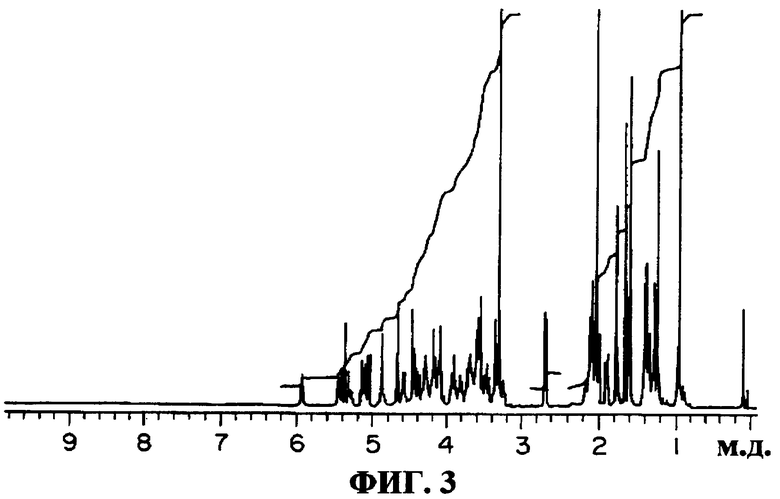
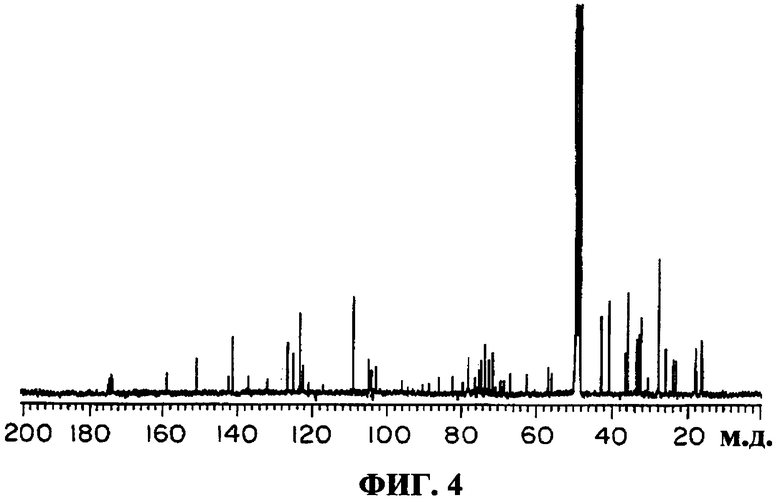
(8) Протонные и углеродные спектры ЯМР: зарегистрированы в дейтерированном метаноле с применением ЯМР-спектрометра Varian Inc. 400 МГц, протонный спектр ЯМР показан на фиг.3 и углеродный спектр ЯМР показан на фиг.4. Химические сдвиги (м.д.) водорода и углерода приведены ниже.
δН: 0,97(6H), 1,26(3H), 1,37(2H), 1,41(3H), 1,60(3H), 1,62(3H), 1,67(3H), 1,78(3H), 1,91(2H), 2,01(2H), 2,04(3H), 2,05(3H), 2,10(4H), 2,13(1H), 2,17(1H), 2,70(1H), 3,25(1H), 3,31(2H), 3,35(1H), 3,46(1H), 3,51(1H), 3,55(3H), 3,60(3H), 3,67(1H), 3,70(1H), 3,71(1H), 3,81(1H), 3,90(1H), 3,93(1H), 4,09(1H), 4,11(1H), 4,15(1H), 4,18(2H), 4,28(1H), 4,29(1H), 4,38(1H), 4,42(1H), 4,45(1H), 4,47(1H), 4,57(1H), 4,66(1H), 4,67(1H), 5,06(1H), 5,10(1H), 5,14(1H), 5,29(1H), 5,38(1H), 5,45(1H), 5,93(1H) м.д.
δс: 16,1, 16,4, 17,8, 18,0, 23,3, 23,5, 24,0 26,0, 27,7, 27,9, 27,9, 32,4, 32,7, 33,5, 35,9, 36,5, 40,9, 42,9, 55,7, 56,9, 62,5, 66,9, 68,5, 69,4, 71,6, 71,6, 72,2, 72,6, 73,8, 73,8, 74,0, 74,1, 74,7, 75,0, 75,2, 75,4, 76,4, 78,0, 78,2, 78,3, 79,7, 82,4, 86,1, 96,2, 103,2, 104,3, 104,7, 105,1, 109,3, 122,7, 123,5, 125,4, 126,8, 132,2, 137,4, 141,6, 142,6, 151,1, 159,2, 173,5, 173,8, 174,2, 174,6, 175,1 м.д.
В результате подробного изучения различных физико-химических свойств и спектральных данных соединения KO1-0144A, было определено, что соединение KO1-0144A обладает химической структурой [I], показанной выше по тексту.
1. Соединение K04-0144B
(1) Внешний вид: белый порошок
(2) Молекулярная формула: C58H93N4O28P
Отр. ИЭР-МС ВР (m/z) [M-H]-:
Вычислено: 1323,5656
Экспериментальное значение: 1323,5634
(3) Молекулярная масса: 1325
Отр. ИЭР-МС (m/z) [M-H]-: наблюдалось значение 1323.
(4) спектр УФ: в метаноле, фиг.5, конечное поглощение
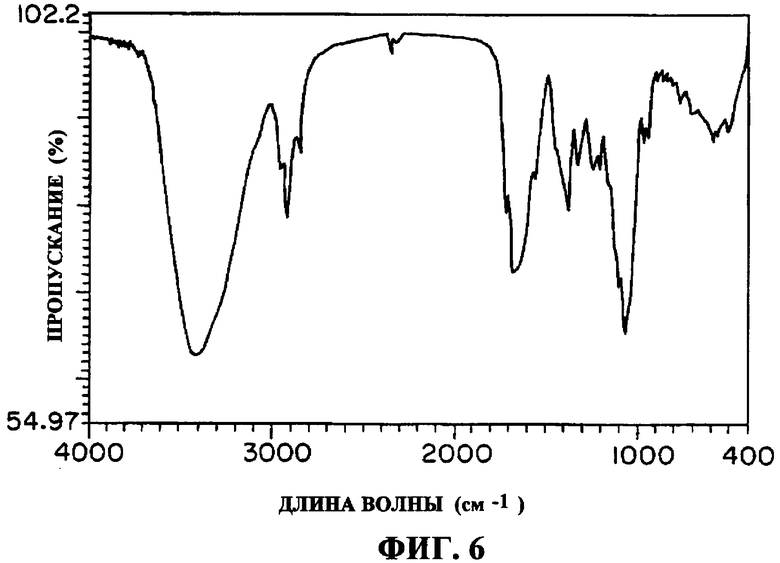
(5) ИК-спектр: KBr, фиг.6, наблюдались специфические полосы поглощения с νmax при 3299, 2923, 1716, 1675, 1068 см-1.
(6) Удельное вращение: [α]D 24=+4,0° (c=0,1 MeOH)
(7) Растворимость в растворителях:
растворимо в метаноле, воде и диметилсульфоксиде
нерастворимо в ацетоне, хлороформе и н-гексане.
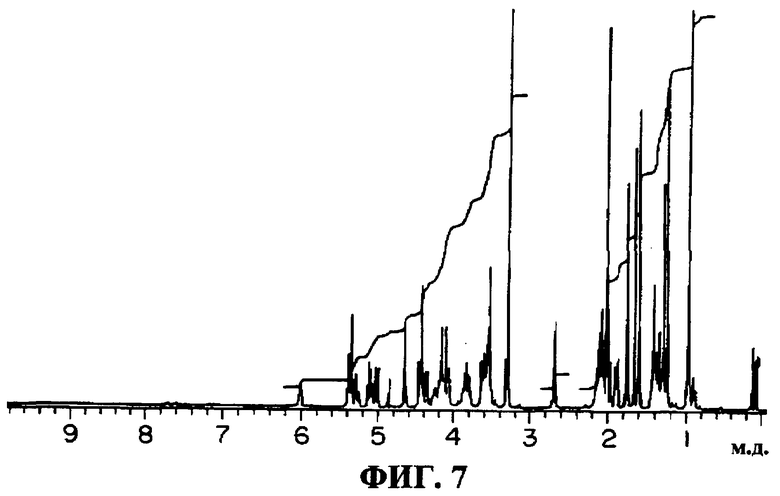
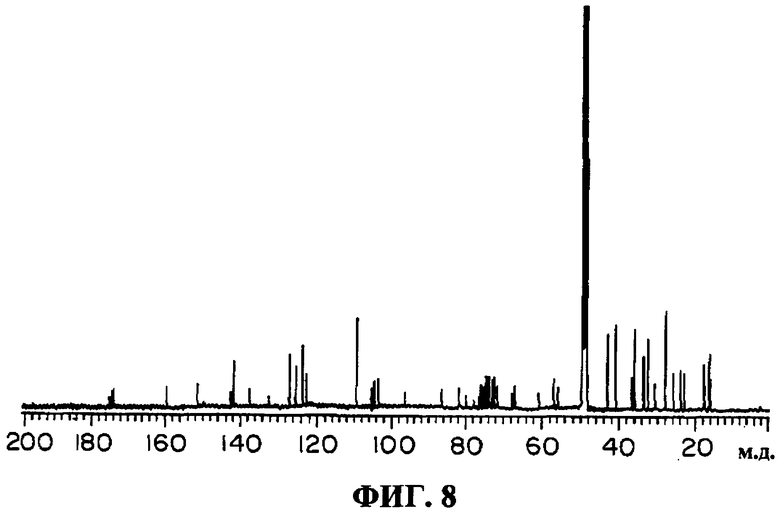
(8) Протонные и углеродные спектры ЯМР: зарегистрированы в дейтерированном метаноле с применением ЯМР-спектрометра Varian Inc. 400 МГц, протонный спектр ЯМР показан на фиг.7 и углеродный спектр ЯМР показан на фиг.8. Химические сдвиги (м.д.) водорода и углерода приведены ниже.
δН: 0,97(6H), 1,26(3H), 1,38(2H), 1,42(3H), 1,60(3H), 1,61(3H), 1,67(3H), 1,77(3H), 1,91(2H), 2,02(3H), 2,03(5H), 2,10(4H), 2,14(2H), 2,70(2H), 3,31(1H), 3,33(1H), 3,54(1H), 3,56(2H), 3,58(1H), 3,62(1H), 3,64(3H), 3,82(1H), 3,84(1H), 3,88(1H), 4,08(1H), 4,12(1H), 4,13(1H), 4,16(1H), 4,17(1H), 4,18(1H), 4,26(1H), 4,37(1H), 4,44(1H), 4,45(1H), 4,47(1H), 4,66(1H), 4,67(1H), 5,04(1H), 5,10(1H), 5,14(1H), 5,29(1H), 5,38(1H), 6,04(1H) м.д.
δс: 16,1, 16,3, 17,8, 18,0, 23,1, 23,3, 24,0 26,0, 27,7, 27,8, 27,9, 32,4, 32,7, 33,4, 36,0, 36,5, 40,9, 42,9, 55,9, 56,7, 60,8, 67,0, 67,7, 71,6, 72,1, 72,6, 73,7, 73,8, 73,9, 74,1, 74,6, 75,1, 76,0, 76,3, 77,9, 79,9, 81,5, 86,4, 96,5, 103,4, 104,6, 105,2, 109,3, 122,8, 123,5, 125,4, 126,8, 132,2, 137,4, 141,7, 142,4, 151,1, 159,2, 173,2, 173,7, 174,1, 174,7, 174,9 м.д.
В результате подробного изучения различных физико-химических свойств и спектральных данных соединения KO1-0144B, было определено, что соединение KO1-0144B обладает химической структурой [II], показанной выше по тексту.
1. Соединение K04-0144С
(1) Внешний вид: белый порошок
(2) Молекулярная формула: C58H94N5O27P
Отр. ИЭР-МС ВР (m/z) [M-H]-:
Вычислено: 1322,5859
Экспериментальное значение: 1322,5795
(3) Молекулярная масса: 1324
Отр. ИЭР-МС (m/z) [M-H]-: наблюдалось значение 1323.
(4) спектр УФ: в метаноле, фиг.9, конечное поглощение
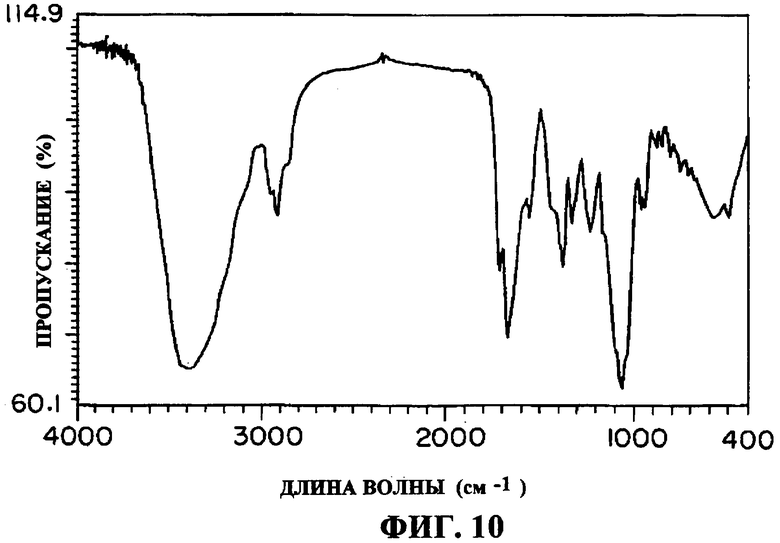
(5) ИК-спектр: KBr, фиг.10, наблюдались специфические полосы поглощения с νmax при 3400, 2925, 1716, 1677, 1648 см-1.
(6) Удельное вращение: [α]D 24=+3,7° (c=0,1 MeOH)
(7) Растворимость в растворителях:
растворимо в метаноле, воде и диметилсульфоксиде
нерастворимо в ацетоне, хлороформе и н-гексане.
(8) Протонные и углеродные спектры ЯМР: зарегистрированы в дейтерированном метаноле с применением ЯМР-спектрометра Varian Inc. 400 МГц, протонный спектр ЯМР показан на фиг.11 и углеродный спектр ЯМР показан на фиг.12. Химические сдвиги (м.д.) водорода и углерода приведены ниже.
δН: 0,97(6H), 1,25(3H), 1,38(2H), 1,42(3H), 1,60(3H), 1,61(3H), 1,67(3H), 1,76(3H), 1,91(2H), 2,01(6H), 2,04(2Н), 2,09(2H), 2,11(2H), 2,14(2H), 2,70(2H), 3,34(2H), 3,56(4H), 3,64(4H), 3,72(1H), 3,83(1H), 3,84(1H), 4,06(1H), 4,11(3H), 4,17(1H), 4,21(2H), 4,42(1H), 4,44(1H), 4,46(1H), 4,54(1H), 4,66(1H), 4,68(1H), 5,07(1H), 5,11(1H), 5,14(1H), 5,29(1H), 5,38(2H), 5,99(1H) м.д.
δс: 16,1, 16,4, 17,8, 17,9, 23,1, 23,3 23,9, 26,0, 27,7, 27,9, 27,9, 32,3, 32,6, 33,4, 36,0, 36,5, 40,9, 42,9, 56,5, 56,7, 61,0, 67,2, 67,6, 70,7, 72,3, 72,8, 73,5, 73,7, 73,9, 74,0, 74,4, 75,7, 76,0, 76,0, 78,3, 79,4, 81,6, 85,1, 96,2, 103,5, 103,9, 104,9, 109,3, 122,6, 123,5, 125,4, 126,8, 132,2, 137,3, 141,6, 142,1, 151,1, 159,2, 173,7, 173,7, 173,7, 174,0 174,0 м.д.
В результате подробного изучения различных физико-химических свойств и спектральных данных соединения KO1-0144C, было определено, что соединение KO1-0144C обладает химической структурой [III], показанной выше по тексту.
1. Соединение K04-0144D
(1) Внешний вид: белый порошок
(2) Температура плавления: 138°C
(3) Молекулярная формула: C25H41NO5S
FAB-МС ВР (МС с бомбардировкой быстрыми атомами высокого разрешения)(m/z) [M-H+2Na]+:
Вычислено: 512,2423
Экспериментальное значение: 512,2416
(4) Молекулярная масса: 467
FAB-МС (m/z) [M-H+2Na]+ 512
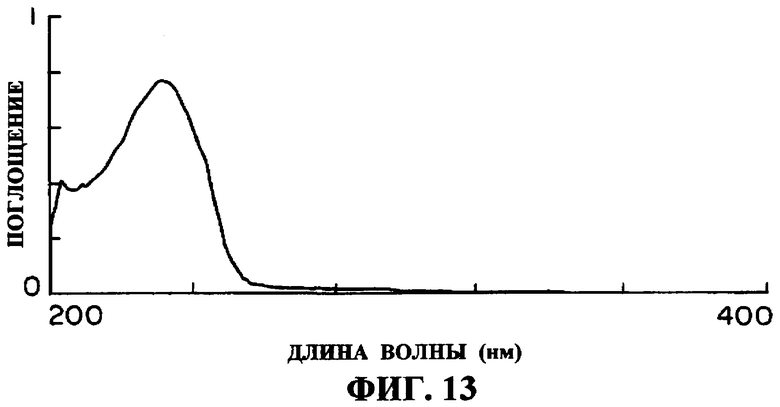
(5) спектр УФ: в метаноле, фиг.13, максимальное поглощение 232 нм
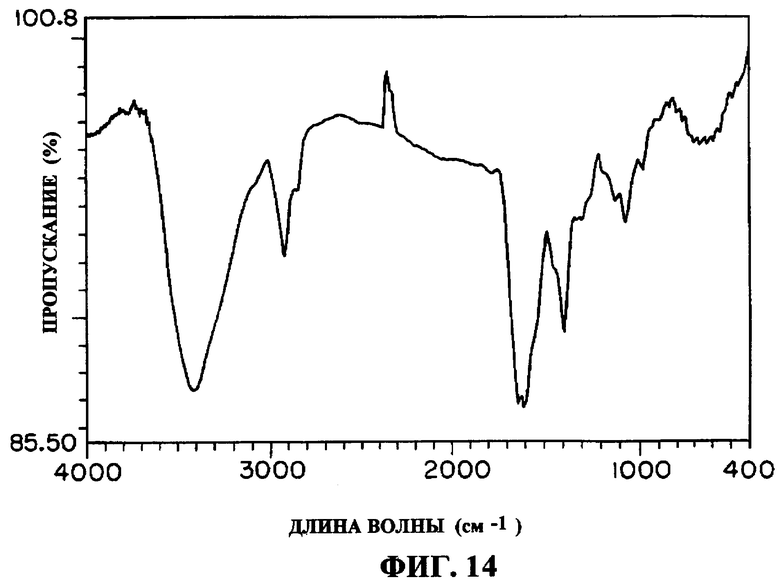
(6) ИК-спектр: KBr, фиг.14, наблюдались специфические полосы поглощения с νmax при 3427, 2927, 2864, 1641, 1604, 1398, 1124 см-1.
(7) Удельное вращение: [α]D 25=+26,8° (c=0,1 MeOH)
(8) Растворимость в растворителях:
растворимо в метаноле, воде и ацетонитриле
нерастворимо в хлороформе, гексане и этилацетате.
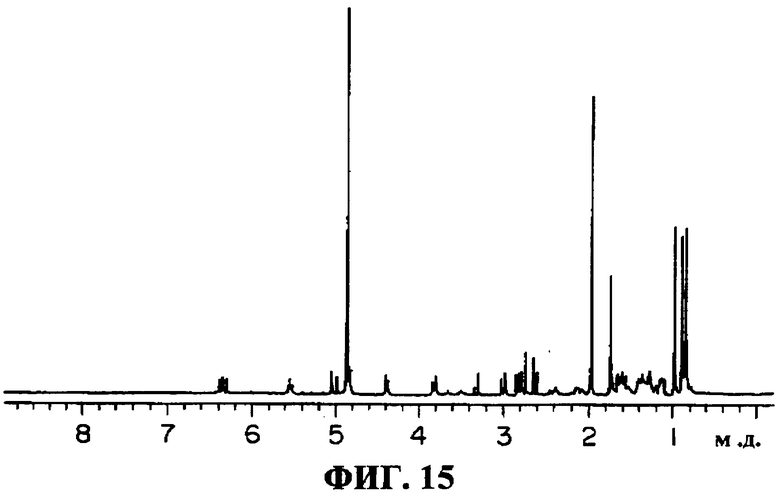
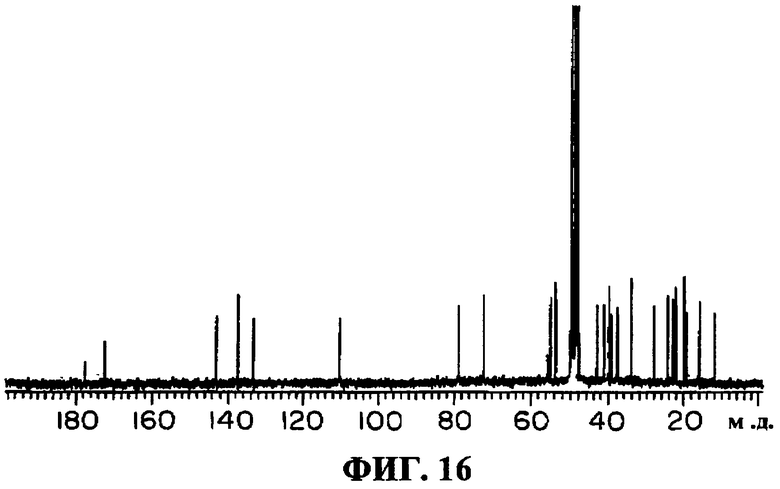
(9) Протонные и углеродные спектры ЯМР: зарегистрированы в дейтерированном метаноле с применением ЯМР-спектрометра Varian Inc. 400 МГц, протонный спектр ЯМР показан на фиг.15 и углеродный спектр ЯМР показан на фиг.16. Химические сдвиги (м.д.) водорода и углерода приведены ниже.
δ: 0,84(5H), 0,91(4H), 1,00(3H), 1,14(1H), 1,35(2H), 1,63(4H), 1,75(3H), 1,98(3H), 2,13(1H), 2,42(1H), 2,63(1H), 2,77(1H), 2,82(1H), 3,02(1H), 3,82(1H), 4,41(1H), 4,86(1H), 5,03(1H), 5,55(2H), 6,35(1H) м.д.
δ: 12,0, 16,0, 19,3, 22,3, 22,8, 24,4, 27,8, 34,0, 34,1, 37,7, 39,2, 39,8, 41,1, 43,0, 53,7, 55,2, 55,8, 72,3, 78,8, 110,1, 133,2, 137,6, 143,1, 172,5, 177,4 м.д.
В результате подробного изучения различных физико-химических свойств и спектральных данных соединения KO1-0144D, было определено, что соединение KO1-0144D обладает химической структурой [IV], показанной выше по тексту.
Биологические свойства:
Ниже подробно описаны биологические свойства соединения K04-0144.
Противомикробная активность соединений K04-0144A, K04-0144B и K04-0144C.
Определение минимальных ингибирующих концентраций (MIC) проводили в соответствии с методикой разбавления на планшете с агаром (методика Японского Общества Химиотерапии, CHEMOTHERAPY 29, 76-79, 1981).
В качестве тестовых микроорганизмов использовали 27 типов микроорганизмов, включая клинические изоляты метициллин-устойчивых Staphylococcus aureus. Каждый из тестовых микроорганизмов культивировали в питательной среде Mueller-Hinton (2,1% масса/объем) (DIFCO) при 37°C в течение 20 часов, культивированные клетки суспендировали в той же среде в количестве примерно 106 шт клеток/мл и затем использовали в качестве суспензии микроорганизмов для засевания. Полученную таким образом суспензию микроорганизмов намазывали с использованием устройства для посева микроорганизмов на питательную среду MHA (Mueller-Hinton 2,1% (масса/объем) и агар 1,5%), содержащую соединение K04-0144A, соединение K04-0144B и соединение K04-0144C, каждое из которых было подвергнуто постадийному двукратному разбавлению, начиная с концентрации 128 мкг/мл. После культивирования при 37°C в течение 20 часов, определяли MIC путем макроскопического подтверждения роста микроорганизмов. В качестве сравнительного контроля использовали ванкомицин, арбекацин и линезолид.
Результаты суммированы в таблице 1.
Результаты оценки активности K04-0144A,B и C против клинических изолятов (MIC) (мкг/мл)
соединение
HR-12002.2.1
Как показывают данные таблицы, соединения K04-0144A, B и C ингибировали рост грам-положительных бактерий, включая MRSA, так же как и контрольные препараты или сильнее.
Оценка активности на модели инфекции MRSA с использованием тутовых шелкопрядов.
Сообщалось об инфекционной системе с использованием тутового шелкопряда, как о альтернативном способе реализации модели in vivo MRSA-инфекции с использованием животных (Kaito et al, Microbial Pathogenesis, 32: 183-190, 2002). Действие соединения K04-0144A измеряли согласно этой методике.
Использованный тестовый микроорганизм представлял собой клинический изолят MRSA (штамм K24). MRSA статически культивировали, используя среду LB-10 (DIFCO) при 37°C в течение 18 часов, и 50 мкл культивированного штамма высевали в гемолимфу тутового шелкопряда, 2 день 5-й возрастной стадии (массой примерно 2 г, Ehime sansyu eggs Co., Japan). Соединение K04-0144A получали в виде раствора 1 мг/мл и с помощью шприца вводили 50 мкл раствора в спинной сосуд 5 тутовых шелкопрядов, инфицированных MRSA (25 мг/кг). Действие соединения K04-0144A оценивали путем сравнения выживаемости в группе, которой вводили образец препарата, и группы, которой не вводили препарат в течение 72 часов после заражения. Поскольку все шелкопряды, которым не вводили образец (контроль), и все шелкопряды, которым вводили только соединение K04-0144A 25 мг/кг, остались в живых по крайней мере через 72 часа, было подтверждено, что в данных условиях соединение K04-0144A не проявляет токсичности в отношении тутовых шелкопрядов. Далее, все шелкопряды, которым вводили 50 мкл бактериальной суспензии MRSA, погибли в течение 72 часов после заражения. В этих же условиях все шелкопряды, которым вводили соединение K04-0144A в количестве 25 мг/кг, выжили в течение 72 часов после заражения. Аналогично, шелкопряды, которым вводили ванкомицин в количестве 25 мг/мл, остались в живых через 72 часа после заражения.
Соответственно, в эксперименте с заражением тутового шелкопряда MRSA была продемонстрирована эффективность соединения K04-0144A.
Усиливающее действие соединения K04-0144D на активность имипенема
1. Способ оценки усиливающего действия на активность имипенема с помощью методики с бумажным диском.
В качестве тестового микроорганизма использовали клинический изолят штамма K24 метициллин-устойчивого Staphylococcus aureus (MRSA). После того как штамм MRSA K24 культивировали в питательной среде Mueller-Hinton (2,1% масса/объем) (DIFCO) при 37°C в течение 20 часов, штамм суспендировали в той же среде до концентрации, соответствующей 0,5 Mc FARAND (примерно 108 CFU/мл). Суспензию намазывали на среду MHA (питательная среда Mueller-Hinton 2,1% (масса/объем), агар 1,5%) и среду того же состава, содержащую имипенем (Tienem для внутримышечных инъекций, 0,5 г, Banyu Pharmaceutical Co., Ltd., Japan) в концентрации, которая не оказывала влияния на рост тестовых микроорганизмов, т.е. конечной концентрации 10 мкг/мл. Намазывание проводили по методике Национального комитета по лабораторным стандартам США (NCCLS) с использованием стерилизованного тампона с ватой на конце (Kawamoto Sangyo Co., Ltd., Japan). Антибактериальную активность против тестовых микроорганизмов на различных средах определяли по диаметру круга ингибирования в единицах мм после инкубирования при 37°C в течение 20 часов с применением способа с бумажным диском (тонкий бумажный диск, диаметр 6 мм, ADVANTEC Inc.). Результаты, приведенные в таблице 1, показывают, что в условиях применения 1 мкг/диск, соединение K04-0144D само по себе не показывало круга ингибирования, тогда как в условиях применения имипенема, наблюдался круг ингибирования диаметром 15 мм, что подтверждало усиливающее действие соединения K04-0144D на активность имипинема.
Усиливающее действие соединения K04-0144D на активность имипинема, определенное с помощью способа с бумажным диском
мкг/6 мм диск
Диаметр круга ингибирования (мм)
Методика оценки усиливающего действия соединения K04-0144D на активность различных антибиотиков с применением способа микроразбавления питательной среды
Оценивали усиливающее действие соединения K04-0144D, которое демонстрирует мощное усиливающее влияние на активность имипенема, определенное с помощью методики с бумажным диском, на активность других антибиотиков с применением способа микроразбавления питательной среды. Другими исследованными антибиотиками были ванкомицин (Wako Pure Chemical Industries, Ltd., Japan), стрептомицин (Meiji Seika Kaisha, Japan) и ципрофлоксацин (Wako Pure Chemical Industries, Ltd.). Оценку проводили с применением частично модифицированной стандартной методики Японского общества химиотерапии (CHEMOTHERAPY 38, 103-105, 1990).
После добавления 85 мкл питательного раствора Mueller-Hinton (2,1% масса/объем) в каждую из лунок 96-луночного планшета (Corning Corp., USA), в каждую лунку добавляли 5 мкл имипенема, который предварительно был подвергнут постадийному разбавлению стерилизованной водой, до получения конечной концентрации от 4,8×10-4 до 256 мкг/мл. Затем в каждую лунку добавляли 5 мкл водного раствора соединения K04-0144D, до получения конечной концентрации 16 мкг/мл, в которой соединение K04-0144D само по себе не оказывает неблагоприятного влияния на рост микроорганизмов. После перемешивания содержимого лунок, суспендировали тестовый микроорганизм MRSA, получая концентрацию, соответствующую 0,5 Mc FARAND (примерно 108 CFU/мл). Полученную суспензию разбавляли в 10 раз, добавляя ту же самую среду, и 5 мкл разбавленной суспензии высевали в каждую лунку. После инкубирования при 37°C в течение 20 часов, определяли MIC, т.е. минимальную концентрацию лекарственного средства, при которой рост бактерий в лунке не наблюдался макроскопически. Значения MIC для каждого антибиотика в чистом виде и в случае совместного применения каждого антибиотика и соединения K04-0144D показаны в таблице 3. Усиливающее влияние на действие имипенема выражалось в снижении MIC в 1024 раза с 32 мкг/мл до 0,03 мкг/мл. Поскольку усиливающего влияния в случае ванкомицина, стрептомицина и ципрофлоксацина не наблюдалось, стало очевидно, что усиление активности под действием соединения K04-0144D, эффективно именно в отношении β-лактамовых антибиотиков.
Усиливающее действие соединения K04-0144D на активность имипенема, определенное способом микроразбавления питательной среды
Тестовый микроорганизм: MRSA (клинический изолят, Kitasato Hospital, Japan)
соединение K04-0144D (16 мкг/мл): концентрация равна ј от минимальной ингибирующей концентрации
Краткое описание чертежей
Фиг 1: УФ спектр соединения K04-0144A (в метаноле);
Фиг.2: ИК спектр соединения K04-0144A (KBr);
Фиг.3: Протонный спектр ЯМР соединения K04-0144A (в дейтерированном метаноле);
Фиг.4: Углеродный спектр ЯМР соединения K04-0144A (в дейтерированном метаноле);
Фиг 5: УФ спектр соединения K04-0144B (в метаноле);
Фиг.6: ИК спектр соединения K04-0144B (KBr);
Фиг.7: Протонный спектр ЯМР соединения K04-0144B (в дейтерированном метаноле);
Фиг.8: Углеродный спектр ЯМР соединения K04-0144B (в дейтерированном метаноле);
Фиг 9: УФ спектр соединения K04-0144С (в метаноле);
Фиг.10: ИК спектр соединения K04-0144С (KBr);
Фиг.11: Протонный спектр ЯМР соединения K04-0144С (в дейтерированном метаноле);
Фиг.12: Углеродный спектр ЯМР соединения K04-0144С (в дейтерированном метаноле);
Фиг 13: УФ спектр соединения K04-0144D (в метаноле);
Фиг.14: ИК спектр соединения K04-0144D (KBr);
Фиг.15: Протонный спектр ЯМР соединения K04-0144D (в дейтерированном метаноле);
Фиг.16: Углеродный спектр ЯМР соединения K04-0144D (в дейтерированном метаноле).
Наилучший способ осуществления настоящего изобретения
Далее по тексту настоящее изобретение будет раскрыто с помощью описания примеров, но эти примеры не следует истолковывать, как ограничивающие.
Способ получения соединения K04-0144
1) Способ получения K04-0144A, B и C
Штамм K04-0144, культивированный на среде скошенного агара (крахмал 1,0% (Kanto Chemical Co., Inc., Japan), NZ амин 0,3% (Wako Pure Chemical Industries, Ltd., Japan), экстракт дрожжей 0,1% (Oriental Yeast Co., Ltd., Japan), мясной экстракт 0,3% (Kyokuto Pharmaceutical Industrial Co., Ltd., Japan), карбонат кальция 0,3% (Kanto Chemical Co., Inc., Japan) и агар 1,2% (Shimizu Shokuhin Kaisha, Ltd., Japan), pH доведен до 7,0) высевали в количестве одной петли для посева в 500 мл колбы Эрленмейера, содержащие 100 мл среды для посева (крахмал 2,4% (Kanto Chemical Co., Inc., Japan), глюкоза 0,1% (Wako Pure Chemical Industries, Ltd., Japan), пептон 0,3% (Kyokuto Pharmaceutical Industrial Co., Ltd., Japan), мясной экстракт (Kyokuto Pharmaceutical Industrial Co., Ltd., Japan), экстракт дрожжей 0,5% (Oriental Yeast Co., Ltd., Japan) и CaCO3 0,4% (Kanto Chemical Co., Inc., Japan), pH доведен до 6,0) и культивировали при 27°C в течение 3 дней на вращающемся шейкере (210 об/мин). Культивированный штамм высевали в количестве 1% в 50 л продуцирующей среды (глюкоза 0,5% (Wako Pure Chemical Industries, Ltd., Japan), порошок кукурузного экстракта 0,5% (Maruko Co., Japan), овсяная мука 1,0% (Nisshoku Co., Ltd., Japan), фармацевтическая среда 1,0% (Iwaki& Co., Ltd., Japan), K2HPO4 0,5% (Kanto Chemical Co., Inc., Japan), MgSO4·7H2O 0,5% (Wako Pure Chemical Industries, Ltd., Japan) и раствор следового количества солей 0,1% (FeSO4·7H2O 0,1% (Kanto Chemical Co., Inc., Japan), MnCl2·4H2O 0,1% (Kanto Chemical Co., Inc., Japan), ZnSO4·7H2O 0,1% (Kanto Chemical Co., Inc., Japan), CuSO4·5H2O 0,1% и CoCl2·6H2O 0,1% (Kanto Chemical Co., Inc., Japan)), значение pH доведено до 7,0) в 90-литровом сосуде для ферментации и культивировали при 27°C в течение 6 дней.
После культивирования центрифугировали 50 л культуральной жидкости с использованием центрифуги Sharpless для разделения супернатанта и мицелиев. Супернатант загружали в колонку HP-20 (ш10×20 см, Mitsubishi Chemical Corp., Japan), промывали 1,5 л воды, элюировали действующие соединения 1,5 л 100% метанола, концентрировали в вакууме и подвергали лиофильной сушке. 15 г из 27 г полученного таким образом неочищенного соединения растворяли в небольшом количестве воды и очищали с применением колонки ODS (ш5×28 см, Senshu Scientific Co., Ltd., Japan). После промывания колонки ODS 40% раствором метанола, осуществляли хроматографию, используя в качестве элюента градиент метанол-очищенная вода (2:1, 3:2, 4:1 и 100:0). Весь элюат общим количеством 4 л собирали в 40 пробирок по 100 мл. Фракцию, содержащую действующее соединение (элюирование смесью 3:2 от фракции №4 до фракции №9), концентрировали и высушивали, получая 450 мг соединения в виде коричневого порошка. Это соединение растворяли в небольшом количестве метанола и очищали, применяя препаративную ВЭЖХ (колонка: PEGASIL ODS, ш20×250 мм, Senshu Scientific Co., Ltd., Japan). В качестве подвижной фазы использовали 50% водный раствор ацетонитрила (10 мМ ацетат аммония, значение pH доведено до 3 добавлением муравьиной кислоты) и наблюдали за поглощением в УФ-диапазоне при 210 нм при скорости потока 8 мл/мин. Наблюдались пики, демонстрирующие выход соединений, соответствующие временам удерживания 21 мин, 33 мин и 37 мин, причем соответствующий элюат собирали. pH собранных растворов доводили до 7 добавлением раствора аммиака, и концентрировали растворы в вакууме. Кроме того, с целью удаления солей, оставшийся водный раствор адсорбировали на колонку ODS, промывали колонку водой и элюировали раствором метанола. Элюат концентрировали и высушивали, получая соединение K04-0144A и соединение K04-0144B в виде частично очищенных фракций и соединение K04-0144C в виде действующего соединения с выходом 19,4 мг.
Затем соединение K04-0144A и соединение K04-0144B подвергали окончательной очистке с применением препаративной ВЭЖХ (колонка: PEGASIL ODS, ш20×250 мм, Senshu Scientific Co., Ltd., Japan). В качестве подвижной фазы использовали 46% водный раствор ацетонитрила (10 мМ дигидрофосфат калия, pH 4,7), и наблюдали за поглощением в УФ-диапазоне при 210 нм при скорости потока 8 мл/мин. Время удерживания соединения K04-0144A составляло 21 минуту, время удерживания соединения K04-0144B составляло 27 минут, и собирали элюат, соответствующий этим пикам. pH собранных растворов доводили до 7 добавлением 10 мМ водного раствора дигидрофосфата калия и концентрировали растворы в вакууме. Кроме того, с целью удаления солей, оставшийся водный раствор адсорбировали на колонку ODS, промывали колонку водой и элюировали раствором метанола. Элюат концентрировали и высушивали, получая соединение K04-0144A и соединение K04-0144B в виде активных соединений с выходами 15,7 мг и 5,6 мг соответственно.
2) Способ получения K04-0144D
Штамм K04-0144 высевали в количестве 1% в 90 л сосуд для ферментации, содержащий 50 л той же продуцирующей среды, которая применялась при получении соединения K04-0144C, и культивировали при 27°C в течение 6 дней.
После культивирования 50 л культуральной жидкости центрифугировали с применением центрифуги Sharpless для разделения супернатанта и мицелиев. Супернатант загружали в колонку HP-20 (ш20×20 см, Mitsubishi Chemical Corp., Japan), промывали 1,5 л воды, элюировали действующие соединения 100% метанолом, концентрировали в вакууме и подвергали лиофильной сушке. 15 г из 27 г полученного таким образом неочищенного соединения растворяли в небольшом количестве воды и очищали с применением колонки ODS (ш5×28 см, Senshu Scientific Co., Ltd., Japan). После промывания колонки ODS 40% раствором метанола, осуществляли хроматографию, используя в качестве элюента градиент метанол-очищенная вода (2:3, 3:2, 4:1 и 100:0). Весь элюат общим количеством 4 л подвергали фракционированию. Фракцию, содержащую действующее соединение (фракция, элюированная смесью 4:1), концентрировали и высушивали, получая 134 мг соединения в виде коричневого порошка. Это соединение растворяли в небольшом количестве метанола и очищали, применяя препаративную ВЭЖХ (колонка: PEGASIL ODS, ш20×250 мм, Senshu Scientific Co., Ltd., Japan). В качестве подвижной фазы использовали 60% водный раствор ацетонитрила (содержащий 0,05% фосфорной кислоты) и наблюдали за поглощением в УФ-диапазоне при 210 нм при скорости потока 8 мл/мин. Наблюдали пик, соответствующий выходу соединения со временем удерживания 32 мин, и собирали соответствующий элюат. pH собранного раствора доводили до 7 добавлением 1н. водного раствора гидроксида натрия и концентрировали раствор в вакууме. Кроме того, с целью удаления солей, оставшийся водный раствор адсорбировали на колонку HP-20 (Mitsubishi Chemical Corp., Japan), промывали колонку водой и элюировали раствором метанола.
Элюат концентрировали и высушивали, получая соединение K04-0144D и соединение K04-0144B в виде частично очищенных фракций, при выходе действующей фракции 17,1 мг.
Промышленная применимость:
Как описано выше по тексту заявки, в соответствующей среде был культивирован микроорганизм, представляющий штамм K04-0144, относящийся к роду Streptomyces, обладающий способностью продуцировать соединение K04-0144, причем выделенные из него соединения, а именно соединение K04-0144A, соединение K04-0144B и соединение K04-0144C обладают сильной антибактериальной активностью против грам-положительных бактерий, включая метициллин-устойчивых Staphylococcus aureus (MRSA), вследствие чего ожидается, что данные соединения применимы в качестве терапевтических средств для лечения инфекционных заболеваний, вызванных MRSA, а также инфекционных заболеваний, вызванных бактериями с мультилекарственной устойчивостью, в т.ч. устойчивых к β-лактамовым антибиотикам. Далее, поскольку новое соединение K04-0144D, выделенное из культуральной жидкости, обладает способностью усиливать действие β-лактамовых антибиотиков, которые применяются в качестве антибактериальных средств, в комбинации с ними, ожидается, что это соединение будет применимо в качестве терапевтического средства для лечения инфекционных заболеваний, вызванных метициллин-устойчивыми Staphylococcus aureus (MRSA) и бактериями, обладающими мультилекарственной устойчивостью, в т.ч. устойчивых к β-лактамовым антибиотикам.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИБИОТИЧЕСКИЕ СОЕДИНЕНИЯ | 2010 |
|
RU2536587C2 |
| НОВЫЕ АНТИБАКТЕРИАЛЬНЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2444526C2 |
| ПРОИЗВОДНЫЕ ДИБЕНЗООКСАЗЕПИНА ИЛИ ДИБЕНЗОДИОКСЕПИНА И ПРОТИВООПУХОЛЕВАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2167871C2 |
| ВАНКОРЕЗМИЦИН (ВАРИАНТЫ), ЕГО ИСПОЛЬЗОВАНИЕ, ШТАММ AMYCOLATOPSIS ВИДА HIL-006734 ДЛЯ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2228337C2 |
| ТИОМАРИНОЛ B И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1993 |
|
RU2101353C1 |
| СОЕДИНЕНИЕ А-87774 ИЛИ ЕГО СОЛЬ, СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ И ЕГО СОЛИ И АГРОХИМИКАТ, СОДЕРЖАЩИЙ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2010 |
|
RU2545403C2 |
| ПРОП-2-ИН-1-ИЛ (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(АЦЕТИЛОКСИ)-3-(БУТИЛАМИНО)-11-ГИДРОКСИ-4,8,10,14-ТЕТРАМЕТИЛГОНАН-17-ИЛИДЕН]-6-МЕТИЛГЕПТ-5-ЕНОАТ, ПРОЯВЛЯЮЩИЙ АНТИБАКТЕРИАЛЬНУЮ И ФУНГИЦИДНУЮ АКТИВНОСТЬ | 2024 |
|
RU2841387C1 |
| ТИОМАРИНОЛ C И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2089548C1 |
| ПРОИЗВОДНЫЕ ЦЕФАЛОСПОРИНА, СОДЕРЖАЩАЯ ИХ АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ, ПРОИЗВОДНЫЕ 2-АМИНОТИАЗОЛОВ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2172317C2 |
| АНТИБИОТИК БАЛИМИЦИН, СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА БАЛИМИЦИНА, ШТАММ ACTINOMYCETESSPECIES DSM 5908 - ПРОДУЦЕНТ БАЛИМИЦИНА | 1991 |
|
RU2043418C1 |





В соответствующей питательной среде культивируют штамм К04-0144, относящийся к роду Streptomyces, обладающий способностью продуцировать группу соединений К04-0144, причем выделенные из него соединения К04-0144А, К04-0144В и К04-0144С обладают сильной антибактериальной активностью против грам-положительных бактерий, включая метициллин-устойчивых Staphylococcus aureus (MRSA), а соединение K04-0144D обладает усиливающей анти-MRSA активностью в комбинации с β-лактамовыми антибиотиками. Для выделенных соединений установлены химические структуры (I-IV), представленные в формуле изобретения. Описан выделенный из почвы штамм Streptomyces sp. K04-0144 NITE BP-107 - продуцент указанной группы соединений. Соединение K04-0144D, обладающее способностью усиливать действие β-лактамовых антибиотиков в комбинации с ними, применимо в качестве терапевтического средства для лечения инфекционных заболеваний, вызванных метициллин-устойчивыми Staphylococcus aureus (MRSA) и бактериями, обладающими мультилекарственной устойчивостью, в т.ч. устойчивых к β-лактамовым антибиотикам. Изобретение позволяет получить новые терапевтические препараты против MRSA- инфекций и инфекционных заболеваний, вызванных бактериями с мультилекарственной устойчивостью. 3 н.п. ф-лы, 16 ил., 3 табл.
1. Группа соединений К04-0144, включающая любое из следующих соединений: соединение К04-0144А формулы (I)
соединение К04-0144В формулы (II)
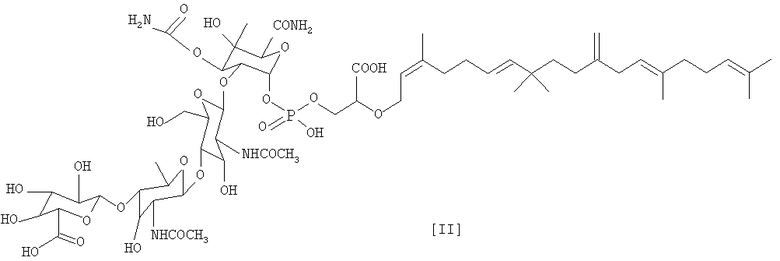
соединение К04-0144С формулы (III)
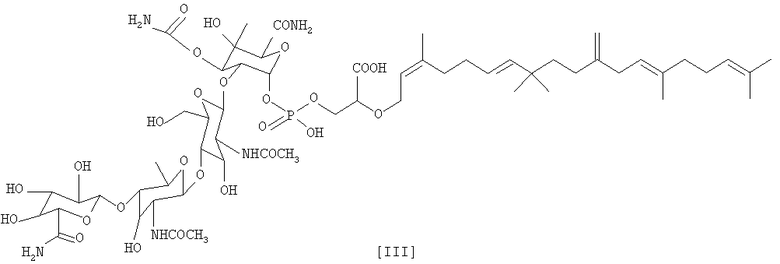
обладающие антимикробной активностью, и соединение K04-0144D формулы (IV)

увеличивающее анти-MRSA активность в комбинации с β-лактамовыми антибиотиками.
2. Способ получения группы соединений К04-0144, включающей К04-0144А, К04-0144В, К04-0144С и K04-0144D, обладающих антимикробной активностью, путем культивирования микроорганизма Streptomyces sp. К04-0144 NITE ВР-107, обладающего способностью продуцировать соединения К04-0144 в культуральной среде, накопления соединений К04-0144 в среде и выделения соединений К04-0144 из культуральной массы с последующим разделением на соединения К04-0144А, К04-0144В, К04-0144С и K04-0144D и их очисткой.
3. Streptomyces sp. K04-0144 NITE BP-107 - продуцент группы соединений К04-0144, обладающих антимикробной активностью и усиливающим действием.
| US 6207820 В1, 27.03.2001 | |||
| Усилитель | 1980 |
|
SU1069130A1 |
| ШТАММ STREPTOMYCES BAMBERGIENSIS - ПРОДУЦЕНТ МОЕНОМИЦИНА А | 1992 |
|
RU2013448C1 |
| MX 9802979 A2, 31.12.1998 | |||
| WO 03015709 A2, 27.02.2003. | |||
Авторы
Даты
2010-07-10—Публикация
2006-05-16—Подача