Изобретение относится к способам переработки титаномагнетитового концентрата, содержащего ванадий, и может быть использовано для получения титановых продуктов, чистого оксида железа и железованадиевого концентрата, пригодного для легирования чугунов, сталей и сплавов.
Титаномагнетитовые концентраты, содержащие, кроме 15-19% TiO2, 56-58% ΣFe и 0,3-1,5% V2O5, являются не только ценным титановым, но и ванадиевым сырьем. Потребление ванадия в мире, возрастающее ежегодно примерно на 2%, связано в основном с его использованием в производстве высокопрочных конструкционных, жаропрочных, быстрорежущих, инструментальных, нержавеющих и других сталей, чугунов, титановых сплавов, в цветной металлургии и др. отраслях промышленности. При переработке титаномагнетитовых концентратов наиболее распространенными пирометаллургическими методами не достигается высокая степень концентрирования ванадия в железосодержащем продукте, при этом существенная часть ванадия теряется с отходами, что снижает комплексность переработки сырья. Кроме того, пирометаллургические методы являются весьма энергоемкими и характеризуются выбросами серы в окружающую среду. В этой связи весьма перспективными являются гидрометаллургические методы. Однако существующие технологические разработки нуждаются в усовершенствовании с точки зрения повышения извлечения ценных компонентов и комплексности переработки сырья.
Известен способ переработки титаномагнетитового концентрата (см. пат. 2025524 РФ, МПК5 С22В 34/22, 34/12, 1994), включающий шихтование концентрата состава, мас.%: 56,43 в пересчете на ΣFe; 15,6 TiO2; 0,42 MgO; 2,6 SiO2; 1,0 V2O5; 1,6 Al2O3; 1,25 CaO; 0,08 S с восстановителем, содержащем серу в виде нефтяного кокса, и сульфидирующей добавкой CaSO4, которую берут в количестве 0,6-0,9% по отношению к концентрату, обжиг шихты в электропечи при 1200-1300°С в течение 2 ч, измельчение полученного спека и мокрую магнитную сепарацию. Полученный магнитный продукт содержит 0,34-0,45% V, 8,8-10,7% TiO2, до 0,1% S, остальное - железо. Извлечение железа в магнитный продукт составляет 96,6-97,1%. Магнитный продукт является сырьем для производства чугуна, легированного ванадием.
К недостаткам данного способа относится недостаточно высокая степень извлечения железа и ванадия в магнитный продукт, значительные потери титана с магнитным продуктом и высокая энергоемкость способа. В способе используются серосодержащие реагенты, что ведет к неизбежному загрязнению серой магнитного продукта, используемого для легирования чугунов и других сплавов, понижая его качество. Способ реализуется с привлечением разнопрофильных процессов и сложного оборудования, что снижает его технологичность.
Известен также способ переработки титаномагнетитового концентрата, с получением синтетического рутила (см. Reductive leaching of ilmenite ore in hydrochloric acid for preparation of synthetic rutile / Mahmoud M.H.H., Afifi A.A.I., Ibrahim I.A. // Hydrometallurgy. - 2004. - 73, №1-2. - С.99-109), включающий выщелачивание концентрата состава, мас.%: 41,1 TiO2; 24,4 FeO; 28,6 Fe2O3; 0,63 Al2O3; 0,64 MgO; 0,45 CaO; 0,36 Mn; 0,36 Cr2O3; 0,40 V2O5; 0,02 P2O5; 2,43 SiO2 с крупностью частиц менее 75 мкм раствором соляной кислоты с концентрацией 20% при расходе кислоты 1,2 от стехиометрии и температуре 110°С в течение 5 ч в присутствии металлического железа в количестве 1,1 от стехиометрии с переводом железа и ванадия в раствор выщелачивания и концентрированием титана в остатке - кеке. Раствор выщелачивания, содержащий железо и ванадий, упаривают для выделения FeCl2, который подвергают пиролизу для регенерации HCl и получения оксида железа. Титансодержащий кек подвергают сушке и прокаливанию при 110 и 900°С соответственно с получением синтетического рутила чистотой >90% TiO2. Общий выход TiO2 в рутил составил 97,7%, потери титана с раствором выщелачивания - 1,7%, эффективность очистки от Fe - 99,4%.
Известный способ характеризуется относительно невысокой степенью извлечения железа и ванадия в раствор выщелачивания, а титана - в остаток за счет потерь с раствором выщелачивания. Излишне высокая температура прокаливания титансодержащего кека обусловливает повышенную энергоемкость процесса. Ассортимент получаемых продуктов ограничен при их невысоком качестве: титансодержащий продукт получают только рутильной модификации с повышенным содержанием примесей, в том числе железа и ванадия, а оксид железа содержит большое количество примесей при низком соотношении V/Fe (около 0,4%).
Настоящее изобретение направленно на достижение технического результата, заключающегося в повышении степени извлечения ванадия, железа и титана, а также в расширении ассортимента и улучшении качества получаемых продуктов при снижении энергоемкости способа.
Технический результат достигается тем, что в способе переработки титаномагнетитового концентрата, включающем выщелачивание соляной кислотой при нагревании в присутствии металлического железа с переводом железа и ванадия в раствор выщелачивания и концентрированием титана в остатке, упаривание раствора с выделением железосодержащего осадка, пиролиз железосодержащего осадка с получением оксида железа и регенерированной соляной кислоты, сушку и прокаливание титансодержащего остатка с получением титанового продукта, согласно изобретению выщелачивание титаномагнетитового концентрата ведут при концентрации соляной кислоты 15-19% и температуре 95-105°С, из раствора выщелачивания осаждают железованадиевый продукт в виде осадка гидроксидов железа и ванадия путем обработки раствором аммиака при рН 2,4-2,8 с получением раствора хлорида железа (II), упариванию подвергают полученный раствор хлорида железа с выделением железосодержащего осадка и пиролизом осадка, а прокаливание титансодержащего остатка ведут при температуре 700-800°С.
Достижению технического результата способствует то, что при осаждении железованадиевого продукта используют раствор аммиака с концентрацией 100-120 г/л.
Достижению технического результата способствует также то, что осадок гидроксидов железа и ванадия прокаливают при температуре 350-500°С.
Сущность заявленного изобретения заключается в следующем. При обработке соляной кислотой титаномагнетитового концентрата, представляющего сложный оксид состава FeO·Fe2O3·TiO2 и включающего ильменит FeO·TiO2 и оксиды примесных элементов Si, Ca, Mn, Mg, Al, V, Со и др., происходит выщелачивание в солянокислый раствор (за исключением SiO2, растворимого только во фтористоводородной кислоте и остающегося в нерастворимом остатке) кислоторастворимых соединений металлов, в том числе и титана в виде его оксохлорида TiOCl2.
Растворение титаномагнетита протекает согласно реакции:
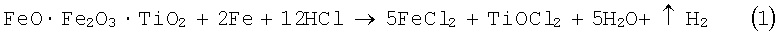
В раствор помимо железа и титана также полностью или частично переходят кислоторастворимые хлориды примесных металлов.
В процессе выщелачивания при повышенной температуре оксохлорид титана TiOCl2 гидролизуется с образованием осадка диоксида титана по реакции:
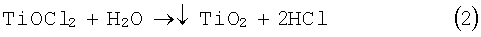
При пониженной концентрации соляной кислоты (менее 20%) снижается кислотность реакционной среды, что способствует более глубокому гидролизу оксохлорида титана TiOCl2 с образованием осадка диоксида титана, вследствие чего повышается его извлечение в нерастворимый остаток и соответственно снижаются потери титана с раствором выщелачивания. Растворимость хлоридов железа (II) и примесных металлов, образующих простые хлориды, с понижением концентрации соляной кислоты увеличивается, что сопровождается повышением извлечения железа и ванадия в раствор выщелачивания. Все это способствует более высокой степени разделения титана с железом и примесными металлами и соответственно повышению очистки титанового продукта. Пониженная концентрация соляной кислоты позволяет осуществить процесс при более низкой температуре (105°С и менее). Выделение диоксида титана из раствора, содержащего значительное количество ионов других элементов, приводит к формированию метастабильного анатаза, сухой нанодисперсный порошок которого обладает высокой удельной поверхностью и фотокаталитической активностью, что позволяет использовать его в качестве фотокатализатора. Особенности формирования анатаза в растворе выщелачивания определяет и более низкую температуру фазового перехода анатазного диоксида титана в рутил, что способствует снижению энергоемкости способа.
Обработка полученного раствора выщелачивания щелочным реагентом, преимущественно раствором аммиака, приводит к образованию объемного коллоидного осадка гидроксида железа (III), обладающего развитой поверхностью и коагулирующими свойствами, присутствие которого в солянокислом растворе выщелачивания железа (II) определяется протеканием в присутствии кислорода реакции окисления железа (II) в железо (III) с одновременным гидролизом и образованием труднорастворимого гидроксида железа (III). Протеканию этих реакций способствует повышение рН раствора.
Извлечение ванадия в железосодержащий осадок основано на его коагуляции гидроксидами железа. При величине рН 2,4-2,8 извлечение ванадия из раствора FeCl2 достигает 99,98%, в то время как извлечение в осадок непосредственно железа составляет 14,4-19,6%. При этом около 80% железа остается в растворе. Помимо ванадия происходит коагуляция и других примесных металлов: Al, Mn, Cr, Ca, Mg, Co и др., что ведет к очистке раствора хлорида железа (II) и обеспечивает при последующей термической обработке получение чистого оксида железа с содержанием основного вещества не менее 99,3%.
Существенные признаки заявленного изобретения, определяющие объем правовой охраны и достаточные для получения вышеуказанного технического результата, выполняют функции и соотносятся с результатом следующим образом.
Выщелачивание титаномагнетитового концентрата соляной кислотой ведут при концентрации кислоты 15-19%, что обеспечивает высокие технические показатели процесса выщелачивания. Использование соляной кислоты пониженной концентрации способствует повышению растворимости железа и других кислоторастворимых примесных соединений и усиливает гидролиз оксихлорида титана, что повышает степень извлечения целевых компонентов и их разделение. Однако снижение концентрации соляной кислоты ниже 15% приводит к снижению эффективности выщелачивания, ведет к необоснованному увеличению технологических потоков и повышению энергозатрат при их обработке. Повышение концентрации кислоты выше 19% приводит к увеличению растворимости соединений титана и соответствующему увеличению его потерь с раствором.
Выщелачивание титаномагнетитового концентрата при температуре 95-105°С обусловлено концентрациями используемой соляной кислоты и соображениями обеспечения требуемой эффективности процесса. Снижение температуры ниже 95°С приводит к снижению степени извлечения железа в раствор выщелачивания и ведет к увеличению продолжительности операции выщелачивания. Повышение температуры выше 105°С является нежелательным, поскольку не приводит к существенному увеличению степени извлечения железа в раствор.
Обработка раствора выщелачивания щелочным реагентом - раствором аммиака при рН 2,4-2,8 позволяет осуществить частичный перевод из раствора в осадок коллоидного гидроксида железа (III) с практически полной коагуляцией на нем ванадия. В качестве щелочного реагента могут быть использованы также щелочи натрия и калия, однако они более дорогостоящие и вносят в конечные продукты свои катионы, что нежелательно. В результате обработки раствора выщелачивания получают железованадиевый продукт в виде осадка гидроксидов железа и ванадия и раствор хлорида железа (II), который подвергают упариванию с выделением железосодержащего осадка и пиролизом полученного осадка. Полученный раствор чистого хлорида железа (II) характеризуется пониженным содержанием не только ванадия, но и других примесных металлов: Са, Mn, Mg, Al, Co.
Понижение рН гидролиза ниже 2,4 ведет к уменьшению степени извлечения ванадия из раствора в железованадиевый осадок и повышению остаточной концентрации ванадия в растворе хлорида железа (II), который упаривают с получением железосодержащего осадка, подвергаемого пиролизу. Повышение рН выше 2,8 приводит к необоснованному повышению степени извлечения железа в железованадиевый осадок и соответственно к снижению в последнем соотношения ванадия и железа (V/Fe<2,3%), поскольку при указанном рН извлечение ванадия в осадок достигает практически 100%.
Прокаливание титансодержащего остатка при температуре 700-800°С обеспечивает полноту перехода диоксида титана из анатазной модификации в рутил. Прокаливание титансодержащего остатка при температуре менее 700°С не гарантирует полноты трансформации анатаза в рутил, а прокаливание при более 800°С технологически нецелесообразно.
Совокупность вышеуказанных признаков необходима и достаточна для достижения технического результата изобретения, заключающегося в повышении степени извлечения ванадия, железа и титана, а также в расширении ассортимента и улучшении качества получаемых продуктов при снижении энергоемкости способа.
В частных случаях осуществления изобретения предпочтительны следующие конкретные операции и режимные параметры.
Обеспечение заданного интервала значений рН при осаждении железованадиевого продукта может быть осуществлено растворами аммиака различных концентраций. Однако предпочтительно использование раствора аммиака с концентрацией 100-120 г/л, что обеспечивает плавное и контролируемое изменение рН реакционной среды. Повышение концентрации раствора аммиака выше 120 г/л усложняет поддержание рН в заданном интервале значений. Снижение концентрации аммиака ниже 100 г/л ведет к необоснованному увеличению объема технологических растворов.
Прокаливание осадка гидроксидов железа и ванадия при температуре 350-500°С обеспечивает дегидратацию гидроксидов и кристаллизацию оксидов железа и ванадия с получением железованадиевого продукта в виде оксидов железа и ванадия.
Вышеуказанные частные признаки изобретения позволяют осуществить способ в оптимальном режиме с точки зрения получения высоких технологических показателей процесса.
Сущность заявляемого изобретения и его преимущества могут быть пояснены следующими Примерами конкретного выполнения.
Пример 1. 100 г титаномагнетитового концентрата, измельченного до крупности менее 40 мкм и содержащего, мас.%: 16,6 TiO2; 1,96 SiO2; 43,0 FeO; 35,0 Fe2O3 (57,9 в пересчете на ΣFe); 0,59 V2O5 (0,33 в пересчете на V); остальное - примеси, обрабатывают в присутствии металлического железа 19% соляной кислотой, взятой с 20% избытком по отношению к общему количеству железа. Металлическое железо берут в виде стружки с 10% избытком относительно содержания железа (III). Выщелачивание ведут при температуре 105°С в течение 7 часов с последующим охлаждением до 25°С. Титансодержащий остаток отделяют фильтрацией от раствора выщелачивания. Извлечение железа в раствор выщелачивания составило 99,6%, ванадия - 98,7%, примесей - 97,0%, а титана в титансодержащий остаток - 98,9%. Раствор выщелачивания объемом 0,418 л, содержащий, г/л: 0,41 TiO2; 241,6 Fe2O3; 1,39 V2O5, 6,60 суммы примесей ΣМеО и 45,3 HCl, обрабатывают раствором аммиака с концентрацией 100 г/л при рН 2,4 с получением осадка гидроксидов железа и ванадия, и 0,437 л раствора хлорида железа (II), содержащего, г/л: 198,3 Fe2O3; 0,089 V2O5; 1,26 суммы примесей ΣМеО; 41,2 HCl. Осадок отделяют фильтрацией. Извлечение железа в осадок массой 20,2 г составило 14,4%, ванадия - 93,3%, суммы примесей - 80%. Полученный железованадиевый продукт содержит, мас.%: 0,88 TiO2; 75,7 Fe2O3; 2,82 V2O5; 20,6 - сумма примесей. Соотношение в железованадиевом продукте V/Fe 2,98. Раствор хлорида железа (II) упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 87,24 г состава, мас.%: 99,32 Fe2O3; 0,04 V2O5; 0,64 суммы примесей ΣМеО. Полученный титансодержащий остаток сушат при 110°С. Доля анатазной формы TiO2 в сухом титановом продукте массой 22,06 г равна 100%. Сухой титановый продукт содержит, мас.%: 74,5 TiO2; 8,88 SiO2; 2,63 Fe2O3; 0,032 V2O5; 0,39 суммы примесей ΣMeO, в т.ч. 16,2% Н2О, и представляет собой нанодисперсный порошок со средним размером частиц 18 нм, обладающий фотокаталитической активностью в области излучений видимого света. После прокаливания сухого титанового продукта при температуре 800°С доля рутила в прокаленном титановом продукте массой 18,48 г составила 100%. Прокаленный титановый продукт содержит, мас.%: 88,9 TiO2; 10,6 SiO2; 3,14 Fe2O3; 0,038 V2O5; 0,46 суммы примесей ΣMeO.
Пример 2. 100 г титаномагнетитового концентрата состава по Примеру 1 обрабатывают аналогично Примеру 1. Отличие заключается в том, что обработку ведут 19% соляной кислотой при температуре 95°С. Извлечение железа в раствор выщелачивания составило 99,3%, ванадия - 98,8%, примесных металлов - 95%, а титана в титансодержащий остаток - 99%. Раствор выщелачивания объемом 0,418 л, содержащий, г/л: 3,97 ТiO2; 242,3 Fe2O3; 1,39 V2O5; 6,48 суммы примесей ΣМеО; 43,35 HCl, обрабатывают раствором аммиака с концентрацией 120 г/л при рН 2,5 с получением осадка гидроксидов железа и ванадия, и 0,437 л раствора хлорида железа (II), содержащего, г/л: 195,6 Fe2O3; 0,053 V2O5 (0,029 в пересчете на V); 1,17 суммы примесей ΣMeO, 39,4 HCl. Осадок отделяют фильтрацией и прокаливают при температуре 500°С. Извлечение железа в осадок массой 18,73 г составило 15,6%, ванадия - 96%, суммы примесей - 81%. Полученный железованадиевый продукт содержит, мас.%: 1,88 TiO2; 84,35 Fe2O3; 2,99 V2O5; 11,74 суммы примесей ΣМеО. Соотношение в железованадиевом продукте V/Fe 2,83. Раствор хлорида железа (II) упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 86,03 г состава, мас.%: 99,38 Fe2O3; 0,03 V2O5; 0,59 суммы примесей ΣМеО. Полученный титансодержащий остаток сушат при 110°С. Доля анатазной формы TiO2 в сухом титановом продукте массой 23,05 г равна 100%. Сухой титановый продукт содержит, мас.%: 71,28 TiO2; 8,50 SiO2; 2,52 Fe2O3; 0,03 V2O5; 0,61 суммы примесей ΣМеО, в т.ч. 17,6% Н2О, и представляет собой нанодисперсный порошок со средним размером частиц 14 нм, обладающий фотокаталитической активностью в области излучений видимого света. После прокаливания сухого титанового продукта при температуре 700°С доля рутила в прокаленном титановом продукте массой 19,0 г составила 100%. Прокаленный титановый продукт содержит, мас.%: 86,47 TiO2; 10,32 SiO2; 3,05 Fe2O3; 0,037 V2O5; 0,73 суммы примесей ΣМеО.
Пример 3. 100 г титаномагнетитового концентрата состава по Примеру 1 обрабатывают аналогично Примеру 1. Отличие заключается в том, что обработку ведут 17% соляной кислотой при температуре 105°С. Извлечение железа в раствор выщелачивания составило 99,6%, ванадия - 98,6%, примесей - 97%, а титана в титансодержащий остаток - 99,2%. Раствор выщелачивания объемом 0,470 л, содержащий, г/л: 0,28 TiO2; 216,0 Fe2O3; 1,24 V2O5; 5,87 суммы примесей ΣМеО, 38,6 HCl, обрабатывают раствором аммиака с концентрацией 100 г/л при рН 2,6 с получением осадка гидроксидов железа и ванадия, и 0,492 л раствора хлорида железа (II), содержащего, г/л: 206,1 Fe2O3; 0,002 V2O5; 1,02 суммы примесей ΣМеО; 35,1 HCl. Осадок отделяют фильтрацией и прокаливают при температуре 450°С. Извлечение железа в осадок массой 20,02 г составило 16,8%, ванадия - 99,8% и суммы примесей - 82%. Полученный железованадиевый продукт содержит, мас.%: 0,65 TiO2; 85,15 Fe2O3; 2,9 V2O5; 11,3 суммы примесей ΣМеО. Соотношение в железованадиевом продукте V/Fe 2,73. Раствор хлорида железа (II) упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 101,9 г состава, мас.%: 99,51 Fe2O3; 0,001 V2O5; 0,489 суммы примесей ΣМеО. Полученный титансодержащий остаток сушат при 110°С. Доля анатазной формы TiO2 в сухом титановом продукте массой 22,72 г равна 100%. Сухой титановый продукт содержит, %: 72,49 TiO2; 8,63 SiO2; 1,45 Fe2O3; 0,035 V2O5; 0,40 суммы примесей ΣМеО, в т.ч. 17% Н2О, и представляет собой нанодисперсный порошок со средним размером частиц 13 нм, обладающий фотокаталитической активностью в области излучений видимого света. После прокаливания сухого титанового продукта при температуре 750°С доля рутила в прокаленном титановом продукте массой 18,86 г составила 100%. Прокаленный титановый продукт содержит, мас.%: 87,3 TiO2; 10,39 SiO2; 1,75 Fe2O3; 0,042 V2O5; 0,48 суммы примесей ΣМеО.
Пример 4. 100 г титаномагнетитового концентрата состава по Примеру 1 обрабатывают аналогично Примеру 1. Отличие заключается в том, что обработку ведут 15% соляной кислотой при температуре 100°С. Извлечение железа в раствор выщелачивания составило 99,4%, ванадия - 98,7%, примесей - 96,9%, а титана в титансодержащий остаток - 99,3%. Раствор выщелачивания объемом 0,537 л, содержащий, г/л: 0,22 TiO2; 188,6 Fe2O3; 1,08 V2O5; 5,14 суммы примесей ΣМеО; 33,7 HCl, обрабатывают раствором аммиака с концентрацией 100 г/л при рН 2,7 с получением осадка гидроксидов железа и ванадия и 0,563 л раствора хлорида железа (II), содержащего, г/л: 147,2 Fe2O3; 0,004 V2O5; 0,48 суммы примесей ΣМеО; 30,6 HCl. Осадок отделяют фильтрацией и прокаливают при температуре 400°С. Извлечение железа в осадок массой 21,41 г составило 18,2%, ванадия - 99,87% и суммы примесей - 83%. Полученный железованадиевый продукт содержит, мас.%: 0,56 TiO2; 86,05 Fe2O3; 2,71 V2O5; 10,68 суммы примесей ΣМеО. Соотношение в железованадиевом продукте V/Fe 2,51. Раствор хлорида железа (II) упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 83,34 г состава, мас.%: 99,43 Fe2O3; 0,003 V2O5; 0,567 суммы примесей ΣМеО. Полученный титансодержащий остаток сушат при 110°С. Доля анатазной формы TiO2 в сухом титановом продукте массой 22,98 г равна 100%. Сухой титановый продукт содержит, мас.%: 71,71 TiO2; 8,53 SiO2; 2,13 Fe2O3; 0,033 V2O5; 0,38 суммы примесей ΣМеО, в т.ч. 17,2% Н2О, и представляет собой нанодисперсный порошок со средним размером частиц 11 нм, обладающий фотокаталитической активностью в области излучений видимого света. После прокаливания сухого титанового продукта при температуре 800°С доля рутила в прокаленном титановом продукте массой 19,03 г составила 100%. Прокаленный титановый продукт содержит, мас.%: 86,6 TiO2; 10,3 SiO2; 2,57 Fe2O3; 0,04 V2O5; 0,46 суммы примесей ΣМеО.
Пример 5. 100 г титаномагнетитового концентрата состава по Примеру 1 обрабатывают аналогично Примеру 1. Отличие заключается в том, что обработку ведут 15% соляной кислотой при температуре 95°С. Извлечение железа в раствор выщелачивания составило 99,1%, ванадия - 98,8%, примесей - 96,7%, а титана в титансодержащий остаток - 99,2%. Раствор выщелачивания объемом 0,537 л, содержащий, г/л: 0,24 TiO2; 188,3 Fe2O3; 1,08 V2O5; 5,13 суммы примесей ΣMeO; 33,7 HCl, обрабатывают раствором аммиака с концентрацией 110 г/л при рН 2,8 с получением осадка гидроксидов железа и ванадия и 0,564 л раствора хлорида железа (II), содержащего, г/л: 144,1 Fe2O3; <0,001 V2O5; 0,79 суммы примесей ΣМеО; 33,8 HCl. Осадок отделяют фильтрацией и прокаливают при температуре 350°С. Извлечение железа в осадок массой 22,83 г составило 19,6%, ванадия - 99,98% и суммы примесей - 84%. Полученный железованадиевый продукт содержит, мас.%: 1,57 TiO2; 86,76 Fe2O3; 2,55 V2O5; 10,12 суммы примесей ΣMeO. Соотношение в железованадиевом продукте V/Fe 2,36. Раствор хлорида железа (II) упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 81,73 г состава, мас.%: 99,45 Fe2O3; 0,0002 V2O5; 0,546 суммы примесей ΣMeO. Полученный титансодержащий остаток сушат при 110°С. Доля анатазной формы TiO2 в сухом титановом продукте массой 23,16 г равна 100%. Сухой титановый продукт содержит, мас.%: 71,1 TiO2; 8,46 SiO2; 3,2 Fe2O3; 0,03 V2O5; 0,41 суммы примесей ΣMeO, в т.ч. 16,8% Н2О, и представляет собой нанодисперсный порошок со средним размером частиц 16 нм, обладающий фотокаталитической активностью в области излучений видимого света. После прокаливания сухого титанового продукта при температуре 700°С доля рутила в прокаленном титановом продукте массой 18,62 г составила 100%. Прокаленный титановый продукт содержит, мас.%: 85,47 TiO2; 10,17 SiO2; 3,84 Fe2O3; 0,036 V2O5; 0,49 суммы примесей ΣМеО.
Пример 6. 100 г титаномагнетитового концентрата, измельченного до крупности менее 75 мкм и содержащего, мас.%: 41,1 TiO2; 2,43 SiO2; 24,4 FeO; 28,6 Fe2O3; 0,40 V2O5; остальное - примеси, в присутствии металлического железа обрабатывают 20% соляной кислотой, взятой с 20% избытком по отношению к общему количеству железа. Металлическое железо берут с 10% избытком относительно содержания железа (III) в концентрате. Выщелачивание ведут при температуре 110°С в течение 5 часов с последующим охлаждением. Титансодержащий остаток отделяют фильтрацией от раствора выщелачивания. Извлечение железа в раствор выщелачивания составило 98,8%, ванадия - 88,98%, примесных металлов - 95%, а титана в титансодержащий остаток - 97,7%. Раствор выщелачивания объемом 0,358 л, содержащий, г/л: 2,65 TiO2; 198,86 Fe2O3; 0,99 V2O5; 8,16 суммы примесей ΣMeO; 50,8 НС1, упаривают с выделением осадка FeCl2, который подвергают пиролизу с получением регенерированной соляной кислоты и оксида железа массой 75,46 г состава, мас.%: 94,4 Fe2O3; 0,47 V2O5; 5,13 суммы примесей ΣМеО. Соотношение в оксиде железа V/Fe 0,40. Полученный титансодержащий остаток сушат и прокаливают при 110°С и 900°С соответственно с получением титанового продукта - синтетического рутила массой 43 г, содержащего, мас.%: 91,0% TiO2; 5,8 SiO2; 0,77 Fe2O3; 0,10 V2O5; 1,83 суммы примесей ΣMeO.
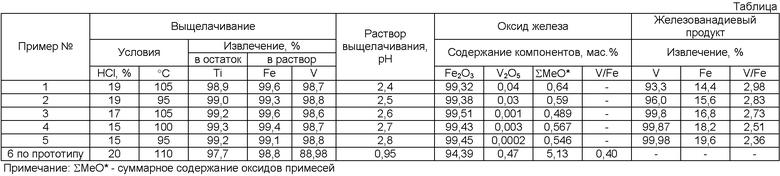
Основные технологические параметры и полученные результаты по Примерам 1-5 согласно заявляемому способу, а также по Примеру 6 по прототипу представлены в Таблице.
Как видно из данных, приведенных в Примерах и Таблице, использование предлагаемого способа обеспечивает повышение извлечения титана в титансодержащий остаток и соответственно титановый продукт - до 99,3%, а извлечения железа и ванадия в раствор выщелачивания - до 99,6% и 98,8% соответственно. Титановый продукт может быть получен в двух модификациях: в виде нанодисперсного анатаза, обладающего фотокаталитическими свойствами, и/или рутила. Дополнительная обработка раствора выщелачивания раствором аммиака обеспечивает практически полное извлечение ванадия и около 20% железа в железованадиевый продукт при содержании в нем V2O5 2,55-2,99 мас.% с повышенным (до 2,98%) соотношением V/Fe. Железованадиевый продукт в сухом виде является сырьем для получения соединений ванадия, а прокаленный - может быть использован для легирования различных сплавов. Способ позволяет получить чистый оксид железа с содержанием не менее 99,3 мас.% Fe2O3. Способ расширяет ассортимент получаемых продуктов повышенного качества. Реализация предлагаемого способа при пониженной температуре прокаливания позволяет снизить его энергоемкость.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ ТИТАНОМАГНЕТИТОВОГО КОНЦЕНТРАТА | 2009 |
|
RU2410449C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ И ОБЕЗВРЕЖИВАНИЯ ПОЛИМЕТАЛЛИЧЕСКИХ ОТХОДОВ ПРОИЗВОДСТВА | 2001 |
|
RU2194782C1 |
| Способ переработки ильменитового концентрата | 2019 |
|
RU2715192C1 |
| СПОСОБ ПЕРЕРАБОТКИ ТИТАНСОДЕРЖАЩЕГО СЫРЬЯ | 1998 |
|
RU2139249C1 |
| СПОСОБ ПЕРЕРАБОТКИ ТИТАНСОДЕРЖАЩЕГО МАТЕРИАЛА | 2014 |
|
RU2571904C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПЕРОВСКИТОВОГО КОНЦЕНТРАТА | 2003 |
|
RU2244726C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЖЕЛЕЗОТИТАНОВОГО КОНЦЕНТРАТА | 2008 |
|
RU2385962C1 |
| Способ комплексной переработки титансодержащего минерального сырья | 2016 |
|
RU2620440C1 |
| ПОЛУЧЕНИЕ ДИОКСИДА ТИТАНА | 2019 |
|
RU2786064C2 |
| Способ получения искусственного рутила из обогащенных титансодержащих продуктов переработки титаномагнетитов | 1985 |
|
SU1414782A1 |
Изобретение относится к переработке титаномагнетитового концентрата, содержащего ванадий, и может быть использовано для получения титановых продуктов, чистого оксида железа и железованадиевого концентрата, пригодного для легирования чугунов, сталей и сплавов. Способ переработки титаномагнетитового концентрата включает выщелачивание концентрата соляной кислотой при нагревании в присутствии металлического железа с переводом железа и ванадия в раствор выщелачивания и концентрированием титана в остатке. Затем проводят упаривание раствора с выделением железосодержащего осадка, пиролиз железосодержащего осадка с получением оксида железа и регенерированной соляной кислоты, а также сушку и прокаливание титансодержащего остатка с получением титанового продукта. При этом выщелачивание титаномагнетитового концентрата ведут при концентрации соляной кислоты 15-19% и температуре 95-105°С. Из раствора выщелачивания осаждают железованадиевый продукт в виде осадка гидроксидов железа и ванадия путем обработки раствором аммиака при рН 2,4-2,8 с получением раствора хлорида железа (II). Подвергают упариванию полученный раствор хлорида железа с выделением железосодержащего осадка и пиролизом осадка. Прокаливание титансодержащего остатка ведут при температуре 700-800°С. Техническим результатом является получение чистого оксида железа с содержанием не менее 99,3 мас.% Fe2O3. 2 з.п. ф-лы, 1 табл.
1. Способ переработки титаномагнетитового концентрата, включающий выщелачивание соляной кислотой при нагревании в присутствии металлического железа с переводом железа и ванадия в раствор выщелачивания и концентрированием титана в остатке, упаривание раствора с выделением железосодержащего осадка, пиролиз железосодержащего осадка с получением оксида железа и регенерированной соляной кислоты, сушку и прокаливание титансодержащего остатка с получением титанового продукта, отличающийся тем, что выщелачивание титаномагнетитового концентрата ведут при концентрации соляной кислоты 15-19% и температуре 95-105°С, из раствора выщелачивания осаждают железованадиевый продукт в виде осадка гидроксидов железа и ванадия путем обработки раствором аммиака при рН 2,4-2,8 с получением раствора хлорида железа (II), упариванию подвергают полученный раствор хлорида железа с выделением железосодержащего осадка и пиролизом осадка, а прокаливание титансодержащего остатка ведут при температуре 700-800°С.
2. Способ по п.1, отличающийся тем, что при осаждении железованадиевого продукта используют раствор аммиака с концентрацией 100-120 г/л.
3. Способ по п.1 или 2, отличающийся тем, что осадок гидроксидов железа и ванадия прокаливают при температуре 350-500°С.
| MAHMOUD M.H.H., AFIFI A.A.I., IBRAHIM LA | |||
| Hydrometallurgy, 2004, 73, №l-2, c.99-109 | |||
| US 6375923 B, 23.04.2002 | |||
| РУТИЛЬНЫЙ ДИОКСИД ТИТАНА И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1996 |
|
RU2171228C2 |
| US 6048505 А, 11.04.2000 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 5277816 А, 11.01.1994. | |||
Авторы
Даты
2010-07-20—Публикация
2009-03-04—Подача