Изобретение относится к области химии, а именно к аналитической химии, и может быть использовано для определения энантиомеров верапамила в субстанциях, таблетках и образцах плазмы крови методом ВЭЖХ.
Уровень техники
Есть два подхода получения энантиомерно чистых веществ: ассиметрический синтез требующихся изомеров и расщепление рацемической смеси на индивидуальные изомеры. Различные синтетические методы, позволяющие получить (определить) индивидуальные изомеры верапамила, были описаны в работе (1). Метод расщепления рацемической смеси включает рекристаллизацию солей диастереомеров, формирование диастереомерных дериватов вследствие хроматографического разделения на ахиральной неподвижной фазе и точное хроматографическое разделение энантиомеров на хиральной неподвижной фазе или хиральной подвижной фазе. Разделение верапамила методом рекристаллизации диастереоизомерных солей описано в работе (2). Эти методы сложны и трудоемки.
В работе (3) предложен простой и быстрый метод ВЖЭХ определения для точного разделения стереоизомеров верапамила. Этот метод включал присоединение ахиральной преколонки Brownlee (Applied Biosystems, San Jose, CA, USA) C18 NewGuard cartridge к хиральной обратно-фазовой колонке 250 mm × 4.6 mm CHIRAL OD-R CSP (Exton, PA, USA). При этом скорость потока составляла - 0,8 мл/мин. Однако сходные подвижные фазы (40% ацетонитрил в 0.2 М NaClO4), используемые для двух колонок, не позволяли выполнить хроматографическое определение оптимально, так как каждая хроматографическая ступень не проводилась с оптимальными условиями, и пики энантиомеров расширялись вследствие диффузии образцов при переходе из одной колонки в другую. Кроме того, время определение было длительным.
В работе (4) была решена эта проблема, используя улучшенный метод переключения высокоэффективных жидкостных хроматографических колонок. Метод был адаптирован для определения верапамила посредством присоединения ахиральной обратно-фазовой колонки (150×4.6 mm I.D. Inertsil ODS-2 column (Gasukuro Kogyo, Tokyo, Japan)) к овомукоидной колонке (протеин овомукоид, иммобилизированный на аминопропиловом силикагеле 150×4.6 mm I.D. Ultron ES-OVM (Shinwa Kako, Kyoto, Japan)). Чтобы помешать подвижной фазе первой колонки из нее течь во вторую колонку, была вставлена дилютирующая трубка и фильтрующая колонка (10×4.0 mm I.D. Ultron ES-OVMG column (ахиральная) ПФ: К2НРO4 и КН2РO4 рН 7.5 (20 mM) элюат (верапамил)/ ПФ=1:9) между двумя колонками, посредством которых подвижная фаза первой колонки (5 mM натрия 1-пентансульфонат с ацетонитрилом с водой (3:7, v/v), доводят рН до 3.0, добавляя фосфорную кислоту) была полностью заменена для того, чтобы во второй колонке была наиболее подходящая фаза (тетрагидрофуран-этанол-вода (1:8:91, v/v/v), содержащий 20mM КН2РO4). При этом длина волны λ составляла 230 нм, а скорость потока во всех колонках кроме фильтрующей - 1.0 мл/мин, в фильтрующей колонке - 4,0 мл/мин, t°C колонок была комнатная.
В обоих исследованиях ахиральная колонка была присоединена к хиральной колонке или к системе колонок. Посредством этих систем определялась фармакокинетика верапамила, но они сложны в применении и занимают слишком много времени.
В работе (5) используется диол-силикагелевая колонка (ахиральная преколонка 50 mm × 4.0 mm I.D. LiChrocart DIOL column (5 µm, Merk, Darmstadt, Germany)) и хиральная колонка на дериватах 3,5-диметилфенилкарбамат амилозы, покрытых силикагелем (250 mm × 4.6 mm I.D.Chiralpak AD column (10 µm, Daicel Chemical Industries, Tokyo, Japan)), которые соединены последовательно. При этом длина волны λех составляла 272 нм и λеm 317 нм, а скорость потока во всех колонках - 1.0 мл/мин, t°C в ахиральной колонке была 22°С, а в хиральной - 30°С.
Способ, предложенный в этом исследовании, проще, чем два предыдущих, так как в нем не применяется метод переключения колонок. Однако в работе (5) исследование предполагает наличие двух колонок - ахиральной и хиральной, а также сложной для приготовления мобильной фазы (гексан-изопропанол-этанол (85:7.5:7.5 v/v/v)+триэтиламин, 1%).
В исследовании (6) используется для хроматографического определения одна обратно-фазовая колонка на целлюлозе (CHIRALCEL OD column 250 mm × 4.6 mm I.D.), но время определения достаточно велико - 20 минут, а также сложна в объемном приготовлении мобильная фаза (ацетонитрил-0.05 М NaClO4 (pH 3.0 с НСlO4) (33:67)). При этом длина волны λ 205 нм, а скорость потока в колонке - 1.0 мл/мин.
В работе (7) используется также одна колонка (250 mm × 4.6 mm CHIRAL OD-R column), в одном случае - время определения оптимально, но мобильная фаза также сложна в приготовлении (0.5 М pH 2 NaClO4 / СН3СН=60/40 (v/v)) (40% aq ацето-нитрил Н2O/СН3СN=60/40 (v/v)) и требует для этого дополнительное время, в другом случае мобильная фаза менее сложная (0.1 М водный (aq) NaPF6/CH3CN=60/40 v/v), но время определения увеличивается до 30 минут. При этом длина волны λ 254 нм, а скорость потока в колонке - 0,5 мл/мин, температура в колонке - 25°С.
Последняя работа принята за прототип.
Поэтому целью настоящего изобретения является разработка оптимального - более простого, но точного метода количественного определения энантиомеров верапамила методом высокоэффективной жидкостной хроматографии (ВЭЖХ) как в субстанциях и таблетках, так и при изучении фармакодинамики и фармакокинетики препаратов верапамила в образцах плазмы.
Техническим результатом заявленного способа является расширение арсенала ВЭЖХ методик определения энантиомеров верапамила. Способ более простой в сравнении с известными, доступен в воспроизведении, а также обеспечивает снижение себестоимости исследовательских работ за счет оптимального выбора оборудования и реагентов.
Осуществление способа
На сегодняшний день наиболее перспективным в фармацевтическом производстве является изучение фармакокинетических и фармакодинамических свойств тех или иных хиральных изомеров с целью дальнейшего исследования этих знаний для улучшения лекарственных средств. Сегодня только 15% синтезируемых лекарств европейских стран созданы на основе определенного хирального изомера, остальные - значительно большая часть - смесь двух форм. Такие препараты могут давать весьма нежелательные явления. Среди них: значительное снижение фармакологической активности препарата, побочные эффекты, мутагенное и токсическое влияние на организм [8, 9, 10, 11]. Помимо малой эффективности подобные препараты могут оказывать серьезные побочные действия на печень, вынужденную справляться с обеими формами изомера, а также на другие органы. Это объясняет неэффективность некоторых синтезированных лекарственных средств, а также вред, который может приносить организму больного их прием.
Оптическая изомерия присуща многим лекарственным препаратам, одним из которых является верапамил.
В последние годы метод ВЭЖХ становится одним из самых распространенных методов анализа лекарственных средств в растворах, а также в биологическом материале, в том числе при изучении фармакокинетики. Это объясняется тем, что метод ВЖЭХ имеет ряд преимуществ по сравнению с другими: отсутствие ограничений по термоустойчивости и летучести анализируемого препарата, возможность работать с водными растворами, возможность собирать разделенные фракции для их последующей идентификации, высокая селективность, точность и чувствительность.
Экспериментальная часть
Разработка методики количественного определения любого лекарственного препарата из раствора включает в себя: подбор условий хроматографирования, количественный анализ.
Для подбора условий хроматографического разделения важное значение имеет выбор сорбента, типа детектора и условий детектирования, а также оптимального состава подвижной фазы и скорости ее подачи. Отрабатывая методику хроматографического разделения, следует добиваться условий, при которых должно быть достаточно хорошее разделение при минимальных затратах времени.
Изомеры верапамила (по литературным данным) определяются с использованием УФ- и флуориметрической детекции. Однако УФ-детекция позволяет анализировать стандарты верапамила и не может быть применена для определения верапамила в клинических образцах, таких как плазма. Поэтому в наших исследованиях мы использовали флуориметрическую детекцию с λех=230 нм и λеm=312 нм.
При подборе состава элюента мы исходили из соображений наилучшего разделения хроматографических пиков, а также доступности растворителей для анализа, простоты и быстроты приготовления подвижной фазы. Следует отметить, что выбор элюента и оптимизация условий разделения - задача достаточно сложная. Нами исследовались подвижные фазы ацетонитрил/вода, а также ацетонитрил/0,03 М КН2РO4 с различным соотношением компонентов. Подвижные фазы модифицировались введением триэтиламина и октасульфоновой кислоты.
Полученный элюент перед анализом фильтровали через фильтр Millipor (0,45) и дегазировали под вакуумом. Разделение проводили при комнатной температуре. Скорость потока (1 мл/мин) подвижной фазы выбирали исходя из времени анализа и давления на хроматографической колонке и определение проводили при комнатной температуре (22°С).
В наших исследованиях мы использовали подвижную фазу (ПФ): смесь ацетонитрила с 0,03 М фосфатным буфером в соотношении 10:90 (v/v) с добавлением 5% триэтиламина с рН 4,5, насос "Shimadzu", LG-6A, Liquid chromatograph, флюориметрический детектор "Shimadzu" (Япония), RF-530, Fluorescence HPLC monitor, с λех=230 нм и λem=312 нм, хиральную колонку ChiraDex® (250×4 мм, 5 µm) LiChroCart® HPLC-Cartridge, Merck, Germany, интегратор "Shimadzu", C-R3A, Chromatopac. Используется известная неподвижная фаза для ВЭЖХ хроматографии - ChiraDex®, которая основана на бета-циклодекстрине, ковалентно сшитым со сферическими частицами силикагеля.
Для приготовления фосфатного буфера брали 100 мл 0,03 М КН2РО4 прибавляли 10 мл 5% триметиламина и доводили рН до 4,5 ортофосфорной кислотой.
Для разработки методики количественного определения верапамила методом ВЖЭХ использовались следующие субстанции: смесь изомеров (SIGMA Germany) (+-) - Verapamil hydrochloride, minimum 99.0% titration (V 4629-1 G 114K0797), R (+)-Verapamil hydrochloride (V 106-5 MG, 124K4601), 5 мг растворяли в 2,5 мл раствора метанола,
S(-)-Verapamil hydrochloride, (>94%, V 105-5 MG, 038H4736), 5 мг растворяли в 2,5 мл раствора метанола.
По литературным данным известно, что R (+), S (-)-изомеры обладают разным фармакологическим действием. Используя разработанный нами метод, мы исследовали соотношение R (+) и S (-)-изомеров, а также их смесь в субстанциях различных производителей. Для этого нами были приготовлены стандартные растворы. Субстанции растворяли в 10 мл метанола или 0,01 М растворе соляной кислоты (НСl). В обоих этих растворителях верапамил растворялся очень хорошо. Для этого 10 мкг исследуемого вещества растворяли в 10 мл метанола или 0,01 М раствора соляной кислоты (НСl), затем к 1 мл полученного раствора добавляем 9 мл растворителя, например раствора НСl, перемешиваем и отбираем 50 мкл для хроматографической пробы. С течением времени в растворах R (+)-изомер переходит в S (-)-изомер.
Коэффициент емкости был равен k1R(+)=2,9, k2S(-)=4,0, коэффициент разделения составил α=1,36, а степень разделения Rs=1,3. Rs характеризует разделение двух пиков на хроматограмме и при Rs>1 наблюдается полное разделение двух компонентов смеси. Время удерживания tуд составило, приблизительно, 15 мин. R(+)-изомер элюируется первым.
Далее мы исследовали соотношение изомеров в субстанциях различных производителей. Представленные на изучение субстанции растворяли в 0,01 М НСl. В таблице 1 представлены результаты исследования.
Соотношение R (+)- и S (-) верапамила в изучаемых субстанциях
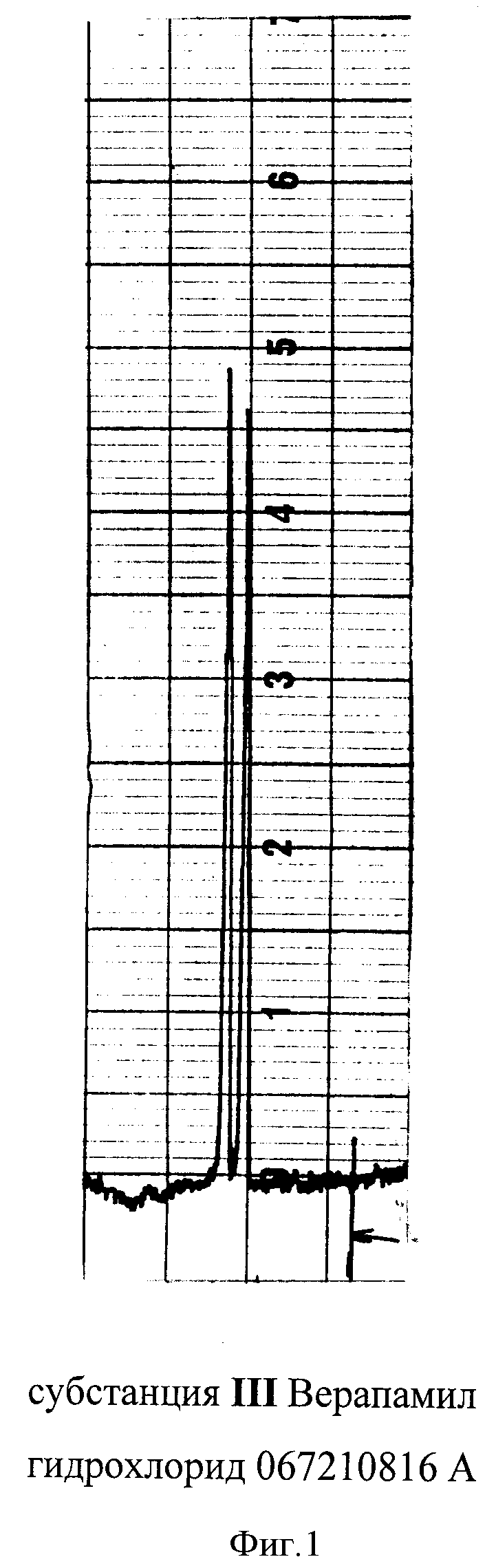
Как видно из таблицы 1, субстанции содержат как R (+)-изомер, так и S (-)-изомер верапамила. Во всех изученных субстанциях преобладает S (-)-изомер. В качестве примера на фиг.1 представлена хроматограмма анализа субстанции III Верапамила гидрохлорид 067210816 А и на фиг.2 субстанции VIВерапамила гидрохлорид 331204904 В.
Далее, мы изучали соотношение R (+)- и S (-)-изомеров верапамила в таблетках.
Для подготовки таблеток к анализу за основу взяли ФСП 42-0017183601 (с.9). 5 таблеток растирали в ступке. Затем 0,32 г растертых таблеток помещали в мерную колбу вместимостью 200 мл, добавляли 150 мл 0,01 М раствора кислоты хлористо-водородной, встряхивали в течение 10 минут. Доводили объем раствора 0,01 М раствором НСl до метки, перемешивали и фильтровали через бумажный фильтр, отбрасывая первые 20 мл фильтрата. Отбирают 50 мкл фильтрата, который анализируют методом ВЭЖХ.
Содержание R (+)- и S (-)-изомеров в таблетках практически одинаковое, однако R (+)-изомера ненамного больше.
На фиг.3 изображена хроматограмма анализа таблеток I Изоптин СР 240 мг АВВОТТ, Германия и на фиг.4 - VI Изоптин, таблетки покрытые оболочкой, 40 мг АВВОТТ, Германия.
Соотношение R (+) и S (-) изомеров верапамила в таблетках
Дозировка
Производитель
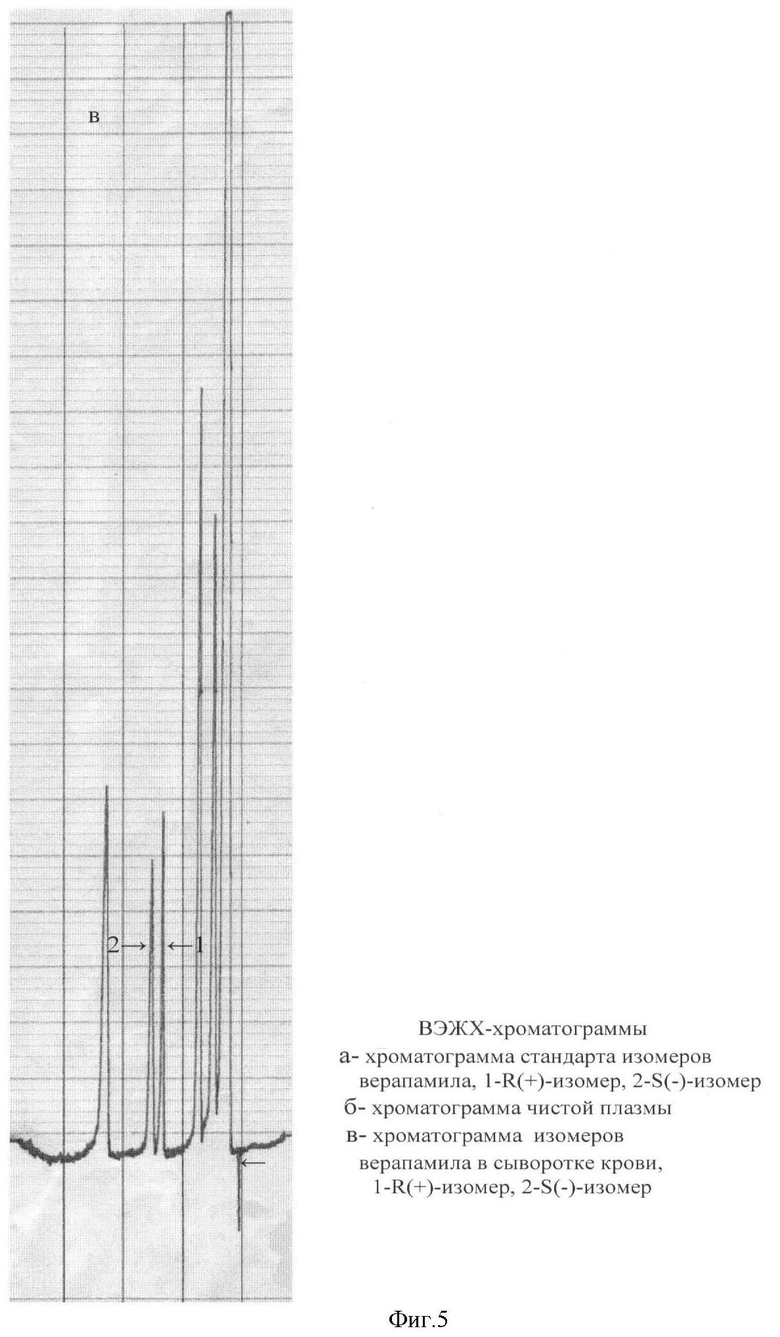
Метод также может быть успешно использован для определения изомеров верапамила в плазме, на фиг.5 представлены ВЭЖХ-хроматограмма стандарта изомеров верапамила, чистой плазмы и типичная хроматограмма изомеров верапамила в сыворотке крови в описанных условиях. Как видно на чертеже, хроматографические пики изомеров верапамила хорошо отделяются от пиков эндогенных веществ сыворотки крови.
Изучалась фармакокинетика изомеров верапамила после однократного приема препаратов: Финоптин (доза 80 мг, Финляндия).
Основной задачей фармакокинетических исследований лекарственных препаратов является повышение эффективности и безопасности их использования в клинической практике. Проблемы фармакокинетики: анализ скорости и интенсивности процессов всасывания, распределения по органам и тканям, направленности и количественной оценки процессов биотрансформации, путей и скорости выведения - в последние годы приобретают решающее значение при создании, испытании и разработке оптимального режима фармакотерапии лекарственными препаратами. Изучение судьбы лекарственного препарата в живом организме предполагает, в первую очередь, определение его содержания в крови. Поэтому, прежде чем приступить к изучению любых фармакокинетических процессов, необходимо выбрать метод количественного определения изучаемого лекарственного вещества в биологических средах.
Материалы и методы
В фармакокинетическое исследование было включено 7 добровольцев (мужчины) в возрасте 20-40 лет, с массой тела 65-80 кг, ростом 165-182 см, без патологий желудочного тракта, печени, почек, сердечно-сосудистой системы (предварительно проведенные клинико-лабораторные и инструментальные исследования не выявили наличия каких-либо заболеваний). В течение 14 дней до начала проведения испытания добровольцы не принимали никаких лекарственных препаратов. В день исследования Финоптин давали добровольцам натощак однократно внутрь по одной таблетке (80 мг). Отбор проб крови проводили через катетер до приема препарата и через 0.5, 1, 1.5, 2, 3, 4, 6, 8 и 12 часов после приема препарата. Образцы крови объемом 5-7 мл отбирали в пластиковые пробирки с гепарином, центрифугировали 10 минут при 3000 об/мин и отделенную плазму хранили до анализа замороженной при температуре -35°С.
При разработке аналитической методики важная роль отводится процессу пробоподготовки. Для подготовки образцов сыворотки крови более оптимальным является способ с применением жидкостной экстракции с последующим концентрированием пробы. Метод с использованием осаждения белков крови с последующим анализом надосадочной жидкости с помощью ВЭЖХ в нашем случае не применим из-за низкой чувствительности метода и большого количества эндогенных веществ, мешающих определению.
Анализ содержания изомеров верапамила в сыворотке крови проводили с помощью ВЭЖХ с флуоресцентной детекцией. Условия хроматографирования проводились аналогично с хроматографированием субстанций и таблеток после экстракции активных веществ.
Как известно, на полноту извлечения веществ из биологического материала органическими растворителями оказывает влияние ряд факторов: природа исследуемого вещества и экстрагента, кратность экстракции, объем экстрагента, рН среды. Детальное изучение экстракции верапамила было проведено такими органическими растворителями, как хлороформ, гексан, диэтиловый эфир, изопропиловый спирт с различными значениями рН среды. В наших исследованиях влияние на степень экстракции верапамила оказывали рН среды и природа экстрагента. Наилучшая степень экстракции была достигнута гексаном в нейтральной среде, коэффициент экстракции составил 79%.
Так, экстракцию проводили следующим образом: к образцу сыворотки крови объемом 1 мл добавляли 5 мл гексана, смесь подвергалась встряхиванию в течение 10 минут на горизонтальном встряхивателе, далее центрифугированию в течение 10 мин при 4500 об/мин, затем органический слой переносили в колбы и экстракт упаривали на роторном испарителе при 40°С. Сухой остаток растворяли в 150 мл подвижной фазы и 50 мкл полученного раствора вводили в хроматограф.
В нулевой точке (перед введением препарата) исследование проб крови у всех испытуемых не выявило в сыворотке R(+) и S(-)-верапамила. В последующие сроки наблюдения в пробах крови было обнаружено достаточное для анализа количество R(+) и S(-)-верапамила.
Анализ проб проводили на жидкостном хроматографе Shimadzu (Япония) с флуориметрической детекцией. Детектирование осуществляли при длине волны возбуждения - 230 нм, испускания - 312 нм.
Основой для количественного определения (метод абсолютной калибровки) R(+) и S(-)-верапамила в сыворотке крови служили калибровочные зависимости, для построения которых были проанализированы образцы сыворотки крови с различной концентрацией определяемых веществ.
При регрессионном анализе выявлена линейная зависимость между концентрацией изомеров верапамила в интервале 5-250 нг/мл и площадью хроматографического пика. Коэффициент корреляции для S(-)-верапамила составил r2=0,9854, для R(+)-верапамила - r2=0,9992.
Воспроизводимость метода шести повторов каждой исследованной концентрации находилась в пределах 90-100%, а коэффициент вариации при этом не превышал 10%.
Динамика концентраций S(-) и R(-)-изомеров верапамила в плазме крови добровольцев после однократного приема 80 мг препарата представлена в табл.3 и 4.
Динамика концентраций R(+) верапамила в плазме крови после однократного приема внутрь Финоптина в дозе 80 мг добровольцами, нг/мл
Динамика концентраций S(-) верапамила в плазме крови после однократного приема внутрь Финоптина в дозе 80 мг добровольцами, нг/мл
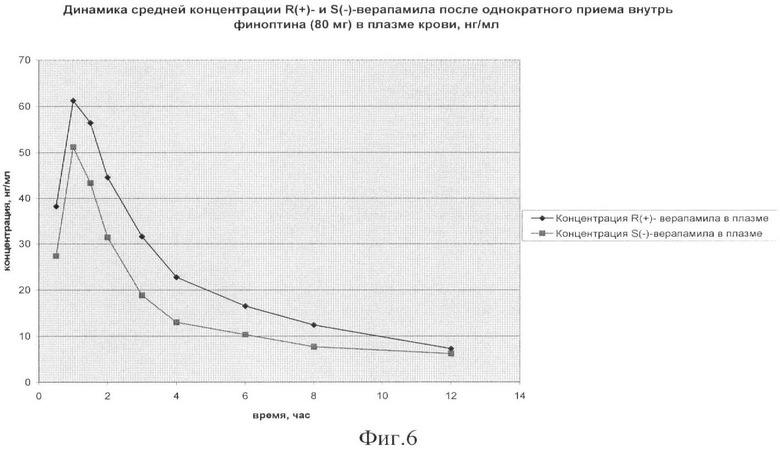
Значения усредненных концентраций S(-) и R(+)-верапамила в плазме крови добровольцев после однократного приема изучаемого препарата представлены на фиг.6.
Исследования показали, что S(-) и R(+)-верапамил после приема внутрь препарата Финоптин достаточно быстро всасывается в желудочно-кишечном тракте. Максимальная концентрация достигается через 1 час после приема препарата, затем происходит медленное экспоненциальное снижение концентрации. Однако концентрация R(+)-верапамила в 1,2±0,3 раза больше значений концентраций S(-)-верапамила во всех точках отбора.
Средние значения концентрации изомеров верапамила статистически достоверно не различались для каждого момента времени (для всех анализов результаты рассматривались как статистически достоверные, если уровень значимости по критерию Фишера F был ниже 0,05).
Следует отметить, что после приема препаратов имеет место межиндивидуальная вариация кинетических кривых во всех точках отбора крови (коэффициент вариации от 13,08 до 38,34%).
Выводы:
1. Нами разработана эффективная методика ВЭЖХ определения изомеров верапамила в субстанциях и таблетках. Относительная погрешность среднего результата ε% составляет от 1,74 до 3,39%. Также метод определения изомеров эффективен при определении в плазме.
2. Исследования показали, что в лекарственных препаратах верапамила содержатся и R(+)-и S(-)-изомеры, что необходимо учитывать при изучении фармакодинамики и фармакокинетики препаратов верапамила.
Литература
1. L.J.Theodore and W.L.Nelson. Stereospecific synthesis of enantiomers of verapamil and gallopamil. //J.Org. Chem., - 1987. - Vol.52(7). P.1309-1328.
2. G.Blaschke German Patent Application, 1987, No. P 3723684.9.
3. Asafu-Adjaye ЕВ, Shiu GK. Solid-phase extraction-high-performance liquid chromatography determination of verapamil and norverapamil enantiomers in urine. // J Chromatogr В Biomed Sci Appl. 1998 Apr 10; 707(1-2):161-7
4. Oda Y., Asakawa N., Kajima Т., Yoshida Y., Sato T. On-line determination and resolution of verapamil enantiomers by high-perfomance liquid chromatography with column switching.// Journal of chromatography, 1991, Vol.541, p.411-418.
5. Shibukawa A., Wainer I.W. Simultaneous direct determination of the enantiomers of verapamil and norverapamil in plasma using a derivatized amylose high-performance liquid chromatographic chiral stationary phase. //Journal of chromatography, 1992 Vol.574 NO. 1 February 7, p.85-92, Biomedical applications, Vol.112 No.1
6. Miller L, Bergeron R. Analytical and preparative resolution of enantiomers of verapamil and norverapamil using a cellulose-based chiral stationary phase in the reversed-phase mode.// Journal of chromatography, 1993, Vol.648, p.381-388.
7. Ishikawa A, Shibata T. Cellulosic chiral stationary phase under reversed-phase condition.// Jomal of liquid chromatography, 1993, Vol.16(4), p.859-878.
8. Eichelbaum M., Mikus G. and Vogelgesang B. Pharmacokinetics of (+)-, (-)-and (+/-)-verapamil after intravenous administration. //Br J Clin Pharmacol. - 1984.- Apr; 17(4). - P.453-458.
9. Echizen H., Vogelgesang B. and Eichelbaum M. Effects of d,l-verapamil on atrioventricular conduction in relation to its stereoselective first-pass metabolism.//Clin Pharmacol Ther. - 1985. - Jul; 38(1). - P.71-76.
10. Vogelgesang В., Echizen H., Schmidt E. et al. Stereoselective first-pass metabolism of highly cleared drugs: studies of the bioavailability of L- and D-verapamil examined with a stable isotope technique. // Br J Clin Pharmacol. - 1984. - Nov; 18(5). - P.733-740.
11. Echizen H., Brecht Т., Niedergaesass S., Vogelgesang B. et al. The effect of dextro-, levo-, and racemic verapamil on atrioventricular conduction in humans. //Am Heart J. - 1985. - Feb; 109(2). - P.210-217.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАЗДЕЛЕНИЯ ОПТИЧЕСКИХ ИЗОМЕРОВ АМЛОДИПИНА | 2008 |
|
RU2357781C1 |
| СПОСОБ МОДЕЛЬНО-ДИСКРИМИНАЦИОННОЙ ОЦЕНКИ ФАРМАЦЕВТИЧЕСКОЙ ЭКВИВАЛЕНТНОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПОКРЫТЫХ КИШЕЧНОРАСТВОРИМОЙ ОБОЛОЧКОЙ | 2016 |
|
RU2629397C2 |
| СПОСОБ АКТИВАЦИИ ИЗОФЕРМЕНТА Р450 (CYP) 3A4 У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2014 |
|
RU2554775C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭНАНТИОМЕРОВ ПЕРВИЧНЫХ АМИНОСОЕДИНЕНИЙ | 2006 |
|
RU2394236C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРНО ЧИСТЫХ (S)-АМИНОКИСЛОТ НА ОСНОВЕ КОМПЛЕКСА [(S)-BPB-GLy]Ni(II), НАПРЯМУЮ СВЯЗАННЫХ С ФУЛЛЕРЕНОВЫМ ЯДРОМ ЧЕРЕЗ α-УГЛЕРОДНЫЙ АТОМ, В ФОРМЕ ХИРАЛЬНЫХ (A) И (C) 1,4-АДДУКТОВ [60]ФУЛЛЕРЕНА | 2015 |
|
RU2614247C2 |
| Способ определения амиодарона и его основного метаболита дезэтиламиодарона в сыворотке крови человека | 2020 |
|
RU2749566C1 |
| Способ определения дабигатрана в сыворотке крови человека | 2018 |
|
RU2683032C1 |
| Способ количественного определения дексаметазона в биологических средах с помощью ВЭЖХ с ультрафиолетовым детектированием | 2022 |
|
RU2792274C1 |
| Лекарственная форма ДНК-аптамера | 2019 |
|
RU2730000C1 |
| Способ определения лозартана, его основного метаболита лозартан карбоновой кислоты и глибенкламида в сыворотке крови и моче человека | 2020 |
|
RU2749567C1 |



Изобретение относится к медицине и касается способа определения энантиомеров верапамила в субстанциях, таблетках и образцах плазмы крови методом ВЭЖХ. Изобретение обеспечивает расширение арсенала ВЭЖХ методик определения энантиомеров верапамила, простоту способа в сравнении с известными, доступность воспроизведения и снижение себестоимости исследовательских работ за счет оптимального выбора оборудования и реагентов. 6 ил., 4 табл.
Способ определения энантиомеров верапамила в субстанциях, таблетках и образцах плазмы крови методом ВЭЖХ, включающий определение энантиомеров на хиральной колонке ChiraDex® (250×4 мм, 5 мкм) с подвижной фазой: смесь ацетонитрила с 0,03 М фосфатным буфером в соотношении 10:90 (v/v) с добавлением 5% триэтиламина с рН 4,5, при скорости потока 1 мл/мин и комнатной температуре, флуориметрическую детекцию осуществляют при длине волны λех=230 нм и λem=312 нм.
| Способ определения азотосодержащих лекарственных веществ | 1986 |
|
SU1461463A1 |
| Способ определения кардиотропной активности веществ | 1988 |
|
SU1635133A1 |
| Shibukawa A., Wainer I.W | |||
| Simultaneous direct determination of the enantiomers of verapamil and norverapamil in plasma using a derivatized amylose high-performance liquid chromatographic chiral stationary phase | |||
| // Journal of chromatography, 1992 Vol.574 NO.1 February 7, p.85-92, Biomedical applications | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
| ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ВЕРАПАМИЛА ГИДРОХЛОРИДА | 2007 |
|
RU2354962C1 |
Авторы
Даты
2010-07-27—Публикация
2008-11-20—Подача