Область изобретения
Изобретение относится к области вакцин для лечения вирусной инфекции, в частности для лечения ВИЧ (вирус иммунодефицита человека) инфекции у людей.
Предшествующий уровень техники
По прошествии двадцати лет после открытия вируса иммунодефицита человека (ВИЧ) все еще отсутствует эффективная профилактическая или терапевтическая вакцина. Недавние проекты Всемирной Организации Здравоохранения и Объединенной программы Организации Объединенных Наций по ВИЧ/СПИД (синдром приобретенного иммунодефицита) свидетельствуют о том, что если пандемия продолжит прогрессировать с существующей скоростью, то к 2010 году будет 45 миллионов вновь инфицированных [1]. Хотя достигнут значительный прогресс в увеличении выживаемости людей, инфицированных ВИЧ, и уменьшении передачи ВИЧ от матери к новорожденному путем антиретровирусной терапии, существует все растущее количество пациентов, у которых развивается резистентность к лекарству и/или тяжелые связанные с лекарством побочные эффекты при длительной антиретровирусной терапии. Поэтому существует острая необходимость в дополнительных альтернативных терапевтических стратегиях для защиты ВИЧ-инфицированных индивидуумов от прогрессирования заболевания.
В недавнем крупномасштабном испытании (III фаза) на людях одной из вакцин-кандидатов, направленной на активацию гуморального иммунитета для нейтрализации ВИЧ, не удалось продемонстрировать свою эффективность [2]. Это отсутствие защиты соответствует хорошо известной неспособности существующих в настоящее время вакцинных разработок вызывать образование эффективных нейтрализующих антител (Nab) против ВИЧ in vivo [3]. Такая неспособность индуцировать эффективные Nab возможно определяется природой инфекционного агента. Например, до настоящего времени отсутствует успешная профилактическая вакцина для таких хронических инфекций, как туберкулез, проказа и инфекция вируса гепатита С. Наоборот, успешные вакцины предотвращают острые инфекционные заболевания, такие как полиомиелит, корь, дифтерия, столбняк или натуральная оспа, путем индукции Nab, которые также могут передаваться трансплацентарно или через молоко для защиты плода или новорожденного от инфекций.
Признано, что длительный клеточный иммунитет потенциально может контролировать заболевание в ситуациях, при которых инфекционный агент не ликвидирован, таких как хронические инфекции, включая туберкулез, проказу, инфекции вируса гепатита В или С и ВИЧ. В этой связи показано, что интенсивные вирусспецифические ответы CD4+ Т-хелперных клеток типа 1 (Th1) и эффекторных (перфорин+) цитотоксических Т-лимфоцитов (CTL), ассоциированы с контролем виремии и длительным отсутствием прогресса у индивидуумов с хронической ВИЧ-1 инфекцией [4-10]. Кроме того, раннее применение высокоактивной антиретровирусной терапии (HAART) во время или сразу после стадии острой инфекции ассоциировалось с усиленными ответами ВИЧ-1-специфических CD4+Тh1-клеток [11, 12]. Наоборот, на более поздней стадии HAART ведет к уменьшению ответов ВИЧ-1-специфических CD4+ Th1-клеток и CTL [5, 13, 14], свидетельствуя о том, что функциональные способности захватывающих ВИЧ-1 антигенпредставляющих клеток (АРС) (которые требуются для индукции иммунного ответа) неуклонно утрачиваются в процессе инфекции [15, 18]. В этом контексте для создания терапевтической вакцины, направленной на индукцию ВИЧ-специфических длительных клеточных иммунных ответов, необходимо выполнение двух условий: 1) открытие подходящего иммуногена, способного вызвать сильный, обширный и длительный защитный клеточный иммунитет; и 2) восстановление in vivo нарушенной функции АРС путем адоптивного переноса активированных ех vivo АРС (т.е. стратегия замены) или путем прямой активации in vivo менее поврежденных дендритных клеток (DC) (таких как клетки Лангерганса) путем совместного комбинирования иммуногена и подходящих цитокинов или адъювантов. Основная задача успешной терапевтической вакцины заключается в устойчивом снижении вирусной нагрузки у ВИЧ-1-инфицированных пациентов до наиболее возможно низкого уровня. Это защитит их от прогрессирования заболевания и таким образом уменьшит потребность во вредных и дорогих антиретровирусных лекарствах. Кроме того, устойчиво сниженная вирусная нагрузка ВИЧ может минимизировать риск передачи вируса здоровым людям половым путем [19].
Индуцированный вакциной защитный иммунный ответ может значительно отличаться в зависимости от природы иммуногена. Живые аттенюированные вакцины вызывают гуморальный и клеточный иммунные ответы, тогда как убитые вирусные вакцины и очищенные синтетические белки предпочтительно вызывают гуморальный (антительный) ответ. В результате проведения многоцентрового клинического исследования, направленного на стимуляцию клеточной составляющей иммунной системы, исследователи были разочарованы полученными результатами, поскольку только у 20% из 205 добровольцев, иммунизированных экспериментальной вакциной, приготовленной из бактериальной ДНК, содержащей гены ВИЧ, возникал значительный ВИЧ-специфический клеточный иммунный ответ (хотя примирование ДНК хорошо работало в экспериментах на мышах) [20]. В этом контексте авторы настоящего изобретения (и другие) недавно обнаружили, что инактивированный цельный ВИЧ-1, в котором конформационная структура оболочечного белка gр120 сохранена (что, например, происходит в том случае, когда вирус обрабатывают альдритиолом-2 [АТ-2]), может быть процессирован и представлен дендритными клетками (DC, наиболее сильные АРС) для индукции сильного HLA-I-ограниченного CTL ответа in vitro [21, 22]. Несколько исследований также продемонстрировали, что адоптивный перенос аутологичных DC, нагруженных in vitro инактивированным цельным ВИЧ-1, индуцировал защитный антивирусный иммунитет у мышей hu-PBL-SCID [23, 24]. Авторы настоящего изобретения ранее продемонстрировали, что терапевтическая вакцина, приготовленная из DC, нагруженных инактивированным цельным обезьяньим вирусом иммунодефицита (SIV) штамм mac251 (SIVmac251), приводит, в отсутствие какой-либо другой противовирусной терапии, к значительной вирусной супрессии у китайских макак-резусов, иммунизированных через два месяца после инфицирования SIVmac251 [25]. Взятые вместе, эти открытия свидетельствуют о том, что АТ-инактивированный цельный вирус может быть использован в качестве эффективного вакцинного иммуногена для индукции защитных ВИЧ-1 -специфических CTL ответов у людей с хронической ВИЧ-1 инфекцией. Однако экстенсивная глобальная вариабельность ВИЧ-1 свидетельствует против концепции фармацевтического применения имеющего чистоту в соответствии с GMP (Надлежащая производственная практика) инактивированного цельного вирусного препарата в качестве универсальной терапевтической вакцины против ВИЧ-1.
Краткое изложение сущности изобретения
В изобретении предложена вакцина, содержащая инактивированный цельный ВИЧ определенного субтипа, возможно с адъювантом. Вакцина может быть использована для лечения индивидуумов, хронически инфицированных ВИЧ, путем индукции защитного клеточного иммунного ответа против того же самого субтипа ВИЧ, который был использован для получения вакцины.
В изобретении также предложена фармацевтическая композиция, содержащая вакцину, содержащую инактивированный цельный ВИЧ определенного субтипа и фармацевтически приемлемый носитель.
В изобретении также предложено применение инактивированного цельного ВИЧ определенного субтипа для изготовления лекарственного средства для лечения индивидуума, хронически инфицированного ВИЧ. Лекарственное средство может быть использовано для лечения индивидуумов, хронически инфицированных ВИЧ, путем индукции защитного клеточного иммунного ответа против того же самого субтипа ВИЧ, который был использован для получения вакцины.
В изобретении также предложен способ лечения индивидуума, хронически инфицированного ВИЧ, включающий введение этому индивидууму вакцины, содержащей инактивированный цельный ВИЧ определенного субтипа, возможно с адъювантом, так что у индивидуума происходит индукция защитного клеточного иммунного ответа против того же самого субтипа ВИЧ, который был использован для получения вакцины. В одном из воплощений инактивированный ВИЧ загружен ex vivo в антигенпредставляющие иммунные клетки (АРС), которые затем вводят индивидууму.
Краткое описание графических материалов
Фиг.1 демонстрирует киллинговую активность цитотоксических Т-лимфоцитов (CTL) вакцин по изобретению.
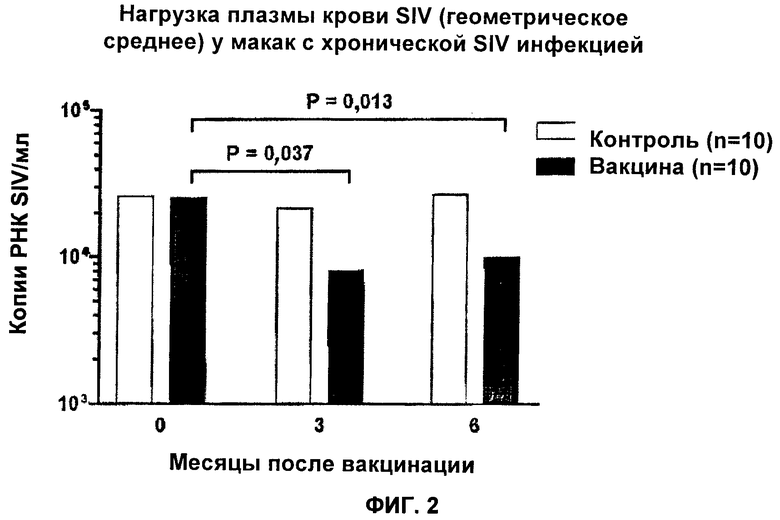
Фиг.2 демонстрирует эффекты интрадермальной иммунизации АТ-2 инактивированным SIV mac251 в отношении вирусной нагрузки в плазме крови макак, хронически инфицированных SIVmac251. Данные представляют собой геометрическое среднее РНК-копий SIV на миллилитр плазмы крови до и после иммунизации. Р-величина представляет статистический анализ парных данных до иммунизации и через 3 или 6 месяцев после иммунизации посредством теста Вилкоксона.
Подробное описание изобретения
Существуют две основные группы ВИЧ (ВИЧ-1 и ВИЧ-2) и множество подгрупп, поскольку геном ВИЧ постоянно мутирует. Основное различие между группами и подгруппами заключается в вирусной оболочке. ВИЧ-1 классифицирован на основную подгруппу (М) и 10-ю обособленную подгруппу (О), где подгруппа М разделена на девять субтипов (кладов, таксонов), обозначенных A-J [28, 29]. Генетическая вариация, обнаруженная в геноме ВИЧ, представляет собой результат мутации, рекомбинации, вставки и делеции.
Вакцины по изобретению против ВИЧ, предпочтительно субтипов ВИЧ-1, таких как субтипы А, В, С или Е, демонстрировали высокую CTL киллинговую активность в отношении вирусных штаммов совместимого субтипа, тогда как обнаружена лишь низкая киллинговая активность в отношении перекрестных субтипов. Хотя в отдельных случаях обнаруживали киллинговую активность в отношении перекрестного субтипа, эффективность CTL киллинга широко варьировала в вирусных штаммах несовместимых субтипов по сравнению с вирусными штаммами совместимых субтипов (см. Пример 1 ниже и Фиг.1). Таким образом, в изобретении предложена субтип-специфичная терапевтическая вакцина против ВИЧ, полученная из инактивированного препарата цельного ВИЧ с заданным субтипом. Вакцины по изобретению могут быть использованы для лечения индивидуума с хронической ВИЧ-инфекцией, где вакцины индуцируют защитный клеточный иммунный ответ против того же самого субтипа ВИЧ, который использован для получения вакцины.
Используемый здесь термин "вакцина" относится к композиции, которую вводят для получения или искусственного увеличения иммунитета против конкретного заболевания.
Предпочтительно вакцины готовят с субтипом ВИЧ, который не аутологичен для индивидуума, которого лечат. Фактически авторы изобретения неожиданно продемонстрировали, что вакцина с субтипом ВИЧ, не аутологичным для индивидуума, которого лечат, дает возможность для значительного уменьшения вирусной нагрузки у указанного индивидуума.
В соответствии с изобретением можно лечить хроническую инфекцию любого субтипа ВИЧ, например хронические инфекции вируса ВИЧ выбраны из одного из субтипов А, В, С или Е (и других) группы М, а также группы ВИЧ-2 и подгруппы О ВИЧ.
В одном из воплощений композиция по изобретению может содержать несколько инактивированных субтипов ВИЧ, например два, три, четыре или более различных инактивированных субтипов ВИЧ.
Используемый здесь термин "лечение" индивидуума с хронической ВИЧ-инфекцией означает, что предотвращают, уменьшают или ингибируют симптомы ВИЧ-инфекции; вирусная нагрузка (в частности, вирусная нагрузка в плазме крови) уменьшается после введения вакцины; и/или у индивидуума индуцируют CTL ответ против ВИЧ. Понятно, что "лечение" индивидуума против хронической ВИЧ-инфекции не требует полной ликвидации ВИЧ у индивидуума.
Используемый здесь термин "индивидуум с хронической ВИЧ-инфекцией" обозначает индивидуума, для которого может быть поставлен диагноз "инфицированный ВИЧ".
Используемый здесь термин "инактивированный цельный ВИЧ" означает полную частицу ВИЧ, которая инактивирована и больше не является инфекционной.
При практическом применении изобретения ВИЧ конкретного субтипа может быть инактивирован при помощи любого подходящего способа, известного в области техники, такого как ультрафиолетовое облучение, тепловая или химическая обработка, такая как обработка формальдегидом, параформальдегидом, пропиолактеном или АТ-2 (2,2'-дитиодипиридин, алдритиол-2).
Предпочтительно ВИЧ конкретного субтипа инактивирован путем воздействия на ВИЧ химической обработкой, и более предпочтительно - обработкой АТ-2. Неожиданно оказалось, что такая инактивация с помощью АТ-2 делает возможным поддержание конформационной структуры белков ВИЧ и индукции реального сильного CTL ответа для неаутологичного субтипа.
Субтип-специфичные иммуногены инактивированного цельного вируса могут быть использованы для нагрузки ex vivo (также называемой "пульсированием", от англ. "pulsing") антигенпредставляющих клеток иммунной системы (АРС), таких как зрелые и незрелые дендритные клетки (DC) или клетки Лангерганса (LC), с получением терапевтической вакцины на основе АРС, или для прямой интрадермальной инъекции in vivo, дающей возможность для нагрузки LC in vivo с получением бесклеточной вакцины.
В одном из воплощений бесклеточные вакцины по изобретению могут быть введены, например, путем прямой (предпочтительно безыгольной) доставки инактивированного субтип-специфичного ВИЧ (например, путем интрадермальной инъекции) в кожу пациента с использованием способов, известных в области техники. Безыгольные устройства для интрадермального введения вакцин хорошо известны специалистам в данной области техники и включают в качестве примера устройства, описанные в патенте США 6933319 и в международной заявке на патент WO 2004/101025, которые включены здесь путем ссылки. Вакцинация через кожу (интрадермальное введение) является особенно благоприятной, поскольку эпидермис содержит большое количество LC. Известно, что LC представляют собой незрелую форму DC и локализованы в тесной близости с наиболее поверхностным слоем кожи - роговым слоем. Эти LC представляют собой сеть иммунных клеток, которые лежат под 25% поверхности кожи [26] и сохраняют функциональную интактность на ранней или асимптоматической фазе хронической ВИЧ/SIV (вирус иммунодефицита обезьян) инфекции. Авторы изобретения продемонстрировали, что такое интрадермальное введение бесклеточных вакцин по изобретению дает возможность для значительного уменьшения вирусной нагрузки SIV.
В еще одном воплощении вакцины по изобретению на основе АРС могут быть введены, например, путем прямой доставки пациенту АРС, нагруженных инактивированным субтип-специфичным ВИЧ (например, при помощи подкожного инжектора), с использованием способов, известных в области техники.
В одном из воплощений способ включает предварительную стадию определения субтипа ВИЧ, инфицировавшего пациента, которого лечат, перед введением композиции по изобретению. Такое определение может быть осуществлено с использованием способов, хорошо известных в области техники, таких как генотипирование специфической области последовательности ВИЧ путем анализа ВИЧ, присутствующего в образце крови указанного пациента. Предпочтительно за этой стадией определения субтипа ВИЧ следует введение основанных на АРС или бесклеточных вакцин по изобретению, содержащих тот же самый субтип ВИЧ, что и субтип, которым инфицирован пациент, которого лечат.
В еще одном воплощении индивидуума лечат АРС, нагруженными инактивированным ВИЧ конкретного субтипа. АРС сначала нагружают инактивированным ВИЧ ex vivo и нагруженные АРС затем вводят пациенту при помощи любого подходящего способа. Предпочтительно нагруженные АРС инъецируют индивидууму подкожно, интрадермально или внутримышечно, предпочтительно путем подкожной инъекции. Более предпочтительно АРС получают путем предварительного отбора у индивидуума, подлежащего лечениют, образца мононуклеарных клеток периферической крови (РВМС) для выделения моноцитов (CD14+), которые затем трансформируют с использованием известных цитокинов в незрелые и затем зрелые дендритные клетки. Такие способы хорошо известны специалистам в данной области техники, в качестве примера такой способ описан в примере 1.
В отличие от бактериальных продуктов сами инактивированные цельные ВИЧ недостаточно эффективны для индукции созревания DC [25] для обеспечения возможности эффективной миграции этих клеток в отводящие лимфатические узлы, где они осуществляют свою иммуностимулирующую функцию. Таким образом, класс сильных молекул, известных как адъюванты, предпочтительно комбинируют с инактивированным цельным ВИЧ для запуска оптимального созревания иммунных клеток, таких как LC, таким образом обеспечивая возможность для генерации эффективного клеточного иммунного ответа против ВИЧ-1.
Термин "адъювант" относится к веществу, добавленному к вакцине для улучшения иммунного ответа.
Подходящие адъюванты включают полный адъювант Фрейнда, неполный адъювант Фрейнда, сапонин, минеральные гели, такие как гидроксид алюминия, поверхностно-активные вещества, такие как лизолецитин, плюроновые полиолы, полианионы, пептиды, масляные или углеводородные эмульсии, гемоцианины морского блюдца, динитрофенол, обычные бактериальные продукты (такие как холерный токсин, термолабильный энтеротоксин, аттенуированные или убитые BCG (бацилла Кальмета-Герена) и Corynebacterium parvum или белки, полученные из BCG), биохимические молекулы (такие как фактор некроза опухоли альфа (TNF-альфа), IL-1-бета, IL-6, простагландин Е2 (PGE2) или CD40L) или олигодезоксинуклеотиды, содержащие мотив CpG. Примеры материалов, подходящих для применения в вакцинных композициях, раскрыты, например, в Osol, A., ed., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa. (1980), pp.1324-1341, полностью включенном посредством ссылки.
Дендритные клетки играют ведущую роль в регуляции дифференцировки моноцитов и, более конкретно, в регуляции дифференцировки CD4-Th1 профиля против CD4-Th2 профиля. Предпочтительно бесклеточная вакцинная композиция по изобретению включает адъюванты, способные стимулировать дендритные клетки для того, чтобы ингибировать клеточную дифференцировку в CD4-Th2 профиль, которая часто индуцируется при хронической инфекции, и одновременно способные стимулировать дендритные клетки для активации клеточной дифференцировки в CD4-Th1 профиль. Такие адъюванты хорошо известны специалисту в данной области техники и включают бактериальные продукты (такие как некоторые полученные из BCG белки, такие как Аg85В) или химические соединения, такие как соединения, обладающие активностью против циклооксигеназы (СОХ) и, более конкретно, активностью против СОХ2 (такие как VIOX®, CELEBREX® или RIBAVERIN®).
Вакцины по изобретению могут быть приготовлены в виде фармацевтических композиций (также называемых "лекарственными средствами") для лечения индивидуумов, хронически инфицированных ВИЧ. Фармацевтические композиции по изобретению предпочтительно являются стерильными и апирогенными и также включают фармацевтически приемлемый носитель. Подходящие фармацевтически приемлемые носители включают воду, солевые растворы (например, физиологический раствор), агенты, регулирующие вязкость, и другие обычные фармацевтические эксципиенты и/или добавки, используемые при приготовлении фармацевтических композиций для применения у людей. Подходящие фармацевтические эксципиенты включают стабилизаторы, антиоксиданты, агенты, регулирующие осмоляльность, буферы и агенты, регулирующие рН. Подходящие добавки включают физиологически биосовместимые буферы (например, трометамина гидрохлорид и т.п.), хелатирующие агенты (например, диэтилентриаминпентауксусная кислота (DTPA), DTPA-бисамид и т.п.) или кальциевые хелатные комплексы (например, кальция DTPA, CaNaDTPA-бисамид и т.п.), или, возможно, добавки кальциевой или натриевой солей (например, хлорида кальция, аскорбата кальция, глюконата кальция, лактата кальция и т.п.). Приготовление фармацевтических композиций по изобретению известно в области техники, например, как описано в Remington's Pharmaceutical Science, 17th ed., Mack Publishing Company, Easton, Pa. (1985), полное описание которого включено здесь путем ссылки.
Типичная схема лечения индивидуумов, хронически инфицированных ВИЧ, который может быть ослаблен клеточным иммунным ответом путем активной терапии, включает введение эффективного количества вакцинной композиции, как описано выше, вводимой в виде разовой обработки или повторяющейся в виде повышающихся или бустерных доз, в течение периода от одной недели до приблизительно 24 месяцев включительно.
В соответствии с настоящим изобретением "эффективное количество" вакцинной композиции представляет собой количество, которое достаточно для достижения желаемого биологического эффекта, в этом случае по меньшей мере одного из клеточного или гуморального иммунного ответа на ВИЧ, предпочтительно одного клеточного иммунного ответа. Понятно, что эффективная доза зависит от возраста, пола, состояния здоровья и массы реципиента, вида сопутствующего лечения, если такое осуществляют, частоты обработок и природы желаемого эффекта. Диапазоны эффективных доз, предложенные ниже, не предназначены для ограничения изобретения и представляют собой предпочтительные диапазоны доз. Тем не менее, наиболее предпочтительную дозировку специально подбирают для индивидуального субъекта, как это понимается и определяется специалистом в данной области техники, без чрезмерного экспериментирования. См., например, Berkow (1987), ниже, Goodman (1990), ниже, Avery (1987), ниже, Ebadi, Pharmacology, Little, Brown and Co., Boston, Mass. (1985), и Katsung (1992), ниже, ссылки на которые и цитированные в них ссылки полностью включены здесь путем ссылки.
Говоря в общем, дозировка для взрослого человека составляет приблизительно 106-1014 инактивированных цельных частиц ВИЧ на дозу, предпочтительно 108-1012. Какую бы дозу не применяли, она должна представлять собой безопасное и эффективное количество, как определено с использованием известных способов, так же, как здесь описано.
Изобретение проиллюстрировано при помощи следующих не ограничивающих объем изобретения примеров.
ПРИМЕРЫ
Пример 1
Способы
Вирусные и клеточные образцы
Штаммы ВИЧ-1 получали при помощи культуры мононуклеарных клеток периферической крови (РВМС), лишенных CD8, от пациентов, инфицированных ВИЧ-1 субтипов А (n=10), В (n=10), С (n=10) или Е (n=10). Эти штаммы ВИЧ-1 субтипов (А, В, С или Е) затем инактивировали при помощи АТ-2 (Sigma, St Louis, Missouri), как описано в [21], полное описание которой включено здесь путем ссылки. Моноцитарные DC получали от каждого пациента при помощи стандартизированной 7-дневной культуры [25] в условиях в соответствии с GMP. Кратко, свежесобранным РВМС давали возможность прикрепиться к пластику с плотностью 106 клеток/см2 в присутствии 0,5% человеческого сывороточного альбумина для клинического использования (LFB, Les Ulis, France). После инкубации в течение 2 часов при 37°С в 5% СO2 неприкрепившиеся клетки удаляли путем промывания стерильным забуференным фосфатом физиологическим раствором (ЗФР). Прикрепившиеся клетки затем культивировали в течение 5 дней в полной среде, содержащей среду CellGro DC, имеющую клиническую чистоту (CellGenix, Freiburg, Germany), дополненную 2000 Ед./мл колониестимулирующего фактора гранулоцитов и макрофагов (GM-CSF) (Schering-Plough, Brinny, Ireland) и 50 нг/мл IL-4, имеющего клиническую чистоту (CellGenix). На 5-й день DC подвергали воздействию АТ-2-инактивированного аутологичного вируса (109 вирусных частиц/мл) при 37°С в течение 2 ч. После 2 промывок для удаления не связавшегося инактивированного вируса клетки культивировали в течение еще 2 дней в полной среде, дополненной цитокинами IL-1β (10 нг/мл) (CellGenix), IL-6 (100 нг/мл) (CellGenix), и TNF-α (50 нг/мл) (CellGenix), имеющими клиническую чистоту. На 7-ой день осуществляли контроль качества (КК) DC путем проточной цитометрии [25], полное описание которой включено здесь путем ссылки. Прошедшие КК жизнеспособные DC затем использовали для получения аутологичных вирусоспецифических CTL при помощи протокола совместной культуры, как описано в [21], выше.
Анализ цитотоксичности
DC обрабатывали АТ-ВИЧ-1 (109/мл) в течение 90 мин, затем метили CFSE (сукцинимидиловый эфир карбоксифлуоресцеина, Molecular Probes, PoortGebouw, The Netherlands) (10 нМ) в течение 15 мин и дважды промывали. Необработанные DC метили CFSE в качестве контроля специфичности. CTL, специфичные в отношении штамма субтипа ВИЧ-1, высевали в Micro Tubes-Bulk (Bio-Rad, Hercules, CA) в присутствии CFSE-меченных АТ-2-ВИЧ-1-сенсибилизированных дендритных клеток (DC) с совместимым или несовместимым субтипом в отношении Е:Т 10:1 в течение 4 ч при 37°С. В конце инкубации в каждую пробирку добавляли 10 мкл йодида пропидия (PI, Sigma) (20 мкг/мл). Направленный цитолиз анализировали на FACSCalibur (BD Immunocytometry System, San Jose, CA). Вирусоспецифическую цитолитическую активность определяли путем расчета процента CFSE/PI-окрашивания DC после вычитания неспецифического CFSE/PI-окрашивания необработанных DC.
Статистический анализ
Непарные данные между активностями клеточного киллинга ВИЧ-1 совместимого и несовместимого субтипа сравнивали при помощи теста Манна-Уитни.
Результаты
Вакцины по настоящему изобретению, специфичные в отношении ВИЧ-1 субтипов А, В, С или Е, демонстрировали высокую CTL киллинговую активность in vitro (28-37%) с вирусными штаммами совместимого субтипа (n=10), тогда как обнаружили лишь незначительную (5-17%) киллинговую активность со штаммами перекрестного субтипа (Р меньше 0,001). Хотя в отдельных случаях обнаружили киллинговую активность для несовместимого субтипа, эффективность CTL киллинга широко варьировала в вирусных штаммах несовместимого субтипа (стндартное отклонение (СО)/среднее больше 50%) по сравнению с вирусными штаммами совместимого субтипа (СО/среднее меньше 20%) (Р меньше 0,001) (Фиг.1). Эти факты свидетельствуют о том, что фармацевтическая субтип-специфичная терапевтическая вакцина против ВИЧ-1 может быть приготовлена при помощи препарата инактивированного цельного вируса, имеющего чистоту в соответствии с GMP.
Пример 2
Идентифицируют индивидуумов, хронически инфицированных ВИЧ, и определяют субтип ВИЧ, которым инфицирован индивидуум. Вирусную нагрузку в плазме крови определяют для каждого индивидуума перед лечением вакциной по изобретению. ВИЧ того же самого субтипа, что и субтип, которым инфицированы индивидуумы, получают, культивируют и инактивируют АТ-2, как описано выше в Примере 1.
Инактивированные субтипы ВИЧ вводят группе хронически инфицированных индивидуумов посредством безыгольной интрадермальной доставки и измеряют вирусную нагрузку в плазме крови. Ожидают, что вирусная нагрузка в плазме крови хронически инфицированных индивидуумов будет значительно уменьшаться после введения вакцин по настоящему изобретению.
Другой группе хронически инфицированных индивидуумов вводят дендритные клетки, которые нагружены ВИЧ, инактивированным АТ-2, как описано выше в Примере 1. Нагруженные ВИЧ дендритные клетки вводят индивидуумам. Ожидают, что вирусная нагрузка в плазме крови хронически инфицированных индивидуумов будет значительно уменьшаться после введения нагруженных дендритных клеток.
Пример 3
40 Хронически (больше 1 года) SIVmac251-инфицированных макак с вирусной нагрузкой плазмы крови больше 1000 копий/мл случайным образом отбирали для осуществления ежемесячной интрадермальной инъекции (25 см2 на спине) SIVac LA2.1 (2,5 мл 0,9%-ного раствора NaCl, содержащего 1010 AT-2-инактивированного SIVmac251) в течение 5 месяцев с использованием автоматического инъецирующего пистолета (AKRA DERMOJET, Pau, France) (100 мкл/см2/инъекция) (n=20); или для осуществления ежемесячной интрадермальной инъекции плацебо (2,5 мл одного 0,9%-ного раствора NaCl) в течение 5 месяцев (n=20). Образцы плазмы крови отбирали в исходный момент и затем каждый месяц в течение 6 месяцев и хранили при -80°С до использования. Наконец, измеряли нагрузку РНК SIV в плазме крови при помощи количественного анализа путем полимеразной цепной реакции с обратной транскриптазой RT-PCR (MUPROVAMA).
Результаты
Бесклеточные вакцины по настоящему изобретению, специфичные в отношении субтипа SIV, вызывали почти 30%-ное уменьшение (Фиг.2) вирусной нагрузки в крови через 3 месяца (Р=0,037) и 6 месяцев (Р=0,013). Эти факты свидетельствуют о том, что фармацевтическая субтип-специфичная терапевтическая вакцина против SIV может быть приготовлена при помощи препарата инактивированного цельного вируса, имеющего чистоту GMP.
Пример 4
140 Хронически (больше 1 года) SIVmac251-инфицированных макак с вирусной нагрузкой в плазме крови больше 1000 копий/мл случайным образом отбирали для осуществления ежемесячной интрадермальной инъекции (25 см2 на спине) SIVac LA2.1 (2,5 мл 0,9%-ного раствора NaCl, содержащего 1010 АТ-2-инактивированного SIVmac251) с различными адъювантами (105 UFC аттенюированной или убитой нагреванием BCG, полученные из BCG рекомбинантные Аg85В) в течение 5 месяцев с использованием автоматического инъецирующего пистолета (AKRA DERMOJET, Pau, France) (100 мкл/см2/инъекция) с ежедневным пероральным введением 200 мг CELEBREX® в течение 4 недель (n=20 для каждой группы) или без него; или для осуществления ежемесячной интрадермальной инъекции плацебо (2,5 мл одного 0,9% раствора NaCl) в течение 5 месяцев (n=20). Образцы плазмы крови отбирали в исходный момент и каждый месяц в течение 6 месяцев и хранили при -80°С до использования. Наконец, измеряли нагрузку РНК SIV в плазме крови при помощи количественного анализа путем полимеразной цепной реакции с обратной транскриптазой RT-PCR (MUPROVAMA).
Источники информации
1. Stover, J. et al. Can we reverse the HIV/AIDS pandemic with an expanded response? Lancet 360, 73-7 (2002).
2. Cohen, J. HIV/AIDS. Vaccine results lose significance under scrutiny. Science 299, 1495 (2003).
3. Srivastava, I.К., Ulmer, J.B. & Barnett, S.W.Neutralizing antibody responses to HIV: role in protective immunity and challenges for vaccine design. Expert Rev Vaccines 3 Suppl 1, S33-52 (2004).
4. Rosenberg, E.S. et al. Vigorous HIV-1-specific CD4+Т cell responses associated with control of viremia. Science 278, 1447-50 (1997).
5. Pitcher, CJ. et al. HIV-1-specific CD4+Т cells are detectable in most individuals with active HIV-1 infection, but decline with prolonged viral suppression. NatMed5, 518-25 (1999).
6. Zaunders, JJ. et al. Identification of circulating antigen-specific CD4+Т lymphocytes with a CCR5+, cytotoxic phenotype in an HIV-1 long-term non-progressor and in CMV infection. Blood (2003).
7. Boaz, M.J., Waters, A., Murad, S., Easterbrook, PJ. & Vyakarnam, A.Presence of HIV-1 Gag-specific IFN-gamma +IL-2+and CD28+IL-2+CD4 Т cell responses is associated with nonprogression in HIV-1 infection. J Immunol 169, 6376-85 (2002).
8. Younes, S.A. et al. HIV-1 viremia prevents the establishment of interleukin 2-producing HIV-specific memory CD4+Т cells endowed with proliferative capacity. J Exp Med 198, 1909-22 (2003).
9. Harari, A., Petitpierre, S., Vallelian, F. & Pantaleo, G. Skewed representation of functionally distinct populations of virus-specific CD4 Т cells in HIV-1-infected subjects with progressive disease: changes after antiretroviral therapy. Blood 103, 966-72 (2004).
10. Hess, С. et al. HIV-1 specific CD8+Т cells with an effector phenotype and control of viral replication. Lancet 363, 863-6 (2004).
11. Malhotra, U. et al. Effect of combination antiretroviral therapy on T-cell immunity in acute human immunodeficiency virus type 1 infection. J Infect Dis 181, 121-31 (2000).
12. Oxenius, A. et al. Early highly active antiretroviral therapy for acute HIV-1 infection preserves immune function of CD8+and CD4+Т lymphocytes. Proc NatI Acad Sci USA 97, 3382-7 (2000).
13. Gray, CM. et al. Frequency of class I HLA-restricted anti-ВИЧ CD8+Т cells in individuals receiving highly active antiretroviral therapy (HAART). J Immunol 162, 1780-8 (1999).
14. Kalams, S.A. et al. Levels of human immunodeficiency virus type 1-specific cytotoxic T-lymphocyte effector and memory responses decline after suppression of viremia with highly active antiretroviral therapy. J Virol 73, 6721-8 (1999).
15. Mcllroy, D. et al. Low CD83, but normal MHC class II and costimulatory molecule expression, on spleen dendritic cells from HIV+patients. AIDS Res Hum Retroviruses 14, 505-13 (1998).
16. Grassi, F. et al. Depletion in blood CD1 1c-positive dendritic cells from HIV-infected patients. Aids 13, 759-66 (1999).
17. Donaghy, H. et al. Loss of blood CD11c(+) myeloid and CDHc(-) plasmacytoid dendritic cells in patients with HIV-1 infection correlates with HIV-1 RNA virus load. Blood 98, 2574-6 (2001).
18. Pacanowski, J. et al. Reduced blood CD123+(lymphoid) and CD11c+ (myeloid) dendritic cell numbers in primary HIV-1 infection. Blood 98, 3016-21. (2001).
19. Quinn, T.C. et al. Viral load and heterosexual transmission of human immunodeficiency virus type 1. Rakai Project Study Group. N Eng J Med 342, 921-9 (2000).
20. Cohen, J. AIDS vaccines. HIV dodges one-two punch. Science 305, 1545-7 (2004).
21. Lu, W. & Andrieu, J.M. In vitro HIV eradication by autologous CD8+Т cells expanded with inactivated-virus-pulsed dendritic cells. J Virol 75, 8949-56 (2001).
22. Buseyne, F. et al. MHC-l-restricted presentation of HIV-1 virion antigens without viral replication. Nat Med 1, 344-9 (2001).
23. Lapenta, С.et al. Potent immune response against HIV-1 and protection from virus challenge in hu-PBL-SCID mice immunized with inactivated virus-pulsed dendritic cells generated in the presence of IFN-alpha. J Exp Med 198, 361-7 (2003).
24. Yoshida, A. et al. Induction of protective immune responses against R5 human immunodeficiency virus type 1 (HIV-1) infection in hu-PBL-SClD mice by intrasplenic immunization with HIV-1-pulsed dendritic cells: possible involvement of a novel factor of human CD4(+) T-cell origin. J Virol 77, 8719-28 (2003).
25. Lu, W., Wu, X., Lu, Y., Guo, W. & Andrieu, J.M. Therapeutic dendritic-cell vaccine for simian AIDS. Nat Med 9, 27-32 (2003).
26. Yu, R.C., Abrams, D.C, Alaibac, M. & Chu, A.C. Morphological and quantitative analyses of normal epidermal Langerhans cells using confocal scanning laser microscopy. BrJ Dermatol 131, 843-8 (1994).
27. Zimmer, M.I. et al. Disrupted homeostasis of Langerhans cells and interdigitating dendritic cells in monkeys with AIDS. Blood 99, 2859-68 (2002).
28. Hu et al., JAMA 275: 210-216 (1996).
29. Korber et al., Science 280: 1868-1871 (1998).
Все документы, на которые ссылаются в этой заявке, включая перечисленные выше, включены здесь путем ссылки. Множество описанных выше модификаций воплощений понятно специалисту в данной области техники из предложенного здесь описания. Таким образом, изобретение может быть воплощено в другие специфические формы, не отступая от сущности изобретения или его важных особенностей.
Изобретение относится к области биотехнологии, вирусологии и медицины. Инактивированный цельный вирус иммунодефицита человека определенного субтипа применяют для получения вакцин и фармацевтических композиций, содержащих такие вакцины. Вакцины могут быть использованы для лечения индивидуумов, хронически инфицированных ВИЧ, путем индукции у этих индивидуумов защитного клеточного иммунного ответа против того же самого субтипа ВИЧ, который был использован для получения вакцины. Изобретение может быть использовано в медицине. 2 н. и 19 з.п. ф-лы, 2 ил.
1. Применение цельного ВИЧ (вирус иммунодефицита человека) определенного субтипа, инактивированного путем обработки альдитриолом-2 (АТ-2), для получения бесклеточной вакцины для лечения индивидуума, хронически инфицированного ВИЧ, путем интрадермального введения, где это лекарственное средство индуцирует защитный клеточный иммунный ответ у индивидуума против того же самого субтипа ВИЧ, который был использован для получения данного лекарственного средства.
2. Применение по п.1, где инактивированный цельный ВИЧ определенного субтипа не аутологичен для индивидуума, которого лечат от хронической ВИЧ-инфекции.
3. Применение по п.1, где инактивированный цельный ВИЧ определенного субтипа выбран из субтипов группы М, группы ВИЧ-2 и подгруппы О ВИЧ.
4. Применение по п.3, где субтип группы М представляет собой А, В, С или Е.
5. Применение по п.1, дополнительно включающее адъювант.
6. Применение по п.5, где адъювант стимулирует созревание дендритных клеток.
7. Применение по п.5, где адъювант способен стимулировать дендритные клетки для ингибирования клеточной дифференцировки в CD4-Th2 профиль.
8. Применение по п.7, где адъювант способен стимулировать дендритные клетки для активации клеточной дифференцировки в CD4-TH1 профиль.
9. Применение по п.6, где дендритная клетка представляет собой клетку Лангерганса.
10. Способ лечения индивидуума, хронически инфицированного ВИЧ, включающий введение индивидууму путем интрадермальной доставки бесклеточной вакцины, содержащей цельный ВИЧ определенного субтипа, инактивированный путем обработки альдитриолом-2 (АТ-2), в количестве 106-1014 инактивированных цельных частиц ВИЧ на дозу предпочтительно 108-1012, при котором у индивидуума индуцируют защитный клеточный иммунный ответ против того же самого субтипа ВИЧ, который был использован для получения вакцины.
11. Способ по п.10, дополнительно включающий введение индивидууму адъюванта.
12. Способ по п.11, где адъювант стимулирует созревание дендритных клеток.
13. Способ по п.12, где дендритная клетка представляет собой клетку Лангерганса.
14. Способ по п.11, где адъювант способен стимулировать дендритные клетки для ингибирования клеточной дифференцировки в CD4-Th2 профиль.
15. Способ по п.11, где адъювант способен стимулировать дендритные клетки для активации клеточной дифференцировки в CD4-Thl профиль.
16. Способ по п.10, где инактивированный цельный ВИЧ определенного субтипа выбран из субтипов группы М, группы ВИЧ-2 и субгруппы О ВИЧ.
17. Способ по п.16, где субтип группы М представляет собой А, В, С или Е.
18. Способ по п.10, где интрадермальную доставку осуществляют путем прямой безыгольной доставки.
19. Способ по п.10, где инактивированный цельный ВИЧ определенного субтипа не аутологичен для индивидуума, которого лечат от хронической ВИЧ-инфекции.
20. Способ по любому из пп.10-19, включающий первую стадию определения субтипа ВИЧ, которым инфицирован индивидуум, которого лечат.
21. Способ по п.20, где вводимый инактивированный ВИЧ и ВИЧ, которым инфицирован индивидуум, которого лечат, имеют одинаковый субтип.
| US 2004009194 A1, 15.01.2004 | |||
| US 2004109876 A1, 10.06.2004 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2010-08-10—Публикация
2005-10-04—Подача