Текст описания приведен в факсимильном виде.






































































| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОТБОРА И ПОЛУЧЕНИЯ СЕЛЕКТИВНЫХ И МУЛЬТИСПЕЦИФИЧЕСКИХ ТЕРАПЕВТИЧЕСКИХ МОЛЕКУЛ С ЗАДАННЫМИ СВОЙСТВАМИ, ВКЛЮЧАЮЩИХ ПО МЕНЬШЕЙ МЕРЕ ДВЕ РАЗЛИЧНЫЕ НАЦЕЛИВАЮЩИЕ ГРУППИРОВКИ, И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2644263C2 |
| СЛОЖНЫЕ КОМПЛЕКСЫ СВЯЗАННОЙ НА ПОВЕРХНОСТИ ТРАНСПОСОМЫ | 2020 |
|
RU2790295C2 |
| ТАГМЕНТАЦИЯ С ПРИМЕНЕНИЕМ ИММОБИЛИЗОВАННЫХ ТРАНСПОСОМ С ЛИНКЕРАМИ | 2018 |
|
RU2783536C2 |
| Композиция системы доставки на основе конъюгата для доставки полинуклеотида РНК-интерференции в клетку печени и способ ее получения | 2011 |
|
RU2623160C9 |
| НОВЫЕ КОНЪЮГАТЫ АНАЛОГОВ СС-1065 И БИФУНКЦИОНАЛЬНЫЕ ЛИНКЕРЫ | 2011 |
|
RU2578719C9 |
| АКТИВИРУЕМЫЕ АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТСЯ С РЕЦЕПТОРОМ ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2713121C2 |
| НОВЫЕ КОНЪЮГАТЫ АНАЛОГОВ СС-1065 И БИФУНКЦИОНАЛЬНЫЕ ЛИНКЕРЫ | 2011 |
|
RU2730502C2 |
| ПРОТОЧНЫЕ КЮВЕТЫ | 2020 |
|
RU2823720C2 |
| КЛЕТОЧНО-РЕАКТИВНЫЕ АНАЛОГИ КОМПСТАТИНА, АНАЛОГИ КОМПСТАТИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ ИЛИ АНАЛОГИ КОМПСТАТИНА НАЦЕЛЕННОГО ДЕЙСТВИЯ И СВЯЗАННЫЕ С НИМИ КОМПОЗИЦИИ И СПОСОБЫ | 2013 |
|
RU2705215C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОНСТРУКЦИИ С ПОВЫШЕННОЙ АФФИННОСТЬЮ СВЯЗЫВАНИЯ С АЛЬБУМИНОМ | 2018 |
|
RU2753880C1 |
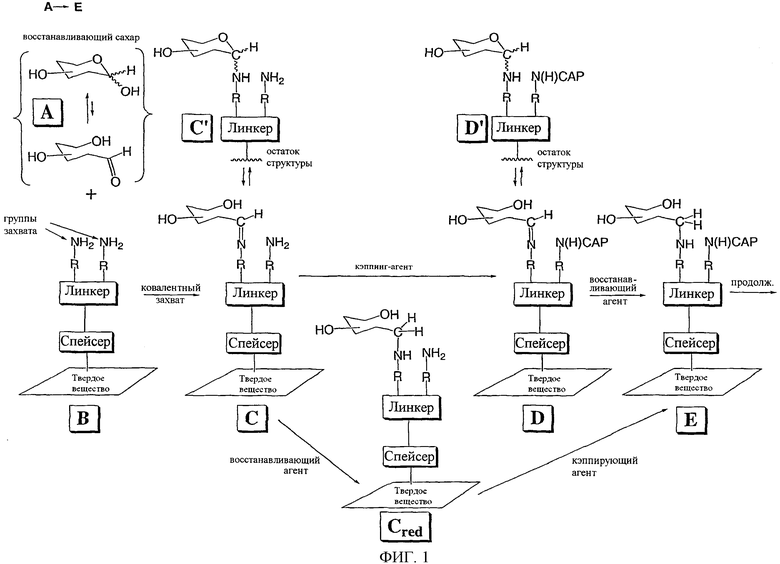
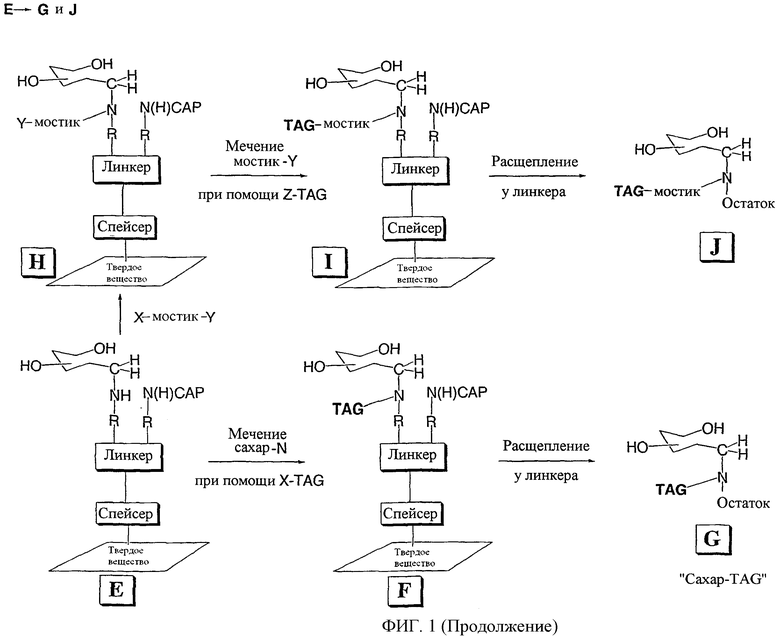
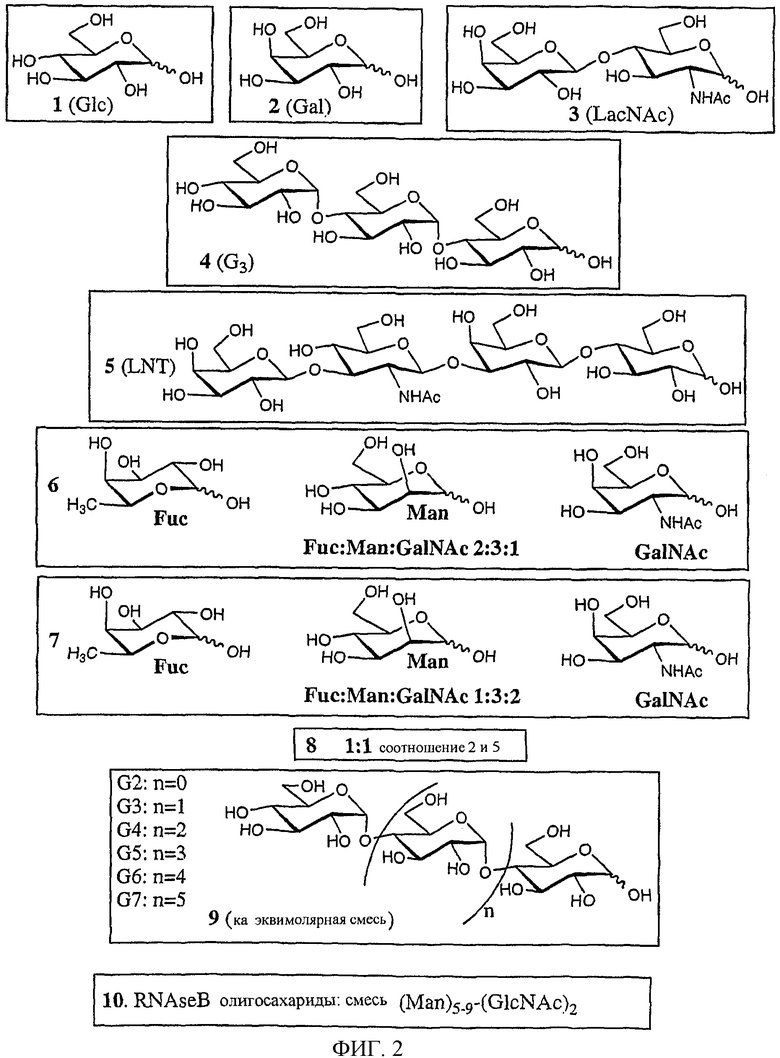
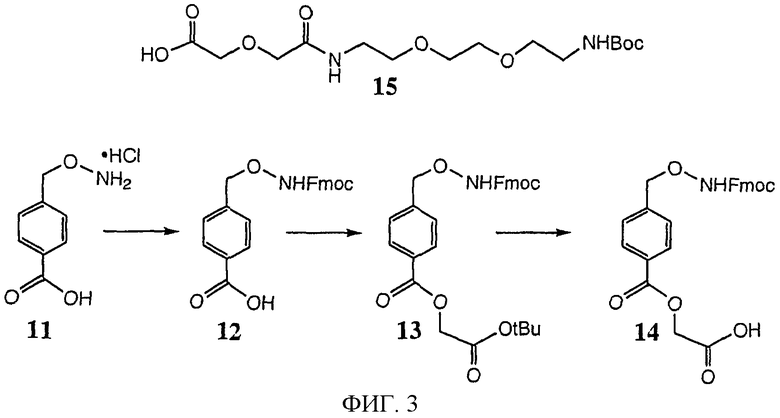
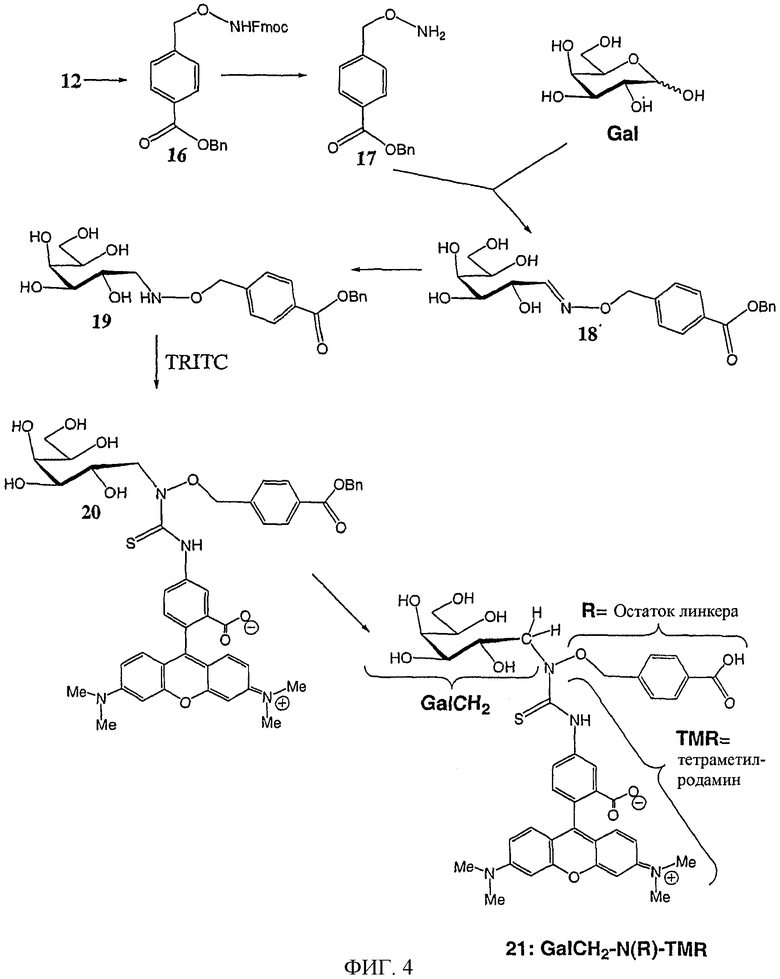
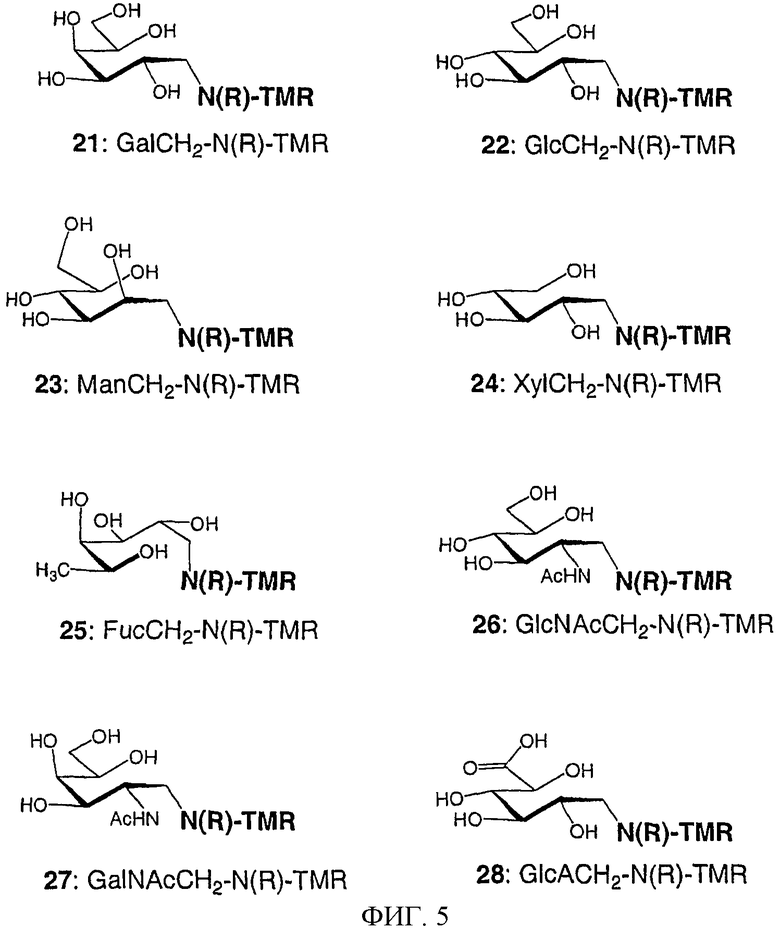
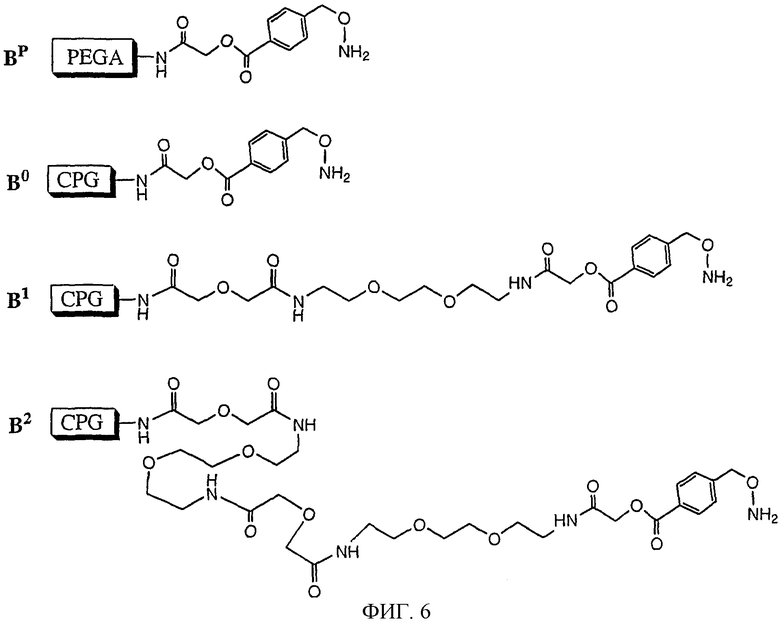
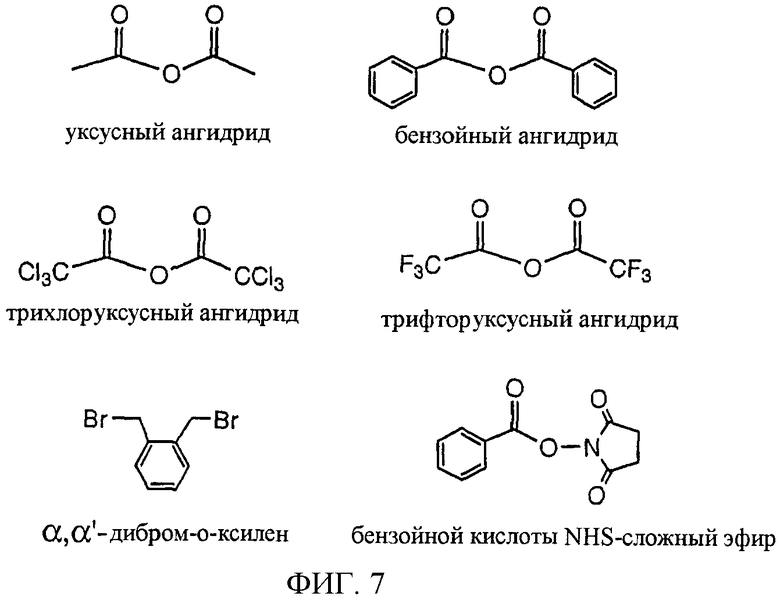
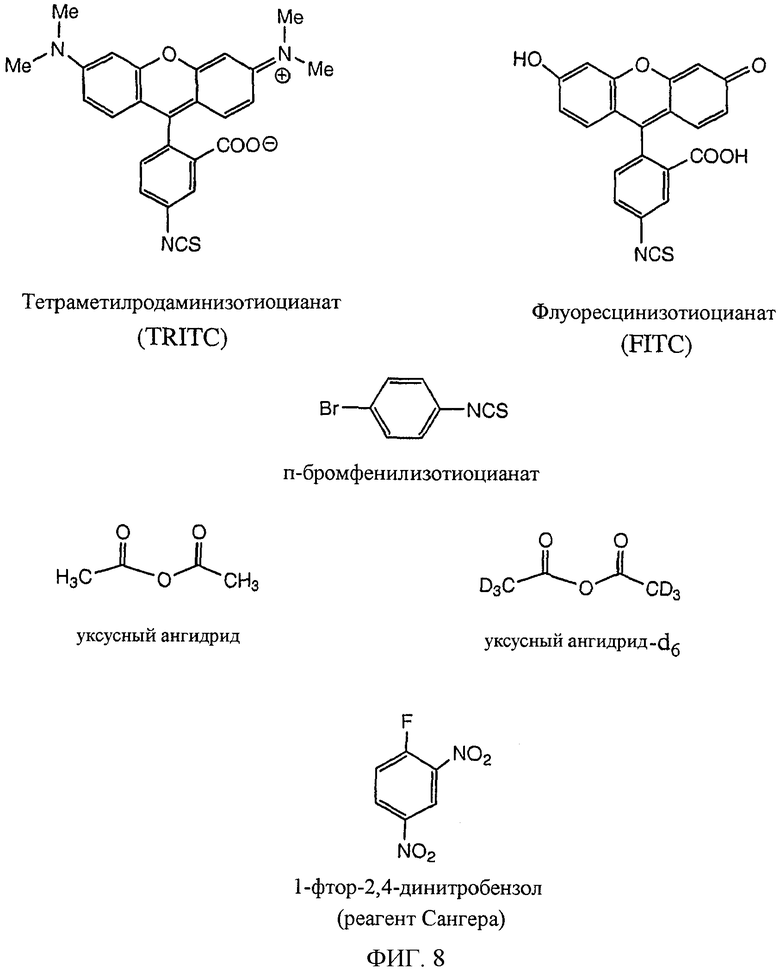
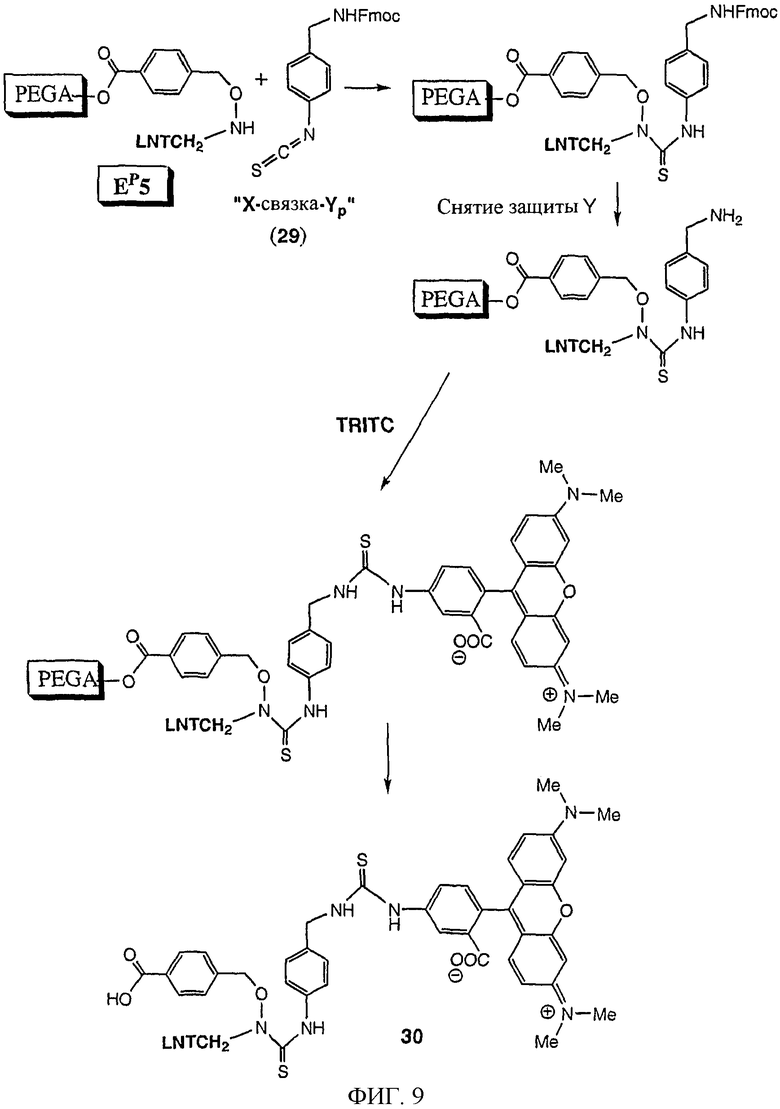
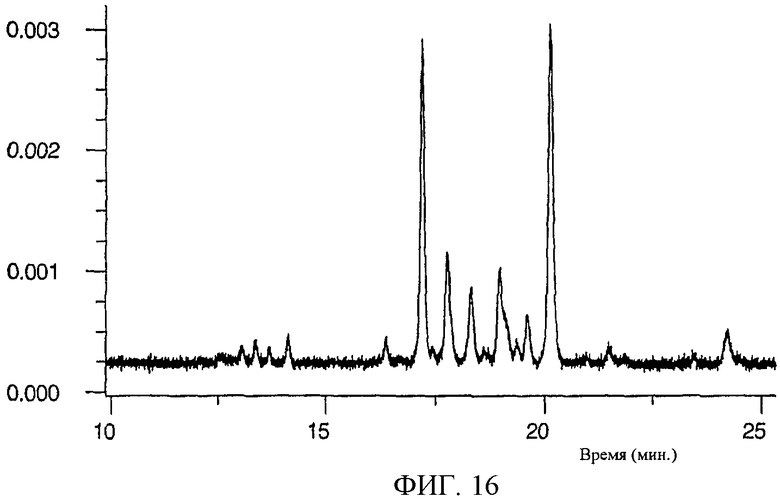
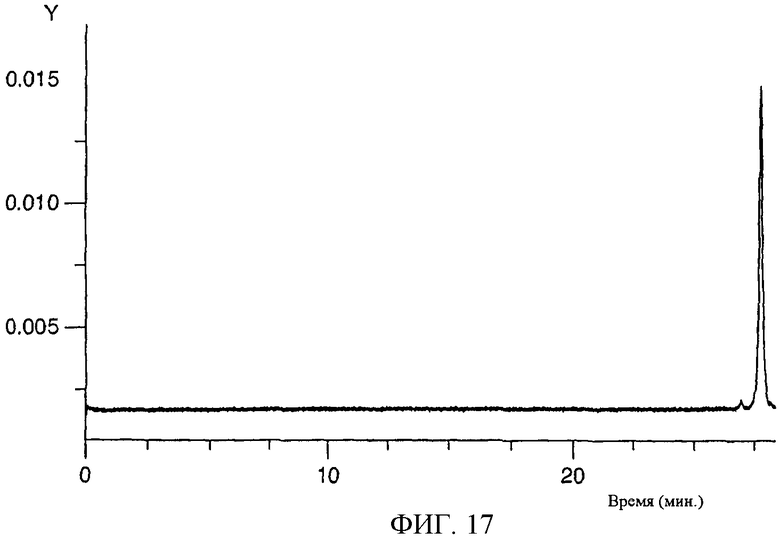
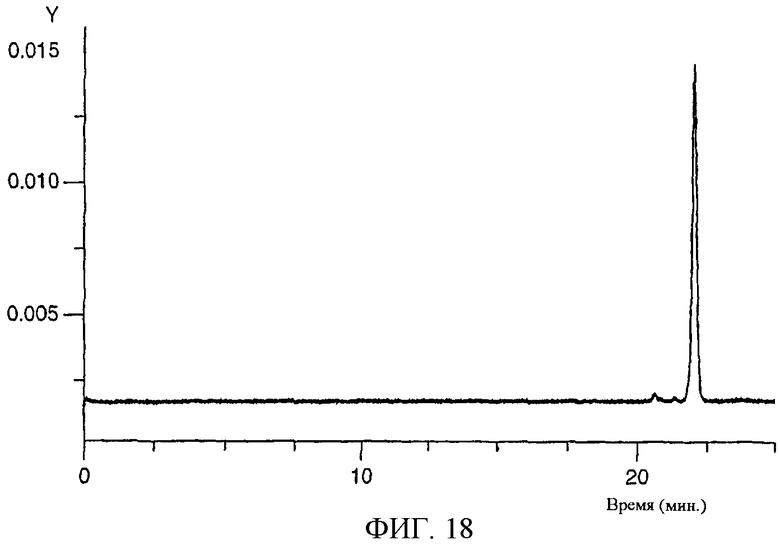
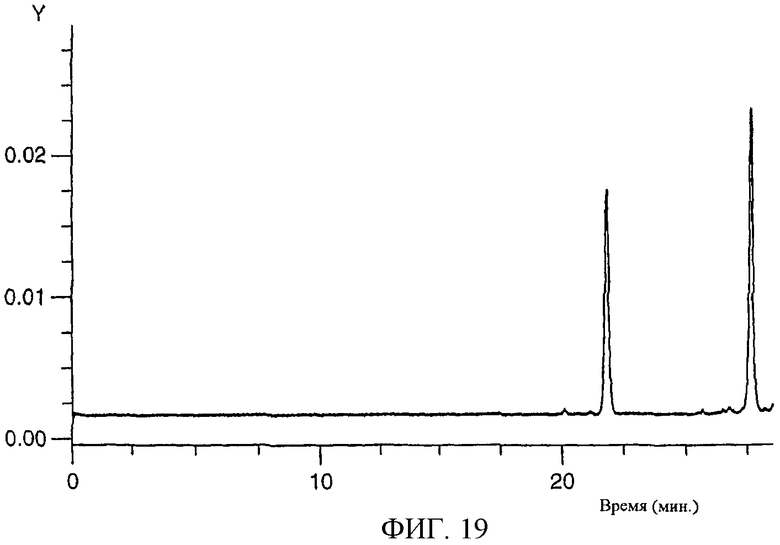
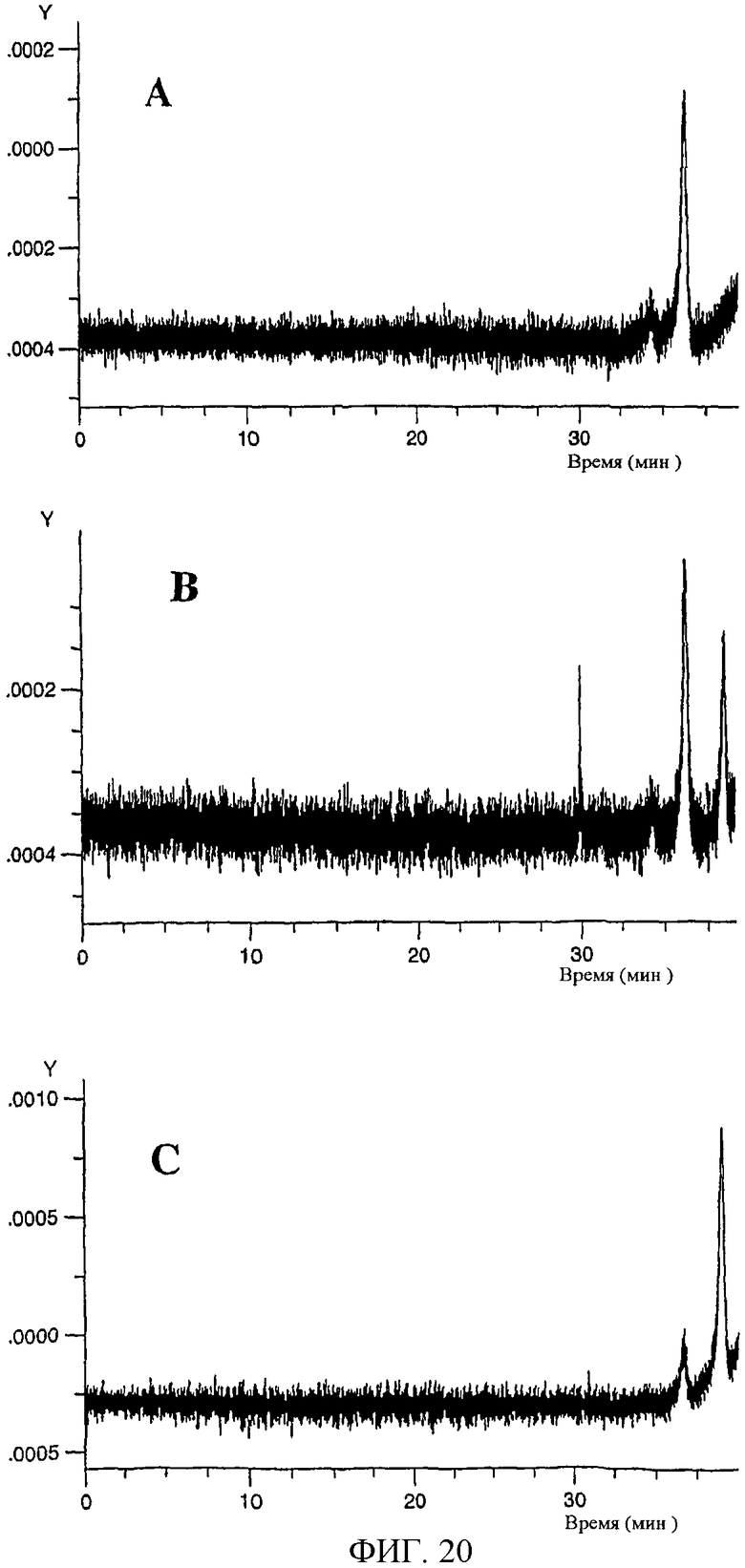
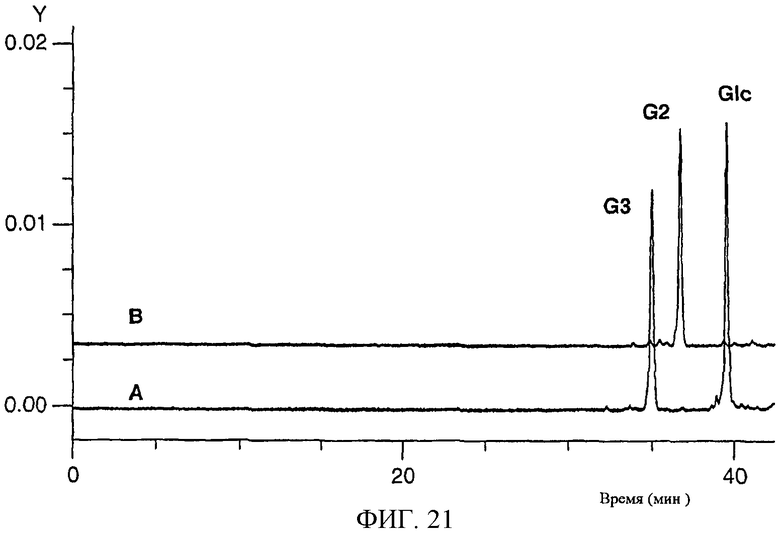
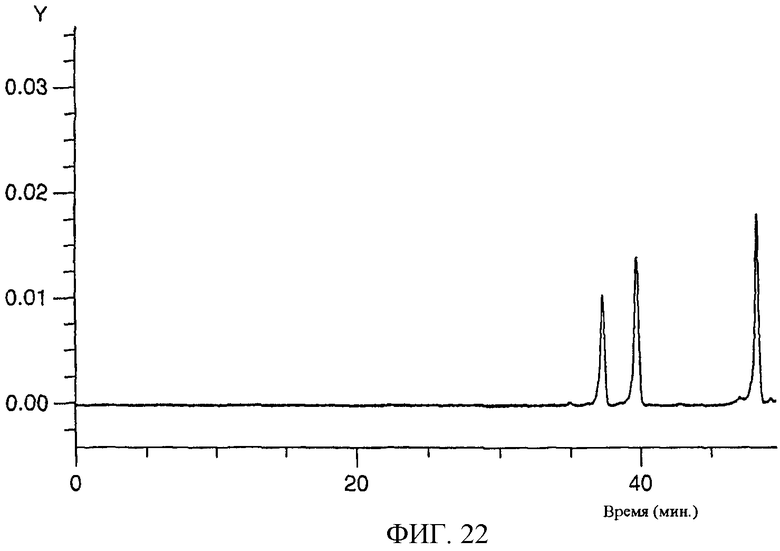
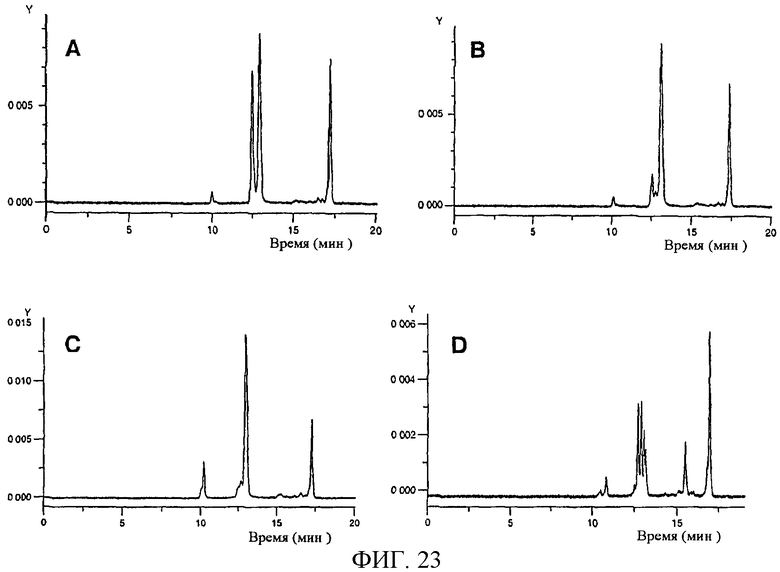
Изобретение относится к области биохимии. Предложен способ получения реактивного сахара, включающий стадии: i) обеспечение образца, содержащего восстанавливающий сахар; ii) обеспечение твердой подложки, ковалентно присоединенной к линкеру, включающему группу захвата, содержащую -NH2 группу, в которой указанный линкер необязательно присоединен к указанной твердой подложке через спейсер; iii) реакция указанного восстанавливающего сахара с указанной -NН2 группой, вследствие чего получают иммобилизированный сахар; iv) реакция свободных -NH2 групп с кэппинг-агентом, причем кэппинг-агент содержит реактивную группу, способную к реакции с -NН2 группой и v) восстановление связей C=N восстановителем, вследствие чего получают реактивный сахар структуры CaxapCHn-NH-, связанный с твердой подложкой через линкер и, необязательно, спейсер, где n - 1 или 2 манипулирования иммобилизированными углеводами путем дериватизации. 44 з.п. ф-лы, 2 табл., 25 ил.
1. Способ получения реактивного сахара, где указанный способ, включает стадии:
i. обеспечение образца, содержащего восстанавливающий сахар;
ii. обеспечение твердой подложки (твердого вещества) ковалентно присоединенной к линкеру, включающему группу захвата, содержащую -NH2 группу, где указанный линкер необязательно присоединен к указанной твердой подложке через спейсер;
iii. реакция указанного восстанавливающего сахара с указанной -NH2 группой, вследствие чего получают иммобилизированный сахар;
iv. реакция свободных -NH2 групп с кэппинг-агентом, причем кэппинг-агент содержит реактивную группу, способную к реакции с -NH2 группой;
v. восстановление связи C^N восстановителем;
vi. вследствие чего получают реактивный сахар структуры CaxapCHn-NH-, связанный с твердой подложкой через линкер и, необязательно, спейсер, где n представляет собой 1 или 2, в котором стадии iv и v могут быть выполнены в любом порядке.
2. Способ по п.1, в котором способ дополнительно включает стадию
vii. реакции -NH-группы реактивного сахара с дериватизирующим агентом, включающим азотсодержащую реактивную функциональную группу (X), вследствие чего получают сахар, ковалентно связанный с указанным агентом.
3. Способ по п.2, в котором указанная азотсодержащая реактивная функциональная группа выбирается из группы, состоящей из изотиоцианатов, активных эфиров, карбоновых кислот, акцепторов Михаэля, альфа-бета ненасыщенных сульфонов, алкилирующих агентов, альдегидов, кетонов и замещенных гетероатомных групп, содержащих электронотрицательные группы.
4. Способ по любому из пп.2 и 3, в котором указанный дериватизирующий агент представляет собой спектроскопически обнаруживаемое соединение, дериватизированное с помощью азотсодержащей реактивной функциональной группы.
5. Способ по любому из пп.2 и 3, в котором указанный дериватизирующий агент представляет собой флуоресцентное соединение, дериватизированное с помощью азотсодержащей реактивной функциональной группы.
6. Способ по п.2, в котором указанный способ дополнительно включает стадию
viii. обнаружения указанного агента, присоединенного к сахару, с помощью спектрометрии.
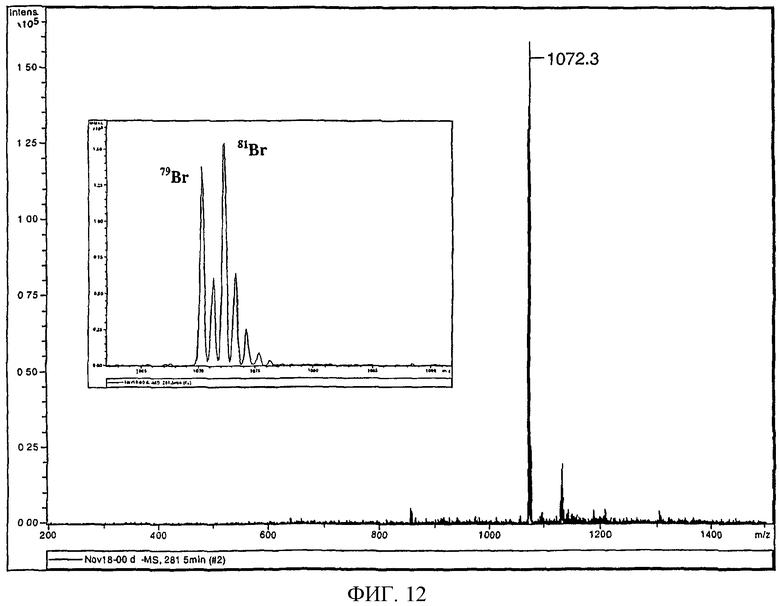
7. Способ по п.2, в котором указанный дериватизирующий агент представляет собой TAG масс-спектрометрии, дериватизированный с помощью азотсодержащей реактивной функциональной группы, где TAG масс-спектрометрии обладает способностью к улучшению обнаружения и/или определения структурных характеристик сахара.
8. Способ по п.7, в котором TAG масс-спектрометрии представляет собой молекулу, содержащую бром.
9. Способ по п.7, в котором TAG масс-спектрометрии представляет собой заряженную молекулу.
10. Способ по п.7, в котором TAG масс-спектрометрии представляет собой меченную изотопом молекулу.
11. Способ по любому из пп.7-10, в котором способ дополнительно включает стадию
viii. обнаружения указанного TAG масс-спектрометрии, присоединенного к сахару, с помощью масс-спектрометрии.
12. Способ по п.2, в котором указанный дериватизирующий агент представляет собой первого связывающего партнера, обладающего способностью к специфичному взаимодействию со вторым связывающим партнером, и где указанный первый связывающий партнер дериватизирован азотсодержащей реактивной функциональной группой.
13. Способ по п.12, в котором один связывающий партнер представляет собой белок, а другой связывающий партнер - лиганд указанного белка.
14. Способ по п.12, в котором один связывающий партнер включает антигенную детерминанту, а другой связывающий партнер представляет собой антитело, специфично распознающее указанную антигенную детерминанту.
15. Способ по п.12, в котором один связывающий партнер представляет собой биотин, а другой связывающий партнер - авидин.
16. Способ по любому из пп.12-15, в котором второй связывающий партнер конъюгирован с обнаруживаемой меткой.
17. Способ по п.2, в котором дериватизирующий агент представляет собой нуклеиновую кислоту, дериватизированную с помощью азотсодержащей реактивной функциональной группы или защищенную азотсодержащей реактивной функциональной группой.
18. Способ по п.17, в котором указанная нуклеиновая кислота представляет собой ДНК.
19. Способ по п.17, в котором способ дополнительно включает стадию
viii. обнаружения указанной нуклеиновой кислоты, присоединенной к указанному сахару.
20. Способ по п.19, в котором указанная нуклеиновая кислота обнаруживается с помощью в значительной мере комплементарной нуклеиновой кислоты, конъюгированной с обнаруживаемой меткой.
21. Способ по п.19, в котором обнаружение указанной нуклеиновой кислоты включает амплификацию нуклеиновой кислоты.
22. Способ по п.2, в котором указанный агент представляет собой бифункциональный реактив структуры Х-мостик-Y или Х-мостик-Yp, где Х представляет собой азотсодержащую реактивную функциональную группу, Y представляет собой вторую реактивную функциональную группу, a Yp представляет собой защищенную реактивную группу Y.
23. Способ по п.22, в котором указанная вторая реактивная функциональная группа Y выбирается из группы, состоящей из тиолов, карбоксигрупп, активированных карбоксигрупп, дисульфидов, активированных дисульфидов, алкилирующих агентов, алкенов, алкинов, альдегидов, кетонов и азидов, или Yp выбирается из группы, состоящей из защищенных производных вышеупомянутых групп Y и защищенных аминов.
24. Способ по п.22, в котором способ дополнительно включает стадии:
viii. обеспечения второго дериватизирующего агента, включающего функциональную группу (Z), обладающую способностью к реакции с Y;
ix. реакции функциональных групп Z и Y, таким образом ковалентно присоединяющих второй дериватизирующий агент к сахару через мостик и первый дериватизирующий агент.
25. Способ по п.24, в котором второй дериватизирующий агент выбирается из группы, состоящей из лекарственных средств, диагностических средств, пептидов, полипептидов, белков, ферментов, нуклеиновых кислот, спектроскопически обнаруживаемых соединений, TAG масс-спектрометрии и первых связывающих партнеров, обладающих способностью к специфичному взаимодействию со вторым связывающим партнером.
26. Способ по любому из пп.22 и 23, в котором способ дополнительно включает стадии:
viii. обеспечения частицы, выбранной из группы, состоящей из микроорганизмов, мицелл, фагов, вирусов и наночастиц, где частица содержит функциональную группу (Z), обладающую способностью к реакции с Y;
ix. реакции функциональных групп Z и Y, таким образом ковалентно присоединяющих частицу к сахару через мостик и агент.
27. Способ по п.1, в котором способ дополнительно включает стадии:
viii. контакта сахара с индикатором, способным к соединению с указанным сахаром;
ix. обнаружения индикатора.
28. Способ по п.27, в котором указанный индикатор содержит арилборонат или гетероарилборонат.
29. Способ по п.27, в котором индикатор представляет собой полипептид.
30. Способ по п.29, в котором указанный полипептид выбирается из группы, состоящей из лектинов, селектинов, токсинов, рецепторов, антител и ферментов.
31. Способ по п.1, в котором группа захвата включает или состоит из структуры M-NH2, где М-гетероатом.
32. Способ по п.1, в котором линкер представляет собой неотщепляемый линкер, выбранный из группы, состоящей из алкилов, арилов, эфиров и амидов, в котором любой из вышеупомянутых может необязательно быть замещенным.
33. Способ по любому из пп.1-3, 6-10, 12-15, 17-25 и 27-31, в котором линкер представляет собой отщепляемый линкер.
34. Способ по п.33, в котором линкер является отщепляемым путем реакций с кислотой, основанием, нуклеофилами, электрофилами, окислением, восстановлением, свободными радикалами, под действием света, повышенной температуры или ферментов.
35. Способ по п.33, в котором способ дополнительно включает стадию отщепления указанного отщепляемого линкера, таким образом, высвобождающего сахар, в котором эта стадия может быть выполнена после стадии v, vi, vii, viii или ix.
36. Способ по п.1, в котором линкер является присоединенным к указанной твердой подложке через спейсер.
37. Способ по п.36, в котором длина спейсера составляет 0-1000 атомов и он является необязательно разветвленным.
38. Способ по п.1, в котором твердая подложка выбирается из группы, состоящей из полимеров, твердых частиц, нерастворимых частиц и поверхностей.
39. Способ по любому из пп.1-3, 6-10, 12-15, 17-25, 27-32 и 34-37, в котором твердая подложка представляет собой датчик.
40. Способ по п.1, в котором способ дополнительно включает стадию контакта сахара с одной или несколькими гликозидазами, в результате чего получают новый восстанавливающий сахар, при условии, что первый сахар представляет собой субстрат для указанной гликозидазы (гликозидаз).
41. Способ по п.40, в котором способ дополнительно включает стадию иммобилизации только что полученного восстанавливающего сахара на твердой подложке.
42. Способ по п.1, в котором способ дополнительно включает стадию контакта сахара с одним или несколькими ферментами, выбранными из классов гликозилтрансфераз, сульфатаз, фосфорилаз, сульфотрансфераз, фосфотрансфераз, гликосинтаз и трансгликозидаз, таким образом преобразовывая указанный сахар в новую структуру.
43. Способ по любому из пп.40-42, включающий обнаружение только что полученных сахаров или структур.
44. Способ по п.1, в котором восстановитель представляет собой боран или борогидрид, содержащий связь ВН или силан, содержащий связь SiH.
45. Способ по п.1, в котором способ включает одновременную инкубацию образца, включающего восстанавливающий сахар, твердой подложки и восстанавливающего агента.
| WO 03014736 А, 20.02.2003 | |||
| WO 9219974 A, 12.12.1992 | |||
| KAKEHI К ЕТ AL: "EFFECT OF CHAIN LENGTH OF OLIGOSACCHARIDE IN HIGH-PERFORMANCE AFFINITY CHROMATOGRAPHY OF A LECTIN ON OLIGOSACCHARIDE IMMOBILIZED COLUMNS" JOURNAL OF CHROMATOGRAPHY, vol | |||
| Мерная кружка для жидких тел | 1914 |
|
SU502A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| АВТОМАТИЧЕСКОЕ УСТРОЙСТВО ДЛЯ ПОДАЧИ УГЛЯ К ТОПКАМ | 1920 |
|
SU297A1 |
| NADKARNI VARSHA D ЕТ AL: "Directional immobilization of heparin onto the | |||
Авторы
Даты
2010-08-27—Публикация
2006-02-08—Подача