Настоящее изобретение относится к новым 1-азабициклоалкильным производным, к способам их получения, к их применению в качестве лекарственных средств и к содержащим их фармацевтическим композициям.
Точнее, в первом варианте осуществления настоящее изобретение относится к соединению формулы I
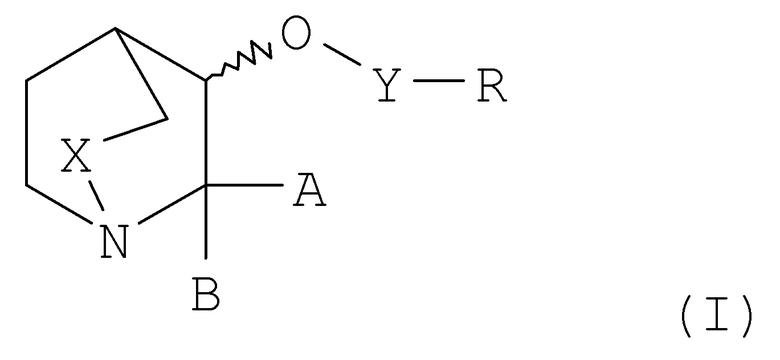
в которой
А и В независимо друг от друга обозначают водород или С1-С7алкил при условии, что оба А и В одновременно не могут обозначать водород, или А и В совместно с атомом углерода, к которому они присоединены, образуют С3-С7циклоалкильную группу; и
Х обозначает СН2 или ординарную связь;
Y обозначает группу формулы
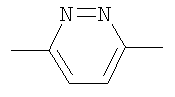 ,
, 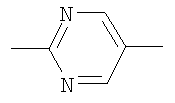 ,
, 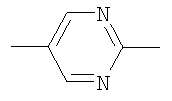 ,
,
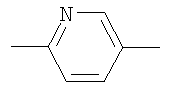 ,
, 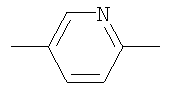 или
или 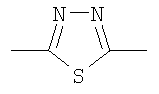 ;
;
в которой левая связь присоединена к атому кислорода, а правая связь присоединена к группе R;
R обозначает замещенный или незамещенный С5-С10арил; замещенный или незамещенный С5-С10гетероарил, группу N(R1)(R5) или группу N(R2)(CHR3R4);
R1 обозначает водород, С1-С4алкил или CF3;
R2 обозначает водород, С1-С4алкил или CF3;
R3 обозначает водород, С1-С4алкил или CF3;
R4 обозначает замещенный или незамещенный С5-С10арил или замещенный или незамещенный С5-С10гетероарил;
R5 обозначает замещенный или незамещенный С5-С10арил или замещенный или незамещенный С5-С10гетероарил;
в форме свободного основания или соли присоединения с кислотой.
Если не указано иное, то общие термины, использующиеся выше и ниже в настоящем изобретении, в контексте настоящего описания предпочтительно обладают указанными ниже значениями:
Термин "незамещенный или замещенный" при использовании в настоящем изобретении означает, что соответствующий радикал может содержит один или большее количество заместителей, предпочтительно - вплоть до 3, более предпочтительно - 1 или 2 заместителя. Заместители предпочтительно выбраны из группы, включающей аминогруппу, С1-С4алкиламиногруппу, ди(С1-С4алкил)-аминогруппу, С3-С5циклоалкиламиногруппу, ди(С3-С5)циклоалкиламиногруппу, N-С1-С4алкил-N-С3-С5циклоалкиламиногруппу, галоген, С1-С4алкил, C4-С6циклоалкил, hydroxy, С1-С4алкоксигруппу, С3-С5циклоалкилоксигруппу, С1-С4алкоксиС1-С4алкоксигруппу, ди(С1-С4алкил)-аминогруппу C1-С4алкоксигруппу, карбамоил, N-С1-С4алкилкарбамоил, N,N-ди(С1-С4алкил)-карбамоил, нитрогруппу, цианогруппу, карбоксигруппу, С1-С4алкоксикарбонил, С1-С4алканоил, С1-С4алканоилоксигруппу, бензоил, амидиновую группу, гуанидиновую группу, уреидную группу, меркаптогруппу, С1-С4алкилтиогруппу, пиридил, фенил, феноксигруппу, С1-С4алкоксифенил, фенилтиогруппу, фенил-С1-С4алкилтиогруппу, С1-С4алкилсульфонил, фенилсульфонил, С1-С4алкилфенилсульфонил, С1-С4алкенил, С1-С4алканоил, С1-С4алкилендиоксигруппу, связанную с соседними атомами С кольца, и С1-С4алкил, который замещен галогеном, гидроксигруппой, С1-С4алкоксигруппой, нитрогруппой, цианогруппой, карбоксигруппой, С1-С4алкоксикарбонилом, С1-С4алканоилом или С1-С4алканоилоксигруппой.
Термины "С5-С10арил", "С5-С10гетероарил" следует понимать как ароматические остатки, которые в каждом случае являются незамещенными или замещенными указанными выше заместителями, предпочтительно в каждом случае являются незамещенными или содержат один или большее количество заместителей, выбранных из группы, включающей галоген, CN и алкил, который может быть незамещенным или замещенным галогеном, например, трифторметил; или С1-С4алкоксигруппой или сконденсирован, например, в бензо[1,3]диоксол или 2,3-дигидробензо[1,4]диоксин и/или в другое гетероциклическое кольцо. С5-С10Гетероарил означает ароматическую гетероциклическую систему, в которой один или большее количество атомов углерода заменены на гетероатомы. Предпочтительными являются 5-9-членные кольцевые системы, содержащие 1, 2 или 3 гетероатома. Примеры С5-С10арильных и С5-С10гетероарильных остатков, указанных выше, включают фенил, нафтил, изобензофуранил, тиенил, индолил.
Термин "алкил" означает обладающую линейной или разветвленной цепью алкильную группу, предпочтительно означает обладающий линейной или разветвленной цепью С1-C7алкил, особенно предпочтительно означает обладающий линейной или разветвленной цепью С1-С4алкил; например, метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, а особенно предпочтительными являются метил, этил, н-пропил и изопропил.
Каждый алкильный фрагмент "алкоксигруппы", "алкоксиалкила", "алкоксикарбонила", "алкоксикарбонилалкила" и "галогеналкила" обладает такими же значениями, которые указаны в приведенном выше определении "алкила". Алкоксигруппа предпочтительно означает С1-С4алкоксигруппу, более предпочтительно - метоксигруппу, этоксигруппу или н-пропоксигруппу.
"Гетероатомами" являются атомы, не представляющие собой углерод и водород, предпочтительно - азот (N), кислород (О) или сера (S).
"Галоген" означает фтор, хлор, бром или йод, предпочтительно означает фтор, хлор или бром и особенно предпочтительно означает хлор.
Вследствие наличия асимметрического атома (атомов) углерода в соединениях формулы I и их солях эти соединения могут существовать в оптически активной форме или в виде смесей оптических изомеров, например, в виде рацемических смесей. Все оптические изомеры и их смеси, включая рацемические смеси, являются частью настоящего изобретения.
Вследствие большого сходства новых соединений в форме свободного основания с соединениями в виде их солей, включая соли, которые можно использовать в качестве промежуточных продуктов, например, при очистке и идентификации новых соединений, любое указание на соединения в форме свободного основания, приведенные выше и ниже в настоящем изобретении, следует понимать как указание также и на соответствующие соли, если они являются подходящими или приемлемыми.
Если соединения, соли и т.п.указаны во множественном чисте, это также означает одно соединение, соль и т.п.
Предпочтительные заместители, предпочтительные диапазоны числовых значений или предпочтительные группы значений радикалов, содержащихся в формуле (I) и соответствующих промежуточных соединениях, определены ниже. Эти заместители, предпочтительные диапазоны числовых значений или предпочтительные группы значений являются предпочтительными по отдельности, совместно и в любой комбинации или подкомбинации:
X предпочтительно обозначает СН2.
А и В совместно с атомом углерода, к которому они присоединены, предпочтительно образуют С3-С7циклоалкильную группу.
А и В совместно с атомом углерода, к которому они присоединены, особенно предпочтительно образуют циклопропильную группу.
А и В предпочтительно обозначают, независимо друг от друга, водород или С1-С4алкил при условии, что оба А и В не могут одновременно обозначать водород.
А и В особенно предпочтительно обозначают, независимо друг от друга, водород или С1-С2алкил при условии, что оба А и В не могут одновременно обозначать водород.
А наиболее предпочтительно обозначает водород и В обозначает метил.
Y предпочтительно обозначает одну из следующих групп:
 ,
,  ,
,  .
.
Y особенно предпочтительно обозначает следующую группу:
 .
.
R предпочтительно обозначает С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, заместители выбраны из группы, включающей галоген; NO2; CN; С1-С4алкоксигруппу, которая является незамещенной или замещена галогеном; С1-С4алкил, который является незамещенным или замещен галогеном, С1-С4алкилС(O)NH, С1-С4алкилсульфонил.
R предпочтительно обозначает гетеро-С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, заместители выбраны из группы, включающей галоген; С1-С2алкоксигруппу; CN и С1-С2алкил, который является незамещенным или замещен галогеном.
R предпочтительно обозначает N(R1)(R5) или N(R2)(CHR3R4).
R особенно предпочтительно обозначает фенил или замещенный фенил, заместители выбраны из группы, включающей хлор, фтор, метил, этил, метоксигруппу, трифторметил, трифторметоксигруппу, цианогруппу, нитрогруппу, ацетамидную группу, метилсульфонил.
R особенно предпочтительно обозначает незамещенный или замещенный гетеро-С5-С10арил, гетероC5-С10арил, выбранный из группы, включающей имидазолил, триазолил, тетразолил, фуранил, тиофенил, бензо[b]тиофенил, оксазолил, изоксазолил, тиазолил, изотиазолил, 1-изобензофуранил, бензо[1,3]-диоксолил, 2,3-дигидробензо[1,4]-диоксинил, бензо[1,2,5]оксадиазолил, бензо[1,2,5]тиадиазолил, хинолинил, изохинолинил; заместители выбраны из группы, включающей хлор, фтор, метил, этил, метоксигруппу, трифторметил, трифторметокси, цианогруппу, нитрогруппу, ацетамидную группу.
R особенно предпочтительно обозначает 5-индолил.
R особенно предпочтительно обозначает 3-метил-2-тиофенил.
R1, R2 и R3 предпочтительно независимо обозначают Н, С1-С4алкил или CF3.
R4 предпочтительно обозначает С5-С10арил или гетеро-С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, заместители выбраны из группы, включающей галоген, C1-С4алкоксигруппу, CN и С1-С2алкил, который является незамещенным или замещен галогеном.
R5 предпочтительно обозначает С5-С10арил или гетеро-С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, заместители выбраны из группы, включающей галоген, С1-С4алкоксигруппу, CN и С1-С2алкил, который является незамещенным или замещен галогеном.
Предпочтительными являются соединения формулы (I), в которой А обозначает водород, В обозначает метил и В находится в транс-положении по отношению к кислороду.
Кроме того, предпочтительными являются соединения формулы (I), в которой исходным соединением формулы (III) является (-)спирт и соединением формулы (II) является производное пиридазина или пиримидина.
Кроме того, предпочтительными являются соединения формулы (I), в которой исходным соединением формулы (III) является (+) спирт и соединением формулы (II) является производное пиридина.
Особенно предпочтительными являются соединения формулы I, в которой
Х обозначает СН2 или ординарную связь,
Y обозначает группу формулы
 ,
,  ,
,  ,
,
 ,
, или
или 
А и В независимо друг от друга обозначают водород или С1-С7алкил при условии, что оба А и В одновременно не могут обозначать водород, или А и В совместно с атомом углерода, к которому они присоединены, образуют С3-С7циклоалкильную группу,
R обозначает С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, выбранных из группы, включающей галоген, NO2, CN, С1-С4алкоксигруппу, которая является незамещенной или замещена галогеном, или С1-С4алкил, который является незамещенным или замещен галогеном; гетеро-С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, выбранных из группы, включающей галоген, С1-С4алкоксигруппу, CN и С1-С2алкил, который является незамещенным или замещен галогеном; N(R1)(R4) или N(R2)(CHR3R4); каждый R1, R2 и R3 независимо обозначает Н, С1-С4алкил или CF3; и R4 обозначает С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, выбранных из группы, включающей галоген, С1-С4алкоксигруппу, CN и С1-С2алкил, который является незамещенным или замещен галогеном; или гетеро-С5-С10арил, который является незамещенным или содержит один или большее количество заместителей, выбранных из группы, включающей галоген, С1-С4алкоксигруппу, CN и С1-С2алкил, который является незамещенным или замещен галогеном.
Кроме того, предпочтительный вариант осуществления настоящего изобретения относится к соединениям формулы I, в которой
Х обозначает СН2 или ординарную связь,
Y обозначает группу формулы

А и В независимо друг от друга обозначают водород или С1-С4алкил при условии, что оба А и В одновременно не могут обозначать водород, или А и В совместно с атомом углерода, к которому они присоединены, образуют С3-С4циклоалкильную группу,
и R обозначает фенил, который является незамещенным или содержит один или большее количество заместителей, выбранных из группы, включающей галоген, NO2, С1-С4алкоксигруппу, которая является незамещенной или замещена галогеном, или С1-С4алкил, который является незамещенным или замещен галогеном.
Особенно предпочтительными соединениями, предлагаемыми в настоящем изобретении, являются соединения, указанные в примерах.
В другом варианте осуществления настоящее изобретение относится к способу получения соединения формулы I, этот способ включает стадию введения в реакцию соединения формулы II

в которой Y и R являются такими, как определено выше для соединения формулы I и Z обозначает отщепляющуюся группу, например, F, Cl, Br, I или OSO2CF3, с соединением формулы III
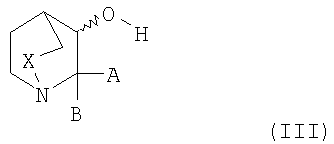
в которой А, В, Х и Y обладают значениями, указанными в определении соединения формулы I, и выделение полученного таким образом соединения формулы I в форме свободного основания или соли присоединения с кислотой.
Эту реакцию можно проводить по стандартным методикам, например, как показано в примерах.
Соединения формулы II являются известными или могут быть получены из соответствующих известных соединений, например, как описано в примерах, например, по аналогии с публикацией Coates WJ, McKillop A (1992) Synthesis 334-342. Соединения формулы III являются известными (Vorob′eva, V.Ya.; Bondarenko, V.A.; Mikhlina, E.E.; Turchin, K.P.; Linberg, L.P.; Yakhontov, L.N. Reaction of 2-methylene-3-oxoquinuclidine with nucleophitic reagents. Khimiya Geterotsiklicheskikh Soedinenii (1977), (10), 1370-6).
Альтернативно соединения формулы I′
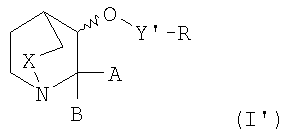
в которой
А, В, Х и R являются такими, как определено выше для соединения формулы I, и
Y′ обозначает одну из следующих групп
 ,
,  ,
, 
 или
или  ,
,
можно получить способом, включающим стадию введения в реакцию соединения формулы IV
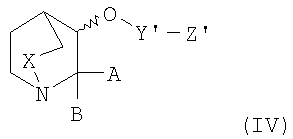
в которой
А, В и Х являются такими, как определено выше для соединения формулы I, и
Y′ является таким, как определено выше для соединения формулы I′,
Z′ обозначает уходящую группу
с соединением формулы V
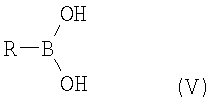
в которой
R является таким, как определено выше для соединения формулы I
В обозначает атом бора,
и выделение полученного таким образом соединения формулы I′ в форме свободного основания или соли присоединения с кислотой.
Соединения формулы IV являются известными или могут быть получены из соответствующих известных соединений, например, путем реакции соединений формулы III с соединениями формулы II′;
 ;
;
в которой
Y′ обозначает одну из следующих групп:
 ,
,  ,
,  ,
, 
Z является таким, как определено выше.
Соединения формулы V (например, незамещенные или замещенные фенилбороновые кислоты) являются известными или могут быть получены из соответствующих известных соединений.
К описанным выше отдельным стадиям реакций относятся следующие положения:
а) Одну или большее количество функциональных групп, например, карбоксигруппу, гидроксигруппу, аминогруппу или меркаптогруппу в исходных веществах может понадобиться защитить. Использующиеся защитные группы могут уже содержаться в предшественниках и защищают соответствующие функциональные группы от нежелательных вторичных реакций, таких как ацилирование, образование простых эфиров, образование сложных эфиров, окисление, сольволиз и аналогичные реакции. Сами защитные группы отличаются тем, что они удаляются легко, т.е. без нежелательных вторичных реакций, обычно путем сольволиза, восстановления, фотолиза или при воздействии ферментов, например, при условиях, аналогичных физиологическим условиям, и что они не содержатся в конечных продуктах. Специалист знает или легко может установить, какие защитные группы являются подходящими для реакций, указанных выше и ниже в настоящем изобретении. Защита таких функциональных групп такими защитными группами, сами защитные группы и реакции их удаления описаны, например, в стандартных справочных пособиях, таких как J.F.W.McOmie, "Protective Groups in Organic Chemistry", Plenum Press, London and New York 1973, в Т.W.Greene, "Protective Groups in Organic Synthesis", Wiley, New York 1981, в "The Peptides"; Volume 3 (editors: E.Gross and J.Meicnhofer), Academic Press, London and New York 1981, в "Methoden der organischen Chemie" (Methods of organic chemistry), Houben Weyl, 4th edition, Volume 15/I, Georg Thieme Verlag, Stuttgart 1974, in H.-D.Jakubke and H.Jescheit, "Aminosäuren, Peptide, Proteine" (Amino acids, peptides, proteins), Verlag Chemie, Weinheim, Deerfield Beach, and Basel 1982, и в Jochen Lehmann, "Chemie der Kohlenhydrate: Monosaccharide und Derivate" (Chemistry of carbohydrates: monosaccharides and derivatives), Georg Thieme Verlag, Stuttgart 1974.
b) Соли присоединения с кислотами можно получить из свободных оснований по известным методикам, и наоборот. Альтернативно можно использовать оптически чистые исходные вещества. Соли присоединения с кислотами, подходящие для применения в контексте настоящего изобретения, включают, например, гидрохлориды.
c) Смеси стереоизомеров, например, смеси диастереоизомеров, можно разделить на соответствующие изомеры по методикам, которые сами по себе известны. Например, смеси диастереоизомеров можно разделить на отдельные диастереоизомеры с помощью фракционной кристаллизации, хроматографии, распределения между растворителями и с помощью аналогичных методик. Это разделение можно выполнить для исходных соединений или для самих соединений формулы I. Энантиомеры можно разделить путем образования солей дистереоизомеров, например, путем образования соли с энантиомерно чистой хиральной кислотой или с помощью хроматографии, например, ВЭЖХ, с использованием хроматографических субстратов с хиральными лигандами. Альтернативно можно использовать оптически чистые исходные вещества.
d) Разбавителями, подходящими для проведения описанных выше процедур, предпочтительно являются инертные органические растворители. К ним, в частности, относятся алифатические, алициклические и ароматические, необязательно галогенированные углеводороды, такие как, например, бензин, бензол, толуол, ксилол, хлорбензол, дихлорбензол, петролейный эфир, гексан, циклогексан, дихлорметан, хлороформ, тетрахлорид углерода; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран и диметиловый эфир этиленгликоля и диэтиловый эфир этиленгликоля; кетоны, такие как ацетон, бутанон и метилизопропилкетон; нитрилы, такие как ацетонитрил, пропионитрил и бутиронитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформамидин, N-метилпирролидон и триамид гексаметилфосфорной кислоты; сложные эфиры, такие как метилацетат и этилацетат; сульфоксиды, такие как диметилсульфоксид, спирты, такие как метанол, этанол н- и изопропанол, монометиловый эфир этиленгликоля, моноэтиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликол. Кроме того, можно использовать смеси разбавителей. В зависимости от исходных веществ, условий проведения реакции и вспомогательных веществ могут быть подходящими вода или содержащие воду разбавители. Кроме того, в качестве разбавителя одновременно можно использовать одно из исходных веществ.
e) Температуру проведения реакции можно менять в относительно широком диапазоне. Обычно способ осуществляют при температурах от 0 до 150°С, предпочтительно - от 10 до 120°С. Условия проведения реакций депротонирования можно менять в относительно широком диапазоне. Обычно способ осуществляют при температурах от -150 до +50°С, предпочтительно - от -75 до 0°С.
f) Реакции обычно проводят при атмосферном давлении. Однако способы, предлагаемые в настоящем изобретении, также можно осуществлять при повышенном или пониженном давлении - обычно от 0,1 до 10 бар.
g) Исходные вещества обычно используются примерно в эквимолярных количествах. Однако также можно использовать относительно большой избыток одного из компонентов. Реакцию обычно проводят в подходящем разбавителе в присутствии вспомогательного вещества для проведения реакции и реакционную смесь обычно перемешивают при повышенной температуре в течение нескольких часов.
h) Обработку реакционных смесей, соответствующих указанным выше способам, и очистку полученных таким образом соединений можно проводить по обычным методикам (см. примеры получения).
Соединения формулы (I) и их фармацевтически приемлемые соли присоединения с кислотами, далее в настоящем изобретении называющимися агентами, предлагаемыми в настоящем изобретении, обладают ценными фармакологическими характеристиками и поэтому применимы в качестве лекарственных средств.
Соединения, предлагаемые в настоящем изобретении, и их фармацевтически приемлемые соли присоединения с кислотами, далее в настоящем изобретении называющимися агентами, предлагаемыми в настоящем изобретении, при исследованиях на животных in vitro проявляют ценные фармакологические характеристики и поэтому применимы в качестве лекарственных средств.
Так, обнаружено, что соединения, предлагаемые в настоящем изобретении, являются холинергическими лигандами nAChR. Кроме того, предпочтительные соединения, предлагаемые в настоящем изобретении, проявляют селективную активность по отношению к α7-nAChR. В частности, может обнаружиться, что соединения, предлагаемые в настоящем изобретении, являются агонистами, частичными агонистами, антагонистами или аллостерическими модуляторами этого рецептора.
Благодаря своим фармакологическим профилям предполагается, что соединения, предлагаемые в настоящем изобретении, применимы для лечения самых различных заболеваний или патологических состояний, включая заболевания, связанные с ЦНС (центральная нервная система), заболевания, связанные с ПНС (периферическая нервная система), заболевания, связанные с воспалением, болью и симптомами отмены, вызванными токсикоманией, заболевания или нарушения, связанные с ЦНС, включают генерализованные тревожные нарушения, нарушения познавательной способности, недостаточность и нарушение способности к обучению и памяти, болезнь Альцгеймера, СДВГ (синдром дефицита внимания с гиперактивностью), болезнь Паркинсона, болезнь Гентингтона, (БАС) боковой амиотрофический склероз, прионные нейродегенеративные нарушения, такие как болезнь Крейтцфельда - Якоба и болезнь куру, болезнь Туретта, психоз, депрессию и депрессивные нарушения, манию, маниакальную депрессию, шизофрению, недостаточность познавательной способности при шизофрении, обсессивно-компульсивные нарушения, панические расстройства, нарушения питания, нарколепсию, ноцицепцию, вызванное СПИД слабоумие, старческое слабоумие, слабое нарушение познавательной способности, связанное с возрастом, аутизм, дислексию, позднюю дискинезию, эпилепсию и судорожные синдромы, посттравматические стрессовые нарушения, временную аноксию, ложное слабоумие, предменструальный синдром, синдром поздней фазы лютеинизации, синдром хронической усталости и десинхроноз, развивающийся при полетах на реактивных самолетах. Кроме того, соединения, предлагаемые в настоящем изобретении, можно применять для лечения эндокринных нарушений, таких как тиреотоксикоз, феохромоцитома, гипертензий и аритмий, а также стенокардии, гиперкинезии, преждевременной эякуляции и затруднения эрекции. В дополнение к этому соединения, предлагаемые в настоящем изобретении, можно применять для лечения воспалительных нарушений (Wang et al., Nature 2003, 421,384), нарушений или патологических состояний, включая воспалительные кожные нарушения, болезнь Крона, воспалительной болезни кишечника, язвенного колита и диареи. Соединения, предлагаемые в настоящем изобретении, также можно применять для лечения симптомов отмены, вызванных прекращением употребления создающих зависимость веществ, таких как табак, никотин, опиоиды, бензодиазепины и алкоголь. Кроме того, соединения, предлагаемые в настоящем изобретении, можно применять для лечения боли, например, вызванной мигренью, послеоперационной боли, фантомной боли в ампутированных конечностях или боли, связанной с раком. Боль может представлять собой воспалительную или невропатическую боль, центральную боль, хроническую головную боль, боль, обусловленную диабетической невропатией, посттерапевтической невралгией или поражением периферического нерва.
Кроме того, дегенеративные глазные заболевания, которые можно лечить, включают глазные заболевания, которые прямо или косвенно могут включать дегенерацию клеток сетчатки, включая ишемические ретинопатии в целом, внутреннюю ишемическую невропатию зрительного нерва, все формы неврита зрительного нерва, возрастную дегенерацию желтого пятна (ВДП) в ее сухих формах (сухая ВДП) и мокрых формах (мокрая ВДП), диабетическую ретинопатию, кистевидный отек желтого пятна (КОЖ), отслоение сетчатки, пигментную дегенерацию сетчатки, дегенерацию желтого пятна Штаргардта, желточноформную дегенерацию желтого пятна, врожденный амавроз Лебера и другие типы наследственной дегенерации сетчатки, патологическую миопию, ретролетальную фиброплазию и наследственную невропатию зрительного нерва Лебера.
В другом варианте осуществления соединения, предлагаемые в настоящем изобретении, применяют в качестве диагностических средств и/или лигандов для ПЭТ, например, для идентификации и локализации никотиновых рецепторов в различных тканях. Соответствующим образом меченые изотопами агенты, предлагаемые в настоящем изобретении, обладают ценными характеристиками при использовании в качестве агентов для мечения образцов для гистопатологических исследований, визуализирующих агентов и/или биомаркеров, далее называемых "маркерами" для селективного мечения nAChR. Агенты, предлагаемые в настоящем изобретении, более предпочтительно применять в качестве маркеров для альфа-7 nAChR рецепторов in vitro или in vivo. В частности, соединения, предлагаемые в настоящем изобретении, соответствующим образом меченые изотопами, применимы в качестве маркеров для ПЭТ. Такие маркеры для ПЭТ помечены одним или большим количеством атомов, выбранных из группы, включающей 11С, 13N, 15О, 18F.
Поэтому агенты, предлагаемые в настоящем изобретении, применимы, например, для определения степени занятости рецептора лекарственным средством, действующим на nAChR, или в диагностических целях при исследовании заболеваний, обусловленных дисбалансом или нарушением функции nAChR, и для мониторинга эффективности медикаментозного лечения таких заболеваний.
В соответствии с указанным выше настоящее изобретение относится к агенту, предлагаемому в настоящем изобретении, предназначенному для применения в качеств маркера для визуализации при нейроисследованиях.
В другом варианте осуществления настоящее изобретение относится к композиции для мечения структур головного мозга и периферической нервной системы, содержащих nAChR, in vivo и in vitro, включающей агент, предлагаемый в настоящем изобретении.
В еще одном варианте осуществления настоящее изобретение относится к способу мечения структур головного мозга и периферической нервной системы, содержащих nAChR, in vivo и in vitro, который включает взаимодействие ткани головного мозга с агентом, предлагаемым в настоящем изобретении.
Способ, предлагаемый в настоящем изобретении, может включать дополнительную стадию, предназначенную для установления того, осуществилось ли мечение целевой структуры агентом, предлагаемым в настоящем изобретении. Эту дополнительную стадию можно провести путем изучения целевой структуры с помощью позитронной эмиссионной томографии (ПЭТ) или однофотонной эмиссионной компьютерной томографии (ОФЭКТ), или любого другого устройства, позволяющего регистрировать радиоактивное излучение.
В частности, агенты, предлагаемые в настоящем изобретении, являются агонистами никотинового ацетилхолинового рецептора α7 (α7 nAChR).
При функциональных анализах агенты, предлагаемые в настоящем изобретении, обнаруживают высокое сродство по отношению к α7 nAChR, о чем свидетельствуют приведенные ниже исследования:
а) Функциональный анализ сродства к α7 nAChR проводят с использованием линии клеток гипофиза крыс, стабильно экспрессирующей α7 nAChR. Вкратце, методика состоит в следующем: Клетки GH3, рекомбинантно экспрессирующие nAChR α7, за 72 ч до эксперимента высевают в черные 96-луночные планшеты и инкубируют при 37°С в увлажненной атмосфере (5% CO2/95% воздуха). В день проведения эксперимента среду удаляют путем встряхивания планшетов и заменяют на 100 мкл среды для выращивания, содержащую чувствительный к кальцию флуоресцентный краситель, в присутствии 2,5 мМ пробеницида (Sigma). Клетки инкубируют при 37°С в увлажненной атмосфере (5% CO2/95% воздуха) в течение 1 ч. Планшеты встряхивают для удаления избытка Fluo-4, дважды промывают забуференным с помощью Hepes (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота) солевым раствором (в мМ: NaCl - 130, KCl - 5,4, CaCl2 - 2, MgSO4 - 0,8, NaH2PO4 - 0,9, глюкоза - 25, Hepes - 20, pH - 7,4; СРХ (сбалансированный солевой раствор Хенкса)) и в них помещают 100 мкл СРХ, при необходимости содержащего антагонист. Инкубирование в присутствии антагониста проводят в течение 3-5 мин. Затем планшеты помещают в визуализирующее устройство считывания планшетов и регистрируют сигнал флуоресценции. В этом анализе соединения, предлагаемые в настоящем изобретении, обладают значениями рЕС50, равными от примерно 5 до примерно 9. В этом исследовании предпочтительными являются частичные и активные агонисты.
b) Для оценки антагонистической активности соединений, предлагаемых в настоящем изобретении, по отношению к нейрональному nAChR α4β2 человека проведен аналогичный функциональный анализ с использованием линии эпителиальных клеток человека, стабильно экспрессирующей подтип α4β2 человека (Michelmore et al., Naunyn-Schmiedeberg′s Arch. Pharmacol. (2002) 366, 235) При этом анализе предпочтительные соединения, предлагаемые в настоящем изобретении, обнаруживают селективность по отношению к подтипам α7 nAChR.
c) Для оценки антагонистической активности соединений, предлагаемых в настоящем изобретении, по отношению к "ганглиозному подтипу" (α3β4), никотиновому рецептору мышечного типа (α1β1γδ) и рецептору 5-НТ3 проведены функциональные анализы, аналогичные описанным выше в разделе а) с использованием линии эпителиальных клеток человека, стабильно экспрессирующей ганглиозный подтип человека, линии клеток, эндогенно экспрессирующей никотиновые рецепторы мышечного типа, или линии клеток, эндогенно экспрессирующей мышиный рецептор 5-НТ3 (Michelmore et al., Naunyn-Schmiedeberg′s Arch. Pharmacol. (2002) 366, 235. Соединения, которые обнаруживают небольшую активность или не обнаруживают активности по отношению к α3β4 nAChR, к никотиновому рецептору мышечного подтипа, а также к рецептору 5-НТ3, являются особенно предпочтительными.
В экспериментах на мышах, характеризующихся недостаточной способностью нервной системы модулировать свою чувствительность по отношению к поступающим сигналам (мыши DBA/2), описанных в публикации S. Leonard et al. in Schizophrenia Bulletin 22, 431-445 (1996), соединения, предлагаемые в настоящем изобретении, значительно стимулируют эту способность при концентрациях, равных от примерно 10 до примерно 40 мкМ.
Можно показать, что соединения, предлагаемые в настоящем изобретении, улучшают внимание при исследовании внимания на грызунах (Robbins, J. Neuropsychiatry Clin. Neurosci. (2001) 13, 326-35), а именно в 5-позиционном исследовании времени реакции (5-CSRTT). При этом исследовании крысы должны смотреть на стенку, содержащую 5 отверстий. Если на одно из них направляется световой импульс, то крыса в течение 5 секунд должна коснуться носом этого отверстия и тогда в качестве награды она получает кусочек пищи, поступающий из кормушки, находящейся в противоположной стенке.
Соединения, предлагаемые в настоящем изобретении, также могут улучшать способность к обучению/память при исследовании группового поведения мышей и крыс (Ennaceur and Delacour, Behav. Brain Res. (1988) 31, 47-59).
Поэтому соединения, предлагаемые в настоящем изобретении, применимы для предупреждения и лечения (включая ослабление и предупреждение) различных нарушений, предпочтительно - указанных выше. Применимость агонистов α7 nAChR в случае нейродегенерации описана в литературе, например, в публикации Wang et al., J. Biol. Chem. 275, 5626-5632 (2000).
Разумеется, при лечении указанных выше и других нарушений подходящая доза соединения (активного ингредиента), предлагаемого в настоящем изобретении, будет меняться в зависимости, например, от субъекта, пути введения и характера и тяжести подвергающегося лечению патологического состояния, а также от относительной активности конкретного использующегося агента, предлагаемого в настоящем изобретении. Например, необходимое количество активного агента можно установить с помощью известных методик исследования in vitro и in vivo путем определения того, как долго концентрация активного агента в плазме крови сохраняется при значении, приемлемом для обеспечения лечебного эффекта. Обычно указывают, что для животных удовлетворительные результаты достигаются при суточных дозах, равных от примерно 0,01 до примерно 30,0 мг/кг при пероральном введении. Для людей назначаемая суточная доза находится в диапазоне от примерно 0,7 до примерно 1400 мг/сутки при пероральном введении, например, от примерно 50 до 200 мг (для человека массой 70 кг), которую обычно вводят однократно или в виде разделенных доз до 4 раз в сутки, или в форме замедленного высвобождения. В соответствии с этим дозированные формы для перорального введения обычно содержат от примерно 1,75 или 2,0 до примерно 700 или 1400 мг соединения, предлагаемого в настоящем изобретении, в смеси с подходящим фармацевтически приемлемым разбавителем или носителем.
Фармацевтические композиции содержат, например, от примерно 0,1 до примерно 99,9%, предпочтительно - от примерно 20 до примерно 60% активного ингредиента (ингредиентов).
Примеры композиций, содержащих соединение, предлагаемое в настоящем изобретении, включают, например, твердую дисперсию, водный раствор, например, содержащий солюбилизирующий агент, микроэмульсию и суспензию, например, соли соединение формулы I или свободного основания соединения формулы I, в диапазоне от 0,1 до 1%, например 0,5%. С помощью подходящей буферной добавки значение рН композиции может быть установлено в диапазоне, например, от 3,5 до 9,5, например до 4,5.
Соединения, предлагаемые в настоящем изобретении, также широко используются в качестве химикатов для исследований.
В случае применения в контексте настоящего изобретения соединение формулы I и/или его фармацевтически приемлемую соль можно вводить в виде одного активного агента или в комбинации с одним или большим количеством других активных агентов формулы I и/или их фармацевтически приемлемых солей или, предпочтительно, других активных агентов, обычно специально применяющихся для лечения нарушений, указанных в настоящем изобретении, или дополнительных других нарушений, любым обычным образом, например, перорально, например, в виде таблеток, капсул, назальных аэрозолей, или парентерально, например, в виде растворов или суспензий для инъекций. Такие другие активные агенты, применяющиеся в таких комбинациях, предпочтительно выбраны из группы, включающей бензодиазепины, селективные ингибиторы повторного поглощения серотонина (СИПС), селективные ингибиторы повторного поглощения серотонина и норэпинефрина (СИПН), обычные нейролептики, атипичные нейролептики, буспирон, карбамазепин, оксакарбазепин, габапентин и прегабалин.
СИПС, пригодный для применения в настоящем изобретении, предпочтительно выбран из группы, включающей флуоксетин, флувоксамин, сертралин, пароксетин, циталопрам и эсциталопрам. СИПН, пригодный для применения в настоящем изобретении, предпочтительно выбран из группы, включающей венлафаксин и дулоксетин. Термин "бензодиазепины" при использовании в настоящем изобретении включает, но не ограничивается только ими клоназепам, диазепам и лоразепам. Термин "обычные нейролептики" при использовании в настоящем изобретении включает, но не ограничивается только ими галоперидол, флуфеназин, тиотиксен и флупентиксол. Термин "атипичные нейролептики" при использовании в настоящем изобретении означает клозарил, рисперидон, оланзапин, кветиапин, зипразидон и арипипразол.
Буспирон можно вводить в виде свободного основания или соли, например, в виде его гидрохлорида, например, в виде, в котором он имеется в продаже, например, под торговым названием буспар™ или беспар™. Его можно получить и вводить, например, как это описано в US 3717634. Флуоксетин можно вводить, например, в виде его гидрохлорида, в котором он имеется в продаже, например, под торговым названием прозак™. Его можно получить и вводить, например, как это описано в СА 2002182. Паркосетин ((3S,4R)-3-[(1,3-бензодиоксол-5-илокси)метил]-4-(4-фторфенил)пиперидин) можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием паксил™. Его можно получить и вводить, например, как это описано в US 3912743. Сертралин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием золофт™. Его можно получить и вводить, например, как это описано в US 4536518. Клоназепам можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием антелепсин™. Диазепам можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием диазепам десинит™. Лоразепам можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием тавор™. Циталопрам можно вводить в виде свободного основания или соли, например, в виде его гидробромида, например, в виде, в котором он имеется в продаже, например, под торговым названием ципрамил™. Эсциталопрам можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием ципралекс™. Его можно получить и вводить, например, как это описано в AU 623144. Венлафаксин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием тревилор™. Дулоксетин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием цимбалта™. Его можно получить и вводить, например, как это описано в СА 1302421. Карбамазепин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием тегретал™ или тегретол™. Окскарбазепин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием трилептал™. Окскарбазепин хорошо известен из литературы [см. например, Schuctz H. et al., Xenobiotica (GB), 16 (8), 769-778 (1986)]. Габапентин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием нейронтин™. Галоперидол можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием галоперидол СТАДА™. Флуфеназин можно вводить, например, в виде его дигидрохлорида, в котором он имеется в продаже, например, под торговым названием проликсин™. Тиотиксен можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием наван™. Его можно получить, например, как это описано в US 3310553. Флупентиксол можно вводить, например, в виде его дигидрохлорида, например, в виде, в котором он имеется в продаже, например, под торговым названием эмергил™ или в виде его деканоата, например, в виде, в котором он имеется в продаже, например, под торговым названием депиксол™. Его можно получить, например, как это описано в ВР 925538. Клозарил можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием лепонекс™. Его можно получить, например, как это описано в US 3539573. Рисперидон можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием риспердал™. Оланзапин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием зипрекса™. Кветиапин можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием сероквел™. Зипразидон можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием геодон™. Его можно получить, например, как это описано в GB 281309. Арипипразол можно вводить, например, в виде, в котором он имеется в продаже, например, под торговым названием абилифи™. Его можно получить, например, как это описано в US 5006528.
Структура активных ингредиентов, обозначаемых кодовыми номерами, родовыми или торговыми названиями, приведена в последнем издании стандартного справочника "The Merck Index" или в базах данных, например, Patents International (например, IMS World Publications). Соответствующее их содержание включено в настоящую заявку в качестве ссылки. Любой специалист в данной области техники вполне может идентифицировать активные агенты и на основании этих ссылок также может изготовить и исследовать фармацевтические показания и характеристики с помощью стандартных моделей, как in vitro, так и in vivo.
В случае комбинации фармацевтические композиции, предназначенные для раздельного введения компонентов комбинации и/или предназначенные для введения компонентов в фиксированной комбинации, т.е. одной галеновой композиции, включающей по меньшей мере 2 компонента комбинации, предлагаемые в настоящем изобретении, можно получить по методике, которая сама по себе известна, и они пригодны для энтерального, такого как пероральное, или ректального и парентерального, введения млекопитающим, включая человека, и содержат терапевтически эффективное количество по меньшей мере одного фармакологически активного компонента комбинации по отдельности или в комбинации с одним или большим количеством фармацевтически приемлемых носителей, особенно подходящих для энтерального или парентерального введения. Если применяющиеся компоненты комбинации вводят в том виде, в котором они имеются в продаже, в виде отдельных лекарственных средств, то, если в настоящем изобретении не указано иное, для обеспечения описанного в настоящем изобретении благоприятного эффекта их дозировка и путь введения могут быть такими, как это указано в информации, приведенной в листке-вкладыше соответствующего имеющегося в продаже лекарственного средства.
Фармацевтическими препаратами для комбинированной терапии при энтеральном или парентеральном введении являются, например, препараты в виде разовых дозированных форм, таких как таблетки, покрытые сахаром, таблетки, капсулы или суппозитории, а также ампулы. Если не указано иное, то их готовят по методикам, которые сами по себе известны, например, с помощью обычных методик смешивания, гранулирования, нанесения покрытия из сахара, растворения или лиофилизации. Следует понимать, что разовое количество компонента комбинации, содержащееся в отдельной дозе каждой дозированной формы само по себе, не должно являться эффективным количеством, поскольку необходимое эффективное количество может быть обеспечено путем введения не только одной дозированной формы, но и двух или большего количества дозированных форм.
В частности, терапевтически эффективное количество каждого компонента комбинации можно ввести одновременно или последовательно в любом порядке и компоненты можно вводить по отдельности (например, последовательно через постоянные или переменные промежутки времени) или в виде фиксированной комбинации. Например, способ лечения (включая ослабление) нарушения в контексте настоящего изобретения может включать (i) введение компонента комбинации (а) (соединения, предлагаемого в настоящем изобретении) в форме свободного основания или фармацевтически приемлемой соли и (ii) введение компонента комбинации (b) (например, другого соединения, предлагаемого в настоящем изобретении, или активного ингредиента, описываемого другой формулой) в форме свободного основания или фармацевтически приемлемой соли одновременно или последовательно в любом порядке, в количествах, которые совместно являются терапевтически эффективными, предпочтительно - в синергетически эффективных количествах, например, в вид суточных доз, содержащих количества, описанные в настоящем изобретении. Отдельные компоненты комбинации можно вводить по отдельности в разные моменты времени в течение курса лечения или одновременно в виде разделенных или разовых комбинированных форм. Кроме того, термин "введение" также включает применение пролекарства компонента комбинации, которое in vivo превращается в сам компонент комбинации. Поэтому следует понимать, что настоящее изобретение включает все такие режимы одновременного и/или поочередного лечения и термин "введение" следует интерпретировать соответствующим образом.
Эффективная использующаяся доза компонентов комбинации может меняться, например, в зависимости от конкретного применяющегося соединения или фармацевтической композиции, пути введения, подвергающегося лечению нарушения и/или тяжести подвергающегося лечению нарушения. Таким образом дозировочный режим выбирается в зависимости от множества факторов, включая путь введения, метаболизм соединения и работы почек и печени пациента. Врач, клиницист или ветеринар с общей подготовкой в данной области техники может легко определить и назначить эффективное количество одного из активных ингредиентов, необходимое для предупреждения, ослабления, противодействия или подавления нарушения. Оптимальная точность при установлении концентраций активных ингредиентов в диапазоне, в котором обеспечивается эффективность без проявления токсичности, требует выбора режима на основании кинетики поступления активного ингредиента в необходимые области организма.
В соответствии с указанным выше настоящее изобретение также относится к:
(1) Соединению формулы I, и/или его соли, предназначенному для применения в целях диагностического или медикаментозного лечения млекопитающего, предпочтительно - человека; предпочтительно - для применения в качестве агониста альфа-7 рецептора, например, для применения в целях лечения (включая ослабление) любого одного или большего количества нарушений, предпочтительно - любого одного или большего количества конкретных нарушений, указанных выше и ниже в настоящем изобретении.
(2) Фармацевтической композиции, включающей в качестве активного ингредиента соединение формулы I и/или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым разбавителем или носителем.
(2′) Фармацевтической композиции, предназначенной для лечения или предупреждения нарушения, при лечении которого играет роль активация альфа-7 рецептора или он участвует и/или в котором проявляется активность альфа-7 рецептора, предпочтительно - любого одного или большего количества нарушений, указанных выше и ниже в настоящем изобретении, включающей соединение формулы I и/или его фармацевтически приемлемую соль и фармацевтически приемлемый разбавитель или носитель.
(3) Способу лечения нарушения, предпочтительно - любого одного или большего количества конкретных нарушений, указанных выше в настоящем изобретении, у субъекта, нуждающегося в таком лечении, включающему введение фармацевтически эффективного количества соединения формулы I или его фармацевтически приемлемой соли.
(3′) Способу лечения или предупреждения нарушения, при лечении которого играет роль активация альфа-7 рецептора или он участвует и/или в котором проявляется активность альфа-7 рецептора, включающему введение нуждающемуся в нем млекопитающему терапевтически эффективного количества соединения формулы I и/или его фармацевтически приемлемой соли.
(4) Применению соединения формулы I и/или его фармацевтически приемлемой соли для приготовления лекарственного средства, предназначенного для лечения или предупреждения заболевания или патологического состояния, при лечении которого играет роль активация альфа-7 рецептора или он участвует и/или в котором проявляется активность альфа-7 рецептора, предпочтительно - одного или большего количества нарушений, указанных выше.
(5) Способ, описанный выше, включающий совместное введение, например, одновременное или последовательное, терапевтически эффективного количества альфа-7 агониста формулы I и/или его фармацевтически приемлемой соли и второго фармацевтически активного соединения и/или его фармацевтически приемлемой соли, указанное второе фармацевтически активное соединение и/или его соль является особенно подходящим для применения при лечении любого одного или большего количества нарушений, указанных выше и ниже в настоящем изобретении.
(6) Комбинации, включающей терапевтически эффективное количество альфа-7 агониста формулы I и/или его фармацевтически приемлемой соли и второго фармацевтически активного соединения и/или его фармацевтически приемлемой соли, указанное второе фармацевтически активное соединение является особенно подходящим для применения при лечении любого одного или большего количества конкретных нарушений, указанных выше в настоящем изобретении.
(7) Продукт, полученный описанным выше способом, характеризующийся тем, что в качестве исходного вещества используется (+)-транс-2-метил-1-азабицикло[2.2.2]октан-3-ол и Y представляет собой пиримидинил или пиридазинил.
(7′) Продукт, полученный описанным выше способом, характеризующийся тем, что в качестве исходного вещества используется (-)-транс-2-метил-1-азабицикло[2.2.2]октан-3-ол и Y представляет собой пиридинил.
Приведенные ниже примеры предназначены для иллюстрации настоящего изобретения без наложения ограничений его объема.
Используются следующие аббревиатуры:
Температуру измеряют в градусах Цельсия. Если не указано иное, то реакции проводят при комнатной температуре. Структуру конечных продуктов, промежуточных продуктов и исходных веществ подтверждают с помощью стандартных аналитических методик, например, микроанализа, и спектроскопических характеристик (например, масс-спектроскопии (МС), ИК-спектроскопии, ЯМР).
Пример 1: Получение рац-транс-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октана
Раствор рац-транс-2-метил-1-азабицикло[2.2.2]октан-3-ола (1,3 ммоль) в ДМФ (5 мл) обрабатывают гидридом натрия (60% в минеральном масле; 1,3 ммоль). Через 1 ч при КТ прибавляют раствор 3-хлор-6-(2-фтор-4-метилфенил)-пиридазина (1,5 ммоль) в ДМФ (30 мл) и реакционную смесь нагревают при 50°С в течение 16 ч. После охлаждения до КТ реакцию в растворе в ДМФ останавливают с помощью 10% раствора NaCl, экстрагируют метилендихлоридом (2×15 мл), а затем раствором хлорида натрия (20 мл). Органический слой сушат над безводным сульфатом магния, фильтруют и выпаривают досуха и оставшееся масло очищают с помощью хроматографии на колонке с силикагелем (элюент: CH2Cl2:СН3ОН:NH3; 95:5:0,1) и получают рац-транс-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан в виде бесцветного масла. МС (ЭР+ - ионизация электрораспылением): m/е=328,4 (МН+).
Пример 2
Аналогичным образом с использованием соответствующих исходных веществ получают указанное ниже соединение:
рац-транс-2-метил-3-(6-фенилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=296,4 (МН+)
Пример 3
С использованием соответствующих исходных веществ по методике, описанной в примере 1, можно получить указанные ниже соединения:
3а) (2S,3R)-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328,4 (МН+)
3b) (2R,3S)-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328,4 (МН+)
3с) (2RS,3RS)-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328,4 (МН+)
3d) (2SR,3RS)-2-метил-3-(6-фенилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=296,4 (МН+)
3е) (2SR,3RS)-2-метил-3-[6-(5-метилтиофен-2-ил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=316 (МН+); т.пл. 148-150°С
3f) (2S,3R)-2-метил-3-[6-(5-метилтиофен-2-ил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан
3g) (2R,3S)-2-метил-3-[6-(5-метилтиофен-2-ил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан
3h) (28R,3RS)-3-[5-(1Н-индол-5-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=334,4 (МН+)
3i) (+)-3-[5-(1Н-индол-5-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=334,4 (МН+), [α]D(25)=+210 (с=1, МеОН)
3j) (-)-3-[5-(1Н-индол-5-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=334,4 (МН+), [α]D(25)=-150 (с=1, МеОН)
3k) (2SR,3RS)-3-[6-(1Н-индол-5-ил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=335 (МН+), т.пл. 210-213°С, хиральная хроматография: [колонка: Chiralpak AD, 250-4,6 мм, 10 мкм; элюент: гексан/EtOH 60:40+0,1% ТФК (трифторуксусная кислота); скорость потока: 1,0 мл/мин; детектор: УФ 254 нм], пик 1: 5,533 мин, пик 2: 9,258 мин
3l) (2S,3R)-3-[6-(1H-индол-5-ил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан
3m) (2R,3S)-3-[6-(1Н-индол-5-ил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан
3n) (2SR,3RS)-3-[5-(1Н-индол-5-ил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=335 (МН+), т.пл.: 219-222°С
3о) (2S,3R)-3-[5-(1Н-индол-5-ил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=335 (МН+)
3р) (2R,3S)-3-[5-(1Н-индол-5-ил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3q) (2SR,3RS)-3-[6-(2,3-диметил-1Н-индол-5-ил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=363 (МН+)
3r) (2SR,3RS)-3-[5-(1Н-индол-5-ил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=335,4 (МН+)
3s) (2SR,3RS)-3-[6-(2,5-дифтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-azabicyclo[2.2.2]октан, МС (ЭР+): m/е=346 (МН+)
3t) (2SR,3RS)-2-метил-3-(6-п-толилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=310 (МН+)
3u) (2SR,3RS)-2-метил-3-(6-м-толилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=310 (МН+)
3v) (2SR,3RS)-2-метил-3-(6-п-толилпиридин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=309 (МН+)
3w) (2SR,3RS)-2-метил-3-[6-(3-нитрофенил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=341 (МН+)
3х) (2SR,3RS)-N-{3-[6-(2-метил-1-азабицикло[2.2.2]окт-3-илокси)-пиридазин-3-ил]-фенил}ацетамид, МС (ЭР+): m/е=353 (МН+)
3y) (2SR,3RS)-3-[6-(5-этил-2-фторфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=342 (МН+)
3z) (2SR,3RS)-3-(6-бензо[1,3]диоксол-5-илпиридазин-3-илокси)-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=340 (МН+)
3аа) (2SR,3RS)-3-[6-(3-метоксифенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=326 (МН+)
3ab) (2SR,3RS)-3-[6-(2-хлор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=344 (МН+)
3ас) (2SR,3RS)-N-{4-[6-(2-метил-1-азабицикло[2.2.2]окт-3-илокси)-пиридазин-3-ил]-фенил}-ацетамид, МС (ЭР+): m/е=353 (МН+)
3ad) (2SR,3RS)-2-метил-3-[6-(1-метил-1Н-индол-5-ил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=349 (МН+)
3ае) (2SR,3RS)-3-[6-(2-фтор-5-метокси-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=358 (МН+)
3af) (2SR,3RS)-3-[5-(3,5-диметилфенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=323,2 (МН+)
3ag) (2SR,3RS)-3-[5-(3,4-дифторфенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=331,1 (МН+)
3ah) (2SR,3RS)-3-[6-(3,4-диметилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=324 (МН+)
3ai) (2SR,3RS)-3-[6-(2-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328,4 (МН+)
3aj) (2SR,3RS)-3-[6-(4-фторфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=314 (МН+)
3ak) (2SR,3RS)-2-метил-3-[6-(3-трифторметоксифенил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=380 (МН+)
2al) (2SR,3RS)-3-[6-(4-этилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=324 (МН+)
3am) (2SR,3RS)-3-[6-(3,4-диметоксифенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=356 (МН+)
3an) (2SR,3RS)-2-метил-3-(5-фенилпиридин-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=295,5 (МН+)
3ао) (2SR,3RS)-3-[6-(3-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328 (МН+)
3ар) (2SR,3RS)-(2RS,3RS)-2-метил-3-(6-п-толилпиридин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=309 (МН+)
3aq) (2SR,3RS)-3-[6-(2,5-диметоксифенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=356 (МН+)
3ar) (2SR,3RS)-2-метил-3-(5-фенил-[1,3,4]тиадиазол-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=302 (МН+)
3as) (2SR,3RS)-3-[6-(3-хлорфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=330 (МН+)
3at) (2SR,3RS)-3-[5-(2-фтор-4-метилфенил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328 (МН+)
3au) (2RS,3RS)-3-[6-(4-этилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=324 (МН+)
3av) (2RS,3RS)-3-[6-(2,5-дифтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=346 (МН+)
3aw) (2SR,3RS)-2-метил-3-[6-(3-трифторметил-фенил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=364 (МН+)
3ах) (2RS,3RS)-2-метил-3-(6-п-толилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=310 (МН+)
3ay) (2SR,3RS)-2-метил-3-(5-м-толилпиридин-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=309,1 (МН+)
3az) (2SR,3RS)-3-(5-фуран-3-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=285,1 (МН+)
3ba) (2SR,3RS)-3-(5-бензо[1,3]диоксол-5-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/e=339,1 (МН+)
3bb) (2SR,3RS)-2-метил-3-(5-п-толилпиридин-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=309,2 (МН+)
3bc) (2SR,3RS)-3-[5-(1Н-индол-6-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=334,2 (МН+)
3bd) (2SR,3RS)-3-[6-(6-метоксипиридин-3-ил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=327 (МН+)
3be) (2SR,3RS)-2-метил-3-[6-(2-метилбензотиазол-5-ил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=367,4 (МН+)
3bg) (2SR,3RS)-3-[6-(3,4-дихлорфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=364 (МН+)
3bh) (2SR,3RS)-3-[5-(2-фторфенил)-пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=314 (MH+)
3bi) (2RS,3RS)-2-метил-3-(5-фенил-[1,3,4]тиадиазол-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=302 (МН+)
3bj) (2SR,3RS)-2-метил-3-[5-(1-метил-1Н-индол-5-ил)-пиридин-2-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=348,2 (МН+)
3bk) (2SR,3RS)-3-[5-(2-фторфенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=313,1 (МН+)
3bl) (2SR,3RS)-3-[6-(3-хлорфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=330 (МН+)
3bm) (2SR,3RS)-2-метил-3-(5-фенилпиримидин-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=296 (МН+)
3bn) (2SR,3RS)-2-метил-3-(5-п-толилпиримидин-2-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=310 (МН+)
3bo) (2RS,3RS)-3-[6-(5-этил-2-фторфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=342 (МН+)
3bp) (2RS,3RS)-3-[6-(2-фтор-5-метокси-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=358 (МН+)
3bq) (2SR,3RS)-3-[5-(2,3-диметил-1Н-индол-6-ил)-пиридин-2-илокси]-2-метил-1 азабицикло[2.2.2]октан, МС (ЭР+): m/е=362,1 (МН+)
3br) (2RS,3RS)-3-[6-(3-фтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=328 (МН+)
3bs) (2SR,3RS)-3-[6-(2,3-дифтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=346 (МН+)
3bt) (2SR,3RS)-3-[5-(4-метоксифенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=325,2 (МН+)
3bu) (2SR,3RS)-3-[5-(2,2-дифтор-бензо[1,3]диоксол-5-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=375,4 (МН+)
3bv) (2RS,3RS)-3-[6-(3,4-дихлорфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=364 (МН+)
3bw) (2SR,3RS)-3-(5-Biphenyl-4-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=371,1 (МН+)
3bx) (2SR,3RS)-2-метил-3-[6-(3-трифторметил-фенил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=364 (МН+)
3by) (2SR,3RS)-3-[5-(2,5-дифтор-4-метилфенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=345,2 (МН+)
3bz) (2SR,3RS)-3-(5-бензо[1,3]диоксол-5-илэтинил-пиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=363,9 (МН+)
3са) (2SR,3RS)-5-[6-(2-метил-1-азабицикло[2.2.2]окт-3-илокси)-пиридин-3-ил]-хинолин, МС (ЭР+): m/е=346,4 (МН+)
3cb) (2RS,3RS)-3-[6-(2,3-дифтор-4-метилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=346 (МН+)
3сс) (2SR,3RS)-3-[5-(2-фтор-4-метилфенил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=327,3 (МН+)
3cd) (2RS,3RS)-2-метил-3-(6-фенилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=296,4 (МН+)
3се) (2RS,3RS)-3-[6-(3,4-диметилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=324 (MH+)
3cf) (2RS,3RS)-2-метил-3-(6-м-толилпиридазин-3-илокси)-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=310 (МН+)
3cg) (2SR,3RS)-3-[6-(4-метансульфонилфенил)-пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=374 (МН+)
3ch) (2SR,3RS)-3-[6-(2-метил-1-азабицикло[2.2.2]окт-3-илокси)-пиридин-3-илэтинил]-хинолин, МС (ЭР+): m/е=370,0 (МН+)
3ci) (2SR,3RS)-(2RS,3RS)-2-метил-3-[6-(3-трифторметоксифенил)-пиридазин-3-илокси]-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=380 (МН+)
3cj) (2SR,3RS)-3-[5-(2,3-дигидробензофуран-5-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан, МС (ЭР+): m/е=337,1 (МН+)
3ck) (2SR,3RS)-3-(5-йодпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан МС (ЭР+): m/е=345,1 (МН+)
3cl) (2SR,3RS)-3-(5-йодпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3cm) (2SR,3RS)-3-(5-йодпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3cn) (2SR,3RS)-3-(5-бензо[b]тиофен-2-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3со) (2SR,3RS)-3-(5-бензо[b]тиофен-3-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3ср) (2SR,3RS)-3-(5-дибензотиофен-4-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3cq) (2SR,3RS)-3-(5-дибензофуран-4-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3cr) (2SR,3RS)-2-метил-3-[5-(1-фенил-1Н-индол-5-ил)-пиридин-2-илокси]-1-азабицикло[2.2.2]октан
3cs) (2SR,3RS)-3-{5-[1-(4-метоксифенил)-1Н-индол-5-ил]-пиридин-2-илокси}-2-метил-1-азабицикло[2.2.2]октан
3ct) (2SR,3RS)-3-[5-(1Н-индол-7-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3cu) (2SR,3RS)-3-[5-(1Н-индол-4-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3cv) (2SR,3RS)-3-[5-(1Н-индол-3-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3cw) (2SR,3RS)-3-[5-(1-бензолсульфонил-1Н-индол-3-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3сх) (2SR,3RS)-3-[5-(1-бензолсульфоннл-1Н-индол-2-ил)-пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3cy) (2SR,3RS)-3-[5-(1Н-индол-2-ил)-пирндин-2-илокси]-2-метил-1-азабицикло[2.2.2]октан
3cz) (2SR,3RS)-3-(5-бензо[b]тиофен-4-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3da) (2SR,3RS)-3-(5-бензо[b]тиофен-7-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3db) (2SR,3RS)-3-(5-бензо[b]тиофен-6-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3dc) (2SR,3RS)-3-(5-бензо[b]тиофен-5-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3dd) (2SR,3RS)-3-(5-бензофуран-5-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3de) (2SR,3RS)-3-(5-бензофуран-6-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3df) (2SR,3RS)-3-(5-бензофуран-7-илпиридин-2-илокси)-2-метил-1-аза6ицикло[2.2.2]октан
3dg) (2SR,3RS)-3-(5-бензофуран-4-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3dh) (2SR,3RS)-3-(5-бензофуран-2-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3di) (2SR,3RS)-3-(5-бензофуран-2-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3dj) (2SR,3RS)-3-(5-бензо[1,2,5]оксадиазол-5-илпиридин-2-илокси)-2-метил-1-азабицикло[2.2.2]октан
3dk) (2SR,3RS)-2-метил-3-[5-(5-метилтиофен-2-ил)-пиридин-2-илокси]-1-азабицикло[2.2.2]октан
3di) (2SR,3RS)-3-[6-(1Н-индол-5-ил)-пиридин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан
3dm) (2SR,3RS)-2-метил-3-[6-(1-метил-1Н-индол-5-ил)-пиридин-3-илокси]-1-азабицикло[2.2.2]октан
3dn) (2SR,3RS)-3-[6-(1-бензил-1Н-индол-5-ил)-пиридин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан
3do) (2SR,3RS)-2-метил-3-[5-(5-метилтиофен-2-ил)-пиримидин-2-илокси]-1-аза-бицикло[2.2.2]октан
Пример 4: Мягкие капсулы
5000 Капсул из мягкого желатина, каждая из которых содержит в качестве активного ингредиента 0,05 г одного из соединений формулы I, указанных в предыдущих примерах, готовят следующим образом:
Состав
Методика приготовления: Измельченный в порошок активный ингредиент суспендируют в лаурогликоле® (лаурат пропиленгликоля, Gattefossé S.A., Saint Priest, France) и размалывают в устройстве для влажного измельчения с получением частиц размером примерно от 1 до 3 мкм. Затем порции смеси по 0,419 г помещают в капсулы из мягкого желатина с помощью машины для наполнения капсул.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 1-АЗАБИЦИКЛО[3.3.1]НОНАНОВ | 2005 |
|
RU2445313C2 |
| АЗАБИЦИКЛОАЛКИЛЬНЫЕ ЭФИРЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТОВ АЛЬФА7-nAChR | 2003 |
|
RU2352569C2 |
| (1-АЗАБИЦИКЛО[3,3,1]НОН-4-ИЛ)-[5-(1Н-ИНДОЛ-5-ИЛ)-ГЕТЕРОАРИЛ]-АМИНЫ, КАК ХОЛИНЕРГИЧЕСКИЕ ЛИГАНДЫ nAChR, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ПСИХОТИЧЕСКИХ И НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2006 |
|
RU2440350C2 |
| АЗАБИЦИКЛИЧЕСКИЕ АЛКАНОВЫЕ ПРОИЗВОДНЫЕ, ЗАМЕЩЕННЫЕ КОНДЕНСИРОВАННЫМ БИЦИКЛОГЕТЕРОЦИКЛОМ | 2007 |
|
RU2437884C2 |
| [(1Н-ИНДОЛ-5-ИЛ)-ГЕТЕРОАРИЛОКСИ]-1-(АЗАБИЦИКЛО[3.3.1]НОНАНЫ, КАК ХОЛИНЕРГИЧЕСКИЕ ЛИГАНДЫ N-ACHR, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ПСИХОТИЧЕСКИХ И НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2006 |
|
RU2471797C2 |
| ЛИГАНДЫ НИКОТИНОВЫХ АЦЕТИЛХОЛИНОВЫХ РЕЦЕПТОРОВ | 2007 |
|
RU2441007C2 |
| НОВЫЕ ХИНУКЛИДИНОВЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2323217C2 |
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, КОМБИНИРОВАННЫЙ ПРОДУКТ И СПОСОБ ИНГИБИРОВАНИЯ МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2003 |
|
RU2314306C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОПИРИДАЗИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2679609C1 |
| ПРОИЗВОДНЫЕ 1,1-ДИОКСОТИОМОРФОЛИНИЛИНДОЛИЛМЕТАНОНА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ГИСТАМИНА 3 (Н3) | 2006 |
|
RU2412182C2 |
Изобретение относится к новым соединениям формулы I

в которой А обозначает водород, В обозначает метил и В находится в транс-положении по отношению к кислороду; X обозначает СН2; Y обозначает группу формулы
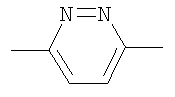 ,
, 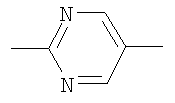 ,
, 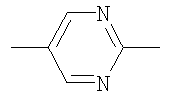 ,
,
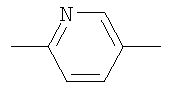 ,
, 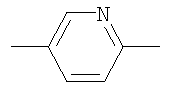 или
или 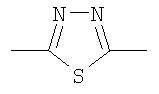 ;
;
в которой левая связь присоединена к атому кислорода, а правая связь присоединена к группе R; R обозначает 5-индолил; в форме свободного основания или соли присоединения с кислотой. Изобретение также относится к фармацевтической композиции, к применению соединений по любому из п.п.1-7, к способу предупреждения и лечения психических и нейродегенеративных нарушений у субъекта, а также к способу лечения или предупреждения заболевания или патологического состояния, в котором играет роль активация α7 nAChR или он участвует. Технический результат - получение новых биологически активных соединений, обладающих агонистической активностью в отношении α7 nAChR. 7 н. и 9 з.п. ф-лы.
1. Соединение формулы I

в которой А обозначает водород, В обозначает метил и В находится в трансположении по отношению к кислороду;
X обозначает СН2;
Y обозначает группу формулы
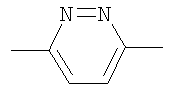 ,
, 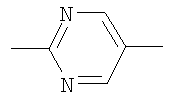 ,
, 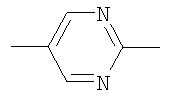 ,
,
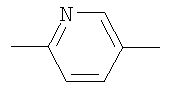 ,
, 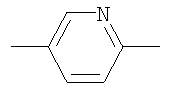 или
или 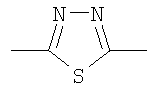 ;
;
в которой левая связь присоединена к атому кислорода, а правая связь присоединена к группе R;
R обозначает 5-индолил;
в форме свободного основания или соли присоединения с кислотой.
2. Соединение формулы I по п.1, где Y обозначает группу формулы
 ,
,  ,
, 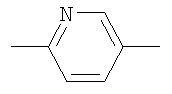 .
.
3. Соединение формулы I по п.1, где Y обозначает
 .
.
4. Соединение формулы I по п.1, выбранное из
(2SR,3RS)-3-[5-(1Н-индол-5-ил)пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(+)-3-[5-(1Н-индол-5-ил)пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(-)-3-[5-(1Н-индол-5-ил)пиридин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2SR,3RS)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2S,3R)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2R,3S)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2SR,3RS)-3-[5-(1Н-индол-5-ил)пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2S,3R)-3-[5-(1Н-индол-5-ил)пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана;
(2S,3R)-3-[5-(1Н-индол-5-ил)пиримидин-2-илокси]-2-метил-1-азабицикло[2.2.2]октана; и
(2SR,3RS)-3-[6-(1Н-индол-5-ил)пиридин-3-илокси]-2-метил-1-азабицикло[2.2.2]октана.
5. Соединение формулы I по п.1, где указанное соединение представляет собой (2SR,3RS)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан.
6. Соединение формулы I по п.1, где указанное соединение представляет собой (2S,3R)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан.
7. Соединение формулы I по п.1, где указанное соединение представляет собой (2R,3S)-3-[6-(1Н-индол-5-ил)пиридазин-3-илокси]-2-метил-1-азабицикло[2.2.2]октан.
8. Соединение по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой, предназначенное для применения в качестве лекарственного средства, обладающего агонистической активностью в отношении α7 nAChR.
9. Соединение по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой, предназначенное для применения с целью предупреждения и лечения психических и нейродегенеративных нарушений.
10. Фармацевтическая композиция, обладающая агонистической активностью в отношении α7 nAChR, включающая соединение по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой совместно с фармацевтическим носителем или разбавителем.
11. Применение соединения по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой в качестве лекарственного средства для предупреждения и лечения психических и нейродегенеративных нарушений.
12. Применение соединения по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой для приготовления лекарственного средства, предназначенного для предупреждения и лечения психических и нейродегенеративных нарушений.
13. Способ предупреждения и лечения психических и нейродегенеративных нарушений у субъекта, нуждающегося в таком лечении, который включает введение такому субъекту терапевтически эффективного количества соединения по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой.
14. Соединение по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой, предназначенное для использования при лечении или предупреждении заболевания или патологического состояния, в котором играет роль активация α7 nAChR или он участвует.
15. Применение соединения по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой в качестве лекарственного средства для лечения или предупреждения заболевания или патологического состояния, в котором играет роль активация α7 nAChR или он участвует.
16. Способ лечения или предупреждения заболевания или патологического состояния, в котором играет роль активация α7 nAChR или он участвует, у субъекта нуждающегося в таком лечении, который включает введение такому субъекту терапевтически эффективного количества соединения по любому из пп.1-7 в форме свободного основания или фармацевтически приемлемой соли присоединения с кислотой.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| БИЦИКЛИЧЕСКИЕ 1-АЗА-ЦИКЛОАЛКАНЫ, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ИНДИВИДУАЛЬНЫЕ ИЗОМЕРЫ, ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ | 1992 |
|
RU2040526C1 |
Авторы
Даты
2010-10-27—Публикация
2005-07-13—Подача