Настоящее изобретение относится к новым 1-азабициклоалкильным производным, к способам их получения, к их применению в качестве фармацевтических средств и к содержащим их фармацевтическим композициям.
Более конкретно, настоящее изобретение в первом аспекте относится к соединению формулы I:
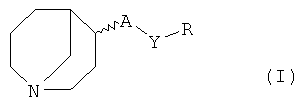
где А представляет собой О или N(R1);
Y представляет собой группу формулы:
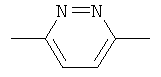 ,
, 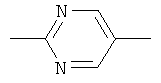 ,
, 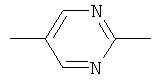 ,
,
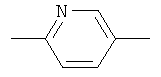 ,
, 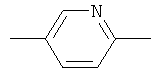 или
или 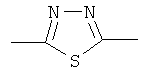 ,
,
где левая связь присоединена к группе А и правая связь присоединена к группе R;
R представляет собой замещенный или незамещенный С5-С10арил, замещенный или незамещенный гетеро-С5-С10арил, группу N(R1)(R4) или группу N(R2)(CHR3R4);
R1 представляет собой водород, С1-С4алкил или CF3;
R2 представляет собой водород, С1-С4алкил или CF3;
R3 представляет собой водород, С1-С4алкил или CF3;
R4 представляет собой замещенный или незамещенный С5-С10арил или
замещенный или незамещенный С5-С10гетероарил,
в форме свободного основания или в форме кислотной аддитивной соли.
Общие термины, используемые выше и далее, в контексте настоящего описания предпочтительно имеют следующие значения, если не указано иное.
Термин "незамещенный или замещенный", как здесь используется, обозначает, что соответствующий радикал может быть замещен одним или несколькими, предпочтительно вплоть до трех, особенно одним или двумя заместителями. Заместители предпочтительно выбраны из группы, состоящей из амино, С1-С4алкиламино, ди(С1-С4алкил)амино, С3-С5циклоалкиламино, ди(С3-С5)циклоалкиламино, N-С1-С4алкил-N-С3-С5циклоалкиламино, галогена, C1-С4алкила, С4-С6циклоалкила, гидрокси, С1-С4алкокси, С3-С5циклоалкилокси, С1-С4алкокси С1-С4алкокси, ди(С1-С4алкил)аминоС1-С4алкокси, карбамоила, N-C1-С4алкилкарбамоила, N,N-ди(С1-С4алкил)карбамоила, нитро, циано, карбокси, С1-С4алкоксикарбонила, С1-С4алканоила, С1-С4алканоилокси, бензоила, амидино, гуанидино, уреидо, меркапто, С1-С4алкилтио, пиридила, фенила, фенокси, С1-С4алкоксифенила, фенилтио, фенил-С1-С4алкилтио, С1-С4алкилсульфонила, фенилсульфонила, С1-С4алкилфенилсульфонила, С1-С4алкенила, С1-С4алканоила, С1-С4алкилендиоксисвязи у соседних С-атомов цикла и С1-С4алкила, который замещен галогеном, гидрокси, С1-С4алкокси, нитро, циано, карбокси, С1-С4алкоксикарбонилом, С1-С4алканоилом или С1-С4алканоилокси.
Термины "С5-С10арил", "С5-С10гетероарил" обозначают ароматические радикалы, которые в каждом случае являются незамещенными или замещены описанными выше заместителями, предпочтительно в каждом случае незамещенными или замещены одним или несколькими заместителями, выбранными из галогена, CN или алкила, который может быть незамещенным или замещен галогеном, например трифторметилом; или С1-С4алкокси, или конденсированными, например в бензо[1,3]диоксол или 2,3-дигидробензо[1,4]диоксин и/или в другое гетероциклическое кольцо. С5-С10гетероарил представляет собой ароматическую гетероциклическую систему, где один или несколько атомов углерода замещены гетероатомами. Предпочтительными являются 5-9-членные циклические системы, содержащие один, два или три гетероатома. Примеры указанных выше С5-С10арильных или С5-С10гетероарильных радикалов включают фенил, нафтил, изобензофуранил, тиенил, индолил.
Термин "алкил" представляет собой линейную или разветвленную алкильную группу, предпочтительно представляет собой линейный или разветвленный С1-7алкил, особенно предпочтительно представляет собой линейный или разветвленный С1-4алкил, например метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, особенно предпочтительно метил, этил, н-пропил и изопропил.
Каждая алкильная часть "алкокси", "алкоксиалкила", "алкоксикарбонила", "алкоксикарбонилалкила" и "галогеналкила" имеет те же значения, как описано выше для определения "алкил". Алкокси особенно представляет собой С1-С4алкокси, в частности метокси, этокси или н-пропокси.
"Гетератомы" представляют собой атомы, отличные от углерода и водорода, предпочтительно азот (N), кислород (О) или серу (S).
"Галоген" представляет собой фтор, хлор, бром или иод, предпочтительно представляет собой фтор, хлор или бром и особенно предпочтительно представляет собой хлор.
В отношении асимметричного атома (атомов) углерода, присутствующих в соединениях формулы I и их солях, соединения могут существовать в оптически активной форме или в форме смесей оптических изомеров, например в форме рацемических смесей. Все оптические изомеры и их смеси, включая рацемические смеси, составляют часть настоящего изобретения.
Благодаря тесной связи новых соединений в свободной форме и соединений в форме их солей, включая те соли, которые могут использоваться в качестве промежуточных соединений, например, для очистки или идентификации новых соединений, любая ссылка на свободные соединения выше и далее относится также к соответствующим солям, если это является подходящим и возможным.
При использовании множественной формы в отношении соединений, солей и им подобных, также подразумевается одно соединение, соль или им подобные.
Предпочтительные заместители, предпочтительные области числовых значений или предпочтительные области радикалов, присутствующих в формуле (I) и соответствующих промежуточных соединениях, указаны далее. Эти заместители, предпочтительные области числовых значений или предпочтительные области являются предпочтительными независимо друг от друга, вместе или в любой комбинации или субкомбинации:
Х предпочтительно представляет собой кислород.
Y предпочтительно представляет собой одну из следующих групп:
 ,
,  ,
, 
Y особенно предпочтительно представляет собой следующую группу:
 .
.
R предпочтительно представляет собой С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, где заместители выбраны из группы, состоящей из галогена; NO2; CN; С1-С4алкокси, который является незамещенным или замещен галогеном; С1-С4алкила, который является незамещенным или замещен галогеном, С1-С4алкилС(O)NH, С1-С4алкилсульфонила.
R предпочтительно представляет собой гетеро-С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, где заместители выбраны из группы, состоящей из галогена; С1-С2алкокси; CN или С1-С2алкила, который является незамещенным или замещен галогеном.
R предпочтительно представляет собой N(R1)(R5) или N(R2)(CHR3R4).
R особенно предпочтительно представляет собой фенил или замещенный фенил, где заместители выбраны из группы, состоящей из хлора, фтора, метила, этила, метокси, трифторметила, трифторметокси, циано, нитро, ацетамида, метилсульфонила.
R особенно предпочтительно представляет собой незамещенный или замещенный гетеро-С5-С10арил, где гетеро-С5-С10арил выбран из группы, состоящей из имидазолила, триазолила, тетразолила, фуранила, тиофенила, бензо[b]тиофенила, оксазолила, изоксазолила, тиазолила, изотиазолила, 1-изобензофуранила, бензо[1,3]диоксолила, 2,3-дигидробензо[1,4]диоксинила, бензо[1,2,5]оксадиазолила, бензо[1,2,5]тиадиазолила, хинолинила, изохинолинила, где заместители выбраны из группы, состоящей из хлора, фтора, метила, этила, метокси, трифторметила, трифторметокси, циано, нитро, ацетамида.
R1, R2 и R3 предпочтительно независимо представляют собой Н, метил или CF3.
R4 предпочтительно представляет собой С5-С10арил или гетеро-С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, где заместители выбраны из группы, состоящей из галогена, С1-С4алкокси, CN или С1-С2алкила, который является незамещенным или замещен галогеном.
В другом варианте осуществления предпочтительными являются соединения формулы I,
где Y представляет собой группу формулы:
 ,
,  ,
,  ,
,
 ,
,  или
или  ;
;
R представляет собой С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, выбранными из галогена, С1-С4алкокси, CN или C1-С2алкила, который является незамещенным или замещен галогеном; гетеро-С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, выбранными из галогена, С1-С4алкокси, CN или С1-С2алкила, который является незамещенным или замещен галогеном; N(R1)(R4) или N(R2)(CHR3R4); каждый из R1, R2 и R3 независимо представляет собой Н, С1-С4алкил или CF3; и
R4 представляет собой С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, выбранными из галогена, С1-С4алкокси, CN или C1-С2алкила, который является незамещенным или замещен галогеном; или гетеро-С5-С10арил, который является незамещенным или замещен одним или несколькими заместителями, выбранными из галогена, С1-С4алкокси, CN или С1-С2алкила, который является незамещенным или замещен галогеном.
В другом варианте осуществления предпочтительными являются соединения формулы I,
где Y представляет собой группу формулы:
 и
и
R представляет собой фенил, который является незамещенным или замещен одним или несколькими заместителями, выбранными из галогена, С1-С4алкокси, CN или С1-С2алкила, который является незамещенным или замещен галогеном.
В другом варианте осуществления предпочтительными являются соединения формулы I, где исходный реагент формулы (III) представляет собой (-) спирт.
Особенно предпочтительными соединениями по изобретению являются соединения, приведенные в примерах.
В другом варианте осуществления настоящее изобретение также относится к способу получения соединения формулы I, который включает стадию реакции соединения формулы II:

где Y и R являются такими, как определено выше для соединения формулы I, и Z представляет собой уходящую группу, например F, Cl, Br, I или OSO2CF3, с соединением формулы III:
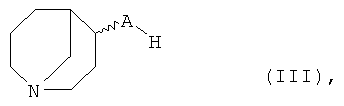
где А имеет значение, приведенное для соединения формулы I, и превращение полученного таким образом соединения формулы I в форму свободного основания или в форму кислотной аддитивной соли.
Реакция может осуществляться в соответствии со стандартными методиками, например, как показано в примерах.
Соединения формулы II являются известными или могут быть получены из соответствующих известных соединений, например, как описано в примерах, например, аналогично способу, описанному Coates WJ, McKillop A, Synthesis, 1992, сс.334-342. Соединения формулы III являются известными (Н.Stenbach, S.Kaiser, J. Amer. Chem. Soc., 1952, 74, с.2219; F.D.King и др., J. Med. Chem., 1993. 36, с.683). Кроме того, соединение формулы III, где А представляет собой О, также может быть превращено в соединение, где А представляет собой NR, способами, известными из уровня техники, например способом, где спирт сначала превращают в перхлорат алкилоксифосфония, как описано в статье Bull. Soc. Chim. Fr., 1971, с.4368.
Альтернативно соединения формулы I':
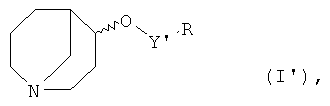
где R является таким, как описано выше для соединения формулы I, и Y' представляет собой группу формулы:
 ,
,  ,
,  ,
,  или
или  ,
,
могут быть получены способом, включающим стадию реакции соединения формулы IV:
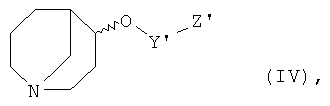
где Y' является таким, как определено выше для соединения формулы I', и Z' представляет собой уходящую группу,
с соединением формулы V:

где R является таким, как определено выше для соединения формулы I, необязательно в присутствии реакционной добавки, например палладиевого катализатора, и превращение полученного таким образом соединения формулы I' в форму свободного основания или в форму кислотной аддитивной соли.
Соединения формулы IV являются известными или могут быть получены из соответствующих известных соединений, например реакцией соединений формулы III с соединениями формулы II':

где Y' представляет собой одну из следующих групп:
 ,
,  ,
,  ,
, 
и Z является таким, как описано выше.
Соединения формулы V (например, незамещенные или замещенные фенилборсодержащие кислоты) являются известными или могут быть получены из соответствующих известных соединений.
К конкретным реакционным стадиям, описанным далее, применяются следующие положения.
а) Одна или несколько функциональных групп, например карбокси, гидрокси, амино или меркапто, могут нуждаться в защите в исходных реагентах защитными группами. Применяемые защитные группы могут уже присутствовать в предшественниках и должны защищать функциональные группы от нежелательных побочных реакций, таких как ацилирование, образование простого эфира, этерификация, окисление, сольволиз и аналогичные реакции. Характеристикой защитных групп является то, что они легко отщепляются сами, то есть без нежелательных побочных реакций, обычно сольволизом, восстановлением, фотолизом или также ферментативной активностью, например, в условиях, аналогичных физиологическим условиям, и что они не присутствуют в конечных продуктах. Специалисту в данной области техники известны или он может легко установить, какие защитные группы подходят для описанных выше и далее реакций. Защита таких функциональных групп защитными группами, сами защитные группы и реакции для их удаления описаны, например, в стандартных источниках, таких как книги J.F.W.McOmie, «Protective Groups in Organic Chemistry», Plenum Press, London и NY (1973); T.W.Greene, «Protective Groups in Organic Synthesis», Wiley, NY (1981); «The Peptides»; T.3, E.Gross и J.Meienhofer, Eds., Academic Press, London и NY (1981); «Methoden der organischen Chemie» (Methods of organic chemistry), Houben Weyl, 4-ое издание, Т.15/1, Georg Thieme Verlag, Stuttgart (1974); H.D.Jakubke и H.Jescheit, «Aminosauren, Peptide, Proteine» (Amino acids, peptides, proteins), Verlag Chemie, Weinheim, Deerfield Beach и Basel (1982); и Jochen Lehmann, «Chemie der Kohlenhydrate: Monosaccharide und Derivate» (Chemistry of carbohydrats: monosaccharides and derivatives), Georg Thieme Verlag., Stuttgart (1974).
б) Кислотные аддитивные соли могут быть получены из свободных оснований известным способом и наоборот. Альтернативно могут использоваться оптически чистые исходные реагенты. Подходящие кислотные аддитивные соли для применения в соответствии с настоящим изобретением включают, например, гидрохлорид.
в) Стереоизомерные смеси, например, смеси диастереоизомеров, могут быть разделены на их соответствующие изомеры известным способом с помощью подходящих способов разделения. Диастереомерные смеси, например, могут быть разделены на их индивидуальные диастереоизомеры с помощью фракционной кристаллизации, хроматографии, разделения растворителя и аналогичными способами. Это разделение может иметь место либо для исходного соединения, либо непосредственно для соединения формулы (I) или (Ia). Энантиомеры могут быть разделены с помощью образования диастереомерных солей, например образованием соли с энантиомерно-чистой хиральной кислотой, или с помощью хроматографии, например ВЭЖХ, используя хроматографические субстраты с хиральными лигандами. Альтернативно могут использоваться оптически чистые исходные реагенты.
г) Подходящими разбавителями для осуществления описанных выше реакций являются предпочтительно инертные органические растворители. Они включают, в частности, алифатические, алициклические или ароматические, необязательно галогенированные углеводороды, такие как, например, бензин, бензол, толуол, ксилол, хлорбензол, дихлорбензол, петролейный эфир, гексан, циклогексан, дихлорметан, хлороформ, тетрахлористый углерод; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран или диметиловый эфир этиленгликоля или диэтиловый эфир этиленгликоля; кетоны, такие как ацетон, бутанон или метилизобутилкетон; нитрилы, такие как ацетонитрил, пропионитрил или бутиронитрил; амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфора; сложные эфиры, такие как метилацетат или этилацетат, сульфоксиды, такие как диметилсульфоксид, спирты, такие как метанол, этанол, н- или изопропанол, монометиловый эфир этиленгликоля, моноэтиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля. Кроме того, могут использоваться смеси разбавителей. В зависимости от исходных реагентов, реакционных условий и добавок может использоваться вода или разбавители, содержащие воду. Возможно также применение одного из исходных материалов одновременно в качестве разбавителя.
д) Температуры реакций могут изменяться в широких пределах. Обычно способы осуществляют при температурах от 0°С до 150°С, предпочтительно от 10°С до 120°С. Температуры реакций депротонирования могут изменяться в относительно широких пределах. Обычно способы осуществляют при температурах от -150°С до +50°С, предпочтительно от -75°С до 0°С.
е) Реакции обычно осуществляют при атмосферном давлении. Однако также возможно осуществление способов в соответствии с изобретением при повышенном или пониженном давлении, обычно от 0,1 бар до 10 бар.
ж) Исходные реагенты обычно используют приблизительно в эквимолярных количествах. Однако также возможно применение относительно большого избытка одного из компонентов. Реакцию обычно осуществляют в подходящем разбавителе в присутствии реакционных добавок и реакционную смесь обычно перемешивают при необходимой температуре в течение нескольких часов.
з) Обработка реакционной смеси указанных выше способов и очистка полученных соединений может осуществляться в соответствии с известными методиками (см. примеры получения).
Соединения по изобретению и их фармацевтически приемлемые кислотные аддитивные соли, далее называемые как соединения по изобретению, проявляют ценные фармакологические свойства при тестировании in vitro и на животных и, следовательно, полезны в качестве фармацевтических средств.
Таким образом, было установлено, что соединения по изобретению являются холинергическими лигандами nAChR. Кроме того, предпочтительные соединения по изобретению проявляют селективную активность в отношении α7-nAChR. В частности, было установлено, что соединения настоящего изобретения являются агонистами, частичными агонистами, антагонистами или аллостерическими модуляторами рецептора.
Благодаря их фармакологическим профилям, предполагается, что соединения по изобретению могут быть полезны для лечения заболеваний или состояний, таких как заболевания, связанные с ЦНС, заболевания, связанные с PNS, заболевания, связанные с воспалением, симптомы боли и зависимости, вызванные употреблением химических веществ, заболевания или нарушения, связанные с ЦНС, включая заболевания общей тревоги, когнитивные заболевания, дефициты и дисфункции обучения и памяти, болезнь Альцгеймера, ADHD, болезнь Паркинсона, болезнь Хантингтона, ALS, прионовые нейродегенеративные заболевания, такие как болезнь Якоба-Крейтцфельдта и болезнь куру, синдром Жиля де ла Туретта, психоз, депрессия и депрессивные заболевания, мания, маниакальная депрессия, шизофрения, когнитивные дефициты при шизофрении, обсессивно-компульсивные заболевания, расстройства панического типа, нарушения приема пищи, нарколепсия, ноцицепция, СПИД-слабоумие, старческое слабоумие, возрастные умеренные когнитивные дисфункции, аутизм, дислексия, поздняя дискинезия, эпилепсия и конвульсивные заболевания, посттравматические стрессовые заболевания, временная аноксия, псевдослабоумие, предменстуальный синдром, синдром последней лютеральной фазы, синдром хронической усталости и десинхроноз. Кроме того, соединения по изобретению могут использоваться для лечения эндокринных заболеваний, таких как тиротоксикоз, феохромоцитома, гипертензия и аритмии, а также стенокардия, гиперкензия, проспермия и эректильная дисфункция. Кроме того, соединения по изобретению могут использоваться для лечения воспалительных заболеваний (Wang и др. Nature 2003, 421, с.384), нарушений или состояний, включая воспалительные заболевания кожи, болезнь Крона, синдром воспаленного кишечника, язвенный колит и диарею. Соединения по изобретению могут также использоваться для лечения симптомов зависимости, вызванных прекращением применения наркотических веществ, таких как табак, никотин, опиоиды, бензодиазепины и спирт. Наконец, соединения по изобретению могут использоваться для лечения боли, например, вызванной мигренью, послеоперационной боли, фантомной боли или боли, вызванной раковым заболеванием. Боль может включать воспалительную или невропатическую боль, центральную боль, хроническую головную боль, боль, вызванную диабетической невропатией, посттерапевтической невралгией или травмой периферического нерва.
Кроме того, дегенеративные заболевания глаз, которые могут быть излечены, включают заболевания глаз, которые могут прямо или непосредственно включать разрушение ретинальных клеток, включая ишемические ретинопатии вообще, раннюю ишемическую оптическую невропатию, все формы глазных невритов, возрастную дистрофию желтого пятна (AMD), в ее сухих формах (сухая AMD) и влажных формах (влажная AMD), диабетическую ретинопатию, цистоидный отек желтого пятна (СМЕ), отслойку сетчатки, пигментную дегенерацию сетчатки, заболевание Штаргардта, вителлиформную дистрофию сетчатки Беста, врожденный амавроз Лебера и другие наследственные дистрофии сетчатки, патологическую миопию, преждевременное развитие ретинопатии и наследственную глазную невропатию Лебера.
В другом аспекте соединения по изобретению используются в качестве диагностических агентов и/или лигандов PET, например, для идентификации и локализации никотиновых рецепторов в различных тканях. Подходящим образом меченные изотопами агенты по изобретению обладают ценными свойствами в качестве гистопатологических агентов-меток, визуализирующих агентов и/или биомаркеров, здесь и далее "маркеров", для селективного маркирования nAChR. Более конкретно, агенты по изобретению являются полезными в качестве маркеров для маркирования альфа7 nAChR рецепторов in vitro или in vivo. В частности, соединения по изобретению, которые подходящим образом изотопно помечены, являются полезными в качестве маркеров PET. Такие маркеры PET маркируются одним или несколькими атомами, выбранными из группы, состоящей из 11С, 13N, 15О, 18F.
Агенты по изобретению, следовательно, являются полезными, например, для определения уровней связанности рецептора с лекарственным средством, действующим на nAChR, или для диагностики заболеваний, происходящих от дисбаланса или дисфункции nAChR, и для мониторинга эффективности фармакотерапий таких заболеваний.
В соответствии с вышеизложенным настоящее изобретение относится к агенту по изобретению для применения в качестве маркера для нейровизуализации.
В другом аспекте настоящее изобретение относится к композиции для маркирования головного мозга и структур периферической нервной системы, включая nAChR in vivo и in vitro, включающей агент по изобретению.
В следующем аспекте настоящее изобретение относится к способу маркирования головного мозга и структур периферической нервной системы, включая nAChR in vitro или in vivo, который включает контактирование ткани головного мозга с агентом по изобретению.
Данный способ по изобретению может включать другую стадию, направленную на определение того, будет ли агент по изобретению маркировать целевую структуру. Указанная другая стадия может осуществляться посредством наблюдения за целевой структурой с помощью позитронной эмиссионной томографии (PET) или компьютерной томографии эмиссии одного фотона (SPECT), или любого устройства, позволяющего определять радиоактивные излучения.
В частности, агенты по изобретению являются агонистами α7 никотинового ацетилхолинового рецептора (α7 nAChR).
В функциональных анализах агенты по изобретению проявляют высокое сродство с α7 nAChR, как показано в следующих тестах.
а) Функциональный анализ сродства с α7 nAChR осуществляли с клеточными линиями гипофиза крысы, стабильно экспрессирующими α7 nAChR. Вкратце, клетки GH3, рекомбинантно экспрессирующие nAChR α7, высаживали за 72 ч до эксперимента в черные 96-луночные планшеты и инкубировали при 37°С во влажной атмосфере (5% CO2/95% воздуха). В день эксперимента среду удаляли декантацией планшетов и замещали 100 мкл среды для роста, содержащей флуоресцентный чувствительный к кальцию краситель, в присутствии 2,5 мМ пробеницида (Sigma). Клетки инкубировали при 37°С во влажной атмосфере (5% CO2/95% воздуха) в течение 1 ч. Планшеты декантировали для удаления избытка Fluo-4, дважды промывали забуференным Hepes солевым раствором (в мМ: NaCl 130, KCl 5,4, CaCl2 2, MgSO4 0,8, NaH2PO4 0,9, глюкоза 25, Hepes 20, pH 7,4; HBS) и заново наполняли 100 мкл HBS, содержащего, когда возможно, антагонисты. Инкубирование в присутствии антагониста длилась от 3 до 5 минут. Планшеты затем помещали в считывающее устройство для планшетов для получения изображений и записывали сигнал флуоресценции. В этом анализе соединения по изобретению показали значения pEC50 от около 5 до около 9. Предпочтительными в этом тесте являются частичные и полные агонисты.
б) Для определения антагонистической активности соединений по изобретению осуществляли сходный функциональный анализ на нейрональном nAChR α4β2 человека, используя эпителиальную клеточную линию человека, стабильно экспрессирующую подтип α4β2 человека (Michelmore и др. Naunyn-Schmiedeberg's Arch. Pharmacol., 2002, 366, с.235) В этом анализе предпочтительные соединения по изобретению проявляют селективность в отношении подтипов α7 nAChR.
в) Для определения антагонистической активности соединений по изобретению в отношении "ганглиозного подтипа" (α3β4), мышечного типа никотинового рецептора (α1β1γδ) и рецептора 5-НТ3, осуществляли сходные функциональные тесты, как описано в подпункте а), с эпителиальными клеточными линиями человека, стабильно экспрессирующими ганглиозный подтип человека, с клеточными линиями, эндогенно экспрессирующими мышечный тип никотиновых рецепторов человека или с клеточными линиями, эндогенно экспрессирующими рецептор 5-НТ3 мыши (Michelmore и др. Naunyn-Schmiedeberg's Arch. Pharmacol., 2002, 366, с.235. Соединения, которые показывают небольшую или никакую активность в отношении α3β4 nAChR, мышечного подтипа никотинового рецептора, а также в отношении 5-НТ3 рецептора, являются особенно предпочтительными.
На модели мыши, показывающей дефицит сенсорной проводимости (DBA/2-мыши), описанной S.Leonard и др. в статье Schizophrenia Bulletin 22, 1996, сс.431-445, соединения по изобретению значительно увеличивают сенсорную проводимость в концентрациях от около 10 до около 40 мкМ.
Может быть показано, что соединения по изобретению повышают внимание в тесте на внимание для грызунов (Robbins, J. Neuropsychiatry Clin. Neurosci., 2001, 13, сс.326-35), а именно в серийном тесте на время по выбору из 5 возможностей (5-CSRTT). В этом тесте крыса должна наблюдать стену с 5 дырами. Когда световая вспышка появляется в одной из дыр, крыса должна реагировать засовыванием носа в правильную дырку в течение 5 секунд для того, чтобы получить еду в качестве вознаграждения, помещенную в кормушку на противоположной стене.
Соединения по изобретению также могут показывать эффекты улучшения обучения/запоминания в тесте на социальное сознание у мышей и крыс (Ennaceur и Delacour, Behav. Brain Res., 1988, 31, сс.47-59).
Соединения по изобретению, следовательно, являются полезными для профилактики и лечения (включая уменьшение и предотвращение) различных заболеваний, особенно тех, которые упомянуты выше. Полезность в качестве агонистов α7 nAChR в нейродегенерации зафиксирована в уровне техники, например в статье Wang и др., J. Biol. Chem., 2000, 275, сс.5626-5632.
Для лечения указанных выше и других заболеваний подходящие дозировки соединения (активного ингредиента) по изобретению будут, конечно, сильно зависеть, например, от пациента, способа введения и природы и степени тяжести излечиваемого состояния, а также от относительной активности конкретного применяемого агента по изобретению. Например, необходимое количество активного агента может быть определено на основе известных методов in vitro и in vivo, определяя, насколько долго концентрация в плазме крови конкретного активного агента остается на приемлемом уровне для терапевтического действия. Обычно удовлетворительные результаты на животных наблюдаются при суточных дозировках от около 0,01 до около 30,0 мг/кг перорально. Для животных рекомендуемая суточная дозировка находится в области от около 0,7 до около 1400 мг/день перорально, например от около 50 до 200 мг (человек весом 70 кг), обычно вводимая одной дозой или несколькими дозами до 4 раз в сутки или в форме длительного высвобождения. Пероральные дозированные формы соответственно обычно включают от около 1,75 или 2,0 до около 700 или 1400 мг соединения по изобретению в смеси с подходящим фармацевтически приемлемым разбавителем или носителем.
Фармацевтические композиции содержат, например, от около 0,1% до около 99,9%, предпочтительно от около 20% до около 60% активного ингредиента(ов).
Примеры композиций, включающих соединение по изобретению, включают, например, твердую дисперсию, водный раствор, например, содержащий солюбилизирующий агент, микроэмульсию и суспензию, например, соли соединения формулы I или свободного соединения формулы I в области от около 0,1 до 1%, например 0,5%. Композиция может содержать буфер для поддержания значения рН в области, например, от 3,5 до 9,5, например значения рН 4,5, с помощью подходящего буфера.
Соединения по изобретению также коммерчески используются в качестве химических средств для исследований.
Для применения в соответствии с изобретением соединение формулы I и/или его фармацевтически приемлемая соль может вводиться в виде отдельного активного агента или в комбинации с одним или несколькими другими активными агентами формулы I и/или их фармацевтически приемлемыми солями, или, особенно, с другими активными агентами, обычно используемыми особенно для лечения указанных здесь заболеваний или других заболеваний, обычным способом, например, перорально, например, в форме таблеток, капсул или в виде назального спрея, или парентерально, например, в форме инъекционных растворов или суспензий. Другие активные агенты, используемые в таких комбинациях, предпочтительно выбирают из группы, состоящей из бензодиазепинов, селективных ингибиторов захвата серотонина (SSRI), селективных ингибиторов захвата серотонина и норепинефрина (SNRI), обычных нейролептиков, атипичных нейролептиков, биспирона, карбамазепина, окскарбазепина, габапентина и прегабалина.
SSRI, подходящие для настоящего изобретения, особенно выбраны из флуоксетина, фувоксамина, сертралина, пароксетина, циталопрама и эскиталопрама. SNRI, подходящие для настоящего изобретения, особенно выбраны из венлафаксина и дулоксетина. Термин "бензодиазепины", как здесь используется, включает, но не ограничивается ими, клоназепам, диазепам и лоразепам. Термин "обычные нейролептики", как здесь используется, включает, но не ограничивается ими, галоперидол, флуфеназин, тиотиксен и флупентиксол. Термин "атипичные нейролептики", как здесь используется, относится к клозарилу, рисперидону, оланзапину, кветиапину, зипразидону и арипипразолу.
Буспирон может быть введен в свободной форме или в виде соли, например в виде гидрохлорида, например, в выпускаемой на рынке форме, например, под товарным знаком Buspar™ или Bespar™. Он может быть получен и введен, например, как описано в патенте US 3717634. Флуоксетин может быть введен, например, в выпускаемой форме его гидрохлорида, например, под товарным знаком Prozac™. Он может быть получен и введен, например, как описано в патенте СА 2002182. Пароксетин ((3S,4R)-3-[(1,3-бензодиоксол-5-илокси)метил]-4-(4-фторфенил)пиперидин) может быть введен, например, в выпускаемой форме, например, под товарным знаком Paxil™. Он может быть получен и введен, например, как описано в патенте US 3912743. Серталин может быть введен, например, в выпускаемой форме, например под товарным знаком Zoloft™. Он может быть получен и введен, например, как описано в патенте US 4536518. Клоназепам может быть введен, например, в выпускаемой форме, например, под товарным знаком Antelepsin™. Диазепам может быть введен, например, в выпускаемой форме, например под товарным знаком Diazepam Desitin™. Лоразепам может быть введен, например, в выпускаемой форме, например, под товарным знаком Tavor™. Циталопрам может быть введен в свободной форме или в виде соли, например в виде его гидробромида, например, в выпускаемой форме, например, под товарным знаком Cipramil™. Эсциталопрам может быть введен, например, в выпускаемой форме, например, под товарным знаком Cipralex™. Он может быть получен и введен, например, как описано в патенте AU 623144. Венлафаксин может быть введен, например, в выпускаемой форме, например, под товарным знаком Trevilor™. Дулоксетин может быть введен, например, в выпускаемой форме, например, под товарным знаком Cymbalta™. Он может быть получен и введен, например, как описано в патенте СА 1302421. Карбамазепин может быть введен, например, в выпускаемой форме, например, под товарным знаком Tegretal™ или Tegretol™. Окскарбазепин может быть введен, например, в выпускаемой форме, например, под товарным знаком Trileptal™. Окскарбазепин является известным из уровня техники [см., например, статью Schuetz H. и др. Xenobiotica (GB), 1986, 16(8), сс.769-778]. Габапентин может быть введен, например, в выпускаемой форме, например, под товарным знаком Neurontin™. Галоперидол может быть введен, например, в выпускаемой форме, например, под товарным знаком Haloperidol STADA™. Флуфеназин может быть введен, например, в выпускаемой форме его дигидрохлорида, например, под товарным знаком Prolixin™. Тиотиксен может быть введен, например, в выпускаемой форме, например, под товарным знаком Navane™. Он может быть получен, например, как описано в патенте US 3310553. Флупентиксол может быть введен, например, в форме его дигидрохлорида, например, в выпускаемой форме, например, под товарным знаком Emergil™, или в форме его деканоата, например, в выпускаемой форме, например, под товарным знаком Depixol™. Он может быть получен, например, как описано в патенте ВР 925538. Клозарил может быть введен, например, в выпускаемой форме, например, под товарным знаком Leponex™. Он может быть получен, например, как описано в патенте US 3539573. Рисперидон может быть введен, например, в выпускаемой форме, например, под товарным знаком Risperdal™. Оланзапин может быть введен, например, в выпускаемой форме, например, под товарным знаком Zyprexa™. Кветиапин может быть введен, например, в выпускаемой форме, например, под товарным знаком Seroquel™. Зипразидон может быть введен, например, в выпускаемой форме, например, под товарным знаком Geodon™. Он может быть получен, например, как описано в патенте GB 281309. Арипипразол может быть введен, например, в выпускаемой форме, например, под товарным знаком Abilify™. Он может быть получен, например, как описано в патенте US 5006528.
Структура активных ингредиентов, идентифицированных кодовыми номерами, общими наименованиями или товарными знаками, может быть взята из действующего издания стандартного сборника "The Merck Index" или из баз данных, например, Patents International (например, IMS World Publications). Соответствующее содержание их приведено здесь в качестве ссылки. Любой специалист в данной области техники может определить активные ингредиенты и, на основе этих ссылок, способен получить и протестировать фармацевтические показания и свойства на стандартных моделях для тестирования как in vitro, так и in vivo.
В случае комбинации фармацевтические композиции для раздельного введения партнеров комбинации и/или композиции для введения в фиксированной комбинации, то есть в одной галеновой композиции, включающей по крайней мере два ингредиента комбинации, в соответствии с изобретением, могут быть получены известным способом и пригодны для энтерального, такого как пероральное или ректальное, и парентерального введения млекопитающим, включая человека, и включают терапевтически эффективное количество по крайней мере одного фармакологически активного ингредиента комбинации отдельно или в комбинации с одним или несколькими фармацевтически приемлемыми носителями, особенно подходящими для энтерального или парентерального применения. Когда используемые ингредиенты комбинации применяются в выпускаемой форме в виде отдельных лекарственных средств, их дозировки и способ введения будут соответствовать информации, приведенной в инструкции соответствующего выпускаемого лекарственного средства для достижения описанного здесь положительно эффекта, если здесь не указано иное.
Фармацевтическими препаратами для комбинированной терапии для энтерального или парентерального введения являются, например, препараты в единичных дозированных формах, такие как покрытые сахаром таблетки, таблетки, капсулы или суппозитории, или ампулы. Если не указано иное, их получают известным способом, например обычными способами смешения, гранулирования, покрытия сахаром, растворения или лиофилизации. Ясно, что единичное содержание ингредиента комбинации, включенное в индивидуальную дозировку каждой дозированной формы, не должно составлять эффективное количество, поскольку необходимое эффективное количество может также достигаться, вместо единичной дозированной формы, введением двух или нескольких дозированных форм.
В частности, терапевтически эффективное количество каждого из ингредиентов комбинации может вводиться одновременно или последовательно и в любом порядке, и компоненты могут вводиться раздельно (например, последовательно через фиксированные или различные периоды времени), или в виде фиксированной комбинации. Например, способ лечения (включая облегчение) заболевания в соответствии с изобретением может включать (i) введение ингредиента комбинации (а) (соединение настоящего изобретения) в свободной форме или в форме фармацевтически приемлемой соли и (ii) введение ингредиента комбинации (б) (например, другое соединение настоящего изобретения или активный ингредиент другой формулы) в свободной форме или в форме фармацевтически приемлемой соли, одновременно или последовательно в любом порядке, в общих терапевтически эффективных количествах, предпочтительно в синергетически эффективных количествах, например, в суточных дозировках, соответствующих описанным здесь количествам. Отдельный ингредиент комбинации может быть введен отдельно в различное время в ходе терапии или конкурентно в раздельных формах или в одной комбинированной форме. Кроме того, термин "введение" также включает применение пролекарства ингредиента комбинации, которое превращается in vivo в ингредиент комбинации. Настоящее изобретение, следовательно, включает все такие режимы одновременного и/или альтернативного лечения, и термин "введение" должен интерпретироваться соответственно.
Эффективная дозировка применяемых ингредиентов комбинации может изменяться, например, в зависимости от конкретного используемого соединения или фармацевтической композиции, способа введения, излечиваемого заболевания и/или степени тяжести излечиваемого заболевания. Таким образом, режим дозировки выбирают в соответствии с различными факторами, включая способ введения, метаболизм и функция почек и печени пациента. Врач, клиницист или ветеринар может легко определить и назначить эффективное количество отдельных активных ингредиентов, необходимых для профилактики, облегчения, предотвращения или остановки заболевания. Оптимальная точность в достижении концентрации активных ингредиентов в области, которая является эффективной без токсичности, требует определения режима на основании кинетики доступности активных ингредиентов к сайтам мишени.
В соответствии с вышеизложенным настоящее изобретение также относится к следующим объектам:
(1) соединение формулы I и/или его соль для применения для диагностики или терапевтического лечения млекопитающего, особенно человека; особенно для применения в качестве агониста альфа-7 рецептора, например для применения для лечения (включая облегчение) любого одного или нескольких заболеваний, особенно любого одного или нескольких конкретных заболеваний, описанных выше и далее;
(2) фармацевтическая композиция, включающая соединение формулы I и/или его фармацевтически приемлемую соль в качестве активного ингредиента вместе с фармацевтически приемлемым разбавителем или носителем;
(2') фармацевтическая композиция для лечения или профилактики заболевания, в котором играет роль или участвует активация альфа-7 рецептора и/или в которое включена активность альфа-7 рецептора, особенно любого одного или нескольких заболеваний, описанных выше и далее, включающая соединение формулы I и/или его фармацевтически приемлемую соль и фармацевтически приемлемый разбавитель или носитель;
(3) способ лечения заболевания, особенно любого одного или нескольких конкретных заболеваний, описанных выше, у пациента, нуждающегося в таком лечении, включающий введение фармацевтически эффективного количества соединения формулы I или его фармацевтически приемлемой соли;
(3') способ лечения или профилактики заболевания, в котором играет роль или участвует активация альфа-7 рецептора и/или в которое включена активность альфа-7 рецептора, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения формулы I и/или его фармацевтически приемлемой соли;
(4) применение соединения формулы I и/или его фармацевтически приемлемой соли для изготовления лекарственного средства для лечения или профилактики заболевания или состояния, в котором играет роль или участвует активация альфа-7 рецептора и/или в которое включена активность альфа-7 рецептора, особенно одного или нескольких заболеваний, описанных выше;
(5) способ как описано выше, включающий совместное введение, например, одновременно или последовательно, терапевтически эффективного количества агониста альфа-7 рецептора формулы I и/или его фармацевтически приемлемой соли и второго фармацевтически активного соединения и/или его фармацевтически приемлемой соли, где указанное второе фармацевтически активное соединение и/или его соль используются для лечения любого одного или нескольких заболеваний, описанных выше или далее;
(6) комбинация, включающая терапевтически эффективное количество агониста альфа-7 рецептора формулы I и/или его фармацевтически приемлемой соли и второе фармацевтически активное соединение и/или его фармацевтически приемлемую соль, где указанное второе фармацевтически активное соединение применяется для лечения любого одного или нескольких конкретных заболеваний, описанных выше;
(7) продукт, полученный в соответствии с описанными выше способами, характеризующийся тем, что (-)-1-азабицикло[3.3.1]нонан-4-ол используют в качестве исходного материала.
Следующие примеры служат для иллюстрации изобретения без ограничения его объема.
Используются следующие сокращения:
Температуры измерены в градусах Цельсия. Если не указано иное, реакции осуществляют при комнатной температуре. Структура конечных продуктов, промежуточных соединений и исходных материалов подтверждена стандартными аналитическими способами, например микроанализом и спектроскопическими характеристиками (например, MS, ИК, ЯМР).
Пример 1 (способ А). Получение (рац.)-4-[6-(2-фтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонана.
Раствор (рац.)-1-азабицикло[3.3.1]нонан-4-ола (1,3 ммоль) в ДМФА (5 мл) обрабатывали гидридом натрия (60% в минеральном масле; 1,3 ммоль). Через 1 час при комнатной температуре добавляли раствор 3-хлор-6-(2-фтор-4-метилфенил)пиридазина (1 ммоль) в ДМФА (30 мл) и реакционную смесь нагревали при 50°С в течение 16 часов. После охлаждения до комнатной температуры раствор ДМФА гасили 10% раствором NaCl, экстрагировали этилацетатом (2×15 мл), затем раствором хлорида натрия (20 мл). Этилацетат сушили безводным сульфатом магния, отфильтровывали и упаривали досуха, оставшееся масло очищали колоночной хроматографией на силикагеле (элюент: этилацетат-метанол-триэтиламин (50:10:2) с получением (рац.)-4-[6-(2-фтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонана в виде бесцветного твердого вещества. MS (ES+): m/e=328 (МН+).
Пример 2 (способ Б). (рац.)-4-[6-(2,5-Дифтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан.
Триметилсилиламин калия (5,25 ммоль) добавляли к раствору (рац.)-1-азабицикло[3.3.1]нонан-4-ола (5,0 ммоль) в ТГФ (20 мл) при комнатной температуре и раствор перемешивали в течение 30 мин. Полученный алкоголят калия медленно добавляли к предварительно охлажденному раствору 3,6-дихлорпиридазина (7,5 ммоль) в ТГФ (50 мл) и полученную смесь перемешивали в течение дополнительных 20 минут. Раствор, нагретый до 0°С, гасили раствором хлорида натрия и экстрагировали диэтиловым эфиром. Органический слой сушили сульфатом магния и упаривали. Коричневое масло очищали колоночной хроматографией на силикагеле (CH2Cl2:MeOH:NH3, 9:1:0,1) с получением (рац.)-4-(6-хлорпиридазин-3-илокси)-1-азабицикло[3.3.1]нонана (320 мг).
(Рац.)-4-(6-Хлорпиридазин-3-илокси)-1-азабицикло[3.3.1]нонан (1,4 ммоль), 2,5-дифтор-4-метилфенилборную кислоту (1,8 ммоль) растворяли в толуоле (7,3 мл), этаноле (1 мл) и растворе Na2CO3 (7,3 мл, 2М). Раствор дегазировали аргоном в ультразвуковой бане, после чего добавляли ацетат палладия (II) (0,003 ммоль) и трифенилфосфин (0,14 ммоль). Полученную смесь нагревали при 100°С в течение 1,5 часов, после чего нагрев останавливали, суспензию отфильтровывали через Hyflo и фильтрат экстрагировали этилацетатом. Органический слой сушили сульфатом магния и упаривали. Масло очищали колоночной хроматографией насиликагеле (CH2Cl2:МеОН:EtOH:NH3, 90:5:5:1) с получением (рац.)-4-[6-(2,5-дифтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонана. MS (ES+): m/e=346 (МН+).
Пример 3
Следующие соединения получали либо способом А, либо способом Б, используя подходящие исходные материалы:
3а) (4S,5S)-4-[6-(2-Фтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=328 (MH+)
3б) (4R,5R)-4-[6-(2-Фтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=328 (MH+)
3в) (4SR,5SR)-4-[6-(2,5-Дифтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=346 (MH+)
3г) N-(3-{6-[(4S,5S)-(1-Азабицикло[3.3.1]нон-4-ил)окси]пиридазин-3-ил}фенил)ацетамид, MS (ES+): m/e=353 (MH+)
3д) N-(3-{6-[(4R,5R)-(1-Азабицикло[3.3.1]нон-4-ил)окси]пиридазин-3-ил}фенил)ацетамид, MS (ES+): m/e=353 (MH+)
3е) N-(3-{6-[(4SR,5SR)-(1-Азабицикло[3.3.1]нон-4-ил)окси]пиридазин-3-ил}фенил)ацетамид, MS (ES+): m/e=353 (MH+): хиральная хроматография [колонка: Chiralcel OD IMMOB (FA-2359/37) 12 мкм; элюент: гексан/CHCl3/МеОН 60:30:10 1 0,1% ТФУК; поток: 1,5 мл/мин; детектор: УФ 254 нм], пик 1: 15,470 мин, пик 2: 20,826 мин.
3ж) (4SR,5SR)-4-[5-(1H-Индол-5-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=334,1 (MH+)
3з) (4S,5S)-4-[5-(1H-Индол-5-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=334 (MH+), m.p. 234-238°C
3и) (4R,5R)-4-[5-(1Н-Индол-5-ил)пиридин-2-илокси]-1-азабицикло [3.3.1] нонан
3к) (4SR,5SR)-4-[5-(1H-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=335 (MH+), tпл 211°С (разруш.)
3л) (4S,5S)-4-[5-(1H-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=335 (MH+)
3м) (4R,5R)-4-[5-(1Н-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонан
3н) (4SR,5SR)-4-[6-(1H-Индол-5-ил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=335 (MH+)
3о) (4SR,5SR)-4-[6-(3-Нитрофенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=341 (MH+)
3к) (4SR,5SR)-4-(6-п-Толилпиридазин-3-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=310 (MH+)
3л) (4SR,5SR)-4-(6-м-Толилпиридазин-3-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=310 (MH+)
3м) (4SR,5SR)-4-(6-Бензо[1,3]диоксол-5-илпиридазин-3-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=340 (MH+)
3н) (4SR,5SR)-4-[6-(3,4-Диметилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=324,5 (MH+)
3о) (4SR,5SR)-4-(6-п-Толилпиридин-3-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=309 (MH+)
3п) (4SR,5SR)-4-[6-(3-Фторфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=314 (MH+)
3р) (4SR,5SR)-4-[6-(3,5-Дифторфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=332 (MH+)
3с) (4SR,5SR)-4-(5-Фенил[1,3,4]тиадиазол-2-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=302 (MH+)
3т) (4S,5S)-5-[6-(1-Азабицикло[3.3.1]нон-4-илокси)пиридазин-3-ил]хинолин, MS (ES+): m/e=347 (МН+)
3у) (4SR,5SR)-4-[6-(3,5-Диметилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=324 (MH+)
3ф) (4SR,5SR)-4-(6-Фенилпиридазин-3-илокси)-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=296 (МН+)
3х) (4SR,5SR)-4-[6-(3,4-Дифторфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=332 (MH+)
3ц) (4SR,5SR)-4-[6-(3-Трифторметоксифенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=380 (MH+)
3ч) (4SR,5SR)-3-[6-(1-Азабицикло[3.3.1]нон-4-илокси)пиридазин-3-ил]бензонитрил, MS (ES+): m/e=321 (MH+)
3ш) (4SR,5SR)-4-[6-(4-Трифторметоксифенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=380 (MH+)
3щ) (4SR,5SR)-4-[6-(3-Фтор-4-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=328 (MH+)
3э) (4SR,5SR)-4-[6-(2,4-Дифторфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=332 (МН+)
3ю) (4SR,5SR)-4-[6-(2-Метилбензотиазол-5-ил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=367,4 (MH+)
3я) (4SR,5SR)-4-[6-(1-Азабицикло[3.3.1]нон-4-илокси)пиридазин-3-ил]бензонитрил, MS (ES+): m/e=321 (MH+)
3аа) (4SR,5SR)-4-[6-(4-Фтор-3-метилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=328 (МН+)
3аб) (4SR,5SR)-4-[6-(4-Этилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=324 (MH+)
3ав) (4SR,5SR)-4-[6-(3-Трифторметилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=364 (MH+)
3аг) (4SR,5SR)-4-[6-(4-Трифторметилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=364 (MH+)
3ад) (4SR,5SR)-4-[6-(3,5-Бистрифторметилфенил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=432 (МН+)
3ае) (4SR,5SR)-4-[6-(5-Метилтиофен-2-ил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=316,4 (MH+)
3аж) (4SR,5SR)-4-[5-(1Н-Индол-5-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=334,4 (MH+)
3аз) (4SR,5SR)-4-[6-(2,3-Диметил-1Н-индол-5-ил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан, MS (ES+): m/e=363,4 (МН+)
3аи) (4SR,5SR)-4-(5-Бензо[1,3]диоксол-5-илпиримидин-2-илокси)-1-азабицикло[3.3.1]нонан
3ак) (4SR,5SR)-4-(5-Бензо[1,3]диоксол-5-илпиридин-2-илокси)-1-азабицикло[3.3.1]нонан
3ал) (4SR,5SR)-4-(6-Бензо[1,3]диоксол-5-илпиридин-3-илокси)-1-азабицикло[3.3.1]нонан
3ам) (4SR,5SR)-4-[5-(2-Фтор-4-метилфенил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонан
3ан) (4SR,5SR)-4-[5-(2-Фтор-4-метилфенил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонан
3ao) (4SR,5SR)-4-[6-(2-Фтор-4-метилфенил)пиридин-3-илокси]-1-азабицикло[3.3.1]нонан
3ап) (4SR,5SR)-4-(5-п-Толилпиримидин-2-илокси)-1-азабицикло[3.3.1]нонан
3ар) (4SR,5SR)-4-(5-п-Толилпиридин-2-илокси)-1-азабицикло[3.3.1]нонан
3ас) (4SR,5SR)-4-[5-(5-Метилтиофен-2-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонан
3ат) (4SR,5SR)-4-[5-(5-Метилтиофен-2-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонан
3ау) (4SR,5SR)-4-[6-(5-Метилтиофен-2-ил)пиридин-3-илокси]-1-азабицикло[3.3.1]нонан
3аф) (4SR,5SR)-(1-Азабицикло[3.3.1]нон-4-ил)-(6-п-толилпиридин-3-ил)амин, МS
(ES+): m/е=308 (МН+).
Пример 4. Мягкие капсулы.
5000 мягких желатиновых капсул, каждая включающая в качестве активного ингредиента 0,05 г одного из соединений формулы I, указанного в предшествующих примерах, получали следующим образом.
Композиция:
Способ получения: измельченный активный ингредиент суспендировали в Lauroglykol® (пропиленгликольлаурат, Gattefossé S.A., Saint Priest, France) и с помощью влажного пульверизатора получали частицы размером от около 1 до 3 мкм. Порции по 0,419 г смеси затем вводили в мягкие желатиновые капсулы с помощью устройства для наполнения капсул.
| название | год | авторы | номер документа |
|---|---|---|---|
| 3-(ГЕТЕРОАРИЛОКСИ)-2-АЛКИЛ-1-АЗАБИЦИКЛОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ, КАК ЛИГАНДЫ АЛЬФА-7-nAChR (НИКОТИНОВЫХ АЦЕТИЛХОЛИНОВЫХ РЕЦЕПТОРОВ), ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2005 |
|
RU2402551C2 |
| АЗАБИЦИКЛОАЛКИЛЬНЫЕ ЭФИРЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТОВ АЛЬФА7-nAChR | 2003 |
|
RU2352569C2 |
| (1-АЗАБИЦИКЛО[3,3,1]НОН-4-ИЛ)-[5-(1Н-ИНДОЛ-5-ИЛ)-ГЕТЕРОАРИЛ]-АМИНЫ, КАК ХОЛИНЕРГИЧЕСКИЕ ЛИГАНДЫ nAChR, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ПСИХОТИЧЕСКИХ И НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2006 |
|
RU2440350C2 |
| [(1Н-ИНДОЛ-5-ИЛ)-ГЕТЕРОАРИЛОКСИ]-1-(АЗАБИЦИКЛО[3.3.1]НОНАНЫ, КАК ХОЛИНЕРГИЧЕСКИЕ ЛИГАНДЫ N-ACHR, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ПСИХОТИЧЕСКИХ И НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ | 2006 |
|
RU2471797C2 |
| АЗАБИЦИКЛИЧЕСКИЕ АЛКАНОВЫЕ ПРОИЗВОДНЫЕ, ЗАМЕЩЕННЫЕ КОНДЕНСИРОВАННЫМ БИЦИКЛОГЕТЕРОЦИКЛОМ | 2007 |
|
RU2437884C2 |
| СОЕДИНЕННЫЕ МОСТИКОВОЙ СВЯЗЬЮ N-ЦИКЛИЧЕСКИЕ СУЛЬФОНАМИДО-ИНГИБИТОРЫ ГАММА-СЕКРЕТАЗЫ | 2006 |
|
RU2422443C2 |
| ЛИГАНДЫ НИКОТИНОВОГО РЕЦЕПТОРА АЛЬФА-7, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2005 |
|
RU2418797C2 |
| СЕЛЕКТИВНЫЕ К ПОДТИПУ РЕЦЕПТОРА АЗАБИЦИКЛОАЛКАНОВЫЕ ПРОИЗВОДНЫЕ | 2008 |
|
RU2417984C1 |
| МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ КИНАЗ TRK | 2019 |
|
RU2778294C2 |
| ПОЛОЖИТЕЛЬНЫЕ АЛЛОСТЕРИЧЕСКИЕ МОДУЛЯТОРЫ МУСКАРИНОВОГО АЦЕТИЛХОЛИНОВОГО РЕЦЕПТОРА M4 | 2017 |
|
RU2750935C2 |
Изобретение относится к новым 1-азабициклоалкильным производным формулы (I):
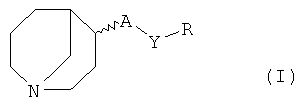
где А представляет собой О или N(R1); Y представляет собой группу формулы:
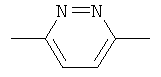 ,
, 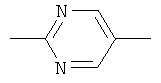 ,
, 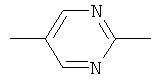 ,
,
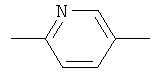 ,
, 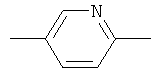 или
или 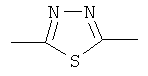 ,
,
R представляет собой замещенный или незамещенный фенил или индолилрадикал, к их применению в качестве фармацевтических средств, к содержащим их фармацевтическим композициям, к способам лечения и профилактики психических и нейродегенеративных заболеваний. 7 н. и 10 з.п.ф-лы.
1. Соединение формулы I

где А представляет собой О или N(R1);
R1 представляет собой водород, С1-С4алкил или CF3;
Y представляет собой группу формул




 или
или 
где левая связь присоединена к группе А и правая связь присоединена к группе R;
R представляет собой фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из галогена, C1-С4алкила, С1-С4алкокси, нитро, циано, С1-С4алкила, который замещен галогеном;
или R представляет собой индолил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из С1-С4алкила и гидрокси;
в форме свободного основания или в форме фармацевтически приемлемой кислотно аддитивной соли.
2. Соединение формулы I по п.1, где
А представляет собой кислород, Y представляет собой группу

и R представляет собой индолил, незамещенный или замещенный 1-3 заместителями, выбранными из С1-С2алкила.
3. Соединение формулы I по п.1, где соединение представляет собой (4SR,5SR)-4-[6-(1Н-Индол-5-ил)пиридазин-3-илокси]-1-азабицикло[3.3.1]нонан.
4. Соединение формулы I по п.1, где А представляет собой кислород,
Y представляет собой группу

и R представляет собой индолил, незамещенный или замещенный 1-3 заместителями, выбранными из C1-С2алкила.
5. Соединение формулы I по п.1, где соединение выбрано из группы, состоящей из
(4SR,5SR)-4-[5-(1Н-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонана,
(4S,5S)-4-[5-(1Н-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонана и
(4R,5R)-4-[5-(1Н-Индол-5-ил)пиримидин-2-илокси]-1-азабицикло[3.3.1]нонана.
6. Соединение формулы I по п.1, где
А представляет собой кислород, Y представляет собой группу

и R представляет собой индолил, незамещенный или замещенный 1-3 заместителями, выбранными из С1-С2алкила.
7. Соединение формулы I по п.1, где соединение выбрано из группы, состоящей из
(4SR,5SR)-4-[5-(1Н-Индол-5-ил)пиридин-2-илокси]-1-азабицикло [3.3.1] нонана,
(4S,5S)-4-[5-(1Н-Индол-5-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонана и
(4R,5R)-4-[5-(1Н-Индол-5-ил)пиридин-2-илокси]-1-азабицикло[3.3.1]нонана.
8. Соединение формулы I пo п.1, где
А представляет собой N(R1), a
R представляет собой фенил, незамещенный или замещенный 1-3 заместителями, выбранными из галогена, NO2,CN, С1-С4алкокси и C1-С4алкила, который является незамещенным или замещен галогеном; или
R представляет собой индолил, незамещенный или замещенный 1-3 заместителями, выбранными из С1-С2алкила.
9. Соединение по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли для применения в качестве фармацевтического средства, обладающего агонистической активностью в отношении α7 nAChR.
10. Соединение по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли для применения для профилактики и лечения психических и нейродегенеративных заболеваний.
11. Фармацевтическая композиция, обладающая агонистической активностью в отношении α7 nAChR, включающая соединение по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли вместе с фармацевтическим носителем или разбавителем.
12. Применение соединения по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли в качестве фармацевтического средства для профилактики и лечения психических и нейродегенеративных заболеваний.
13. Применение соединения по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли для изготовления лекарственного средства для профилактики и лечения психических и нейродегенеративных заболеваний.
14. Способ профилактики и лечения психических и нейродегенеративных заболеваний у пациента, нуждающегося в таком лечении, который включает введение такому пациенту терапевтически эффективного количества соединения по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли.
15. Соединение по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли для применения для лечения или профилактики заболевания или состояния, в котором играет роль или участвует активация α7 nAChR.
16. Применение соединения по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли в качестве фармацевтического средства для лечения или профилактики заболевания или состояния, в котором играет роль или участвует активация α7 nAChR.
17. Способ лечения или профилактики заболевания или состояния, в котором играет роль или участвует активация α7 nAChR, у субъекта, нуждающегося в таком лечении, который включает введение такому пациенту терапевтически эффективного количества соединения по любому из пп.1-8 в форме свободного основания или в форме фармацевтически приемлемой кислотной аддитивной соли.
| JP 04208267 А, 29.07.1992 | |||
| ABOUL-ENEIN, EUROPEAN JOURNAL OF MEDICINAL CHEMISTRY, vol.11, no.2, 1976, p.133-137 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| СИНТЕЗ ПОЛИМОРФА ГИДРАТА 4-АМИНО-5-ХЛОРО-2-МЕТОКСИ-N-(1-АБАЗИЦИКЛО[3.3.1]НОН-4-ИЛ)БЕНЗАМИДА ГИДРОХЛОРИДА | 2004 |
|
RU2337102C2 |
Авторы
Даты
2012-03-20—Публикация
2005-06-17—Подача