Область техники
Представленное изобретение относится к сокристаллической форме (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (в дальнейшем иногда именуемого как «производное С-гликозида A» или просто «известное соединение А») с L-пролином. Более конкретно, настоящее изобретение относится к сокристаллической форме производного С-гликозида A с L-пролином, имеющей постоянное качество и улучшенную стабильность при хранении, в качестве кристаллической лекарственной субстанции для приготовления фармацевтических препаратов, а также к фармацевтическим композициям, содержащим сокристаллическую форму, в качестве активного ингредиента, применимым, в частности, в качестве средств для лечения диабета.
Уровень техники
Авторы данного изобретения показали, что (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцит (известное соединение А), представленное следующей химической формулой, является соединением, применимым в качестве ингибитора сотранспортера Na+-глюкозы для лечения и предотвращения диабета, такого как инсулиннезависимый диабет (диабет 1 типа) и инсулиннезависимый диабет (диабет 2 типа), заболеваний, связанных с резистентностью к инсулину и ожирением (патентный документ 1, см. пример 138).
[Химическая формула 1]
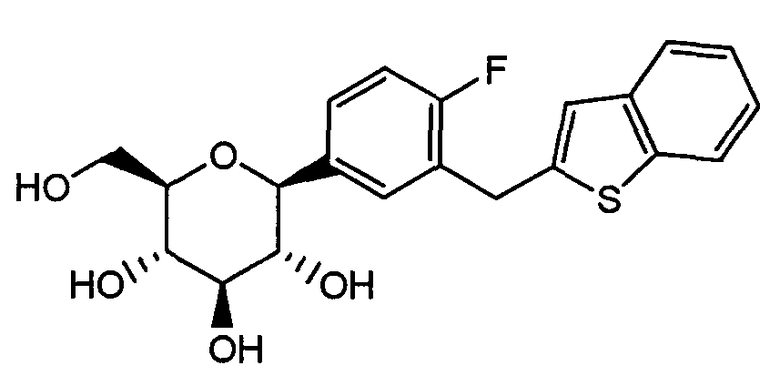
Патентный документ 1: WO2004/080990
Раскрытие изобретения
Было обнаружено, что кристаллическая форма известного соединения А, описанная в патентном документе 1, образует клатратный гидрат и обратимо превращается из безводного соединения в не-стехиометрический гидрат в зависимости от гигротермических условий. Таким образом, было обнаружено, что известное соединение А неспособно сохранять постоянное качество в качестве лекарственной субстанции, используемой для изготовления фармацевтических препаратов.
По этой причине авторы настоящего изобретения провели исследования условий кристаллизации для получения кристаллической формы известного соединения А, которая не образует клатратного гидрата. Выражаясь более детально, авторы представленного изобретения провели исследования таких условий кристаллизации путем растворения известного соединения А, при нагревании, в одном растворителе, выбранном из метанола, этанола, 2-пропанола, диметилформамида, тетрагидрофурана, ацетона, метилэтилкетона, этилацетата, уксусной кислоты, пиридина, 1,4-диоксана, ацетонитрила, анизола, воды, толуола, диэтилового эфира, диизопропилового эфира, ди-н-бутилового эфира, н-гексана, циклогексана, н-гептана, хлороформа и четыреххлористого углерода, или в смешанных растворителях, являвшихся сочетаниями двух или более типов перечисленных выше отдельных растворителей с последующим медленным охлаждением полученного раствора.
В результате приведенных выше исследований были получены кристаллические формы, которые образуют клатратный гидрат и, при некоторых условиях кристаллизации, только кристаллическая форма, частично или полностью сольватированная использованным для кристаллизации растворителем. Любая сольватированная кристаллическая форма, содержащая растворитель, вызывающий проблемы с безопасностью, в больших количествах является непригодной в качестве субстанции для использования в лекарственном препарате. Таким образом, возникла проблема, заключающаяся в том, что применение известного соединения А в свободной форме в качестве лекарственной субстанции при производстве лекарственных средств практически неосуществимо.
Далее, в обычном диапазоне pH известное соединение А присутствует в виде неионного соединения. Таким образом, было невозможно избежать указанной выше проблемы путем образования фармацевтически приемлемой соли известного соединения А.
Представленное изобретение было выполнено с целью решения упомянутых выше проблем. Объектом представленного изобретения является предоставление сокристаллической формы известного соединения А, имеющей постоянное качество и улучшенную стабильность при хранении и пригодной в качестве кристаллической лекарственной субстанции для приготовления фармацевтических препаратов.
Для достижения упомянутой выше цели авторы представленного изобретения провели исследования формирования сокристаллической формы известного соединения с аминокислотами. В результате, оказалось, что кристаллические формы известного соединения А с глицином, L-аспарагином, L-аспарагиновой кислотой, L-глютамином, L-глутаминовой кислотой, L-лизином, L-аргинином, L-гистидином, L-серином, L-треонином, L-цистеином, L-метионином, L-фенилаланином, L-тирозином, L-триптофаном, L-аланином, L-валином, L-лейцином, L-изолейцином, D-аспарагином, D-аспарагиновой кислотой, D-глютамином, D-глутаминовой кислотой, D-аргинином, D-серином, D-треонином, D-метионином, D-фенилаланином, D-аланином, D-валином, D-лейцином, D-изолейцином и D-пролином не могут быть получены.
С другой стороны, было обнаружено, что известное соединение А и L-пролин образуют, при молярном соотношении 1:1, единую сокристаллическую форму, с постоянным качеством и хорошей воспроизводимостью. Также обнаружено, что сокристаллическая форма имеет превосходство по стабильности при хранении и может стабильно поставляться в качестве кристаллической лекарственной субстанции для изготовления фармацевтических препаратов. Эти результаты привели к созданию представленного изобретения.
Для достижения упомянутой выше цели, в соответствии с представленным изобретением предложены сокристаллические формы производного С-гликозида А с L-пролином (сокристаллическая форма в дальнейшем именуемая время от времени как «сокристаллическая форма в соответствии с представленным изобретением») и фармацевтическая композиция, содержащая сокристаллическую форму в качестве активного ингредиента, практически применимая в качестве средства для лечения диабета.
[1] Сокристаллическая форма (13)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином.
[2] Сокристаллическая форма в соответствии с [1], где молярное соотношение (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита и L-пролина составляет 1:1.
[3] Сокристаллическая форма в соответствии с [1], имеющая эндотермический пик от 201 до 213°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC).
[4] Сокристаллическая форма в соответствии с [1], имеющая пики при 2θ(°) 4,14, 8,98, 12,4, 16,5, 17,5, 18,7, 20,5 и 21,5, по данным измерений дифракции рентгеновского излучения на порошке.
[5] Сокристаллическая форма в соответствии с [1], имеющая эндотермический пик от 201 до 213°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC) и пики при 2θ(°) 4,14, 8,98, 12,4, 16,5, 17,5, 18,7, 20,5 и 21,5, по данным измерений дифракции рентгеновского излучения на порошке.
[6] Фармацевтическая композиция, включающая сокристаллическую форму в соответствии с любым из пунктов [1]-[5] в качестве активного ингредиента.
[7] Фармацевтическая композиция, полученная с использованием сокристаллической формы в соответствии с любым из пунктов [1]-[5].
[8] Фармацевтическая композиция по пунктам [6] или [7], далее включающая фармацевтически приемлемый наполнитель.
[9] Фармацевтическая композиция по любому из пунктов [6]-[8], являющаяся средством для лечения диабета.
[10] Применение сокристаллической формы по любому из пунктов [1]-[5] для производства средства для лечения диабета.
[11] Способ лечения диабета, включающий введение пациенту эффективной терапевтической дозы сокристаллической формы по любому из пунктов [1]-[5] пациентам.
В соответствии с представленным изобретением предложена сокристаллическая форма известного соединения А и L-пролина, имеющая постоянное качество и улучшенную стабильность при хранении в качестве кристаллической лекарственной субстанции, используемой для приготовления фармацевтических препаратов, и фармацевтическая композиция, содержащая сокристаллическую форму в качестве активного ингредиента, пригодная, в частности, в качестве средства для лечения диабета.
Кратное описание чертежей
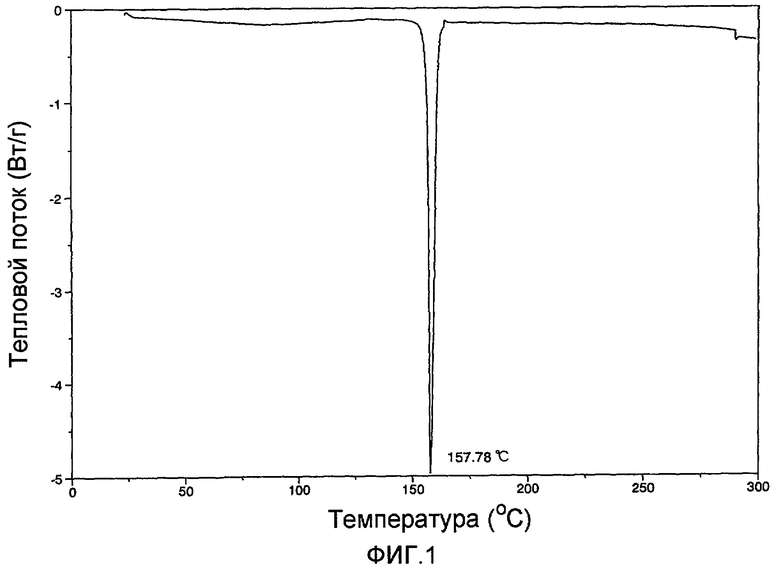
[Фиг.1] Фиг.1 представляет собой диаграмму дифференцирующей сканирующей калориметрии (диаграмму DSC анализа) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А).
[Фиг.2] Фиг.2 представляет собой диаграмму дифракции рентгеновского излучения на порошке (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А).
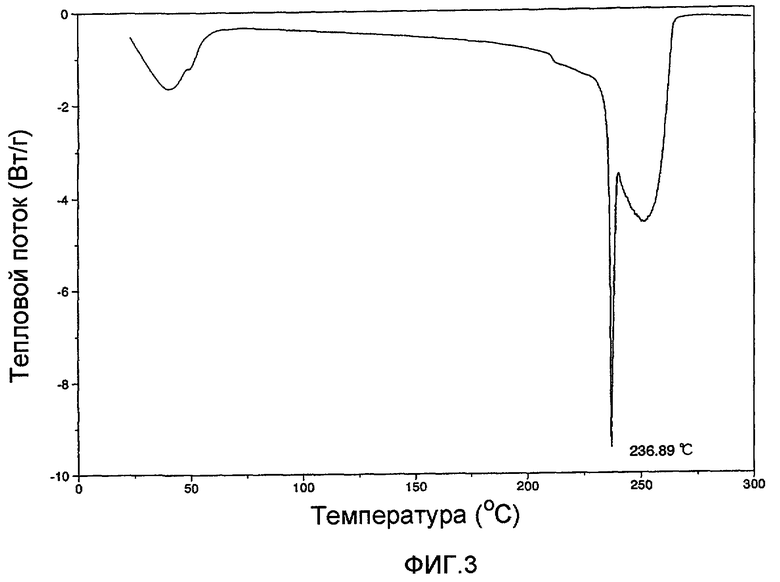
[Фиг.3] Фиг.3 представляет собой диаграмму дифференцирующей сканирующей калориметрии (диаграмму DSC анализа) L-пролина.
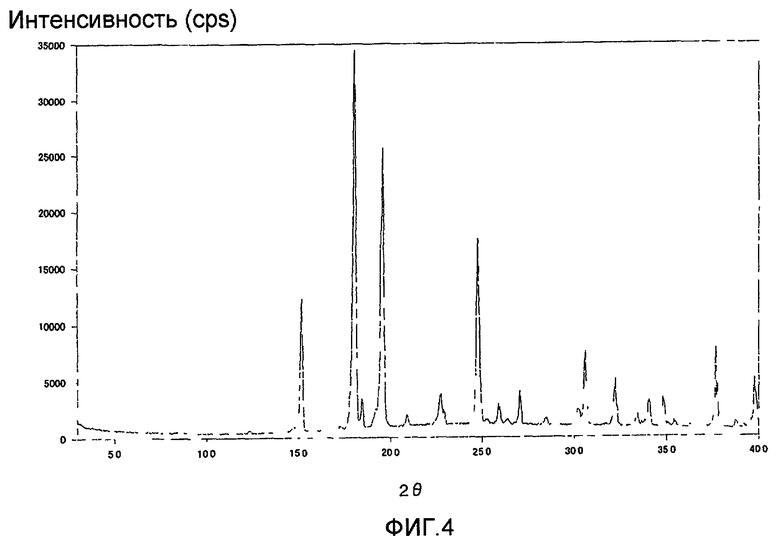
[Фиг.4] Фиг.4 представляет собой диаграмму дифракции рентгеновского излучения на порошке L-пролина.
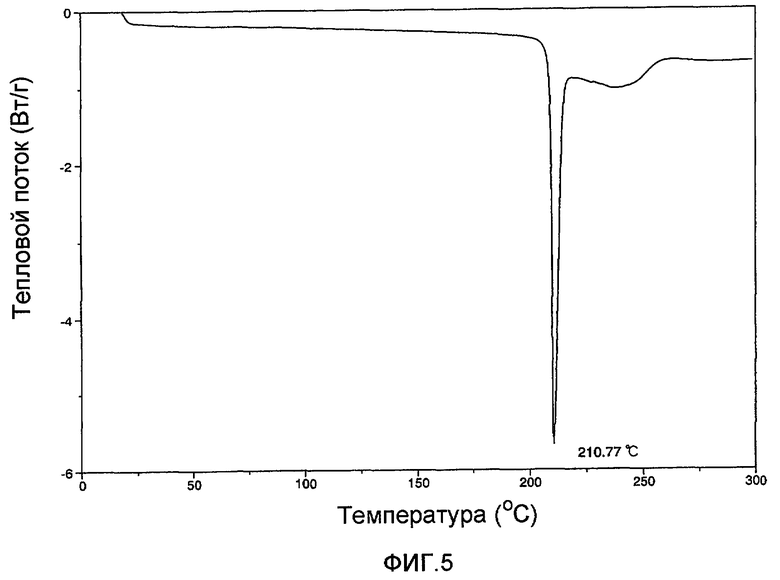
[Фиг.5] Фиг.5 представляет собой диаграмму дифференцирующей сканирующей калориметрии (диаграмму DSC анализа) сокристаллической формы (сокристаллической формы в соответствии с представленным изобретением) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином.
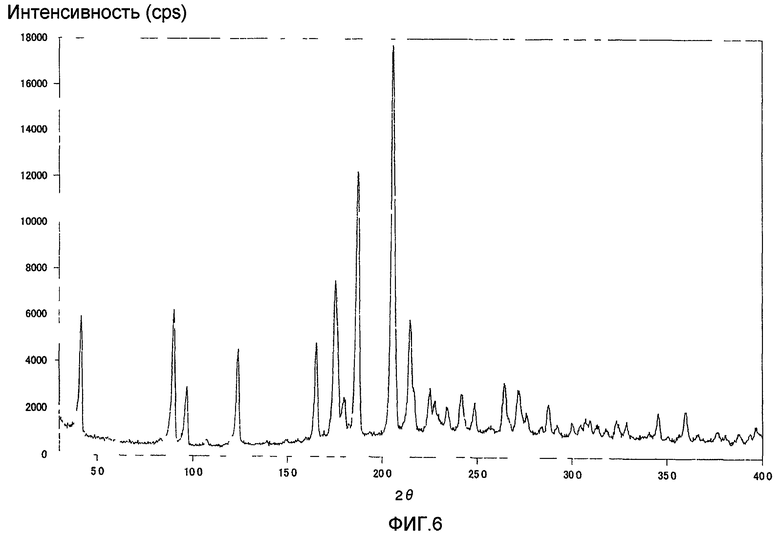
[Фиг.6] Фиг.6 представляет собой диаграмму дифракции рентгеновского излучения на порошке сокристаллической формы (сокристаллической формы в соответствии с представленным изобретением) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином.
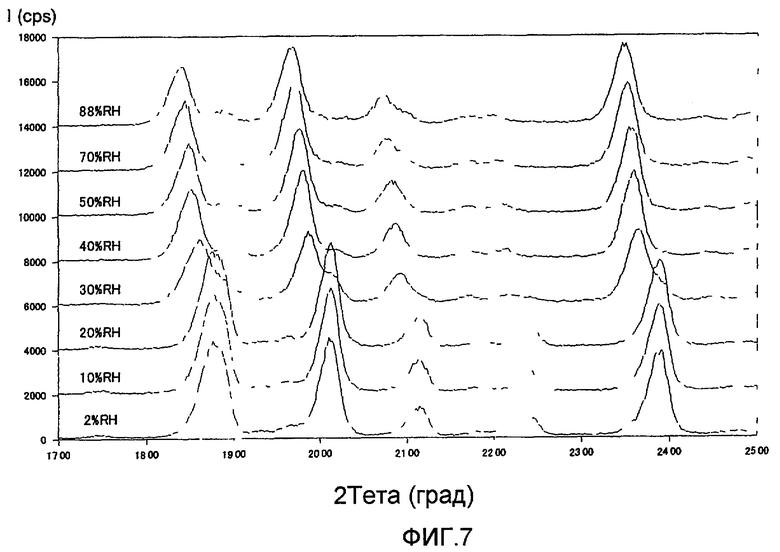
[Фиг.7] Фиг.7 представляет собой диаграмму дифракции рентгеновского излучения на порошке (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А), полученную путем измерения при различных значениях влажности.
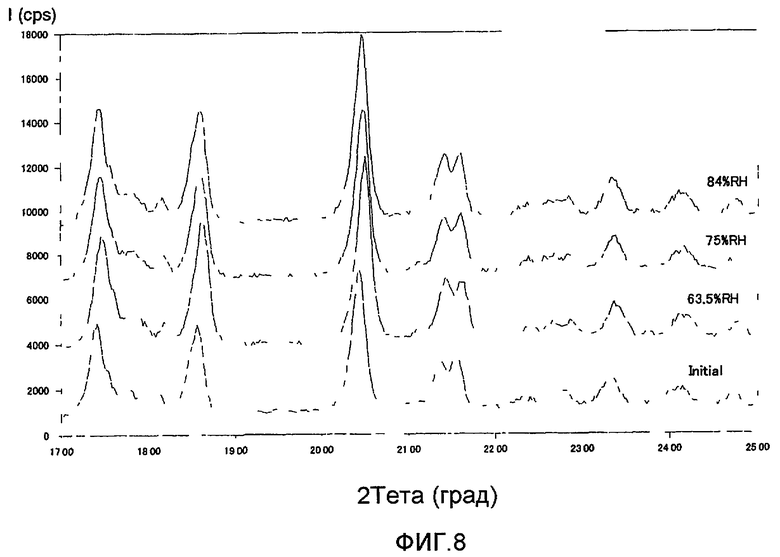
[Фиг.8] Фиг.8 представляет собой диаграмму дифракции рентгеновского излучения на порошке сокристаллической формы (сокристаллической формы в соответствии с представленным изобретением) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином, который хранился в течение 7 дней при различных значениях влажности, по сравнению с диаграммой дифракции рентгеновского излучения на порошке этой же сокристаллической формы до хранения.
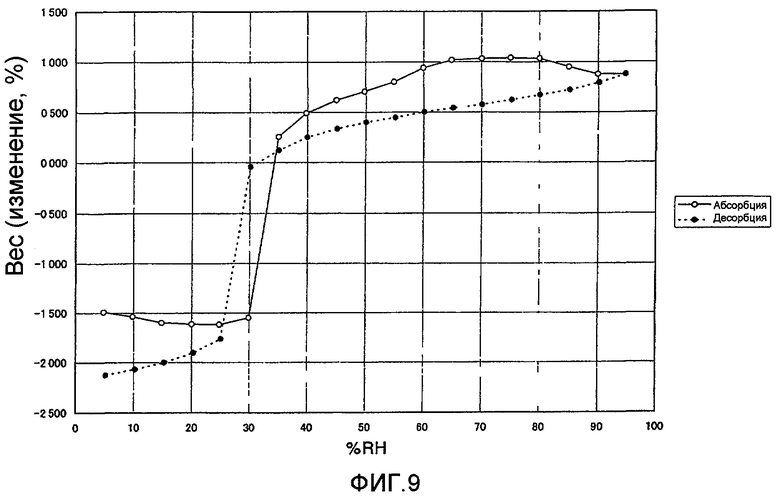
[Фиг.9] Фиг.9 представляет собой изотерму абсорбции-десорбции (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А).
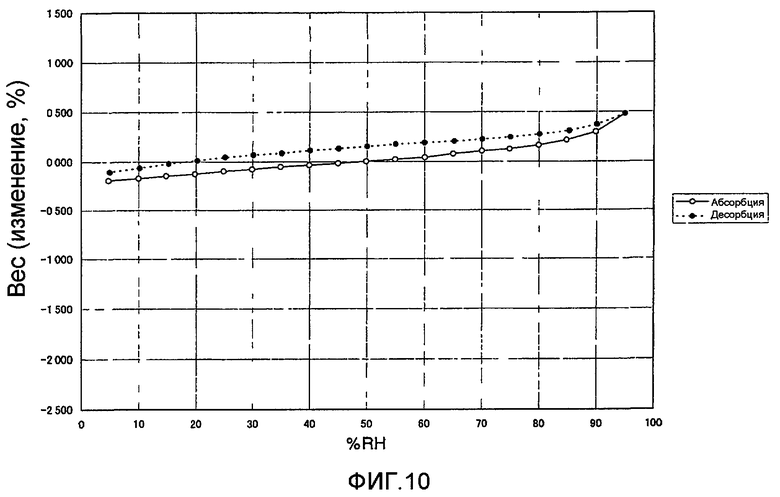
[Фиг.10] Фиг.10 представляет собой изотерму абсорбции-десорбции сокристаллической формы (сокристаллической формы в соответствии с представленным изобретением) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином.
Предпочтительный вариант осуществления изобретения
Предпочтительный вариант осуществления изобретения описан ниже более конкретно. Сокристаллическая форма (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином в соответствии с представленным изобретением имела химическую структуру, показанную ниже.
[Химическая формула 2]
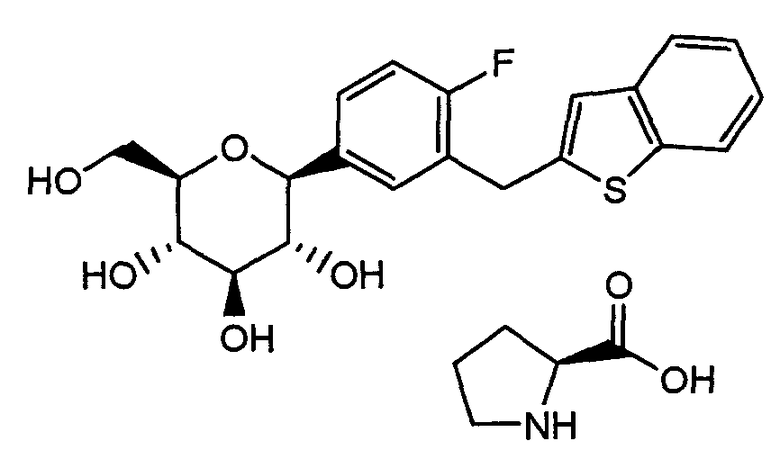
Как упомянуто выше, в отличие от кристаллической формы, образующей клатратный гидрат, сокристаллическая форма в соответствии с представленным изобретением получается в виде сокристаллическая форма, имеющей постоянное качество, хорошую воспроизводимость, может поставляться стабильно в качестве кристаллической лекарственной субстанции, используемой для приготовления фармацевтических препаратов, и имеет улучшенную стабильность при хранении. Различия в кристаллической форме между известным соединением А, которое образует клатратный гидрат, и сокристаллической формой в соответствии с представленным изобретением видны, в частности, из результатов дифференцирующего сканирующего калориметрического анализа (анализа DSC) и дифракции рентгеновского излучения на порошке.
В частности, сокристаллическая форма в соответствии с представленным изобретением имела эндотермический пик от 201 до 213°С, по измерениям при помощи дифференциальной сканирующей калориметрии (анализа DSC)и пики при 2θ(°) 4,14, 8,98, 12,4, 16,5, 17,5, 18,7, 20,5 и 21,5, по данным измерения дифракции рентгеновского излучения на порошке.
Известное соединение А характеризуется углами дифракции (2θ(°)) и относительной интенсивностью, измеренной методами дифракции рентгеновского излучения на порошке, показанными в таблице 1. С другой стороны, сокристаллическая форма в соответствии с представленным изобретением характеризуется углами дифракции (2θ(°)) и относительной интенсивностью, измеренными методом дифракции рентгеновского излучения на порошке и показанными в таблице 2. При этом в силу природы данных, полученных методом дифракции рентгеновского излучения на порошке, интервал кристаллической решетки и общая структура являются важными при идентификации кристаллической формы, а относительная интенсивность, которая в большей или меньшей мере зависит от направления роста кристаллов, размера частиц и условий измерения, не должны строго ограничиваться.
В кристаллической форме (известного соединения А), которая образует клатратный гидрат, наблюдается следующий феномен: когда кристаллы образуют нестехиометрический гидрат, возникает изменение во внешнем слое кристалла, и как результат, возникает сдвиг угла дифракции.
«Дифракция рентгеновского излучения на порошке» и «дифференциальная сканирующая калориметрия (анализ DSC)» проводились при следующих условиях.
(1) Стандартные измерения
«MAC Science MXP18TAHF22», снабженный медной рентгеновской трубкой, использовали при токе 200 мА, напряжении на трубке 40 кВ, ширине выборки 0,020°, скорости сканирования 3°/мин, длине волны 1,54056 Ǻ и углами измерения дифракции, изменяющимися от (2θ) 3 до 40°.
(2) Измерения при управляемой влажности
«MAC Science MXP 18 TAHF 22, с мультифункциональным конвертером температуры и влажности (VAISALA MHP 235)», снабженный медной рентгеновской трубкой, использовали при токе 350 мА, напряжении на трубке 50 кВ, ширине выборки 0,020°, скорости сканирования 3°/мин, длине волны 1,54056 Ǻ, и углами измерения дифракции (2θ), изменяющимися от 5 до 40°.
(Дифференциальный сканирующий калориметрический анализ (анализ DSC))
«TA Instrument TA 5000» использовали при температуре от комнатной температуры до 300°С (10°С/мин) и скорости подачи N2 50 мл/мин с использованием алюминиевой кюветы для образцов.
(Способ получения)
Сокристаллическая форма в соответствии с представленным изобретением может быть получена с применением свободной формы производного С-гликозида А, описанного в примере 138 патентного документа 1, и L-пролина, как показано нижеследующей формулой. То есть (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцит (известное соединение А) и L-пролин перемешивают в молярном соотношении приблизительно 1:1 при нагревании в подходящем растворителе. После медленного охлаждения при перемешивании реакционной смеси полученное твердое вещество отделяют путем фильтрования. Твердое вещество, промытое соответствующим растворителем, высушивают, после чего подвергают перекристаллизации с применением соответствующего растворителя. Полученные кристаллы собирают при помощи фильтрации, промывают соответствующим растворителем, после чего сушат, таким образом может быть получена сокристаллическая форма (сокристаллическая форма в соответствии с представленным изобретением) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином.
[Химическая формула 3]
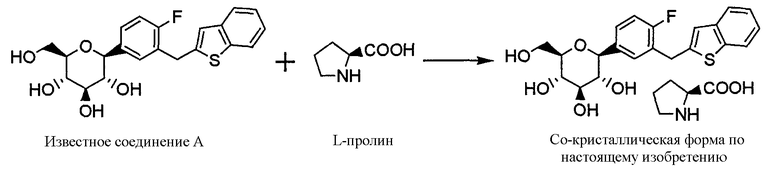
В качестве конкретных примеров растворителя могут быть приведены спирты (например, метанол, этанол, 2-пропанол и н-пропанол), вода и растворители, являющиеся их смесями. Температура перемешивания при нагревании обычно была приблизительно от 40 до 150°С, предпочтительно приблизительно от 60 до 100°С. Время перемешивания при нагревании обычно составляло приблизительно от 15 минут до 2 часов, предпочтительно от приблизительно 20 минут до 1 часа. Температура перемешивания с охлаждением обычно была приблизительно от -20 до 20°С, предпочтительно приблизительно от 0 до 10°С. Время перемешивания при охлаждении обычно было приблизительно от 30 минут до 3 часов, предпочтительно приблизительно от 1 до 2 часов. Высушивание обычно проводилось при нагревании под вакуумом. Температура сушки обычно составляла приблизительно от 30 до 100°С, предпочтительно приблизительно от 40 до 60°С.
Сокристаллическую форму в соответствии с представленным изобретением, полученную упомянутым выше методом, получают с использованием производного С-гликозида А и L-пролина в молярном соотношении 1:1. Таким образом, сокристаллическая форма в соответствии с представленным изобретением считается обычно сокристаллической формой производного С-гликозида А и L-пролина с молярным соотношением 1:1.
Фармацевтическая композиция в соответствии с представленным изобретением содержит вышеупомянутую сокристаллическую форму в соответствии с представленным изобретением в качестве активного компонента. Также фармацевтическая композиция в соответствии с представленным изобретением изготавливается с использованием вышеупомянутой сокристаллической формы в соответствии с представленным изобретением. Фармацевтическая композиция в соответствии с представленным изобретением может далее включать фармацевтически приемлемый наполнитель, такой как компонент, отличный от сокристаллической формой в соответствии с представленным изобретением. Фармацевтическая композиция в соответствии с представленным изобретением может применяться, в частности, в качестве средства для лечения диабета. Фармацевтическая композиция, содержащая ко-кристалл в соответствии с представленным изобретением в качестве активного ингредиента, может быть представлена в форме таблеток, порошков, мелких гранул, гранул, капсул, пилюль, жидких препаратов, инъекций, суппозиториев, мазей, паст и тому подобного, с применением наполнителей, носителей и иных добавок, обычно применяемых при изготовлении фармацевтических препаратов. Эти препараты вводятся орально или иным способом.
Хотя клиническая доза (эффективная доза для выздоровления) сокристаллической формы в соответствии с изобретением для человека приблизительно определяется с учетом симптомов, веса, возраста, пола и подобных данных пациента, которому вводится фармацевтический препарат, дневная доза для взрослого обычно составляет от 0,1 до 500 мг для перорального и от 0,01 до 100 мг для иного пути введения. Эти дозы вводят пациенту однократно или в несколько приемов. Поскольку доза может изменяться в соответствии с различными условиями, доза, меньшая, чем приведенные выше пределы, в некоторых случаях является достаточной.
Для перорального введения твердой композиции сокристаллической формы в соответствии с изобретением используются таблетки, порошки, гранулы и подобные формы. В таких твердых композициях один или более активных компонентов смешивается по меньшей мере с одним инертным разбавителем, таким как лактоза, манит, глюкоза, гидроксипропилцеллюлоза, микрокристаллическая целлюлоза, крахмал, поливинилпирролидон и алюмометасиликат магния. В соответствии с обычной практикой композиция может содержать добавки, отличные от инертного разбавителя. Например, могут быть добавлены смазка, такая как стеарат магния, дезинтегратор, такой как гликолят целлюлозы-кальция, стабилизатор, такой как лактоза, и солюбилизирующий агент, такой как глутаминовая кислота или аспарагиновая кислота. Если требуется, таблетки или пилюли могут быть снабжены покрытием из сахаров, таким как покрытие из сахарозы, желатина, гидроксипропилцеллюлозы, или фталата гидроксипропилметилцеллюлозы, или пленкой из растворимого в кишечнике или в желудке вещества.
Жидкие композиции для перорального введения содержат фармацевтически приемлемый эмульгатор, растворяющий фактор, суспендирующий агент, сироп, эликсир и тому подобные компоненты, а также обычный инертный разбавитель, такой как очищенная вода или этиловый спирт. В дополнение к инертным разбавителям композиция может содержать вспомогательный агент, такой как солюбилизирующий агент, солюбилизирующий адъювант, смачивающий агент, и суспендирующий агент, а также подсластитель, ароматизатор, отдушку и антисептический агент.
Инъекционный препарат для введения не-оральным способом содержит стерильный водный или неводный растворяющий агент, суспендирующий агент и эмульгатор. В качестве примеров водного растворяющего агента и водного разбавителя суспендирующего агента могут быть приведены дистиллированная вода для инъекций или физиологический раствор. В качестве примеров неводного растворяющего агента и неводного разбавителя для суспендирующего агента могут быть приведены растительные масла, такие как пропиленгликоль, полиэтиленгликоль и оливковое масло; спирты, такие как этиловый спирт; и Polisolvate 80 (коммерческое наименование).
Композиция может далее включать другие добавки, такие как изотонический агент, антисептический агент, смачивающий агент, эмульгатор, диспергирующее средство, стабилизатор (например, лактозу), солюбилизирующий агент и солюбилизирующий адъювант. Эти добавки были стерилизованы путем фильтрования через бактериальный фильтр, добавления дезинфицирующего вещества или облучения. Из этих добавок может быть приготовлено стерильное твердое вещество, которое можно растворить в асептической воде или в стерильном растворителе для инъекций перед использованием.
Примеры
Представленное изобретение будет описано более детально в примерах, которые не предназначены для ограничения представленного изобретения.
(Эталонный пример 1)
К раствору (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторофенил]-2,3,4,6-тетра-О-бензил-D-глюцита (2,5 г) в дихлорметане (50 мл, охлажден до -78°С) добавляли в потоке аргона пентаметиленбензол (4,85 г) и раствор 1,0 М трихлорида бора в н-гептане. Смесь перемешивали при этой же температуре в течение 2 часов. После завершения реакции для разрушения избыточного реагента добавляли метанол (100 мл), после чего удаляли растворители путем дистилляции под вакуумом. Остаток очищали методом колоночной хроматографии на силикагеле (хлороформ-метанол). Полученный остаток суспендировали в смешанном растворителе из этанола и воды и нагревали с обратным холодильником до растворения. Полученный раствор медленно охлаждали до комнатной температуры для рекристаллизации. Полученные кристаллы собирали путем фильтрации, после чего сушили при нагревании под вакуумом для получения 1,1 г (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А) в виде белых кристаллов. Полученная диаграмма дифференцирующей сканирующей калориметрии (диаграмма DSC анализа) известного соединения А показана на фиг.1, а его диаграмма дифракции рентгеновского излучения на порошке показана на фиг.2.
(Эталонный пример 2)
Диаграмма дифференцирующей сканирующей калориметрии (диаграмма DSC анализа) L-пролина показана на фиг.3, а его диаграмма дифракции рентгеновского излучения на порошке показана на фиг.4.
(Пример 1)
К 25 мл суспензии (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (известного соединения А) (2,0 г) в этаноле (25 мл) добавляли L-пролин (570 мг). Реакционную смесь перемешивали при 100°С в течение 30 минут. После этого реакционную смесь медленно охлаждали до комнатной температуры, полученное твердое вещество собирали путем фильтрации и промывали этанолом. Полученное твердое вещество сушили под вакуумом при нагревании, после чего твердое вещество суспендировали в смешанном растворителе из этанола и воды. Суспензию подвергали нагреванию с обратным холодильником до растворения. Полученный раствор медленно охлаждали и перемешивали в течение 1 часа при охлаждении льдом. Полученные кристаллы собирали путем фильтрования, промывали этанолом и сушили под вакуумом при нагревании для получения сокристаллической формы (сокристаллическая форма в соответствии с представленным изобретением) (1,7 г) (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином. Диаграмма дифференцирующей сканирующей калориметрии (диаграмма DSC анализа) полученной сокристаллической формы в соответствии с представленным изобретением показана на фиг.5, а его диаграмма дифракции рентгеновского излучения на порошке показана на фиг.6.
Как показывают профили диаграмм дифференциального сканирующего калориметрического анализа (диаграмм анализа DSC) и диаграммы дифракции рентгеновского излучения на порошке на фиг. от 1 до 6, был сделан вывод, что в примере 1 была получена сокристаллическая форма известного соединения А и L-пролина, а не обычная смесь известного соединения А и L-пролина.
Промышленное применение
Поскольку сокристаллическая форма в (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином в соответствии с представленным изобретением имеет превосходную стабильность при хранении и демонстрирует ингибирующее котранспортер Na+-глюкозы и антигипергликемическое действие сокристаллическая форма может применяться в качестве фармацевтического средства, в частности в качестве ингибитора котранспортера Na+-глюкозы, для лечения и профилактики диабета, такого как инсулинозависимый сахарный диабет (диабет 1 типа) и инсулиннезависимый сахарный диабет (диабет 2 типа), заболевания, связанные с инсулинрезистентностью и ожирение.
Прекрасная стабильность при хранении и превосходное ингибирующее человеческий ко-транспортер Na+-глюкозы и антигипергликемическое действие сокристаллической формы в соответствии с представленным изобретением были подтверждены [Исследованием стабильности при хранении] [Исследованием способности поглощать влагу] и [Фармакологическими исследованиями] (Исследованием 1 и Исследованием 2), приведенными ниже.
[Исследование стабильности при хранении]
Измерения дифракции рентгеновского излучения на порошке проводились непрерывно при температуре 25°С в диапазоне относительной влажности от 2 до 88%. Как результат, было подтверждено, что известное соединение А показывает сдвиг угла дифракции, связанный с изменением относительной влажности (см. Фиг.7). Далее его кристаллы в любой свободной форме, полученные при различных условиях кристаллизации, являлись физически нестабильными кристаллами, имеющими тенденцию обратимо формировать нестехиометрический клатратный гидрат при комнатной температуре и низкой влажности.
Напротив, сокристаллические формы в соответствии с представленным изобретением показывали отсутствие физических изменений, будучи оставленными на срок 7 дней при комнатной температуре (25°С) при влажности от 63,5% RH до 84% RH (см. фиг.8). Далее, сокристаллическая форма была физически стабильна в течение по меньшей мере двух месяцев, даже если она была оставлена при 40°С/75% RH/открытым, 60°С/при неконтролируемой влажности или при 80°С/неконтролируемой влажности.
[Исследование способности поглощать влагу]
Исследования веса проводились с применением «VTI SGS-100» при температуре 25°С, диапазоне относительной влажности от 5 до 95% и интервале изменения относительной влажности 5%. В результате, известное соединение А показало нестехиометрическое поглощение влаги, сопровождаемое физическими изменениями при низкой влажности. Особенно резкое увеличение веса происходило при относительной влажности от 25 до 35% (см. Фиг.9). Далее, несмотря на то, что известное соединение А дает слегка отличающиеся друг от друга в зависимости от размеров частиц и формы кристаллизации, был случай, когда при 25°С при изменении влажности от 5 до 95% RH было десорбировано и абсорбировано 3,2% воды.
Напротив, сокристаллические формы в соответствии с представленным изобретением имели содержание влаги 0,7% или менее во всем диапазоне относительной влажности от 5 до 95% и показывали отсутствие способности поглощать влагу (см. фиг.10). Также кристаллы были физически стабильны.
[Фармакологические исследования]
(Исследование 1) [Исследование для подтверждения эффекта ингибирующего действия на человеческий котранспортер Na+-глюкозы (человеческий SGLT2)]
1) Получение экспрессионного вектора человеческого SGLT2
Сначала из тотальной РНК, происходящей из селезенки человека (производства BD Biosciences Clontech), получали при помощи обратной транскрипции с использованием Superscript II (производства Invitrogen Corporation) и случайных гексамеров одноцепочечную кДНК. Затем с использованием кДНК в качестве матрицы амплифицировали с применением реакции ПЦР с использованием Pyrobest DNA polymerase (производства Takara Bio Inc.) фрагмент, кодирующий человеческий SGLT2 (Wells R.G. et al., Am. J. Physiol., 1992,263(3) F459) (были использованы праймеры, в которых сайт HindIII и сайт EcoRI были введены на 5' и на 3'конец фрагмента ДНК, соответственно).
Амплифицированный фрагмент клонировали в вектор pCR2.1-Topo с использованием набора для клонирования Topo TA (производства Invitrogen Corporation), после чего вектором с клонированным фрагментом трансфецировали компетентные клетки Escherichia coli JM109. Устойчивые к ампициллину клоны культивировали в среде LB, содержащей ампициллин (100 мг/л). Плазмиду выделяли из культуры Escherichia coli с использованием метода Ханахана (см. Maniatis et al/, “Molecular Cloning”). Фрагмент ДНК, кодирующий человеческий SGLT2, получали путем рестрикции плазмиды HindIII/EcoRI, после чего лигировали и клонировали по тем же сайтам в экспрессионный вектор pcDNA3.1 (производства Invitrogen Corporation) с применением лигазы Т4 (производства Roche Diagnostics). Полученной лигированной ДНК трансфецировали компетентные клетки Escherichia coli JM109 описанным выше методом, после чего клетки культивировали на среде LB, содержащей ампициллин, экспрессионный вектор, содержащий человеческий SGLT2, выделяли с использованием метода Ханахана.
2) Получение экспрессирующих человеческий SGLT2 клеток.
Вектором для экспрессии человеческого SGLT2 трансфецировали клетки CHO-K1 c использованием Lipofectamine 2000 (производства Invitrogen Corporation). Клетки культивировали в среде Хэма F12 (производства Nissui Pharmaceutical Co. Ltd.), содержащей пенициллин (50 IU/мл, производства Dainippon Pharmaceutical Co. Ltd.), стрептомицин (50 мкг/мл, производства Dainippon Pharmaceutical Co. Ltd.), генетицин (40 мкг/мл, производства Invitrogen Corporation) и 10% фетальной телячьей сыворотки в присутствии 5% СО2 при 37°С в течение двух недель, в результате чего были получены устойчивые к генетицину клоны. Из этих клонов отбирали клетки, которые стабильно экспрессировали человеческий SGLT2, который демонстрирует натрий-зависимое поглощение метил-α-D-глюкопиранозида (метод измерения поглощения метил-α-D-глюкопиранозида приведен ниже).
3) Измерения ингибирования поглощения метил-α-D-глюкопиранозида
После удаления среды из клеток CHO, которые стабильно экспрессируют человеческий SGLT2, к ним добавляли буферный раствор для предварительной обработки (буферный раствор с pH 7,4, содержащий хлорид холина (140 мМ), хлорид калия (2 мМ), хлорид кальция (1 мМ), хлорид магния (1 мМ), 2-[4-(2-гидроксиэтил)-1-пиперазинил]этансульфониловую кислоту (10 мМ) и трис ((гидроксиметил)аминометан (5 мМ)) в количестве 100 мкл на лунку, после чего инкубировали при 37°С в течение 20 минут.
Для того чтобы подготовить буфер для поглощения 11 мкл метил-α-D(U-14C)-глюкопиранозида (производства Amersham Pharmacia Biotech) добавляли к 1000 мкл буферного раствора для поглощения, содержащего сокристаллическую форму в соответствии с представленным изобретением (буферный раствор с pH 7,4, содержащий хлорид натрия (140 мМ), хлорид калия (2 мМ), хлорид кальция (1 мМ), хлорид магния (1 мМ), метил-α-D-глюкопиранозид (50 мкМ), 2-[4-(2-гидроксиэтил)-1-пиперазинил]этансульфониловую кислоту (10 мМ) и трис ((гидроксиметил)аминометан (5 мМ)). Для контрольной группы был приготовлен буфер для поглощения без исследуемой кристаллической формы. Также был приготовлен буферный раствор для фонового поглощения, содержащий хлорид холина (140 мМ) вместо хлорида натрия для измерения фонового поглощения в отсутствие натрия. Также был приготовлен буферный раствор для фонового поглощения, содержащий хлорид холина (140 мМ) вместо хлорида натрия для измерения фонового поглощения в отсутствие Na и сокристаллической формы в соответствии с изобретением.
После удаления буферного раствора для предварительной обработки добавляли буферный раствор для поглощения (25 мкл на лунку) и инкубировали в течение двух часов при 37°С. После удаления буферного раствора для поглощения добавляли буферный раствор для промывки (буферный раствор с pH 7,4, содержащий хлорид холина (140 мМ), хлорид калия (2 мМ), хлорид кальция (1 мМ), хлорид магния (1 мМ), метил-α-D-глюкопиранозид (10 мМ), 2-[4-(2-гидроксиэтил)-1-пиперазинил]этансульфониловую кислоту (10 мМ) и трис ((гидроксиметил)аминометан (5 мМ)) (200 мкл в каждую лунку). Смесь немедленно удаляли. Эту операцию промывки выполняли еще раз. Для растворения клеток добавляли 0,5% лаурилсульфата (25 мкл на лунку). К растворенным клеткам добавляли 75 мкл Microscint 40 (производства Packard, Corp.), после чего измеряли радиоактивность с использованием микросцинцилляционного счетчика TopCount (производства Packard, Corp.). Значение, полученное путем вычитания значения фонового поглощения из значения поглощения контрольной группы, было принято за 100%. Концентрация для 50% ингибирования приведенного выше значения (значение IC50) была вычислена из кривой концентрации-ингибирования с использованием метода наименьших квадратов. В результате, значение IC50 для сокристаллической формы в соответствии с представленным изобретением было 5,8 нМ.
(Исследование 2) [Исследование для подтверждения антигиперглекимического действия]
В качестве лабораторных животных были использованы не голодавшие мыши KK-Ay (самцы, Clea Japan, Inc.). Сокристаллическую форму в соответствии с представленным изобретением суспендировали в 0,5% растворе метилцеллюлозы, в концентрации 1 мг/10 мл. Измеряли вес тела каждой мыши, после чего принудительно вводили перорально в количестве 10 мл/кг суспензию сокристаллической формы в соответствии с представленным изобретением. Контрольной группе вводили только водный 0,5% раствор метилцеллюлозы. Количество мышей в каждой группе составляло 6. Из хвостовой вены каждой мыши брали образцы крови непосредственно перед введением и через 1, 2, 4 и 8 часов после введения. Количество сахара в крови измеряли с использованием теста Wako Glucose CII (Wako Pure Chemical Industries, ltd.). На основе значений количества сахара в крови группы, которой была введена сокристаллическая форма в соответствии с представленным изобретением на часы от 0 до 8, после введения вычисляли площадь под кривой (AUC) значения концентрации сахара-времени в соответствии с методом трапезоидов; определяли соотношение (в %) этой площади и площади под кривой контрольной группы; это соотношение было использовано в качестве показателя интенсивности антигиперглекимического действия. В результате сокристаллическая форма в соответствии с изобретением показала сильное антигипогликемическое действие.
По результатам Исследования 1 и Исследования 2 сокристаллическая форма в соответствии с представленным изобретением демонстрирует превосходное ингибирующее ко-транспортер Na+-глюкозы действие и сильное антигипергликемическое действие. Таким образом, ожидается, что сокристаллическая форма в соответствии с представленным изобретением может стать средством для лечения диабетов, имеющим одинаковую или более высокую эффективность по сравнению с эффективностью обычных препаратов для лечения диабетов.
| название | год | авторы | номер документа |
|---|---|---|---|
| С-ГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ И ИХ СОЛИ | 2004 |
|
RU2317288C2 |
| АЗУЛЕНОВОЕ ПРОИЗВОДНОЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2003 |
|
RU2295522C2 |
| АМИДНЫЕ СОЕДИНЕНИЯ | 2015 |
|
RU2684906C2 |
| АМИННЫЙ СОЛЬВАТ ИНГИБИТОРА НАТРИЙ-ГЛЮКОЗНОГО КОТРАНСПОРТЕРА И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2710230C1 |
| СОЕДИНЕНИЕ С-ФЕНИЛГЛИЦИТОЛА ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА | 2007 |
|
RU2437876C2 |
| НОВЫЕ КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРОВ ДИПЕПТИДИЛПЕПТИДАЗЫ-IV | 2012 |
|
RU2598072C2 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА НИФЛУМОВОЙ КИСЛОТЫ С ИЗОНИКОТИНАМИДОМ ИЛИ КОФЕИНОМ | 2013 |
|
RU2536484C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ДИФЛУНИСАЛА | 2016 |
|
RU2617849C1 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОИЗВОДНЫХ ДИГИДРОПИРИМИДИНА | 2013 |
|
RU2646599C2 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА БИКАЛУТАМИДА | 2012 |
|
RU2510392C1 |

Данное изобретение сносится к сокристаллической форме (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита (соединение А) с L-пролином. Данная сокристаллическая форма известного соединения А характеризуется постоянным составом, улучшенной стабильностью при хранении, а также низкой гигроскопичностью и подходит для использования в качестве кристаллической лекарственной субстанции для изготовления фармацевтических препаратов. В частности, заявляемая сокристаллическая форма является перспективным антидиабетическим средством. 5 н. и 6 з.п. ф-лы, 2 табл., 10 ил.
1. Сокристаллическая форма (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита с L-пролином, где молярное соотношение (1S)-1,5-ангидро-1-[3-(1-бензотиен-2-илметил)-4-фторфенил]-D-глюцита и L-пролина составляет 1:1, имеющая пики при 2θ(°) 4,14, 8,98, 12,4, 16,5, 17,5, 18,7, 20,5 и 21,5, по данным измерения дифракции рентгеновского излучения на порошке.
2. Сокристаллическая форма по п.1, имеющая эндотермический пик от 201 до 213°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC).
3. Сокристаллическая форма по п.1, имеющая эндотермический пик от 201 до 213°С, по данным измерений при помощи дифференциальной сканирующей калориметрии (анализа DSC) и пики при 2θ(°) 4,14, 8,98, 12,4, 16,5, 17,5, 18,7, 20,5 и 21,5, по данным измерения дифракции рентгеновского излучения на порошке.
4. Фармацевтическая композиция, обладающая ингибирующим действием по отношению к человеческому котранспортеру Na+-глюкозы (SGLT2), включающая сокристаллическую форму по любому из пп.1-3 в качестве активного ингредиента.
5. Фармацевтическая композиция, обладающая ингибирующим действием по отношению к человеческому котранспортеру Na+-глюкозы (SGLT2), полученная с использованием сокристаллической формы по любому из пп.1-3.
6. Фармацевтическая композиция по п.4, далее включающая фармацевтически приемлемый наполнитель.
7. Фармацевтическая композиция по п.5, далее включающая фармацевтически приемлемый наполнитель.
8. Фармацевтическая композиция по п.4, являющаяся средством для лечения диабета.
9. Фармацевтическая композиция по п.5, являющаяся средством для лечения диабета.
10. Применение сокристаллической формы в соответствии с любым из пп.1-3 для производства средства для лечения диабета.
11. Способ лечения диабета, включающий введение пациенту эффективной терапевтической дозы сокристаллической формы по любому из пп.1-3 пациенту.
| WO 2004080990 A1 23.09.2004 | |||
| WO 2005023198 A2 17.03.2005 | |||
| С-АРИЛГЛЮКОЗИДНЫЕ ИНГИБИТОРЫ SGLT2 | 2000 |
|
RU2262507C2 |
| О-АРИЛГЛЮКОЗИДНЫЕ ИНГИБИТОРЫ SGLT2 И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2001 |
|
RU2269540C2 |
| Rogowska P | |||
| et al, Tetrahedron Letters, Feb | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2011-01-10—Публикация
2007-04-04—Подача