Настоящее изобретение относится к органическим соединениям, к их получению и применению в качестве фармацевтических препаратов. Одним объектом изобретения являются соединения формулы I
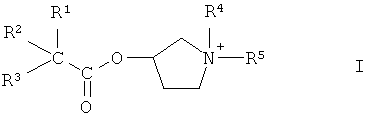
в форме соли или цвиттериона,
где
R1 и R3 каждый независимо означают С3-С15 карбоциклическую группу или 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы,
R2 означает водород, гидрокси или С1-С4алкил, необязательно замещенный группой гидрокси,
или -CR1R2R3 вместе образуют группу формулы
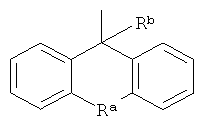
где Ra означает химическую связь, -О-, -S-, -СН2-, -СН=СН-, -СН2-СН2-, амино или -N(СН3)-, а Rb означает водород, гидрокси или С1-С4алкил, необязательно замещенный группой гидрокси,
R4 означает С1-С4алкил,
R5 означает С1алкил, замещенный группами -CO-O-R6 или -CO-NH-R6, или R5 означает С2-С10алкил, замещенный группами -O-CO-R6, -CO-O-R6, -NH-CO-R6 или -CO-NH-R6,
или R5 означает С2-С10алкенил или С2-С10алкинил, необязательно замещенный группой -R7 или -R8,
R6 означает С3-С15карбоциклическую группу или 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы,
или R6 означает C1-С10кил, необязательно замещенный группой C1-С10алкокси, -O-R7, C3-C15 карбоциклическую группу или 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы,
R7 означает 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы, а
R8 означает С3-С15карбоциклическую группу.
Термины, используемые в описании заявки, имеют следующие значения.
"Необязательно замещенный" означает группу, которая необязательно замещена в одном или более положений, предпочтительно в одном, двух или трех положениях, любым одним или любой комбинацией указанных радикалов.
Термин "галоген", используемый в описании заявки, означает элемент, относящийся к группе 17 (ранее к группе 7) Периодической таблицы элементов, например фтор, хлор, бром или йод.
Термин "C1-С10алкил", используемый в описании заявки, означает алкил с прямой или разветвленной цепью, содержащий от 1 до 10 атомов углерода.
Термин "С1-С2алкилен", используемый в описании заявки, означает алкилен с прямой или разветвленной цепью, содержащий 1 или 2 атома углерода.
Термин "С2-С10алкенил", используемый в описании заявки, означает алкенил с прямой или разветвленной цепью, содержащий от 2 до 10 атомов углерода.
Термин "С2-С10алкинил", используемый в описании заявки, означает алкинил с прямой или разветвленной цепью, содержащий от 2 до 10 атомов углерода.
Термин "C1-С10алкокси", используемый в описании заявки, означает алкокси с прямой или разветвленной цепью, содержащий от 1 до 10 атомов углерода.
Термин "С3-С15карбоциклическая группа", используемый в описании заявки, означает карбоциклическую группу, содержащую в цикле от 3 до 15 атомов углерода, например, моноциклическую группу или циклоалифатическую группу, такую как С3-С8циклоалкил, например, циклопентил, циклогексил, циклогептил или циклооктил, или ароматическую группу, такую как фенил, замещенный одной или более, обычно одной или двумя С1-С4алкильными группами, или бициклическую группу, такую как С8бициклическая, С9бициклическая или С10бициклическая группа, которая является циклоалифатической или ароматической, такой как инданил, инденил или нафтил, каждая из которых замещена одной или более, обычно одной или двумя С1-С4алкильными группами. C3-С15карбоциклическая группа является замещенной или незамещенной.
Термин "С3-С8циклоалкил", используемый в описании заявки, означает циклоалкил, содержащий от 3 до 8 атомов углерода.
Термин "C1-С10галогеналкил", используемый в описании заявки, означает C1-С10алкил, указанный выше, замещенный одним или более атомами галогена, предпочтительно одним, двумя или тремя атомами галогена.
Термин "C1-С10алкилкарбонил", используемый в описании заявки, означает C1-С10алкил, указанный выше, связанный с карбонильной группой.
Термин "C1-С10-алкилсульфонил", используемый в описании заявки, означает C1-С10алкил, указанный выше, связанный с группой -SO2-.
Термин "5-12-членная гетероциклическая группа, содержащая в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы", используемый в описании заявки, означает моногетероциклическую, бигетероциклическую или тригетероциклическую группу, насыщенную или ненасыщенную, содержащую в цикле от 5 до 12 атомов. 5-12-членная гетероциклическая группа является незамещенной или замещенной, например, одним, двумя, тремя или четырьмя заместителями.
Термин "аминокарбонил", используемый в описании заявки, означает аминогруппу, присоединенную через атом азота к карбонильной группе.
Термин "С6-С10арил", используемый в описании заявки, означает одновалентную карбоциклическую ароматическую группу, содержащую от 6 до 10 атомов углерода, например, моноциклическую группу, такую как фенил, или бициклическую группу, такую как нафтил.
Термин "С7-С15аралкил", используемый в описании заявки, означает алкил, например, С1-С5алкил, указанный выше, замещенный группой С6-С10арил, указанной выше.
В соединениях формулы I пригодными или предпочтительными объектами изобретения являются следующие группы, выбранные независимо или в любой комбинации.
R2 предпочтительно означает гидрокси. Однако если R2 означает C1-С4алкил, то R2 предпочтительно означает метил или этил.
Rb предпочтительно означает гидрокси. Однако если Rb означает С1-С4алкил, то Rb предпочтительно означает метил или этил.
R4 предпочтительно означает метил.
R5 предпочтительно означает С1алкил, замещенный группой -CO-NH-R6, где R6 означает 5- или 6-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы. Однако если R5 означает С2-С10алкил, то R5 предпочтительно означает С2-С5алкил, прежде всего этил. Если R5 означает С2-С10алкенил, то R5 предпочтительно означает С2-С4алкенил, а если R5 означает С2-С10алкинил, то R5 предпочтительно означает С2-С8алкинил, предпочтительно С2-С4алкинил.
R6 предпочтительно означает 5- или 6-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы. Однако если R6 означает C1-С10алкил, то R6 предпочтительно означает С1-С5алкил, прежде всего метил или этил, а если R6 означает C1-С10алкил, необязательно замещенный группой C1-С10алкокси, то R6 предпочтительно означает С1-С5алкил, замещенный в одном, двух или трех положениях группой С1-С4алкокси, прежде всего метокси или этокси.
Если R1 или R3 означает С3-С15карбоциклическую группу, то R1 или R3 предпочтительно означает С3-С10карбоциклическую группу, например, С3-С8циклоалкил, фенил, инданил или нафтил, прежде всего циклопентил, циклогексил или фенил.
R1 и R3 предпочтительно означают незамещенные С3-С15карбоциклические группы. Однако если R1 или R3 означает С3-С15карбоциклическую группу, которая является замещенной, то такая группа предпочтительно замещена в одном, двух или трех положениях одной или более группами галоген (прежде всего фтор), циано, гидрокси, амино, нитро, карбокси, C1-С10алкил, C1-С10галогеналкил, C1-С10алкокси, C1-С10алкилкарбонил, C1-С10алкилсульфонил, -SO2NH2, -СОО-(С6-С10арил), -СОО-(С7-С15аралкил), причем С3-С15карбоциклическая группа и 5-12-членная гетероциклическая группа содержат в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы.
Если R6 или R8 означает С3-С15карбоциклическую группу, то такая группа предпочтительно означает С3-С10карбоциклическую группу, например, С3-С8циклоалкил, фенил, инданил или нафтил, прежде всего фенил.
R6 и R8 предпочтительно означают незамещенные С3-С8карбоциклические группы. Однако если R6 или R8 означает С3-С15карбоциклическую группу, которая является замещенной, то такая группа предпочтительно замещена в одном, двух или трех положениях одной или более группами галоген (прежде всего фтор), циано, гидрокси, амино, нитро, карбокси, C1-С10алкил, C1-С10галогеналкил, C1-С10алкокси, C1-С10алкилкарбонил, C1-С10алкилсульфонил, -SO2NH2, -СОО-(С6-С10арил), -СОО-(С7-С15аралкил), причем С3-С15карбоциклическая группа и 5-12-членная гетероциклическая группа содержат в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы.
Если R1, R3, R6 или R8 означает замещенную С3-С15карбоциклическую группу, то такая группа предпочтительно замещена в одном, двух или трех положениях незамещенным фенилом.
Если R1, R3, R6 или R8 означает замещенную С3-С15карбоциклическую группу, замещенную галогеном, то такая группа предпочтительно замещена в одном, двух или трех положениях фтором, хлором или бромом.
Если R1, R3, R6 или R8 означает С3-С15карбоциклическую группу, которая замещена C1-С10галогеналкилом, то такая группа предпочтительно замещена в одном, двух или трех положениях С1-С4 галогеналкилом.
Если R1, R3, R6 или R8 означает С3-С15карбоциклическую группу, замещенную C1-С10алкилкарбонилом, то такая группа предпочтительно замещена в одном, двух или трех положениях С1-С4алкилкарбонилом.
Если R1, R3, R6 или R8 означает С3-С15-карбоциклическую группу, замещенную группой C1-С10алкилсульфонил, то такая группа предпочтительно замещена в одном, двух или трех положениях группой С1-С4алкилсульфонил.
Если R1, R3, R6 или R8 означает С3-С15карбоциклическую группу, замещенную группой -СОО-(С6-С10арил), то такая группа предпочтительно замещена в одном, двух или трех положениях группой -СОО-(С6-С8арил), прежде всего -СОО-фенил.
Если R1, R3, R6 или R8 означает С3-С15карбоциклическую группу, замещенную группой -СОО-(С7-С15аралкил), то такая группа предпочтительно замещена в одном, двух или трех положениях группой -СОО-(С7-С10аралкил), прежде всего -СОО-(С1-С4алкилфенил).
Если R1 или R3 означает 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы, то R1 или R3 предпочтительно означает 5-9-членную гетероциклическую группу, например, моногетероциклическую группу, такую как фурил, пирролил, пирролидинил, пиразолил, имидазолил, триазолил, тетразолил, тиенил, тиадиазолил, изотиазолил, оксадиазолил, пиридинил, оксазолил, изоксазолил, пиперидинил, пиридинил, пиразинил, пиридазинил, пиримидинил, пиперазинил, морфолинил, триазинил, оксазинил или тиазолил, или бигетероциклическую группу, такую как бензазолил, бензимидазолил, индазолил и бензотиазолил. Если R1 или R3 означает 5-9-членную гетероциклическую группу, то такая группа предпочтительно означает фурил, пирролил, триазолил, тиенил, тиадиазолил, оксазолил, изоксазолил, пиперидинил, пиридинил, пиразинил, бензазолил, бензимидазолил, индазолил или бензотиазолил, прежде всего тиенил. 5-12-членная гетероциклическая группа незамещена или замещена, например, одним, двумя, тремя или четырьмя заместителями, выбранными из группы, включающей галоген, циано, оксо, гидрокси, карбокси, нитро, C1-С10алкил, C1-С10алкилкарбонил и C1-С10алкокси, необязательно замещенный аминокарбонилом. Однако если R1 или R3 означает 5-12-членную гетероциклическую группу, то такая группа, прежде всего, означает незамещенный тиенил.
Если R6 или R7 означает 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы, то такая группа предпочтительно означает 5-9-членную гетероциклическую группу, например, моногетероциклическую группу, такую как фурил, пирролил, пирролидинил, пиразолил, имидазолил, триазолил, тетразолил, тиенил, тиадиазолил, изотиазолил, оксадиазолил, пиридинил, оксазолил, изоксазолил, пиперидинил, пиридинил, пиразинил, пиридазинил, пиримидинил, пиперазинил, морфолинил, триазинил, оксазинил или тиазолил, или бигетероциклическую группу, такую как бензазолил, бензимидазолил, индазолил и бензотиазолил. Если R6 или R7 означает 5-9-членную гетероциклическую группу, то такая группа предпочтительно означает фурил, пирролил, триазолил, тиенил, тиадиазолил, оксазолил, изоксазолил, пиперидинил, пиридинил, пиразинил, бензазолил, бензимидазолил, индазолил или бензотиазолил, прежде всего тиенил. 5-12-членная гетероциклическая группа незамещена или замещена, например, одним, двумя, тремя или четырьмя заместителями, выбранными из группы, включающей галоген, циано, оксо, гидрокси, карбокси, нитро, C1-С10алкил, C1-С10алкилкарбонил и C1-С10алкокси, необязательно замещенный аминокарбонилом. Однако если R6 или R7 означает 5-12-членную гетероциклическую группу, то такая группа наиболее предпочтительно означает пиразинил, изоксазолил, пиридазинил, триазинил или пиримидинил, прежде всего пиразин-2-ил, изоксазол-3-ил, 5-метилизоксазол-3-ил, пиридазин-3-ил, [1,3,5]триазин-2-ил или пиримидин-4-ил.
Если не указано иное, подразумевается, что термин «включать» или его варианты, такие как «включает» или «включающий», используемый в описании заявки и в пунктах формулы изобретения, означает включение указанного целого числа, или стадии, или группы целых чисел или стадий, а не исключение любого другого целого числа, или стадии, или группы целых чисел или стадий.
Предпочтительные соединения включают соединения формулы I в форме соли или цвиттериона, в которых
R1 и R3 каждый независимо означает С3-С15карбоциклическую группу или 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы,
R2 означает гидрокси,
R4 означает С1-С4алкил,
R5 означает С1алкил, замещенный группой -CO-NH-R6,
R6 означает 5-12-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы.
Более предпочтительные соединения включают соединения формулы I в форме соли или цвиттериона, в которых
R1 и R3 каждый независимо означает С3-С10карбоциклическую группу или 5-9-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы,
R2 означает гидрокси,
R4 означает С1-С4алкил, предпочтительно метил,
R5 означает С1алкил, замещенный группой -CO-NH-R6,
R6 означает 5-9-членную гетероциклическую группу, содержащую в цикле по меньшей мере один гетероатом, выбранный из атомов азота, кислорода и серы, предпочтительно пиразинил, изоксазолил или пиридазинил.
Соединения формулы I представляют собой соли четвертичного аммонийного основания. Пригодные противоионы являются фармацевтически приемлемыми противоионами, включающими, например, фторид, хлорид, бромид, йодид, нитрат, сульфат, фосфат, формиат, ацетат, трифторацетат, пропионат, бутират, лактат, цитрат, тартрат, малат, малеат, сукцинат, бензоат, пара-хлорбензоат, дифенилацетат или трифенилацетат, орто-гидроксибензоат, пара-гидроксибензоат, 1-гидроксинафталин-2-карбоксилат, 3-гидроксинафталин-2-карбоксилат, метансульфонат и бензолсульфонат.
Соединения формулы I, содержащие основные группы, могут образовывать кислотно-аддитивные соли, прежде всего фармацевтически приемлемые кислотно-аддитивные соли. Фармацевтически приемлемые кислотно-аддитивные соли соединения формулы I включают соли неорганических кислот, например, галоидводородных кислот, таких как фтористоводородная кислота, хлористоводородная кислота, бромистоводородная кислота или йодистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, и органических кислот, например, алифатических монокарбоновых кислот, таких как муравьиная кислота, уксусная кислота, трифторуксусная кислота, пропионовая кислота и масляная кислота, алифатических гидроксикислот, таких как молочная кислота, лимонная кислота, винная кислота или яблочная кислота, дикарбоновых кислот, таких как малеиновая кислота или янтарная кислота, ароматических карбоновых кислот, таких как бензойная кислота, пара-хлорбензойная кислота, дифенилуксусная кислота или трифенилуксусная кислота, ароматических гидроксикислот, таких как орто-гидроксибензойная кислота, пара-гидроксибензойная кислота, 1-гидроксинафталин-2-карбоновая или 3-гидроксинафталин-2-карбоновая кислота, и сульфокислот, таких как метансульфоновая кислота или бензолсульфоновая кислота. Указанные соли получают из соединений формулы I известными методами.
Соединения формулы I, содержащие кислотные группы, например, карбоксильные группы, могут также образовывать соли оснований, прежде всего фармацевтически приемлемых оснований, например, известных оснований. Пригодные соли включают соли металлов, прежде всего соли щелочных или щелочно-земельных металлов, такие как соли натрия, калия, магния или кальция, или соли аммония или фармацевтически приемлемых органических аминов или гетероциклических оснований, таких как этаноламины, бензиламины или пиридин. Указанные соли получают из соединений формулы I известными методами.
Соединения по изобретению включают по меньшей мере один хиральный центр и, следовательно, могут присутствовать в форме индивидуальных оптически активных изомерных форм или их смесей, например рацемических или диастереомерных смесей. Настоящее изобретение включает индивидуальные оптически активные R и S изомеры, а также их смеси, например рацемические или диастереомерные смеси. Более предпочтительные соединения по изобретению являются индивидуальными изомерами, энантиомерами или диастереоизомерами. Неожиданно было установлено, что указанные индивидуальные изомеры являются наиболее эффективным компонентом выбранной смеси и неожиданно могут обеспечить более продолжительное связывание с рецептором М3 и, следовательно, являются агентами доставки с пролонгированным действием, что, прежде всего, является пригодным для введения в виде однократной дозы.
Более предпочтительные соединения по настоящему изобретению описаны ниже в разделе Примеры.
Примеры более предпочтительных соединений формулы I в форме соли или цвиттериона включают также следующие соединения:
(R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиний,
(R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-[(5-метилизоксазол-3-илкарбамоил)метил]пирролидиний,
(R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-([1,3,5]триазин-2-илкарбамоилметил)пирролидиний,
(R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-(пиримидин-4-илкарбамоилметил)пирролидиний,
(R)-3-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-[(5-метилизоксазол-3-илкарбамоил)метил]пирролидиний,
(R)-3-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиримидин-4-илкарбамоилметил)пирролидиний,
(R)-3-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-([1,3,5]триазин-2-илкарбамоилметил)пирролидиний,
(R)-3-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-[(5-метилизоксазол-3-илкарбамоил)метил]пирролидиний,
(R)-3-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиримидин-4-илкарбамоилметил)пирролидиний,
(R)-3-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-([1,3,5]триазин-2-илкарбамоилметил)пирролидиний,
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-метил-1-[(5-метилизоксазол-3-илкарбамоил)метил]пирролидиний,
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-метил-1-(пиримидин-4-илкарбамоилметил)пирролидиний,
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-метил-1-([1,3,5]триазин-2-илкарбамоилметил)пирролидиний,
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиний,
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиний, и
(R)-3-(9-гидрокси-9Н-флуорен-9-карбонилокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиний.
Изобретение также относится к способу получения соединения формулы I, заключающемуся в том, что
(1) (А) соединение формулы II
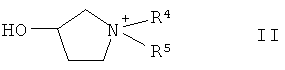
или его натриевая соль, где R4 и R5 имеют значения, указанные выше, взаимодействует с соединением формулы III

или с его эфиробразующим производным производным, где R1, R2 и R3 имеют значения, указанные выше, или (В) соединение формулы IV
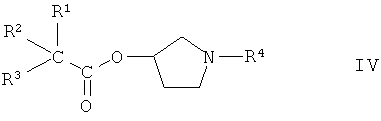
или его производное с защитной группой, где R1, R2, R3 и R4 имеют значения, указанные выше, взаимодействует с соединением формулы V

где R5 имеет значения, указанные выше, а Х означает хлор, бром или йод, и (2) продукт выделяют в форме соли или цвиттериона.
Способ по варианту (А) проводят по известным методикам взаимодействия гидроксисоединений или их натриевых солей с карбоновыми кислотами или их эфиробразующими производными производными, такими как галоидангидриды, или аналогично тому, как описано ниже в разделе Примеры. Реакцию между гидроксихинуклидином и карбоновой кислотой обычно проводят в органическом растворителе, например, диметилформамиде (ДМФА), в присутствии конденсирующего агента, например, 1,1′-карбонилдиимидазола (CDI), предпочтительно в атмосфере инертного газа, например, аргона. Пригодная температура реакционной смеси составляет от 0°С до 60°С, предпочтительно от 30°С до 50°С, прежде всего приблизительно 40°С.
Способ по варианту (В) проводят по известным методикам взаимодействия насыщенных гетероциклических аминов с галогенидами или аналогично тому, как описано ниже в разделе Примеры. Реакцию обычно проводят в органическом растворителе, например, диметилсульфоксиде, диметилформамиде, простом эфире, ацетонитриле или ацетоне. Реакцию проводят при температуре 20°С до 120°С, обычно от комнатной температуры до 80°С.
Соединения формулы II или III известны или их можно получить по известным методикам или аналогично тому, как описано в разделе Примеры.
Соединения формулы IV могут существовать в виде индивидуальных оптически активных изомерных форм или их смесей, например, в виде рацемических или диастереомерных смесей. Предпочтительными соединениями формулы IV являются соединения формулы IVa или IVb

или
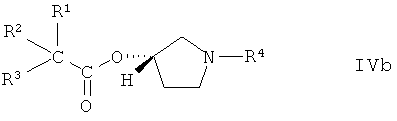
или их производные, содержащие защитную группу, где R1, R2, R3 и R4 имеют значения, указанные выше.
Если соединение формулы IV является индивидуальным энантиомером или является ахиральным, то при алкилировании третичного амина получают соединение формулы I в виде смеси двух диастереоизомеров. Указанные изомеры разделяют известными методами, например, фракционной кристаллизацией или хроматографией на колонке.
Соединения формулы IV известны или их можно получить по реакции соединения формулы VI
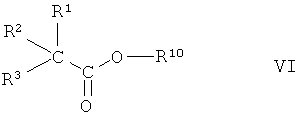
или его защищенной формы, где R1, R2 и R3 имеют значения, указанные выше, а R10 означает С1-С4алкил, с соединением формулы VII

где R4 имеет значения, указанные выше. Реакцию проводят с использованием известных методик взаимодействия эфиров карбоновых кислот со спиртами или аналогично тому, как описано в разделе Примеры. Обычно реакцию проводят в органическом растворителе, например, циклогексане или толуоле, предпочтительно в присутствии щелочного металла, например, натрия, в атмосфере инертного газа, такого как аргон. Реакцию проводят при температуре от 40°С до 120°С, предпочтительно при кипячении с обратным холодильником.
Соединения формулы IV, где R2 означает гидроксил, получают по реакции соединения формулы VIII
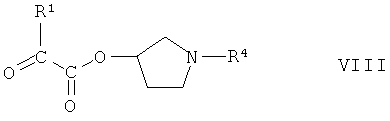
или его защищенной формы, где R1 и R4 имеют значения, указанные выше, с соединением формулы IX

где R3 имеет значения, указанные выше, а Х означает хлор, бром или йод.
Соединения формулы V или VI известны или их можно получить известными методами или аналогично тому, как описано ниже в разделе Примеры.
Соединения формулы VII известны или их можно получить алкилированием соответствующего вторичного амина. Например, соединения формулы VII, где R4 означает метил, получают по реакции соединения формулы Х
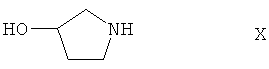
с формальдегидом в присутствии муравьиной кислоты. Обычно реакцию проводят в растворителе, например в воде, при температуре от 40°С до 120°С, предпочтительно при приблизительно 80°С.
Соединения формулы VIII получают по реакции соединения формулы VII, где R4 имеет значения, указанные выше, с соединением формулы XI
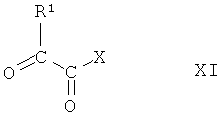
где R1 имеет значения, указанные выше, а Х означает хлор, бром или йод.
Соединения формул IX, Х или XI известны или их можно получить известными методами или аналогично тому, как описано ниже в разделе Примеры.
При ссылке на защищенные функциональные группы или защитные группы подразумевается, что защитные группы выбирают в соответствии с природой функциональной группы, например, как описано в монографии Protective Groups in Organic Synthesis, T.W.Greene и P.G.M.Wuts, John Wiley & Sons Inc, Third Edition (1999), где приводятся методики, пригодные для замены защитных групп на атом водорода.
Соединения формулы I представляют собой соли четвертичного аммония и их можно превращать в другие соли с использованием ионообменной хроматографии. Соединения получают в форме гидратов или сольватов, содержащих растворитель, используемый при кристаллизации. Соединения формулы I выделяют из реакционной смеси и очищают известными методами. Соединения выделяют в виде диастереомерных смесей, однако в большинстве случаев соединения предпочтительно используют в составе фармацевтических композиций по изобретению в виде индивидуальных энантиомеров или диастереоизомеров.
Соединения формулы I в форме фармацевтически приемлемой соли или цвиттериона, обозначаемые ниже по тексту как агенты по изобретению, используются в качестве лекарственных препаратов. Соответственно, в изобретении предлагается также соединение формулы I в форме фармацевтически приемлемой соли или цвиттериона для применения в качестве лекарственного препарата. Агенты по изобретению являются антагонистами мускаринового рецептора, прежде всего антагонистами мускаринового рецептора М3, действуя в качестве ингибиторов бронхостеноза.
Сродство (Ki) агентов по изобретению к мускариновому ацетилхолиновому рецептору М3 человека определяют анализом конкурентного связывания на фильтре с использованием радиоактивного антагониста [3Н] н-метилскополаминметилхлорида (NMS).
Мембранную фракцию получали из клеток СНО, стабильно трансфектированных рецептором М3 человека, помещали в планшет по 10 мкг белка в лунку и инкубировали с агентами по изобретению при серийном разведении и [3H]NMS при концентрации Kd (0,25 нМ) в буферном растворе для анализа (20 мМ HEPES, 1 мМ MgCl2, pH 7,4) при комнатной температуре в течение 17 ч. А анализ проводили в конечном объеме 250 мкл в присутствии диметилсульфоксида при конечной концентрации 1%. Общее связывание [3H]NMS определяли в отсутствие агентов по изобретению в соответствующем объеме буферного раствора для анализа. Неспецифическое связывание [3Н]NMS определяли в присутствии 300 нМ ипратропийбромида. После инкубации мембранные фракции переносили на планшет для фильтрования Unifilter™ GF/B, содержащий 0,05% полиэтиленимин, с использованием сборщика Brandel™ 9600. Планшеты для фильтрования сушили в течение 2 ч при 35°С, добавляли сцинтиллятор Microscint™ 'О' и регистрировали на планшет-ридере Packard Topcount™ по числу импульсов 3Н. Все значения IC50 рассчитывали с использованием программы XL-Fit, а значения Ki определяли с использованием коррекции Ченга-Прусоффа (Cheng Y., Prusoff W.H., Biochem. Pharmacol., 22 3099-3109(1973)).
По данным указанного анализа соединения, указанные в примерах, характеризовались значениями IC50 менее 1 мкМ.
Благодаря ингибированию связывания ацетилхолина с мускариновыми рецепторами М3 агенты по изобретению могут использоваться при лечении состояний, опосредованных мускариновым рецептором М3, прежде всего состояний, ассоциированных с повышенным парасимпатическим тонусом, приводящим, например, к избыточной железистой секреции или сокращению гладкой мускулатуры. Лечение по изобретению является симптоматическим или профилактическим.
Благодаря наличию антимускариновой активности агенты по изобретению можно использовать для релаксации бронхиальной гладкой мускулатуры и для снижения интенсивности бронхостеноза, который оценивают на моделях, таких как плетизмографические модели in vivo, как описано в статьях Chong и др., J. Pharmacol. Toxicol. Methods, 39, 163 (1998), Hammelmann и др. Am. J. Respir. Crit. Care Med., 156, 766 (1997), и на аналогичных моделях. Следовательно, агенты по изобретению можно использовать при лечении обструктивных или воспалительных заболеваний дыхательных путей. Благодаря продолжительному действию агенты по изобретению можно вводить при лечении таких заболеваний однократно. Кроме того, агенты по изобретению обычно обладают слабыми побочными действиями, обычно характерными для β2-агонистов, такими как тахикардия, тремор и беспокойное состояние, и, следовательно, такие агенты пригодны для применения при неотложной терапии, а также профилактической терапии обструктивных или воспалительных заболеваний дыхательных путей.
Воспалительные или обструктивные заболевания дыхательных путей, в отношении которых может применяться настоящее изобретение, включают астму любого типа и любой этиологии, включая врожденную (неаллергическую) астму и приобретенную (аллергическую) астму. Подразумевается также, что лечение астмы включает лечение субъектов, например детей в возрасте младше 4 или 5 лет, у которых наблюдается симптоматическое свистящее дыхание или с диагнозом "дети с одышкой", и которые относятся к категории пациентов первостепенного медицинского значения, и которых в настоящее время относят к астматикам в ранней фазе. Такое астматическое состояние называют "синдромом детей со стерторозным дыханием".
Профилактическое действие при лечении астмы наглядно проявляется в снижении частоты или тяжести симптоматических приступов, например острых астматических приступов или бронхостеноза, в улучшении функционирования легких или повышении гиперреактивности дыхательных путей. Кроме того, профилактическое действие проявляется как снижение необходимости в другом симптоматическом лечении, предназначенном для подавления или остановки приступов астмы при их наличии, например, необходимости в противовоспалительном (например, с применением кортикостероидов) или бронхолитическом лечении. Профилактика при лечении астмы, прежде всего, необходима для субъектов, подверженных "утренним приступам". "Утренние приступы" являются известным астматическим синдромом, свойственным большинству астматиков, который характеризуется астматическими приступами, например, между приблизительно 4 и 6 утра, т.е. через значительный промежуток времени после любого предшествующего введения симптоматического астматического терапевтического средства.
Другие воспалительные или обструктивные заболевания и состояния дыхательных путей, в отношении которых может применяться настоящее изобретение, включают острый респираторный дистресс-синдром у взрослых пациентов (ARDS), хроническое обструктивое заболевание легких или дыхательных путей (COPD или COAD), включая хронический бронхит, или ассоциированную с ним одышку, эмфизему, а также обострение гиперреактивности дыхательных путей вследствие применения других лекарственных средств, прежде всего другого ингаляционного медикаментозного лечения. Настоящее изобретение можно также использовать при лечении бронхитов любого типа или этиологии, включая, например, острый, арахноидальный, катаральный, крупозный, хронический или гнойный туберкулезный бронхит. Другие воспалительные или обструктивные заболевания дыхательных путей, в отношении которых может применяться настоящее изобретение, включают пневмокониоз (воспалительное заболевание легких, которое обычно связано с профессиональной деятельностью, сопровождающееся в большинстве случаев хронической или острой обструкцией дыхательных путей, а также возникающее при повторном вдыхании пыли) любого типа или этиологии, включая, например, алюминоз, антракоз, азбестоз, халикоз, кистозный фиброз, птилоз, сидероз, силикоз, табакоз и биссиноз.
Благодаря антимускариновой активности агенты по изобретению можно использовать при лечении состояния, требующего расслабления гладкой мускулатуры матки, мочевого пузыря или сосудистой системы. Таким образом, их можно использовать для предотвращения или снижения интенсивности болей при преждевременных родах. Указанные агенты можно также использовать при лечении хронической и острой крапивницы, псориаза, аллергического конъюнктивита, актинита, ринита, включая аллергический ринит, мастоцитоза, нарушений мочеиспускания, таких как недержание мочи (прежде всего, вызываемого повышенно активным мочевым пузырем), поллакиурия, нейрогенный или нестабильный мочевой пузырь, цитоспазм и хронический цистит; нарушений желудочно-кишечного тракта, таких как синдром раздраженной толстой кишки, спастический колит, дивертикулит и пептическая язва; и сердечно-сосудистых нарушений, таких как вагусно-индуцируемая синусная брадикардия, в также глазных заболеваний.
Агенты по изобретению можно также использовать в качестве комбинированных терапевтических агентов для применения в сочетании с другими лекарственными препаратами, такими как противовоспалительные, бронхолитические, антигистаминные, противоотечные или противокашлевые лекарственные средства, прежде всего при лечении обструктивных или воспалительных заболеваний дыхательных путей, таких как заболевания, упомянутые выше, например, в качестве средств, потенцирующих терапевтическую активность указанных лекарственных препаратов, или в качестве средств, предназначенных для снижения требуемой дозы или возможных побочных действий указанных лекарственных препаратов. Агент по изобретению смешивают с одним или более другими лекарственными средствами в фиксированной фармацевтической композиции или его вводят отдельно перед введением другого лекарственннного соединения, одновременно с ним или после него. Таким образом, изобретение включает комбинацию агента по изобретению, описанного выше, с противовоспалительным, бронхолитическим, антигистаминным, противоотечным или противокашлевым лекарственным средством, причем указанный агент по изобретению и указанное лекарственное средство могут находиться в одной и той же или в различных фармацевтических композициях.
Пригодные противовоспалительные средства включают стероиды, прежде всего глюкокортикостероиды, такие как будезонид, дипропионат бекламетазона, пропионат флутиказона, циклезонид, или фуроат мометазона, или стероиды, описанные в WO 02/88167, WO 02/12266, WO 02/100879, WO 02/00679 (прежде всего в примерах 3, 11, 14, 17, 19, 26, 34, 37, 39, 51, 60, 67, 72, 73, 90, 99 и 101), WO 03/35668, WO 03/48181, WO 03/62259, WO 03/64445, WO 03/72592, WO 04/39827 и WO 04/66920, нестероидные агонисты рецептора глюкокортикоидов, такие, как описанные в DE 10261874, WO 00/00531, WO 02/10143, WO 03/82280, WO 03/82787, WO 03/86294, WO 03/104195, WO 03/101932, WO 04/05229, WO 04/18429, WO 04/19935 и WO 04/26248, антагонисты LTD4, такие как монтелукаст и зафирлукаст, ингибиторы PDE4, такие как циломиласт (Ariflo®, фирма GlaxoSmithKline), рофлумиласт (фирма Byk Gulden),V-11294A (фирма Napp), BAY19-8004 (фирма Bayer), SCH-351591 (фирма Schering-Plough), арофиллин (фирма Almirall Prodesfarma), PD189659/PD168787 (фирма Parke-Davis), AWD-12-281 (фирма Asta Medica), CDC-801 (фирма Celgene), SelCID(TM) CC-10004 (фирма Celgene), VM554/UM565 (фирма Vernalis), T-440 (фирма Tanabe), KW-4490 (фирма Kyowa Hakko Kogyo), и агенты, описанные в WO 92/19594, WO 93/19749, WO 93/19750, WO 93/19751, WO 98/18796, WO 99/16766, WO 01/13953, WO 03/39544, WO 03/104204, WO 03/104205, WO 04/000814, WO 04/000839, WO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/018431, WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944, WO 04/019945, WO 04/045607 и WO 04/037805, WO 04/063197, WO 04/103998, WO 04/111044, WO 05/012252, WO 05/012253, WO 05/013995, WO 05/030725, WO 05/030212, WO 05/087744, WO 05/087745, WO 05/087749 и WO 05/090345, агонисты А2А, такие, как описанные в ЕР 1052264, ЕР 1241176, ЕР 409595А2, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319, WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264, WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130, WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462 и WO 03/086408, WO 04/039762, WO 04/039766, WO 04/045618 и WO 04/046083, и антагонисты A2B, такие, как описанные в WO 02/42298.
Агенты по изобретению можно использовать в комбинированной терапии в сочетании с антагонистами рецептора хемокина, блокаторами кальциевых каналов, антагонистами α-адренорецептора, агонистами допамина, антагонистами эндотелина, антагонистами вещества Р, ингибиторами 5-LO, антагонистами VLA-4 и теофиллином.
Агенты по изобретению можно также использовать в качестве комбинированных терапевтических агентов для применения в сочетании с бронхолитическими средствами, прежде всего, агонистами β2-адренорецептора. Пригодные агонисты β2-адренорецептора включают албутерол (салбутамол), метапротеренол, тербуталин, салметерол, фенотерол, прокатерол и, прежде всего, формотерол, кармотерол и их фармацевтически приемлемые соли, и соединения (в свободной форме, в форме соли или сольвата) формулы I, описанные в WO 0075114, включенной в описание заявки в качестве ссылки, предпочтительно соединения, описанные в примерах, прежде всего соединение формулы
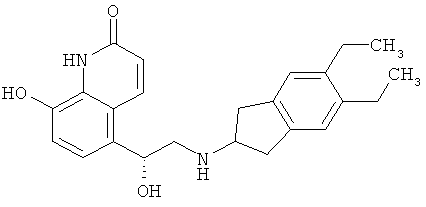
и его фармацевтически приемлемые соли, а также соединения (в свободной форме, в форме соли или сольвата) формулы I, описанные в WO 04/16601, а также соединения, описанные в ЕР 147719, ЕР 1440966, ЕР 1460064, ЕР 1477167, JP 05025045, WO 93/18007, WO 99/64035, US 2002/0055651, US 2004/0242622, US 2004/0229904, US 2005/0133417, US 2005/5159448, WO 01/42193, WO 01/83462, WO 02/66422, WO 02/ 70490, WO 02/76933, WO 03/24439, WO 03/42160, WO 03/42164, WO 03/72539, WO 03/91204, WO 03/99764, WO 04/16578, WO 04/22547, WO 04/32921, WO 04/33412, WO 04/37768, WO 04/37773, WO 04/37807, WO 04/39762, WO 04/39766, WO 04/45618, WO 04/46083, WO 04/80964, WO 04/087142, WO 04/089892, WO 04/108675, WO 04/108676, WO 05/033121, WO 05/040103, WO 05/044787, WO 05/058867, WO 05/065650, WO 05/066140 и WO 05/07908.
Пригодные антигистаминные средства для комбинированной терапии включают гидрохлорид цетиризина, ацетаминофен, фумарат клемастина, прометазин, лоратидин, деслоратидин, дифенгидрамин и гидрохлорид фексофенадина.
Комбинации агентов по изобретению с одним или более агонистами β2-адренорецептора, стероидами, ингибиторами PDE4, агонистами A2A, антагонистами A2B и антагонистами LTD4 можно использовать, например, при лечении заболеваний дыхательных путей, включая астму и прежде всего COPD. Предпочтительные тройные комбинации включают агент по изобретению, агонист β2-адренорецептора и стероид.
В соответствии с вышеизложенным в настоящем изобретении предлагается также способ лечения обструктивного или воспалительного заболевания дыхательных путей, который включает введение субъекту, прежде всего человеку, который нуждается в лечении, соединения формулы I или его фармацевтически приемлемой соли или сольвата, указанного выше. Другим объектом изобретения является соединение формулы I или его фармацевтически приемлемая соль или сольват, описанное выше, для применения при получении лекарственного средства, предназначенного для лечения обструктивного или воспалительного заболевания дыхательных путей.
Агенты по изобретению можно вводить любым обычным способом, например, перорально, например, в форме таблетки или капсулы, парентерально, например, втутривенно, местно на кожу, например, при лечении псориаза, интраназально, например, при лечении сенной лихорадки, или предпочтительно ингаляцией, прежде всего при лечении обструктивных или воспалительных заболеваний дыхательных путей. Прежде всего, агенты по изобретению вводят в форме состава для ингаляции для лечения COPD и астмы.
Еще одним объектом изобретения является также фармацевтическая композиция, включающая соединение формулы I в свободной форме или в форме его фармацевтически приемлемой соли или сольвата, необязательно в смеси с фармацевтически приемлемым разбавителем или носителем. Такие композиции получают с использованием обычных разбавителей или эксципиентов известными в фармакологии методами. Таким образом, формы для перорального введения включают таблетки и капсулы. Формы для местного введения включают кремы, мази, гели или системы трансдермальной доставки, например, пластыри. Композиции для ингаляции включают аэрозоль или другие распыляемые составы или порошкообразные составы.
Если композиция включает аэрозольный состав, то такая композиция предпочтительно содержит фторуглеводородный пропеллент (HFA), такой как HFA134a, или HFA227, или их смесь, и может содержать один или более сорастворителей, известных в данной области техники, таких как этанол (до 20 мас.%) и/или один или более ПАВ, таких как олеиновая кислота или триолеат сорбита, и/или один или более наполнителей, таких как лактоза. Если композиция включает порошкообразный состав, то такая композиция предпочтительно содержит, например, соединение формулы I в виде частиц диаметром до 10 мкм, необязательно в смеси с разбавителем или носителем, таким как лактоза, с требуемым размером частиц и соединением, которое защищает продукт от повреждения за счет увлажнения, таким как стеарат магния, например, от 0,05 до 2,0%. Если композиция включает распыляемый состав, то такая композиция предпочтительно содержит, например, соединение формулы I, растворенное или суспендированное в носителе, содержащем воду, сорастворитель, такой как этанол или пропиленгликоль, и стабилизатор, который может означат ПАВ.
Изобретение также включает (А) соединение формулы I, указанное выше, в свободной форме или в форме его фармацевтически приемлемой соли или сольвата в форме для ингаляции, (В) лекарственное средство для ингаляции, включающее такое соединение в форме для ингаляции в смеси с фармацевтически приемлемым носителем в ингалируемой форме, (С) фармацевтический продукт, включающий такое соединение в ингалируемой форме вместе с ингалятором, и (D) ингалятор, содержащий такое соединение в ингалируемой форме.
Дозы, используемые при осуществлении изобретения, изменяются в зависимости, например, от конкретного состояния, подлежащего лечению, требуемого результата, и способа введения. В общем случае, пригодная суточная доза для введения ингаляцией составляет от 0,0001 до 30 мг/кг, обычно от 0,01 до 10 мг на одного пациента, при пероральном введении пригодные суточные дозы составляют от 0,01 до 100 мг/кг.
Изобретение иллюстрируется следующими примерами.
Примеры
Все соединения, описанные в примерах, сначала выделяли в виде смесей диастереоизомеров по четвертичному атому азота. Индивидуальные диастереоизомеры, указанные в примерах, выделяли фракционной кристаллизацией таких смесей. Стереохимическую структуру таких индивидуальных изомеров определяли методом ЯМР и/или рентгеноструктурным анализом.
Более предпочтительные соединения формулы I включают соединения формулы XII

где Т имеет значения, указанные ниже в таблице 1, способ получения описан ниже. Все соединения являются солями аммония. В таблице 1 приведены данные масс-спектрометрии. Соответствующий противоион указан в способе получения.

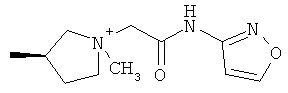

Другие более предпочтительные соединения формулы I включают соединения формулы XIII

где Т имеет значения, указанные ниже в таблице 2, способ получения описан ниже. Все соединения являются солями аммония. В таблице 2 приведены данные масс-спектрометрии. Соответствующий противоион указан в способе получения.
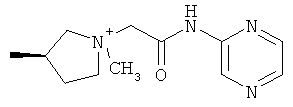


Еще одни более предпочтительные соединения формулы I включают соединения формулы XIV
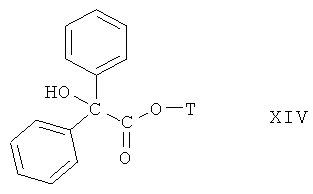
где Т имеет значения, указанные ниже в таблице 3, способ получения описан ниже. Все соединения являются солями аммония. В таблице 3 приведены данные масс-спектрометрии. Соответствующий противоион указан в способе получения.


Получение промежуточных соединений
Список сокращений: ДХМ означает дихлорметан, ДМФА означает диметилформамид, ДМСО означает диметилсульфоксид, ТГФ означает тетрагидрофуран, ЖХВР жидкостная хроматография высокого разрешения, ЖХ-МС означает жидкостная хроматография/масс-спектрометрия, CDI означает 1,1'-карбонилдиимидазол.
Промежуточное соединение А
2-Бром-N-пиразин-2-илацетамид
В раствор аминопиразола (10 г, 105 ммолей) в ацетоне (100 мл) при перемешивании добавляли триэтиламин (16,1 мл, 115 ммолей), а затем охлаждали до 0-5°С на ледяной бане. В охлажденный раствор добавляли по каплям хлорангидрид бромуксусной кислоты (8,76 г, 105 ммолей) в ацетоне (10 мл). Охлажденную реакционную смесь перемешивали в течение 3 ч, а затем фильтровали. Растворитель удаляли в вакууме, остаток очищали хроматографией на силикагеле (элюент: градиент этилацетат/изогексан, от 2:1 до 100% этилацетата), при этом получали указанное в заголовке соединение.
Промежуточное соединение В
Бромид (1R/S,3R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния
В раствор 2-бром-N-пиразин-2-илацетамида (промежуточное соединение А, 3,0 г, 13,9 ммоля) в ацетонитриле (80 мл) добавляли (R)-гидроксиметилпирролидон (1,4 г, 13,9 ммоля). Полученную суспензию перемешивали при комнатной температуре в течение 3 ч, а затем фильтровали. Твердое вещество промывали ацетонитрилом и высушивали в вакууме в течение ночи, при этом получали указанное в заголовке соединение в виде твердого вещества коричневого цвета.
Промежуточное соединение С
2-Бром-N-изоксазол-3-илацетамид
В раствор бромангидрида бромуксусной кислоты (5,36 мл, 61,6 ммоля) в диэтиловом эфире (100 мл) при перемешинии при -40°С в течение 20 мин добавляли по каплям раствор 3-аминоизоксазола (5,0 мл, 67,0 ммолей) и триэтиламин (8,5 мл, 61,4 ммоля) в диэтиловом эфире (20 мл). Затем добавляли вторую порцию диэтилового эфира (50 мл) и смесь перемешивали в течение еще 3 ч. Реакционную смесь фильтровали и раствор промывали 1 М раствором карбоната натрия, 1 М соляной кислотой и солевым раствором, а затем концентрировали. Продукт очищали экспресс-хроматографией на колонке с силикагелем (элюент: этилацетат/изогексан, 4:7), при этом получали указанное в заголовке соединение в виде твердого вещества белого цвета.
Промежуточное соединение D
Бромид (1R/S,3R)-3-гидрокси-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния
Указанное в заголовке соединение получали аналогично тому, как описано при получении бромида (R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (промежуточное соединение В), при замене 2-бром-2-пиразин-2-илацетамида (промежуточное соединение А) на 2-бром-М-изоксазол-3-илацетамид (промежуточное соединение С).
Промежуточное соединение Е
2-Бром-N-пиридазин-3-илацетамид
Стадия Е1. Пиридазин-3-иламин
Суспензию 3-амино-6-хлорпиридина (5 г, 38,6 ммоля), 10% палладия на угле (0,45 г) в этаноле (200 мл) при перемешивании в атмосфере аргона трижды продували азотом, а затем выдерживали в атмосфере водорода в течение ночи. Затем смесь фильтровали через целит и растворитель удаляли в вакууме. Полученное твердое вещество растворяли в воде и подщелачивали до рН более 12 при добавлении 2 М раствора NaOH (20 мл). Растворитель удаляли в вакууме, полученное твердое вещество растирали в этилацетате, при этом получали указанное в заголовке соединение.
Стадия Е2. 2-Бром-N-пиридазин-3-илацетамид
В суспензию пиридазин-3-иламина (стадия Е1, 2,0 г, 21 ммоль), DIPEA (4,6 мл) в ДХМ (100 мл) при охлаждении (0°С) и перемешивании медленно добавляли раствор ангидрида бромуксусной кислоты (6,57 г, 25,2 ммоля) в ДХМ (20 мл). Реакционную смесь перемешивали при 0°С в течение 30 мин, а затем нагревали до комнатной температуры. Полученную суспензию фильтровали, остаток на фильтре промывали ДХМ и высушивали в вакууме, при этом получали указанное в заголовке соединение.
Промежуточное соединение F
Бромид (R)-3-гидрокси-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиния
В суспензию 2-бром-N-пиридазин-3-илацетамида (0,5 г, 2,31 ммоля) в ацетонитриле (10 мл) при перемешивании добавляли (R)-3-гидрокси-1-метилпирролидин (0,234 г, 2,31 ммоля). Суспензию перемешивали при комнатной температуре в течение 2 ч, а затем фильтровали, остаток на фильтре промывали ацетонитрилом, при этом получали указанное в заголовке соединение.
Примеры
Пример 1
Бромид (1R/S,3R)-3-(R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния
В раствор бромида (1R/S,3R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (промежуточное соединение В, 0,317 г, 1,0 ммоль) в ДМФА (3 мл) одной порцией добавляли гидрид натрия (0,08 г, 60% дисперсия в масле, 2,0 ммоля). Суспензию перемешивали при 40°С в течение 30 мин, при этом наблюдалось выделение газа. В другом сосуде в раствор циклогексилгидроксифенилуксусной кислоты в ДМФА (3 мл) одной порцией добавляли CDI (0,168 г, 1 ммоль), при этом наблюдалось выделение газа. Реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Полученное промежуточное соединение CDI добавляли в реакционный сосуд, содержащий натриевую соль бромида (1R/S,3R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния, и реакционную смесь перемешивали при 40°С в течение 1 ч. Растворитель удаляли в вакууме, остаток растворяли в воде (10 мл) и раствор подкисляли при добавлении 5% HBr (5 мл). Полученный маслообразный осадок экстрагировали этилацетатом (2×30 мл) и объединенные органические экстракты упаривали досуха. Неочищенный продукт очищали обращенно-фазовой хроматографией на колонке С-18 (элюент: вода +1% ТФУ/ацетонитрил+1% ТФУ), при этом получали указанное в заголовке соединение.
Пример 2
Бромид (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (пример 1), при замене бромида (1R/S,3R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (промежуточное соединение В) на бромид (1R/S,3R)-3-гидрокси-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния (промежуточное соединение D).
Пример 3
Бромид(1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (пример 1), при замене бромида (1R/S,3R)-3-гидрокси-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (промежуточное соединение В) на бромид (R)-3-гидрокси-1-метил-1-(пиридазин-3-илкарбамоилметил)-1-метилпирролидиния (промежуточное соединение F).
Пример 4
Бромид(1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (пример 1), при замене циклогексилгидроксифенилуксусной кислоты на циклопентилминдальную кислоту.
Пример 5
Бромид(1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилапетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния (QAX003, пример 2), при замене циклогексилгидроксифенилуксусной кислоты на циклопентилминдальную кислоту.
Пример 6
Бромид(1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-(1-пиридазин-3-илкарбамоилметил)пирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиния (пример 3), при замене циклогексилгидроксифенилуксусной кислоты на циклопентилминдальную кислоту.
Пример 7
Бромид (1R/S,3R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния (пример 1), при замене циклогексилгидроксифенилуксусной кислоты на бензиловую кислоту.
Пример 8
Бромид(1R/S,3R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния
Указанное соединение получали аналогично тому, как описано при получении бромида (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния (пример 2), при замене циклогексилгидроксифенилуксусной кислоты на бензиловую кислоту.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ МУСКАРИНОВЫХ РЕЦЕПТОРОВ М3 | 2005 |
|
RU2399620C2 |
| СОЛИ ЧЕТВЕРТИЧНОГО АММОНИЯ В КАЧЕСТВЕ АНТАГОНИСТОВ М3 | 2005 |
|
RU2394031C2 |
| КОМБИНАЦИИ ГЛИКОПИРРОЛАТА И АГОНИСТОВ В-2 АДРЕНОЦЕПТОРА | 2005 |
|
RU2388465C2 |
| ПРОИЗВОДНЫЕ 5-ГИДРОКСИБЕНЗОТИАЗОЛА В КАЧЕСТВЕ АГОНИСТОВ β-АДРЕНОРЕЦЕПТОРОВ | 2005 |
|
RU2402540C2 |
| ПРОИЗВОДНЫЕ БИЦИКЛО[2,2,1]ГЕПТ-7-ИЛАМИНА И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2442771C2 |
| ИНГИБИТОРЫ БЕТА-СЕКРЕТАЗЫ | 2016 |
|
RU2712272C2 |
| ПРЕДОТВРАЩАЮЩИЙ ПРЕЖДЕВРЕМЕННУЮ ОВУЛЯЦИЮ АГЕНТ | 2006 |
|
RU2419435C2 |
| КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ АГОНИСТ РЕЦЕПТОРА S1P И ИНГИБИТОР КИНАЗЫ JAK3 | 2005 |
|
RU2415678C2 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ АГЕНТОВ | 2006 |
|
RU2426733C2 |
| АЗОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОТИВОГРИБКОВАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ГРИБКОВОЙ ИНФЕКЦИИ | 1998 |
|
RU2189982C2 |
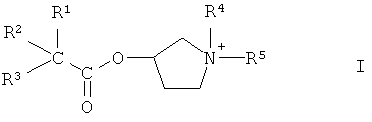
Изобретение относится к новым производным пирролидиния формулы I
в форме энантиомера и его фармацевтически приемлемой соли, где R1 и R3 каждый независимо означает циклопентил, циклогексил, фенил; R2 означает ОН; R4 означает С1-С4алкил; R5 означает С1алкил, замещенный группой -CO-NH-R6; R6 означает 5-членную ненасыщенную гетероциклическую группу, содержащую в цикле один атом N и один атом О, 6-членную гетероциклическую группу, содержащую в цикле два атома N. Соединения обладают способностью ингибировать связывание ацетилхолина с мускариновым рецептором МЗ, что позволяет использовать их в фармацевтической композиции. Описан способ их получения. 4 н. и 2 з.п. ф-лы, 3 табл.
1. Соединение формулы I
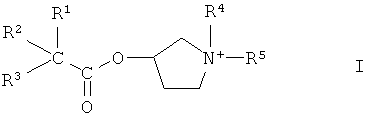
в форме энантиомера его фармацевтически приемлемой соли, где
R1 и R3 каждый независимо означает циклопентил, циклогексил или фенил,
R2 означает гидрокси,
R4 означает С1-С4алкил,
R5 означает С1алкил, замещенный группой -CO-NH-R6, и
R6 означает 5-членную ненасыщенную гетероциклическую группу, содержащую в цикле один атом азота и один атом кислорода или 6-членную ненасыщенную гетероциклическую группу, содержащую в цикле два атома азота.
2. Соединение по п.1, где R6 означает изоксазолил, пиразинил или пиридазинил.
3. Соединение по любому из предшествующих пунктов, выбранное из группы, включающей
бромид (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния,
бромид (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния,
бромид (1R/S,3R)-3-((R/S)-(2-циклогексил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиния,
бромид (1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния,
бромид (1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния,
бромид (1R/S,3R)-3-((R/S)-(2-циклопентил-2-гидрокси-2-фенилацетокси)-1-метил-1-(пиридазин-3-илкарбамоилметил)пирролидиния,
бромид (1R/S,3R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-метил-1-(пиразин-2-илкарбамоилметил)пирролидиния и
бромид (1R/S,3R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-метилпирролидиния.
4. Фармацевтическая композиция, обладающая способностью ингибировать связывание ацетилхолина с мускариновым рецептором М3, включающая в качестве активного ингредиента соединение по любому из пп.1-3 вместе с фармацевтически приемлемым разбавителем или носителем.
5. Применение соединения по любому из пп.1-3 для получения лекарственного препарата, обладающего способностью ингибировать связывание ацетилхолина с мускариновым рецептором М3.
6. Способ получения соединения формулы I по п.1, заключающийся в том, что
(1) (А) соединение формулы II в форме энантиомера

или его натриевую соль, где R4 и R5 имеют значения, указанные в п.1, вводят в реакцию с соединением формулы III

или его эфиробразующим производным, где R1, R2 и R3 имеют значения, указанные в п.1, и (2) выделяют продукт в форме его фармацевтически приемлемой соли.
| ЭНАНТИОМЕРНО ЧИСТЫЕ ОСНОВНЫЕ ЭФИРЫ АРИЛ-ЦИКЛОАЛКИЛГИДРОКСИКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В ЛЕКАРСТВЕННЫХ СРЕДСТВАХ | 1997 |
|
RU2238936C2 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| EP 1302458 A1, 10.07.2001. | |||
Авторы
Даты
2011-02-20—Публикация
2005-12-22—Подача