Изобретение относится к способу очистки и производства основных аминокислот, в частности к получению аргинина, лизина и гистидина из растворов низких концентраций, и может быть использовано в пищевой и фармацевтической промышленности, а также в анализе аминокислот как метод предварительного концентрирования.
Для аналитических целей часто необходимо концентрирование растворов с низким содержанием компонентов, лежащим на уровне и ниже предела обнаружения.
Для концентрирования растворов с малым содержанием аминокислот известен метод выпаривания (The determination of amino acids in sea water / Y.K.Chau, J.P.Riley // Deep Sea Research and Oceanographic Abstracts. - 1966. V.13, I.6. - P. 1115-1124), однако он связан с большими энергозатратами.
Известен способ очистки растворов белка и аминокислот методом электродиализа с добавлением в раствор сильного электролита (А.с. СССР №710568, B01D 13/02, опубл. 25.01.80), причем сильный электролит, не являющийся токсичным для организма, вводят в раствор после уменьшения концентрации минеральных ионов до 15-20% от начальной. Данный способ связан с существенными затратами реагентов.
Описан способ очистки аминокислот электродиализом с чередующимися катионообменными, анионообменными и биполярными мембранами (авт. свид. СССР №1685481, МПК B01D 61/00, опубл. 23.10.89). При этом в электродиализаторе образуются три типа камер: обессоливания (дилюатные), щелочные и кислотные. Биполярные мембраны используются с целью увеличения степени очистки и уменьшения потерь аминокислоты. Процесс осуществлен для β-аланина. Предложенный способ позволяет производить очистку аминокислот от минеральных ионов, но не пригоден для концентрирования раствора аминокислоты.
Описан способ получения L-лизина из лизинсодержащих растворов, включающий обработку рацемата разделяющим агентом с получением солей D- и L-лизина, удаление D-формы и разложение гидротартрата лизина методом электродиализа в электродиализаторе с чередующимися катионообменными и биполярными мембранами в интенсивном токовом режиме (12-18 мА/см2) с выделением чистого L-лизина (Пат. РФ №2223946, МПК С07С 227/34; 229/26, опубл. 20.02.2004). Предложенный способ позволяет производить выделение лизина из растворов его солей с разделяющим оптически активным агентом без использования концентрированных растворов кислот, но не предполагает концентрирования раствора аминокислоты.
Описан электродиализный способ очистки ряда аминокислот (U.S. Pat. №6531803 С12Р 13/04; C12P 13/08, опубл. 22.04.2003). Электродиализ раствора, содержащего лизин, проводили с применением биполярных мембран в две ступени. При этом процесс включал следующие стадии:
1) внесение исходного раствора в кислотный или щелочной контур трехконтурного электродиализатора с биполярными мембранами, при этом получали заряженные формы аминокислот; 2) внесение раствора, содержащего заряженную форму аминокислот, в дилюатный контур следующего трехконтурного электродиализатора с биполярными мембранами с получением аминокислоты в виде свободного основания в щелочном или кислотном контуре. Также разработан процесс для раствора, содержащего Gly, Ala, Val, Ser, Leu, Ileu, Glu, Gln, Pro, Tre, Tyr, Cys, Asp, Yrp, Lys, Arg, His. Недостатком указанного способа является его многостадийность.
Наиболее близким по совокупности признаков является описанный электродиализный способ получения основной аминокислоты (Пат. US №6800185, B01D 61/44, опубл. 05.10.2004) в электродиализаторе с чередующимися катионообменными и анионообменными мембранами, причем во время электродиализа к исходному раствору добавляют щелочной раствор, а также в электродиализаторе с чередованием только анионообменных мембран и добавлением щелочного раствора. Катионообменные мембраны содержали в качестве функциональных групп сульфо- и карбоксильные группы, в анионообменных мембранах функциональными группами являлись четвертичные и третичные амины. Применяли мембраны SELEMION AMV, SELEMION CMV производства Asahi Glass Co., а также ACIPLEX А-211, ACIPLEX А-201, ACIPLEX К-101 производства Asahi Kasei Co. Использовали электродиализаторы двух типов: 1) 22-камсрный электродиализатор "Micro Acilyzer G3" производства Asahi Kasei Co с чередующимися катионообменными и анионообменными мембранами с рабочей площадью мембран 400 см2; 2) электродиализатор "SELEMION ELECTRODIALYSER DU-06" производства Asahi Kasei Со с использованием только анионообменных мембран площадью 209 см2/лист. Исходный раствор, полученный в результате ферментации, содержал гидрохлорид лизина с концентрацией около 10% (мас.) и минеральные соли (сульфаты и хлориды щелочных металлов) с концентрацией не более 5% (мас.). Для поддержания рН в диапазоне от 7 до 10 к исходному раствору добавляли раствор аммиака с концентрацией 28%. Таким образом поддерживали рН в щелочной области для предотвращения переноса лизина. В процессе электродиализа исходный раствор подавался в секции обессоливания (дилюатные). Время процесса составляло 120-270 мин, скорость циркуляции растворов 35 л/ч. Сила тока составляла 1.0-5.0 А/дм2, напряжение на электродиализаторе 11.2-13.8 В. Степень извлечения лизина в процессе электродиализа составляла 92-94%, при этом удалялось 90-95% ионов щелочных металлов, 80-90% ионов аммония, 75-90% сульфатов и 95-97% хлоридов. После электродиализа раствор концентрировали отдувкой аммиака. Подобный процесс был проведен для аргинина и гистидина.
К недостаткам вышеизложенного способа относятся:
1. наличие дополнительных стадий введения и удаления вспомогательного реактива - корректора рН;
2. использование дополнительных реагентов;
3. необходимость удаления аммиака для получения чистого раствора аминокислоты связано с большими энергозатратами;
4. применение ионообменных мембран на основе слабокислотных и слабоосновных ионообменников (функциональные группы - карбоксильные, третичные амины) нерентабельно, т.к. они имеют более низкие числа переноса, чем мембраны, содержащие сульфогруппы и четвертичные аммониевые основания.
Технический результат: понижение энергоемкости и упрощение процесса выделения и концентрирования основных аминокислот путем исключения лишних стадий, отказ от использования дополнительных реагентов и мембран с низкими числами переноса.
Технический результат достигается тем, что способ концентрирования основных аминокислот электродиализом включает внесение исходного раствора, содержащего основную аминокислоту в низкой концентрации, в дилюатные секции элсктродиализатора с расположенными между электродами чередующимися катионообменными и биполярными мембранами, характеризующимися высокими числами переноса, при рН исходного раствора, равном рI соответствующей основной аминокислоты, перед началом процесса камеры концентрирования заполняют исходным раствором, а в электродные камеры подают раствор сульфат натрия с концентрацией 0.025 моль/дм3, причем образовавшиеся в дилюатных камерах катионы аминокислот переносятся через катионообменные мембраны в камеры концентрирования, и, если они являются непроточными, процесс осуществляется в периодическом режиме, а если являются проточными, то процесс осуществляется в непрерывном режиме.
Концентрирование проводится в электродиализаторе с платиновым анодом и никелевым катодом (см. чертеж), состоящем из семи камер, разделенных чередующимися ионообменными мембранами, при плотности электрического тока 0.1-10 мА/см2.
Используются биполярные мембраны МБ-3 (производство ОАО «Щекиноазот», Россия) или Fumasep FBM (производство FuMa-Tech GmbH, Германия) и сульфокатионообменные мембраны МК-40 (производство ОАО «Щекиноазот», Россия).
В качестве раствора аминокислоты в процессе концентрирования может быть взят раствор лизина, аргинина или гистидина.
Возможно концентрирование основных аминокислот из растворов низких концентраций - 10-2-10-4 моль/дм3.
На чертеже представлена схема электродиализного аппарата с чередующимися катионообменными и биполярными мембранами (1-7 номера секций, К - катионообменные мембраны, АК - биполярные мембраны).
Таблица 1 - Величины факторов концентрирования при использовании различных мембран и токов.
Таблица 2 - Зависимость фактора концентрирования от плотности электрического тока при электродиализном концентрировании аргинина с различной исходной концентрацией С0.
Таблица 3 - Энергозатраты при концентрировании лизина С0=10-4 моль/дм3.
Таблица 4 - Энергозатраты при концентрировании аргинина с различной исходной концентрацией С0.
Таблица 5. - Зависимость фактора концентрирования от плотности электрического тока при электродиализном концентрировании аргинина с проточной секцией концентрирования.
Электродиализатор
Концентрирование проводили в электродиализаторе с платиновым анодом и никелевым катодом, состоящем из семи камер, разделенных чередующимися ионообменными мембранами - см. чертеж.
Использовали биполярные мембраны МБ-3 (производство ОАО «Щекиноазот», Россия) или Fumasep FBM (производство FuMa-Tech GmbH, Германия) и катионообменные мембраны МК-40 (производство ОАО «Щекиноазот», Россия).
Гетерогенные катионообменные мембраны МК-40 изготовлены на основе катионита КУ-2, функциональными группами в котором являются сульфогруппы. Биполярные мембраны МБ-3 изготавливаются прессованием в один лист катионообменной мембраны МК-41 и анионообменной мембраны МА-41. Мембрана МК-41 изготовлена на основе катионита КФ-1, который содержит в качестве функциональных групп остатки фосфорной кислоты. Гетерогенные анионообменные мембраны МА-41 получаются на основе анионита АВ-17, который содержит четвертичные группы аммониевого основания. Мембрана FBM имеет многослойную структуру: катионобменный слой (сульфокислотные группы в сшитом полиэфиркетоне), анионобменный слой (четверичные ионы аммония, внедренные в матрицу полисульфона) и очень тонкий промежуточный слой (толщиной приблизительно 10 нм), содержащий третичные аминогруппы. Этот слой был помещен между двумя ионообменными слоями, чтобы улучшить способность FBM к ускорению диссоциации воды.
Рабочая площадь каждой из мембран составляла 20 см2. Через камеры обессоливания (дилюатные) 2, 4, 6 пропускали исходный раствор, камеры концентрирования 3 и 5, куда осуществлялся перенос аминокислоты, являлись непроточными, их объем составлял 20 см3. Линейная скорость протока в камерах обессоливания составляла 0.11-0.22 см/с. В электродные камеры 1, 7 подавался вспомогательный электролит - сульфат натрия с концентрацией 0.025 моль/дм3. Объем исходного раствора, пропускаемого через камеры обессоливания, составлял 1 дм3.
Эффективность процесса концентрирования оценивали по величине фактора концентрирования, который рассчитывали по формуле:
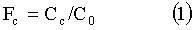 ,
,
где Сс - концентрация раствора в камерах концентрирования, С0 - концентрация исходного раствора.
При подаче напряжения на электроды катионы аминокислоты мигрировали через катионообменные мембраны к катоду. Таким образом, согласно чертежу, нечетные камеры являлись камерами концентрирования, а четные - камерами обессоливания (дилюатными). Биполярные мембраны не участвуют в миграционном переносе ионов, они используются для подкисления и подщелачивания растворов в секциях за счет разложения воды. Таким образом, применение биполярных мембран позволяет избежать использования дополнительных реагентов.
Исходный раствор, содержащий основную аминокислоту в низкой концентрации, подавали в камеры обессоливания 2, 4, 6, ограниченные с катодной стороны катионообменными, а с анодной стороны биполярными мембранами. Величина рН исходного раствора была равной рI соответствующей основной аминокислоты, таким образом, аминокислота присутствовала в исходном растворе преимущественно в виде биполярных ионов, которые не способны мигрировать в электрическом поле. За счет использования биполярных мембран происходило безреагентное подкисление раствора и образование катионов аминокислоты, которые переносились через катионообменные мембраны в камеры концентрирования. Камеры концентрирования 3 и 5, куда осуществлялся перенос аминокислоты, являлись непроточными, перед началом процесса их заполняли исходным раствором, содержащим аминокислоту. Таким образом, из камер обессоливания (2, 4, 6) вытекал раствор, обедненный аминокислотой, - дилюат. Продукт - раствор, содержащий аминокислоту в концентрации, существенно превышающей исходную, получали после проведения процесса электродиализа, сливая раствор из камер концентрирования (3, 5).
Модификацией процесса электродиализного концентрирования раствора аминокислоты является использование электродиализатора с проточными камерами концентрирования, скорость протока в которых существенно ниже, чем в секциях обессоливания. Конструкция электродиализатора аналогична представленной на чертеже, за исключением того, что камеры 3 и 5 являются проточными. В них подают исходный раствор, а на выходе получают концентрат - раствор, обогащенный аминокислотой. При этом процесс концентрирования осуществляется в непрерывном, а не в периодическом режиме.
Объем исходного раствора, пропускаемого через камеры обессоливания, составлял 1 дм3, а концентрата - 20 см3. В электродные камеры 1, 7 подавали вспомогательный электролит - сульфат натрия с концентрацией 0.025 моль/дм3. Процесс проводили в гальваностатическом режиме, при плотности тока 0.1-10 мА/см3. Использовали катионообменные мембраны МК-40 и биполярные мембраны МБ-3 (производство ОАО «Щекиноазот», Россия) или Fumasep FBM (производство FuMa-Tech GmbH, Германия). Рабочая площадь каждой из мембран составляла 20 см2.
Пример 1. В качестве основной аминокислоты был выбран лизин. Эксперименты были проведены с раствором низкой концентрации (Со=10-4 моль/дм3). Эксперименты проводились в электродиализаторе, представленном на чертеже. Линейная скорость протока в секции обессоливания составляла 0.11 см/с. Таблица 1 демонстрирует влияние плотности тока и вида биполярной мембраны на фактор концентрирования при электродиализе растворов лизина. Результаты опытов, представленные в таблице 1, свидетельствуют о том, что лучшие показатели при концентрировании раствора лизина получены с применением биполярной мембраны Fumasep FBM. Увеличение используемой плотности тока способствует более эффективному концентрированию раствора аминокислоты. Так, при плотности тока не ниже 0.5 мА/см2 раствор концентрируется в 40-45 раз.
Следует отметить, что при электромембранном концентрировании основной аминокислоты на выходе из секции концентрирования получается аминокислота в форме гидрата.
Пример 2.
В качестве основной аминокислоты был выбран аргинин.
Эксперименты были проведены с растворами различных концентраций (С0=10-4-10-2моль/дм3). В таблице 2 приведены величины фактора концентрирования, характеризующие концентрирование растворов аргинина с различной исходной концентрацией и различной величиной плотности тока. Величина i/ilim показывает, во сколько раз плотность тока в опыте превышала предельную диффузионную плотность тока. Было предварительно установлено, что для раствора аминокислоты с С0=10-4 моль/дм3 ilim=0.01 мА/см2, при С0=10-3 моль/дм3 ilim=0.13 мА/см2, а для С0=10-2 моль/дм3 ilim=1.25 мА/см2.
Как видно из данных таблицы 2, увеличение плотности тока увеличивает фактор концентрирования, а при уменьшении исходной концентрации факторы концентрирования уменьшаются.
При концентрации исходного раствора менее 10-4 моль/дм3 процесс становится малоэффективным из-за снижения фактора концентрирования и увеличения электросопротивления раствора.
Пример 3.
Осуществлено сравнение энергозатрат процессов концентрирования растворов предлагаемым методом и методом выпаривания.
Расчет проводили следующим образом. Осуществляя концентрирование раствора массы m в Fc раз методом испарения воды из раствора, необходимо нагреть исходный раствор до кипения, а затем испарить массу воды, равную (1-1/Fc)m. Для оценочного расчета примем теплоемкость раствора равной теплоемкости воды (4200 Дж/кг·К). Энергозатраты при этом можно рассчитать по формуле:
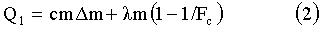 ,
,
где Q1 - энергия, необходимая для концентрирования раствора в Fc раз путем упаривания,
с - удельная теплоемкость воды,
m - масса исходного раствора,
ΔT - разность температур от исходной до температуры кипения,
λ - удельная теплота парообразования.
Энергозатраты при электродиализном концентрировании рассчитывали по формуле:
 ,
,
где U - напряжение на электродиализной ячейке,
I - сила тока,
t - время процесса.
Энергозатраты при концентрировании раствора лизина с исходной концентрацией 10-4 моль/дм3 методом выпаривания (Q1) и методом электродиализа (Q2) представлены в таблице 3. Приведены данные выигрыша в энергии Q1/Q2 для различных мембран и токовых режимов.
В таблице 4 приведены аналогичные величины, характеризующие концентрирование растворов аргинина с различной исходной концентрацией (применялись мембраны МК-40 и МБ-3) и величиной плотности тока (величина i/ilim показывает, во сколько раз ток в опыте превышал предельную диффузионную плотность тока).
Анализ данных таблиц 3 и 4 показывает, что применение электродиализного метода для концентрирования растворов дает выигрыш в энергии в сотни раз. Особенно выгодным является применение электродиализного концентрирования для растворов низких концентраций (10-4 моль/дм3). При сравнении процесса, проводимого с различными мембранами, наиболее выгодным является применение мембран FBM.
Что касается токовых режимов, то в интенсивных токовых режимах фактор концентрирования увеличивается, однако эффективность использования энергии при этом снижается. Тем не менее, во всех случаях энергозатраты намного меньше, чем при концентрировании растворов методом выпаривания.
Пример 4.
Проведено концентрирование раствора аргинина с проточными камерами концентрирования. Применение проточных камер концентрирования позволяет сделать процесс непрерывным, дает возможность автоматизации управления и контроля. Концентрирование происходило за счет различия скоростей в камерах обессоливания и концентрирования. Линейная скорость в камерах обессоливания составляла 0.81 см/с, а в камерах концентрирования 0.06 см/с. Стационарное состояние устанавливалось в течение 40 минут. Концентрация исходного раствора аргинина составляла 10-2 моль/дм3.
В таблице 5 представлены значения факторов концентрирования в электродиализном процессе с проточными камерами концентрирования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАЗДЕЛЕНИЯ АМИНОКИСЛОТ И УГЛЕВОДОВ ЭЛЕКТРОДИАЛИЗОМ | 2009 |
|
RU2426584C2 |
| Способ модификации анионообменной мембраны | 2022 |
|
RU2801038C1 |
| Способ модификации анионообменной мембраны | 2022 |
|
RU2801035C1 |
| СПОСОБ ОБЕССОЛИВАНИЯ РАСТВОРОВ НЕЙТРАЛЬНЫХ АМИНОКИСЛОТ | 2016 |
|
RU2647739C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ХЛОРИСТОГО ЛИТИЯ, ДИМЕТИЛАЦЕТАМИДА И ИЗОБУТИЛОВОГО СПИРТА ИЛИ ХЛОРИСТОГО ЛИТИЯ И ДИМЕТИЛАЦЕТАМИДА ИЗ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ ПРОИЗВОДСТВА ПАРААРАМИДНЫХ ВОЛОКОН | 2014 |
|
RU2601459C2 |
| СПОСОБ ИЗМЕНЕНИЯ ХАРАКТЕРИСТИК ЭЛЕКТРОДИАЛИЗАТОРА С ЧЕРЕДУЮЩИМИСЯ КАТИОНООБМЕННЫМИ И АНИОНООБМЕННЫМИ МЕМБРАНАМИ | 2014 |
|
RU2566415C1 |
| Способ модификации анионообменных мембран | 2018 |
|
RU2699646C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОРМОВОЙ ДОБАВКИ "НОВИЛ" ДЛЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1991 |
|
RU2010538C1 |
| СПОСОБ УТИЛИЗАЦИИ РАСТВОРОВ, ОБРАЗУЮЩИХСЯ ПРИ ПЕРЕРАБОТКЕ ОТРАБОТАННЫХ СВИНЦОВЫХ АККУМУЛЯТОРОВ | 2005 |
|
RU2304627C1 |
| СПОСОБ РЕГЕНЕРАЦИИ ПАКЕТА ИОНООБМЕННЫХ МЕМБРАН ЭЛЕКТРОДИАЛИЗАТОРА ОТ ПРОДУКТОВ ДЕГРАДАЦИИ АМИНОВОГО АБСОРБЕНТА | 2023 |
|
RU2824632C1 |
Изобретение относится к способу очистки и производства основных аминокислот, в частности к получению аргинина, лизина и гистидина из растворов низких концентраций, и может быть использовано в пищевой и фармацевтической промышленности, а также в анализе аминокислот, как метод предварительного концентрированна. Способ концентрирования основных аминокислот электродиализом включает внесение исходного раствора, содержащего основную аминокислоту в низкой концентрации, в дилюатные секции элсктродиализатора, с расположенными между электродами чередующимися катионообменными и биполярными мембранами, характеризующимися высокими числами переноса, при рН исходного раствора, равном р1 соответствующей основной аминокислоты, причем образовавшиеся катионы аминокислот переносятся через катионообменные мембраны в камеры концентрирования, при этом процесс осуществляется в периодическом режиме, если камеры концентрирования являются непроточными, или процесс осуществляется в непрерывном режиме, если камеры концентрирования являются проточными. 4 з.п. ф-лы, 5 табл., 1 ил.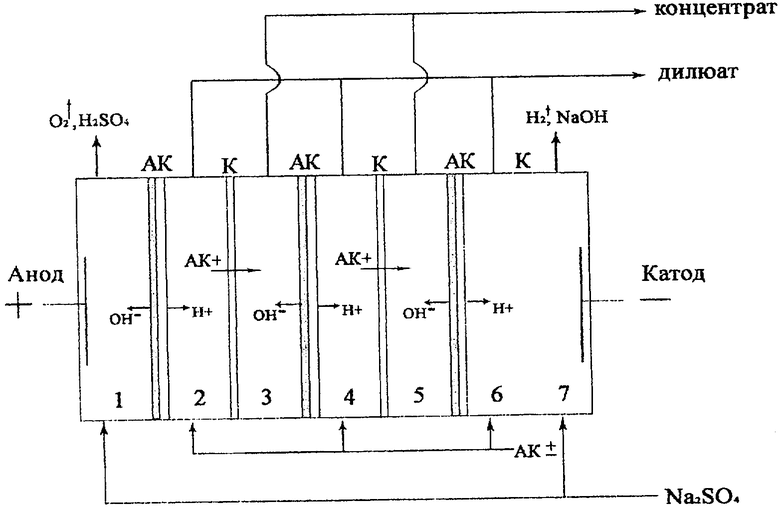
1. Способ концентрирования аминокислот электродиализом, включающий внесение исходного раствора, содержащего основную аминокислоту в низкой концентрации, в дилюатные камеры электродиализатора, с расположенными между электродами чередующимися катионообменными и биполярными мембранами, характеризующимися высокими числами переноса, при рН исходного раствора, равном рI соответствующей основной аминокислоты, перед началом процесса камеру концентрирования заполняют исходным раствором, а в электродные камеры подают раствор сульфат натрия с концентрацией 0,025 моль/дм3, причем образовавшиеся в дилюатных камерах катионы аминокислот переносятся через катионообменные мембраны в камеры концентрирования и, если они являются непроточными, процесс осуществляется в периодическом режиме, а если являются проточными, то процесс осуществляется в непрерывном режиме.
2. Способ по п.1, отличающийся тем, что исходный раствор имеет концентрацию не менее 10-4 моль/д3.
3. Способ по п.1, отличающийся тем, что процесс электродиализа ведут при плотности тока 0,1-10 мА/см2.
4. Способ по п.1, отличающийся тем, что в качестве исходного раствора используют растворы лизина, аргинина и гистидина.
5. Способ по п.1, отличающийся тем, что используют биполярные мембраны, например, МБ-3 или FBM, и катионообменные мембраны, например, МК-40.
| US 6800185 В2, 05.10.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНОВЫХ КИСЛОТ И ЩЕЛОЧИ | 1991 |
|
RU2016636C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ИЗ РАСТВОРОВ СОЛЕЙ ТВЕРДЫХ МАЛОРАСТВОРИМЫХ КИСЛОТ, ОСНОВАНИЙ И КАРБОНАТА КАЛЬЦИЯ, ВЫПАДАЮЩИХ В ОСАДОК ПРИ СДВИГЕ ЗНАЧЕНИЙ РН РАСТВОРОВ | 2003 |
|
RU2261753C2 |
| US 6551803 B1, 22.04.2003 | |||
| Регенератор цифровых систем передачи сигналов | 1983 |
|
SU1102049A1 |
| JP 62210007 A, 16.09.1987 | |||
| ЭЛЕКТРОДИАЛИЗАТОР | 1992 |
|
RU2050176C1 |
Авторы
Даты
2011-02-27—Публикация
2009-05-20—Подача