Настоящее изобретение относится к человеческим антителам к рецептору альфа1 IL-13 (IL-13Rα (альфа)1), способам их получения и их применению.
Предпосылки создания изобретения
IL-13 представляет собой мономерный пептид, который продуцируется в основном Th2-клетками, а также тучными клетками и NK-клетками (естественными клетками-киллерами). Биологическими функциями IL-13 являются регуляция производства IgE и модуляция развития Th2. IL-13 связывается с рецепторным комплексом, состоящим из цепи рецептора альфа1 IL-13 (IL-13Rα1) и цепи рецептора альфа IL-4 (IL-4Rα). Связывание с IL-13 запускает каскад сигналов трансдукции в основном через STAT6. IL-13 связывается с IL-13 Rα1 индивидуально с низкой аффинностью и не связывается с IL-4Rα1. В отличие от этого IL-4 связывается с IL-4Rα индивидуально и не связывается с IL-13Rα1 индивидуально. В литературе описан другой рецептор IL-13, а именно IL-13Rα2. IL-13 обладает высокой аффинностью к связыванию с этим рецептором. По-видимому, этот рецептор действует в качестве «рецептора-ловушки».
Индуцибельная сверхэкспрессия IL-13 в организме трансгенных мышей приводит к фенотипу, который обладает многими характеристиками, присущими пациентам, страдающим астмой. К ним относятся метаплазия слизи, воспаление, сопровождающееся высоким содержанием макрофагов, лимфоцитов и эозинофилов, повышающая регуляция протеаз типа ММР-9, -12, -13, -2 и -14, катепсина В, Н, K и S, и при этом присутствует также субэпителиальный фиброз. Для мышей с отсутствием (с «выключенным») IL-13 характерно существенное снижение производства цитокинов Th2-клетками вследствие нарушения развития Th2-клеток. У этих мышей не развивается гиперреактивность дыхательных путей (AHR) вследствие наличия эозинофильного воспаления. AHR восстанавливалась после введения IL-13, что свидетельствует о том, что присутствие IL-13 является необходимым и достаточным для индукции AHR у мышей. Другими важными биологическими функциями IL-13, связанными с астмой, являются индукция метаплазии бокаловидных клеток и образование слизи. Он воздействует непосредственно на эпителиальные клетки дыхательных путей, фибробласты и гладкомышечные клетки дыхательных путей и индуцирует различные программы транскрипции в каждом из указанных типов клеток. Интересно отметить, что IL-13 приводит к уменьшению альфа-адренергического ответа в гладкомышечных клетках, что способствует сужению дыхательных путей. Полиморфизм промотора IL-13 связан с повышенным риском возникновения аллергической астмы. Полиморфизм гена IL-13 связан с высокими уровнями IgE в сыворотке. Полиморфизм одного нуклеотида в межгенной последовательности между генами IL-4 и IL-13 связан с атонической астмой.
Антагонисты IL-13 применяли в моделях с использованием животных. Например, слитый белок растворимый мышиный IL-13Rα2-IgGFc применяли для демонстрации эффективности осуществления полной реверсии индуцированной альбумином AHR и большого количества содержащих слизь клеток. Реверсию достигали даже в том случае, когда обработку проводили после полного развития фенотипа. Кроме того, обработка мышей молекулой цитотоксина, слитой с IL-13, приводила к уменьшению всех признаков заболевания дыхательных путей при хроническом индуцированном грибками аллергическом воспалении. И, наконец, IL-13 является имеющим решающее значение медиатором эффекторного «плеча» аллергического ответа.
IL-13Rα1 является представителем суперсемейства рецепторов гематопоэтина (семейство цитокиновых рецепторов типа 1), он идентифицирован и описан Obiri N.I. и др., J. Biol. Chem., 270, 1995, cc.8797-8804) и в WO 96/29417. Он представляет собой белок, состоящий из 427 аминокислот, включая сигнальную последовательность. Его последовательности ДНК и белка представлены в WO 97/15663 и SwissProt No. P78552. IL-13Rα1 представляет собой гликозилированный белок, который связывается с IL-13 с низкой аффинностью, но будучи связанным с IL-4Rα с образованием гетеродимера, он связывается с IL-13 с высокой аффинностью. Этот комплекс является также рецептором для IL-4.
Антитела к IL-13Rα1 описаны также в WO 96/29417, WO 97/15663, WO 03/080675, у Graber Р. и др., Eur. J. Immunol., 28, 1998, cc.4286-4298; Poudrier J. и др., J. Immunol., 163, 1999, cc.1153-1161; Poudrier J. и др., Eur. J. Immunol., 30, 2000, cc.3157-3164; Aikawa М. и др., Cytokine, 13, 2001, cc.75-84. Антитела к IL-13Rα1 поступают в продажу от фирмы R&D Systems Inc. USA.
Краткое изложение сущности изобретения
Изобретение относится к антителу, которое связывается с IL-13Rα1 и ингибирует биологическую активность IL-13, отличающемуся тем, что аминокислотную последовательность CDR3 вариабельной области тяжелой цепи антитела выбирают из группы, включающей последовательности CDR3 тяжелой цепи, представленные в SEQ ID NO:1, 3, 5, 7 или 9.
Антитело предпочтительно представляет собой человеческое антитело.
Антитело предпочтительно отличается тем, что аффинность связывания с IL-13Rα1 составляет 10-9 М (KD) или менее, предпочтительно от 10-9 до 10-13 М.
Предпочтительно антитело отличается тем, что его последовательности CDR1, CDR2 и CDR3 тяжелой цепи выбирают из группы, включающей последовательности CDR1, CDR2 и CDR3, представленные в SEQ ID NO:1, 3, 5, 7 или 9.
Антитело предпочтительно отличается тем, что аминокислотные последовательности CDR1, CDR2 и CDR3 вариабельной области легкой цепи антитела выбирают из группы, включающей последовательности CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10.
Антитело предпочтительно отличается тем, что аминокислотные последовательности CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи антитела выбирают из группы, включающей последовательности CDR тяжелой цепи, представленные в SEQ ID NO:1, 3, 5, 7 или 9, и аминокислотные последовательности CDR1, CDR2 и CDR3 вариабельной области легкой цепи антитела выбирают из группы, включающей последовательности CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10.
Последовательности CDR предпочтительно выбирают независимо друг от друга и их разделяют каркасными участками (FR).
Антитело предпочтительно отличается тем, что оно содержит в качестве CDR тяжелой цепи CDR, представленные в SEQ ID NO:1, и в качестве CDR легкой цепи CDR, представленные в SEQ ID NO:2, в качестве CDR тяжелой цепи CDR, представленные в SEQ ID NO:3, и в качестве CDR легкой цепи CDR, представленные в SEQ ID NO:4, в качестве CDR тяжелой цепи CDR, представленные в SEQ ID NO:5, и в качестве CDR легкой цепи CDR, представленные в SEQ ID NO:6, в качестве CDR тяжелой цепи CDR, представленные в SEQ ID NO:7, и в качестве CDR легкой цепи CDR, представленные в SEQ ID NO:8, или в качестве CDR тяжелой цепи CDR, представленные в SEQ ID NO:9, и в качестве CDR легкой цепи CDR, представленные в SEQ ID NO:10.
Последовательности CDR можно определять с использованием стандартного определения, приведенного у Kabat и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991. Согласно этому определению гипервариабельные участки (CDR), представленные в SEQ ID NO:1-8, имеют следующие последовательности:
CDR тяжелой цепи: CDR1 (ак 31-35) SEQ ID NO:1, 3, 5, 7, 9, CDR2 (ак 50-66) SEQ ID NO:1, 3, 5, 7, 9, CDR3 (ак 99-108) SEQ ID NO:1, 3, 9, CDR3 (ак 99-107) SEQ ID NO:5, CDR3 (ак 99-112) SEQ ID NO:7;
CDR легкой цепи: CDR1 (ак 24-34) SEQ ID NO:2, 4, 6, 10, CDR1 (ак 24-35) SEQ ID NO:8, CDR2 (ак 50-56) SEQ ID NO:2, 4, 6, 10, CDR2 (ак 51-57) SEQ ID NO:8 и CDR3 (ак 89-97) SEQ ID NO:2, 4, 6, 10, CDR3 (ак 90-97) SEQ ID NO:8.
Предпочтительно антитело, предлагаемое в изобретении, содержит в качестве гипервариабельных участков (CDR) следующие последовательности:
а) тяжелая цепь антитела содержит CDR тяжелой цепи, представленные в SEQ ID NO:1, 3, 5, 7 или 9;
б) легкая цепь антитела содержит CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10,
где CDR выбирают независимо друг от друга.
Антитело предпочтительно отличается тем, что содержит в качестве вариабельной области тяжелой цепи SEQ ID NO:1 и в качестве вариабельной области легкой цепи SEQ ID NO:2, в качестве вариабельной области тяжелой цепи SEQ ID NO:3 и в качестве вариабельной области легкой цепи SEQ ID NO:4, в качестве вариабельной области тяжелой цепи SEQ ID NO:5 и в качестве вариабельной области легкой цепи SEQ ID NO:6, в качестве вариабельной области тяжелой цепи SEQ ID NO:7 и в качестве вариабельной области легкой цепи SEQ ID NO:8 или в качестве вариабельной области тяжелой цепи SEQ ID NO:9 и в качестве вариабельной области легкой цепи SEQ ID NO:10.
Антитело предпочтительно отличается тем, что содержит
а) в качестве вариабельной области тяжелой цепи SEQ ID NO:1, в качестве вариабельной области легкой цепи SEQ ID NO:2, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
б) в качестве вариабельной области тяжелой цепи SEQ ID NO:3 и в качестве вариабельной области легкой цепи SEQ ID NO:4, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
в) в качестве вариабельной области тяжелой цепи SEQ ID NO:5 и в качестве вариабельной области легкой цепи SEQ ID NO:6, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
г) в качестве вариабельной области тяжелой цепи SEQ ID NO:7 и в качестве вариабельной области легкой цепи SEQ ID NO:8, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A, или
д) в качестве вариабельной области тяжелой цепи SEQ ID NO:9 и в качестве вариабельной области легкой цепи SEQ ID NO:10, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A.
Предпочтительно антитело отличается тем, что антитело связывается с IL-13Rα1 конкурентно с антителом LC5002-002, LC5002-003, LC5002-005, LC5002-007 и/или LC5002-018. Предпочтительно антитело отличается тем, что содержит в качестве вариабельных областей вариабельные области LC5002-002, LC5002-003, LC5002-005, LC5002-007 или LC5002-018. Вариабельные области этих антител представлены в SEQ ID NO:1-10. Пригодные константные области хорошо известны в данной области. Их примеры представлены в SEQ ID NO:11-12.
Антитело предпочтительно представляет собой моноклональное или полученное рекомбинантным путем антитело.
В одном из вариантов осуществления изобретения антитело относится к классу измененных человеческих антител.
В предпочтительном варианте осуществления изобретения антитело содержит человеческую тяжелую γ1-цепь, включающую
а) аминокислотную последовательность Pro233Val234Ala235, имеющую делецию Gly236, и/или аминокислотную последовательность Gly327Leu328Pro329Ser330Ser331,
б) аминокислотную последовательность Ala234Ala235 или
в) аминокислоты Ala265 и Ala297.
Предпочтительно антитело, предлагаемое в изобретении, обладает способностью ингибировать индуцируемое IL-13 фосфорилирование Stat-6, характеризующейся значением IC50, составляющим 6нМ или менее, способностью ингибировать индуцируемое IL-13 производство эотаксина, характеризующейся значением IC50, составляющим 20 нМ или менее и/или способностью ингибировать индуцируемую IL-13 или IL-4 пролиферацию клеток, предпочтительно TF-1-клеток (АТСС CRL 2003), характеризующуюся значением IC50, составляющим 10 нМ или менее (IL-13) и 60 нМ или менее (IL-4). Индуцируемое IL-13 фосфорилирование Stat-6, производство эотаксина и индукцию пролиферации клеток определяют согласно методам, описанным в примерах 6-8.
Антитело, предлагаемое в изобретении, предпочтительно не связывается с денатурированным IL-13Rα1 (значение KD для аффинности связывания составляет 10-6 М или более). Антитело предпочтительно отличается тем, что практически не обладает перекрестной реактивностью с IL-13Rα2 и IL-4Rα (значение KD для аффинности связывания составляет 10-6 М или более).
В изобретении предложены также линии клеток гибридомы, продуцирующие антагонистические моноклональные антитела к IL-13Rα1.
Предпочтительные линии клеток гибридомы, предлагаемые в изобретении (hu-MAB<h-IL-13R alpha>LC.5002-002 (DSM ACC2709), hu-MAB<h-IL-13Ralpha>LC.5002-003 (DSM ACC2710), hu-MAB<h-IL-13Ralpha>LC.5002-005 (DSM ACC2711), hu-MAB<h-IL-13R alpha>LC.5002-007 (DSM ACC2712)) депонированы 13.01.2005 г. в Немецкой коллекции микроорганизмов и клеточных культур (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH) (DSMZ), Германия.
Антитела, которые можно получать с помощью указанных линий клеток, также являются вариантами осуществления изобретения.
Кроме того, изобретение относится к нуклеиновым кислотам, кодирующим полипептиды, из которых состоят антитела, предлагаемые в изобретении, экспрессионным векторам, содержащим такие нуклеиновые кислоты, и клеткам-хозяевам, предназначенным для рекомбинантного получения таких антител. Кроме того, в изобретении предложены способы рекомбинантного получения таких антител.
Полипептиды, кодируемые нуклеиновыми кислотами, предлагаемыми в изобретении, представляют собой
а) тяжелую цепь антитела, содержащую CDR тяжелой цепи, представленные в SEQ ID NO:NO:1, 3, 5, 7 или 9, и
б) легкую цепь антитела, содержащую CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10.
Эти полипептиды обладают способностью к сборке с соответствующей другой цепью антитела с образованием антитела.
Антитела, предлагаемые в изобретении, обладают преимуществами для пациентов, нуждающихся в лечении с применением кортикостероидов. Антитела, предлагаемые в изобретении, имеют новые и патентоспособные свойства, обладая преимуществом для пациента, который страдает астмой или аллергическим заболеванием.
Кроме того, в изобретении предложены способы лечения астмы и аллергических заболеваний.
Изобретение относится также к применению антитела, предлагаемого в изобретении, для лечения астмы и для приготовления фармацевтической композиции, предлагаемой в изобретении. Кроме того, изобретение относится к способу приготовления фармацевтической композиции, предлагаемой в изобретении.
Изобретение относится также к фармацевтической композиции, содержащей антитело, предлагаемое в изобретении, в фармацевтически эффективном количестве необязательно в сочетании с буфером и/или адъювантом, которые можно применять для приготовления содержащей антитела препаративной формы для фармацевтических целей.
Изобретение относится также к фармацевтической композиции, содержащей указанное антитело в фармацевтически приемлемом носителе. В одном из вариантов осуществления изобретения фармацевтическую композицию можно включать в изделие или набор.
Изобретение относится также к вектору, содержащему нуклеиновую кислоту, предлагаемую в изобретении, который обладает способностью осуществлять экспрессию нуклеиновой кислоты в прокариотической или эукариотической клетке-хозяине.
Изобретение относится также к прокариотической или эукариотической клетке-хозяину, содержащей вектор, предлагаемый в изобретении.
Изобретение относится также к способу получения рекомбинантного человеческого антитела, предлагаемого в изобретении, отличающемуся тем, что осуществляют экспрессию нуклеиновой кислоты, предлагаемой в изобретении, в прокариотической или эукариотической клетке-хозяине и выделяют антитело из клетки. Кроме того, изобретение относится к антителу, которое можно получать таким способом рекомбинации.
Изобретение относится также к способу получения фармацевтической композиции, отличающемуся тем, что отбирают антитело к IL-13Rα1 из множества антител к IL-13Rα1 на основе сравнения с использованием анализа без применения антитела, получают антитело с помощью рекомбинантной экспрессии, выделяют антитело и объединяют антитело с фармацевтически приемлемым буфером и/или адъювантом. Предпочтительно антитело обладает одним или несколькими из указанных выше дополнительных свойств.
Подробное описание изобретения
Понятия «IL-13Rα1, мышиный IL-13Rα1, IL-13, IL-13Rα2 и IL-4Rα» и их домены хорошо известны в данной области и представлены, например, в SwissProt P78552, 009030, Р35225, Q14627 и Р24394. Если не указано иное, понятия «IL-13Rα1, IL-13, IL-13Rα2 и IL-4Rα» в контексте настоящего описания обозначают человеческие полипептиды IL-13Rα1, IL-13, IL-13Rα2 и IL-4Rα.
Понятие «человеческое антитело» в контексте настоящего описания включает антитела, имеющие вариабельные и константные области (домены), которые можно отнести к последовательностям иммуноглобулинов человеческой зародышевой линии на основе их высокой степени сходства или идентичности с этими последовательностями зародышевой линии. Человеческие антитела хорошо известны в данной области (van Dijk М.А. и van de Winkel J.G., Curr. Opin. Chem. Biol. 5, 2001, cc.368-374). Человеческие антитела можно получать также в трансгенных животных (например, мышах), которые в результате иммунизации могут продуцировать полный спектр или набор человеческих антител при отсутствии производства эндогенного иммуноглобулина. Перенос набора генов иммуноглобулинов человеческой зародышевой линии в такую мутантную зародышевую линию мышей должен приводить к производству человеческих антител после антигенной стимуляции (см., например, Jakobovits А., и др., Proc. Natl. Acad. Sci. USA 90, 1993, cc.2551-2555; Jakobovits А. и др., Nature 362, 1993, cc.255-258; Bruggemann M. и др., Year Immunol. 7, 1993, cc.33-40). Человеческие антитела можно получать также с помощью фаговых дисплейных библиотек (Hoogenboom H.R. и Winter, G., J. Mol. Biol. 227, 1992, cc.381-388; Marks J.D. и др., J. Mol. Biol. 222, 1991, cc.581-597). Для получения человеческих моноклональных антител можно использовать также методы Cole с соавторами и Boerner с соавторами (Cole и др., Monoclonal Antibodies and Cancer Therapy, под ред. Alan R. Liss, 1985, с.77; и Boerner Р. и др., J. Immunol. 147, 1991, cc.86-95). Понятие «человеческое антитело» относится к различным формам антител, предпочтительно моноклональных антител, включая (но, не ограничиваясь ими) полные антитела, фрагменты антител, антитела измененного (переключенного) класса и генетически сконструированные антитела (варианты или мутантные антитела), если они сохраняют характерные особенности, присущие антителам, предлагаемым в изобретении. Наиболее предпочтительными являются рекомбинантные человеческие антитела. Понятие «моноклональное антитело» в контексте настоящего описания относится к получению молекул антитела, которые все имеют практически одинаковые аминокислотные последовательности.
Подразумевается, что понятие «рекомбинантное человеческое антитело» в контексте настоящего описания включает все человеческие антитела, которые получают, экспрессируют, создают или выделяют с помощью методов рекомбинации, такие как антитела, выделенные из клетки-хозяина, такой как NS0- или СНО-клетка, или из организма животного (например, мыши), которое является трансгенным из-за присутствия человеческих генов иммуноглобулинов, или антитела, экспрессируемые с использованием рекомбинантного экспрессионного вектора, которым трансфектирована клетка-хозяин. Такие рекомбинантные человеческие антитела имеют вариабельную и константную области, которые находятся в преобразованной форме. Рекомбинантные человеческие антитела, предлагаемые в изобретении, подвергают соматической гипермутации in vivo. Таким образом, аминокислотные последовательности VH- и VL-областей рекомбинантных антител представляют собой последовательности, которые, хотя и выведены из человеческой зародышевой линии последовательностей VH и VL, могут не существовать в естественных условиях в спектре зародышевой линии человеческих антител in vivo. Понятие «антитело переключенного класса» относится к моноклональному антителу, предпочтительно человеческому антителу, содержащему вариабельную область, т.е. связывающую область, из одного источника или зародышевой линии и, по меньшей мере часть константной области, соответствующей константной области антитела из другого источника или зародышевой линии, которое, как правило, получают методами рекомбинантной ДНК. Такие антитела переключенного класса не встречаются в естественных условиях и, следовательно, не могут быть получены непосредственно из ксенотрансплантированных мышей. Формы «антител переключенного класса», подпадающие под объем настоящего изобретения, представляют собой формы, в которых константная область имеет отличия от последовательности константной области дикого типа, что приводит к получению антител, предлагаемых в изобретении, обладающих различными свойствами, прежде всего касательно связывания с C1q и/или связывания с рецептором Fc (FcR), т.е. путем изменения или мутации Fc. Антитела переключенного класса являются продуктом экспрессируемых генов иммуноглобулина, которые содержат сегменты ДНК, кодирующие вариабельные области иммуноглобулина, и сегменты ДНК, кодирующие константные области иммуноглобулина. Методы получения антител переключенного класса включают общепринятые методы рекомбинантной ДНК и генной трансфекции, хорошо известные в данной области (см., например, Morrison S.L. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc.6851-6855; US 5202238 и 5204244).
Понятие «вариабельная область» (вариабельная область легкой цепи (VL), вариабельная область тяжелой цепи (VH)) в контексте настоящего описания относится к каждой из пары легких и тяжелой цепей, которые участвуют непосредственно в связывании антитела с антигеном. Домены вариабельных человеческих легких и тяжелых цепей имеют одинаковую общую структуру, и каждый домен содержит четыре каркасных участка (FR), последовательности которых являются весьма консервативными, связанных тремя «гипервариабельными участками» (или определяющими комплементарность участками, CDR). Каркасные участки адаптированы к β-складчатой конформации, а CDR могут образовывать петли, соединяющие β-складчатую структуру. CDR в каждой цепи сохраняют их трехмерную структуру с помощью каркасных участков, и образуют вместе с CDR из другой цепи антигенсвязывающий центр. CDR3-участки тяжелой и легкой цепей антитела, предпочтительно CDR3 тяжелой цепи, играют особенно важную роль в специфичности связывания/аффинности антител, предлагаемых в изобретении, и поэтому являются еще одним объектом изобретения.
Понятия «гипервариабельный участок» или «антигенсвязывающий центр антитела» в контексте настоящего описания относятся к аминокислотным остаткам антитела, которые ответственны за связывание антигена. Гипервариабельный участок содержит аминокислотные остатки из «определяющих комплементарность участков» или «CDR». «Каркасные» или «FR»-участки представляют собой участки вариабельной области, отличные от указанных в настоящем описании остатков гипервариабельного участка. Таким образом, легкие и тяжелые цепи антитела содержат в направлении от N- к С-концу участки FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. CDR- и FR-участки определяют с помощью стандартной номенклатуры Кэбота (Kabat и др., Sequences of Proteins of Immunological Interest, 5-изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD (1991).
«Константные области» не принимают непосредственного участия в связывании антитела с антигеном, но обладают различными эффекторными функциями. В зависимости от аминокислотной последовательности константной области их тяжелых цепей антитела или иммуноглобулины подразделяют на следующие классы: IgA, IgD, IgE, IgG и IgM, некоторые из которых можно дополнительно подразделять на подклассы (изотипы), например, IgG1, IgG2, IgG3 и IgG4, IgA1 и IgA2. Константные области тяжелой цепи, соответствующие различным классам иммуноглобулинов, обозначают µ, δ, γ, α и ε соответственно. Антитела, предлагаемые в изобретении, предпочтительно относятся к IgG1-типу.
Fc-фрагмент антитела принимает непосредственное участие в активации комплемента, связывании C1q, активации С3 и связывании Fc-рецептора. Связывание с C1q обусловлено определенными сайтами связывания в Fc-фрагменте. Такие сайты связывания известны в данной области и описаны, например, у Lukas T.J. и др., J. Immunol. 127, 1981, cc.2555-2560; Brunhouse R. и Cebra J.J., Mol. Immunol. 16, 1979, cc.907-917; Burton D.R. и др., Nature 288, 1980, cc.338-344; Thommesen J.E. и др., Mol. Immunol. 37, 2000, cc.995-1004; Idusogie E.E. и др., J. Immunol. 164, 2000, cc.4178-4184; Hezareh M. и др., J. Virol. 75, 2001, cc.12161-12168; Morgan А. и др., Immunology 86, 1995, cc.319-324; и ЕР 0307434. Такие сайты связывания представляют собой, например, L234, L235, D270, N297, Е318, K320, K322, Р331 и Р329 (нумерация согласно EU-индексу, предложенному Кэботом, см. ниже). Антитела подклассов IgG1, IgG2 и IgG3, как правило, обусловливают активацию комплемента, связывание C1q и активацию С3, в то время как антитело подкласса IgG4 не активирует систему комплемента, не связывает C1q и не активирует С3. В контексте настоящего описания понятие «Fc-фрагмент, который имеет человеческое происхождение» обозначает Fc-фрагмент, который предпочтительно имеет аминокислотную последовательность Fc-фрагмента человеческого антитела подкласса IgG1, модифицированный таким образом, что нельзя обнаружить ни связывание с C1q, ни активацию С3 и/или связывание с FcR, или связывание которого уменьшено по меньшей мере на 50%, предпочтительно на 70% по сравнению с человеческим антителом подкласса IgG1. Понятие «Fc-фрагмент антитела» хорошо известно специалисту в данной области и этот фрагмент определяют на основе расщепления антител папаином. Антитела, предлагаемые в изобретении, содержат в качестве Fc-фрагмента предпочтительно аминокислотную последовательность Fc-фрагмента, имеющего человеческое происхождение и предпочтительно все другие части человеческих константных областей. Предпочтительно Fc-фрагмент представляет собой мутантный фрагмент человеческого иммуноглобулина подкласса IgG1. Наиболее предпочтительными являются Fc-фрагменты, содержащие константную область тяжелой γ1-цепи (например, представленную в SEQ ID NO:11) с мутациями L234A и L235A или D235A и N297A (WO 99/51642).
Подробное описание цепей человеческих константных областей, например, тяжелых γ1-цепей, приведено у Kabat и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD., 1991; у Brüggemann M. и др., J. Exp. Med. 166, 1987, cc.1351-1361; и у Love T.W. и др., Methods Enzymol. 178, 1989, cc.515-527. Константные области, которые являются предпочтительными согласно изобретению, не обеспечивают связывания комплемента. Понятие «вариабельная область» (вариабельная область легкой цепи (VL), вариабельная область тяжелой цепи (VH)) в контексте настоящего описания относится к каждой из пары легких и тяжелой цепей, которые участвуют непосредственно в связывании антитела с антигеном.
Подразумевается, что понятие «нуклеиновая кислота или молекула нуклеиновой кислоты» в контексте настоящего описания включает молекулы ДНК и молекулы РНК. Молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, но предпочтительно представляет собой двухцепочечную ДНК.
Нуклеиновую кислоту «функционально связывают», когда создают функциональную связь между ней и другой нуклеотидной последовательностью. Например, ДНК предпоследовательности или лидера секреции функционально связана с ДНК полипептида, если она экспрессируется в виде предбелка, который участвует в секреции полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он оказывает воздействие на транскрипцию последовательности; или сайт связывания рибосом функционально связан с кодирующей последовательностью, если он помещен так, чтобы он облегчал трансляцию. Как правило, понятие «функционально связаны» означает, что последовательности ДНК, будучи связаны, находятся в цис-положении (являются смежными), а в случае лидера секреции, смежными и находящимися в рамке считывания. Однако для энхансеров не является необходимым, чтобы они были смежными. Связывание осуществляют путем лигирования в удобных сайтах рестрикции. Если такие сайты не существуют, то согласно общепринятой практике используют синтетические олигонуклеотидные адаптеры или линкеры.
В контексте настоящего описания понятия «клетка», «клеточная линия» и «клеточная культура» используются взаимозаменяемо, и все такие определения включают потомство. Так, понятия «трансформанты» и «трансформированные клетки» относятся к первичной клетке субъекта и полученным из нее культурам безотносительно к количеству переносов. Следует понимать также, что все потомство может не быть полностью идентичным по составу ДНК из-за преднамеренных или случайных мутаций. Под объем изобретения подпадает вариант потомства, имеющего такую же функцию или биологическую активность, которая обнаружена у исходной трансформированной клетки. Если используются другие определения, то это будет очевидно из контекста.
Понятие «связывание с IL-13Rα1» в контексте настоящего описания означает связывание антитела с IL-13Rα1, которое оценивают с помощью анализа in vitro, предпочтительно анализа связывания, в котором антитело связывают с поверхностью и связывание с IL-13Rα1 измеряют с помощью поверхностного плазменного резонанса (SPR). Наличие связывания означает, что аффинность к связыванию (KD) составляет 10-8 М или менее, предпочтительно от 10-13 до 10-9 М. «Отсутствие связывания» означает, что значение KD составляет 10-6 М или более. Антитела, предлагаемые в изобретении, связываются с внеклеточным доменом человеческого IL-13Rα1 и предпочтительно также мышиного IL-13Rα1.
Связывание с IL-13Rα1 можно оценивать с помощью BIAcore-анализа (фирма Pharmacia Biosensor AB, Уппсала, Швеция). Аффинность связывания оценивают, используя в качестве критериев ka (константа скорости ассоциации антитела с антигеном), kd (константа скорости диссоциации антитела из комплекса антитело/антиген) и KD (kd/ka).
Антитела, предлагаемые в изобретении, ингибируют связывание IL-13 с IL-13Rα1. Ингибирование оценивают по величине IC50 при оценке с помощью ELISA связывания IL-13 с гетеродимером IL-13Rα1/IL-4Rα. Для осуществления такого анализа IL-13Rα1 иммобилизуют и добавляют IL-13 и IL-4Rα. Значения IC50 для антител, предлагаемых в изобретении, при оценке связывания IL-13 с IL-13Rα1 составляют не более 6 нМ. Величины IC50 определяют в виде средних или медианных значений по меньшей мере по трем независимым экспериментам. Отдельные значения IC50 могут выпадать из указанного диапазона.
Антитела, предлагаемые в изобретении, предпочтительно обладают способностью к связыванию с теми же самыми эпитопами IL-13Rα1, что и антитело, выбранное из группы, включающей антитела LC5002-002, LC5002-003, LC5002-005, LC5002-007 или LC5002-018, или ингибируют связывание с IL-13Rα1 вследствие стерической помехи к связыванию, создаваемой этими антителами. Ингибирование связывания можно оценивать с помощью SPR-анализа с использованием иммобилизованного антитела, выбранного из группы, включающей антитела LC5002-002, LC5002-003, LC5002-005, LC5002-007 или LC5002-018, и IL-13Rα1 в концентрации 20-50 нМ и антитела, подлежащего оценке, в концентрации 100 нМ. Уменьшение сигнала на 50% или более свидетельствует о том, что антитело конкурирует с антителом, выбранным из группы, включающей антитела LC5002-002, LC5002-003, LC5002-005, LC5002-007 или LC5002-018. Понятие «эпитоп» обозначает белковую детерминанту, обладающую способностью специфически связываться с антителом. Эпитопы, как правило, состоят из химически активных расположенных на поверхности групп молекул, таких как боковые цепи аминокислот или сахаров, и, как правило, имеют характеристики специфической трехмерной структуры, а также специфические характеристики зарядов. Конформационные и неконформационные эпитопы различаются тем, что связывание с эпитопами первого, но не второго типа, нарушается в присутствии денатурирующих растворителей. Изобретение относится также к связыванию человеческого антитела с IL-13Rα1 и ингибированию биологической активности IL-13, которое характеризуется аффинностью, составляющей 10-9 М (KD) или менее, предпочтительно от 10-9 до 10-13 М, для связывания с IL-13Rα1 и аффинностью, составляющей 10-7 М (KD) или менее, предпочтительно от 10-8 до 10-9 М, для связывания с мышиным IL-13Rα1.
В предпочтительном варианте осуществления изобретения антитела, предлагаемые в изобретении, отличаются также наличием одной или нескольких характеристик связывания (выбранных из параметров связывания ka, kd и KD) с тем же самым эпитопом, с которым связывается антитело, выбранное из группы, включающей антитела LC5002-002, LC5002-003, LC5002-005, LC5002-007 или LC5002-018.
Антитела, предлагаемые в изобретении, предпочтительно получают методами рекомбинации. Такие методы широко известны в данной области и представляют собой экспрессию белков в прокариотических и эукариотических клетках с последующим выделением полипептида антитела и, как правило, очистку до фармацевтически приемлемой чистоты. Для экспрессии белка нуклеиновые кислоты, кодирующие легкие и тяжелые цепи или их фрагменты, встраивают в экспрессионные векторы стандартными методами. Экспрессию осуществляют в пригодных прокариотических или эукариотических клетках-хозяевах типа СНО-клеток, NS0-клеток, SP2/0-клеток, HEK293-клеток, COS-клеток, клеток дрожжей или клеток E.coli, и антитело выделяют из клеток (из супернатанта или клеток после лизиса).
Рекомбинантное получение антител хорошо известно в данной области и описано, например, в обзорных статьях Makrides S.C., Protein Expr. Purif. 17, 1999, cc.183-202; Geisse S. и др., Protein Expr. Purif. 8, 1996, cc.271-282; Kaufman R.J., Mol. Biotechnol. 16, 2000, cc.151-161; Werner R.G. и др., Drug Res. 48, 1998, cc.870-880.
Антитела могут присутствовать в целых клетках, в клеточном лизате или в частично очищенной или практически чистой форме. Очистку осуществляют для удаления других клеточных компонентов или других загрязнителей, например, других клеточных нуклеиновых кислот или белков, стандартными методами, которые включают обработку щелочью/ДСН, CsCl-бэндинг, хроматографию на колонках, элекрофорез в агарозном геле и другие методы, хорошо известные в данной области (см. в Current Protocols in Molecular Biology, под ред. Ausubel F., и др., изд-во Greene Publishing and Wiley Interscience, New York, 1987).
Экспрессия в NS0-клетках описана, например, у Barnes L.M. и др., Cytotechnology 32, 2000, cc.109-123; и Barnes L.M. и др., Biotech. Bioeng. 73, 2001, cc.261-270. Кратковременная экспрессия описана, например, у Durocher Y. и др., Nucl. Acids. Res. 30, 2002, с.Е9. Клонирование вариабельных областей описано у Orlandi R. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.3833-3837; Carter Р. и др., Proc. Natl. Acad. Sci. USA 89, 1992, cc.4285-4289; и Norderhaug L. и др., J. Immunol. Methods 204, 1997, cc.77-87. Предпочтительная система кратковременной экспрессии (НЕК 293) описана у Schlaeger E.-J. и Christensen K. в Cytotechnology 30, 1999, cc.71-83 и у Schlaeger E.-J. в J. Immunol. Methods 194, 1996, cc.191-199.
Контролирующие последовательности, которые можно применять для прокариот, представляют собой, например, промотор, необязательно последовательность оператора и сайт связывания рибосом. Известно, что эукариотические клетки могут использовать промоторы, энхансеры и сигналы полиаденилирования.
Моноклональные антитела можно отделять от культуральной среды с помощью общепринятых методов очистки иммуноглобулинов, таких, например, как хроматография на протеин А-сефарозе, гидроксилапатите, гель-электрофорез, диализ или аффинная хроматография. ДНК и РНК, которые кодируют моноклональные антитела, легко выделять и секвенировать с помощью общепринятых методов. Клетки гибридом могут служить источником таких ДНК и РНК. Для осуществления синтеза рекомбинантных моноклональных антител в клетках-хозяевах ДНК после выделения можно встраивать в экспрессионные векторы, которыми затем трансфектируют клетки-хозяева, такие как СНО-клетки, HEK 293-клетки или клетки миеломы, которые в ином варианте не могут продуцировать белок иммуноглобулина.
К антителам, предлагаемым в изобретении, относятся также антитела, несущие «консервативные модификации последовательностей», модификации нуклеотидных и аминокислотных последовательностей, которые не оказывают воздействия или не изменяют вышеуказанные характеристики антитела, предлагаемого в изобретении. Модификации можно интродуцировать стандартными методами, известными в данной области, такими как сайтнаправленный мутагенез и опосредуемый ПЦР мутагенез. Консервативные аминокислотные замены включают замены, при которых аминокислотный остаток заменяют аминокислотным остатком с такой же боковой цепью. Семейства аминокислотных остатков, имеющих аналогичные боковые цепи, известны в данной области. Эти семейства включают аминокислоты с основными боковыми цепями (например лизин, аргинин, гистидин), кислотными боковыми цепями (например аспарагиновую кислоту, глутаминовую кислоту), незаряженными полярными боковыми цепями (например глицин, аспарагин, глутамин, серии, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например треонин, валин, изолейцин) и ароматическими боковыми цепями (например тирозин, фенилаланин, триптофан, гистидин). Таким образом, выбранный остаток заменимой аминокислоты в человеческом антителе к IL-13Rα1 предпочтительно можно заменять другим аминокислотным остатком из семейства с такой же боковой цепью.
Аминокислотные замены можно осуществлять путем мутагенеза, основанного на молекулярном моделировании, согласно методу, описанному у Riechmann L. и др., Nature 332, 1988, cc.323-327 и у Queen С. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.10029-10033.
Варианты аминокислотных последовательностей антитела к человеческому IL-13Rα1 получают путем интродукции соответствующих нуклеотидных замен в ДНК антитела или с помощью пептидного синтеза. Однако такие модификации можно осуществлять только в очень ограниченном диапазоне, например, указанном выше. Например, модификации не должны изменять вышеуказанные характеристки антитела, такие как изотип IgG и связывание с эпитопом, но они могут повышать выход рекомбинантного производства, стабильность белка или облегчать очистку.
Любой остаток цистеина, который не участвует в поддержании правильной конформации антитела к IL-13Rα1, также можно заменять, как правило, серином, для повышения стабильности молекулы при окислении и предупреждения аномального перекрестного сшивания. И наоборот, можно вводить в антитело цистеиновую(ые) связь(и) для повышения его стабильности (прежде всего, когда антитело представляет собой фрагмент антитела, такой как Fv-фрагмент).
Другой тип аминокислотного варианта антитела изменяет исходную схему гликозилирования антитела. Под изменением понимают делецию одного или нескольких углеводных остатков, присутствующих в антителе, и/или добавление одного или нескольких сайтов гликозилирования, которые не присутствуют в антителе. Гликозилированные антитела, как правило, являются N-связанными. Понятие «N-связанный» относится к присоединению углеводного остатка к боковой цепи аспарагинового остатка. Трипептидные последовательности аспарагин-Х-серин и аспарагин-Х-треонин, где Х обозначает любую аминокислоту кроме пролина, представляют собой распознаваемые последовательности для ферментативного присоединения углеводного остатка к боковой цепи аспарагина. Таким образом, присутствие любой из этих трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования. Введение сайтов гликозилирования в антитело удобно осуществлять путем изменения аминокислотной последовательности так, чтобы она содержала одну или несколько из вышеуказанных трипептидных последовательностей (для N-связанных сайтов гликозилирования).
Молекулы нуклеиновых кислот, которые кодируют варианты аминокислотных последовательностей антитела к IL-13Rα1, получают с помощью различных методов, известных в данной области. Эти методы включают (но, не ограничиваясь ими) выделение из встречающегося в естественных условиях источника (в случае встречающихся в естественных условиях вариантов аминокислотных последовательностей) или получение с помощью опосредуемого олигонуклеотидами мутагенеза (или сайтнаправленного мутагенеза с использованием олигонуклеотидов), ПЦР-мутагеназа или кассетного мутагенеза ранее полученного варианта или исходной версии гуманизированного антитела к IL-13Rα1.
Другой тип ковалентной модификации включает химическое или ферментативное сочетание гликозидов с антителом. Указанные методы имеют преимущество, состоящее в том, что при этом не требуется производство антитела в клетке-хозяине, которая обладает способностью к гликозилированию, т.е. N- или O-связанному гликозилированию. В зависимости от применяемого пути сочетания сахар(а) можно присоединять к (а) аргинину и гистидину, (б) свободным карбоксильным группам, (в) свободным сульфгидрильным группам, таким как сульфгидрильные группы цистеина, (г) свободным гидроксильным группам, таким как гидроксильные группы серина, треонина или гидроксипролина, (д) ароматическим остаткам, таким как остатки фенилаланина, тирозина или триптофана, или (е) амидной группе глутамина. Эти методы описаны в WO 87/05330 и у Aplin J.D. и Wriston J.C. Jr., CRC Crit. Rev. Biochem. 4, 1981, cc.259-306.
Удаление любого из углеводных остатков, присутствующих в антителе, можно осуществлять химически или ферментативно. Для химического дегликозилирования требуется обработка антитела таким соединением, как трифторметансульфоновая кислота, или эквивалентным соединением. Такая обработка приводит к расщеплению большей части или всех сахаров за исключением связующего сахара (N-ацетилглюкозамин или N-ацетилгалактозамин), при этом антитело остается интактным. Химическое дегликозилирование описано у Sojahr Н.Т. и Bahl О.Р., Arch. Biochem. Biophys. 259, 1987, cc.52-57 и у Edge A.S. и др., Anal. Biochem. 118, 1981, cc.131-137. Ферментативное расщепление углеводных остатков антител можно осуществлять, применяя различные эндо- и экзогликозидазы, описанные у Thotakura N.R. и Bahl O.P., Meth. Enzymol. 138, 1987, cc.350-359.
Другой тип ковалентной модификации антитела включает связывание антитела с одним из многочисленных небелковых полимеров, например, полиэтиленгликолем, полипропиленгликолем или полиоксиалкиленами, с помощью методов, описанных в US 4640835; 4496689; 4301144; 4670417; 4791192 или 4179337.
Другим объектом изобретения являются В-клетки, выделенные из трансгенного животного кроме человека, например трансгенной мыши, в которой экспрессируются человеческие антитела к IL-13Rα1, предлагаемые в изобретении. Предпочтительно выделенные В-клетки получают из трансгенного животного кроме человека, например трансгенной мыши, которую иммунизировали очищенным или обогащенным препаратом антигена IL-13Rα1 и/или клетками, экспрессирующими IL-13Rα1. Предпочтительно трансгенное животное кроме человека, например трансгенная мышь, имеет геном, который содержит трансген человеческой тяжелой цепи и трансген человеческой легкой цепи, которые кодируют все антитело, предлагаемое в изобретении, или его часть. Выделенные В-клетки затем иммортализуют для создания источника (например, гибридомы) человеческих антител к IL-13Rα1. Таким образом, настоящее изобретение относится также к гибридоме, обладающей способностью продуцировать человеческие моноклональные антитела, предлагаемые в изобретении. В одном из вариантов осуществления изобретения гибридома включает В-клетку, полученную из трансгенного животного кроме человека, например трансгенной мыши, геном которой содержит трансген человеческой тяжелой цепи и трансген человеческой легкой цепи, которые кодируют все антитело, предлагаемое в изобретении, или его часть, слитые с иммортализованной клеткой.
В конкретном варианте осуществления изобретения трансгенное животное кроме человека представляет собой трансгенную мышь, геном которой содержит трансген человеческой тяжелой цепи и трансген человеческой легкой цепи, которые кодируют все антитело, предлагаемое в изобретении, или его часть. Трансгенное животное кроме человека можно иммунизировать очищенным или обогащенным препаратом антигена IL-13Rα1 и/или клетками, экспрессирующими IL-13Rα1. Предпочтительно трансгенное животное кроме человека, например трансгенная мышь, обладает способностью продуцировать изотипы IgG1 человеческих моноклональных антител к IL-13Rα1.
Человеческие моноклональные антитела, предлагаемые в изобретении, можно получать путем иммунизации трансгенного животного кроме человека, например, трансгенной мыши, геном которой содержит трансген человеческой тяжелой цепи и трансген человеческой легкой цепи, которые кодируют все антитело, предлагаемое в изобретении, или его часть, очищенным или обогащенным препаратом антигена IL-13Rα1 и/или клетками, экспрессирующими IL-13Rα1. Затем получают В-клетки (например, селезеночные В-клетки) животного и сливают с клетками миеломы с получением иммортализованных клеток гибридомы, которые секретируют человеческие моноклональные антитела к IL-13Rα1.
Согласно предпочтительному варианту осуществления изобретения человеческие моноклональные антитела к IL-13Rα1 можно создавать с использованием трансгенных мышей, несущих части человеческой иммунной системы вместо мышиной системы. Такие трансгенные мыши, обозначенные в контексте настоящего описания как мыши линии «HuMab» («HuMab»), содержат минилокусы гена человеческого иммуноглобулина, который кодирует неперегруппированные гены человеческих иммуноглобулинов, включая гены тяжелой (µ- и γ-цепи) и легкой κ-цепи (гены константной области), в сочетании с целенаправленными мутациями, которые инактивируют эндогенные локусы µ- и κ-цепей (Lonberg N. и др., Nature 368, 1994, cc.856-859). В результате для мышей характерен пониженный уровень экспрессии мышиного IgM или IgK, и в ответ на иммунизацию интродуцированные трансгены человеческой тяжелой и легкой цепи подвергаются переключению класса и соматическим мутациям, что приводит к созданию обладающих высокой аффинностью человеческих моноклональных антител типа IgG (Lonberg N. и др., Nature 368, 1994, cc.856-859; см. обзор у Lonberg N., Handbook of Experimental Pharmacology 113, 1994, cc.49-101; Lonberg N. и Huszar, D., Intern. Rev. Immunol. 25, 1995, cc.65-93; и Harding F. и Lonberg N., Ann. N. Acad. Sci. 764, 1995, cc.536-546). Получение HuMAт-мышей описано у Taylor L. и др., Nucleic Acids Res. 20, 1992, cc.6287-6295; Chen J. и др., Int. Immunol. 5, 1993, cc.647-656; Tuaillon N. и др., Proc. Natl. Acad. Sci. USA 90, 1993, cc.3720-3724; Choi Т.К. и др., Nat. Genet. 4, 1993, cc.117-123; Chen J. и др., ЕМВО J. 12, 1993, cc.821-830; Tuaillon N. и др., J. Immunol. 152, 1994, cc.2912-2920; Lonberg N. и др., Nature 368, 1994, cc.856-859; Lonberg N., Handbook of Experimental Pharmacology 113, 1994, cc.49-101; Taylor L. и др., Int. Immunol. 6, 1994, cc.579-591; Lonberg N. и Huszar D., Intern. Rev. Immunol. 25, 1995, cc.65-93; Harding, F., and Lonberg, N., Ann. N. Acad. Sci. 764 (1995) 536-546; Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851, содержание всех указанных публикаций полностью включено в настоящее описание в качестве ссылки (см. также US 5545806; 5569825; 5625126; 5633425; 5789650; 5877397; 5661016; 5814318; 5874299; 5545807; 5770429; WO 98/24884; WO 94/25585; WO 93/1227; WO 92/22645 и WO 92/03918).
Для создания полностью человеческих моноклональных антител к IL-13Rα1 HuMAт-мышей можно иммунизировать очищенным или обогащенным препаратом антигена IL-13Rα1 и/или клетками, экспрессирующими IL-13Rα1, согласно общему методу, описанному у Lonberg N. и др., Nature 368, 1994, cc.856-859; Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851 и в WO 98/24884. Предпочтительно к моменту иммунизации мыши должны быть 6-16-недельного возраста. Например, для внутрибрюшинной иммунизации HuMAт-мышей можно использовать очищенный или обогащенный препарат растворимого антигена IL-13Rα1 (например, очищенного из экспрессирующих IL-13Rα1 клеток). В том случае, когда иммунизация с использованием очищенного или обогащенного препарата антигена IL-13Rα1 не приводит к продуцированию антител, мышей можно иммунизировать также клетками, экспрессирующими IL-13Rα1, например, линией опухолевых клеток, для стимуляции иммунных ответов. С помощью кумулятивного опыта с использованием различных антигенов установлено, что трансгенные HuМАт-мыши дают наиболее хороший ответ, когда осуществляют начальную внутрибрюшинную иммунизацию (i.p.) с использованием антигена в полном адъюванте Фрейнда с последующими чередующимися i.p.- или s.c.-иммунизациями каждую вторую неделю (например, в целом вплоть до шести иммунизации) антигеном в неполном адъюванте Фрейнда. Иммунный ответ можно оценивать в процессе осуществления протокола иммунизации с использованием образцов плазмы, получаемых из ретроорбитального сплетения. Плазму можно анализировать с помощью ELISA, и мышей, у которых обнаружены достаточные по уровню титры человеческого иммуноглобулина к IL-13Rα1, можно использовать для иммортализации соответствующих В-клеток. Мышей можно подвергать бустер-инъекциям антигеном внутривенно за 3-4 дня до умерщвления и удаления у них селезенки и лимфатических узлов. Следует ожидать, что для каждого антигена может потребоваться провести 2-3 слияния. Каждым антигеном можно иммунизировать несколько мышей. Например, можно иммунизировать всего от 5 до 12 HuМАт-мышей линий НСо7 и НСо12.
Мыши линии НСо7 имеют JKD-нарушение в генах эндогенной легкой цепи (каппа) (описанное у Chen J. и др., EMBO J. 12, 1993, cc.821-830), CMD-нарушение в генах эндогенной тяжелой цепи (описанное в примере 1 WO 01/14424), трансген КСо5 человеческой легкой каппа-цепи (описанный у Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851) и трансген НСо7 человеческой тяжелой цепи (описанный в US 5770429).
Мыши линии НСо12 имеют JKD-нарушение в генах эндогенной легкой цепи (каппа) (описанное у Chen J. и др., EMBO J. 12, 1993, cc.821-830), CMD-нарушение в генах эндогенной тяжелой цепи (описанное в примере 1 WO 01/14424), трансген КСо5 человеческой легкой каппа-цепи (описанный у Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851) и трансген НСо12 человеческой тяжелой цепи (описанный в примере 2 WO 01/14424).
Мышиные лимфоциты можно выделять и сливать с линий клеток мышиной миеломы с использованием основанных на применении ПЭГ стандартных протоколов получения гибридом. Затем образовавшиеся гибридомы подвергают скринингу в отношении производства специфических для антигена антител. Например, суспензионные культуры лимфоцитов, полученных из селезенки и лимфатических узлов иммунизированных мышей, сливают с 1/6 (по количеству) мышиных клеток SP 2/0, несекретирующих миелому (АТСС, CRL 1581), с 50% ПЭГ. Клетки высевают с плотностью примерно 2×105 в плоскодонный титрационный микропланшет, затем инкубируют в течение примерно 2 недель в избирательной среде.
Затем индивидуальные лунки подвергают скринингу с помощью ELISA в отношении человеческих моноклональных антител к IL-13Rα1 типа IgM и IgG. На стадии интенсивного роста гибридомы среду анализируют, как правило, через 10-14 дней. Секретирующие антитела гибридомы пересевают, вновь подвергают скринингу, и если они еще остаются позитивными в отношении человеческих моноклональных антител IgG к IL-13Rα1, то их можно субклонировать по меньшей мере дважды путем ограничивающего разведения. Затем стабильные субклоны культивируют in vitro в среде для культуры тканей для производства антитела с целью оценки характеристик.
Поскольку последовательности CDR ответственны за взаимодействия антитело-антиген, то можно экспрессировать рекомбинантные антитела, предлагаемые в изобретении, путем конструирования экспрессионных векторов, которые содержат последовательности CDR, предлагаемые в изобретении, в последовательностях каркасного участка из другого человеческого антитела (см., например, Riechmann L. и др., Nature 332, 1998, cc.323-327; Jones P. и др., Nature 321, 1986, cc.522-525; и Queen С. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.10029-10033). Такие последовательности каркасного участка можно получать из опубликованных баз данных ДНК, которые включают последовательности генов зародышевых линий человеческих антител. Эти последовательности зародышевых линий могут отличаться от последовательностей зрелых генов антител, поскольку они не содержат полностью собранные гены вариабельных областей, которые образуются с помощью V(D)J-слияния в процессе созревания В-клеток. Последовательности генов зародышевых линий могут отличаться также от последовательностей обладающего высокой аффинностью антитела из вторичного набора по индивидуальным параметрам вариабельной области.
Предпочтительным вариантом осуществления изобретения является фрагмент нуклеиновой кислоты, который кодирует полипептид, связывающийся с IL-13Rα1, где указанный полипептид ингибирует связывание IL-13 с IL-13Rα1 и выбран из группы, включающей
а) тяжелую цепь антитела, которая содержит CDR тяжелой цепи, представленные в SEQ ID NO:1, 3, 5, 7 или 9;
б) легкую цепь антитела, которая содержит CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10.
Реконструированные вариабельные области тяжелой и легкой цепи объединяют с последовательностями промотора, инициации трансляции, константной области, с 3'-нетранслируемой последовательностью, последовательностями полиаденилирования и терминации транскрипции с получением конструкций экспрессионных векторов. Конструкции для экспрессии тяжелой и легкой цепи можно объединять в одном векторе, их можно применять для котрансфекции, серийной трансфекции или раздельной трансфекции клеток-хозяев, которые затем сливают с получением индивидуальной клетки-хозяина, которая экспрессирует обе цепи.
Таким образом, в изобретении предложен способ получения рекомбинантного человеческого антитела, предлагаемого в изобретении, заключающийся в том, что экспрессируют нуклеиновую кислоту, которая кодирует
а) тяжелую цепь антитела, которая содержит CDR тяжелой цепи, представленные в SEQ ID NO:1, 3, 5, 7 или 9;
б) легкую цепь антитела, которая содержит CDR легкой цепи, представленные в SEQ ID NO:2, 4, 6, 8 или 10.
Изобретение относится также к применению антитела, предлагаемого в изобретении, для обнаружения IL-13Rα1 in vitro, предпочтительно, основанному на определении с помощью иммунологического анализа связывания IL-13Rα1 образца и антитела, предлагаемого в изобретении.
Другим объектом настоящего изобретения является композиция, например фармацевтическая композиция, содержащая одно человеческое моноклональное антитело или их комбинацию, или их антигенсвязывающий центр, предлагаемые в настоящем изобретении, в сочетании с фармацевтически приемлемым носителем.
В контексте настоящего описания понятие «фармацевтически приемлемый носитель» включает любой и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, придающие изотоничность и замедляющие абсорбцию агенты и т.п., которые являются физиологически совместимыми. Предпочтительно носитель можно применять для внутривенного, внутримышечного, подкожного, парентерального, спинального или эпидермального введения (например, путем инъекции или инфузии).
Понятие «фармацевтически приемлемая соль» обозначает соль, которая сохраняет требуемую биологическую активность антитела и не обладает никакими нежелательными токсикологическими действиями (см., например, Berge S.M. и др., J. Pharm. Sci. 66, 1977, cc.1-19). Такие соли подпадают под объем настоящего изобретения. Примерами таких солей являются кислотно-аддитивные соли и соли присоединения оснований. Кислотно-аддитивные соли включают соли, полученные из нетоксичных неорганических кислот, такие как соли соляной кислоты.
Композицию, предлагаемую в настоящем изобретении, можно вводить различными методами, известными в данной области. Как должно быть очевидно специалисту в данной области, путь и/или механизм введения должен варьироваться в зависимости от требуемых результатов.
Для введения соединения, предлагаемого в изобретении, с помощью конкретных путей введения может оказаться необходимым наносить покрытие на соединение из материала, препятствующего его инактивации, или осуществлять совместное введение соединения с таким материалом. Например, соединение можно вводить пациенту в соответствующем носителе, например, липосомах или разбавителе. Фармацевтически приемлемые разбавители включают физиологические и водные буферные растворы.
Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления без дополнительной подготовки стерильных инъецируемых растворов или дисперсий. Применение таких сред и агентов для фармацевтически активных субстанций известно в данной области.
Понятия «парентеральное введение» и «введенный парентерально» в контексте настоящего описания означают пути введения, отличные от энтерального и местного применения, как правило, путем инъекции, и включают (но, не ограничиваясь ими) внутривенную, внутримышечную, внутриартериальную, подоболочечную, внутрикапсулярную, внутриглазничную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, подкутикулярную, внутрисуставную, субкапсулярную, субарахноидальную, интраспинальную, эпидуральную и интрастернальную инъекцию и инфузию.
Указанные композиции могут содержать также адъюванты, такие как консерванты, смачивающие агенты, эмульгаторы и диспергирующие агенты. Предупреждение присутствия микроорганизмов можно гарантировать как применением процессов стерилизации (см. выше), так и асептических условий производства, и путем введения различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенола, сорбиновой кислоты и т.п. Может также требоваться введение в композицию придающих изотоничность агентов, таких как сахара, хлорид натрия и т.п. Кроме того, для пролонгированной абсорбции инъецируемой фармацевтической формы можно вводить агенты, которые замедляют абсорбцию, такие как моностеарат алюминия и желатин.
Независимо от выбранного пути введения соединения, предлагаемые в настоящем изобретении, которые можно применять в виде пригодной гидратированной формы, и/или фармацевтические композиции, предлагаемые в настоящем изобретении, приготавливают в виде фармацевтически приемлемых лекарственных форм с помощью общепринятых методов, известных специалисту в данной области.
Фактические уровни доз действующих веществ в фармацевтических композициях, предлагаемых в настоящем изобретении, могут варьироваться так, чтобы они содержали количество действующего вещества, которое является эффективным для получения требуемого терапевтического ответа у конкретного пациента в зависимости от состава и пути введения, не являясь при этом токсичными для пациента. Выбранный уровень доз должен зависеть от разнообразных фармакокинетических факторов, таких как активность конкретных применяемых композиций, предлагаемых в настоящем изобретении, путь введения, время введения, скорость экскреции конкретного применяемого соединения или его сложного эфира, соли или амида, продолжительность лечения, другие лекарственные средства, соединения и/или материалы, применяемые в сочетании с конкретными композициями, возраст, пол, вес, общее состояние здоровья и предыдущая история болезни пациента, подлежащего лечению, и подобных факторов, которые хорошо известны в медицине.
Композиция должна быть стерильной и текучей в той степени, чтобы композицию можно было вводить с помощью шприца. Помимо воды носитель может представлять собой изотоничный забуференный физиологический раствор, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.) и их приемлемые смеси.
Требуемую текучесть можно поддерживать, например, нанося покрытие, с использованием, например, лецитина, поддерживая требуемый размер частиц в случае дисперсии, или с использованием поверхностно-активных веществ. Во многих случаях предпочтительным является добавление в композицию придающих изотоничность агентов, например сахаров, полиспиртов, таких как маннит или сорбит, и хлорида натрия. Для достижения продолжительной абсорбции инъецируемых композиций можно, например, включать в состав композиции агент, замедляющий абсорбцию, например моностеарат алюминия или желатин.
Приведенные ниже примеры, ссылки, перечень последовательностей и чертежи даны с целью лучшего понимания настоящего изобретения, полный объем которого представлен в прилагаемой формуле изобретения. Следует понимать, что в изложенные процессы можно вносить модификации без отклонения от сущности изобретения.
Описание перечня последовательностей
SEQ ID NO:1 вариабельная область тяжелой цепи HuМАт LC5002-002
SEQ ID NO:2 вариабельная область легкой цепи НuМАт LC5002-002
SEQ ID NO:3 вариабельная область тяжелой цепи НuМАт LC5002-003
SEQ ID NO:4 вариабельная область легкой цепи НuМАт LC5002-003
SEQ ID NO:5 вариабельная область тяжелой цепи НuМАт LC5002-005
SEQ ID NO:6 вариабельная область легкой цепи НuМАт LC5002-005
SEQ ID NO:7 вариабельная область тяжелой цепи НuМАт LC5002-007
SEQ ID NO:8 вариабельная область легкой цепи НuМАт LC5002-007
SEQ ID NO:9 вариабельная область тяжелой цепи НuМАт LC5002-018
SEQ ID NO:10 вариабельная область легкой цепи НuМАт LC5002-018
SEQ ID NO:11 константная область легкой κ-цепи
SEQ ID NO:12 константная область тяжелой γ1-цепи
Описание чертежей
На чертежах показано:
на фиг.1 - связывание антител к IL-13Rα1 с иммобилизованным рекомбинантным человеческим полипептидом IL-13Rα1. Представлены данные для поликлонального кроличьего антитела к человеческому IL-13Rα1 AF152 (фирма R&D systems) и антитела к KLH, используемого в качестве отрицательного контроля для НuМАт;
на фиг.2 - ингибирование антителами к IL-13Rα1 связывания IL-13 с иммобилизованным рецептором IL-13Rα1/IL-4Rα;
на фиг.3 - блокирование антителами к IL-13Rα1 связывания IL-13 с СНО-клетками (экспрессирующими IL-13Rальфа1 и IL-4Rα2). Представлены данные для поступающего в продажу поликлонального антитела к IL-13Rα1 AF152 (фирма R&D Systems, Миннеаполис, шт.Миннесота), которое использовали в качестве положительного контроля;
на фиг.4 - связывание антител к IL-13Rα1 с hIL-13Rα1 и характеристики связывания с функционально близкими рецепторами hIL-13Rα2 и hIL-4Rα;
на фиг.5 - способность антител к IL-13Rα1 связываться с иммобилизованным рекомбинантным мышиным полипептидом IL-13Rα1. Представлены данные для поликлонального козьего антитела к человеческому IL-13Rα1 AF152 (фирма R&D Systems) и антитела к KLH, используемого в качестве отрицательного контроля для НuМАт.
Примеры
Пример 1
Получение гибридом
Человеческие моноклональные антитела, предлагаемые в изобретении, можно получать путем иммунизации трансгенного животного кроме человека, например трансгенной мыши, геном которой содержит трансген человеческой тяжелой цепи и трансген человеческой легкой цепи, которые кодируют все антитело, предлагаемое в изобретении, или его часть, клетками, экспрессирующими IL-13Rα1. Затем получают В-клетки (например, селезеночные В-клетки) животного и сливают с клетками миеломы с получением иммортализованных клеток гибридомы, которые секретируют человеческие моноклональные антитела к IL-13Rα1. Человеческие моноклональные антитела к человеческому IL-13Rα1 можно создавать с использованием трансгенных мышей, несущих части человеческой иммунной системы вместо мышиной системы. Такие трансгенные мыши, обозначенные в контексте настоящего описания как мыши линии «НuМАт», содержат минилокус гена человеческого иммуноглобулина, который кодирует неперегруппированные гены человеческих иммуноглобулинов, включая гены тяжелой (µ- и γ-цепи) и легкой κ-цепи (гены константной области), в сочетании с целенаправленными мутациями, которые инактивируют эндогенные локусы µ- и κ-цепей (Lonberg N. и др., Nature 368, 1994, cc.856-859). В результате для мышей характерен пониженный уровень экспрессии мышиного IgM или IgK, и в ответ на иммунизацию интродуцированные трансгены человеческой тяжелой и легкой цепи подвергаются переключению класса и соматическим мутациям для создания обладающих высокой аффинностью человеческих моноклональных антител IgG-класса. Для создания полностью человеческих моноклональных антител к IL-13Rα1 НuМАт-мышей можно иммунизировать клетками, экспрессирующими IL-13Rα1, согласно общему методу, описанному у Lonberg N. и др., Nature 368, 1994, cc.856-859; Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851 и в WO 98/24884. Предпочтительно к моменту иммунизации мыши должны быть 6-16-недельного возраста. Например, для внутрибрюшинной иммунизации НuМАт-мышей можно использовать клетки, трансфектированные IL-13Rα1. Иммунный ответ можно оценивать в процессе осуществления протокола иммунизации с использованием образцов плазмы, получаемых из ретроорбитального сплетения. Плазму можно анализировать с помощью ELISA и/или FACS (клеточный сортер с возбуждением флуоресценции). Мышей, у которых обнаружены достаточные по уровню титры человеческого иммуноглобулина к человеческому IL-13Rα1, можно использовать для иммортализации соответствующих В-клеток. Мышей можно подвергать бустер-инъекциям антигеном внутривенно за 3-4 дня до умерщвления и удаления у них селезенки и лимфатических узлов. Например, можно иммунизировать НuМАт-мышей линий НСо7 и НСо12. Мыши линии НСо7 имеют JKD-нарушение в генах эндогенной легкой цепи (каппа) (описанное у Chen J. и др., EMBO J. 12, 1993, cc.821-830), CMD-нарушение в генах эндогенной тяжелой цепи (описанное в примере 1 WO 01/14424), трансген KCo5 человеческой легкой каппа-цепи (описанный у Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851) и трансген НСо7 человеческой тяжелой цепи (описанный в US 5770429). Мыши линии НСо12 имеют JKD-нарушение в генах эндогенной легкой цепи (каппа) (описанное у Chen J. и др., EMBO J. 12, 1993, cc.821-830), CMD-нарушение в генах эндогенной тяжелой цепи (описанное в примере 1 WO 01/14424), трансген КСо5 человеческой легкой каппа-цепи (описанный у Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851) и трансген НСо12 человеческой тяжелой цепи (описанный в примере 2 WO 01/14424). Мышиные лимфоциты можно выделять и сливать с линий клеток мышиной миеломы с использованием основанных на применении ПЭГ стандартных протоколов получения гибридом. Затем образовавшиеся гибридомы подвергают скринингу в отношении производства специфических для антигена антител. Например, суспензионные культуры лимфоцитов, полученных из селезенки и лимфатических узлов иммунизированных мышей, сливают с клетками мышиной миеломы, несекретирующими SP 2/0 (АТСС, CRL 1581), с 50% ПЭГ. Клетки высевают с плотностью примерно 0,75×105 в плоскодонный титрационный микропланшет, затем инкубируют в течение примерно 2 недель в избирательной среде. Затем индивидуальные лунки подвергают скринингу с помощью ELISA и/или FACS в отношении человеческих моноклональных антител к IL-13Rα1 типа IgM и IgG. На стадии интенсивного роста гибридомы секретирующие антитела гибридомы пересевают, вновь подвергают скринингу, и если они еще остаются позитивными в отношении человеческих моноклональных антител типа IgG к IL-13Rα1, то их можно субклонировать по меньшей мере дважды путем ограничивающего разведения. Затем стабильные субклоны культивируют in vitro в среде для культуры тканей для производства антитела с целью оценки характеристик.
Процедура иммунизации трансгенных мышей
Три НСо7-мыши (3 самца), линия GG2201 (фирма Medarex, Сан-Хосе, шт.Калифорния, США), и 2 НСо12-мыши (1 самец и 1 самка), штамм GG2198 (фирма Medarex, Сан-Хосе, шт.Калифорния, США), подвергали иммунизации с использованием 1×106 клеток линии HEK293, трансфектированных экспрессионным вектором, несущим IL-13Rα1. Проводили всего 8 иммунизации, осуществляя поочередно внутрибрюшинные (i.p.) и подкожные (s.c.) введения в основание хвоста. Для первой иммунизации 100 мкл 1×106 HEK293: IL-13Rα1-клеток смешивали с 100 мкл полного адъюванта Фрейнда (CFA; фирма Difco Laboratories, Детройт, США). Для всех других иммунизации 100 мкл клеток в ЗФР смешивали с 100 мкл неполного адъюванта Фрейнда (ICFA; фирма Difco).
Бустер-иммунизация мышей
После установления того факта, что титры в сыворотке антител к IL-13Rα1 являются достаточными, мышей дополнительно дважды подвергали бустер-инъекции путем внутривенного (i.v.) введения 1×106 HEK293: IL-13Rα1-клеток в 200 мкл ЗФР за 4 и 3 дня до слияния.
Пример 2
Оценка с помощью ELISA способности НuМАт связываться с иммобилизованным IL-13Rα1
Для определения способности антител, предлагаемых в изобретении, связываться с рекомбинантным IL-13Rα1 внеклеточный домен IL-13Rα1 (фирма R&D Systems, Великобритания) растворяли в ЗФР (1 мкг/мл) и давали адсорбироваться на титрационные микропланшеты (типа NUNC Maxisorb) путем инкубации в течение ночи при 4°С. После отмывки планшетов буфером для отмывки (ОБ = 0,9% NaCl; 0,1% Tween® 20) неспецифические сайты связывания блокировали путем добавления 100 мкл буфера для инкубации (ИБ = ЗФР, дополненный 1% кротеина С и 0,1% Tween® 20) и инкубации в течение 30 мин при комнатной температуре (КТ). Затем добавляли серийные разведения НuМАт и контрольные антитела (100 мкл/лунку; разведения в ИБ) и инкубировали в течение 1 ч при КТ. Планшеты отмывали еще один раз и связанные человеческие антитела выявляли путем инкубации с конъюгированным с пероксидазой кроличьим антителом к каппа-цепи человеческого IgG (фирма DAKO, Дания) в конечном разведении 1:500 в ИБ. Поликлональные козьи антитела к hIL-13Rα1 выявляли с помощью конъюгированного с пероксидазой поликлонального ослиного антитела к козьему IgG (фирма Santa Cruz; разведение 1:1000 в ИБ). После инкубации в течение 1 ч при КТ и последующей отмывки планшеты обрабатывали при КТ в темноте готовым к применению раствором ABTS® (фирма Roche Diagnostics GmbH). Абсорбцию измеряли при 405 нм после того, как при использовании самой высокой концентрации достигалась достаточная величина ОП.
Все тестируемые антитела к IL-13Rальфа1 обладали способностью связываться с иммобилизованными внеклеточными доменами человеческого IL-13Rα1. Значения ЕС50, определенные в эксперименте, находились в диапазоне 0,5-2 нМ для различных протестированных LC-антител. Используемое в качестве отрицательного контроля для НuМАт антитело к KLH не связывалось с иммобилизованными внеклеточными доменами IL-13Rα1. Поликлональное козье антитело к человеческому IL-13Rα1, которое применяли в качестве положительного контроля, также эффективно связывалось с иммобилизованными внеклеточными доменами IL-13Rα1 (фиг.1).
Пример 3
Ингибирование связывания IL-13 с гетеродимером IL-13Rα1/IL-4Rα (ELISA)
Титрационные микропланшеты сенсибилизировали в течение ночи при 4°С на шейкере 100 мкл химерного белка hIL-13Rα1:hFc (фирма R&D Systems, Великобритания) в ЗФР в концентрации 3 мкг/мл. После отмывки планшетов с помощью ОБ добавляли серийные разведения НuМАт и используемые в качестве контроля антитела (100 мкл/лунку; разведения в ИБ) и инкубировали в течение 30 мин при КТ. Планшеты снова отмывали и затем добавляли смесь IL-13 (фирма R&D Systems, Великобритания; 0,5 мкг/мл; разведение в ИБ) и IL-4Rα (фирма R&D Systems, Великобритания; 0,75 мкг/мл; разведения в ИБ) и инкубировали в течение 1 ч при КТ. После отмывки планшетов добавляли 100 мкл биотинилированного антитела к IL-13 (BAF213; фирма R&D Systems, Великобритания) в концентрации 0,4 мкг/мл и инкубировали в течение 1 ч при КТ. После отмывки планшетов проводили обнаружение связанного IL-13 с помощью связанного с пероксидазой стрептавидина (фирма Roche Diagnostics GmbH, Германия) в разведении 1:5000 в ИБ (период инкубации 1 ч при КТ). И, наконец, планшеты отмывали и обрабатывали готовым к применению раствором ABTS® (фирма Roche Diagnostics GmbH, Германия) при комнатной температуре (КТ) в темноте. Абсорбцию измеряли через 45-60 мин при 405 нм.
Антитела LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018 обладали способностью ингибировать связывание IL-13 с гетеродимерным рецептором, причем максимальные величины ингибирования составляли примерно от 50 до 80-85%. В качестве положительного контроля использовали AF152 (поликлональное кроличье антитело). Как и ожидалось, используемое в качестве отрицательного контроля антитело к KLH, не ингибировало связывание IL-13 с гетеродимерным рецептором. Значения IC50, полученные для LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018, составляли от 1,5 до 10,1 нМ (фиг.2).
Пример 4
Анализ связывания радиолигандов
Анализ связывания 125I-IL-13 проводили с использованием СНО-клеток, экспрессирующих человеческий IL-13Rα1 и человеческий IL-4Rα, в буфере для связывания (25 мМ HEPES, 150 м MNaCl, 1 мМ CaCl2, 5 мМ MgCl2 и 0,5% бычьего сывороточного альбумина, значение pH доводили до pH 7,2). 1×105 клеток на лунку смешивали с антителами и осуществляли предварительную инкубацию в течение периода времени от 15 мин до 1 ч. Добавляли 0,1 нМ 125I-IL-13 и смесь инкубировали в течение 4 ч при 4°С. Концентрацию используемого в анализе 125I-IL-13 определяли с помощью анализа насыщения связывания, конкурентного анализа и определения вносимого количества 125I-IL-13, требуемого для достижения равновесия связывания с клеточной линией. Образцы собирали на фильтрационный планшет GF/C, предварительно обработанный 1% PEI/0,5% БСА, и осуществляли подсчет с помощью сцинтилляционного счетчика типа Packard TopCount. Анализ данных проводили с помощью PRISM с использованием аппроксимации нелинейной регрессионной кривой (фирма GraphPad Software, Сан-Диего, шт.Калифорния).
Все протестированные антитела к IL-13Ralpha1 блокировали связывание меченного IL-13 с комплексом IL-13Rα1/IL-4Rα. Рассчитанные значения IC50 составляли от 0,09 до 0,32 нМ для антител LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018 и 84,8 нМ для AF152 (фиг.3).
Пример 5
Оценка ингибирования НuМАт индуцируемой IL-13 повышающей регуляции CD23 на человеческих В-клетках и моноцитах
Мононуклеарные клетки периферической крови (РВМС) выделяли путем центрифугирования в градиенте плотности фикол-пак. После отмывки клеток с помощью RPMI их ресуспендировали в RPMI/10% ФТС и вносили с плотностью 3×105 РВМС/лунку (объем 50 мкл) в 96-луночный плоскодонный титрационный микропланшет (фирма Corning Incorporated Costar). Затем добавляли 25 мкл антитела к человеческому CD40 (фирма Immunotech) в конечной концентрации 0,5 мкг/мл в RPMI/10% ФТС и 25 мкл антитела к человеческому IgA+IgG+IgM (фирма Immunoresearch) в конечной концентрации 10 мкг/мл в RPMI/10% ФТС. После этого добавляли серийные разведения НuМАт и контрольных антител (50 мкл/лунку; разведения в RPMI/10% ФТС) и клетки инкубировали в течение 30 мин в инкубаторе (37°С; 5% СО2). Затем добавляли рекомбинантный человеческий IL-13 (фирма R&D Systems) в конечной концентрации 0,67 нг/мл (50 мкл/лунку) и клетки инкубировали в течение 72 ч при 37°С/5% СО2. После этой инкубации планшеты центрифугировали и среду удаляли аспирацией. Для отделения прилипших клеток добавляли 200 мкл аккутазы (РАА) и клетки инкубировали в течение примерно 5 мин при 37°С; 5% СО2. Клетки отделяли путем повторной отмывки и переносили в круглодонный планшет. После центрифугирования и аспирации супернатантов клетки инкубировали с 200 мкл смеси антитела к CD23-ФЭ (фосфатидилэтаноламин), антитела к CD20-ФИТЦ (флуоресцинизотиоцианат) и антитела к CD14-APC (все антитела получали от фирмы BD Biosciences Pharmingen, Сан-Диего, шт.Калифорния). Клетки инкубировали в течение 30 мин при 4°С, затем центрифугировали и супернатанты удаляли аспирацией. Эту стадию отмывки повторяли еще один раз и, наконец, клетки ресуспендировали в 200 мкл ЗФР/0,1% человеческого сывороточного альбумина и анализировали с помощью проточного цитометра типа FACS Calibur (фирма BD Biosciences Pharmingen, Сан-Диего, шт.Калифорния) с использованием программы CellQuest. В большинстве случаев собирали по 10000 вариантов и пропускали через светорассеивающее дискриминационное окно для отбора только жизнеспособных лимфоцитов и моноцитов. Клетки предварительно разделяли на CD9-позитивный кластер В-лимфоцитов или CD14-позитивный кластер моноцитов и затем подвергали анализу в отношении экспрессии CD23.
Полученные значения IC50, характеризующие ингибирование повышающей регуляции CD23 на В-лимфоцитах, составляли от 0,5 до более чем 70 нМ для антител LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018 и 13,6 нМ для AF152. Близкий профиль был выявлен при анализе ингибирования индуцируемой IL-13 повышающей регуляции CD23 на человеческих моноцитах. На моноцитах значения IC50 составляли от 0,1 до 62,8 нМ для антител LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018 и 62,9 нМ для AF152.
Пример 6
Анализ пролиферации TF-1-клеток в ответ на IL-13 или IL-4, используемые в качестве стимула
TF-1-клетки (АТСС № CRL 2003) выращивали в средах, содержащих модифицированную по способу АТСС среду RPMI, 10% ФТС, 1× пенициллин/стрептомицин, 2 нг/мл GM-CSF (колониестимулирующий фактор гранулоцитов и макрофагов). В течение одного дня перед анализом клетки выдерживали в среде, не содержащей GM-CSF. 5×103 клеток на лунку инкубировали с соответствующими концентрациями антител к IL-13Rα1 в течение 1 ч при 37°С. Затем клетки стимулировали 2 нг/мл человеческого IL-13 (фирма R&D Systems, Миннеаполис, шт.Миннесота) или 0,1 нг/мл человеческого IL-4 (фирма R&D Systems, Миннеаполис, шт.Миннесота) и инкубировали в течение 48 ч при 37°С. В клетки импульсно вносили 3Н-тимидин (0,5 мкКи) и инкубировали в течение 16-18 ч при 37°С. Образцы собирали на GFC-планшеты, предварительно обработанные 1% PEI/0,25% БСА, с использованием харвестера типа Perkin Elmer Filtermate 96. GFC-планшеты считывали с помощью сцинтилляционного счетчика типа Perkin Elmer Top. Анализ данных проводили с помощью PRISM с использованием аппроксимации нелинейной регрессионной кривой (фирма GraphPad Software, Сан-Диего, шт.Калифорния).
В этом анализе не было обнаружено никаких ингибирующих свойств антитела к KLH. То же самое было установлено для LC5002-007. Все другие антитела ингибировали ответ, хотя даже LC5002-007 ингибировало ответ с более высоким значением IC, чем другие антитела. Для различных антител были установлены следующие значения IC50: 13,50 нМ для AF152, 9,21 нМ для LC5002-002, 3,07 нМ для LC5002-003 и 0,39 нМ для LC5002-005. Близкий профиль был выявлен для индуцируемой IL-4 пролиферации TF-1-клеток, однако эффективность антител была более низкой по сравнению с индуцируемыми IL-13 ответами. Значения IC50 для индуцируемой IL-4 пролиферации составляли 0,02 нМ для антитела к IL4R, 74,37 нМ для AF152 и от 4,68 до 60 нМ для антител LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018.
Пример 7
Ингибирование производства эотаксина человеческими легочными фибробластами в ответ на обработку IL-13
Анализ проводили с использованием клеток линии HFL-1 (человеческие легочные фибробласты, АТСС № CCL-153). Клетки высевали с плотностью 100000 клеток на лунку в 12-луночный планшет и инкубировали в течение 72 ч при 37°С до достижения конфлюэнтности. Затем клетки выращивали в бессывороточной среде в течение 24 ч и обрабатывали антителом к IL-13Rα1 в течение 1 ч при 37°С. После этой обработки клетки стимулировали с помощью 10 нг/мл IL-13 (фирма R&D Systems, Миннеаполис, шт.Миннесота) в течение 48 ч при 37°С. Супернатанты собирали и обнаружение эотаксина проводили с помощью набора для ELISA, поступающего в продажу от фирмы R&D Systems (каталожный номер DTX00). Абсорбцию измеряли с помощью ридера для микропланшетов типа Spectromax и данные анализировали с помощью PRISM (фирма GraphPad Software, Сан-Диего, шт.Калифорния).
Протестированные антитела обладали различной способностью ингибировать высвобождение эотаксина. За исключением LC5002-007 все другие протестированные антитела обладали определенной ингибирующей способностью. Рассчитанные по трем-четырем различным экспериментам средние значения IC50 составляли 11,5 нМ для AF152 и от 2,45 до 19,8 нМ для антител LC5002-002, LC5002-003, LC5002-005, LC5002-007 и LC5002-018.
Пример 8
Ингибирование индуцируемого IL-13 фосфорилирования Stat-6 в человеческих бронхиальных гладкомышечных клетках
Человеческие бронхиальные гладкомышечные клетки (BSMC; фирма Clonetics, каталожный номер СС-2576) выращивали, следуя инструкциям производителя. Клетки выращивали в 12-луночных планшетах для культур тканей до достижения конфлюэнтности. Клетки выращивали в течение 24 ч в бессывороточной среде и добавляли антитела в различных количествах. Планшеты инкубировали в течение 1 ч и затем стимулировали с помощью 2,5 нг/мл IL-13 (фирма R&D System). После инкубации в течение 15 мин супернатант удаляли, клетки промывали фосфатным буфером и добавляли 100 мкл буфера для лизиса. Смесь облучали в течение короткого промежутка времени ультразвуком на льду и центрифугировали. Лизат использовали для обнаружения фосфорилированного Stat-6 методом Вестерн-блоттинга. Такое же количество белка вносили на ДСН-гель, разгоняли и переносили на мембрану. Антитело к Stat-6 получали от фирмы Santa Cruz Biotechnology (каталожный номер SC-11762R) и использовали вторичное антитело, связанное с пероксидазой. Обнаружение проводили с использованием системы ECL Plus фирма Amersham (каталожный номер RPN 2132). Количественную оценку проводили с помощью устройства типа Typhoon 9400 Imager.
Оба НuМАт, протестированных в этом анализе (LC50002-003 и LC5002-005), ингибировали индуцируемое IL-13 фосфорилирование Stat-6. Эффективность, выявленная в этом анализе, была близкой к эффективности, полученной при проведении других функциональных анализов. Рассчитанные значения IC50 составляли 18,64 нМ для AF152, 5,98 нМ для LC5002-003 и 1,18 нМ для LC5002-005.
Пример 9
Клонирование и анализ последовательности вариабельных областей НuМАт к hIL-13Rα1 (легкая κ- и тяжелая γ1-цепи)
Нуклеотидные последовательности, кодирующие вариабельную область VL легкой цепи и вариабельную область VH тяжелой цепи НuМАт к hIL-13Rα1, выделяли с помощью стандартной процедуры синтез кДНК/ПЦР. Общую РНК получали из 1×106-1×107 клеток гидридомы с использованием набора GeneRacer™ (фирма Invitrogen). Полученную из гибридомы РНК использовали в качестве матрицы для синтеза первой цепи кДНК и лигирования с входящим в набор GeneRacer™ олиго-дТ-праймером. Синтез второй цепи кДНК и последующую ПЦР-амплификацию кДНК-фрагментов, кодирующих VL и VH, проводили с использованием обратных праймеров для легкой и тяжелой цепей, комплементарных нуклеотидным последовательностям константной области легкой κ- и тяжелой γ1-цепи и 5'-специфических праймеров из набора GeneRacer™ соответственно. ПЦР-продукты клонировали с использованием набора для клонирования ТОРО™ ТА фирмы InvitrogenTM Life Technologies и pCR4-TOPO™ в качестве клонирующего вектора. Клонированные ПЦР-продукты идентифицировали путем рестрикционного картирования соответствующих плазмид с использованием EcoRI для расщепления и ожидаемых/рассчитанных размеров фрагментов ДНК, составляющих примерно 740 и 790 пар оснований для VL и VH соответственно. Последовательность ДНК клонированных ПЦР-фрагментов определяли путем двухцепочечного секвенирования. Для общей обработки данных использовали пакет программ GCG (Группа компьютерной генетики (Genetics Computer Group), Мэдисон, шт.Висконсин), версия 10.2, и Vector-NTI 8 (фирма InforMax, Inc). Последовательности ДНК и белка сравнивали с помощью модуля CLUSTALW GCG. Сравнительный анализ последовательностей проводили с помощью программы GENEDOC (версия 2.1).
Пример 10
Конструирование экспрессионных плазмид для НuМАт к hIL-13Rα1 IgG1-изотипа
Гены, кодирующие легкую и тяжелую цепь НuМАт к hIL-13Rα1, собирали по отдельности в экспрессионных векторах, предназначенных для клеток млекопитающих. При этом сегменты генов, кодирующих вариабельную область легкой цепи (VL) НuМАт к hIL-13Rα1 и константную область человеческой легкой κ-цепи (CL, SEQ ID NO:11), соединяли с сегментами генов, кодирующих вариабельную область тяжелой цепи (VH) НиМАт к hIL-13Rα1 и константную область человеческой тяжелой γ1-цепи (CH1-шарнир-CH2-CH3, SEQ ID NO:12). Общая информация, касающаяся нуклеотидных последовательностей человеческих легких и тяжелых цепей, из которых можно выводить наиболее часто встречающиеся кодоны, дана у Kabat E.A., и др., Sequences of Proteins of Immunological Interest, 5-е изд., NIH Publication No. 91-3242 (1991). Единица транскрипции легкой κ-цепи НuМАт к hIL-13Rα1 состоит из следующих элементов:
- немедленно-ранний энхансер и промотор из человеческого цитомегаловируса (HCMV),
- синтетический 5'-UT, включающий последовательность Козака,
- сигнальная последовательность тяжелой цепи мышиного иммуноглобулина, включающая интрон сигнальной последовательности,
- клонированная кДНК вариабельной области легкой цепи НuМАт к hIL-13Rα1, содержащая уникальный сайт рестрикции BsmI на 5'-конце и сайт донора сплайсинга и уникальный сайт рестрикции NotI на 3'-конце,
- человеческий ген константной области κ-цепи, включающий интрон 2 мышиного энхансера Ig-каппа [Picard D. и Schaffner W., Nature 307, 1984, cc.80-82], и
- сигнальная последовательность полиаденилирования («поли-А») κ-цепи человеческого иммуноглобулина.
Единица транскрипции тяжелой γ1-цепи НuМАт к hIL-13Rα1 состоит из следующих элементов:
- немедленно-ранний энхансер и промотор из человеческого цитомегаловируса (HCMV),
- синтетический 5'-UT, включающий последовательность Козака,
- модифицированная сигнальная последовательность тяжелой цепи мышиного иммуноглобулина, включающая интрон сигнальной последовательности,
- клонированная кДНК вариабельной области тяжелой цепи НuМАт к hIL-13Rα1, содержащая уникальный сайт рестрикции BsmI на 5'-конце и сайт донора сплайсинга и уникальный сайт рестрикции NotI на 3'-конце,
- человеческий ген константной области тяжелой γ1-цепи, включающий µ-энхансер мышиного Ig (Neuberger M.S., EMBO J. 2, 1983, cc.1373-1378),
- сигнальная последовательность полиаденилирования («поли-А») γ1-цепи человеческого иммуноглобулина.
Функциональные элементы экспрессионных плазмид легкой κ-цепи и тяжелой γ1-цепи НuМАт к hIL-13Rα1:
Помимо полигенного экспрессирующего кластера, включающего легкую κ-цепь и тяжелую γ1-цепь НuМАт к hIL-13Rα1, эти плазмиды содержат:
ген, обусловливающий устойчивость к гигромицину,
сайт инициации репликации, oriP, вируса Эпштейна-Барра (EBV),
сайт инициации репликации из вектора pUC18, обеспечивающий репликацию этой плазмиды в Е.coli, и
ген β-лактамазы, который придает устойчивость Е.coli к ампициллину.
Пример 11
Конструирование экспрессионных плазмид для мутантного (вариантного) IgG1 к hIL-13Rα1
Экспрессионные плазмиды, кодирующие мутантные тяжелые γ1-цепи антитела к hIL-13Rα1, можно создавать путем сайтнаправленного мутагенеза экспрессионных плазмид дикого типа с использованием набора для сайтнаправленного мутагенеза типа QuickChangeTM (фирма Stratagene), и они приведены в таблице 1. Нумерация аминокислот соответствует EU-нумерации (Edelman G.M. и др., Proc. Natl. Acad. Sci. USA 63, 1969, cc.78-85; Kabat E.A., и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, NIH Publication No.91-3242, Bethesda, MD (1991)).
Пример 12
Получение рекомбинантных НuМАт к hIL-13Rα1
Рекомбинантные НuМАт получали путем кратковременной трансфекции прикрепленных клеток HEK293-EBNA (АТТС CRL-10852), которые культивировали в среде DMEM (фирма Gibco), дополненной 10% ФТС с ультранизким содержанием IgG (фирма Gibco), 2 мМ глутамином (фирма Gibco), 1 об.% заменимых аминокислот (фирма Gibco) и 250 мкг/мл G418 (фирма Roche Diagnostics GmbH, Германия). Для трансфекции использовали трансфекционный реагент Fugene™ 6 (фирма Roche Diagnostics GmbH, Германия) в соотношении реагент (мкл): ДНК (мкг) от 3:1 до 6:1. Легкие и тяжелые цепи иммуноглобулина экспрессировали в двух различных плазмидах, используя молярное соотношение плазмид, кодирующих легкую цепь и тяжелую цепь, от 1:2 до 2:1. Содержащие НuМАт супернатанты клеточной культуры собирали через 4-11 дней после трансфекции.
Общую информацию, касающуюся рекомбинантной экспрессии человеческого антитела, например, в клетках линии НЕК293, можно почерпнуть из публикации: Meissner Р. и др., Biotechnol. Bioeng. 75, 2001, cc.197-203.
Пример 13
а) Анализ аффинности НuМАт LC5002-003, -005 и -007 с использованием химерного hIL-13Rα1:hFc
Для анализа взаимодействий использовали устройство Biacore 3000. В качестве буфера для погона и реакционного буфера применяли HBS-P (10 мМ HEPES, 150 мМ NaCl, 0,005% полисурфактанта Р, pH 7,4) при 25°С. Иммобилизующие молекулы (козье антитело к человеческому IgG, Fcγ-специфическое) сочетали с амином в концентрации 20 мкг/мл при скорости потока 5 мкл/мин в течение 20 мин. НuМАт инъецировали в концентрации 1 мкг/мл при скорости потока 10 мкл/мин в течение 1 мин. Блокирование свободного козьего антитела к человеческому IgG, Fcγ-специфического, осуществляли путем инъекции человеческого гамма-глобулина в концентрации 500 нМ при скорости потока 30 мкл/мин в течение 3 мин. Инъекцию аналита (химерный белок hIL-13Rα1:hFc) осуществляли с использованием 5 концентраций от 5,63 до 90 нМ в течение 2 мин и отмывали HBS-P в течение 5 мин. Регенерацию поверхности осуществляли с помощью двух инъекций по 100 мМ HCl в течение 1 мин каждая. Информация о типе чипа, формате анализа и последовательности инъецируемых образцов и кинетических данных приведена ниже в таблице 2. Данные, полученные для отрицательного контроля (например, кривые, полученные с использованием буфера) вычитали из приведенных на графиках данных для образцов для коррекции системного внутреннего сдвига основного уровня и снижения шумового сигнала. Для анализа сенсограмм и для оценки аффинности использовали программное обеспечение BiaEvaluation, версия 4.01. Кинетические данные рассчитывали путем подгонки кинетических данных к Лэнгмюровской модели связывания 1:1.
б) Анализ аффинности НuМАт LC5002-003, -005 и -007 с использованием внеклеточного домена hIL-13Rα1, отщепленного от химерного hIL-13Rα1:hFc
Для анализа взаимодействий использовали устройство Biacore 3000. В качестве буфера для погона и реакционного буфера применяли HBS-P (10 мМ HEPES, 150 мМ NaCl, 0,005% полисурфактанта Р, рН 7,4) при 25°С. Молекулы иммобилизующего антитела (анти-hFcγ) сочетали с амином в концентрации 100 мкг/мл при скорости потока 5 мкл/мин в течение 20 мин. НuМАт инъецировали в концентрации 10 мкг/мл при скорости потока 10 мкл/мин в течение 30 с. Инъекцию отщепленных молекул hIL-13Rα1 (ММ 40 кДа) осуществляли в течение 200 с с использованием 7 концентраций от 1,56 до 100 нМ и отмывали HBS-P в течение 5 мин. Регенерацию поверхности осуществляли с помощью двух инъекций по 100 мМ HCl в течение 1 мин каждая при скорости потока 10 мкг/мин. Информация о типе чипа, формате анализа и последовательности инъецируемых образцов и кинетических данных приведена ниже в таблице 3. Кинетические данные рассчитывали путем подгонки кинетических данных к Лэнгмюровской модели связывания 1:1.
в) Сравнительный анализ аффинности рекомбинантных вариантов LC5002-005 с использованием внеклеточного домена hIL-13Rα1, отщепленного от химерного белка hIL-13Rα1:hFc
В этих экспериментах аффинность исходного IgG1, полученного из гибридомы, сравнивали с аффинностями рекомбинантного варианта IgG1-Ala-Ala. Для анализа взаимодействия использовали устройство Biacore 3000. В качестве буфера для погона и реакционного буфера применяли HBS-P (10 мМ HEPES, 150 мМ NaCl, 0,005% полисурфактанта Р, pH 7,4) при 25°С. Молекулы иммобилизующего антитела (анти-hFcγ) сочетали с амином в концентрации 20 мкг/мл при скорости потока 5 мкл/мин в течение 20 мин. НuМАт инъецировали в концентрации 10 мкг/мл при скорости потока 10 мкл/мин в течение 1 мин. Инъекцию отщепленных молекул hIL-13Rα1 (аналит) осуществляли в течение 5 мин с использованием 8 концентраций от 1,56 до 200 нМ и отмывали HBS-P в течение 5 мин. Регенерацию поверхности осуществляли с помощью двух инъекций по 100 мМ HCl в течение 1 мин каждая. Информация о типе чипа, формате анализа и последовательности инъекций и кинетических данных приведена ниже в таблице 4. Кинетические данные рассчитывали путем подгонки кинетических данных к модели связывания бивалентного аналита.
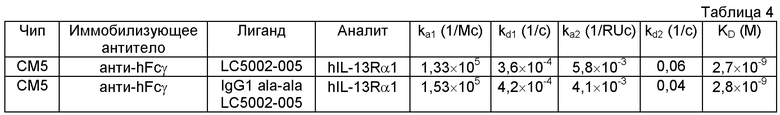
Пример 4
Тестирование с помощью ELISA перекрестной реактивности НuМАт с hIL-13Rα2 и hIL-4Rα
Химерные белки hIL-13Rα2:hFc и hIL-4Rα:hFc (фирма R&D Systems, Великобритания) растворяли в ЗФР (1 мкг/мл) и давали адсорбироваться на титрационные микропланшеты (типа NUNC Maxisorb) путем инкубации в течение ночи при 4°С. После отмывки планшетов буфером для отмывки (ОБ = 0,9% NaCl; 0,1% Tween® 20) сайты неспецифического связывания блокировали путем добавления 100 мкл буфера для инкубации (ИБ = ЗФР с добавлением 1% кротеина С и 0,1% Tween® 20) и инкубации в течение 30 мин при комнатной температуре (КТ). Затем добавляли серийные разведения НuМАт и контрольных антител (100 мкл/лунку; разведения в ИБ) и инкубировали в течение 1 ч при КТ. Планшеты отмывали еще один раз и связанное антитело выявляли путем инкубации с конъюгированным с пероксидазой кроличьим антителом к человеческой каппа-цепи (фирма DAKO, Дания) в конечном разведении 1:500 в ИБ. После инкубации в течение 1 ч при КТ и последующей отмывки планшеты обрабатывали при КТ в темноте готовым к применению раствором ABTS® (фирма Roche Diagnostics GmbH). Абсорбцию измеряли при 405 нм после того, как при использовании самой высокой концентрации достигалась достаточная величина ОП.
Все тестируемые антитела к IL-13Rальфа1 обладали способностью связываться с иммобилизованными внеклеточными доменами человеческого IL-13Rα1, но не обладали способностью связываться ни с hIL-13Rα2, ни с hIL-4Rα (фиг.4).
Пример 15
Перекрестная реактивность НuМАт с мышиным IL-13Rα1
Химерный мышиный белок hIL-13Rα1:hFc (фирма R&D Systems, Великобритания) растворяли в ЗФР (1 мкг/мл) и давали адсорбироваться на титрационные микропланшеты (типа NUNC Maxisorb) путем инкубации в течение ночи при 4°С. После отмывки планшетов буфером для отмывки (ОБ = 0,9% NaCl; 0,1% Tween® 20) сайты неспецифического связывания блокировали путем добавления 100 мкл буфера для инкубации (ИБ = PBS с добавлением 1% кротеина С и 0,1% Tween® 20) и инкубации в течение 30 мин при комнатной температуре (КТ). Затем в лунки добавляли серийные разведения НuМАт и контрольных антител (НuМАт к KLH и поликлональное козье антитело к hIL-13Rα1 (фирма R&D Systems) (100 мкл/лунку; разведения в ИБ) и инкубировали в течение 1 ч при КТ. Планшеты промывали еще один раз и связанные человеческие антитела выявляли путем инкубации с конъюгированным с пероксидазой кроличьим антителом к человеческой каппа-цепи (фирма DAKO, Дания) в конечном разведении 1:500 в IB. Козьи антитела к человеческому hIL-13Rα1, связанные с планшетами, выявляли с помощью конъюгированного с пероксидазой ослиного антитела к козьему IgG (фирма Santa Cruz; разведение 1:1000 в ИБ). После инкубации в течение 1 ч при КТ и последующей отмывки планшеты обрабатывали при КТ в темноте готовым к применению раствором ABTS® (фирма Roche Diagnostics GmbH). Абсорбцию измеряли при 405 нм после того, как при использовании самой высокой концентрации достигалась достаточная величина ОП (фиг.5).
Пример 16
Перекрестная реактивность НuМАт с IL-13Rα1 макак-крабоедов
Ген, кодирующий IL-13Rα1, выделяли с помощью ОФ-ПЦР из ткани обезъян крабоедов (Cynomolgus) и им трансфектировали мышиную линию клеток Ва/F3. Для определения того, дает ли НuМАт перекрестную реакцию с IL-13Rα1 обезъян-крабоедов, стабильно трансфектированные клетки линии Ва/F3, а также родительские клетки линии Ва/F3 инкубировали с 10 мкг/мл НuМАт и контрольными антителами. В качестве положительного контроля использовали поликлональное козье антитело к hIL-13Rα1 (фирма R&D Systems). В качестве отрицательных контролей использовали: белок человеческого IgG1 миеломы (фирма Nordic) и сыворотку здоровой козы. Связанные антитела выявляли с помощью FACS-анализа с использованием антитела к человеческому IgG, конъюгированного с ФИТЦ, для выявления НuМАт и антитела к козьему IgG, конъюгированного с ФИТЦ, для выявления козьих антител. Сравнивали средние интенсивности флюоресценции (СИФ), измеренные для индивидуальных антител, протестированных с использованием трансфектированной линии Ba/F3 и родительской линии.
Все НuМАт, предлагаемые в изобретении, обладали способностью связываться с IL-13Rα1 обезъян-крабоедов, который экспрессировался в трансфектированных клетках линии Ba/F3. Как и следовало ожидать, учитывая высокую степень гомологии между человеческим IL-13Rα1 и IL-13Rα1 обезъян-крабоедов, поликлональное антитело AF152 также связывалось с IL-13Rα1 обезъян-крабоедов. Для антител, используемых в качестве отрицательного контроля, было выявлено лишь незначительное увеличение СИФ при тестировании с использованием трансфектированной линии клеток Ba/F3 (таблица 5).

Пример 17
Связывание НuМАт к IL-13Rα1 с рецепторами Fcγ (связывание с FcγRIIIa на NK-клетках)
Для определения способности антител, предлагаемых в изобретении, связываться с FcγRIIIa (CD16) на естественных клетках-киллерах (NK-клетках) выделяли мононуклеарные клетки периферической крови (РВМС) и инкубировали с 20 мкг/мл антитела НuМАт и контрольных антител в присутствии 20 мкг/мл блокирующего мышиного антитела к FcγRIIIa (анти-CD16, клон 3G8, фирма RDI, Фландерс, шт.Нью-Джерси) или без него для оценки связывания через FcγRIIIa. В качестве отрицательных контролей использовали человеческие IgG2 и IgG4 (сайт связывания), которые не связываются с FcγRIIIa. В качестве положительных контролей для связывания с FcγRIIIa использовали человеческие IgG1 and IgG3 (сайт связывания). Связанные антитела на NK-клетках выявляли с помощью FACS-анализа с использованием меченного с помощью ФЭ мышиного антитела к человеческому CD56 (маркер поверхности NK-клеток) (фирма BD Biosciences Pharmingen, Сан-Диего, шт.Калифорния) в сочетании с меченным с помощью ФИТЦ козьим F(ab)2-фрагментом антитела к человеческому IgG (Fc) (фирма Protos Immunoresearch, Бурлингам, шт.Калифорния). Определяли максимальное связывание тестируемого НuМАт при 20 мкг/мл (Вmax: СИФ±С.К.О.).
LC5002-005 обладало способностью эффективно связываться с FcγRIIIa (по сравнению с контрольным антителом IgG1-изотипа), о чем свидетельствует величина Bmax (СИФ), составляющая 580,6±245,8. Добавление блокирующего антитела к FcγRIIIa приводило к резкому снижению связывания LC5002-005 с NK-клетками (величина Bmax (СИФ) составляла 260,4±95,90), что свидетельствует о наличии специфического связывания с FcγRIIIa.
Перечень ссылок
Aikawa М., и др., Cytokine 13, 2001, cc.75-84
Aplin J.D. и Wriston J.C. Jr., CRC Crit. Rev. Biochem., 1981, cc.259-306
Current Protocols in Molecular Biology, под ред. Ausubel F., и др., изд-во Greene Publishing and Wiley Interscience, New York, 1987
Barnes L.M. и др., Cytotechnology 32, 2000, cc.109-123
Barnes L.M. и др., Biotech. Bioeng. 73, 2001, cc.261-270
Berge S.M. и др., J. Pharm. Sci. 66, 1977, cc.1-19
Boerner P. и др., J. Immunol. 147, 1991, cc.86-95
Brueggemann М. и др., J. Exp. Med. 166, 1987, cc.1351-1361
Bruggemann M. и др., Year Immunol. 7, 1993, cc.33-40
Brunhouse R. и Cebra, J.J., Mol. Immunol. 16, 1979, cc.907-917
Burton D.R. и др., Nature 288, 1980, cc.338-344
Carter Р. и др., Proc. Natl. Acad. Sci. USA 89, 1992, cc.4285-4289
Chen J. и др., International Immunology 5, 1993, cc.647-656
Chen J. и др., ЕМВО J. 12, 1993, cc.821-830
Choi Т.K. и др., Nature Genetics 4, 1993, cc.117-123
Cole и др. Monoclonal Antibodies and Cancer Therapy, под ред. Alan R. Liss, 1985, с.77
Durocher Y. и др., Nicl. Acids. Res. 30, 2002, с.Е9
Edelman G.M. и др., Proc. Natl. Acad. Sci. USA 63, 1969, cc.78-85
Edge A.S. и др., Anal. Biochem. 118, 1981, cc.131-137
ЕР 0307434
Fishwild D.M. и др., Nat. Biotechnol. 14, 1996, cc.845-851
Geisse S. и др., Protein Expr. Purif. 8, 1996, cc.271-282
Graber P. и др., Eur. J. Immunol. 28, 1998, cc.4286-4298
Harding F. и Lonberg N., Ann. N. Acad. Sci 764, 1995, cc.536-546
Hezareh M. и др., J. Virol. 75, 2001, cc.12161-12168
Hoogenboom H.R. и Winter G., J. Mol. Biol. 227, 1992, cc.381-388
Idusogie E.E. и др., J. Immunol. 164, 2000, cc.4178-4184
Jakobovits А. и др., Proc. Natl. Acad. Sci. USA 90, 1993, cc.2551-2555
Jakobovits А. и др., Nature 362, 1993, cc.255-258
Jones P. и др., Nature 321, 1986, cc.522-525
Kabat E.A. и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD., 1991, NIH Publication No. 91-3242
Kaufman R.J., Mol. Biotechnol. 16, 2000, cc.151-161
Lonberg N. и др., Nature 368, 1994, cc.856-859
Lonberg N., Handbook of Experimental Pharmacology 113, 1994, cc.49-101
Lonberg N. и Huszar D., Intern. Rev. Immunol. 25, 1995, cc.65-93
Love T.W. и др., Methods Enzymol. 178, 1989, cc.515-527
Lukas T.J. и др., J. Immunol. 127, 1981, cc.2555-2560
Makrides S.C., Protein Expr. Purif. 17, 1999, cc.183-202
Marks J.D. и др., J. Mol. Biol. 222, 1991, cc.581-597
Meissner Р. и др., Biotechnol Bioeng 75, 2001, cc.197-203
Morgan А. и др., Immunology 86, 1995, cc.319-324
Morrison S.L. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc.6851-6855
Neuberger M.S., EMBO J. 2, 1983, cc.1373-1378
Norderhaug L. и др., J. Immunol. Methods 204, 1997, cc.77-87
Obiri N.I. и др., J. Biol. Chem. 270, 1995, cc.8797-8804
Orlandi R. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.3833-3837
Picard D. и Schaffner W., Nature 307, 1984, cc.80-82
Poudrier J. и др., J. Immunol. 30, 2000, cc.3157-3164
Poudrier J. и др., J. Immunol., 163, 1999, cc.1153-1161
Queen С. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.10029-10033
Riechmann L. и др., Nature 332, 1988, cc.323-327
Schlaeger E.-J. и Christensen K., Cytotechnology 30, 1999, cc.71-83
Schlaeger E.-J., J. Immunol. Methods 194, 1996, cc.191-199
Sojahr H.T. и Bahl, O.P., Arch. Biochem. Biophys. 259, 1987, cc.52-57
SwissProt No. O09030
SwissProt No. P24394
SwissProt No. P35225
SwissProt No. P78552
SwissProt No. Q14627
Taylor L. и др., Nucleic Acids Research 20, 1992, cc.6287-6295
Taylor L. и др., Int. Immunol. 6, 1994, cc.579-591
Thommesen J.E. и др., Mol. Immunol. 37, 2000, cc.995-1004
Thotakura N.R. и Bahl, O.P., Meth. Enzymol. 138, 1987, cc.350-359
Tuaillon N. и др., Proc. Natl. Acad. Sci USA 90, 1993, cc.3720-3724
Tuaillon N. и др., Immunol. 152, 1994, cc.2912-2920
US 4640835
US 4496689
US 4301144
US 4670417
US 4791192
US 4179337
US 5202238
US 5204244
US 5545806
US 5545807
US 5569825
US 5625126
US 5633425
US 5661016
US 5770429
US 5789650
US 5814318
US 5874299
US 5877397
van Dijk M.A. и van de Winkel J.G., Curr. Opin. Chem. Biol 5, 2001, cc.368-374
Werner R.G., Drug Res. 48, 1998, cc.870-880
WO 87/05330
WO 92/22645
WO 92/03918
WO 93/1227
WO 94/25585
WO 96/29417
WO 97/15663
WO 98/24884
WO 01/14424
WO 03/080675








| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА К РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-1 И ИХ ПРИМЕНЕНИЕ | 2004 |
|
RU2369617C2 |
| ИММУНОГЛОБУЛИНЫ | 2005 |
|
RU2404192C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2012 |
|
RU2605327C2 |
| АНТАГОНИСТИЧЕСКИЕ АНТИТЕЛА К IL-17 | 2005 |
|
RU2426741C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2007 |
|
RU2472807C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2016 |
|
RU2650767C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ IL-1БЕТА | 2001 |
|
RU2286351C2 |
| Антитело против IL-4R и его применение | 2018 |
|
RU2758091C1 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ ИНТЕРЛЕЙКИНУ-2 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2745451C1 |
| IL-17A-СВЯЗЫВАЮЩИЙ АГЕНТ И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2014 |
|
RU2682046C1 |
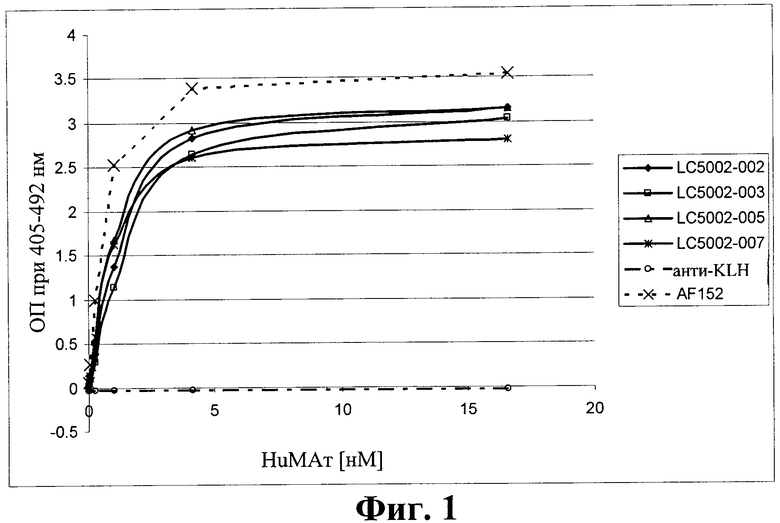
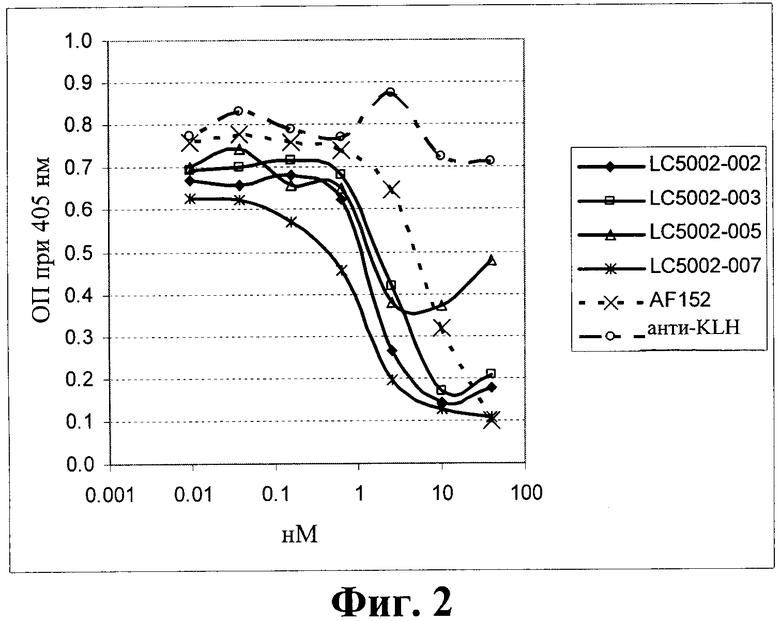
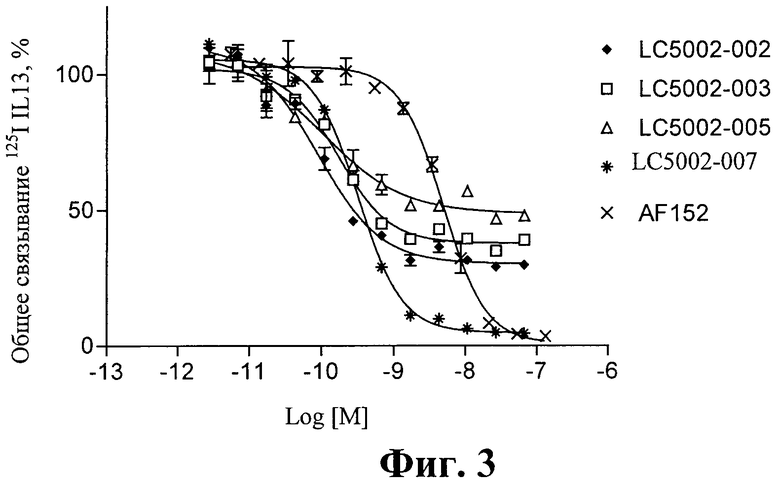
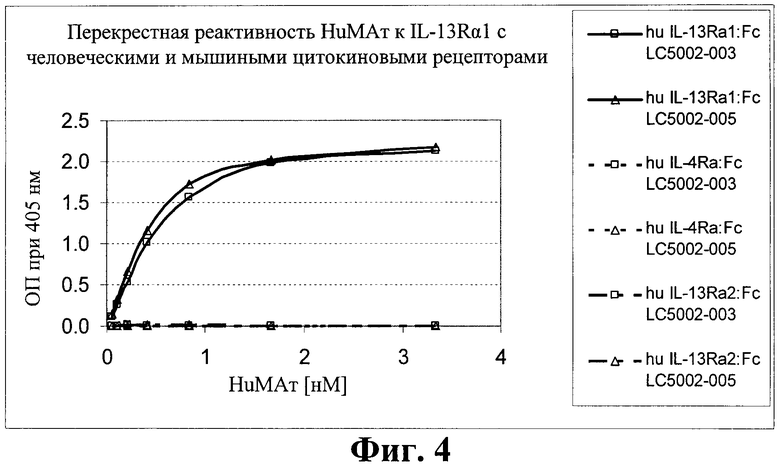
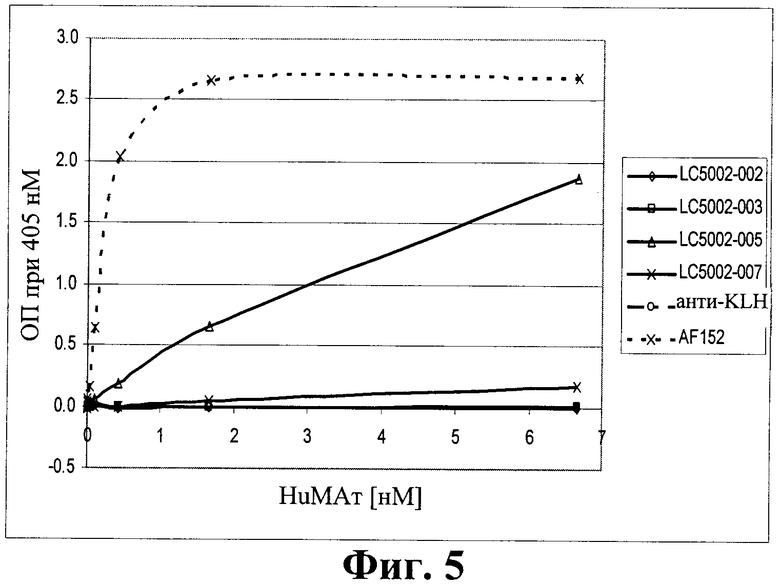
Изобретение относится к биотехнологии и представляет собой антитело, которое обладает способностью связываться с IL-13Rα1 и ингибировать биологическую активность IL-13. Антитело можно эффективно применять для лечения астмы и аллергических заболеваний. 5 з.п. ф-лы, 5 ил., 5 табл.
1. Антитело, которое обладает способностью связываться с IL-13Rα1 и ингибировать биоактивность IL-13, отличающееся тем, что оно содержит в качестве вариабельной области тяжелой цепи SEQ ID NO:1 и в качестве вариабельной области легкой цепи SEQ ID NO:2, в качестве вариабельной области тяжелой цепи SEQ ID NO:3 и в качестве вариабельной области легкой цепи SEQ ID NO:4, в качестве вариабельной области тяжелой цепи SEQ ID NO:5 и в качестве вариабельной области легкой цепи SEQ ID NO:6, в качестве вариабельной области тяжелой цепи SEQ ID NO:7 и в качестве вариабельной области легкой цепи SEQ ID NO:8 или в качестве вариабельной области тяжелой цепи SEQ ID NO:9 и в качестве вариабельной области легкой цепи SEQ ID NO:10.
2. Антитело по п.1, отличающееся тем, что константная область человеческой тяжелой цепи содержит:
а) аминокислотную последовательность Pro233Val234Ala235 с делецией Gly236 и/или аминокислотную последовательность Gly327Leu328Pro329Ser330Ser331,
б) аминокислотную последовательность Ala234Ala235 или
в) аминокислоты Ala265 и Ala297.
3. Антитело по п.1, отличающееся тем, что оно представляет собой человеческое антитело.
4. Антитело по п.1, отличающееся тем, что оно обладает аффинностью связывания с IL-13Rα1, составляющей 10-9 М (KD) или менее, предпочтительно от 10-9 до 10-13 M.
5. Антитело по п.1, полученное из линии клеток гибридомы DSM АСС2709, DSM ACC2710, DSM ACC2711 или DSM ACC2712.
6. Антитело по п.1, отличающееся тем, что содержит
а) в качестве вариабельной области тяжелой цепи SEQ ID NO:1, в качестве вариабельной области легкой цепи SEQ ID NO:2, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
б) в качестве вариабельной области тяжелой цепи SEQ ID NO:3 и в качестве вариабельной области легкой цепи SEQ ID NO:4, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
в) в качестве вариабельной области тяжелой цепи SEQ ID NO:5 и в качестве вариабельной области легкой цепи SEQ ID NO:6, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A,
г) в качестве вариабельной области тяжелой цепи SEQ ID NO:7 и в качестве вариабельной области легкой цепи SEQ ID NO:8, в качестве константной области легкой κ-цепи SEQ ID NO:11 и в качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A, или
д) в качестве вариабельной области тяжелой цепи SEQ ID NO:9 и в качестве вариабельной области легкой цепи SEQ ID NO:10, в качестве константной области легкой κ-цепи SEQ ID NO:11 ив качестве константной области тяжелой γ1-цепи SEQ ID NO:12, необязательно имеющую мутации L234A и L235A или D265A и N297A.
| Стенд для исследований судовой пропульсивной установки | 1986 |
|
SU1449851A2 |
| WO 2003080675, 02.10.2003 | |||
| AKAIWA M., ET AL | |||
| Насос | 1917 |
|
SU13A1 |
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Насос | 1917 |
|
SU13A1 |
Авторы
Даты
2011-03-10—Публикация
2006-01-02—Подача