Область техники
Настоящее изобретение относится к иммуногенному гибридному полипептиду, в котором пептид-миметик В-клеточного эпитопа аполипопротеина B-100; эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В и С-концевой пептидный фрагмент мышиного аполипопротеина CII или пептид-миметик В-клеточного эпитопа аполипопротеина B-100 слиты друг с другом в таком порядке в направлении от их N-конца к С-концу. Также настоящее изобретение относится к вакцинной композиции для профилактики и лечения ожирения, содержащей иммуногенный гибридный полипептид в качестве активного ингредиента. Далее настоящее изобретение относится к полинуклеотиду, кодирующему иммуногенный гибридный полипептид, рекомбинантному вектору экспрессии, несущему этот полинуклеотид, клетке-хозяину, трансформированной рекомбинантным вектором экспрессии, и способу получения иммуногенного гибридного полипептида путем культивирования клетки-хозяина, трансформированной рекомбинантным вектором экспрессии.
Предшествующий уровень техники
В последнее время возросло число больных диабетом, артериосклерозом и ишемической болезнью сердца (ИБС) в Корее вследствие сдвига в сторону западных особенностей питания, и это относится к домашним питомцам, таким как собаки или кошки, или домашним животным, а также к людям. Сывороточные липиды, вызывающие эти заболевания, включают в себя холестерин, триглицериды (ТГ), свободные жирные кислоты и фосфолипиды. Эти сывороточные липиды образуют липопротеины с аполипопротеинами и переносятся по кровотоку. Среди них липопротеины очень низкой плотности (ЛПОНП) и липопротеины низкой плотности (ЛПНП) функционируют для переноса главным образом ТГ и холестерина, и изменения уровней ЛПНП-холестерина являются показателями прогноза заболеваний. ЛПНП-холестерин, который является главным фактором заболеваний, связанных с метаболизмом липидов у взрослых людей, связывается с рецепторами ЛПНП на плазматической мембране клеток в каждой ткани, и хранится, и используется в этой ткани. Альтернативно, ЛПНП-холестерин, поглощенный макрофагами и гидролизованный, и свободный холестерин переносятся к ЛПВП наряду с апо E липопротеином для утилизации в печени или превращаются в выделяемую соль желчной кислоты. Во время этого процесса аполипопротеин выполняет очень важные функции для поддержания структурного гомеостаза липопротеинов, служит в качестве кофактора фермента липопротеинлипазы и играет решающую роль в связывании со специфическим рецептором на цитоплазматической мембране.
Аполипопротеин B-100 (Apo B-100) является главным белковым компонентом ЛПНП, а также присутствует в ЛПСП и ЛПОНП. Таким образом, когда антитела в крови индуцируются для распознавания апо B-100, будет легко осуществляться клиренс ЛПНП фагоцитами. В этом отношении некоторые последние исследования были сфокусированы на использовании вакцин для снижения уровней плазменного ЛПНП-холестерина и снижения числа новых случаев артериосклероза. Антителами, индуцированными такой антихолестериновой вакцинной терапией, являются типы IgM, которые предположительно связываются с ЛПОНП, ЛПСП и ЛПНП, и такая стратегия говорит о возможности разработки вакцин для профилактики и лечения гиперхолестеринемии и атеросклероза (Bailey, et al., Cholesterol vaccines. Science 264, 1067-1068, 1994; Palinski W et al., Proc. Natl. Acad Sci U.S.A. 92, 821-5, 1995; Wu R, de Faire U et al., Hypertension. 33, 53-9, 1999). Также аполипопротеин B-100 представляет собой огромную белковую молекулу, которая состоит из 4560 аминокислотных остатков, содержит сигнальный пептид из 24 аминокислотных остатков и имеет молекулярную массу более 500 кДа (Elovson J et al., Biochemistry, 24:1569-1578, 1985). Поскольку аполипопротеин B-100 секретируется главным образом печенью и является амфипатической молекулой, он может взаимодействовать с липидными компонентами плазменных липопротеинов и водным окружением (Segrest J. P et al., Adv. Protein Chem., 45:303-369, 1994). Аполипопротеин B-100 стабилизирует размер и структуру частиц ЛПНП и играет решающую роль в контролировании гомеостаза плазменного ЛПНП-холестерина посредством связывания с его рецептором (Brown MS et al., Science, 232:34-47, 1986).
В корейском патенте №10-0639397, выданном авторам настоящего изобретения, описывается пептид-миметик для эпитопа аполипопротеина B-100, который демонстрирует ингибирующее действие на ожирение, иммуногенный гибридный полипептид (B4T), в котором пептид-миметик слит с эпитопом Т-клетки хелпера, и композиция против ожирения, содержащая их. Однако не предполагается, что гибридный полипептид, полученный в результате слияния пептида-миметика В-клеточного эпитопа аполипопротеина В-100 с эпитопом Т-клетки хелпера, будет одинаково эффективным для профилактики и для лечения животных и людей вследствие различия между веществами, связанными с их иммунитетом, и метаболическими процессами. Кроме того, хотя иммунизация проводилась в пределах одной группы, слитый полипептид запускает иммунные реакции с большой степенью расхождения соответственно индивидуальным особенностям вследствие их низкой конформационной стабильности.
С другой стороны, было предпринято много попыток слияния гаптена с белком-носителем для усиления иммуногенности гаптена, но получить постоянные эффекты усиления не удалось. В частности, линейная связь В-клеточного эпитопа и Т-клеточного эпитопа подобно настоящему изобретению приводит в результате к утрате иммуногенности в соответствии с ориентацией эпитопов, типом каждого эпитопа и подобным (Francis, M. J. et al., Nature 330:168-170, 1987), а наличие линкера приводило к сниженной антигенности (Partidos, C. et al., Mol. Immunol. 29:651-658, 1992). То есть, не существует постоянного правила, применимого для создания пептидных вакцин, и эффективность созданных вакцин является непредсказуемой. По тем же причинам, в тех случаях, когда высокогидрофобный пептид-миметик В-клеточного эпитопа аполипопротеина В-100, слитый с эпитопом Т-клетки хелпера вируса бешенства, эпитопом Т-клетки хелпера поверхностного антигена вируса гепатита В или аполипопротеина С II, антигенная область может быть интернализирована в слитый белок, приводя к снижению его способности индуцировать антительные реакции.
Описание изобретения
Техническая задача
Перед созданием настоящего изобретения авторы настоящего изобретения провели глубокое и тщательное исследование для получения стабильной вакцины против ожирения, которая применима у животных, таких как собаки, крупный рогатый скот и т.д., а также у людей, и которая может запускать однотипные антительные реакции у всех индивидуумов.
Соответственно, авторы настоящего изобретения неожиданно обнаружили, что гибридный полипептид, содержащий тетрамерный пептид-миметик для В-клеточного эпитопа аполипопротеина B-100 (B4), либо эпитоп Т-клетки хелпера вируса бешенства (R), либо эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В (T), либо С-концевой пептидный фрагмент (CII) аполипопротеина CII, либо димерный пептид-миметик для В клеточного эпитопа аполипопротеина B-100 (B2) в таком порядке от их N-конца, может эффективно применяться для профилактики или лечения ожирения у животных, а также у людей в дополнение к проявлению прекрасных иммуностимулирующих эффектов, таким образом осуществляя настоящее изобретение.
Техническое решение
Таким образом, одной целью настоящего изобретения является получение иммуногенного гибридного полипептида, в котором тетрамерный пептид-миметик В-клеточного эпитопа аполипопротеина B-100, либо эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В и либо С-концевой пептидный фрагмент аполипопротеина CII, либо димерный пептид-миметик В-клеточного эпитопа аполипопротеина B-100 слиты в таком порядке от их N-конца.
Другой целью настоящего изобретения является получение вакцинной композиции для профилактики или лечения ожирения, содержащей иммуногенный гибридный полипептид.
Еще одной целью настоящего изобретения является получение полинуклеотида, кодирующего иммунногенный гибридный полипептид.
Еще одной целью настоящего изобретения является получение рекомбинантного вектора экспрессии, содержащего этот полинуклеотид.
Еще одной целью настоящего изобретения является получение клетки-хозяина, трансформированной рекомбинантным вирусом экспрессии.
Еще одной целью настоящего изобретения является разработка способа получения иммуногенного гибридного полипептида путем культивирования клетки-хозяина, трансформированной рекомбинантным вектором экспрессии.
Краткое описание чертежей
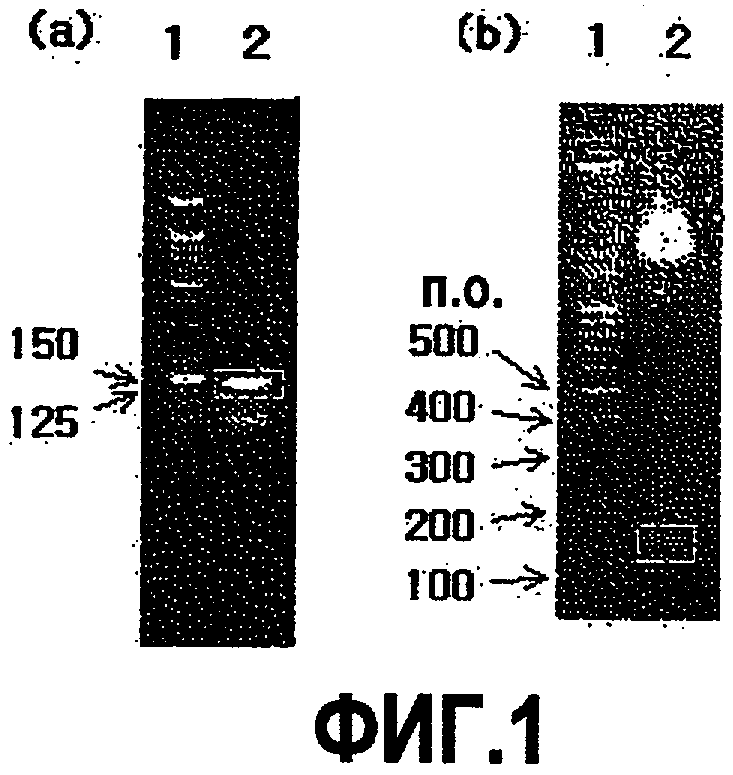
На фиг.1(a) представлена фотография после электрофореза продукта ПЦР гена аполипопротеина на дорожке 2, вместе со смесью ДНК-маркера 25/100 н.п. на дорожке 1, на 2% агарозном геле в буферной системе TBE с загрузкой 2 мкл на лунку.
На фиг.1(b) представлена фотография, показывающая вставку полинуклеотидного фрагмента, представляющего интерес, в рекомбинантный вектор ApoCII/pQE30, трансформированный в E.coli JM109.
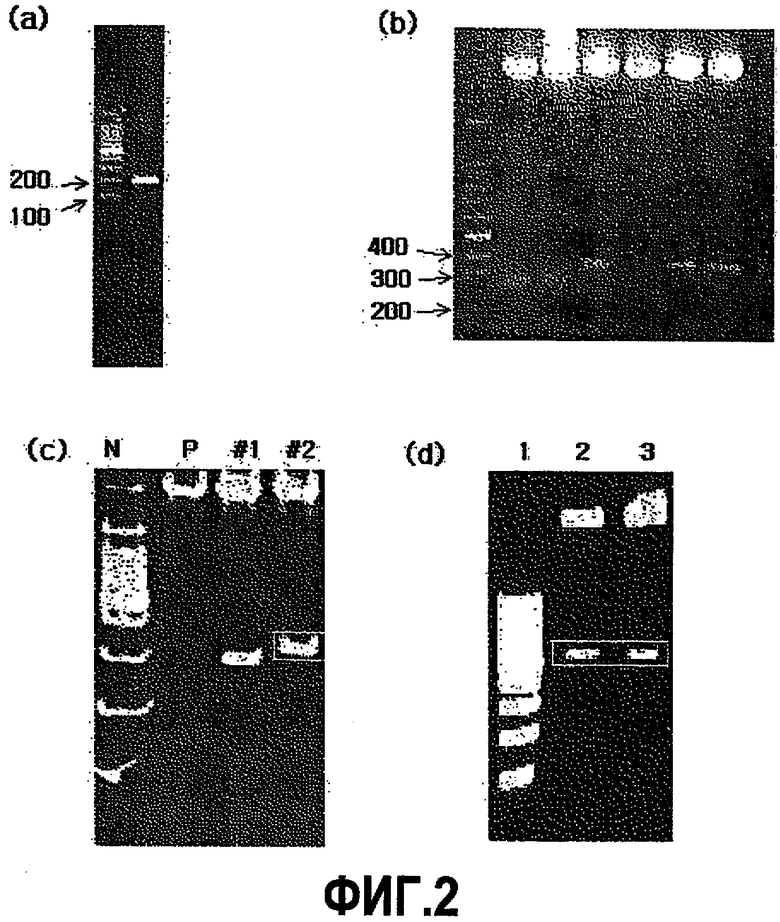
На фиг.2(a) представлена фотография после электорофореза ПЦР продукта гена RVNP на дорожке 2, вместе с маркером 100 н.п. (Bioneer) на дорожке 1, на 2% агарозном геле в буферной системе TBE с загрузкой 2 мкл на лунку.
На фиг.2(b) представлена фотография, показывающая вставку SalI-расщепленного фрагмента в соответствующем направлении в рекомбинантный вектор B4RCII/pQE30, трансформированный в E.Coli JM109.
На фиг.2(c) представлена фотография, показывающая вставку SalI-расщепленного фрагмента в соответствующем направлении в рекомбинантный вектор B4RB2/pQE30, трансформированный в E.coli JM109.
На фиг.2(d) представлена фотография, показывающая вставку SalI-расщепленного фрагмента в соответствующем направлении в рекомбинантный вектор B4TB2/pQE30, трансформированный в E.coli JM109.
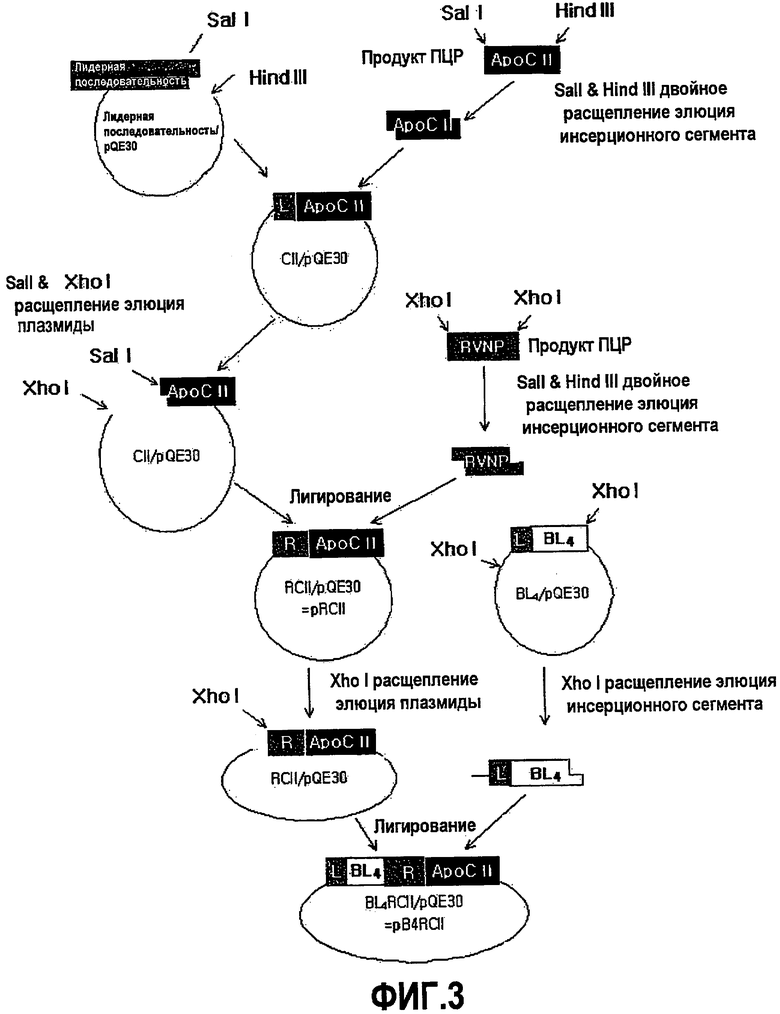
На фиг.3 представлена схематическая диаграмма, иллюстрирующая процесс получения рекомбинантного вектора экспрессии для экспрессии слитого полипептида B4RCII.
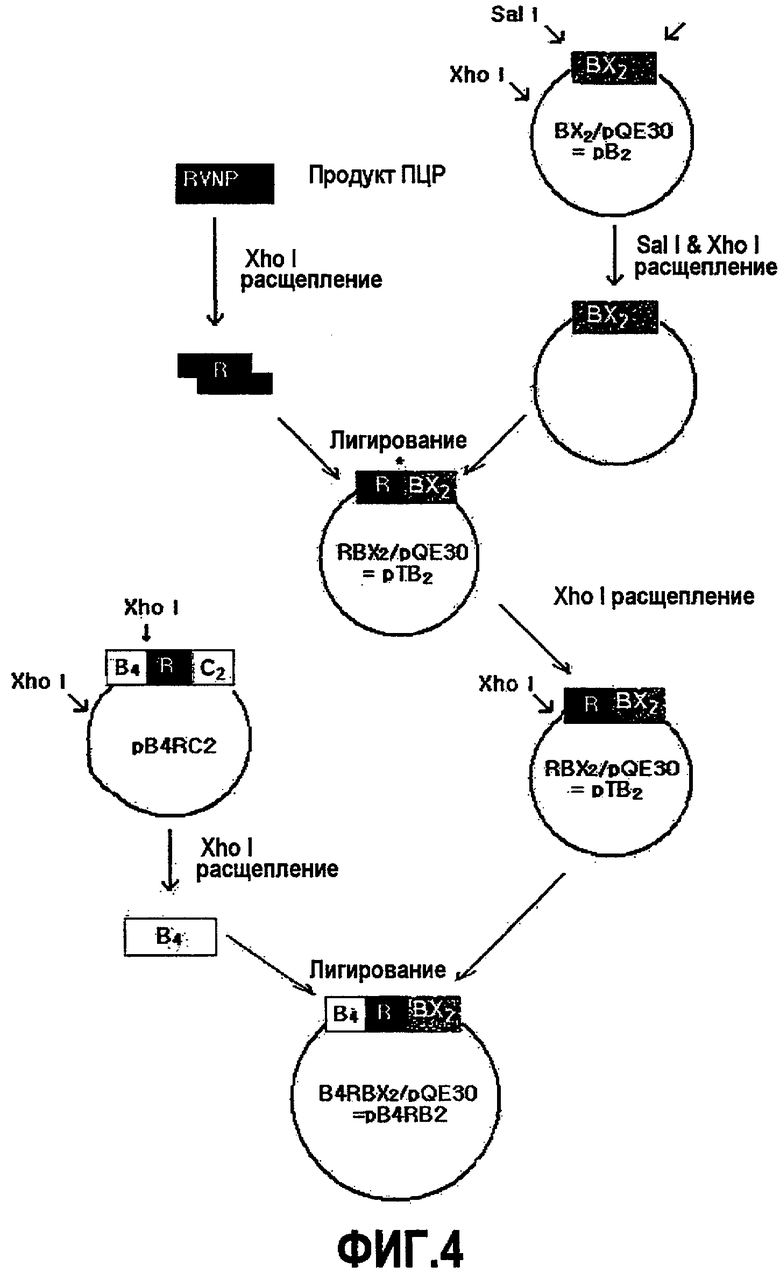
На фиг.4 представлена схематическая диаграмма, иллюстрирующая процесс получения рекомбинантного вектора экспрессии для экспрессии слитого полипептида B4RB2.
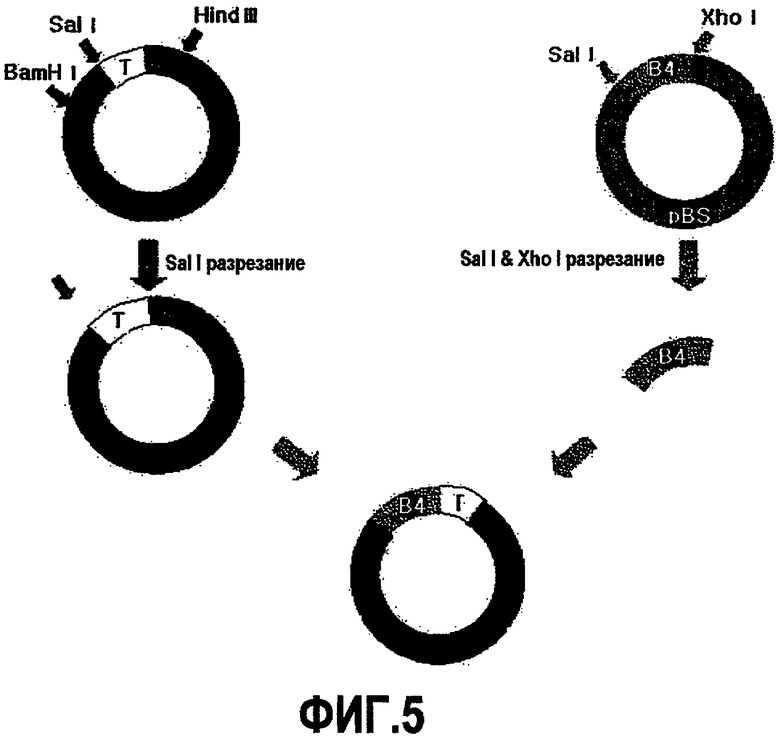
На фиг.5 представлена схематическая диаграмма, иллюстрирующая процесс получения рекомбинантного вектора экспрессии для экспрессии слитого полипептида B4TB2.
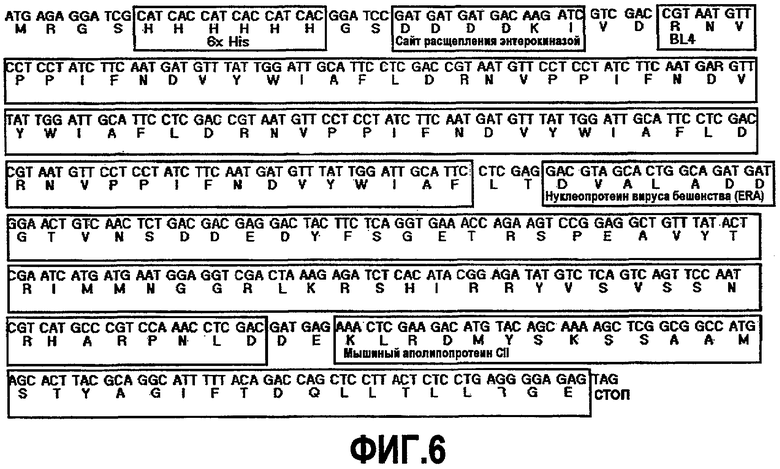
На фиг.6 показана нуклеотидная последовательность pB4RCII вместе с кодируемой таким образом аминокислотной последовательностью, которая была идентифицирована путем секвенирования ДНК.
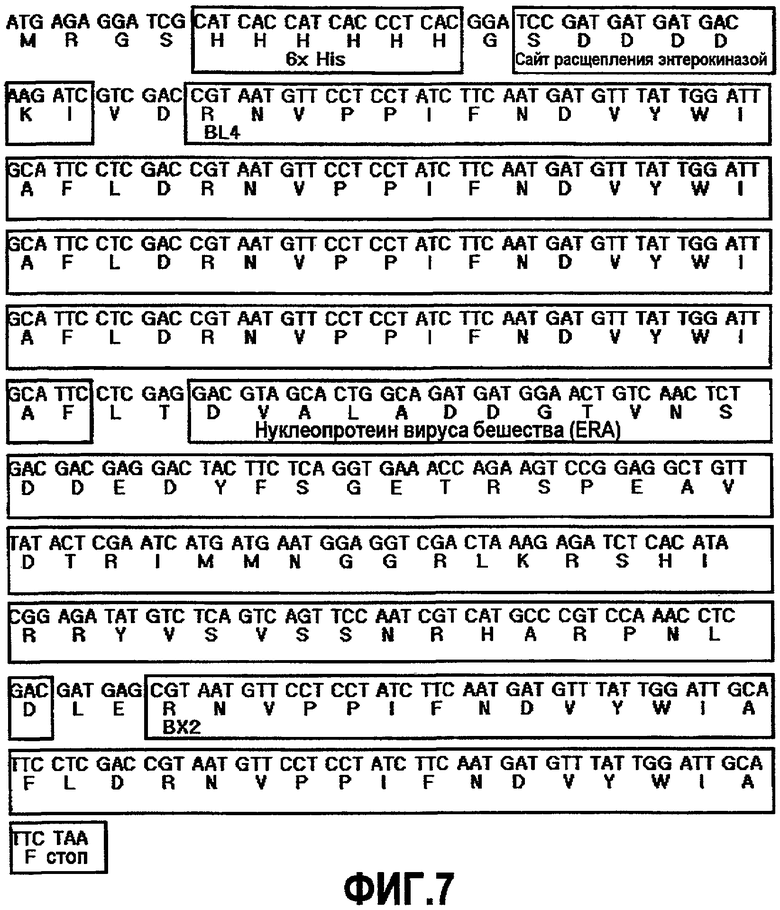
На фиг.7 показана нуклеотидная последовательность pB4RB2 вместе с кодируемой таким образом аминокислотной последовательностью, которая была идентифицирована путем секвенирования ДНК.
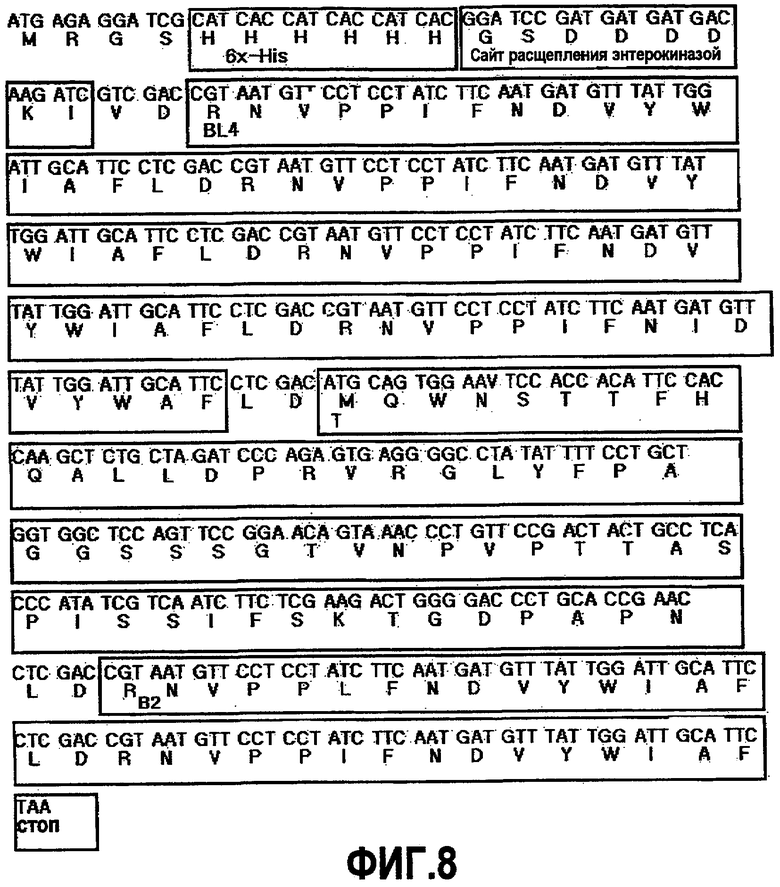
На фиг.8 показана нуклеотидная последовательность pB4TB2 вместе с кодируемой таким образом аминокислотной последовательностью, которая была идентифицирована путем секвенирования ДНК.
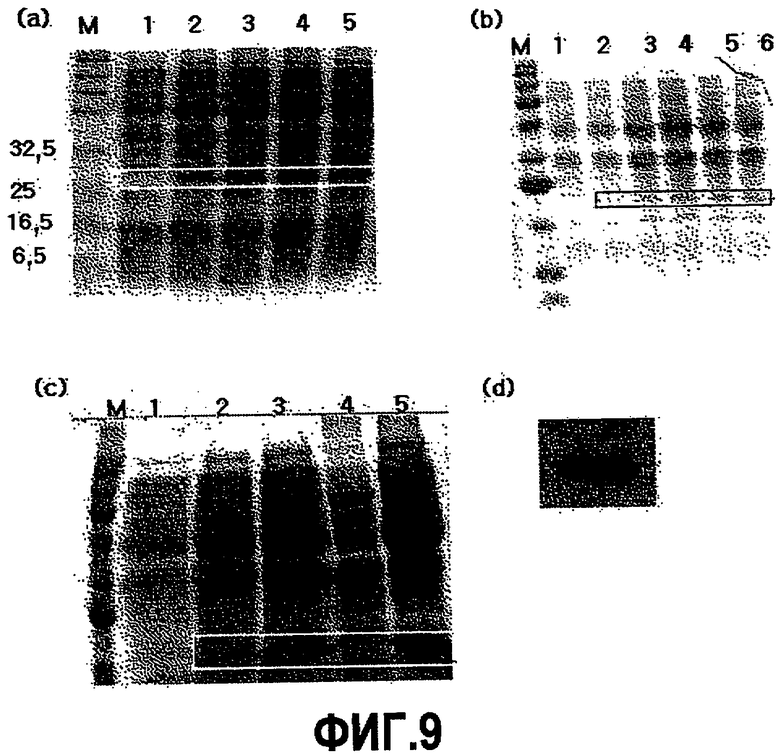
На фиг.9(a) представлена фотография SDS-PAGE, показывающая изменения в экспрессии B4RCII со временем, где B4RCII, полученный из Escherichia coli M15/pB4RCII через 1-4 часа после IPTG-индукции, подвергали электрофорезу на дорожках 2-5, вместе с маркером (NEB) на дорожке M и не-IPTG-индуцированной E.coli M15/pB4RCII на дорожке 1.
На фиг.9(b) представлена фотография SDS-PAGE, показывающая изменения в экспрессии B4RB2 со временем, где B4RB2, полученный из Escherichia coli M15/pB4RB2 через 2~5 часов после IPTG-индукции, подвергали электрофорезу на дорожках 2-5, вместе с маркером (NEB) на дорожке M и не-IPTG-индуцированной E.coli M15/pB4RB2.
На фиг.9(c) представлена фотография SDS-PAGE, показывающая изменения в экспрессии B4TB2 со временем, где B4TB2, полученный из Escherichia coli M15/pB4TB2 через 3-5 часов после IPTG-индукции, подвергали электрофорезу на дорожках 2 и 3, вместе с маркером (NEB) на дорожке M1, не-IPTG-индуцированной E.coli M15 на дорожке 1, общим растворимым белком на дорожке 4 и общим белком, солюбилизированным 8 М мочевиной на дорожке 5.
На фиг.9(d) представлена фотография, показывающая присутствие B4RCII посредством анализа Вестерн-блоттинг, с использованием кроличьего поликлонального антитела к PB14.
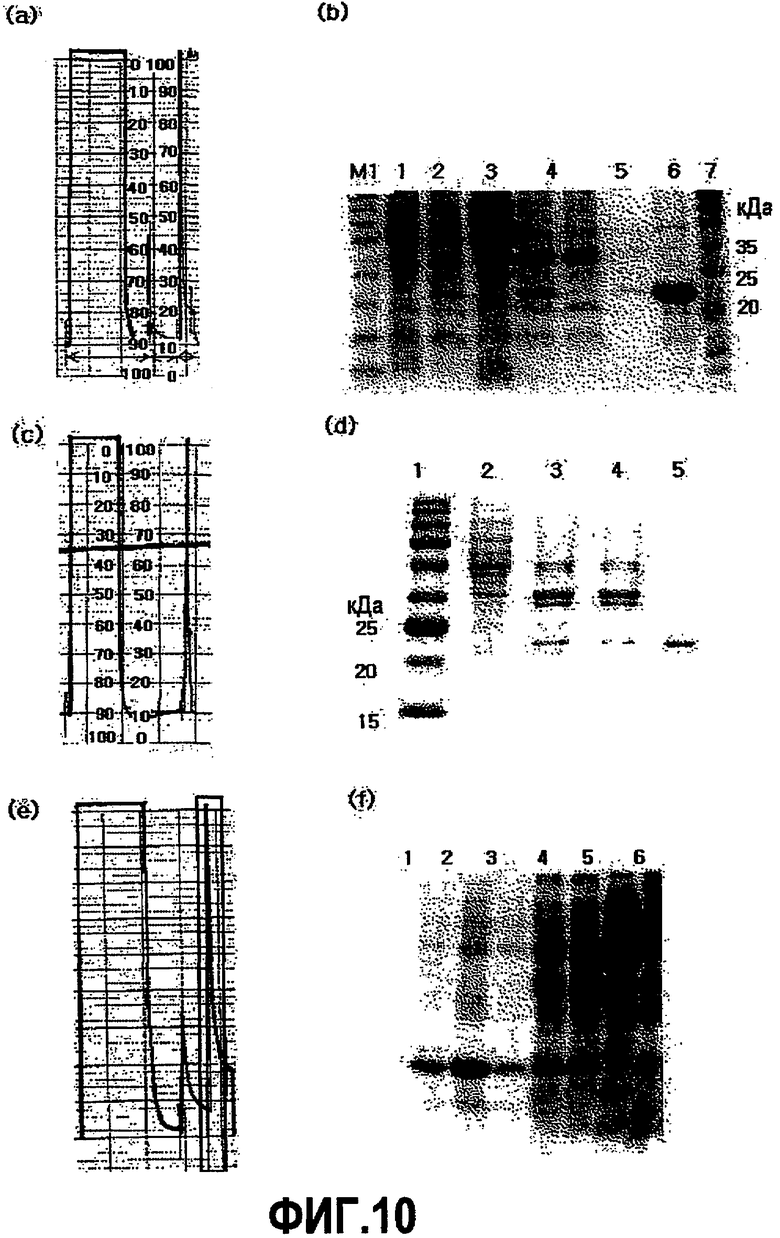
На фиг.10 показана элюция B4RCII из связанного со смолой B4RCII в соответствии с линейными градиентами концентрации имидазола на графике (a) и на фотографии SDS-PAGE (b) (M1: NEB предварительно окрашенный маркер, дорожка 1: суммарный клеточный экстракт без индукции, дорожка 2:4-часовая индукция суммарный клеточный экстракт, дорожка 3: общий растворимый белок, дорожка 4: общий белок, солюбилизированный 8 М мочевиной (до связывания со смолой), дорожка 5: фильтрат, дорожка 6: промывочная фракция (50 мМ имидазол), и дорожка 7: элюированная фракция (500 мМ имидазол), загрузка 7,5 мкл/лунку).
На фиг.10 показана элюция B4RB2 из связанного со смолой B4RB2 в соответствии с линейными градиентами концентрации имидазола на графике (c) и на фотографии SDS-PAGE (d) (дорожка 1: предварительно окрашенный белковый маркер Elpis, дорожка 2: общий растворимый белок, дорожка 3: общий белок, солюбилизированный 8 М мочевиной (до связывания со смолой), дорожка 4: фильтрат, дорожка 6: элюированная фракция (500 мМ имидазол), загрузка 3 мкл/лунку).
На фиг.10 показана элюция B4TB2 из связанного со смолой B4TB2 в соответствии с линейными градиентами концентрации имидазола на графике (e) и на фотографии SDS-PAGE (f) (дорожка 1: предварительно окрашенный белковый маркер Elpis, дорожка 2: общий растворимый белок, дорожка 3: общий белок, солюбилизированный 8 М мочевиной (до связывания со смолой), дорожка 4: фильтрат, дорожка 5: промывочная фракция (50 мМ имидазол), дорожка 6: элюированная фракция (500 мМ имидазол), дорожка 7: элюированная фракция (500 мМ имидазол), загрузка 7,5 мкл/лунку).
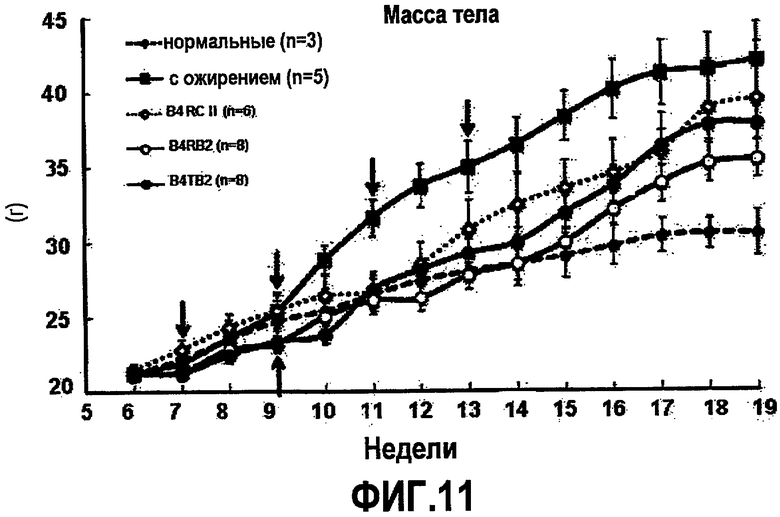
На фиг.11 представлен график, показывающий прирост массы тела в группах мышей C57BL/6, которые были иммунизированы B4RCII, B4RB2 и B4TB2 в моменты времени, указанные красными стрелками, с отправной точкой DIO, указанной синей стрелкой.
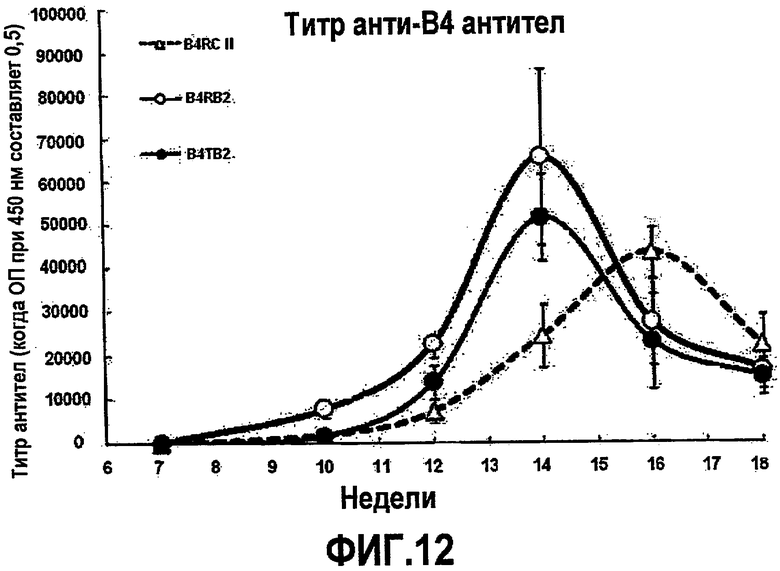
На фиг.12 представлен график, показывающий изменения титра анти-B4 антитела за период времени для животных, иммунизированных B4RCII, B4RB2 и B4TB2.
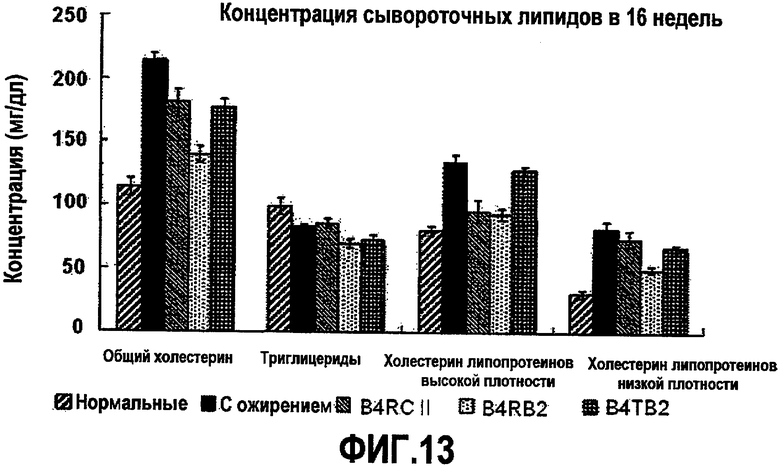
На фиг.13 представлен график, показывающий уровни липидов в крови у животных через одну неделю после четвертой повторной иммунизации вакцинами по настоящему изобретению (возраст 16 недель).
Наилучший способ осуществления изобретения
В соответствии с одним аспектом настоящее изобретение направлено на иммуногенный гибридный полипептид, в котором пептид-миметик В-клеточного эпитопа аполипопротеина В-100, либо эпитоп Т-клетки хелпера вируса бешенства, либо эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В и либо С-концевой пептидный фрагмент аполипопротеина CII, либо димерный пептид-миметик В-клеточного эпитопа аполипопротеина В-100 слиты в таком порядке от их N-конца.
Термин «пептид-миметик эпитопа» в контексте настоящего изобретения относится к пептиду, который имитирует минимальную часть эпитопа, представляющую собой эпитоп, который является достаточно сходным с нативным эпитопом, так что его может распознать антитело, специфичное к нативному эпитопу, или который может усиливать поперечное связывание антитела с нативным эпитопом. Пептид-миметик также называют мимотопом. Такой пептид-миметик является предпочтительным, поскольку он распознается как «не свое» in vivo и, следовательно, решает проблему самотолерантности при иммунных ответах. Пептид-миметик В-клеточного эпитопа апо В-100 распознается антителом, специфически связывающимся с апо B-100. Антитело, специфически связывающееся с апо В-100, включает в себя поликлональные или моноклональные антитела, которые специфически распознают и связываются с апо В-100, и его фрагментами, например Fc, Fab и F(ab')2. Среди них предпочтительными являются моноклональные антитела, Mab B9 и Mab B23 являются более предпочтительными.
Пептид-миметик В-клеточного эпитопа апо В-100 в соответствии с настоящим изобретением включает в себя аминокислотную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3. Авторы настоящего изобретения выделили пептиды-миметики (SEQ ID NO: 1, 2 и 3), которые распознаются моноклональным антителом против apo B-100, Mab B9 или Mab B23, из пептидной библиотеки, подвергаемой фаговому дисплею, путем биопэннинга библиотеки. Пептид-миметик эпитопа апо В-100, который включает в себя аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, может быть в мономерной форме, которая состоит из одной копии аминокислотной последовательности, имеющей любую одну из SEQ ID NO, или для дальнейшего усиления иммуногенности пептида-миметика может быть в мультимерной форме, в которой две или более, предпочтительно от трех до восьми, и более предпочтительно от трех до шести копий аминокислотной последовательности, имеющей любую одну из последовательностей SEQ ID NO, являются связанными. Наиболее предпочтительным является тетрамер, в котором соединены четыре копии. В тех случаях, когда пептид-миметик находится в мультимерной форме, аминокислотные последовательности, каждая из которых составляет мономер, могут быть ковалентно связаны напрямую или через линкер. В тех случаях, когда аминокислотные последовательности соединены через линкер, линкер может состоять из одного-пяти аминокислотных остатков, которые выбраны, например, из глицина, аланина, валина, лейцина, изолейцина, пролина, серина, треонина, аспарагина, аспарагиновой кислоты, цистеина, глутамина, глутаминовой кислоты, лизина и аргинина. Предпочтительные аминокислоты, доступные в линкере, могут включать в себя валин, лейцин, аспарагиновую кислоту, глицин, аланин и пролин. Более предпочтительно, принимая во внимание упрощение манипуляции с генами, две аминокислоты, выбранные из валина, лейцина, аспарагиновой кислоты и т.д., могут быть связаны и использованы в качестве линкера. Предпочтительный пептид-миметик получают путем связывания двух или нескольких копий аминокислотной последовательности, выбранной из последовательностей SEQ ID NO: 1, 2 и 3, посредством линкера.
Термин «Т-клеточный эпитоп» в контексте настоящего изобретения относится к аминокислотной последовательности, которая способна связываться с молекулами MHC II класса с подходящей эффективностью и стимулировать Т-клетки или связываться с Т-клетками в комплекс с MHC II класса. В этом случае Т-клеточный эпитоп распознается специфическим рецептором, присутствующим на Т-клетках, и действует для предоставления сигнала, необходимого для дифференцировки В-клеток в антителопродуцирующие клетки и индукции цитотоксических Т-лимфоцитов (CTL) для разрушения клеток-мишеней. Для целей настоящего изобретения эпитопы Т-клеток хелперов предпочтительно используют в качестве мишеней распознавания специфического рецептора. Из них обнаружено, что эпитоп Т-клеток хелперов вируса бешенства или эпитоп Т-клеток хелперов поверхностного антигена вируса гепатита В дает лучшие эффекты.
Вирус бешенства поражает домашний скот и диких животных, а также домашних любимцев, таких как собаки и кошки, вызывая острый энцефалит. Бешенство можно предотвратить вакцинацией как у людей, так и у других животных. Для применения в настоящем изобретении пептидный фрагмент (R) длиной 58 аминокислот, содержащий эпитоп Т-клетки хелпера хозяина, получали из гена рибонуклеопротеина вируса бешенства (NCBI ген ID; AF406695) путем манипуляции с геном, аминокислотная последовательность которого представлена последовательностью SEQ ID NO: 6 (Ertl, H.C.J., et al., Journal of Virology, 63(7), 2885-2892, 1989).
Геном вируса гепатита В (HBV) составляет 3,2 тыс. оснований в длину, содержит информацию о четырех важных белках и содержит четыре открытые рамки считывания, S ген (белок поверхностного антигена), C ген (ядерный белок), P ген (ДНК полимераза) и X ген. S ген разделяется на S участок, кодирующий HBsAg, и преS участок. ПреS участок разделяется на преS1, кодирующий 108 или 119 аминокислот, соответствующих штаммам HBV, и преS2, кодирующий 55 аминокислот, независимо от подтипа. Белок преS2 HBV активирует Т-клетки хелперы во время иммунных ответов in vivo, тем самым стимулируя образование антитела против HBV. SEQ ID NO: 7 указывает аминокислотную последовательность эпитопа Т-клетки хелпера HBV.
В С-концевом участке иммуногенного гибридного полипептида расположен С-концевой пептидный фрагмент мышиного аполипопротеина CII или пептид-миметик В-клеточного эпитопа аполипопротеина B-100.
Мышиный аполипопротеин CII, состоящий из 79 аминокислотных остатков с молекулярной массой 8800 Да (Hoffer, M.J., et al., Genomics 17(1), 45-51, 1993), главным образом продуцируется в тонкой кишке и в печени и может быть обнаружен в хиломикронах, ЛПОНП и ЛПВП, функционируя как необходимый кофактор для ферментативной активности аполипопротеинлипазы (LPL) (Storjohann, R., et al., Biochimica et Biophysica Acta, 1486, p.253~264, 2000). В предпочтительном примере настоящего изобретения пептид, состоящий из 33 C-концевых аминокислотных остатков аполипопротеина CII, которые отвечают за контроль активности LPL, был клонирован из гена мышиного аполипопротеина CII (NCBI ген ID; NM009695) и представлен последовательностью SEQ ID NO: 8.
Пептид-миметик эпитопа аполипопротеина B-100, который пристроен к C-концевому участку иммуногенного гибридного полипептида по настоящему изобретению, содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3. Пептид-миметик эпитопа апо B-100, который включает в себя аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3, может быть в мономерной форме, которая состоит из одной его копии. Для дальнейшего усиления его иммуногенности пептид-миметик может быть в мультимерной форме, в которой от двух до четырех копий аминокислотной последовательности связаны с большим предпочтением димерной формы, состоящей из двух копий. В случае мультимерной формы аминокислотные последовательности, каждая из которых составляет мономер, могут быть ковалентно связаны напрямую или через линкер.
Термин «иммуногенность» в контексте настоящего изобретения относится к способности индуцировать как клеточный, так и гуморальный иммунный ответ для защиты организма от посторонних веществ. Вещество, индуцирующее такие иммунные ответы, называется иммуногеном. В слитом полипептиде в соответствии с настоящим изобретением В-клеточный эпитоп аполипопротеина В-100, эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В и С-концевой пептидный фрагмент аполипопротеина CII используются в качестве иммуногенов.
Когда В-клеточный эпитоп и Т-клеточный эпитоп слиты для получения иммуногенного полипептида подобно полипептиду по настоящему изобретению, известно, что В-клеточный эпитоп должен быть вынесен на внешнюю поверхность складчатой структуры полипептида с Т-клеточным эпитопом, расположенным внутри, для эффективной индукции иммунных реакций (Partidos C, et al., Eur J Immunol., 22(10):2675-80, 1992). Дополнительно к структуре слитого белка B4T предшествующего уровня техники, в котором только пептид-миметик В-клеточного эпитопа аполипопротеина B-100 и Т-клеточный эпитоп являются связанными, фрагмент аполипопротеина CII или пептид-миметик В-клеточного эпитопа аполипопротеина В-100 связан с С-концом Т-клеточного эпитопа в соответствии с настоящим изобретением. Обнаружено, что полученный в результате слитый полипептид имеет улучшенную стабильность складчатой белковой структуры и индуцирует стандартные антительные реакции среди всех индивидуумов, поскольку Т-клеточный эпитоп дополнительно окружен В-клеточным эпитопом, с минимальным выходом на внешнюю поверхность.
Термин «полипептид», используемый в контексте настоящего изобретения, является термином, включающим полноразмерную аминокислотную цепь, в которой остатки, содержащие две или более аминокислот, конъюгированы ковалентными пептидными связями, и включает в себя дипептиды, трипептиды, олигопептиды и полипептиды. В частности, в настоящем изобретении полипептид означает гибридный полипептид, в котором два или более пептидов, в которых от нескольких до нескольких десятков аминокислот, являющихся ковалентно связанными, соединены друг с другом. Каждая пептидная последовательность, содержащая этот полипептид, включает в себя последовательность, соответствующую упомянутому выше эпитопу, и может дополнительно включать в себя последовательность, смежную с этим эпитопом. Эти пептиды могут быть составлены из L- или D-аминокислот или могут находиться в различных комбинациях аминокислот в двух различных конфигурациях.
Термин «гибридный полипептид», используемый в контексте настоящего изобретения, в основном обозначает пептид, в котором связаны гетерогенные пептиды, имеющие различное происхождение. В настоящем изобретении гибридный полипептид представляет собой пептид, в котором В-клеточный эпитоп, либо эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатипа В и либо С-концевой пептидный фрагмент аполипопротеина CII либо пептид-миметик В-клеточного эпитопа аполипопротеина B-100 расположены в таком порядке, от N-конца к С-концу, со связью между ними.
В предпочтительном варианте осуществления в соответствии с настоящим изобретением гибридный полипептид представляет собой полипептид (B4RCII), в котором четыре копии аминокислотной последовательности SEQ ID NO: 1 (B4), эпитоп Т-клетки хелпера вируса бешенства (R) и С-концевой пептидный фрагмент (CII) мышиного аполипопротеина CII связаны последовательно от N-конца к С-концу (SEQ ID NO: 9). В другом предпочтительном варианте осуществления настоящего изобретения гибридный полипептид представляет собой полипептид (B4RB2), который содержит четыре копии аминокислотной последовательности SEQ ID NO: 1 (B4), эпитоп Т-клетки хелпера вируса бешенства (R) и две копии аминокислотной последовательности SEQ ID NO: 1 (B2), связанные последовательно от N-конца к С-концу (SEQ ID NO: 10). Еще в одном предпочтительном варианте осуществления настоящего изобретения гибридный полипептид представляет собой полипептид (B4TB2), который содержит четыре копии аминокислотной последовательности SEQ ID NO: 1 (B4), эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В (T) и две копии аминокислотной последовательности SEQ ID NO: 1 (B2), связанные последовательно от N-конца к С-концу (SEQ ID NO: 11).
В соответствии с настоящим изобретением гибридный полипептид может состоять полностью из иммуногенных частей, в том числе В-клеточного эпитопа, эпитопа Т-клетки хелпера вируса бешенства или эпитопа Т-клетки хелпера поверхностного антигена вируса гепатита В, С-концевого пептидного фрагмента аполипопротеина CII и смежной с ним последовательности, и, кроме того, необязательно может содержать дополнительную последовательность. Однако дополнительную последовательность предпочтительно формируют для предотвращения снижения суммарной иммуногенности. Дополнительная последовательность содержит линкерную последовательность. В том случае, когда линкеры используют для связывания через них участков эпитопов, они должны быть выбраны таким образом, чтобы не оказывать отрицательного воздействия на индукцию иммунных реакций.
В другом аспекте настоящее изобретение относится к рекомбинантному вектору, содержащему полинуклеотид, кодирующий иммуногенный гибридный полипептид и рекомбинантный вектор экспрессии, содержащий полинуклеотид, и клетке-хозяину, трансформированной рекомбинантным вектором экспрессии, и способу получения иммуногенного гибридного полипептида путем культивирования клетки-хозяина, трансформированной рекомбинантным вектором экспрессии.
Иммуногенный гибридный полипептид по настоящему изобретению может быть получен путем химического синтеза или путем генной рекомбинации. Подробно способ получения иммуногенного гибридного полипептида по настоящему изобретению путем генетической рекомбинации включает в себя следующие четыре стадии:
Первой стадией является вставка гена, кодирующего гибридный полипептид, в вектор для конструирования рекомбинантного вектора. Вектор, в который вводят чужеродную ДНК, может быть плазмидой, вирусом, космидой или подобным. Рекомбинантный вектор включает в себя клонирующий вектор и вектор экспрессии. Клонирующий вектор содержит точку начала репликации, например точку начала репликации плазмиды, фага или космиды, который представляет собой «репликон», в котором начинается репликация фрагмента экзогенной ДНК, присоединенного к нему. Вектор экспрессии был разработан для использования в белковом синтезе. Рекомбинантный вектор служит в качестве носителя для фрагмента чужеродной ДНК, вставленного в него, который обычно обозначает фрагмент двухспиральной ДНК. Термин «чужеродная ДНК», используемый в контексте настоящего изобретения, относится к ДНК, полученной из гетерогенных видов, или по существу модифицированной форме нативной ДНК из гомогенных видов. Также чужеродная ДНК включает в себя немодифицированную ДНК последовательность, которая не экспрессируется в клетках в нормальных условиях. В этом случае чужеродный ген представляет собой специфическую транскрибируемую целевую нуклеиновую кислоту, которая кодирует полипептид. Рекомбинантный вектор содержит целевой ген, который оперативно связан с регуляторными последовательностями экспрессии на уровне транскрипции и трансляции, которые проявляют свои функции в выбранной клетке-хозяине, для повышения уровней экспрессии трансфектированного гена в клетке-хозяине. Рекомбинантный вектор представляет собой генетическую конструкцию, которая содержит необходимые регуляторные элементы, с которыми генная вставка оперативно связана для экспрессии в клетках индивидуума. Такую генную конструкцию получают, используя стандартную технологию рекомбинантных ДНК. Тип рекомбинантного вектора особым образом не ограничен, при условии, что этот вектор экспрессирует целевой ген в различных клетках-хозяевах, в том числе прокариотах и эукариотах, и функционирует для получения целевого белка. Однако предпочтительным является вектор, который способен к массовой продукции чужеродного белка в форме, аналогичной нативной форме, обладая сильным промотором для достижения высокой экспрессии целевого белка. Рекомбинантный вектор предпочтительно содержит по меньшей мере промотор, стартовый кодон, ген, кодирующий целевой белок, стоп-кодон и терминатор. Рекомбинантный вектор подходящим образом дополнительно может содержать ДНК, кодирующую сигнальный пептид, энхансерную последовательность, 5'- и 3'-нетранслируемые области целевого гена, область селективного маркера, единицу репликации или подобное.
Второй стадией является трансформирование клетки-хозяина рекомбинантным вектором и культивирование клетки-хозяина. Рекомбинантный вектор вводят в клетку-хозяина для получения трансформанта способом, описанным Sambrook, J. et al., Molecular Cloning, A Laboratory Manual (2nd Ed.), Cold Spring Harbor Laboratory, 1.74, 1989, этот способ включает в себя фосфат кальциевый или хлорид кальциевый/хлорид рубидиевый способ, электропорацию, электроинъекцию, химические обработки, такие как обработка ПЭГ, и генную пушку. Подходящий белок может быть получен и выделен в промышленном масштабе путем культивирования трансформанта, экспрессирующего рекомбинантный вектор в питательной среде. Обычная среда и условия культивирования могут быть подходящим образом выбраны в соответствии с клетками-хозяевами. Условия культивирования, в том числе температура, рН среды и время культивирования, должны поддерживаться подходящими для клеточного роста и массовой продукции белка, представляющего интерес. Клетки-хозяева, способные трансформироваться рекомбинантным вектором, в соответствии с настоящим изобретением включают в себя как прокариоты, так и эукариоты. Обычно могут быть использованы клетки-хозяева с высокой эффективностью введения ДНК, имеющие высокие уровни экспрессии введенной ДНК. Примеры клеток-хозяев включают в себя известные прокариотические и эукариотические клетки, такие как Escherichia sp., Pseudomonas sp., Bacillus sp., Streptomyces sp., грибы и дрожжи, клетки насекомых, таких как Spodoptera frugiperda (Sf9), и клетки животных, такие как CHO, COS 1, COS 7, BSC 1, BSC 40 и BMT 10. Предпочтительно может быть использована E.coli.
Третьей стадией является введение гибридного полипептида для экспрессии и аккумуляции. В настоящем изобретении IPTG индуктор был использован для индукции экспрессии пептида, и время индукции было подобрано для получения максимального выхода белка.
Конечной стадией является выделение и очистка гибридного полипептида. Обычно рекомбинантно полученный пептид может быть восстановлен из среды или клеточного лизата. В тех случаях, когда пептид находится в мембраносвязанной форме, он может быть высвобожден из мембраны с использованием подходящего раствора поверхностно-активного вещества (например, Тритона-X 100) или путем ферментативного расщепления. Клетки, использованные в экспрессии гибридного пептида, могут быть разрушены с помощью целого ряда физических или химических средств, таких как повторное замораживание и оттаивание, обработка ультразвуком, механическое разрушение или средство, разрушающее клетки, и гибридный полипептид может быть выделен и очищен с помощью обычно используемых биохимических способов выделения (Sambrook et al, Molecular Cloning: A laborarory Manual, 2nd Ed., Cold Spring Harbor Laboratoiy Press, 1989; Deuscher, M., Guide to Protein Purification Methods Enzymology, Vol.182. Academic Press. Inc., San Diego, CA, 1990). Неограничивающие примеры биохимических способов выделения включают в себя электрофорез, центрифугирование, гель-фильтрацию, преципитацию, диализ, хроматографию (ионобменную хроматографию, аффинную хроматографию, иммуносорбционную аффинную хроматографию, ВЭЖХ с обращенной фазой, гельпроникающую ВЭЖХ), изоэлектрофокусирование и их варианты и сочетания.
В предпочтительном варианте осуществления настоящего изобретения ген, кодирующий С-концевую область B4, тетрамерную форму пептида-миметика аполипопротеина B-100, который демонстрирует активность против ожирения, функциональный пептид, содержащий В-клеточный эпитоп, но не Т-клеточные эпитопы, был связан с частью гена, кодирующего нуклеопротеин вируса бешенства, содержащий Т-клеточный эпитоп (R фрагмент), а затем с частью гена аполипопротеина мыши (CII фрагмент) для конструирования гена B4RCII (фиг.3).
Использованный в настоящем изобретении фрагмент представляет собой фрагмент В4, который был описан в патенте Кореи №10-0639397. Аполипопротеин CII и гены RVNP (нуклеопротеина вируса бешенства, содержащего эпитоп Т-клетки хелпера) были получены с использованием ОТ-ПЦР. pQE30 был выбран в качестве вектора экспрессии для B4RCII, поскольку он инициирует экспрессию белка из его внутреннего стартового кодона вместе с шестью остатками гистидина для удобства очистки белка, за которыми следует сайт расщепления энтерокиназой. Было обнаружено, что размер белка, полученного таким образом, составляет 21 кДа, как подсчитано исходя из молекулярных масс его аминокислот, и приблизительно 22 кДа по измерениям с помощью SDS-PAGE. SDS-PAGE, с образцами, взятыми по времени, демонстрирует экспрессию белка, представляющего интерес (фиг.9).
В другом аспекте настоящее изобретение относится к вакцинной композиции для профилактики и лечения ожирения, содержащей иммуногенный гибридный полипептид.
Не существует единого правила, применимого к созданию пептидных вакцин, и эффективность созданных вакцин также является непредсказуемой. По некоторым причинам в тех случаях, когда высокогидрофобный пептид PB14 слит с Т-клеточным эпитопом, который представляет собой гетерогенный пептид, антигенная область может быть интернализована в слитом белке, приводя к снижению ее способности индуцировать антительные реакции. На этом фоне при трудноинтерпретируемых результатах был сконструирован гибридный полипептид, в котором пептид-миметик В-клеточного эпитопа аполипопротеина В-100, эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В, и С-концевой пептидный фрагмент аполипопротеина CII или пептид-миметик В- клеточного эпитопа аполипопротеина В-100 были слиты в таком порядке в направлении от N-конца к С-концу, и продемонстрировал наличие иммуногенности в отношении ожирения.
Крыс иммунизировали иммуногенным гибридным полипептидом по настоящему изобретению, экспрессированным и очищенным путем генной рекомбинации, и действие антигена на индукцию иммунных реакций оценивали путем исследования (a) увеличения массы тела, (b) титров сывороточных антител и (c) изменений профиля сывороточных липидов, тем самым определяя высокоэффективную форму антигена. В результате по сравнению с контрольной группой группа, вакцинированная гибридным полипептидом (B4RCII, B4RB2 и B4TB2), демонстрировала замедленное увеличение массы тела, высокие титры и более длительное сохранение антитела против пептида-миметика и сниженные сывороточные уровни ТГ и ЛПНП-холестерина.
Подробно, 50 мкл/150 мкл каждого очищенного B4RCII, B4RB2 и B4TB2 вводили внутрибрюшинно крысам ICR в возрасте 6 недель три раза с 2-недельными интервалами, и изменения массы тела крыс наблюдали и наносили на график (фиг.12). После первой иммунизации крыс сажали на диету с высоким содержанием жира, чтобы вызвать DIO (диета, индуцирующая ожирение). У всех крыс была примерно одинаковая масса тела, в интервале от 22 до 23 г, во всех группах до первой инъекции и иммунизации. Однако с начала DIO было обнаружено, что в контроле (ожирение) увеличивается масса тела, тогда как в группах, которым вводили B4RCII, B4RB2 или B4TB2, было показано только незначительное увеличение массы тела. В возрасте 14-недель (8 недель после первой инъекции) контрольная группа и группа, в которой вводили инъекцию B4RB2, отличались по массе тела приблизительно на 8 г, указывая на то, что слабая иммунная реакция, индуцированная первичной инъекцией, была усилена вторичной инъекцией до степени, достаточной для задержки увеличения массы. После третьей инъекции измеренная масса сохранялась в пределах ожидаемого диапазона отклонения.
Кроме того, мышей ICR в вакцинированных группах анализировали на титр антител в возрасте 7, 10, 12, 14, 16 и 18 недель, используя непрямой ELISA (фиг.12). Что касается уровня липидов в крови, у вакцинированных групп были обнаружены сниженные уровни общего холестерина крови (TC), триглицеридов (ТГ), ЛПВП холестерина и ЛПНП холестерина по сравнению с контролем (фиг.13).
Взятые вместе эти результаты демонстрируют, что гибридные полипептиды, B4RCII, B4RB2 и B4TB2 в соответствии с настоящим изобретением могут быть использованы в качестве эффективных вакцин против ожирения. Обладая способностью индуцировать более однородные и стабильные иммунные реакции по сравнению с традиционным гибридным полипептидом B4T, гибридные полипептиды в соответствии с настоящим изобретением могут быть использованы в получении эффективных вакцинных композиций против ожирения.
Вакцина против ожирения по настоящему изобретению состоит из антигена, фармацевтически приемлемого носителя, подходящего адъюванта и других общепринятых веществ, и ее вводят в иммунологически эффективном количестве. Термин «иммунологически эффективное количество», используемый в контексте настоящего изобретения, относится к количеству, которого достаточно для проявления терапевтического и профилактического эффекта при ожирении и которое не вызывает побочных эффектов или тяжелых или чрезмерных иммунных реакций. Точная дозировка может варьировать в зависимости от конкретного вводимого антигена и может быть определена специалистами в данной области, используя известный способ оценки развития иммунной реакции. Также эта дозировка может варьировать в зависимости от форм и путей введения, возраста реципиента, состояния здоровья и массы тела, свойств и степени развития симптомов, типов применяемой в текущий момент терапии и частоты введения. Носители известны в уровне техники и включают в себя стабилизаторы, разбавители и буферы. Подходящие стабилизаторы включают в себя углеводы, такие как сорбит, лактоза, маннит, крахмал, сахароза, декстран и глюкоза, и белки, такие как альбумин или казеин. Подходящие разбавители включают в себя солевой раствор, сбалансированный солевой раствор Хенкса и раствор Рингера. Подходящие буферы включают в себя фосфат щелочного металла, карбонат щелочного металла и карбонат щелочноземельного металла. Вакцина также может содержать один или несколько адъювантов для улучшения или усиления иммунных реакций. Подходящие адъюванты включают в себя пептиды; гидроксид алюминия; фосфат алюминия; оксид алюминия; и композицию, которая состоит из минерального масла, например Marcol 52, или растительного масла и одного или нескольких эмульгирующих агентов, или поверхностно-активных веществ, таких как лизолецитин, поликатионы и полианионы. Вакцинную композицию по настоящему изобретению можно вводить в качестве индивидуального терапевтического средства или в комбинации с другим терапевтическим средством, и ее можно вводить совместно либо последовательно, либо одновременно с общепринятым терапевтическим средством. Вакцинную композицию можно вводить с помощью известных путей введения. Способы введения включают пероральный, внутрикожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный и интраназальный пути, но не ограничиваются ими. Также фармацевтическую композицию можно вводить, используя определенный прибор, который может осуществлять доставку активного вещества к клеткам-мишеням.
Способ осуществления изобретения
Лучшее понимание настоящего изобретения достигается посредством следующих примеров, которые изложены для иллюстрации, а не для ограничения настоящего изобретения.
Пример 1
Подготовка экспериментальных материалов и экспериментальных животных
Набор DNA miniprep и набор, используемый для экстракции ДНК из геля, приобретали у фирмы Nucleogen, триптон Bacto, дрожжевой экстракт Bacto, агар и т.д. - у фирмы Difco (Detroti, MI), ферменты рестрикции - у Takara, и T4 ДНК-лигазу - у NEB. Использовали pBluescript II SK (Stratagene), ПЦР 2.1 (Invitrogen, Carlsbad, CA) и pQE30 (Qiagen) векторы и E.coli штаммов JM109 и M15 (Qiagen). IPTG, используемый для индукции продукции белка, приобретали у фирмы Sigma, смолу Ni-NTA, используемую для очистки экспрессированных белков, приобретали у Novagen, и предварительно окрашенный маркер, используемый в SDS-PAGE, Вестерн-блоттинге, ЭХЛ, и т.д. - у NEB. Мочевину, используемую для денатурации белков, приобретали у Duchefa, и имидазол, используемый при очистке белка, - у USB. Мембрану, используемую при диализе, представляющую собой MWCO 3500, приобретали у Spectrum, и реактив, используемый для предотвращения агрегации белка, представлял собой CHAPS от фирмы Amresco. Антитело, используемое в ELISA, представляло собой HRP-конъюгированный антикрысиный IgG от фирмы Sigma. Субстратный раствор, используемый в Вестерн-блоттинге и ЭХЛ, представлял собой BCIP/NBT от фирмы Sigma, и реактив для детекции ECL Plus Western Blotting Detection Reagent приобретали у фирмы Amersham. Используемые адъюванты представляли собой адъювант Фрейнда (Sigma) и гидроксид алюминия (Reheis). Концентрацию белка определяли с помощью методики анализа белка Pierce's BCA protein assay и Biorad's Bradford assay.
Самок мышей ICR в возрасте 6 недель приобретали в Central Lab. Animal Inc., Корея. Мышей ICR разводили на нормальной диете (Samtako, Inc., натуральные белки 18% или выше, неочищенный жир 5,3%, сырая клетчатка 4,5%, минералы 8,0%) до активизации иммунного ответа, а затем на диете с высоким содержанием жира (60% жировых кКал, D12492, Research Diets Inc., New Brunswick, NJ).
Пример 2
Клонирование гена мышиного ApoCII
2-1. Выделение общей РНК из печеночной ткани мышей
Выделение общей РНК проводили с использованием TRIzol (Invitrogen). Все растворы, используемые для выделения РНК, обрабатывали водой, обработанной 0,1% диэтилпирокарбонатом (DEPC-dH2O) для ингибирования РНазной активности. 50 мг ткани печени мышей смешивали с 2 мл TRIzol с последующей гомогенизацией. Гомогенат помещали на лед на 20 минут и центрифугировали при 4°C при 14000 об/мин в течение 15 мин. Супернатант переносили в новую пробирку с осторожностью для исключения любого белка из пробирки. В пробирку добавляли 200 мкл хлороформа (Merck), которую затем встряхивали в течение 30 сек. Еще раз реакция на льду в течение 20 мин сопровождалась центрифугированием при 4°C, 14000 об/мин в течение 15 мин. В новую пробирку переносили только супернатант и смешивали с таким же объемом фенола/хлороформа и 0,2 М ацетата натрия (pH 5,2) перед интенсивным перемешиванием в течение 5 сек. После помещения на лед на 20 мин смесь центрифугировали при 4°C и 14000 об/мин в течение 15 мин. Супернатант смешивали с равным объемом изопропанола (Merck) и хранили при -70°C в течение 1 часа с последующим центрифугированием при 4°C и 14000 об/мин в течение 10 мин с получением осадка РНК. Этот осадок промывали 1 мл 75% этанола, сушили и суспендировали в DEPC-dH2O перед хранением при -70°C. Полученную таким образом РНК идентифицировали путем электрофореза на 1% агарозном геле (0,5% TAE), а концентрацию РНК определяли с помощью GeneQuant II (Pharmacia biotech).
2-2. Синтез кДНК из общей РНК
Синтез кДНК осуществляли, используя набор cDNA cycle™ (Invitrogen). 400 нг РНК помещали в пробирку для ПЦР и смешивали с DEPC-dH2O для получения конечного объема 11,5 мкл. Реакционную смесь хорошо перемешивали с 1 мкл праймеров олиго-dT и реакцию проводили в течение 10 мин на водяной бане 65°C, а затем в течение 2 мин при комнатной температуре. Смесь ингибитора РНазы 1,0 мкл, 5X RT буфера 4,0 мкл, 100 мМ dNTPs 1,0 мкл, 80 мМ пирофосфата натрия 1,0 мкл и обратной транскриптазы AMV 0,5 мкл добавляли в пробирку, которую затем слегка закручивали, помещали на 1 час на водяную баню 42°C и на 2 мин при 95°C и сразу же хранили на льду. После добавления 1,0 мкл 0,5 M EDTA (pH 8,0) и 20 мкл фенолхлороформа смесь интенсивно перемешивали и центрифугировали при 4°C, 14000 об/мин в течение 15 мин. Полученный таким образом супернатант переносили в новую пробирку, добавляли 22 мкл ацетата аммония и 88 мкл 75% этанола, перемешанные путем встряхивания, и хранили в течение ночи при -70°C. После центрифугирования при 4°C, 14000 об/мин в течение 15 мин полученный в результате осадок ресуспендировали в 20 мкл деионизированной воды. кДНК идентифицировали электрофорезом на 1% агарозном геле (0,5% буфер TAE).
2-3. ПЦР С-концевого фрагмента мышиного аполипопротеина CII
ДНК-амплификатор 480 использовали для всех ПЦР в этом примере. Для использования в ПЦР для амплификации 99 генов, в том числе области, активирующей липазу, мышиного аполипопротеина CII, синтезировали пару праймеров apoCII-прямой (5'-tc aga GTC GAC gat gag aaa ctc agg gac-3') и apoCII-обратный (5'-tat AAG CTT ggg ctt gcc tgg cag cag cta c-3'). Сначала в пробирку для ПЦР добавляли по 1 мкл прямого праймера apoCII и обратного праймера apoCII (2 пмоль/мкл) и 2 мкл кДНК, синтезированной в примере 2-2. Наконец, готовили 50 мкл ПЦР-смеси, содержащей 5 мкл 10 X буфера, 8 мкл dNTP и 1 мкл Taq ДНК полимеразы (Takara). ПЦР начинали предварительной денатурацией при 94°C в течение 5 мин, а затем 30 циклами денатурации при 98°C в течение 30 сек, отжига при 56°C в течение 30 сек и удлинением при 72°C в течение 30 сек с последующим удлинением при 72°C в течение 5 мин. Продукт ПЦР идентифицировали электрофорезом на 1,5% агарозном геле (0,5% буфер TAE) (фиг.1b).
2-4. Конструирование АпоСII/pQE30
ПЦР продукт apoCII расщепляли с помощью SalI и HindIII. Те же ферменты рестрикции применяли для pQE30.
Продукт расщепления CII лигировали в течение ночи с линейным вектором pQE30 в присутствии ДНК лигазы T4 при 16°C. pQE30, экспрессионный вектор, создают для продукции белка с пришитыми 6 остатками гистидина, что позволяет осуществлять удобную очистку белка. Полученную таким образом рекомбинантную плазмиду трансформировали в JM109 E.coli и амплифицировали. После получения из трансформанта плазмиду обрабатывали SalI и HindIII для идентификации вставки в нее гена, представляющего интерес.
Пример 3
Конструирование искусственного гена RCII
3-1. Выделение геномной ДНК из штамма ERA вируса бешенства
Выделение общей РНК проводили с использованием TRIzol (Invitrogen). Все растворы, используемые для выделения РНК, обрабатывали водой, обработанной 0,1% диэтилпирокарбонатом (DEPC-dH2O) для ингибирования РНазной активности. Для использования в выделении общей РНК вирус бешенства получали из вакцины против вируса бешенства. Сначала 200 мкл 20% (мас./об.) раствора полиэтиленгликоля-800, содержащего 2,5 M NaCl, добавляли к 1,2 мл вакцины и помещали на лед на 1 час с последующим центрифугированием при 4°C и 14000 об/мин в течение 10 мин. Полученный таким образом вирусный осадок смешивали с 1 мл TRIzol и пипетировали в достаточной степени. Гомогенат помещали на лед на 20 минут и центрифугировали при 4°C и 14000 об/мин в течение 15 мин. Супернатант переносили в новую пробирку с осторожностью, предпринятой, чтобы исключить из пробирки любой белок. 200 мкл хлороформа (Merck) добавляли в пробирку, которую затем интенсивно встряхивали в течение 30 сек. Еще раз реакция на льду в течение дополнительных 20 мин сопровождалась центрифугированием при 4°C и 14000 об/мин в течение 15 мин. Только супернатант переносили в новую пробирку и перемешивали с таким же объемом фенол/хлороформа и 0,2 M ацетата натрия (pH 5,2) перед интенсивным перемешиванием в течение 5 сек. После размещения на льду в течение 20 мин смесь центрифугировали при 4°C и 14000 об/мин в течение 15 мин. Супернатант перемешивали с равным объемом изопропанола (Merck) и хранили при -70°C в течение 1 часа с последующим центрифугированием при 4°C и 14000 об/мин в течение 10 мин для идентификации осадка РНК. Этот осадок промывали 1 мл 75% этанола, сушили и ресуспендировали в DEPC-dH2O перед хранением при -70°C. Полученную таким образом РНК идентифицировали электрофорезом на 1% агарозном геле (0,5% TAE), а концентрацию РНК определяли, используя GeneQuant II (Pharmacia biotech).
3-2. Синтез кДНК из геномной РНК
Синтез кДНК осуществляли, используя набор cDNA Cycle™ (Invitrogen). 400 нг РНК помещали в пробирку для ПЦР и смешивали с DEPC-dH2O с получением конечного объема 11,5 мкл. Смесь хорошо перемешивали с 1 мкл случайного гексамера и реакцию проводили в течение 10 мин на водяной бане 65°C, а затем в течение 2 мин при комнатной температуре. В пробирку добавляли смесь ингибитора РНазы 1,0 мкл, 5X ОТ буфера 4,0 мкл, 100 мМ dNTPs 1,0 мкл, 80 мМ фосфата натрия 1,0 мкл и обратную транскриптазу AMV 0,5 мкл, которую затем слегка закручивали, помещали на 1 час на водяную баню 42°C и на 2 мин при 95°C и сразу же хранили на льду. После добавления 1,0 мкл 0,5 M EDTA (pH 8,0) и 20 мкл фенолхлороформа, смесь интенсивно перемешивали и центрифугировали при 4°C, 14000 об/мин в течение 15 мин. Образованный таким образом супернатант переносили в новую пробирку, в которую добавлено 22 мкл ацетата аммония и 88 мкл 75% этанола, перемешивали встряхиванием и хранили в течение ночи при -70°C. После центрифугирования при 4°C 14000 об/мин в течение 15 мин полученный в результате осадок ресуспендировали в мкл деионизированной воды. кДНК идентифицировали электрофорезом на 1% агарозном геле (0,5% буфер TAE).
3-3. ПЦР гена нуклеопротеина штамма ERA вируса бешенства
Для амплификации 174 генов нуклеопротеина штамма ERA вируса бешенства, которые, как известно, кодируют Т-клеточные эпитопы (2), проводили ПЦР с парой прямых праймеров RVNP (5'-ATA CTC GAG GAC GTA GCA CTG GCA GAT G-3') и обратных праймеров RVNP (5'-ATA CTC GAG GTT TGG ACG GGC ATG ACG-3'). Сначала в пробирку для ПЦР добавляли по 1 мкл прямого праймера RVNP и обратного праймера RVNP (2 пмоль/мкл) и 2 мкл кДНК, синтезированной в примере 3-2. Наконец, готовили 50 мкл ПЦР-смеси, содержащей 5 мкл 10 X буфера, 8 мкл dNTP и 1 мкл ДНК полимеразы Taq (Takara). ПЦР начинали предварительной денатурацией при 94°C в течение 5 мин, а затем 30 циклами денатурации при 98°C в течение 30 сек, отжига при 54°C в течение 30 сек и удлинения при 72°C в течение 30 сек с последующим удлинением при 72°C в течение 5 мин. Продукт ПЦР идентифицировали электрофорезом на 1,5% агарозном геле (0,5% буфер TAE).
3-4. Конструирование RCII/pQE30
ПЦР продукт RVNP расщепляли XhoI, а вектор ApoCII/pQE30 обрабатывали XhoI и SalI.
Продукт расщепления ПЦР RVNP лигировали в течение ночи с линеаризованным вектором ApoCII/pQE30 в присутствии ДНК лигазы T4 при 16°C. Полученную в результате рекомбинантную плазмиду трансформировали в JM109 E.coli и амплифицировали. После получения из трансформанта плазмиду обрабатывали SalI и HindIII для идентификации вставки гена, представляющего интерес, в соответствующем направлении.
Пример 4
Конструирование вектора pB4RCII
Тот же фрагмент B14, вставленный в pQE30, как описано в корейском патенте № 10-0639397, получали обработкой XhoI. Отдельно вектор pQE30, несущий фрагмент RCII, резали с помощью XhoI и лигировали в течение ночи с фрагментом Bl4 в присутствии ДНК лигазы T4 при 16°C с получением рекомбинантной плазмиды BL4RCII/pQE30(pB4RCII). 300-500 нг/мкл pB4RCII передавали Cosmo Co. Ltd. для секвенирования ДНК. После получения из E.coli JM109 якорного вектора BL4RCII/pQE30 его обрабатывали SalI для идентификации вставки гена в соответствующем направлении (фиг.2b). Аминокислотная последовательность B4RCII представлена последовательностью SEQ ID NO: 9.
Пример 5
Конструирование вектора pB4RB2
Вектор BX2/pQE30(pB2), описанный в корейском патенте № 10-0472841, расщепляли с помощью SalI и XhoI. Фрагмент R, полученный в примере 3, лигировали в течение ночи с линеаризованным BX2/pQE30 в присутствии ДНК лигазы T4 при 16°C с получением рекомбинантной плазмиды RBX2/pQE30(pRB2).
Фрагмент B4, который может быть получен путем разрезания pB4RCII из примера 4 с помощью XhoI, лигировали с pTB2, который также предварительно обрабатывали XhoI, в присутствии ДНК лигазы T4 при 16°C в течение 15 часов с получением рекомбинантной плазмиды B4RBX2/pQE30(pB4RB2). После получения из E.coli JM109 якорного вектора B4RBX2/pQE30 его обрабатывали SalI для идентификации вставки гена в соответствующем направлении (фиг.2c). Аминокислотная последовательность B4RB2 представлена последовательностью SEQ ID NO: 10.
Пример 6
Конструирование вектора pB4TB2
Вектор BX2/pQE30(pB2), описанный в корейском патенте № 10-0472841, расщепляли с помощью SalI и XhoI. Фрагмент T получали путем расщепления вектора ПЦР 2.1, описанного в корейском патенте №10-0639397. Фрагмент T лигировали в течение ночи с линеаризованным BX2/pQE30 в присутствии ДНК лигазы Т4 при 16°C с получением рекомбинантной плазмиды TBX2/pQE30(pRB2).
Фрагмент B4, который был получен разрезанием pBluescriptII SK 4 с помощью SalI и XhoI, лигировали в течение ночи с pTB2, который также предварительно обрабатывали SalI, в присутствии ДНК лигазы Т4 при 16°C с получением рекомбинантной плазмиды B4TBX2/pQE30(pB4TB2). После получения из E.coli JM109 якорного вектора B4TBX2/pQE30 его обрабатывали SalI и HindIII для идентификации вставки гена в соответствующем направлении (фиг. 2d). Аминокислотная последовательность B4TB2 представлена последовательностью SEQ ID NO: 11.
Пример 7
Экспрессия рекомбинантных векторов B4RCII, B4RB2 и B4TB2
M15 для использования в качестве клетки-хозяина при экспрессии белка распределяли по чашке LB, содержащей ампициллин и канамицин, и появлялись колонии. Одну из них культивировали в течение ночи в 10 мл жидкой питательной среды LB, содержащей Amp (50 мкг/мл) и Kan (50 мкг/мл). 1 мл культуры инокулировали в 50 мл свежей жидкой питательной среды LB для наблюдения за индукцией белка с течением времени. Культуру инкубировали при 37°C в течение 1,5 часов со встряхиванием до достижения поглощения при 600 нм 0,4~0,5, после чего добавляли IPTG в конечной концентрации 1 мМ и брали образец 1 мл культуры с равными промежутками времени 1 час во время инкубирования в течение дополнительных 5 часов. Перед добавлением IPTG брали 1 мл культуры и использовали в качестве контроля. Каждую культуру центрифугировали при 14000 об/мин в течение 1 мин и осадки, полученные таким образом, ресуспендировали в 30 мкл 2 X SDS буфера для образцов перед SDS-PAGE. Было вычислено, что белки имеют размер 22 кДа для B4RCII, 21кДа для B4RB2 и 20 кДа для B4TB2. Результаты SDS-PAGE представлены на фиг.9(a)-9(c), демонстрирующие экспрессию белков с течением времени.
Пример 8
Вестерн-блоттинг для рекомбинантного пептида B4RCII, B4RB2 и B4TB2
Пептид B4RCII, B4RB2 и B4TB2 идентифицировали фракционным анализом, используя SDS-PAGE, но для дальнейшего подтверждения того, что экспрессированный белок представляет собой B4RCII, B4RB2 и B4TB2, проводили Вестерн-блоттинг, используя два антитела, способные распознавать B4RCII, B4RB2 и B4TB2. В качестве контроля в Вестерн-блоттинге для B4RCII, B4RB2 и B4TB2 E.coli M15 трансформировали вектором pQE30, не содержащим фрагмент B4RCII, B4RB2 и B4TB2. Образцы брали до IPTG индукции и через четыре часа после IPTG индукции.
Кроличьи поликлональные антитела против PBl4 разводили 1:10000 в PBS и использовали в качестве первичных антител. В качестве вторичных антител, способных распознавать первичные антитела, использовали козьи антикроличьи IgG, слитые пероксидазой, после разведения в PBS 1:10000. Полученный в результате блот проявляли, используя набор ECL Plus Western Blotting Kit. Блот помещали в кассету и лист медицинской рентгеновской пленки Fuji располагали на блоте. Блот экспонировали с пленкой в течение 10 сек и проявляли. Как показано на фиг.9(d), B4RCII экспрессировался правильно.
Пример 9
Идентификация рекомбинантного B4RCII, B4RB2 и B4TB2 в бактериальной клетке
После центрифугирования клеточных культур, индуцированных для экспрессии белка, как в примере 5, при 4°C, 9000 об/мин в течение 30 мин, осадки замораживали в течение короткого периода времени при -20°C и размораживали на льду. По 1 г каждого осадка ресуспендировали в 5 мл буфера для обработки ультразвуком и разрушали с помощью 15 циклов обработки ультразвуком в течение 30 сек с перерывом на 1 мин на цикл. Центрифугирование при 4°C, 9000 об/мин в течение 30 мин давало растворимые белки в супернатанте (сырой экстракт A) и нерастворимые белки в осадке (сырой экстракт B). Каждый образец смешивали с 2 X SDS буфера и кипятили при 95°C в течение 5 мин непосредственно перед SDS-PAGE (фиг.10).
Пример 10
Получение буферов для очистки рекомбинантного B4RCII, B4RB2 и B4TB2
Буферы готовили следующим образом: 5 мМ имидазол, 0,5 M NaCl, 20 мМ Трис-Cl, pH 7,9 для буфера для ультразвуковой обработки; 5 мМ имидазол, 0,5 M NaCl, 20 мМ Трис-Cl, 8 M мочевина, pH 7,9 для связывающего буфера; 50 мМ имидазол, 0,5 M NaCl, 20 мМ Трис-Cl, 8 M мочевина, pH 7,9 для промывочного буфера; 400 мМ имидазол, 0,5 M NaCl, 20 мМ Трис-Cl, 8 M мочевина, pH 7,9 для элюирующего буфера.
Пример 11
Очистка рекомбинантного белка B4RCII, B4RB2 и B4TB2
Пептидную очистку проводили, используя смолу Ni-NTA (Novagen) для белков, меченных гистидином. Такая очистка представляет собой метод аффинной хроматографии с помощью взаимодействия между Ni+ связанного со смолой и гистидиновым гексамером на N-конце слитого белка. После предварительного культивирования клеток E.coli в 10 мл среды LB в течение ночи 10-мл культуры инокулировали в 500 мл среды LB и культивировали при 37°C до достижения ОП при 600 нм от 0,4 до 0,5. Затем к среде добавляли 1 мМ IPTG и клетки дополнительно культивировали в течение 4 часов. Эти клетки центрифугировали при 9000 об/мин в течение 30 мин и клеточный осадок размещали при -20°C. После размораживания замороженных клеток на льду их ресуспендировали в буфере для разрушения ультразвуком (5 мл/г сырых клеток) и обрабатывали ультразвуком. Клеточный лизат затем центрифугировали при 9000 об/мин при 4°C в течение 30 мин. Осадок ресуспендировали в объеме связывающего буфера, равном объему супернатанта, обрабатывали ультразвуком три раза для удаления клеточного дебриса и центрифугировали при 9000 об/мин, 4°C в течение 30 мин. Полученный таким образом супернатант подвергали аффинной хроматографии, используя смолу Ni-NTA. Диаметр колонки составлял 1 см, высота колонки составляла 15 см, и колонка была заполнена 2 мл смолы, и все стадии проводились со скоростью потока 2 мл/мл. После заполнения колонки смолой смолу промывали дистиллированной водой тремя - пятью объемами колонки и смолу заряжали Ni2+, используя пять объемов колонки Ix заряжающим буфером (50 мМ NiSO4), и уравновешивали связывающим буфером, таким образом получая аффинную колонку Ni-хелат. После загрузки образцов на колонку дважды колонку промывали связывающим буфером до достижения поглощения при 280 нм фонового значения 1,0, а затем промывочным буфером в течение 10 мин. После того как колонка была полностью уравновешена, через колонку пропускали только элюирующий буфер и собирали элюированные белки. Поскольку элюированный пептид был растворен в 8 M мочевине, его подвергали диализу в PBS для удаления мочевины. Диализ проводили медленным снижением концентрации мочевины для правильной переукладки белков. Поглощение при 280 нм фракций белков с переукладкой структуры при хроматографии было показано на фиг.6(a), 6(c) и 6(e). Фракции, полученные на различных стадиях, были идентифицированы с помощью SDS-PAGE, как показано на фиг.10(b), 10(d) и 10(f).
Пример 12
Количественная оценка рекомбинантных белков B4RCII, B4RB2 и B4TB2
Поскольку B4RCII не агрегировал в преципитаты, хотя подвергался диализу с медленным снижением концентрации мочевины, его количество определяли при таком условии. Количественную оценку белка проводили, используя белковый анализ BCA и УФ-поглощение. Стандарты BSA для белкового анализа ВСА готовили разведением 2,0 мг/мл маточного раствора BSA в 1000, 500, 250, 125 и 62,5 мкг/мл. Образцы взаимодействовали со смесью 50:1 Реактив A: Реактив B при 37°C в течение 30 мин и проводили измерение поглощения при 562 нм. Концентрации белка определяли, используя стандартную кривую. Что касается УФ-поглощения, концентрации белка определяли путем деления поглощения при 280 нм на 1,63, что представляет собой величину ε B4RCII.
Пример 13
Иммунизация мышей ICR
Мышей ICR распределяли на пять групп, в том числе группу положительного контроля (ожирение, индуцированное рационом питания (DIO)), отрицательного контроля (не-DIO, нормальная группа), группу, иммунизированную B4RCII, группу, иммунизированную B4RB2, и группу, иммунизированную B4TB2. Мышам ICR в возрасте 6 недель внутрибрюшинно вводили 100 мкл раствора, содержащего 50 мкг B4RCII, B4RB2 или B4TB2. После повторения инъекции три раза с равными промежутками времени в две недели регистрировали массу тела и изменения отмечали на графике. После первой иммунизации мышей сажали на диету с высоким содержанием жира, чтобы подвергнуть мышей DIO (ожирению, индуцированному рационом питания). Образцы крови брали из хвоста через одну неделю после первой иммунизации и через три недели и через пять недель после вторичной иммунизации.
Как показано на фиг.11, масса тела отдельных мышей была сходной, в интервале от 22 до 23 г, во всех группах до первой инъекции и иммунизации. Однако со времени DIO было обнаружено, что в контрольной группе (с ожирением) масса тела животных увеличивается, тогда как в группах, в которых вводили B4RCII, B4RB2 или B4TB2, было показано только незначительное увеличение массы тела. В возрасте 14 недель (8 недель после первой инъекции) контрольная группа и группа, в которой вводили инъекцию B4RB2, отличались по массе тела животных приблизительно на 8 г, указывая на то, что слабый иммунный ответ, индуцированный первой инъекцией, был усилен вторичной инъекцией до степени, достаточной для замедления увеличения массы тела. После третьей инъекции измеренный прирост массы тела оставался в пределах ожидаемого диапазона отклонения.
Пример 14
Титры антител измеряли с помощью непрямого ELISA, используя образцы сыворотки
100 мкл (100 нг) PB14 помещали в каждую лунку микротитровального планшета. Планшет инкубировали при 4°C в течение ночи и инкубировали в блокирующем растворе (PBS, 0,5% казеина, 0,02% NaN3) при 37°C в течение 1 часа. Каждую лунку промывали промывочным буфером три раза. Образцы сыворотки, полученные в примере 10, разводили в PBS от 1:1000 до 1:8000. 100 мкл каждого разведенного образца сыворотки добавляли в каждую лунку и инкубировали при 37°C в течение 1 часа. Каждую лунку промывали промывочным буфером три раза и инкубировали с разведенным 1:1000 козьим антимышиным IgG в качестве вторичного антитела.
Как показано фиг.12, в группах, иммунизированных B4RB2 или B4TB2, повышался титр антител до 14-недельного возраста, но снижался с этого момента времени, тогда как титр антител в группе, иммунизированной B4RCII, повышался до 16-недельного возраста и снижался с этого момента времени.
Пример 15
Оценка профилей сывороточных липидов
Уровни ТГ и холестерина измеряли следующим образом. 4 мкл образца сыворотки смешивали с 200 мкл проявляющего реактива и инкубировали при 37°C в течение 5 мин, а затем измеряли поглощение при 505 нм и 500 нм. Для измерения уровней ЛПВП образец сыворотки смешивали с осаждающим реагентом в соотношении 1:1, оставляли при комнатной температуре на 10 мин и центрифугировали свыше 3000 об/мин в течение 10 мин. 4 мкл центрифугированного супернатанта смешивали с 200 мкл проявляющего реагента и инкубировали при 37°C в течение 5 мин, а затем измеряли поглощение при 555 нм. Уровни холестерина ЛПНП измеряли, используя набор EZ LDL cholesterol (Sigma) и калибратор ЛПНП (Randox). В соответствии с протоколом, предоставляемым производителем, 4 мкл образца сыворотки смешивали с 1150 мкл реактива, содержащегося в этом наборе, инкубировали при 37°C в течение 5 мин, дополняли 250 мкл этого реактива и снова инкубировали при 37°C в течение 5 мин. Затем измеряли поглощение при 600 нм. Сывороточные уровни каждого липида определяли, используя измеренное поглощение, и получали стандартную кривую, используя стандартные растворы.
Что касается уровней липидов в крови, как показано на фиг.13, было обнаружено, что в вакцинированных группах в крови ниже уровни общего холестерина (ОХ), триглицеридов (ТГ), холестерина ЛПВП и холестерина ЛПНП по сравнению с контролем (ожирение).
Промышленная применимость
Как описано в настоящем изобретении, иммуногенные гибридные полипептиды в соответствии с настоящим изобретением могут применяться у млекопитающих, таких как собаки, кошки, крупный рогатый скот и т.д., а также у людей. Обладая способностью индуцировать более однотипные и стабильные иммунные реакции, гибридные полипептиды применимы для профилактики и лечения ожирения у животных, а также у людей.







Изобретение относится к биотехнологии и представляет собой иммуногенный гибридный полипептид для профилактики или лечения ожирения. Также описана вакцина для профилактики или лечения ожирения, содержащая иммуногенный гибридный полипептид. Кроме того, описаны полинуклеотид, кодирующий иммуногенный гибридный полипептид, рекомбинантный вектор экспрессии, несущий этот полинуклеотид, клетка-хозяин, трансформированная рекомбинантным вектором экспрессии, и способ получения иммуногенного гибридного полипептида путем культивирования клетки-хозяина, трансформированной рекомбинантным вектором экспрессии. Изобретение может эффективно использоваться в качестве средства для профилактики или лечения ожирения. 6 н. и 12 з.п. ф-лы, 25 ил.
1. Иммуногенный гибридный полипептид для вакцины для профилактики или лечения ожирения, содержащий (i) мультимер размером от димера до тетрамера пептида, имеющего аминокислотную последовательность SEQ ID NO: 1; (ii) эпитоп Т-клетки хелпера вируса бешенства или эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В; и (iii) С-концевой пептидный фрагмент мышиного аполипопротеина CII или мультимер размером от димера до тетрамера пептида, имеющего аминокислотную последовательность SEQ ID NO: 1, в порядке в направлении от их N-конца к С-концу.
2. Иммуногенный гибридный полипептид по п.1, в котором тетрамер содержит четыре пептида, имеющих аминокислотную последовательность SEQ ID NO: 1.
3. Иммуногенный гибридный полипептид по п.1, в котором тетрамер имеет аминокислотную последовательность SEQ ID NO: 5.
4. Иммуногенный гибридный полипептид по п.1, в котором эпитоп Т-клетки хелпера вируса бешенства имеет аминокислотную последовательность SEQ ID NO: 6.
5. Иммуногенный гибридный полипептид по п.1, в котором эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В имеет аминокислотную последовательность SEQ ID NO: 7.
6. Иммуногенный гибридный полипептид по п.1, в котором С-концевой пептидный фрагмент аполипопротеина CII имеет аминокислотную последовательность SEQ ID NO: 8.
7. Иммуногенный гибридный полипептид по п.1, в котором димер содержит два пептида, имеющих аминокислотную последовательность SEQ ID NO: 1.
8. Иммуногенный гибридный полипептид по п.1, содержащий (i) тетрамер пептида, имеющего аминокислотную последовательность SEQ ID NO: 1;
(ii) эпитоп Т-клетки хелпера вируса бешенства; и (iii) С-концевой пептидный фрагмент мышиного аполипопротеина CII, в порядке в направлении от их N-конца к С-концу.
9. Иммуногенный гибридный полипептид по п.8, имеющий аминокислотную последовательность SEQ ID NO: 9.
10. Иммуногенный гибридный полипептид по п.1, содержащий (i) тетрамер пептида, имеющего аминокислотную последовательность SEQ ID NO: 1; (ii) эпитоп Т-клетки хелпера вируса бешенства; и (iii) димер пептида, имеющего аминокислотную последовательность SEQ ID NO: 1, в порядке в направлении от их N-конца к С-концу.
11. Иммуногенный гибридный полипептид по п.10, имеющий аминокислотную последовательность SEQ ID NO: 10.
12. Иммуногенный гибридный полипептид по п.1, содержащий (i) тетрамер пептида, имеющего аминокислотную последовательность SEQ ID NO: 1; (ii) эпитоп Т-клетки хелпера поверхностного антигена вируса гепатита В; и (iii) димер пептида, имеющего аминокислотную последовательность SEQ ID NO: 1, в таком порядке в направлении от их N-конца к С-концу.
13. Иммуногенный гибридный полипептид по п.12, имеющий аминокислотную последовательность SEQ ID NO: 11.
14. Вакцина для профилактики или лечения ожирения, содержащая иммуногенный гибридный полипептид по одному из пп.1-13, в качестве активного ингредиента.
15. Полинуклеотид, кодирующий иммуногенный гибридный полипептид по одному из пп.1-13.
16. Рекомбинантный вектор экспрессии, содержащий полинуклеотид по п.15.
17. Клетка-хозяин, трансформированная рекомбинантным вектором экспрессии по п.16.
18. Способ получения иммуногенного гибридного полипептида по п.1, предусматривающий культивирование клетки-хозяина, трансформированной рекомбинантным вектором экспрессии по п.16.
| US 2003211997, 13.11.2003 | |||
| US 2004242474, 02.12.2004 | |||
| WO 2005014622, 17.02.2005 | |||
| Partidos С | |||
| et al | |||
| "The effect of orientation of epitopes on the immunogenicity of chimeric synthetic peptides representing measles virus protein sequences" | |||
| Mol Immunol | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
Авторы
Даты
2011-05-10—Публикация
2007-09-21—Подача