Область техники, к которой относится изобретение
Настоящее изобретение имеет отношение к иммуногенному гибридному полипептиду, который включает аминокислотную последовательность миметического пептида В-клеточного эпитопа аполипопротеина В-100, в котором С-конец миметического пептида слит с N-концом Т-хелперного эпитопа; и к вакцинной композиции для предупреждения или лечения ожирения, включающей этот полипептид.
Уровень техники
В последнее время в Корее постепенно участились случаи атеросклероза и сосудистых атеросклеротических заболеваний (CAD, coronary atherosclerotic disease), являющиеся основной причиной возросшей смертности и возникающие из-за перехода к пище, предпочитаемой на Западе. Сывороточные липиды, вызывающие эти заболевания, включают холестерин, триглицериды (TG), свободные жирные кислоты и фосфолипиды. Они образуют липопротеины с аполипопротеинами и транспортируются через кровяное русло. Среди них липопротеины низкой плотности (LDL, low density lipoproteins) функционируют для транспортировки в основном TG и холестерина, и изменение в уровне LDL-холестерина является указанием для прогноза заболеваний.
LDL-холестерин, который является главным фактором заболеваний, ассоциированных с обменом липидов у взрослых людей, присоединяется к рецепторам LDL на плазматической мембране клеток любых тканей и хранится и используется в ткани. Альтернативно, LDL-холестерин поглощается гистофагоцитами и гидролизуется, свободный холестерин переносится к липопротеинам высокой плотности (HDL) вместе с липопротеином Е для рециркуляции в печени или превращается в желчную соль для выделения. Во время этого процесса аполипопротеин выполняет очень важные функции для поддержания структурного гомеостаза липопротеинов, служит как кофактор для фермента липопротеинлипазы и играет решающую роль в связывании со специфическим рецептором на плазматической мембране.
Аполипопротеин В-100 (Аро В-100) является главным белковым компонентом LDL и также присутствует в липопротеинах промежуточной плотности (IDL) и липопротеинах очень низкой плотности (VLDL). Таким образом, если в крови индуцируются антитела, узнающие аро В-100, будет легко происходить выведение LDL фагоцитами. В этой связи некоторые недавние исследования были сфокусированы на применении вакцин для снижения уровня плазматического LDL-холестерина и уменьшения случаев атеросклероза. Антитела, индуцированные с помощью такой антихолестериновой вакцинной терапии, относятся к IgM-типам, которые, как полагают, связываются с VLDL, IDL и LDL, такая стратегия предполагает возможность разработки вакцин для предупреждения и лечения гиперхолестеринемии и атеросклероза (Bailey et al., Cholesterol vaccines. Science 264, 1067-1068, 1994; Palinski W. et al., Proc Natl Acad Sci U.S.A. 92, 821-825, 1995; Wu R., de Faire U. et al., Hypertension. 33, 53-59, 1999). Также аполипопротеин В-100 представляет собой огромную белковую молекулу, которая включает 4560 аминокислотных остатков, содержит сигнальный пептид из 24 аминокислотных остатков и имеет молекулярную массу более чем 500 кДа (Elovson J. et al., Biochemistry, 24:1569-1578, 1985). Так как аполипопротеин В-100 секретируется в основном с помощью печени и представляет собой амфипатическую (гидрофильно-гидрофобную) молекулу, он может взаимодействовать с липидными компонентами плазматических липопротеинов и водным окружением (Segrest J.P. et al., Adv. Protein Chem., 45, 303-369, 1994). Аполипопротеин В-100 стабилизирует размер и структуру LDL-частиц и играет важнейшую роль в контроле гомеостаза плазматического LDL-холестерина через связывание с его рецептором (Brown M.S. et al., Science, 232, 34-47, 1986).
Корейская патентная публикация №2002-0018971, опубликованная для всеобщего ознакомления и зарегистрированная авторами настоящего изобретения, описывает пептид, миметирующий эпитоп аро В-100, обладающий эффектом против ожирения. Однако эта публикация только раскрывает тот факт, что миметирующий пептид В-клеточного эпитопа обладает эффектом против ожирения.
До настоящего изобретения в литературе отсутствовали сообщения об увеличении иммуногенности аполипопротеина с помощью слияния В-клеточного эпитопа аполипопротеина и Т-клеточного эпитопа, за исключением попытки повысить иммунные ответы с помощью применения белкового носителя или адъюванта.
Как описано в американском патенте U.S. Pat. №5843446, в котором гормон, высвобождающий лютеинизирующий гормон (LHRH), конъюгируют с другим белком для повышения иммуногенности LHRH, основная часть иммунных ответов направлена скорее на белок-переносчик, чем на LHRH, что приводит к иммунному подавлению, вызванному переносчиком. Таким образом, для выбора дополнительных материалов и определения соединительных структур и соединительных участков, способных повысить иммуногенность В-клеточного эпитопа, необходимы дальнейшие интенсивные усилия.
Было предпринято много попыток слияния гаптена с белком-переносчиком для повышения иммуногенности гаптена, но они не привели к получению стабильных повышающих эффектов. В частности, линейное слияние В-клеточного эпитопа и Т-клеточного эпитопа, как в настоящем изобретении, привело к потере иммуногенности в соответствии с ориентацией эпитопов, типом каждого эпитопа и т.п. (Francis M.J. et al., Nature 330, 168-170, 1987), а в присутствии линкера привело к пониженной иммуногенности (Partidos С.et al., Mol. Immunol. 29, 651-658, 1992). То есть не существует непротиворечивого правила, применимого к разработке пептидных вакцин, и эффективность разрабатываемых вакцин также непредсказуема. По указанным выше причинам, если сильно гидрофобный пептид PBl4, который является пептидом, миметирующим аро-В, сливают с Т-клеточным эпитопом, антигенный участок может быть помещен внутрь слитого белка, что приводит к уменьшению его способности индуцировать иммунные реакции.
На основании этого авторы настоящего изобретения предприняли различные попытки для повышения иммуногенности PBL4, который является миметическим пептидом В-клеточного эпитопа аполипопротеина В-100 и который обладает эффектом против ожирения. В результате гибридный полипептид, в котором N-концевая часть Т-хелперного эпитопа слита с С-концевой частью миметического пептида, продемонстрировал превосходный иммуноусиливающий эффект, указывающий на то, что полипептид эффективен для предупреждения или лечения ожирения. Это было неожиданным результатом, так как гибридные полипептиды демонстрируют прекрасную активность против ожирения без индукции иммунных ответов, которые нейтрализуют полезные активности или эффекты В-клеточного эпитопа аполипопротеина В-100, и не вызывают опасные побочные эффекты.
Раскрытие изобретения
В одном аспекте настоящее изобретение обеспечивает иммуногенный гибридный полипептид, который включает аминокислотную последовательность миметического пептида В-клеточного эпитопа аполипопротеина В-100 и в котором С-концевая часть миметического пептида слита с N-концевой частью Т-хелперного эпитопа.
В другом аспекте настоящее изобретение обеспечивает вакцину для предупреждения или лечения ожирения, которая включает иммуногенный гибридный полипептид, который включает аминокислотную последовательность миметического пептида В-клеточного эпитопа аполипопротеина В-100 и в котором С-концевая часть миметического пептида слита с N-концевой частью Т-хелперного эпитопа.
В другом аспекте настоящее изобретение обеспечивает рекомбинантный вектор, включающий ген, кодирующий иммуногенный гибридный полипептид, трансформант, включающий рекомбинантный вектор и способ получения гибридного полипептида с помощью культивирования клеток-хозяев, трансформированных рекомбинантным вектором.
Краткое описание фигур
Указанные выше другие объекты, детали и другие преимущества настоящего изобретения будут более ясно поняты из следующего детализированного описания, включающего фигуры [в обозначении продуктов прописная "р" относится к ДНК (плазмида), например pBl4Т - рекомбинантная плазмида, кодирующая пептид PBl4Т, где заглавная "Р" относится к пептиду], в которых:
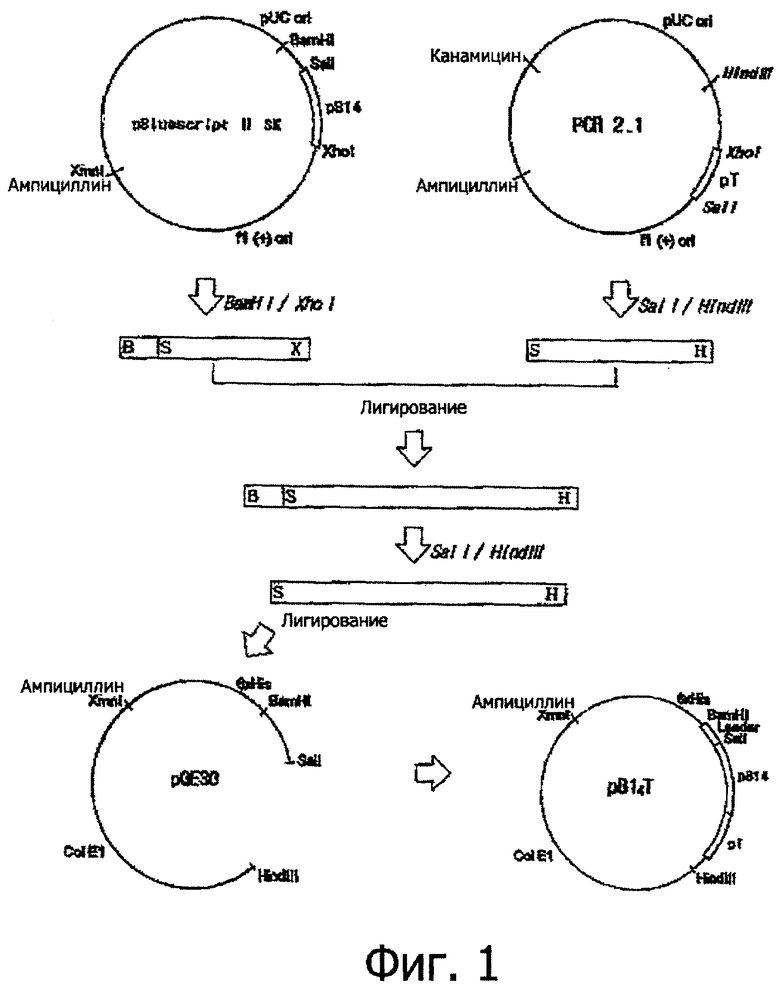
Фиг.1 демонстрирует способ конструирования pBl4Т;
Фиг.2 демонстрирует результаты расщепления PBl4Т с помощью рестриктаз;
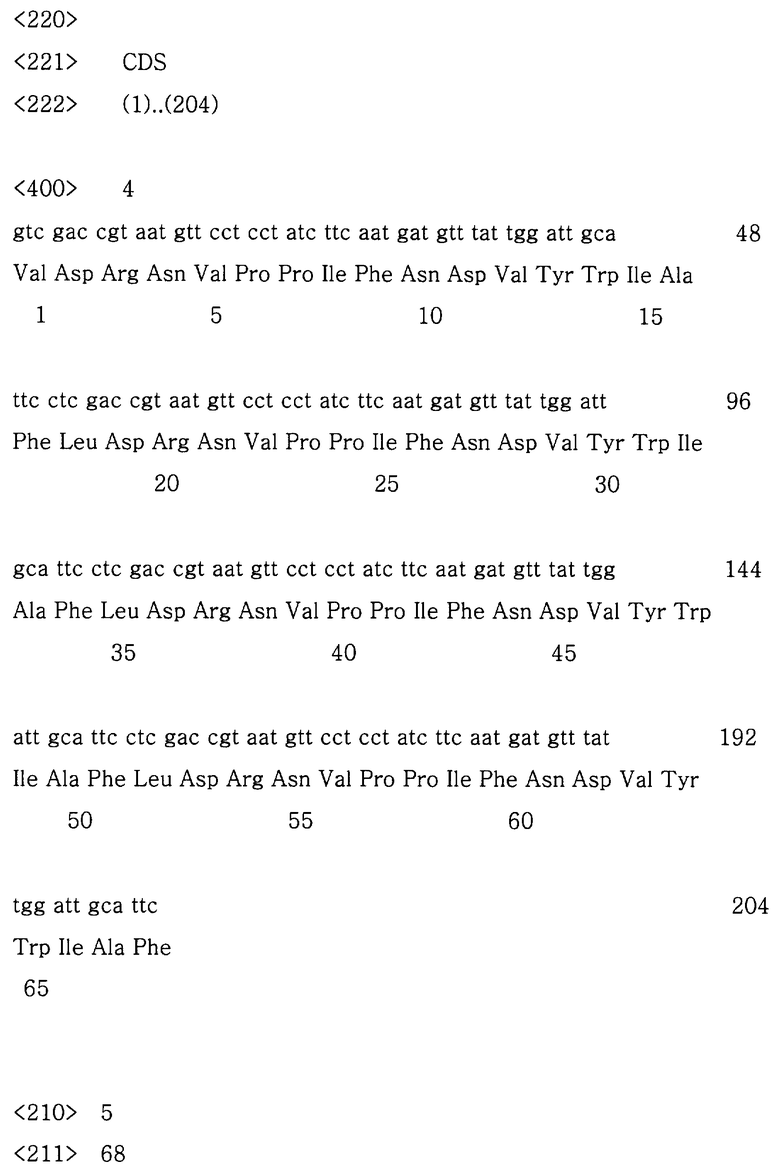
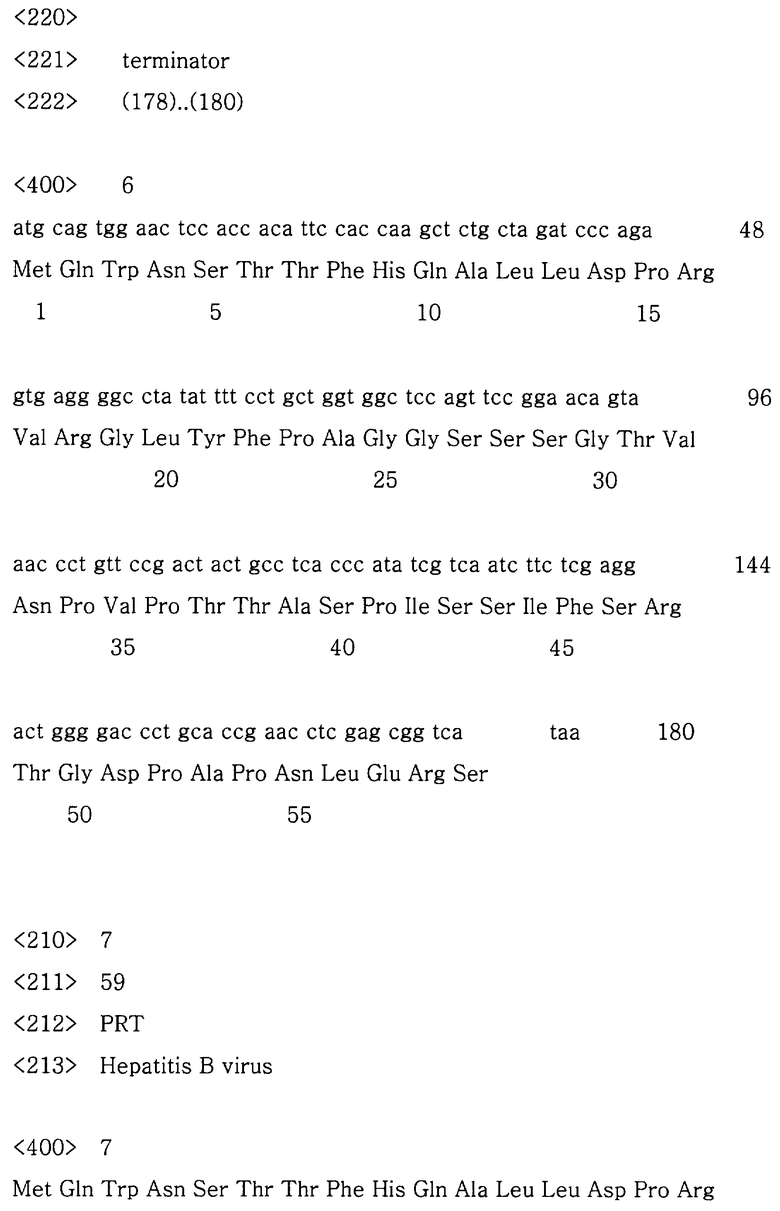
Фиг.3 демонстрирует последовательность ДНК PBl4Т и аминокислотную последовательность, предсказанную из нее;
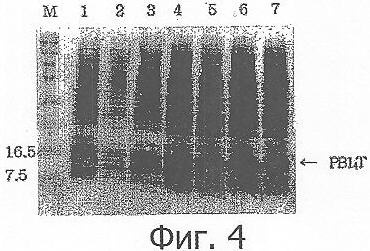
Фиг.4 демонстрирует результаты анализа SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия) для экспрессии PBl4T в трансформированной линии Escherichia coli M15/pBl4T, которая была обработана IPTG для индукции экспрессии PBl4Т, где экспрессированный рекомбинантный PBl4T указан стрелкой (М: предварительно окрашенный маркер молекулярной массы белков; дорожка 1: Е.coli M15, не индуцированная IPTG; и дорожки 3-7: IPTG-индуцированная Е.coli M15/pBl4T, собранная через 1, 2, 3, 4 и 5 ч, соответственно, после индукции IPTG);
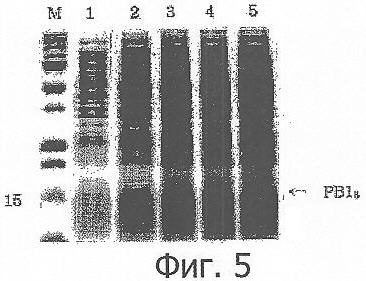
Фиг.5 демонстрирует результаты анализа SDS-PAGE для экспрессии PBl8 в трансформированной линии Escherichia coli M15/pBl8, которая была обработана IPTG для индукции экспрессии PBl8, где экспрессированный рекомбинантный PBl8 указан стрелкой (М: предварительно окрашенный маркер молекулярной массы белков; дорожка 1: Е.coli M15, не индуцированная IPTG; и дорожки 3-7: IPTG-индуцированная Е.coli M15/pBl8, собранная через 1, 2, 3, 4 и 5 ч, соответственно, после индукции IPTG);
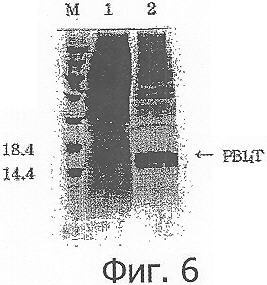
Фиг.6 демонстрирует результаты анализа SDS-PAGE супернатанта после центрифугирования (дорожка 1) и осадка (дорожка 2) лизата Е.coli, где экспрессированный PBl4Т указан стрелкой и обнаруживается в осадке;
Фиг.7 демонстрирует результаты анализа SDS-PAGE лизата Е.coli (дорожка 1: целый лизат; дорожка 2: супернатант после центрифугирования; дорожка 3: осадок после центрифугирования), где экспрессированный PBl8 указан стрелкой и обнаруживается в осадке;
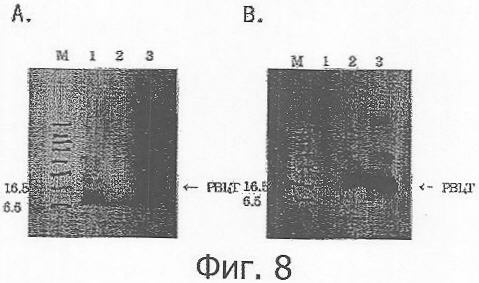
Фиг.8 демонстрирует результаты вестерн-блоттинга очищенного PBl4Т с кроличьим антителом к PBl4 (А) и моноклональным антителом к preS2 (В) (дорожка 1: Е.coli M15; дорожка 2: Е.coli M15/pBl4T, не индуцированная IPTG; дорожка 3: IPTG-индуцированная Е.coli M15/pBl4T, собранная через 3 ч после индукции IPTG);
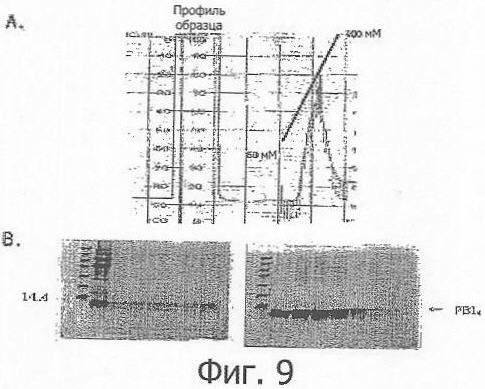
Фиг.9 демонстрирует профиль элюции PBl4, полученный аффинной хроматографией на колонке Ni-NTA с помощью линейного градиента имидазола;
Фиг.10 демонстрирует профиль элюции PBl4Т, полученный аффинной хроматографией на колонке Ni-NTA с помощью линейного градиента имидазола;
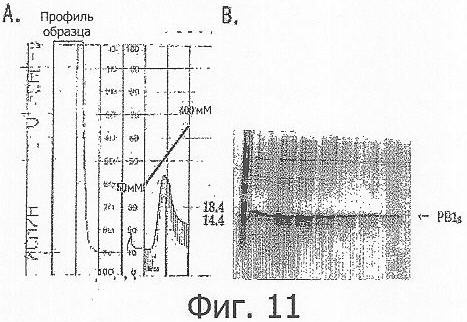
Фиг.11 демонстрирует профиль элюции PBl8, полученный аффинной хроматографией на колонке Ni-NTA с помощью линейного градиента имидазола;
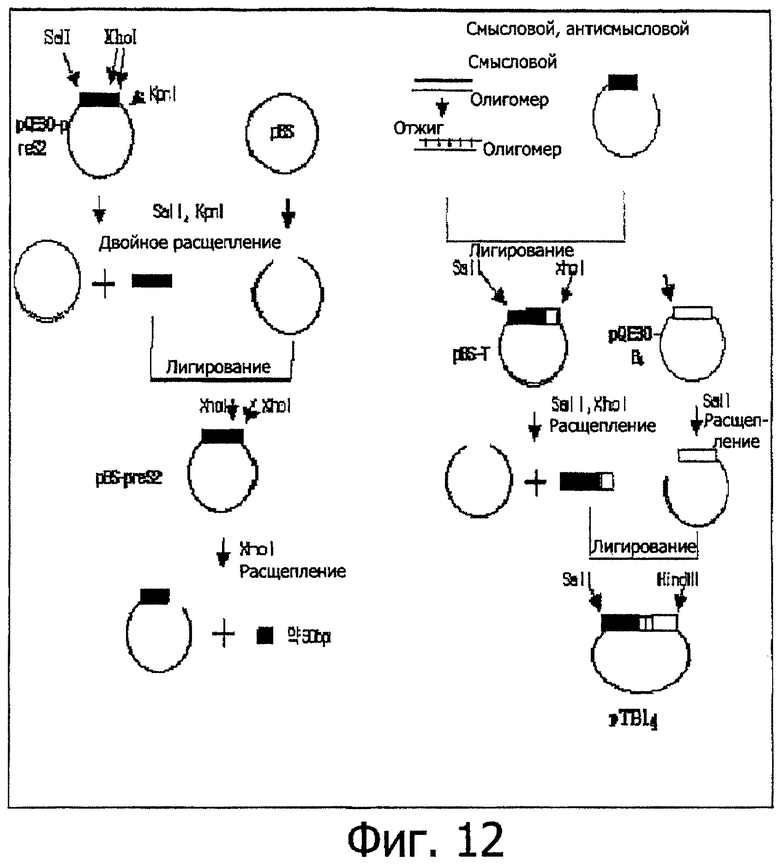
Фиг.12 демонстрирует способ конструирования pTBl4;
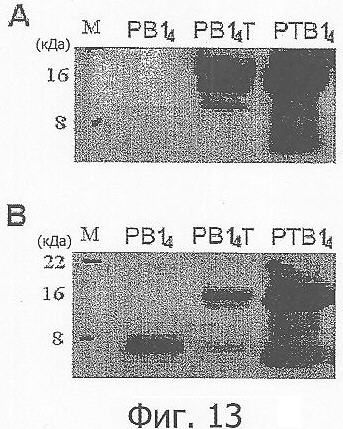
Фиг.13 демонстрирует результаты вестерн-блоттинга очищенного PBl4, PBl4Т и PTBl4 с мышиным моноклональным антителом к preS2 и козьим антителом к мышиным IgG, конъюгированным с пероксидазой хрена (А) и с антисывороткой к PBl4 и козьим антителом к кроличьим IgG, конъюгированным с пероксидазой хрена (В);
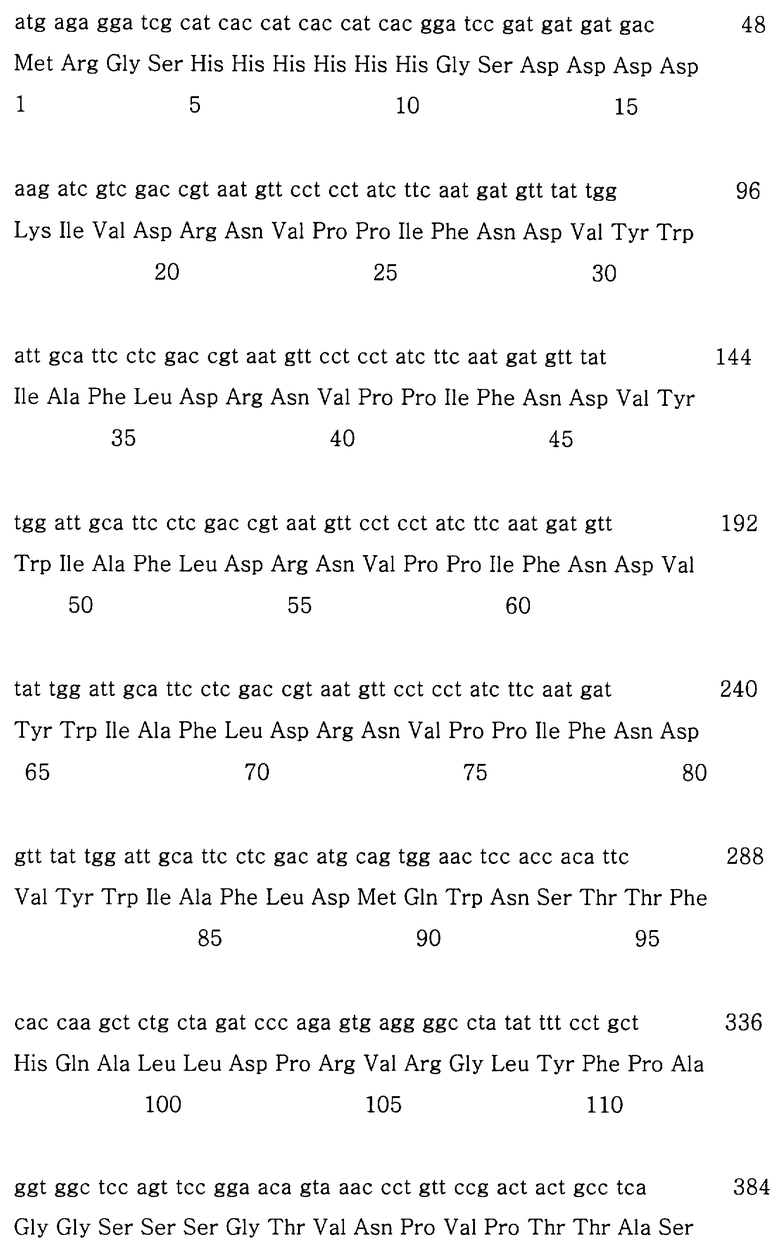
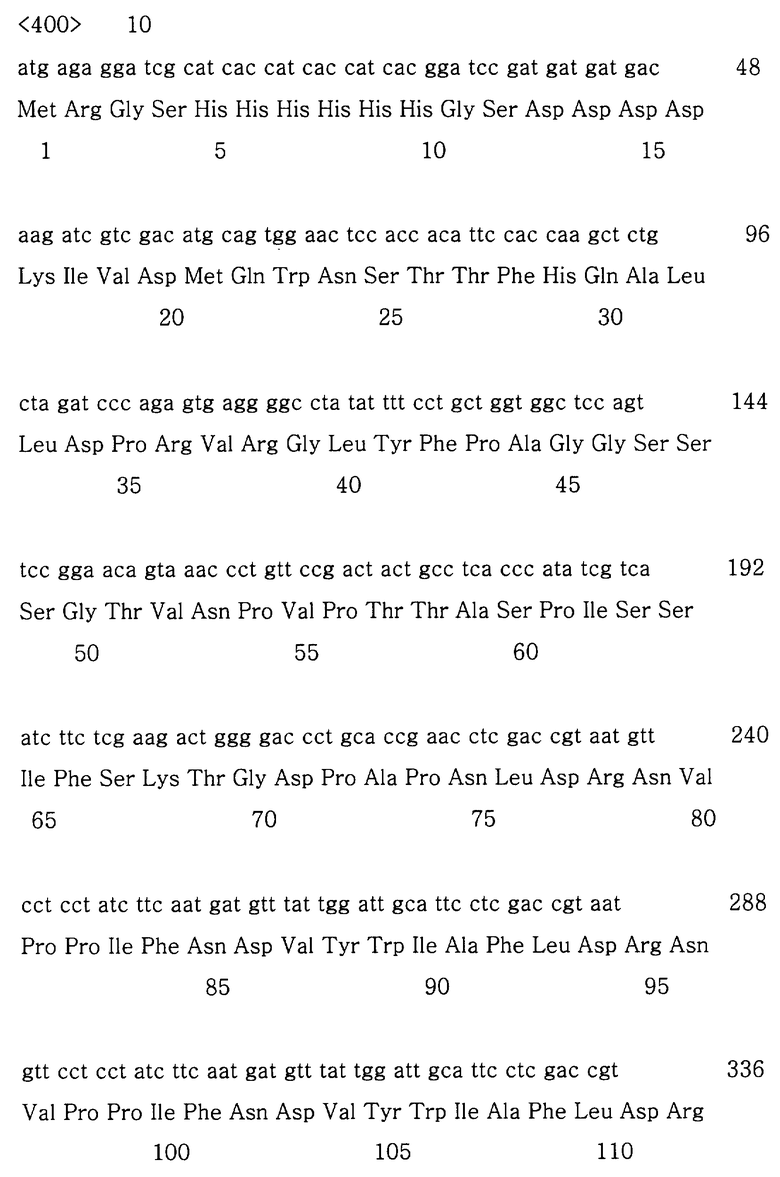
Фиг.14 демонстрирует последовательность ДНК TBl4/pQE30 и аминокислотную последовательность, предсказанную из нее;
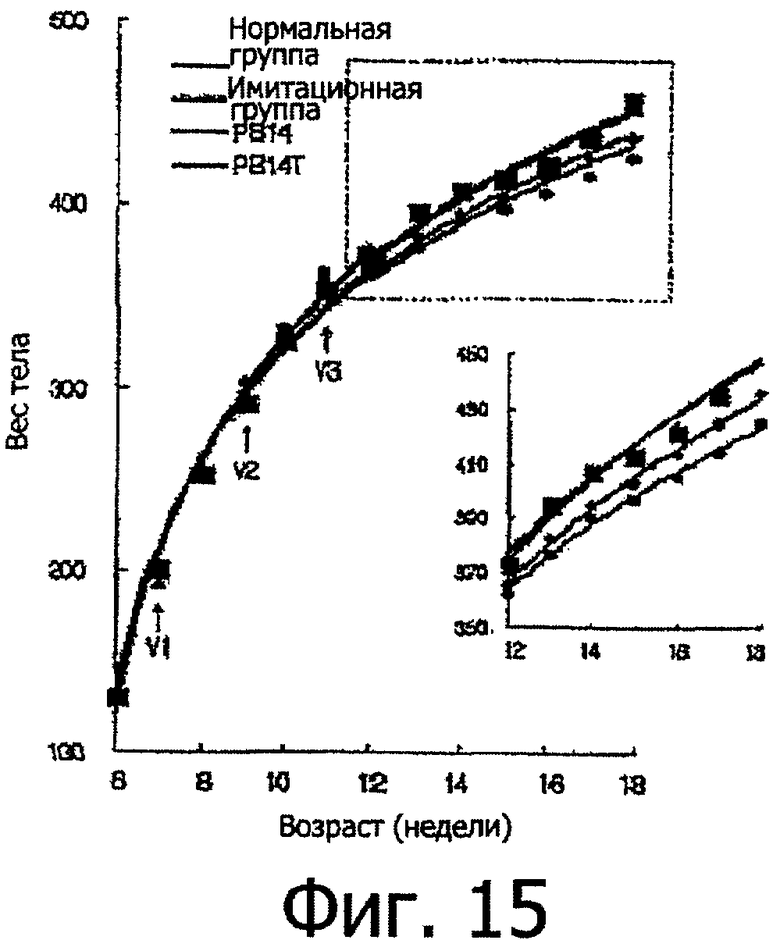
Фиг.15 представляет собой график, показывающий прирост веса тела белых крыс линии Sprague Dawley (SD) в нормальной, имитирующей и вакцинированной группах, в которых нормальной группе  вводили PBS, имитирующей группе
вводили PBS, имитирующей группе  вводили овальбумин, вакцинированной группе
вводили овальбумин, вакцинированной группе  вводили PBl4, конъюгированный с овальбумином (PBl4+OVA); и в другой вакцинированной группе
вводили PBl4, конъюгированный с овальбумином (PBl4+OVA); и в другой вакцинированной группе  которой вводили пептид PBl4T; каждый пептид вводили три раза с двухнедельными перерывами; стрелки указывают временные точки, когда проводили вакцинацию;
которой вводили пептид PBl4T; каждый пептид вводили три раза с двухнедельными перерывами; стрелки указывают временные точки, когда проводили вакцинацию;
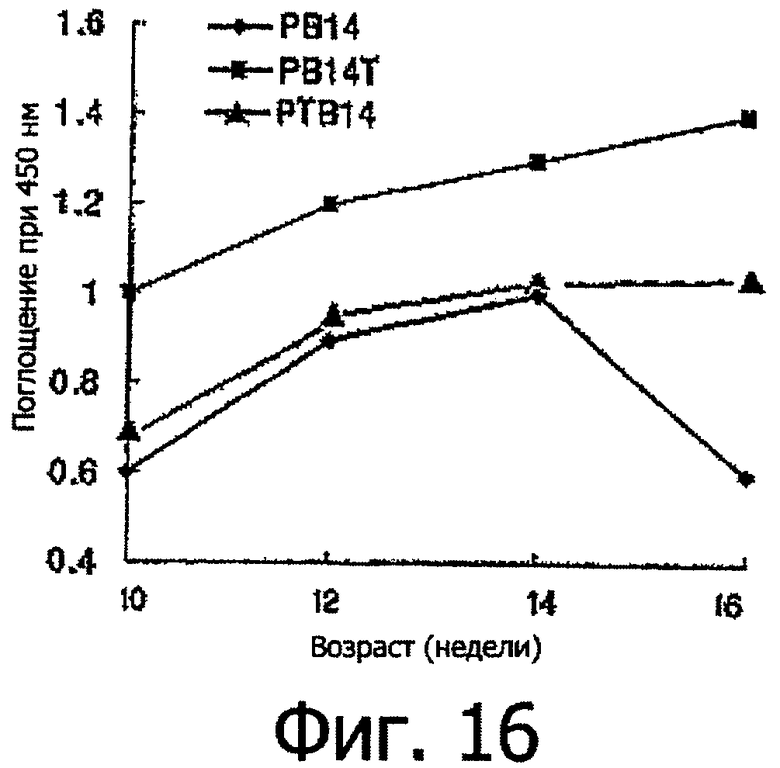
Фиг.16 представляет собой график, показывающий изменения титра антител к РВ1, индуцированные иммунизацией PBl4, PBl4Т и PTBl4, соответственно; и
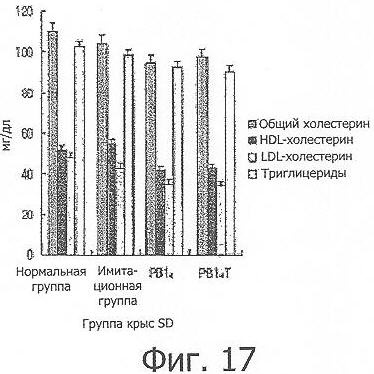
Фиг.17 представляет собой график, показывающий уровень триглицеридов, HDL, LDL и общего холестерина в сыворотке.
Осуществление изобретения
В одном аспекте настоящее изобретение имеет отношение к иммуногенному гибридному полипептиду, который включает аминокислотную последовательность миметического пептида В-клеточного эпитопа аполипопротеина В-100 и в котором С-концевая часть миметического пептида слита с N-концевой частью Т-хелперного эпитопа.
В стратегии повышения иммуногенности аполипопротеина настоящее изобретение планирует обеспечить иммуногенный гибридный полипептид, в котором Т-клеточный эпитоп слит с миметическим пептидом В-клеточного эпитопа аполипопротеина, в особенности аполипопротеина В-100 (аро В-100). Когда Т-клеточный эпитоп соединен с миметическим пептидом В-клеточного эпитопа аро В-100, PBl4 обладал улучшенной способностью индуцировать иммунные ответы и демонстрировал вакцинную эффективность более продолжительный период времени и, таким образом, обладал улучшенным эффектом, направленным против ожирения.
Термин "миметический пептид эпитопа" так, как он применяется в тексте, имеет отношение к пептиду, который имитирует минимальную часть эпитопа, представляющего собой эпитоп, который в достаточной степени сходен с нативным эпитопом, так что он может быть узнаваемым антителом, специфичным к нативному эпитопу, или который способен увеличить связь антитела с нативным эпитопом. Миметический пептид также называют мимотопом. Такой миметический пептид является полезным, так как он узнаваем как "чужой" in vivo и, таким образом, преодолевается проблема самотолерантности иммунных ответов. Миметический пептид В-клеточного эпитопа аро В-100 узнается антителом, специфически связывающимся с аро В-100. Антитело, специфически связывающееся с аро В-100, включает поликлональные и моноклональные антитела, которые специфически узнают и связывают аро В-100 и его фрагменты, например Fc, Fab и F(ab′)2.
Миметический пептид В-клеточного эпитопа аро В-100 в соответствии с настоящим изобретением включает аминокислотную последовательность, выбранную из SEQ Nos. 1, 2 и 3. Таким образом, в предпочтительном аспекте настоящее изобретение имеет отношение к иммуногенному гибридному полипептиду, который включает аминокислотную последовательность, выбранную из SEQ ID Nos.1, 2 и 3, и в котором С-концевая часть пептида, узнаваемая антителом, специфически связывающимся с аро В-100, слита с N-концевой частью Т-хелперного эпитопа.
Авторы настоящего изобретения получили миметические пептиды (SEQ ID Nos.1, 2 и 3), которые узнаются моноклональным антителом к аро В-100, Mab B9 или Mab B23, из библиотеки фагового отображения пептидов с помощью биопэннинга указанной библиотеки.
Миметический пептид эпитопа аро В-100, который включает аминокислотную последовательность, выбранную из SEQ ID Nos.1, 2 и 3, может существовать в мономерной форме, которая состоит из единственной копии аминокислотной последовательности, имеющей любой единственный из номеров SEQ ID, или для дальнейшего повышения иммуногенности миметического пептида может быть в мультимерной форме, в которой две или более, предпочтительно от трех до восьми и более предпочтительно от трех до шести, копии аминокислотных последовательностей, имеющих любой отдельный номер из номеров SEQ ID, соединенных между собой. Наиболее предпочтительным является тетрамер (SEQ ID No.4), в котором 4 копии соединены между собой. Если миметический пептид находится в мультимерной форме, аминокислотные последовательности каждой копии, содержащей мономер, могут ковалентно сшиваться непосредственно или с помощью линкера. Если аминокислотные последовательности сшиваются через линкер, линкер может состоять из одного-пяти аминокислотных остатков, которые выбирают из, например, глицина, аланина, валина, лейцина, изолейцина, пролина, серина, треонина, аспарагина, аспарагиновой кислоты, цистеина, глутамина, глутаминовой кислоты, лизина и аргинина. Предпочтительные аминокислоты, полезные в линкере, могут включать валин, лейцин, аспарагиновую кислоту, глицин, аланин и пролин. Более предпочтительно, принимая во внимание простоту генной манипуляции, две аминокислоты, выбранные из валина, лейцина, аспарагиновой кислоты и т.п., могут быть соединены и использованы в качестве линкера. Предпочтительный миметический пептид получают с помощью соединения через линкер двух или нескольких копий аминокислотных последовательностей, выбранных из SEQ ID Nos.1, 2 и 3.
Термин "Т-клеточный эпитоп" так, как он применяется в тексте, имеет отношение к аминокислотной последовательности, которая способна с достаточной эффективностью связывать молекулы МНС класса II и стимулировать Т-клетки или которая способна связываться с Т-клетками в комплексе с МНС класса II. В этом случае Т-клеточный эпитоп узнается специфическим рецептором, присутствующим на Т-клетках, и функционирует для обеспечения сигнала, необходимого для дифференцировки В-клеток в клетки, продуцирующие антитела, и индуцирует цитотоксичные Т-лимфоциты (CTL) для разрушения клеток-мишеней. Т-клеточный эпитоп специальным образом не ограничен до тех пор, пока он стимулирует Т-клетки и усиливает иммунные реакции; и имеется в распоряжении множества белков, пептидов и т.п., подходящих для этой цели. Что касается объектов настоящего изобретения, Т-клеточный эпитоп предпочтительно является Т-хелперным эпитопом. Примеры Т-хелперного эпитопа могут включать Т-хелперные эпитопы поверхностного антигена гепатита В, Т-хелперные эпитопы главного белка внешней мембраны Chlamydia trachomitis, Т-хелперные эпитопы Plasmodium falciparum circumsporozoite, Т-хелперные эпитопы TraT Escherichia coli, T-хелперные эпитопы столбнячного токсоида, Т-хелперные эпитопы дифтерийного токсоида, Т-хелперные эпитопы триозофосфатизомеразы Schistosoma mansoni, T-хелперные эпитопы F-белка вируса кори, последовательности Т-хелперных эпитопов, происходящие из коклюшных вакцин, BCG (Бацилла Кальметта-Герена), полиомиелитных вакцин, вакцин против свинки, краснушных вакцин, вакцин против бешенства, очищенных производных белка туберкулина, гемоцианина моллюска фиссуреллии (keyhole limpet hemocyanin) и их фрагменты или комбинации. Т-клеточный эпитоп может включать вставку, делецию или замещение выбранного аминокислотного остатка в соответствии со специфической целью и может предоставляться в мультимерной форме, в которой соединены два или более различных Т-клеточных эпитопов. В одном воплощении настоящего изобретения применяется поверхностный антиген гепатита В. Геном вируса гепатита В (HBV) имеет размер 3,2 т.п.н., содержит информацию для четырех важных белков и содержит четыре открытые рамки считывания, ген S (антигенный поверхностный белок), ген С (коровый белок), ген Р (ДНК полимераза) и ген X. Ген S разделен на S-участок, кодирующий HBsAg, и участок preS. Участок preS разделен на preS1, кодирующий 108 или 119 аминокислот в зависимости от штаммов HBV, и preS2 (Т-кассета), кодирующий 55 аминокислот независимо от подтипа. Белок HBV preS2 активирует Т-хелперы во время иммунных реакций, стимулируя, таким образом, образование антител против HBV.
Термин "гибридный полипептид" так, как он применяется в тексте, в основном означает пептид, в котором соединены гетерогенные пептиды различного происхождения, и в настоящем изобретении относится к пептиду, в котором соединены В-клеточный эпитоп и Т-клеточный эпитоп. Этот гибридный полипептид можно получить с помощью химического синтеза или с помощью экспрессии и очистки с применением генетической рекомбинации после того, как определен каждый участник. Предпочтительно гибридный ген, в котором генная последовательность, кодирующая В-клеточный эпитоп, присоединена к другой генной последовательности, кодирующей Т-клеточный эпитоп, экспрессируют в клеточной экспрессионной системе. В таком гибридном полипептиде В-клеточный эпитоп и Т-клеточный эпитоп могут быть соединены между собой непосредственно или с помощью соединительного элемента, такого как линкер. При использовании линкера он не должен отрицательно влиять на индукцию иммунных реакций гибридным полипептидом.
Термин "полипептид" так, как он применяется в тексте, является термином, включающим полноразмерную аминокислотную цепь, в которой остатки, включающие две или более аминокислот, соединены с помощью ковалентных пептидных связей и включают дипептиды, трипептиды, олигопептиды и полипептиды. В частности, в настоящем изобретении термин "полипептид" означает гибридный полипептид, в котором соединены два или более пептида, в составе которых несколько или несколько десятков аминокислот ковалентно связаны между собой. Гибридный полипептид настоящего изобретения является полипептидом, в котором соединены два или более пептида, например В-клеточный эпитоп и Т-клеточный эпитоп. Каждая последовательность пептида, составляющего полипептид, включает последовательность, соответствующую указанному выше эпитопу, и может, кроме того, включать последовательность, расположенную вблизи эпитопа. Эти пептиды могут быть сделаны из L- или D-аминокислот или могут представлять собой комбинацию аминокислот в двух различных конфигурациях. Гибридный полипептид настоящего изобретения может полностью состоять из антигенного участка, включающего указанные выше В-клеточный эпитоп, Т-клеточный эпитоп и некоторую последовательность, расположенную вблизи этих эпитопов, и может, кроме того, включать дополнительную последовательность. Однако эта дополнительная последовательность предпочтительно не должна понижать общую иммуногенность. Примером такой дополнительной последовательности может служить линкерная последовательность.
Термин "иммуногенность" так, как он применяется в тексте, относится к способности индуцировать как клеточные, так и гуморальные иммунные реакции для защиты организма против загрязнений (impurities). Вещество, вызывающее такие иммунные реакции, называют иммуногеном. В настоящем изобретении применяют полипептид, имеющий как В-клеточный эпитоп, так и Т-клеточный эпитоп, которые являются иммуногенными веществами.
Авторы настоящего изобретения соединили С-концевую часть PBl4, который представляет собой тетрамерный миметический пептид аро В-100, являющегося функциональным пептидом против ожирения и имеющего в своем составе В-клеточный эпитоп, но дефицитного по Т-клеточному эпитопу, с частью (Т-фрагментом) HBV preS2, имеющей Т-клеточный эпитоп, создав, таким образом, генный фрагмент для экспрессии PBl4Т (Фиг.1). Фрагмент PBl4 получали, используя рестриктазы BamHI и XhoI, а Т-фрагмент получали, используя рестриктазы SalI и Hind III. Фрагмент гена PBl4Т вставляли в вектор pQЕ30 и трансформировали в Е.coli JM109. Появившуюся колонию анализировали с помощью рестрикционного картирования (Фиг.2) и секвенирования ДНК (Фиг.3), и было обнаружено, что она является правильным клоном, в котором В-клеточный эпитоп соединен с Т-клеточным эпитопом. Этот клон обозначили как "pBl4T". Вектор pQE30, применяемый для экспрессии PBl4Т и PBl8, инициирует экспрессию белка от внутреннего стартового кодона, содержащего 6 гистидиновых остатков для удобства при очистке белка, и затем энтерокиназный участок расщепления. Таким образом, экспрессированный PBl4Т имеет молекулярную массу 16,2 кДа, a PBl8 - 16,5 кДа. Белковую экспрессию изучали с помощью электрофоретического анализа SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия) образцов, отобранных в определенные промежутки времени (Фиг.4 и 5).
Таким образом, фактически в настоящем изобретении может быть обеспечен иммуногенный гибридный полипептид с SEQ ID No.9, в котором тетрамерный миметический пептид аро В-100 соединен с поверхностным антигеном HBV preS2.
Иммуногенный полипептид настоящего изобретения может быть получен с помощью химического синтеза или генетической рекомбинации. Предпочтительно гибридный полипептид настоящего изобретения может быть получен с помощью трансформации клеток-хозяев рекомбинантным вектором и выделения и очистки полипептида, экспрессированного в клетке-хозяине.
Таким образом, в другом аспекте настоящее изобретение обеспечивает рекомбинантный вектор, включающий ген, кодирующий иммуногенный гибридный полипептид, и клетку-хозяина, трансформированную рекомбинантным вектором.
В еще одном аспекте настоящее изобретение обеспечивает способ получения иммуногенного гибридного полипептида с помощью культивирования клетки-хозяина, трансформированного рекомбинантным вектором.
Способ получения иммуногенного гибридного полипептида настоящего изобретения с помощью генетической рекомбинации включает следующие четыре стадии.
Первая стадия предназначена для введения гена, кодирующего гибридный полипептид, в вектор для конструирования рекомбинантного вектора. Вектор, в который вставляют чужеродную ДНК, может быть плазмидой, вирусом, космидой и т.п. Рекомбинантный вектор включает клонирующий вектор и экспрессионный вектор. Клонирующий вектор содержит точку начала репликации, например точку начала репликации плазмиды, фага или космиды, и является "репликоном", который реплицирует экзогенный фрагмент ДНК, присоединенный к вектору. Экспрессионный вектор был разработан для применения в белковом синтезе. Рекомбинантный вектор служит носителем фрагмента чужеродной ДНК, вставленной в него, который обычно означает двуспиральный фрагмент ДНК. Термин "чужеродная ДНК" так, как применяется в тексте, относится к ДНК, происходящей из разных видов, или в значительной степени модифицированной форме нативной ДНК из однородных видов. Также чужеродная ДНК включает немодифицированную последовательность ДНК, которая не экспрессируется в клетках в нормальных условиях. В этом случае чужеродный ген является специфической нуклеиновой кислотой, мишенью для транскрипции, которая кодирует полипептид. Рекомбинантный вектор содержит ген-мишень, который оперативно соединен с транскрипционными и трансляционными экспрессионными регуляторными последовательностями, которые проявляют свои функции в клетках выбранного "хозяина", для того чтобы повысить уровень экспрессии трансфицированного гена в клетке-хозяине. Рекомбинантный вектор представляет собой генетическую конструкцию, которая содержит необходимые регуляторные элементы, к которым оперативно присоединяется вставляемый ген для экспрессирования в клетках организма. Такую генетическую конструкцию получают с применением стандартных методов рекомбинантных ДНК. Тип рекомбинантного вектора специально не ограничен, до тех пор, пока этот вектор экспрессирует ген-мишень во множестве клеток-хозяев, включающих прокариоты и эукариоты, и функционирует для продуцирования белка-мишени. Однако предпочтительным является вектор, который способен крупномасштабно продуцировать чужеродный белок в форме, похожей на нативную форму, в то же время имеющий в своем составе сильный промотор для достижения усиленной экспрессии белка-мишени. Рекомбинантный вектор предпочтительно содержит, по меньшей мере, промотор, стартовый кодон, ген, кодирующий белок-мишень, стоп-кодон и терминирующий кодон. Рекомбинантный вектор, кроме того, может подходящим образом содержать ДНК, кодирующую сигнальный пептид, энхансерную последовательность, 5′- и 3′-нетранслируемый участок гена-мишени, область селективного маркера, репликационную единицу и т.п.
Вторая стадия предназначена для трансформации клетки-хозяина рекомбинантным вектором и культивирование клетки-хозяина. Рекомбинантный вектор вводят в клетку-хозяина для создания трансформанта с помощью метода, описанного Sambrook, et al., Molecular Cloning, A Laboratory Manual (2nd Ed.), Cold Spring Harbor Laboratory, 1. 74, 1989, метода с применением фосфата кальция или хлорида кальция/хлорида рубидия, электропорации, электроинъекции, химической обработки, например обработки PEG и баллистической трансфекции ("генной пушки", gene gun). Полезный белок можно получить и выделить в крупном масштабе с помощью культивирования трансформанта, экспрессирующего рекомбинантный вектор в питательной среде. В зависимости от типа клеток-хозяев обычную среду и условия культивирования можно выбирать правильным образом. Условия культивирования, включая температуру, рН среды и время культивирования необходимо поддерживать подходящими для роста клеток и продуцирования интересующего белка образом. Клетки-хозяева, которые могут быть трансформированы с помощью рекомбинантного вектора в соответствии с настоящим изобретением, включают как прокариоты, так и эукариоты. Обычно можно применять клетки-хозяева, имеющие высокую эффективность для введения ДНК и обладающие высоким уровнем экспрессии вводимой ДНК. Примеры клеток-хозяев включают известные прокариотические и эукариотические клетки, например Escherichia sp., Pseudomonas sp., Bacillus sp., Streptomyces sp., грибы и дрожжи, клетки насекомых, такие как Spodoptera frugiperda (Sf9), и клетки животных, такие как СНО, COS 1, COS 7, BSC 1, BSC 40 и ВМТ 10. Предпочтительно можно применять Е.coli.
Третья стадия предназначена для индукции гибридного полипептида для экспрессии и аккумуляции. В настоящем изобретении в качестве индуктора применяли IPTG для индукции экспрессии белка и регулировали время индукции таким образом, чтобы получить максимальный выход белка.
Заключительная стадия предназначена для выделения и очистки гибридного полипептида. Обычно белок, продуцируемый с помощью рекомбинации, можно получить из среды или лизата клеток. Если пептид является мембранно-связанной формой, его можно освободить из мембраны, используя подходящий поверхностно-активный раствор (например, Тритон Х-100) или с помощью ферментативного расщепления. Клетки, применяемые для экспрессии гибридного пептида, могут быть разрушены с помощью множества физических или химических способов, таких как повторное замораживание и оттаивание, обработка ультразвуком, механическое разрушение или с помощью соединения, разрушающего клетки; и гибридный полипептид можно выделить и очистить с помощью обычно применяемых методов биохимического выделения (Sambrook et al., Molecular Cloning: A laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press, 1989; Deuscher, M., Guide to Protein Purification Methods Enzymology, Vol.182. Academic Press. Inc., San Diego, CA, 1990). Неограниченные примеры методов биохимического выделения, включающие электрофорез, центрифугирование, гель-фильтрацию, осаждение, диализ, хроматографию (ионообменную хроматографию, аффинную хроматографию, иммуносорбентную хроматографию, обратнофазовую ЖХВД, гель-фильтрацию при высоком давлении ЖХВД), изоэлектрическое фокусирование и вариации и комбинации этих методов.
Более подробно, в настоящем изобретении генный фрагмент PBl4T лигировали с вектором рQЕ30 и трансформировали в Е.coli. Вектор рQЕ30 применяли для суперпродуцирования белков в Е.coli, так как он содержит промоторный элемент, состоящий из промотора фага Т5 и lac- оперонной системы, использующий IPTG в качестве индуктора. Экспрессию PBl4Т подтверждали с помощью вестерн-блоттинга, в котором в качестве первичных антител использовали два антитела, узнающие PBl4Т: кроличье поликлональное антитело к РВ14 и мышиное моноклональное антитело к preS2, и экспрессированные белки затем очищали. PBl4 и PBl4Т денатурировали 8М мочевиной, так как они нерастворимы, и очищали с помощью аффинной хроматографии с использованием колонки Ni-NTA, применяемой для белков, содержащих концевую гистидиновую метку.
Крыс иммунизировали экспрессированным и очищенным полипептидом и оценивали прирост веса тела крыс, титры сывороточных антител и изменения липидного профиля в сыворотке крови. В результате по сравнению с нормальной группой или группой, вакцинированной неслитым миметическим пептидом, группа, вакцинированная гибридным полипептидом, продемонстрировала пониженный привес тела, высокие титры и устойчивую способность сохранять антитела к миметическому пептиду и пониженный уровень TG и LDL-холестерина.
Не существует постоянного правила, пригодного для разработки пептидной вакцины, и эффективность сконструированных вакцин также непредсказуема. По этим же причинам, если сильно гидрофобный пептид PBl4 сливают с Т-клеточным эпитопом, который является гетерогенным пептидом, антигенная область может оказаться внутри слитого белка, что приводит к снижению его способности индуцировать иммунные реакции. В этой сложной ситуации, чтобы проследить результаты слияния, авторы настоящего изобретения сконструировали гибридный полипептид, в котором миметический пептид эпитопа В-100 соединен с Т-клеточным эпитопом, и продемонстрировали, что гибридный полипептид обладал повышенной иммуногенностью, что приводило к повышенному эффекту против ожирения.
Иммуногенность искусственно синтезированного гибридного полипептида и вакцины, включающей его, достигается в том случае, если В-клеточный эпитоп и Т-хелперный эпитоп присутствуют одновременно. Также эффективность вакцины можно определить в соответствии с ориентацией В-клеточного эпитопа и Т-хелперного эпитопа. То есть способность гибридного полипептида индуцировать иммунные реакции может различаться в зависимости от того, расположен Т-хелперный эпитоп в N-концевой части или в С-концевой части В-клеточного эпитопа (Partidos, С, Stanley, С, and Steward, M, The effect of orientation of epitope on the immunogenicity of chimeric synthetic peptides representing measles virus protein sequences. Molecular Immunology, 29 (5), 651-658, 1992).
Чтобы исследовать эффект ориентации В-клеточного эпитопа и Т-хелперного эпитопа на индукцию иммунных реакций, авторы настоящего изобретения получили фрагмент гена TBl4 с помощью присоединения N-концевой части PBl4 к Т-фрагменту (Фиг.12), отличающемуся от фрагмента гена Bl4Т, вовлеченного в связывание С-концевой части PBl4 с Т-фрагментом. Более подробно, вектор pTBl4 был сконструирован в соответствии с методом, описанным в Примере 9, трансформирован в Е.coli M15 и экспрессирован в ней. Экспрессированный гибридный полипептид PTBl4, который имел концевую гистидиновую метку, был очищен с помощью аффинной хроматографии с применением His-связывающей смолы Ni-NTA.
Чтобы сравнить PTBl4 и PBl4Т по их способности индуцировать иммунные реакции и иммуногенность, крыс линии Sprague Dawley (SD) иммунизировали каждым полипептидом и собирали образцы крови. По сравнению с PBl4 PTBl4 обладал повышенной способностью индуцировать иммунные реакции и период сохранения сывороточного антитела к PTBl4 был более продолжительным. Однако было обнаружено, что эти усовершенствования по иммунизации PTBl4 были на 50-60% менее эффективны, чем для PBl4Т-полипептида (Фиг.16). Такие же результаты были обнаружены для супрессии прироста веса тела крыс (Таблица 2). Эти результаты указывают на то, что полипептид PBl4Т, полученный соединением С-концевой части PBl4 с Т-фрагментом, обладает более сильной иммуногенностью и эффектами против ожирения.
Таким образом, еще в одном аспекте настоящее изобретение имеет отношение к вакцине, направленной на предупреждение или лечение ожирения, включающей иммуногенный гибридный полипептид, который включает аминокислотную последовательность миметического пептида эпитопа аро В-100 и в котором С-концевая часть миметического пептида слита с N-концевой частью Т-хелперного эпитопа.
Можно определить, что иммуноген полезен в качестве вакцины, обладающей хорошей эффективностью, с помощью сравнения уровня ответов на иммуноген и соотношения наблюдаемых индивидуумов. В настоящем изобретении относительно настоящего объекта для того, чтобы обеспечить вакцину для предупреждения и лечения ожирения, оценивали эффект антигена на индукцию иммунных реакций с помощью исследования (а) увеличения веса тела, (б) титров сывороточных антител и (в) изменений липидного профиля в сыворотке крови, определяя таким образом высоко эффективную форму антигена.
Подробнее, 100 мкг каждого из очищенных пептидов PBl4 и PBl4Т вводили внутрибрюшинно 7-недельным белым крысам SD три раза с 2-недельными перерывами, наблюдали изменения веса тела крыс и полученные величины откладывали на графике (Фиг.15). От первой инъекции до повторной иммунизации (вторая инъекция) крысы из каждой группы демонстрировали похожий вес тела, который находился в диапазоне от 292 г до 297 г. Однако через одну неделю после вторичной инъекции наблюдали различие веса тела крыс между вакцинируемыми группами и нормальной и имитационной группами. Это указывает на то, что слабые иммунные реакции, индуцированные первичной инъекцией, усиливались после повторной иммунизации с помощью второй инъекции и что усиленные иммунные реакции приводили к уменьшению прироста веса тела крыс. По сравнению с нормальной и имитационной группами вакцинированные группы демонстрировали снижение прироста веса тела. Также пептид PBl4Т обладал более выраженным ингибирующим эффектом на прирост веса тела по сравнению с пептидом PBl4 (Таблица 2). Это различие в приросте веса тела сохранялось даже после третьей инъекции. Кроме того, было обнаружено, что химерный антиген PBl4, который был гомогенным, более эффективно индуцировал иммунные реакции по сравнению с пептидом PBl4, конъюгированным с белком-носителем, овальбумином. У вакцинированных белых крыс SD титры сывороточных антител измеряли в возрасте 10, 12, 14 и 16 недель с помощью метода ELISA (Фиг.16). PBl4Т-иммунизированная группа демонстрировала повышенные титры антител по сравнению с PBl4-иммунизированной группой. В возрасте 14 недель PBl4Т-иммунизированная группа демонстрировала оптическое поглощение (О.D.: оптическая плотность), в 1,5 раза превышающее значение для PBl4-иммунизированной группы. В возрасте 16 недель PBl4-иммунизированная группа демонстрировала снижение титра антител, тогда как PBl4Т-иммунизированная группа сохраняла повышенные титры антител. Что касается липидов сыворотки крови, вакцинированные группы демонстрировали низкие уровни TG и холестерина по сравнению с нормальной и имитационной группами. В частности, уровень LDL-холестерина был снижен до 60% по сравнению с нормальным уровнем (Фиг.17).
Эти результаты демонстрируют, что форма PBl4, слитая с Т-клеточным эпитопом, обладает более высокой иммуногенностью, чем PBl4 сам по себе, который имеет в своем составе В-клеточный эпитоп, и, таким образом, может быть применена в эффективной вакцинной композиции.
Кроме того, авторы настоящего изобретения провели клиническое тестирование эффективности Bl4T на домашних собаках. Bl4Т смешивали с окисью алюминия и дважды вводили десяти домашним собакам с 2-недельными перерывами, и наблюдали за изменением веса тела. В результате у собак не было обнаружено прироста веса тела даже тогда, когда собаки питались без ограничения легкой пищей или находились на очень жирной диете (Таблица 4). Также, если образцы сыворотки крови отбирали у иммунизированных собак после вторичной инъекции и с помощью метода ELISA измеряли титры антител, было обнаружено высокое значение поглощения, даже если образцы сыворотки были разведены в 5000-50000 раз, что указывает на то, что пептид Bl4T обладает превосходным эффектом на индукцию иммунных реакций.
Вакцина против ожирения настоящего изобретения составлена из антигена, фармацевтически приемлемого носителя, подходящего адъюванта и других общепринятых материалов и вводится в иммунологически эффективном количестве. Термин "иммунологически эффективное количество" так, как применяется в этом тексте, относится к количеству, которое достаточно для того, чтобы вызвать терапевтический или превентивный эффект, направленный на ожирение, и не вызвать побочные эффекты или тяжелые или избыточные иммунные реакции. Точную дозировку для введения можно варьировать в зависимости от специфического иммуногена, и она может быть определена специалистами в этой области техники с помощью известного метода, анализирующего развитие иммунных реакций. Также дозировка может зависеть от форм и способов введения, возраста реципиентов, состояния здоровья и веса тела, свойств и степени выраженности симптомом, типов применяемой в текущий момент терапии и частоты лечения. Носители известны в этой области техники и включают стабилизатор, разбавитель и буфер. Подходящие стабилизаторы включают углеводы, такие как сорбит, лактозу, манит, крахмал, сахарозу, декстран и глюкозу, и белки, такие как альбумин или казеин. Подходящие разбавители включают соли, сбалансированные соли Хэнкса и раствор Рингера. Подходящие буферы включают фосфат щелочных металлов, карбонат щелочных металлов и карбонат щелочно-земельных металлов. Вакцины могут также содержать один или несколько адъювантов для повышения или усиления иммунных реакций. Подходящие адъюванты включают пептиды; гидроокись алюминия; фосфат алюминия; окись алюминия; и композицию, которая состоит из минерального масла, такого как Marcol 52, или растительного масла и одного или нескольких эмульгирующих соединений или поверхностно-активных соединений, таких как лизолецитин, поликатионы и полианионы. Вакцинную композицию настоящего изобретения можно вводить в виде индивидуального терапевтического средства или в комбинации с другим терапевтическим средством и также можно вводить совместно с подходящим терапевтическим средством либо последовательно, либо одновременно. Вакцинную композицию можно вводить с помощью известных способов введения. Способы введения включают, но не ограничиваются только ими, оральный, интрадермальный, внутримышечный, внутрибрюшинный, внутривенный, подкожный и интраназальный способы. Также фармацевтическую композицию можно вводить с помощью некоторых аппаратов, которые могут доставлять активное соединение в клетки-мишени.
Глубже понять настоящее изобретение можно через приведенные ниже Примеры, которые приведены в иллюстративных целях и никоим образом не ограничивают объем настоящего изобретения.
ПРИМЕРЫ
Материалы тестов
Набор для выделения ДНК (DNA miniprep) и набор, применяемый для экстракции ДНК из геля, были получены из фирмы "Nucleogen", триптон Bacto, дрожжевой экстракт Bacto, агар и т.д. - из фирмы "Difco" (Detroit, MI), ферменты рестрикции - из фирмы "Takara" и ДНК-лигаза фага Т4 - из фирмы "NEB". Были использованы pBluescript II SK ("Stratagene"), PCR 2.1 ("Invitrogen", Carlsbad, CA), векторы pQE30 ("Qiagen") и штаммы E.coli JM109 и M15 ("Qiagen").
IPTG, используемый для индукции продуцирования белка, получали из фирмы "Sigma", смолу Ni-NTA, используемую для очистки экспрессированных белков, - из фирмы "Novagen", и предварительно окрашенные маркеры молекулярной массы, используемые в SDS-PAGE, вестерн-блоттинг, ECL и т.д. - из фирмы "NEB". Мочевину, используемую для денатурации белков, получали из фирмы "Duchefa", а имидазол, используемый при очистке белков, - из фирмы "USB". Мембрану MWCO 3500, используемую для диализа, получали из фирмы "Spectrum"; реагентом, используемым для предупреждения агрегации белков, был CHAPS из фирмы "Amresco". Антитело, используемое в анализе ELISA, было антителом к крысиным IgG фирмы "Sigma", конъюгированным с пероксидазой хрена. Раствор субстрата, используемый в вестерн-блоттинге и ECL, был BCIP/NBT из фирмы "Sigma" и ECL Plus Western Blotting Detection Reagent был из фирмы "Amersham". Используемые адъюванты были адъювантом Фрейнда ("Sigma") и гидроокисью алюминия ("Reheis"). Концентрацию белка определяли с помощью набора ВСА protein assay ("Pierce") и набора Bradford assay ("Biorad").
Триглицериды, общий холестерин, холестерин HDL и холестерин LDL в сыворотке крови измеряли с помощью наборов triglyzyme-V, cholestezyme-V, HDL-C555 ("Shinyang Diagnostics", Korea) и EZ LDL cholesterol ("Sigma") соответственно. Использовали LDL calibrator ("Randox").
5-недельных самцов белых крыс линии Sprague Dawley (SD) получали из фирмы "Daehan Biolink Co. Ltd", Korea, их содержали с использованием корма фирмы "Samtako Inc." (Корея), который содержал более чем 18% натуральных белков, 5,3% неочищенных жиров, 4,5% неочищенных волокон и 8,0% золы.
Для очистки рекомбинантных пептидов PBl4Т и PBl4 применяли следующие буферы: буфер для ультразвукового разрушения (5 мМ имидазол, 0,5 М NaCl, 20 мМ трис-HCl, рН 7,9), буфер для связывания (5 мМ имидазол, 0,5 М NaCl, 20 мМ трис-HCl, 8 М мочевина, рН 7,9), буфер для промывания (50 мМ имидазол, 0,5 М NaCl, 20 мМ трис-HCl, 8 М мочевина, рН 7,9) и буфер для элюции (400 мМ имидазол, 0,5 М NaCl, 20 мМ трис-HCl, 8 М мочевина, рН 7,9).
ПРИМЕР 1: Получение искусственного гена для продукции пептида PBl4Т против ожирения.
Вектор pBluescript II SK расщепляли с помощью рестриктаз BamHI и XhoI для получения фрагмента Bl4 и вектор PCR 2.1 расщепляли с помощью рестриктаз SalI и HindIII для получения Т-фрагмента. Так как XhoI и SalI имеют совместимые липкие концы, фрагменты Bl4 и Т, полученные из двух векторов, лигировали с помощью ДНК-лигазы фага Т4 при 16°С в течение 12 ч. Так как лигированный участок не расщепляется SalI или XhoI, снова проводили расщепление с помощью SalI и HindIII для получения фрагмента Bl4Т. Для экспрессии белка в качестве векторной системы выбрали плазмиду pQE30, которая разработана для экспрессии желаемого белка в форме, слитой с шестью гистидиновыми остатками для облегчения процедуры очистки белка. Фрагмент гена Bl4Т вставляли в сайты SalI/HindIII вектора pQE30. Полученный экспрессионный вектор был назван "PBl4Т" (Фиг.1). Экспрессионный вектор трансформировали в Е.coli JM109. Из трансформированных клеток выделяли плазмиду ДНК и подвергали рестрикционному картированию с помощью SalI и HindIII. В результате фрагмент, содержащий 450 п.н., был благополучно вставлен в вектор pQE30 (Фиг.2).
Рекомбинантный вектор PBl4Т был депонирован в форме, предназначенной для трансформации в Е.coli (Е.coli M15/pBl4T), в Корейский центр культур микроорганизмов (КССМ, 361-221, Yurim B/D, Honje 1-dong, Sudaemum-gu, Seoul, Republic of Korea), 4 марта 2004 г., и ему был присвоен инвентарный номер КССМ-10562.
ПРИМЕР 2: Получение искусственного гена для продукции пептида PBl4 против ожирения.
Вектор pBluescript II SK был расщеплен с помощью SalI и XhoI для получения фрагмента Bl4. Вектор рВХ4 (вектор pQE30, имеющий вставку фрагмента Bl4, Korean Pat. Laid-open Publication No. 2002-0018971) был лианезирован с помощью расщепления рестриктазой SalI и лигирован с Bl4 с помощью ДНК-лигазы фага Т4 при 16°С в течение ночи.
ПРИМЕР 3: Определение нуклеотидной последовательности гена.
Чтобы подтвердить, правильно ли был вставлен фрагмент гена Bl4Т в рекомбинантный вектор PBl4Т, рекомбинантный вектор получали в концентрации 300-500 нг/мкг и подвергали ДНК-секвенированию, которое было проведено Core Bio System Co. Ltd., Korea. В результате было обнаружено, что выбранный рекомбинантный вектор представляет собой правильный клон (Фиг.3).
ПРИМЕР 4: Экспрессия рекомбинантного пептида PBl4Т.
Пептиды PBl4Т и PBl8 экспрессировали из вектора pQE30, который начинает экспрессию белка с его внутреннего инициирующего кодона с шестью гистидиновыми остатками для удобства процедуры очистки белка с последующим энтерокиназным участком расщепления. В качестве клетки-хозяина для экспрессии пептида использовали штамм Е.coli M15. Штамм Е.coli M15 трансформировали рекомбинантным вектором и наносили на чашки с LB-средой, содержавшей ампициллин (Amp) и канамицин (Kan). Выросшие колонии выращивали в 10 мл LB-среды, содержащей Amp (100 мкг/мл) и Kan (25 мкг/мл) в течение ночи. Чтобы исследовать экспрессию белка в зависимости от времени культивирования, 1 мл культуры, выращенной в течение ночи, вносили в 50 мл свежей LB-среды. Затем клетки инкубировали при перемешивании при 37°С в течение 1,5 ч, когда OD при 600 нм составляла от 0,4 до 0,5. На этой стадии в среду добавляли IPTG до конечной концентрации 1 мМ и клетки затем культивировали в течение 5 ч, в течение этого времени каждый час отбирали по 1 мл культуры. Перед добавлением IPTG отбирали 1 мл культуры для того, чтобы использовать ее в качестве не индуцированного контроля. Собранные образцы центрифугировали при 14000 об/мин в течение 1 мин. Осадки клеток растворяли в 30 мкл двукратного буфера для образцов, содержавшего SDS, и проводили SDS-PAGE. Результаты представлены на Фиг.4 и 5. Анализ SDS-PAGE обнаружил, что PBl4Т имеет молекулярную массу 16,2 кДа, a PBl8 - 16,5 кДа.
ПРИМЕР 5: Вестерн-блоттинг рекомбинантного пептида PBl4Т.
Пептид PBl4Т идентифицировали, анализируя его размер методом SDS-PAGE, но для дальнейшего подтверждения, является ли экспрессированный белок PBl4Т, проводили вестерн-блоттинг с применением двух видов антител, способных узнавать PBl4Т. Для контроля PBl4T при вестерн-блоттинге Е.coli M15 трансформировали вектором pQE30, не содержавшим фрагмент Bl4T. Образцы отбирали до индукции IPTG и через три часа после индукции IPTG. Кроличье поликлональное антитело к PBl4 и мышиное моноклональное антитело к preS2 разводили 1:10000 в PBS и использовали как первичные антитела. В качестве вторичных антител, способных узнавать первичные антитела, применяли козьи антитела к кроличьим IgG, конъюгированные с пероксидазой хрена, и козьи антитела к мышиным IgG после их разведения 1:10000 в PBS. Полученный блоттинг (мембрана с перенесенными на нее из геля белками, обработанная антителами) окрашивали с использованием набора ECL Plus Western Blotting Kit. Блоттинг переносили в кассету и на него помещали полоску медицинской рентгеновской пленки "Fuji". Блоттинг оставляли под пленкой на 10 с и окрашивали. Так как кроличье моноклональное антитело к PBl4 узнает PBl4-фрагмент PBl4Т, а мышиное моноклональное антитело к preS2 узнает Т-фрагмент (Т-кассету) PBl4T, в том случае, если белок PBl4Т правильно экспрессируется, полосы должны были наблюдаться на обоих блоттингах, которые индивидуально инкубировали с каждым из первичных антител. Как показано на Фиг.8, первичные антитела по отдельности узнавали PBl4 и Т-фрагмент PBl4Т, что указывает на то, что PBl4Т правильно экспрессировался.
ПРИМЕР 6: Оценка экспрессионной формы рекомбинантных пептидов PBl4Т и PBl8 в Е.coli.
Чтобы определить, экспрессировались ли PBl4Т и PBl8 как растворимые или нерастворимые белки, клетки собирали через 3 ч после индукции IPTG с помощью центрифугирования. Собранные клетки ресуспендировали в буфере для ультразвуковой обработки и обрабатывали ультразвуком. Полученный осадок и супернатант анализировали с помощью SDS-PAGE. Более подробно, клетки, обработанные IPTG для индукции экспрессии белка, центрифугировали при 9000 об/мин при 4°С в течение 30 мин. Осажденные клетки на время замораживали при -20°С размораживали на льду и ресуспендировали в буфере для ультразвукового разрушения (5 мл на 1 г осадка). Клетки обрабатывали ультразвуком пятнадцать раз по 30 с (каждый раз с 1-минутными перерывами). Клеточный лизат затем центрифугировали при 9000 об/мин при 4°С в течение 30 мин. Получали супернатант, выделяя таким образом неочищенный экстракт А, содержащий непроцессированные растворимые белки. Также получали осадок, выделяя, таким образом, неочищенный экстракт В, содержащий непроцессированные нерастворимые белки. Неочищенные экстракты А и В по отдельности смешивали с 2-кратным SDS-буфером для образцов, кипятили при 95°С в течение 5 мин и проводили SDS-PAGE. Анализ SDS-PAGE обнаружил, что целевые белки присутствовали в основном в осадке, а не в супернатанте, что указывает на то, что белки PBl4Т и PBl8 экспрессировались в нерастворимой форме (Фиг.6 и 7).
ПРИМЕР 7: Очистка рекомбинантных пептидов PBl4, PBl4Т и PBl8.
Очистку белков проводили, используя смолу Ni-NTA, предназначенную для выделения белков с концевой гистидиновой меткой. Эта очистка представляла собой аффинный хроматографический способ, использующий взаимодействие Ni+, связанного со смолой, и гистидинового гексамера на концевой части слитого белка. После того как трансформированные клетки Е.coli предварительно культивировали в 10 мл LB-среды в течение ночи, 10 мл культуры вносили в 500 мл LB-среды и культивировали при 37°С до тех пор, пока величина OD при 600 нм не достигала значений 0,4-0,5. Затем в среду добавляли 1 мМ IPTG и клетки культивировали еще 4 ч. Клетки центрифугировали при 9000 об/мин в течение 30 мин и осадок клеток хранили при -20°С. Затем замороженные клетки размораживали на льду, суспендировали в буфере для ультразвукового разрушения (5 мл на 1 г сырого веса клеток) и обрабатывали ультразвуком. Лизат клеток затем центрифугировали при 9000 об/мин при 4°С в течение 30 мин. Осадок ресуспендировали в объеме буфера для связывания, равном объему супернатанта, обрабатывали ультразвуком три раза для удаления обломков клеток и центрифугировали при 9000 об/мин при 4°С в течение 30 мин. Полученный таким образом супернатант подвергали аффинной хроматографии на колонке со смолой Ni-NTA.
Колонку диаметром 1 см и высотой 15 см заполняли 2 мл смолы, и все стадии проводили при скорости потока 2 мл/мин. После того как колонка была заполнена смолой, смолу промывали дистиллированной водой в количестве, равном трем-пяти объемам колонки, смолу заполняли ионами Ni2+, используя 1-кратный буфер (50 мМ NiSO4) в количестве, равном пяти объемам колонки, и уравновешивали буфером для связывания, получая, таким образом, Ni2+-хелатирующую аффинную колонку. После двукратного нанесения образца на колонку ее промывали буфером для связывания до тех пор, пока поглощение при 280 нм не достигало базового уровня 1.0, а затем буфером для промывания в течение 10 мин. После того как колонка была полностью уравновешена, проводили элюцию буфером для элюции, содержащим более высокие концентрации имидазола, чем буфер для промывания, создавая, таким образом, градиент имидазола, и элюцию продолжали еще в течение следующих 10 мин для полной элюции белка, связавшегося со смолой. Собирали все двадцать фракций объемом по 2 мл. Так как элюируемый пептид был растворен в 8 М мочевине, его диализовали в PBS в течение ночи для удаления мочевины.
Как было описано выше, так как каждый из белков был в высшей степени нерастворимым, его очищали после денатурации в буфере, содержащем 8 М мочевину, и белки, связавшиеся со смолой элюировали, используя градиент имидазола от 50 мМ до 400 мМ. Результаты приведены на Фиг.9, 10 и 11. Большинство белка элюировалось при концентрации имидазола, равной около 300 мМ. Выход белков на 1 л культуры составлял 3-3,5 мг для PBl8 и 4-4,5 мг для PBl4Т.
ПРИМЕР 8: Количественная оценка рекомбинантных пептидов PBl4, PBl4Т и PBl8.
После того как элюированные пептиды PBl4Т, PBl4 и PBl8 диализовали в PBS, из-за того, что убрали мочевину, белки агрегировали, образуя осадки. В таком состоянии точную концентрацию белка определить невозможно. Агрегированные очищенные белки растворяли, применяя 50 мМ CHAPS. Концентрацию белка определяли с помощью наборов ВСА protein assay и Bradford assay. Делали серийное разведение раствора BSA 2 мг/мл до 1000, 500, 250, 125 и 62,5 мкг/мл и эти разведения использовали в качестве стандарта. Анализ с ВСА проводили в соответствии с протоколом, предоставляемым фирмой "Pierce". Цветную реакцию белка с ВСА проводили при 37°С в течение 30 мин и затем измеряли поглощение при 562 нм. Кроме того, образцы оставляли для проведения реакции с реагентом Бредфорд при комнатной температуре в течение 10 мин и затем проводили измерение при 595 нм. Получали стандартные кривые, используя поглощение серийных разведений BSA или цветных реакций белка по Бредфорду, и концентрации белков в образцах определяли, используя стандартные кривые.
ПРИМЕР 9: Конструирование вектора pTBl4 для экспрессии PTBl4.
Вектор pQE30, трансформированный в Е.coli M15, был дважды расщеплен с помощью KpnI и SalI ("Takara") для вырезания Т-кассеты (preS2). Плазмиду pBluescript также обрабатывали теми же рестриктирующими ферментами. Вырезанную Т-кассету и лианезированную pBluescript разделяли на геле, очищали и лигировали друг с другом, используя ДНК-лигазу фага Т4. 4 мкл pBluescript, 4 мкл Т-кассеты, 1 мкл ДНК-лигазы фага Т4 ("MBI Fermentas") смешивали в пробирке объемом на 1,5 мл и смесь для лигирования инкубировали при 16°С в течение ночи. Затем рекомбинированный вектор смешивали с JМ109-компетентными клетками, подвергали тепловому шоку при 42°С в течение 90 с и инкубировали в LB-среде при 37°С в течение 1 ч. Затем трансформированные клетки размазывали по поверхности LB/Amp-чашек и инкубировали при 37°С. Случайным образом из выросших колоний выбирали несколько колоний и культивировали их. Затем из культуры клеток выделяли плазмидную ДНК, расщепляли с помощью рестриктирующих ферментов и для анализа размера фрагментов ДНК проводили электрофорез на агарозном геле. Для того чтобы получить ТВ4-кассету, из Т-кассеты удаляли сайт XhoI. To есть, так как Т-кассета (ген HBV preS2, 183 п.н.) не может быть использована для клонирования из-за того, что сайт XhoI находится около ее 3′-конца (около 150 п.н. от 5′-конца Т-кассеты), Т-кассета была точечно мутирована по внутреннему сайту XhoI и, таким образом, приобретала новую последовательность. Короткий фрагмент ДНК (30 п.н.) был вырезан из pBluescript-preS2, так как в Т-кассете был внутренний сайт XhoI. В это положение вставляли синтетические олигомеры. Чтобы предотвратить самолигирование, вектор обрабатывали щелочной фосфатазой ("Boehringer Mannheim", GmbH, Germany) при 37°С в течение 30 мин, дефосфорилировали при 95°С в течение 5 мин и элюировали из геля. Олигомеры были фосфорилированы на их 5′-концах с помощью обработки полинуклеотидкиназой при 37°С в течение 30 мин и при 65°С в течение 20 мин. Затем вектор и олигомеры оставляли при 95°С на 5 мин и медленно охлаждали в нагревательном блоке для отжига. Олигомеры и pBluescript-Т затем обрабатывали лигазой при 16°С в течение ночи. Рекомбинированный pBluescript-T трансформировали в JМ109-клетки и размазывали по поверхности LB/Amp-чашек. После того как плазмидная ДНК была выделена из выросших колоний и проанализирована, получали клон, несущий желаемую плазмиду. Олигомеры состояли из 28 нуклеотидов, соответствующих preS2, в котором пять нуклеотидов G на 5′-конце смысловой цепи были заменены на А для удаления сайта XhoI и, таким образом, имели замену лизина на аргинин. Смысловую и антисмысловую цепи, каждая из которых была сконструирована 28-мерной, отжигали и вставляли в обработанный XhoI pBluescript-preS2. После того как pBluescript-T был дважды расщеплен с помощью SalI и XhoI, a рQЕ30-В4 был расщеплен с помощью SalI, их очищали из гелей. Полученный Т фрагмент вставляли в pQE30-B4, расщепленный на его 5′-конце, сконструировав, таким образом, рQЕ30-рТВ4. Структура рекомбинированного ТВ4 была подтверждена с помощью рестрикционного картирования рестриктазами SalI и HindIII. Полученный вектор был назван pTBl4 (Фиг.13).
ПРИМЕР 10: Экспрессия и очистка PTBl4.
Экспрессионный вектор pTBl4 вводили в Е.coli M15 и трансформированные клетки культивировали в 2 л LB-среды, содержащей Amp и Kan. Выращенные клетки центрифугировали при 7000 об/мин в течение 10 мин, получая, таким образом, 9 г влажных клеток. Так как рекомбинантный экспрессированный гибридный полипептид РТВ4 имел концевую гистидиновую метку, его подвергали аффинной хроматографии на His-связывающей колонке со смолой Ni-NTA. Колонка, в которой применяли 4 мл смолы, была размером 1,8 см в диаметре и высотой 8 см. Диапазон измеряемого поглощения в Econo system составлял 0,5, скорость лентопротяжки в самописце была 2 см/ч, и скорость нанесения образца составляла 2 мл/мин. Сначала влажные клетки суспендировали в буфере для ультразвукового разрушения, обрабатывали ультразвуком и центрифугировали при 10000 об/мин при 4°С в течение 30 мин. Осадок растворяли в буфере для связывания и подвергали аффинной хроматографии. Раствор для связывания пропускали через колонку для того, чтобы смола уплотнилась. После того как с помощью детектора была установлена базовая линия и была зафиксирована предварительно установленная величина, обработанный ультразвуком образец наносили на колонку. Когда образец вошел в колонку и была зафиксирована предварительно установленная величина, через колонку пропускали раствор для промывания. После достижения заданной величины через колонку пропускали раствор для элюции, выделяя, таким образом, PTBl4. Экспрессированный и очищенный гибридный полипептид анализировали с помощью SDS-PAGE и вестерн-блоттинга. PTBl4, разделенный с помощью SDS-PAGE, переносили на мембрану с помощью полусухого переноса. Блоттинг инкубировали в блокирующем буфере (0,5% казеин - забуференный фосфатом физиологический раствор - Tween, 0,02% NaN3) при 37°С в течение 2 ч и дважды промывали смесью - забуференный трисом физиологический раствор - Tween (TBS-T, рН 7,6), по 2 мин на каждую промывку. Затем блоттинг инкубировали с первичным антителом при 37°С в течение 1 ч и четыре раза промывали TBS-T, по 5 мин на каждую промывку. Блоттинг инкубировали 1 ч с вторичным антителом и промывали тем же самым способом. Чтобы идентифицировать Т-кассету, применяли моноклональное антитело к preS2 (1:10000) и козье антитело к мышиным IgG, конъюгированное с пероксидазой хрена (1:10000). В-кассету обнаруживали с помощью кроличьей антисыворотки к PBl4 (1:10000) и козьего антитела к кроличьим IgG, конъюгированного с пероксидазой хрена (1:10000). После высушивания блоттинг обрабатывали с помощью ECL-реагентов в течение 5 мин для обнаружения полос. В результате в В-кассете, которую диагностировали с помощью кроличьей антисыворотки к РВЦ и козьего антитела к кроличьим IgG, конъюгированного с пероксидазой хрена, в образцах PBl4Т и PTBl4 была обнаружена полоса 16 кДа. В Т-кассете, которую диагностировали с помощью моноклонального антитела к preS2 и козьего антитела к мышиным IgG, конъюгированного с пероксидазой хрена, в образце PBl4 обнаруживали полосу размером около 8 кДа и в образцах PBl4Т и PTBl4 была обнаружена полоса 16 кДа. Эти результаты указывают на то, что каждый гибридный полипептид был точно экспрессирован и очищен (Фиг.13).
ПРИМЕР 11: Конъюгация PBl4 и овальбумина.
PBl4 конъюгировали с белком-носителем овальбумином. Белок-носитель и PBl4 смешивали в молярном отношении около 1:10 и оставляли реагировать с образованием осадка при 4°С в течение примерно 1 ч в реакционном флаконе. После того как в реакционную смесь добавляли 2%-ный глутаральдегид, смесь оставляли для реакции в течение 3 ч. Реакционную смесь затем диализовали, применяя диализную мембрану MWCO 3,000, против PBS-буфера в течение ночи для удаления оставшегося глутаральдегида.
ПРИМЕР 12: Вакцинация (иммунизация).
7-недельных белых крыс SD разделили на шесть групп и вакцинировали (Таблица 1). Как описано в Таблице 1, 100 мкг каждого пептида, очищенного и оцененного количественно в Примере 7 и 10, смешивали с каждым адъювантом, чтобы получить общий объем 100 мкл, и вводили внутрибрюшинно крысам. Инъекцию проводили три раза с 2-недельными перерывами, то есть в возрасте 7, 9 и 11 недель. Адъювантами были адъювант Фрейнда и гидроокись алюминия. Адъювант Фрейнда применяли в том же количестве, что и пептид. Гидроокись алюминия 5,8 мг/мл доводили до конечной концентрации 0,2 мг/мл, смешивали с каждым пептидом и инкубировали для осаждения при комнатной температуре. Образцы крови собирали через пять дней после первой иммунизации и через пять дней, две недели и четыре недели после второй иммунизации.
Изменения веса тела крыс SD после вакцинации были нанесены на график (Фиг.15). От первичной инъекции до повторной иммунизации (вторичная инъекция) крысы демонстрировали одинаковый вес в диапазоне от 292 до 297 г. Однако через одну неделю после вторичной инъекции наблюдали различие в весе крыс между вакцинированными группами и нормальной и имитационной группами. В возрасте 18 недель по сравнению с имитационными группами PBl4-вакцинированная группа демонстрировала разницу веса тела в 16 г, а PBl4Т-вакцинированная группа показала разницу веса тела в 27 г (Таблица 2). Это указывает на то, что слабые иммунные реакции, индуцированные первичной инъекцией, усиливались после повторной иммунизации с помощью вторичной инъекции и что усиленные иммунные реакции приводят к подавлению прироста веса тела крыс. Это различие прироста веса тела сохранялось после третьей инъекции.
В Таблице 2 все данные представлены в виде среднего значения ±SD, где SD (стандартное отклонение) рассчитывали для пяти белых крыс Sprague Dawley, и единицы измерения - граммы.
ПРИМЕР 13: Измерение титров антител.
Титры антител измеряли, используя образцы сыворотки крови, с помощью метода непрямого иммуноферментного анализа (ELISA). 100 мкл (100 нг) PBl4 помещали в каждую лунку микротитровального планшета. Планшет инкубировали при 4°С в течение ночи и инкубировали в блокирующем растворе (PBS, 0,5%-ный казеин, 0,02%-ный NaN3) при 37°С в течение 1 ч. Каждую лунку промывали три раза PBST. Образцы сыворотки крови, собранные у вакцинированных крыс SD, были разведены PBS от 1:500 до 1:8000. 100 мкл каждого разведенного образца сыворотки вносили в каждую лунку и инкубировали при 37°С в течение 1 ч. Каждую лунку промывали три раза PBST и инкубировали с козьими антителами к крысиным IgG в качестве вторичных антител в разведении 1:1000. Планшет обрабатывали OPD для развития окраски и измеряли поглощение при 450 нм.
Фиг.16 демонстрирует титры антител крыс SD из вакцинированных групп в возрасте 10, 12, 14 и 16 недель. Титры определяли с помощью метода ELISA на основании величины поглощения, равной 0,6, когда каждый образец сыворотки был разведен от 1:500 до 1:8000; группы, которым вводили PBL4, PBl4Т и PTBl4 демонстрировали повышенные титры антител вплоть до 14-недельного возраста. PBl4Т-иммунизированная группа показала значения OD, которые были в 1,5 раза выше, чем у PBl4-иммунизированной группы, а PTBl4-иммунизированная группа показала слабое повышение по сравнению с группой PBl4. В возрасте 16 недель группа PBl4 демонстрировала снижение титра антител, а группы PBl4Т и PTBl4 сохраняли повышенные титры антител. Однако было обнаружено, что PTBl4 обладал значительно более слабым эффектом на повышение титров антител, составляющим примерно 50-60% в сравнении с PBl4Т.
ПРИМЕР 14: Оценка профиля сывороточных липидов.
Уровни TG и холестерина измеряли, как описано ниже. 4 мкл образца сыворотки крови смешивали с 200 мкл окрашивающего реагента и инкубировали при 37°С в течение 5 мин и затем измеряли поглощение при 505 и 500 нм. Для измерения уровня HDL образец сыворотки крови смешивали с осаждающим реагентом в соотношении 1:1, оставляли при комнатной температуре на 10 мин и центрифугировали при 3000 об/мин или выше в течение 10 мин. 4 мкл супернатанта смешивали с 200 мкл окрашивающего реагента и инкубировали при 37°С в течение 5 мин и затем измеряли поглощение при 555 нм. Уровни LDL-холестерина измеряли с помощью набора EZ LDL cholesterol kit ("Sigma") и калибратора LDL ("Randox"). В соответствии с протоколом фирмы-производителя 4 мкл образца сыворотки смешивали с 1150 мкл реагента, поставляемого с набором, инкубировали при 37°С в течение 5 мин, добавляли 250 мкл реагента и снова инкубировали при 37°С в течение 5 мин. Затем измеряли поглощение при 600 нм. Уровни каждого липида в сыворотке крови определяли на основании измеренных значений поглощения и стандартной кривой, полученной при использовании стандартных растворов.
Результаты исследований липидных профилей в образцах сыворотки крови, собранных после третьей инъекции крысам SD, представлены ниже в Таблице 3.
В Таблице 3 все данные представлены в виде среднего значения ±SD, где SD (стандартное отклонение) рассчитывали для пяти белых крыс Sprague Dawley, и единицы измерения - мг/дл.
Нормальная и имитационная группы демонстрировали уровни TG и холестерина, превышающие приблизительно на 10 мг/мл уровни вакцинированных групп. При сравнении вакцинированных групп между собой были обнаружены более высокие уровни TG и LDL-холестерина в PBl4-вакцинированной группе, но различие было незначительным (Фиг.17).
ПРИМЕР 15: Клинический тест с домашними собаками
PBl4Т смешивали с окисью алюминия, применяемого в качестве адъюванта. 0,5 мл смеси (2 мг/мл) дважды вводили внутримышечно или подкожно десяти домашним собакам (находящимся на лечении от ожирения в ветеринарном госпитале в Ансане, Корея) с двухнедельными перерывами. В течение периода времени от 1,5 до 3 месяцев наблюдали за изменением веса собак. В результате уровень антител слегка снизился (время полужизни: три месяца) и не было обнаружено увеличения веса тела домашних собак даже тогда, когда собакам разрешалось неограниченно питаться легкой пищей или когда они находились на очень жирной диете. Более подробно, прирост веса тела был подавлен у всех десяти собак даже тогда, когда собаки усваивали легкую пищу или высококалорийную еду. В частности, йоркширские терьеры не увеличивали вес тела после инъекции PBl4Т даже в ситуации, когда вес тела собаки прогнозированно должен был увеличиваться в соответствии с их полом и возрастом.
Кроме того, у иммунизированных домашних собак собирали образцы сыворотки крови, чтобы оценить степень индукции уровня иммунных реакций. С помощью метода ELISA через одну неделю после вторичной инъекции измеряли титры антител к PBl4T и PBl4 в сыворотке крови. Было обнаружено высокое значение поглощения, равное 0,5, когда образцы сыворотки разводили в 5000-50000 раз, что указывает на то, что пептид PBl4Т обладает превосходным эффектом на индукцию иммунных реакций.
Промышленное применение
Как было описано выше, гибридный полипептид настоящего изобретения, в котором С-концевая часть миметического пептида В-клеточного эпитопа аро В-100, обладающего эффектом против ожирения, слита с N-концевой частью Т-хелперного эпитопа, демонстрирует превосходную активность против ожирения без индукции иммунных реакций, которые нейтрализуют полезные активности или эффекты В-клеточного эпитопа аполипопротеина В-100, или без тяжелых побочных эффектов. Таким образом, гибридный полипептид очень полезен для предупреждения или лечения ожирения.













Изобретение касается иммуногенного гибридного полипептида, включающего миметический пептид В-клеточного эпитопа аполипопротеина В-100, в котором С-конец миметического пептида слит с N-концом Т-хелперного эпитопа. Аминокислотные последовательности вариантов полипептида представлены в описании. Описан способ получения указанного полипептида, предусматривающий использование клетки-хозяина, трансформированной рекомбинантным экспрессионным вектором, включающим ген, кодирующий указанный полипептид. Изобретение также касается вакцинной композиции, включающей указанный иммуногенный гибридный полипептид, для предупреждения или лечения ожирения, рекомбинантного экспрессионного вектора и клетки-хозяина. Полипептид по изобретению демонстрирует превосходную активность против ожирения без индукции иммунных реакций или тяжелых побочных эффектов. 5 н. и 10 з.п. ф-лы, 17 ил., 4 табл.
| US 6284533 B1, 04.09.2001 | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| ПРОИЗВОДНЫЕ ОВ-ПРОТЕИНА | 1996 |
|
RU2178307C2 |
| RU 97104072 A, 20.05.1999 | |||
| RU 93005218 A, 20.09.1996. | |||
Авторы
Даты
2008-12-20—Публикация
2005-03-18—Подача