Изобретение относится к аналитической химии, а именно к способам определения ионов металлов сурьмы, висмута, меди, и может быть использовано для определения их содержания в водных растворах в присутствии растворенного кислорода методом инверсионной анодно-катодной вольтамперометрии (АКВА).
Изучено электрохимическое поведение сурьмы, висмута, меди в разных объектах, на фоновых электролитах (HCl, H3PO4, HNO3, лимонная, винная, щавелевая кислоты), в нейтральных растворах хлоридов калия и натрия, аммиачных и растворах различных солей, а также щелочных растворах [Ф.Выдра, К.Штулик, Э.Юлакова. Инверсионная вольтамперометрия. М.: Мир, 1980, 278 с.].
Установлены условия определения микроконцентраций сурьмы, висмута, меди в водных объектах как при совместном определении, так и раздельно [Захаров М.С., Захарчук Н.Ф. Электрохимические методы анализа природных и сточных вод. 1985, Новосибирск, 222 с.]. Сущность методики состоит в электронакоплении на ртутно-графитовых, ртутных электродах с последующим растворением концентрата при анодной развертке потенциала. Исследованы различные факторы, влияющие на электрохимические сигналы сурьмы, висмута, меди (типы электродов, влияние анеонов и катионов в фоне, pH), приведены потенциалы полупиков.
Описан способ одновременного определения Cu, Bi, Sb в объектах окружающей среды методом дифференциально-импульсной анодной инверсионной вольтамперометрии с системой остановки потока [Wang F., Li F., Liu S., Zhang Y., Liu Z. Anal. Leff, 1994, 27, №9, p.1779-1787]. Оптимизированы условия электроконцентрирования на индикаторном Hg электроде типа «висящая капля» на фоне 0.1 М HCl при -0,5 В (отн. х.с) в течение 40 с при скорости потока 1,5 мл/мин и стадией анодного растворения на фоне смеси 0,25 М малоновой кислоты и 0.1 М HCl после остановки потока. Интервал определяемых концентраций 10-9 до 10-6 моль/л.
Изучена возможность одновременного определения Cu, Bi, Sb с использованием квадратно-волновой и дифференциально-импульсной анодной вольтамперометрии с применением в качестве индикаторного электрода стационарной Hg-капли при времени электроконцентрирования менее 10 мин [Kitamura Hudeki, Okawa Kazunobu, Kuge Yoshibo, Asada Shingo // J. Chem. Soc. Jap., Chem., and Ind. Chem. /, 1979, №12, p.1702-1707].
Чувствительным методом является инверсионно-вольтамперометрический метод одновременного определения сурьмы, висмута и меди на ртутном электроде [Бабич Г.А., Кисиль Е.П., Салихджанова Р.М.-Ф. Одновременное инверсионно-вольтамперометрическое определение Zn, Cd, Pb, Tl, Sb, Bi и Cu в воздухе // Заводская лаборатория. Диагностика материалов, 1998, 64, №11, С.3-5] (прототип). Определение сурьмы, висмута, меди проводят по следующей методике. Для измерений применяют трехэлектродную систему. В качестве индикаторного используют ртутный капельный электрод клапанного типа, электрод сравнения - хлоридсеребряный и вспомогательный - платиновый. Потенциал электролиза -1,25 В, пики анодного растворения элементов в ацетатном буферном растворе (pH 5,2) после деаэродорирования азотом в течение 15 мин, регистрируют в интервале потенциалов от -1,25 до 0,2 В, скорость развертки 10 мВ/с. Для устранения наложения и образования суммарных пиков (из-за близости потенциалов пиков элементов) используют комплексен (III). Чувствительность метода для меди - 2·10-4 мг/дм3, для висмута - 1,2·10-3 мг/дм3, для сурьмы - 4·10-3 мг/дм3.
Все вышеперечисленные методики отличают использование токсической ртути, длительность анализа, мешающее влияние кислорода, ограниченный диапазон определяемых концентраций Sb, Bi и Cu и близость потенциалов пиков этих элементов.
Основной задачей предложенного решения является определение сурьмы, висмута, меди на золотосодержащей поверхности электродов методом инверсионной анодно-катодной вольтамперометрии (АКВА) в присутствии растворенного кислорода.
Поставленная задача достигается тем, что сурьму, висмут и медь электрохимически концентрируют на золотосодержащую поверхность различных типов углеродсодержащих электродов (стеклоуглеродного (СУЭ), импрегнированного графитового (ИГЭ), сажевого композиционного (СКЭ)) с образованием соединений сурьмы, висмута, меди с золотом и последующим растворением осадков с регистрацией анодных и катодных вольтамперограмм.
В предлагаемом способе впервые установлена способность одновременного определения сурьмы, висмута, меди на золотосодержащей поверхности электрода различных типах углеродсодержащих электродов в присутствии растворенного кислорода. В качестве проводящей основы для индикаторного золотосодержащего электрода применяли ИГЭ, СУЭ, СКЭ (в прототипе применяли ртутно-капельный электрод клапанного типа). Использование таких электродов обусловлено высокой химической и электрохимической устойчивостью графита, широкой областью рабочих потенциалов, а также простотой механического обновления поверхности и требованиями техники безопасности.
Новым в способе является то, что электроконцентрируют Sb, Bi и Cu на золотосодержащую поверхность углеродсодержащего электрода в перемешиваемом растворе в течение 60-120 с при потенциалах электролиза Eэ(-0,9÷-1,1) В на фоне 0,1 М HCl, затем проводят стадию выдерживания раствора без перемешивания в области предельного тока растворенного в фоне кислорода (-0,3÷-0,6) B в течение 40-60 с с последующим циклическим изменением потенциала (ЦВА) от -0,3 до 0,4 В и обратно от 0,4 до -0,3 В при 50÷100 мВ/с. Сигнал меди (Eп(Cu) 0,22÷0,26 В) регистрируют и оценивают методом добавок аттестованных растворов при анодной развертке ЦВА. Сигнал висмута (Eп(Bi) 0,11÷0,18 В) и сурьмы (Eп(Sb) 0,0÷0,07 В) регистрируют и оценивают при катодной развертке потенциала ЦВА (отн. нас.х.э.). Для повышения чувствительности определения сурьмы и висмута сигнал получают в форме первой производной dI/dE.
В прототипе количественное одновременное определение Sb, Bi и Cu основано на анодном окислении амальгамы сурьмы, висмута и меди, которое возможно только при удалении растворенного кислорода из раствора и невысокой скорости изменения потенциала (10 мВ/с).
Максимальное значение регистрируемого тока наблюдается у золотосодержащих ИГЭ, СУЭ, СКЭ электродов, все типы электродов пригодны к использованию. Срок службы электродов с площадью поверхности золотой пленки S>0,05 см2 составляет больше месяца. Чистку электродов проводят электрохимичиски при потенциале 0,5 B в области потенциалов растворения сурьмы, висмута и меди до потенциала растворения золота. В связи с этим нет необходимости перед каждым анализом наносить новую пленку золота.
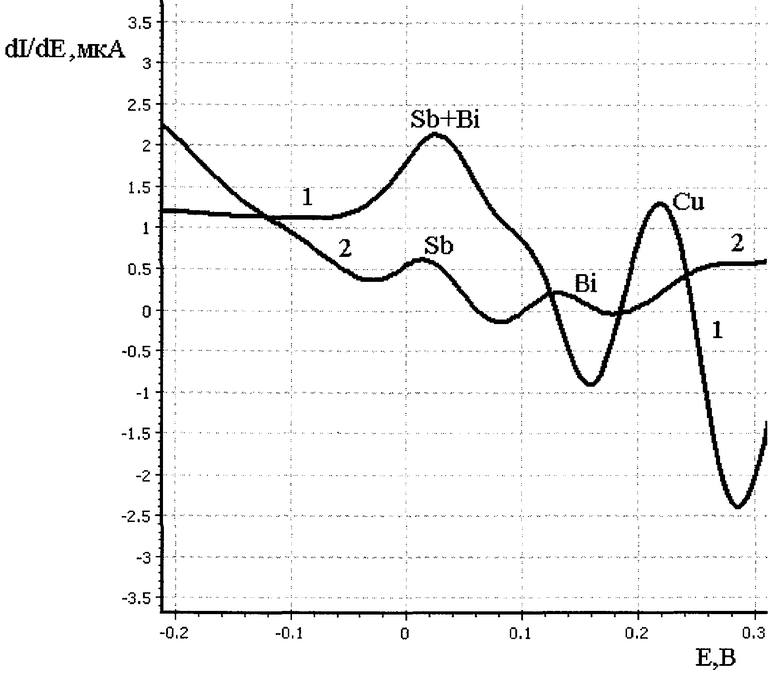
Применение ЦВА позволяет одновременно определить сурьму, висмут, медь. На чертеже представлены вольтамперограммы сурьмы, висмута, меди на золотосодержащем ИГ электроде. Фон 0,01 М HCl, CBi(III)=0,003 мг/дм3, CCu(II)=0,003 мг/дм3, CSb(III)=0,003 мг/дм3, 1 - анодная вольтамперная кривая, 2 - катодная вольтамперная кривая. При сканировании потенциала в анодную область (см. чертеж, кривая 1), регистрируют отдельный пик меди (II), при сканировании потенциала в катодную область (см. чертеж, кривая 2) пики сурьмы (III) и висмута (III) хорошо разделяются. В прототипе из-за близости потенциалов пиков элементов применяют комплексен (III) для устранения наложения и образования суммарных пиков.
Для уменьшения влияния растворенного кислорода используют выдерживание раствора без перемешивания в течение 40÷60 с в области восстановления растворенного кислорода (-0,3÷-0,6) В (в прототипе дезактивацию кислорода проводят инертным газом).
Использование приема, получение сигнала в форме первой производной dI/dE значительно увеличивает чувствительность метода. Нижняя граница определяемых концентраций для сурьмы, висмута и меди 1·10-4 мг/дм3 (в прототипе чувствительность метода Cu 0,4 мг/дм3, Bi 12 мг/дм3, Sb 4 мг/дм3 (табл.1).
Время предварительного электролиза (τэ) выбирают в зависимости от концентрации определяемого вещества. Максимальное значение величины тока окисления достигается при τэ, равном 60÷120 с. При τэ меньше 90 снижается чувствительность определения и увеличивается ошибка определения, а при τэ больше 120 снижается экспрессность.
Важным для определения является выбор скорости развертки потенциала. Оптимальной является скорость 50÷100 мВ/с. Увеличение скорости более 100 мВ/с увеличивает чувствительность, но при этом растет остаточный ток и уменьшается разрешающая способность способа. Использование скорости менее 50 мВ/с существенно снижает величину анодного тока, и понижается чувствительность определения (в прототипе 10 мВ/с).
Примеры конкретного выполнения.
Пример 1. Измерения были проведены на аттестованных растворах. Нанесение золотой пленки на электрод. 10 мл раствора ГСО Au (III) концентрацией 100 мг/дм3 помещают в кварцевый стаканчик. Проводят электронакопление золота на индикаторный ИГЭ при перемешивании из раствора при условии: Еэ=-1,00 В, τэ=100 с.
10 мл 0,1 М HCl фонового электролита помещают в кварцевый стаканчик. Не прекращая перемешивания, проводят электролиз раствора на золотосодержащий ИГЭ при условии: Eэ -1,0 В, τэ 120 с, затем проводят выдерживание раствора без перемешивания в области предельного тока кислорода -0,5 В с последующим циклическим изменением потенциала (ЦВА) при скорости развертки 100 мВ/с, начиная с потенциала -0,3 В до 0,4 В и обратно в режиме первой производной dI/dE. Отсутствие пиков свидетельствует о чистоте фона. Затем добавляют 0,02 мл аттестованных растворов сурьмы, висмута, меди концентрацией 1 мг/дм3 и проводят электрохимическое концентрирование осадка при аналогичных условиях. Сигнал меди регистрируют при анодной развертке ЦВА Eп(Cu) 0,22÷0,26 В, сигнал сурьмы и висмута регистрируют при обратной катодной развертке потенциала ЦВА Eп(Bi) 0,11÷0,18 В, Eп(Sb) 0,0÷0,07 В (отн. нас.х.э.).
Вводят в анализируемый раствор 0,02 мл добавку аттестованных растворов сурьмы, висмута и снова регистрируют аналитические сигналы. По разнице токов вычисляют концентрацию ионов металлов в растворе. Погрешность измерений составляет порядка 5-10%.
Пример 2. Измерения были проведены в водопроводной воде.
В 100 мл исследуемой пробы вносят 1 мл 68% HNO3 и упаривают до влажного остатка при температуре 170°С, добавляют 1 мл 98% H2SO4 и упаривают на плитке до сухого остатка. Затем помещают стаканчик в муфельную печь и прокаливают осадок при 400-450°С. Стаканчик с осадком охлаждают, добавляют 1 мл 1 М HCl и 0,01 г солянокислого гидразина и упаривают до влажного остатка.
В исследуемую пробу вносят 10 мл 0,1 М HCl фонового электролита. Не прекращая перемешивания, проводят электролиз раствора на золотосодержащий СКЭ при условии: Eэ -0,9 В, τэ 60 с, затем проводят выдерживание раствора без перемешивания при -0,6 В с последующим циклическим изменением потенциала при 80 мВ/с, начиная с потенциала -0,30 до 0,400 В и обратно в режиме первой производной dI/dE. Регистрируют вольтамперные анодные кривые меди в диапазоне потенциалов 0,22÷0,26 В, а затем катодные вольтамперные кривые висмута 0,11÷0,18 В и сурьмы 0,0÷0,07 В (отн. нас.х.э.).
Затем добавляют 0,02 мл аттестованных растворов сурьмы, висмута, меди концентрацией 1 мг/дм3 и снова регистрируют аналитические сигналы металлов. По разнице токов пиков вычисляют концентрацию сурьмы, висмута, меди в растворе.
Таким образом, впервые установлена способность одновременного количественного анализа сурьмы, висмута, меди на золотосодержащем электроде в диапазоне концентраций 0,0001-0,1 мг/дм3 методом анодно-катодной вольтамперометрии.
Предложенный способ прост, не используется ртуть из-за ее токсического действия, не требуется дополнительное лабораторное оснащение для удаления мешающего влияния кислорода в растворе. Способ может быть применен в любой химической лаборатории, имеющей компьютеризированные анализаторы типа ТА, СТА или полярограф. Предложенный способ может быть использован для определения сурьмы, висмута, меди в питьевых, природных и сточных водах (табл.2).
Изобретение может быть использовано в различных отраслях народного хозяйства для определения содержания в растворах различных концентраций ионов металлов. Способ согласно изобретению заключается в том, что проводят вольтамперометрическое определение сурьмы, висмута, меди, при этом электроконцентрируют Sb, Bi и Cu на золотосодержащей поверхности различных типов углеродсодержащих электродов в перемешиваемом растворе в течение 60-120 с при потенциалах электролиза Еэ(-0,9÷-1,1) В на фоне 0,1 М HCl. Затем выдерживают раствор без перемешивания в области предельного тока кислорода при (-0,3÷-0,6) В с последующим циклическим изменением потенциала (ЦВА) от -0,3 до 0,4 и обратно при 50÷100 мВ/с. Сигнал меди регистрируют и оценивают методом добавки аттестованных растворов при анодной развертке ЦВА Еп(Cu) 0,22÷0,26 В, сигнал сурьмы и висмута регистрируют и оценивают методом добавки аттестованных растворов при катодной развертке потенциала ЦВА Eп(Sb) 0,0÷0,07, Еп(Bi) 0,11÷0,18 в форме первой производной dI/dE относительно насыщенного хлоридсеребряного электрода (нас.х.э). Техническим результатом изобретения является определение сурьмы, висмута, меди в водных растворах методом АКВА. 1 ил., 2 табл.
Способ определения сурьмы, висмута, меди в водных растворах методом инверсионной анодно-катодной вольтамперометрии, заключающийся в том, что проводят вольтамперометрическое определение сурьмы, висмута, меди, отличающийся тем, что электроконцентрируют Sb, Bi и Cu на золотосодержащей поверхности различных типах углеродсодержащих электродов в перемешиваемом растворе в течение 60÷120 с при потенциалах электролиза Еэ(-0,9÷-1,1) В на фоне 0,1 М HCl, затем проводят выдерживание раствора без перемешивания в области предельного тока кислорода при (-0,3)÷-(0,6) В, с последующим циклическим изменением потенциала (ЦВА) от -0,3 до 0,4 и обратно при 50÷100 мВ/с, сигнал меди регистрируют и оценивают методом добавки аттестованных растворов при анодной развертки ЦВА Еп(Cu) 0,22÷0,26 В, сигнал сурьмы и висмута регистрируют и оценивают методом добавки аттестованных растворов при катодной развертке потенциала ЦВА Eп(Sb) 0,0÷0,07, Eп(Bi) 0,11÷0,18 в форме первой производной dI/dE относительно насыщенного хлоридсеребряного электрода (нас.х.э).
| Бабич Г.А., Кисиль Е.П., Салихджанова Р.М.-Ф | |||
| Одновременное инверсионно-вольтамперометрическое определение Zn, Cd, Pb, Tl, Sb, Bi и Cu в воздухе | |||
| Заводская лаборатория | |||
| Диагностика материалов | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Kitamura Hudeki, Okawa Kazunobu, Kuge Yoshibo, Asada Shingo./ J | |||
| Chem | |||
| Soc | |||
| Jap., Chem | |||
| and Ind | |||
| Chem | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
2011-05-27—Публикация
2010-03-22—Подача