Изобретение относится к медицине и химико-фармацевтической промышленности, в частности к созданию, производству и применению препарата сердечно-сосудистого действия - триметазидина дигидрохлорида в форме таблеток, содержащих 20 мг или 35 мг действующего вещества.
Триметазидина дигидрохлорид имеет формулу:
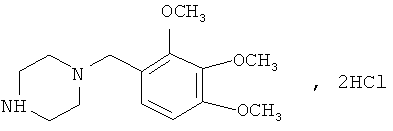
Триметазидина дигидрохлорид - белый микрокристаллический порошок, хорошо растворимый в воде (до 80%), и именно поэтому быстро усваивается организмом и поддерживает энергетический обмен в клетках, повышает уровень аденозинтрифосфата, защищая клетки от гипоксии. Триметазидина дигидрохлорид применяется для профилактики стенокардии, лечения ишемии, головокружения сосудистого происхождения.
Триметазидина дигидрохлорид как лекарственное вещество известен с 1966 года, но нет исследований относительно взаимного влияния кристаллических веществ на кристаллическую структуру композиции в таблетках. Известно, что изменение кристаллических свойств может привести к изменению биофармацевтических показателей препарата или может быть причиной осложнений технологического процесса [патент USA 3262852, 514/252.12, 514/929, 544/394, 1966].
При изготовлении таблеточной лекарственной формы используются различные вспомогательные вещества: наполнители, разрыхлители, скользящие вещества и другие вещества, часть которых является кристаллическими, а часть аморфными.
Известен следующий состав для изготовления таблеток триметазидина, мг:
[патент Франции №8020919, А61К 31/495, 3.09.1980].
В справочниках лекарственных препаратов Украины, России, Франции (Vidal 2006-2007, Компендиум 2007) остался такой же качественный, а в некоторых случаях количественный состав вспомогательных веществ для этого препарата. Такой же качественный состав имеют генерические препараты триметазидина дигидрохлорида, изготовляемые фармацевтическими предприятиями Украины.
Известно, что суточная доза триметазидина дигидрохлорида 60 мг должна быть раздроблена на трехразовое применение на сутки [FR 2490963, А61К 9/20, 04.02.1982].
Однако при этом не достигается равномерного высвобождения триметазидина дигидрохлорида на протяжении суток, особенно наименьшее его высвобождение перед утренним применением, а в это время чаще всего случаются критические моменты сердечной деятельности.
Поэтому созданы препараты с пролонгированным высвобождением действующего вещества.
Известна матриксная таблетка триметазидина дигидрохлорида на основе твердой матрицы. В составе используется маннитол как наполнитель для создания матрицы, а также применяется грануляция лекарственного и вспомогательного веществ и воска монтанового раствора эудрагита RS РО 100 [UA 12297, МПК А61К 31/495, 2006].
В этих таблетках кристаллические вещества имеют следующий состав от массы таблетки, мас.%:
Известна матриксная таблетка, в которой используются другие вспомогательные вещества: кальция дифосфат как наполнитель и гидроксипропилметилцеллюлоза как регулятор скорости растворения.
В этих таблетках кристаллические вещества имеют следующий состав: триметазидин - 17,5 мас.%, кальция дигидрофосфат - 40,45 мас.% от массы таблетки [UA 80087, МПК CD А61К 31/495].
Таким образом, промышленные способы приготовления таблеток триметазидина с различными формами высвобождения используют кристаллические наполнители (маннитол или кальция дифосфат, микрокристаллическую целлюлозу) и аморфные вещества для обеспечения механических свойств таблетки и разнообразных программ растворения. Аморфные вещества не имеют кристаллической структуры и не могут быть отдельно определены на дифрактограммах. Они могут суммарно проявляться в виде гало определенных размеров в отдельных диапазонах 2Θ°.
Ближайшим аналогом заявляемого изобретения является триметазидина дигидрохлорид, который имеет следующую кристаллическую структуру [UA №28550, C07D 209/00, 2007]
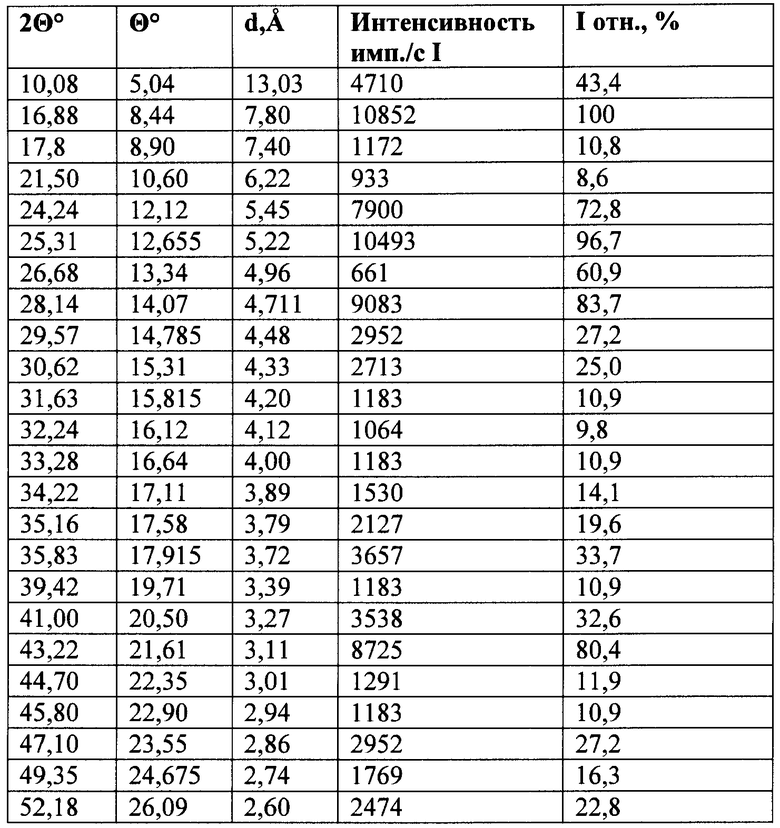
В этом патенте отмечено, что для более точной характеристики максимумов, определяющих наличие кристаллических структур с определенными межплоскостными расстояниями, было применено излучение 2,29Å. Однако большинство исследований применяют для этой цели излучения 1,5405Å, поэтому результаты трудно сравнивать. При таком режиме дифрактометр имеет более значительную инерционность и более вероятна возможность неопределения отдельных параметров дифрактограммы. В патенте нет информации относительно того, какие образцы субстанции изучались и была ли предварительная подготовка образцов, например перекристаллизация.
В основу изобретения поставлена задача определить кристаллическую структуру различных фиксированных доз триметазидина дигидрохлорида при использовании излучения 1,5405Å для определения качества лекарственного препарата в форме таблеток и возможности предупреждения фальсификации.
Поставленная задача решается тем, что в кристаллической структуре лекарственного препарата в форме таблеток, содержащем триметазидина дигидрохлорид в фиксированной лекарственной дозе, кристаллический наполнитель и вспомогательные вещества, согласно изобретению фиксированная доза триметазидина дигидрохлорида составляет 20 мг, в качестве кристаллического наполнителя используют маннитол, а лекарственный препарат имеет следующую кристаллическую структуру
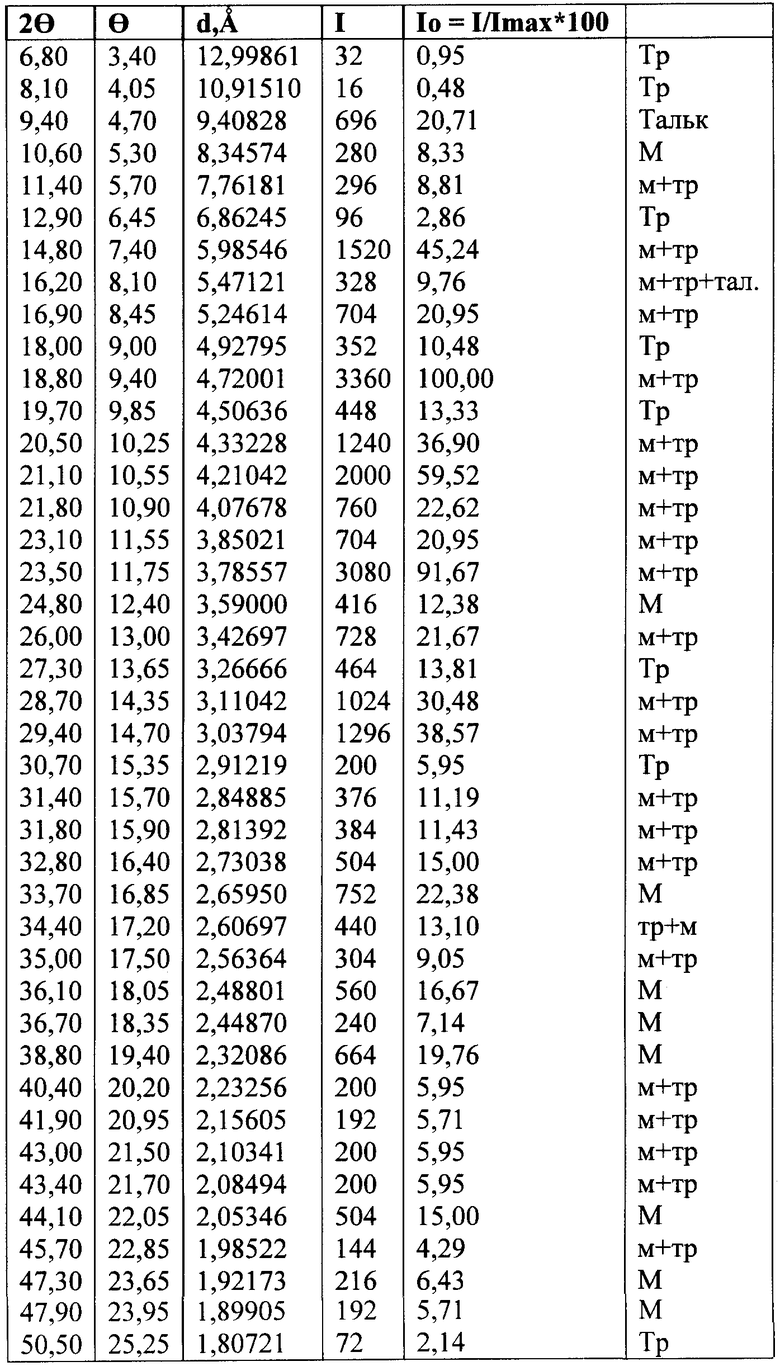
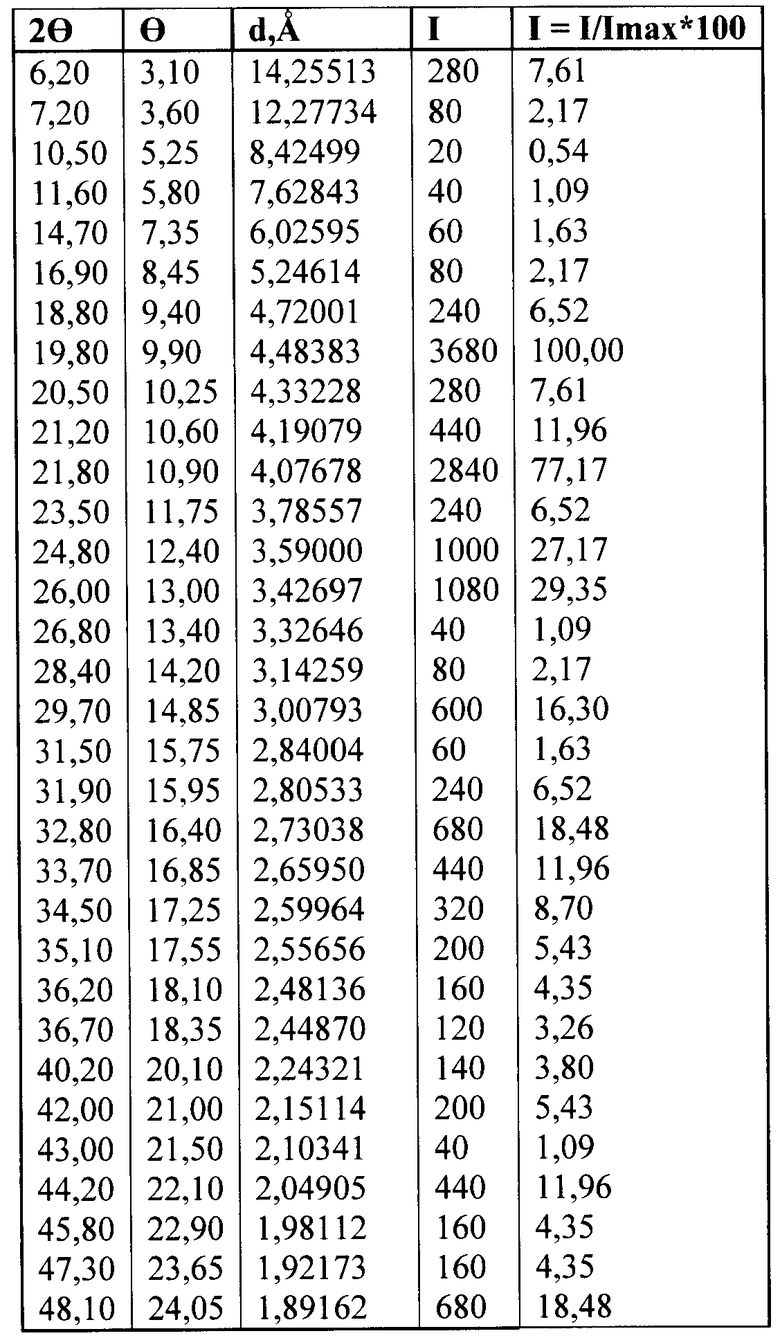
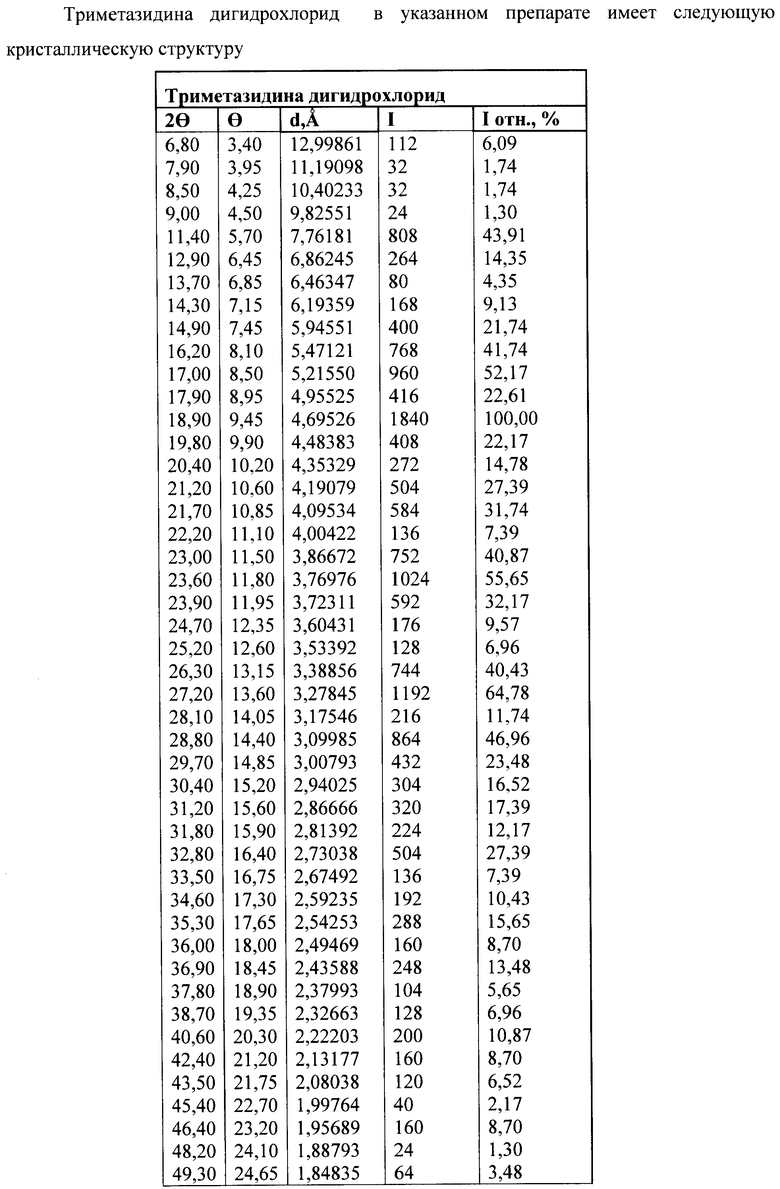
Триметазидина дигидрохлорид в указанном лекарственном препарате имеет следующую кристаллическую структуру
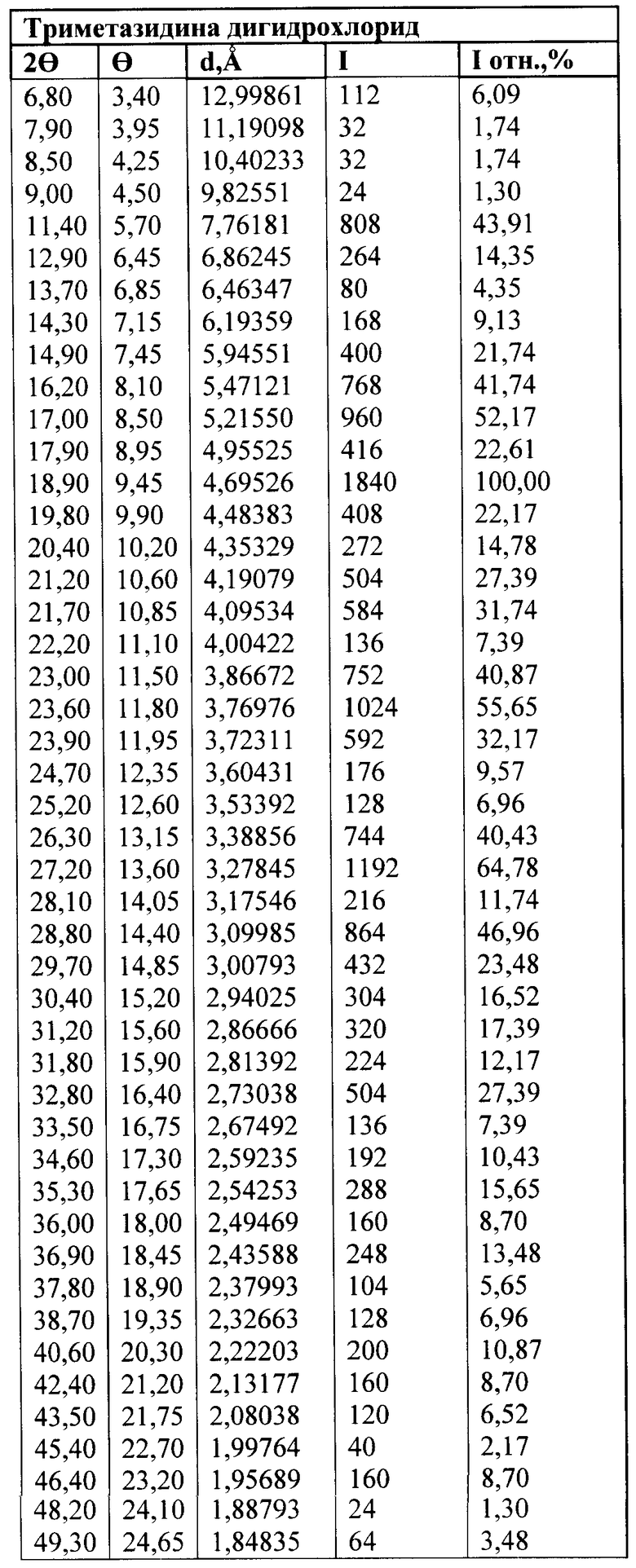
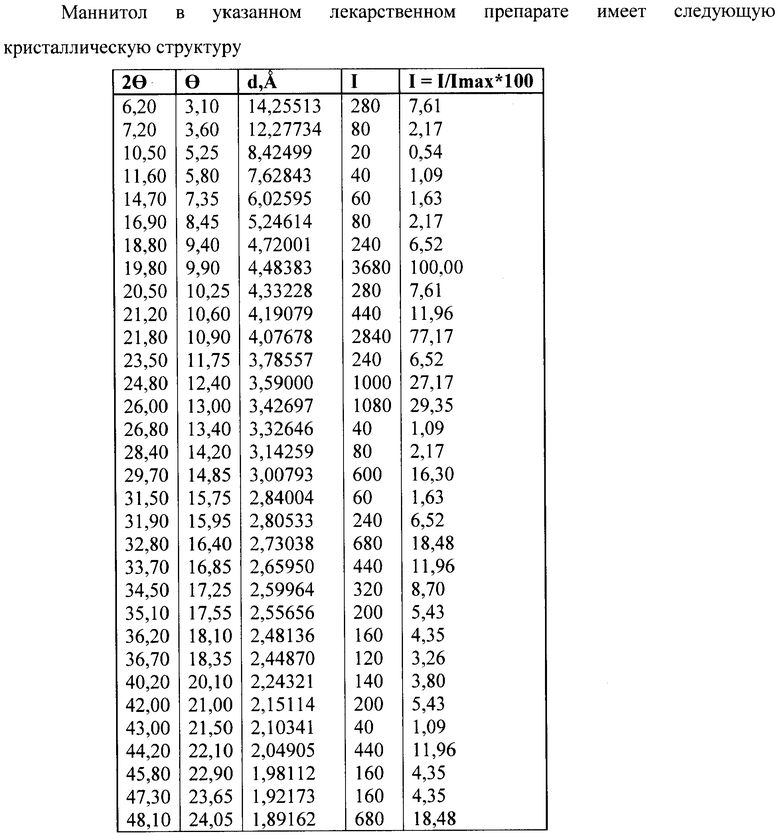
Маннитол в указанном лекарственном препарате имеет следующую кристаллическую структуру
Определенные независимо кристаллы триметазидина дигидрохлорида имеют следующие межплоскостные расстояния: d, Å=12,99, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81.
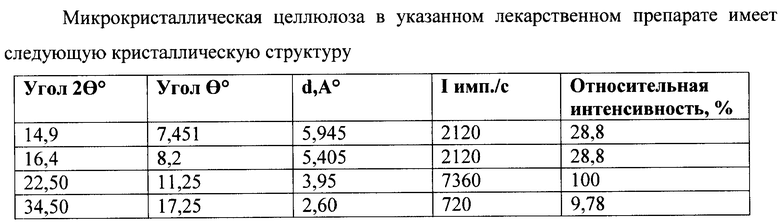
Поставленная задача решается также тем, что в лекарственном препарате в форме таблеток, содержащем триметазидина дигидрохлорид в фиксированной лекарственной дозе, кристаллический наполнитель и вспомогательные вещества, согласно изобретению фиксированная доза триметазидина дигидрохлорида составляет 35 мг, в качестве кристаллического наполнителя используют маннитол и микрокристаллическую целлюлозу, а лекарственный препарат имеет следующую кристаллическую структуру

Определенные независимо кристаллы триметазидина дигидрохлорида имеют следующие межплоскостные расстояния: d, Å=13,18, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81.
Кристаллическая структура ретардной формы триметазидина дигидрохлорида имеет дополнительную кристаллическую фазу с брегговским углом 2θ=25,4 и d=3,505.
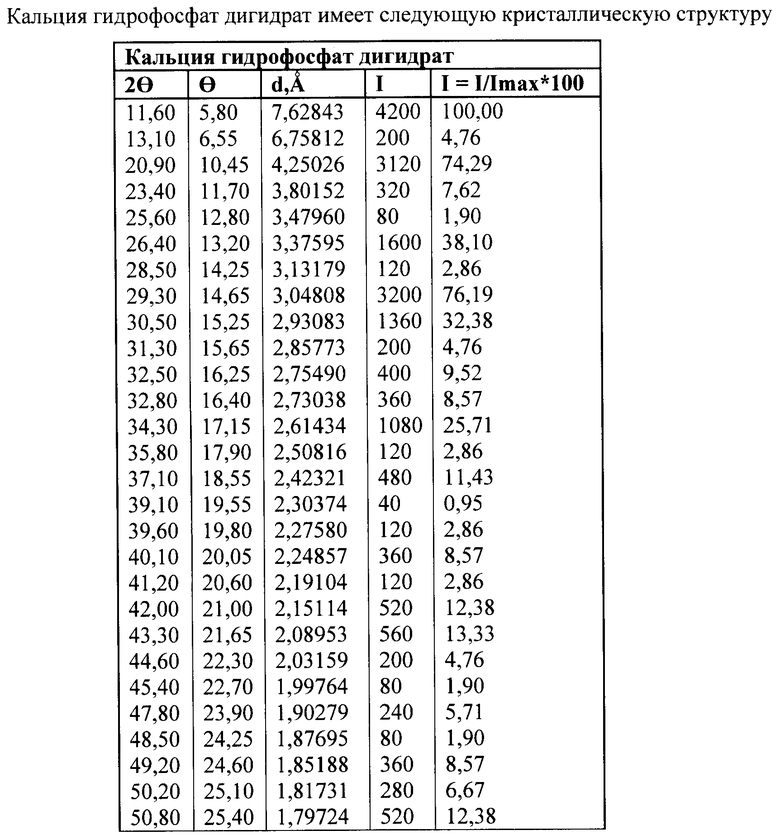
Поставленная задача решается еще тем, что в лекарственном препарате в форме таблеток, содержащем триметазидина дигидрохлорид в фиксированной лекарственной дозе, кристаллический наполнитель и вспомогательные вещества, согласно изобретению фиксированная доза триметазидина дигидрохлорида составляет 35 мг, в качестве кристаллического наполнителя используют кальция гидрофосфат дигидрат, а лекарственный препарат имеет следующую кристаллическую структуру
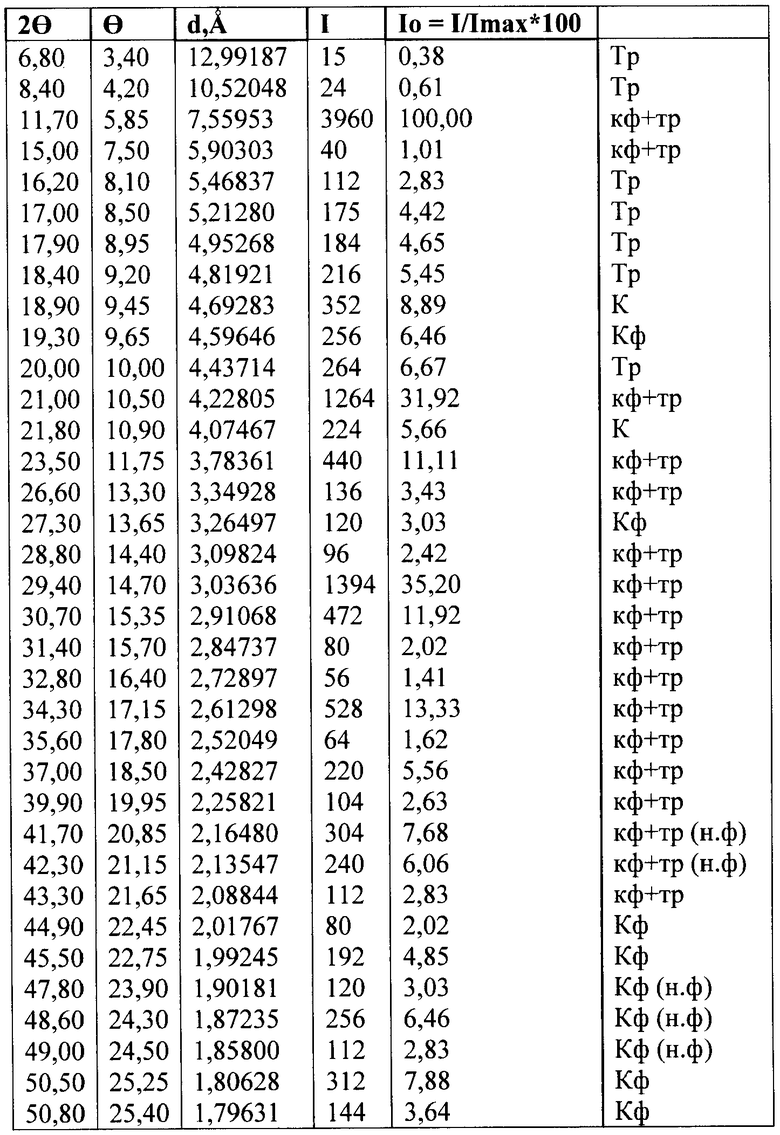
Определенные независимо кристаллы триметазидина дигидрохлорида имеют следующие межплоскостные расстояния: d, Å=12,99, 10,52, 5,47, 5,21, 4,95, 4,82, 4,38.
Определена кристаллическая структура различных фасованных доз триметазидина дигидрохлорида, позволяющая определять качество лекарственного препарата в форме таблеток и предупреждающая фальсификацию.
Исследования кристаллических структур различных образцов субстанции осуществляли в следующих условиях:
- дифрактометр ДРОН 3, сцинтилляционный детектор;
- медный антикатод λ=1,5405Å, напряжение 40 кВ, сила тока 40 мА;
- размещение θ-θ;
- диапазон измерений 5-40°;
- непрерывная регистрация на бумаге с уточнением положения путем точечной регистрации со временем измерения на этапе 10 с;
- прирост перед каждым измерением 0,02°.
Таким же методом получены кристаллические структуры запрессованных порошков триметазидина дигидрохлорида двух фирм - Sochinas (Швейцария) и Orgasynth (Франция), которые приведены в таблицах 1 и 2.
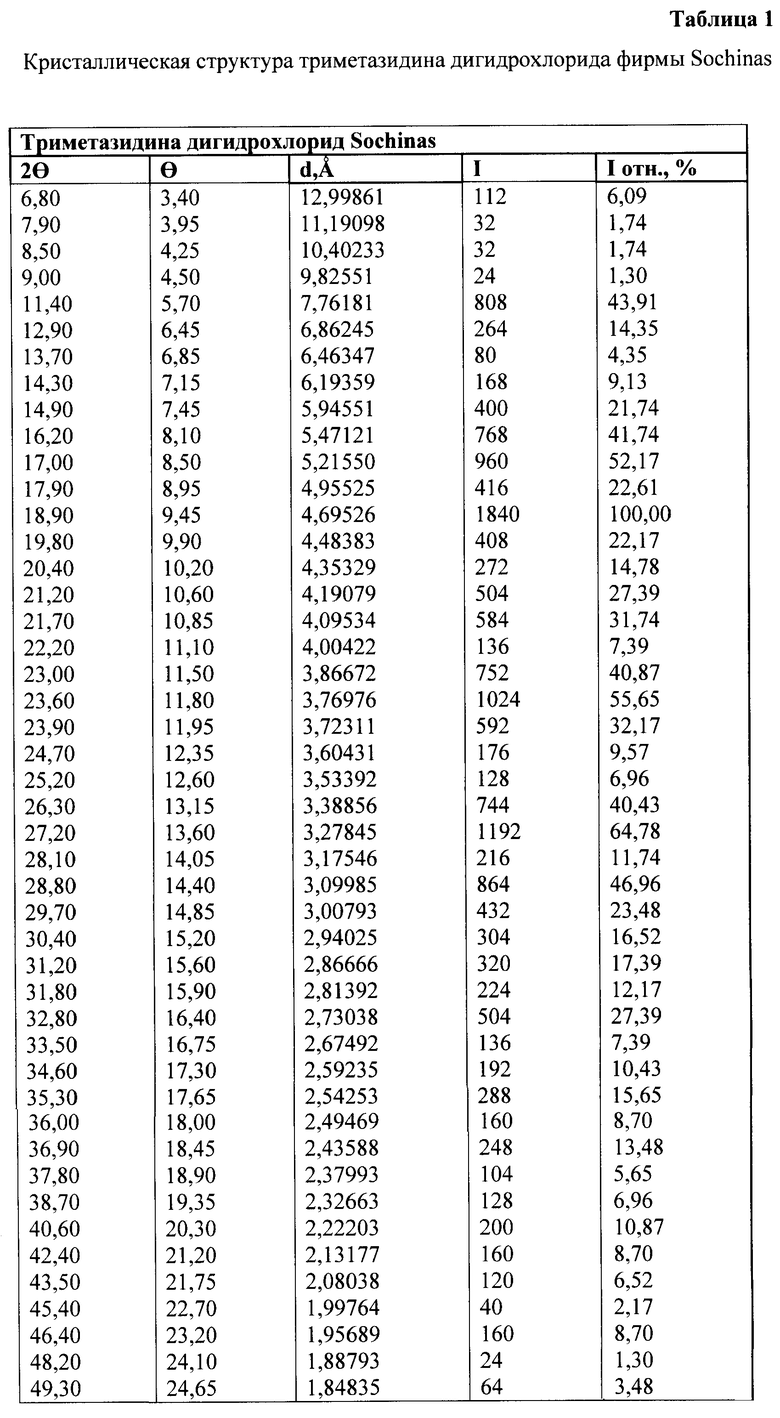
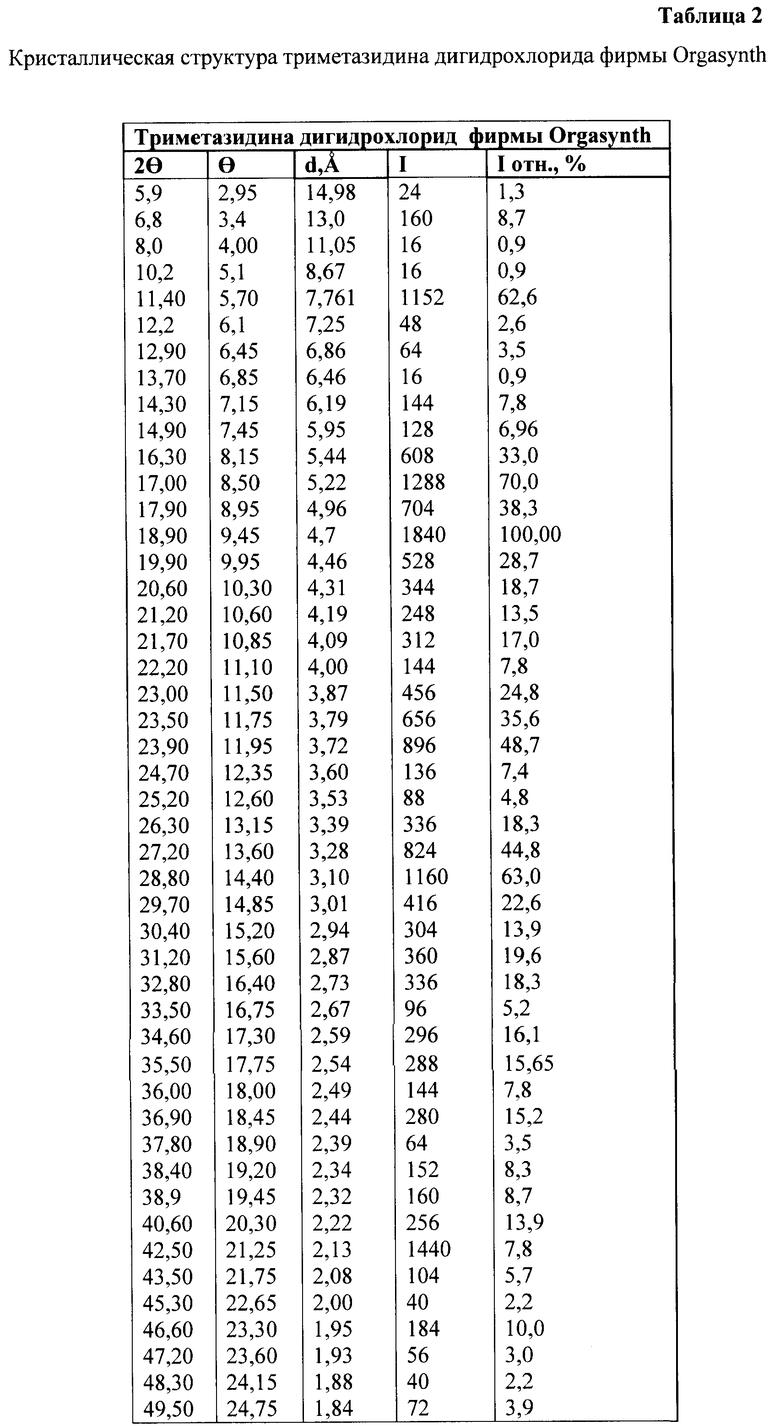
Сравнение таблиц показывает, что триметазидина дигидрохлорид не имеет полиморфизма.
Полученные данные могут быть основой для исследований, в которых структуры субстанции могут определять воспроизводимость технологического процесса и их влияние на физико-механические свойства таблетки.
При изготовлении лекарственных таблетированных форм использовали кристаллические вспомогательные вещества, имеющие другие кристалло-физические свойства. Кристаллические структуры этих вспомогательных веществ получены при тех же условиях эксперимента.
Микрокристаллическая целлюлоза чаще всего самостоятельно не воспроизводится в кристаллических структурах таблеток, а вместе с другими аморфными вспомогательными веществами влияет на высоту отдельных групп пиков над базовой линией дифрактограммы в некоторых диапазонах углов, отвечая положениям максимумов на дифрактограмме этого вспомогательного вещества.
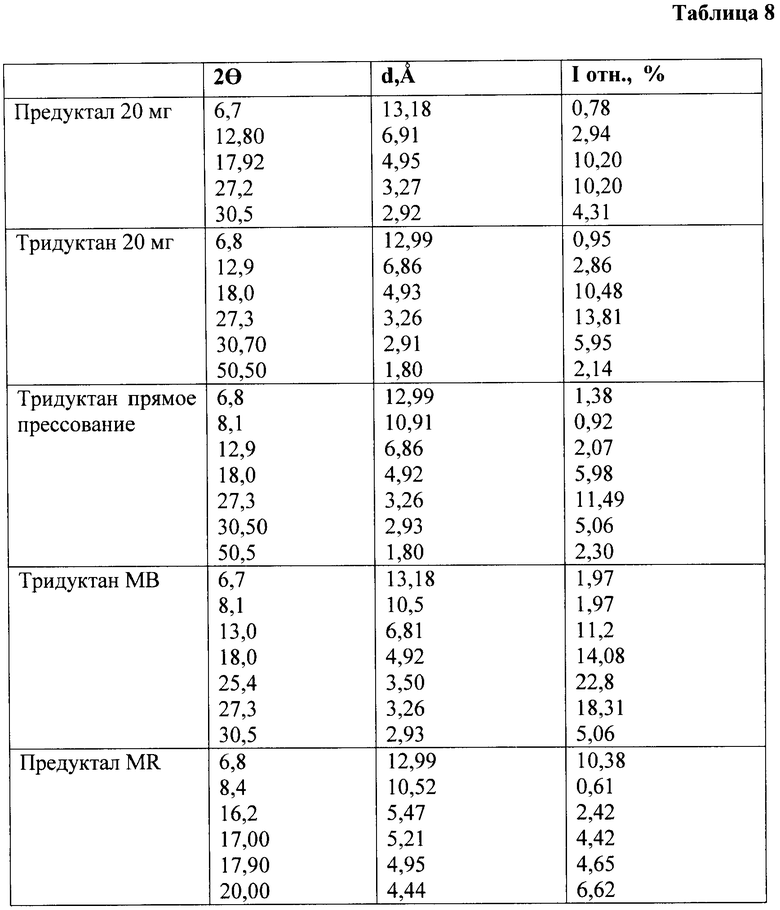
В таблице 3 приведена кристаллическая структура таблеток „Тридуктан 20 мг", которые изготовляются ОАО "Фарма Старт".
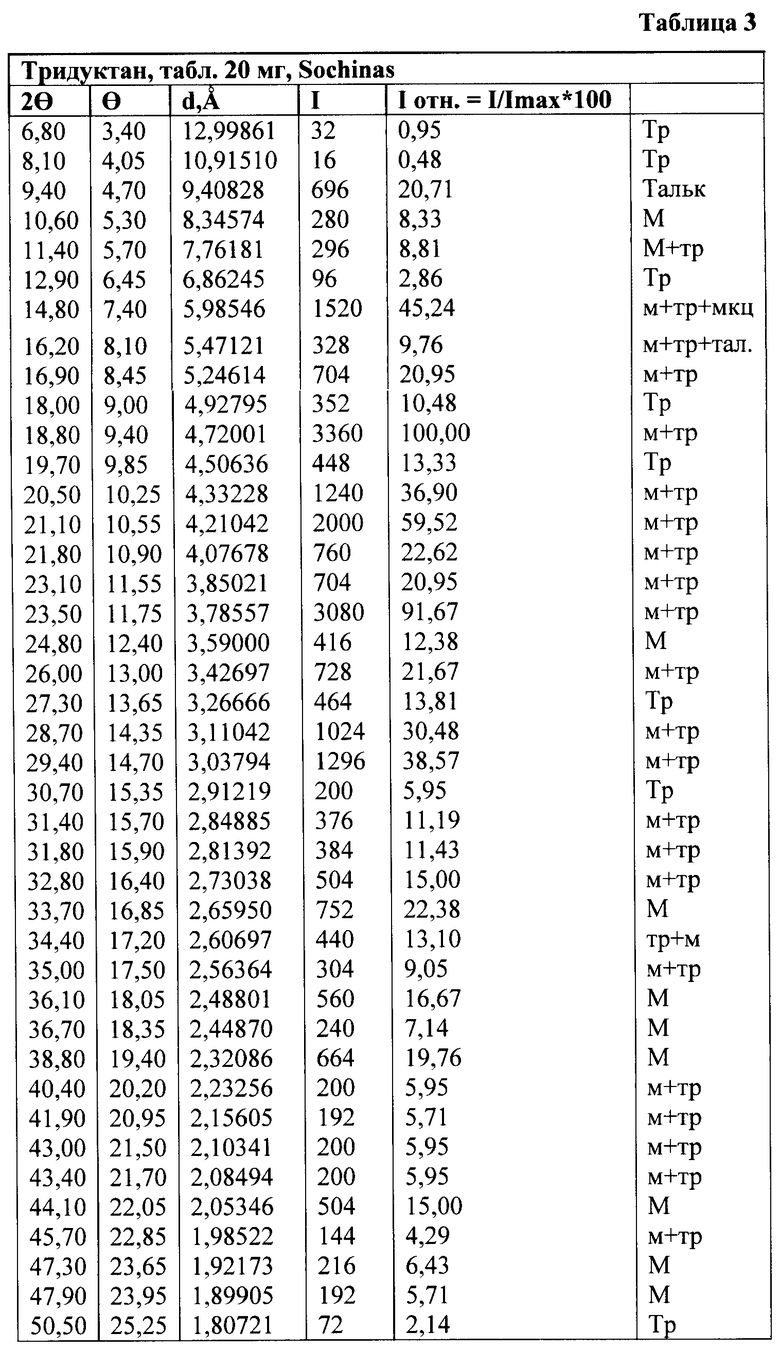
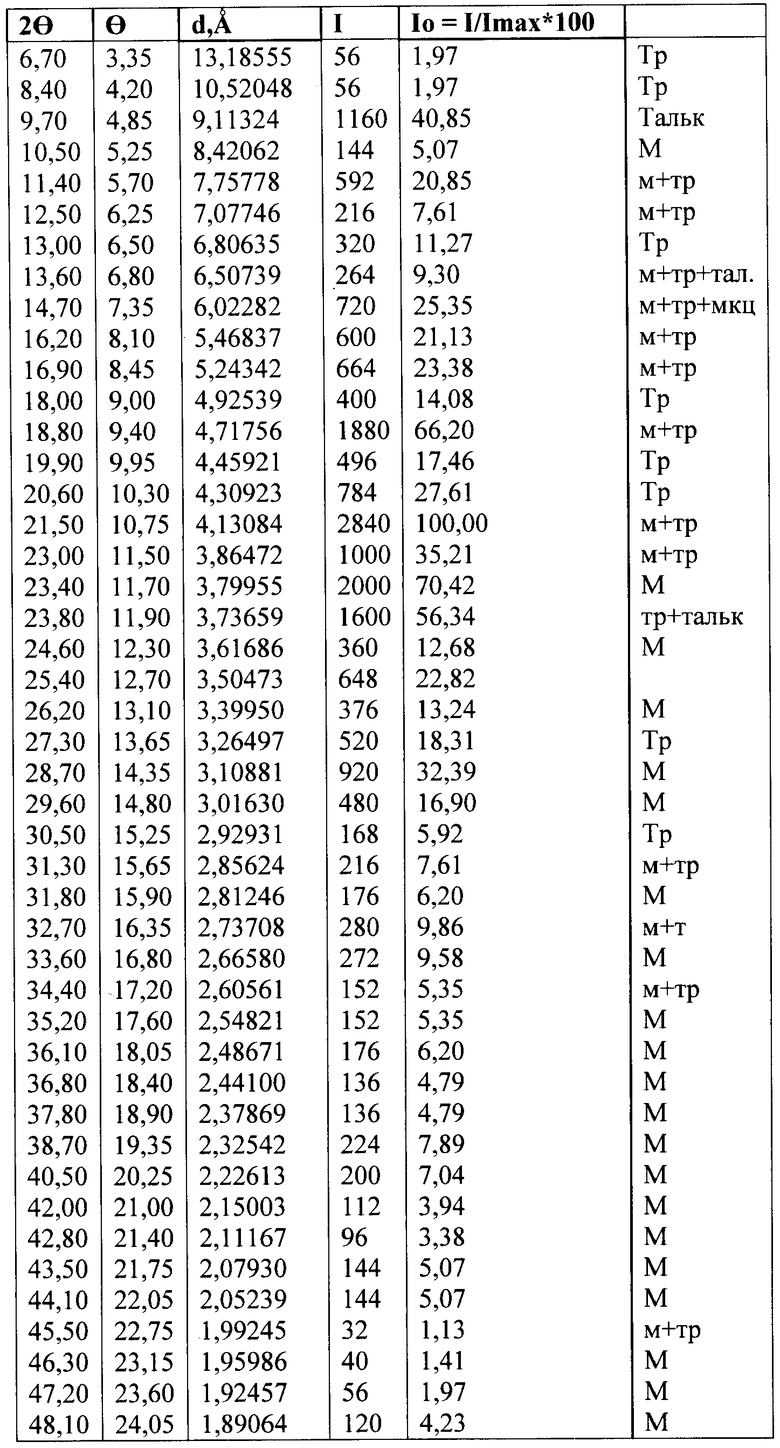
В таблице 4 приведена кристаллическая структура таблеток Предуктал фирмы SERVIER
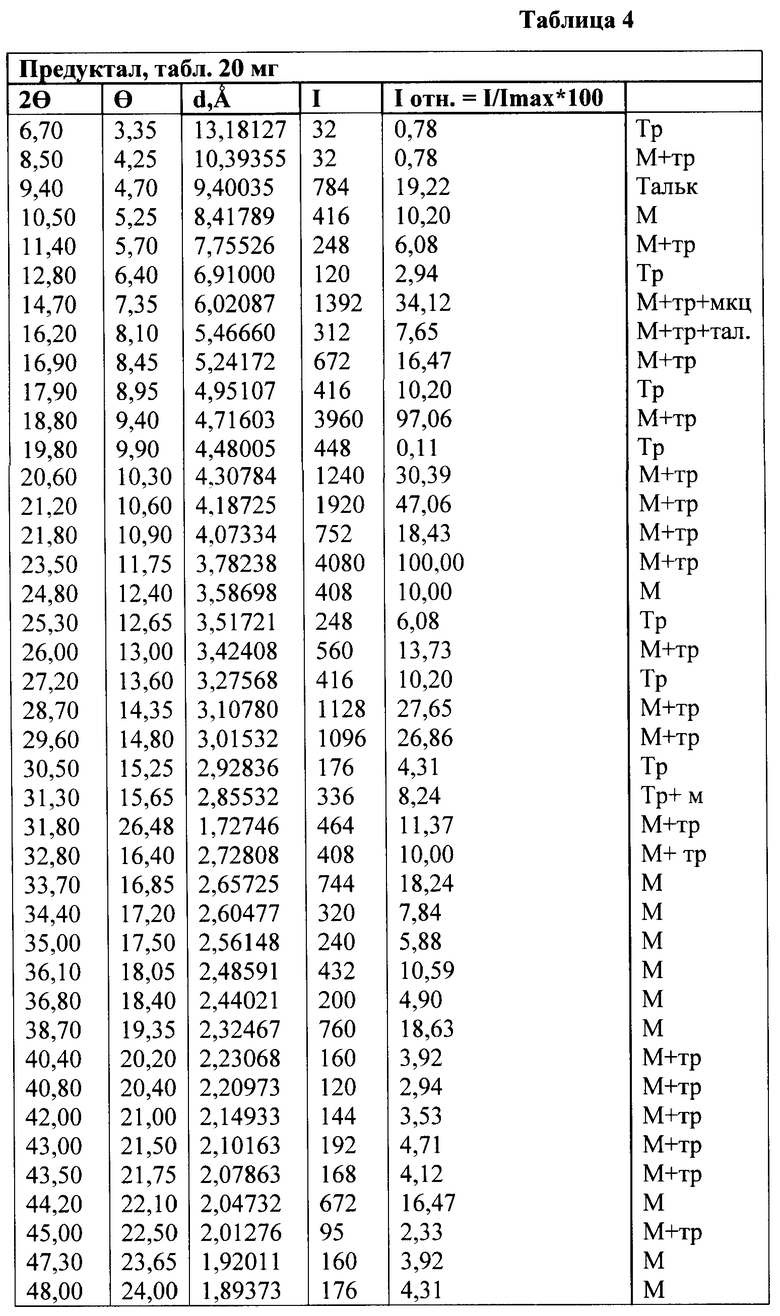
Оба препарата Предуктал SERVIER, Франция, и Тридуктан ОАО „Фарма Старт", Украина, изготовляются методом влажной грануляции при использовании раствора поливинилпирролидона. Несмотря на то что триметазидина дигидрохлорид не имеет полиморфных форм, массы для таблетирования во время грануляции поддаются воздействию повышенной температуры и влажности, что может быть причиной образования дополнительных структурных фаз. Поэтому были изготовлены таблетки методом прямого прессования, кристаллическая структура которых приведена в следующей таблице 5.
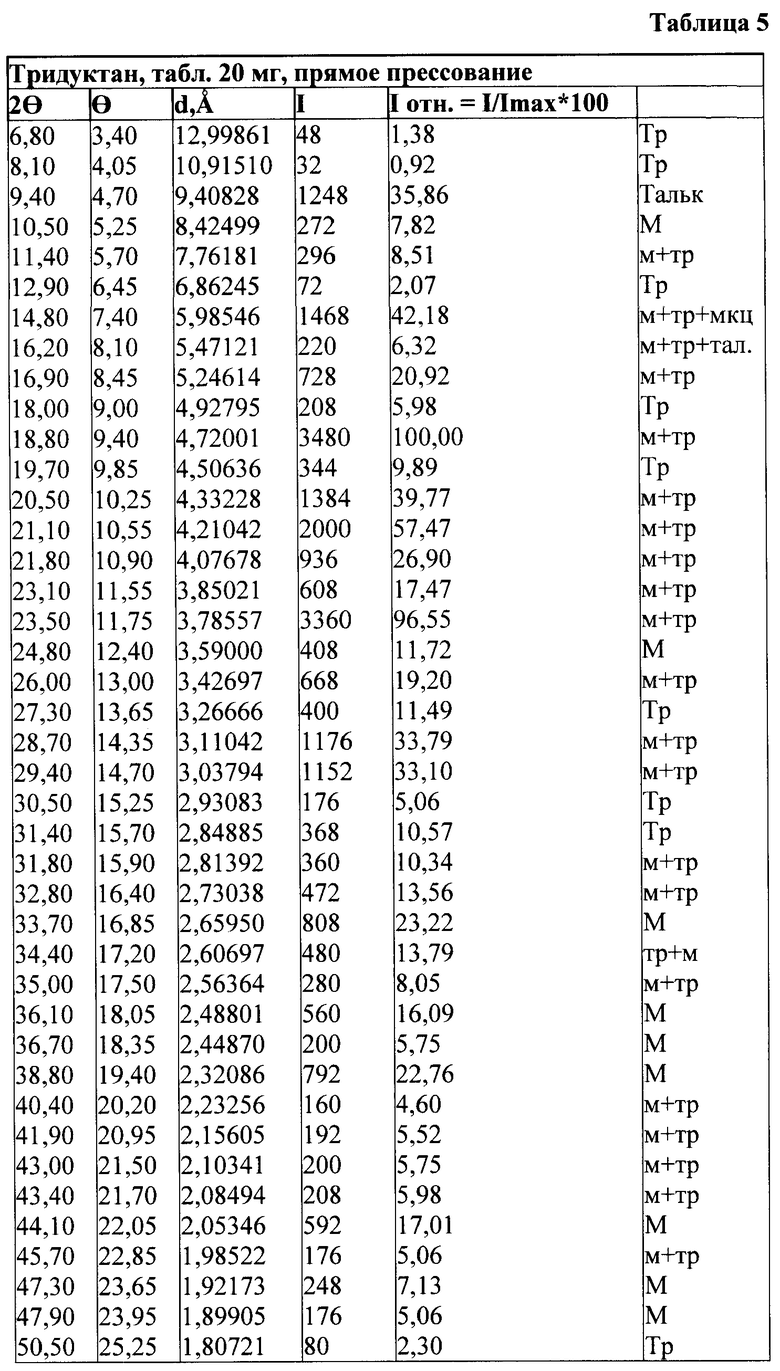
Маннитол как вспомогательное вещество используют также в твердой матрице для ретардной формы триметазидина дигидрохлорида [патент UA 12297, А61К 31/495, 2006]. Таблетки Тридуктан MB имеют следующее содержимое: действующее вещество триметазидина дигидрохлорида в количестве 15-30 мас.%, преимущественно 17,5-25 мас.% от массы таблетки - ядра, микрокристаллическая целлюлоза в количестве 10-17%, предпочтительно 12-14 мас.% от массы таблетки - ядра, полиметакрилат, который независимо от РН медленно пропускает водные растворы, в количестве 18-27 мас.%, предпочтительно 20-26 мас.% от массы таблетки, как гидрофобные полимеры используются различные виды восков в количестве 20-31 мас.% общей массы таблетки - ядра. Кристаллическая структура этого препарата приведена в таблице 6.
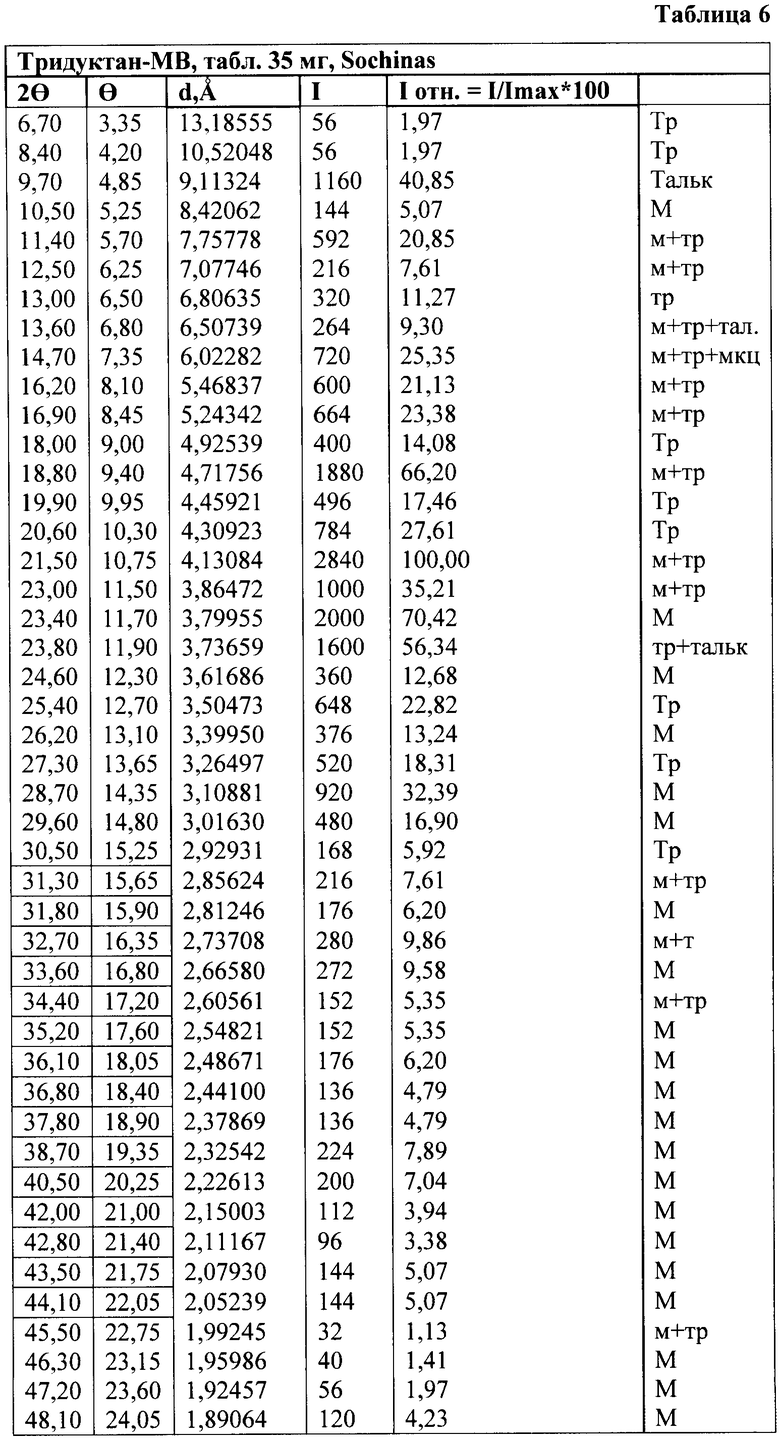
В препарате фирмы SERVIER Предуктал MR другое вспомогательное кристаллическое вещество, и кристаллическая структура имеет значения, приведенные в таблице 7.
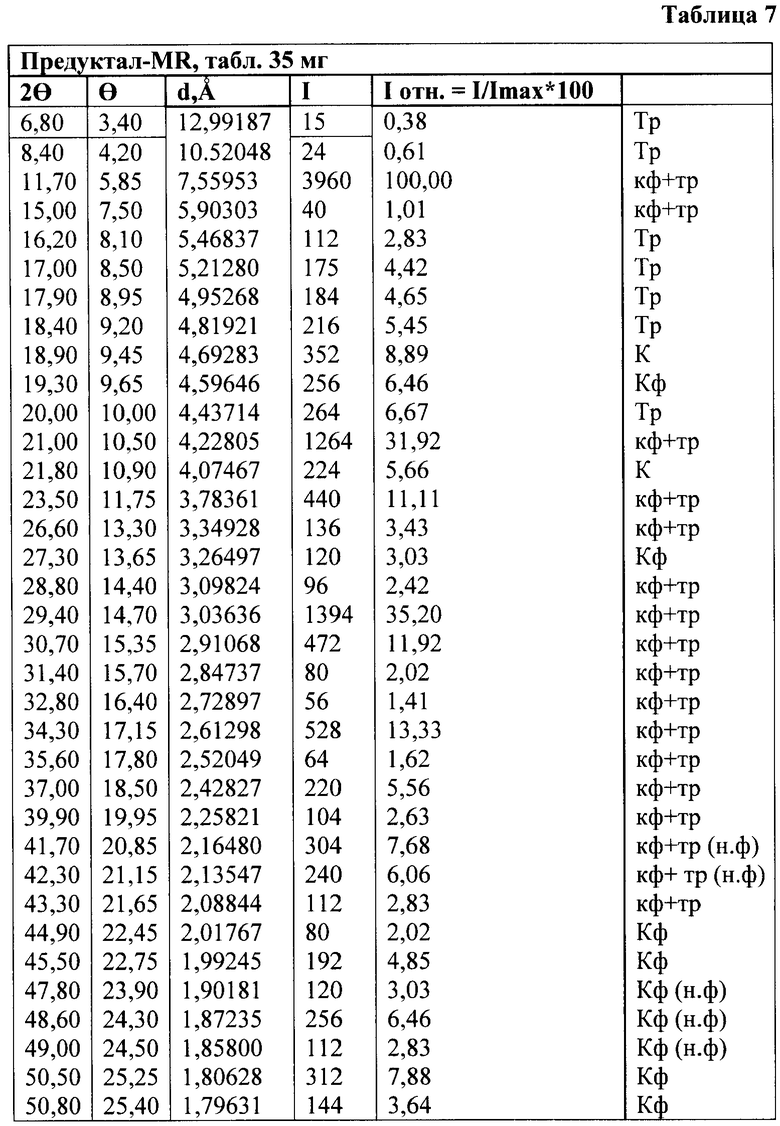
В этой кристаллической структуре появляются некоторые отличия от смесей компонентов, образующих таблетку. Во-первых, максимальное значение интенсивности определяется в таблетках при другом угле излучения, чем в отдельных компонентах; во-вторых, относительные значения интенсивностей триметазидина дигидрохлорида значительно ниже, чем для суммы ингредиентов триметазидина дигидрохлорида и кальция гидрофосфата дигидрата.
Анализ приведенных кристаллических структур показывает, что триметазидина дигидрохлорид независимо воспроизводится в препаратах при следующих условиях
В кристаллической структуре тридуктана MB появляется новое значение для независимого воспроизведения действующего вещества, имеющего значительную относительную интенсивность, и может быть показателем отличия данного препарата от препаратов разового действия. Этот результат может быть доказательством того, что в этой системной матрице существуют новые кристаллические фазы.
Важное значение имеет возможность прогнозирования растворения таблеток триметазидина дигидрохлорида по результатам рентгеноструктурного анализа для создания методов неразрушающего контроля для предупреждения фальсификации препарата и для прогнозирования качества таблеток в критических зонах технологического режима. Такое решение стало возможным за счет анализа интенсивности излучения. Для различных видов таблеток триметазидина гидрохлорида существуют следующие требования растворения: для таблеток по 20 мг за 45 минут должно перейти в раствор не менее чем 75% триметазидина. Для таблеток пролонгированного действия „ретард" по 35 мг в раствор должно перейти: за 1 час - 25-45%, за 2 часа - 43-63%, за 8 часов - не менее чем 80%.
Анализ максимальных значений относительной интенсивности показывает, что для таблеток с растворением до 45 мин соответствуют величины 2θ=18,8° с d=4,72Å, 2θ=21,5° с d=4,2lÅ, 2θ=23,5° с d=3,80Å. При этих координатах одновременно определяется триметазизидина дигидрохлорид, маннитол, целлюлоза микрокристаллическая. При этом не обязательно условия наличия в этих значениях максимальных значений компонентов. Для таблеток пролонгированного действия, содержащих как наполнитель маннитол, точки максимальных значений относительной интенсивности также соответствуют одновременному наличию всех трех кристаллических компонентов 2θ=18,8° с d=4,72Å, 2θ=21,5° с d=4,13Å, 2θ=23,5° с d=3,8Å. Наличие не самых больших интенсивностей у триметазидина дигидрохлорида при 2θ=21,2-27,4% и 2θ=21,7-31,7%, у маннитола при 2θ=21,2-11,96% и 2θ=21,8-77,17% приведено к изменению угла 2θ=21,5° и максимальному значению интенсивности 100%.
Эти изменения и наличие новой точки 2θ=25,4° характеризуют пролонгированную лекарственную форму триметазидина дигидрохлорида и соответствующую этой форме программу растворения в таблетках Предуктал MR. В таблетках Предуктал MR также проявляется дополнительное значение 2θ=41,7-d=2,16480% I отн.=7,68.
Проведение исследований показывает для препаратов ретардного действия, что брегговский угол 2θ максимального значения относительной интенсивности отличается от брегговского угла 2θ максимального значения относительной интенсивности субстанции триметазидина. В таблетках разового действия брегговский угол 2θ максимального значения относительной интенсивности таблеток и субстанции совпадают.
Значение интенсивностей триметазидина дигидрохлорида в вышеприведенных кристаллических структурах для таблеток, изготовленных из одной субстанции и вспомогательных веществ, приведены в таблице 9.
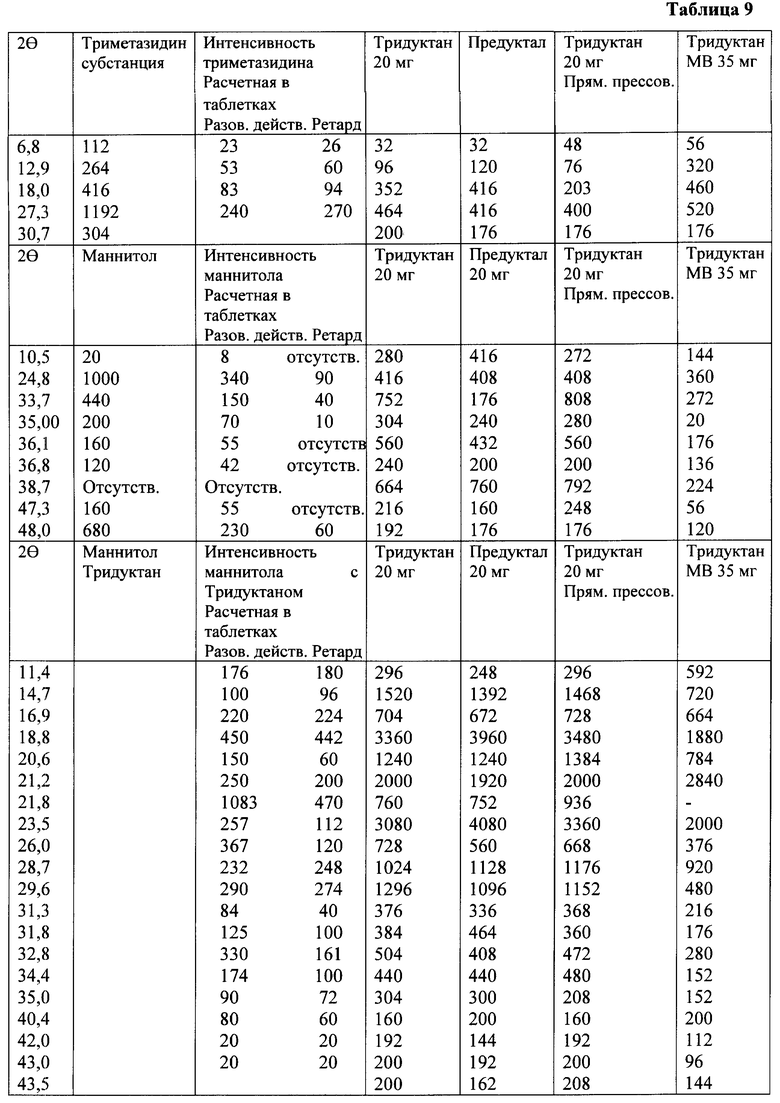
Доза триметазидина дигидрохлорида в таблетках разового действия равна 20% и 22,5%, то есть интенсивность в таблетках разового действия в 1,5-2,0 раза превышает теоретическое значение интенсивности, а в таблетках ретардного действия - в 2,5-3,0 раза выше. В таблетках Предуктал MR, в которых используется кальция гидрофосфат дигидрат, значения интенсивности значительно ниже, чем теоретические.
Анализ интенсивностей маннитола, приведенный в таблице 8, показывает, что их значения в таблетках значительно более высоки, чем в самом маннитоле, запрессованном в таблетку отдельно, без других компонентов. Если принять во внимание интенсивность излучения, рассчитанную на количество маннитола в таблетке, то такой эффект наблюдается для большинства брегговских углов маннитола, кроме 2θ=480. Но в ретардной форме интенсивность маннитола значительно меньше, чем в препаратах разового действия, причем интенсивность в таблетках, полученных прямым прессованием, не отличается от таблеток, полученных влажной грануляцией. То есть частичное растворение, механические влияния, затем сушка не влияют на распределение кристаллических фаз.
Фазы, содержащие кристаллы триметазидина и маннитола с одинаковыми межплоскостными расстояниями и объединяющиеся в таблетках, тоже имеют интенсивности значительно выше, чем можно ожидать из правила аддитивности. В ретардном препарате интенсивности для этих фаз меньше, чем для препаратов разового действия, кроме фазы с 2θ=11,4. Кроме того, в ретардном препарате появляется новая кристаллическая фаза, которая существует только в препарате с маннитолом при 2θ=25,4, для Предуктала MR, где используется кальция дифосфат, дополнительная фаза при 2θ=41,7 c d=2,1648Å.
Проведенный анализ свидетельствует, что образованные в таблетках триметазидина дигидрохлорида структуры являются самостоятельными структурами действующего вещества с кристаллическими вспомогательными веществами. Эти структуры можно использовать для контроля за производством, прогнозирования растворимости действующего вещества и неразрушающего контроля для предупреждения фальсификации.
Способ определения кристаллической структуры лекарственного препарата триметазидина в форме таблеток, содержащего триметазидина дигидрохлорид, кристаллический наполнитель и вспомогательные вещества, заключается в том, что определение кристаллической структуры производят дифрактометром ДРОН 3 с медным антикатодом при излучении λ=1,5405Å, напряжении 40 кВ и силе тока 40 мА для таблеток с фиксированной дозой триметазидина дигидрохлорида 20 мг при использовании в качестве кристаллического наполнителя маннитола, для таблеток с фиксированной дозой триметазидина дигидрохлорида 35 мг при использовании в качестве кристаллического наполнителя маннитола или кальция гидрофосфата дигидрата. Измеренные кристаллические структуры можно использовать для контроля за производством, прогнозирования растворимости действующего вещества и качества таблеток препарата. 3 н. и 12 з.п. ф-лы, 9 табл.
1. Способ определения кристаллической структуры лекарственного препарата триметазидина в форме таблеток, содержащего триметазидина дигидрохлорид, кристаллический наполнитель и вспомогательные вещества, с применением излучения, отличающийся тем, что определение кристаллической структуры производят дифрактометром ДРОН 3 с медным антикатодом при излучении λ=1,5405Å, напряжении 40 кВ и силе тока 40 мА для таблеток с фиксированной дозой триметазидина дигидрохлорида 20 мг при использовании в качестве кристаллического наполнителя маннитола, получая при этом следующую кристаллическую структуру
2. Способ по п.1, отличающийся тем, что используют субстанцию триметазидина дигидрохлорид следующей кристаллической структуры
3. Способ по п.1, отличающийся тем, что используют маннитол следующей кристаллической структуры
4. Способ по п.1, отличающийся тем, что в нем независимо определяют триметазидина дигидрохлорид при следующих межплоскостных расстояниях d, Å =12,99, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81.
5. Способ по п.1, отличающийся тем, что используют микрокристаллическую целлюлозу следующей кристаллической структуры
6. Способ определения кристаллической структуры лекарственного препарата триметазидина в форме таблеток, содержащего триметазидина дигидрохлорид, кристаллический наполнитель и вспомогательные вещества, с применением излучения, отличающийся тем, что определение кристаллической структуры производят дифрактометром ДРОН 3 с медным антикатодом при излучении λ=1,5405Å, напряжении 40 кВ и силе тока 40 мА для таблеток с фиксированной дозой триметазидина дигидрохлорида 35 мг при использовании в качестве кристаллического наполнителя маннитола, получая при этом следующую кристаллическую структуру
7. Способ по п.6, отличающийся тем, что используют субстанцию триметазидина дигидрохлорид следующей кристаллической структуры
8. Способ по п.6, отличающийся тем, что используют маннитол следующей кристаллической структуры
9. Способ по п.6, отличающийся тем, что используют микрокристаллическую целлюлозу следующей кристаллической структуры
10. Способ по п.6, отличающийся тем, что в нем независимо определяется триметазидина дигидрохлорид при следующих межплоскостных расстояниях d, Å=12,99, 10,52, 6,86, 4,93, 3,27, 2,91, 1,81.
11. Способ по п.6, отличающийся тем, что имеет дополнительную кристаллическую фазу с бреговским углом 2θ=25,4 и d=3,505.
12. Способ определения кристаллической структуры лекарственного препарата триметазидина в форме таблеток, содержащего триметазидина дигидрохлорид, кристаллический наполнитель и вспомогательные вещества, с применением излучения, отличающийся тем, что определение кристаллической структуры производят дифрактометром ДРОН 3 с медным антикатодом при излучении λ=1,5405Å, напряжении 40 кВ и силе тока 40 мА для таблеток с фиксированной дозой триметазидина дигидрохлорида 35 мг при использовании в качестве кристаллического наполнителя кальция гидрофосфат дигидрата, получая следующую кристаллическую структуру
13. Способ по п.12, отличающийся тем, что используют субстанцию триметазидина дигидрохлорид следующей кристаллической структуры
14. Способ по п.12, отличающийся тем, что используют кальция гидрофосфат дигидрат следующей кристаллической структуры
15. Способ по п.12, отличающийся тем, что в нем независимо определяют триметазидина дигидрохлорид при следующих межплоскостных расстояниях d, Å=12,99, 10,52, 5,47, 5,21, 4,95, 4,82, 4,38.
| RU 2006122367 A, 10.01.2008 | |||
| Счетная машина | 1927 |
|
SU12297A1 |
| ЛЕКАРСТВЕННАЯ ФОРМА, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2003 |
|
RU2260431C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2005 |
|
RU2281772C1 |
| Центробежный эмульгатор | 1934 |
|
SU40963A1 |
| Устройство для регулирования давления газов в сборных камерах при электролизе воды под давлением | 1932 |
|
SU40964A1 |
| Устройство для питания водой паровых котлов | 1933 |
|
SU41523A1 |
Авторы
Даты
2011-06-10—Публикация
2009-01-11—Подача