Изобретение относится к фармацевтической промышленности, а именно к лекарственной форме триметазидина дигидрохлорида с модифицированным высвобождением в виде таблетки для перорального приема.
1-[(2,3,4-Триметоксифенил)метил]пиперазин (триметазидин) в виде дигидрохлорида применяют в современной медицине при хориоретинальных сосудистые нарушениях, головокружениях сосудистого происхождения, головокружениях при болезни Меньера, шуме в ушах, в комплексной терапии стенокардии и ишемической болезни сердца.
Известны различные виды таблетированных форм триметазидина дигидрохлорида: обычные таблетки обеспечивают быстрое разовое высвобождение, таблетки с модифицированным высвобождением (данный термин является синонимом других терминов, которыми определяют характер высвобождения активного вещества из таблетки: замедленное, контролируемое, регулируемое, пролонгированное) обеспечивают длительное дозированное высвобождение активного вещества. По сравнению с обычными таблетками таблетки с модифицированным высвобождением для пациентов обладают рядом преимуществ: уменьшается частота приема, появляется возможность уменьшения курсовой дозы и, как следствие, уменьшаются раздражающее действие на желудочно-кишечный тракт и возможность проявления побочных эффектов. К каждой из форм подбирают определенные вспомогательные компоненты, которые обеспечивают различные технологические свойства таблеткам, конкретный режим и скорость высвобождения триметазидина дигидрохлорида.
Известны фармацевтические композиции триметазидина для пролонгированного высвобождения.
Известна лекарственная форма, обладающая антиангинальным действием, состоящая из ядра, содержащего в качестве активного вещества триметазидина дигидрохлорид и в качестве вспомогательных веществ кальций фосфат дигидрат, магний стеариновокислый, гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, натрия альгинат и тальк, и оболочки, нанесенной на ядро, содержащей твин-80, один компонент, выбранный из группы, включающей гидроксипропилметилцеллюлозу, метилцеллюлозу водорастворимую и гидроксипропилцеллюлозу, а также двуокись титана пигментную и железа оксид красный (РФ 2281772 С1, 20.08.2006).
Присутствие в составе ядра гидроксипропилцеллюлозы и гидроксиэтилцеллюлозы, имеющих малую насыпную плотность, существенно уменьшает сыпучесть и прессуемость таблеток, что усложняет технологический процесс.
В настоящее время одним из лучших лекарственных средств для лечения стенокардии, ишемической болезни сердца считается ПРЕДУКТАЛ MB от Сервье, Франция. Согласно информации с сайта Федерального государственного учреждения «Научный центр экспертизы средств медицинского применения» Федеральной службы по надзору в сфере здравоохранения и социального развития (ФГУ НЦЭСМП), страница с адресом из Реестра зарегистрированных лекарственных средств http://www.rlsnet.ru/prep_index_id_70434.htm, таблетки покрыты оболочкой и содержат 35 мг триметазидина дигидрохлорида и вспомогательные вещества: кальция гидрофосфата дигидрат, повидон, магния стеарат, кремния диоксид коллоидный безводный, титана диоксид (Е171), железа оксид красный (Е172), глицерол, макрогол, гипромеллозу (гидроксипропилметилцеллюлоза).
Данное лекарственное средство соответствует техническому решению, защищенному патентом ЕА008223 В1, опубл. 27.04.2007, патентообладатель - ЛЕ ЛАБОРАТУАР СЕРВЬЕ, Франция. В патенте описана таблетка для пролонгированного высвобождения триметазидина, где пролонгированное высвобождение контролируют с использованием гидроксипропилметилцеллюлозы, содержащейся в матрице. Гидроксипропилметилцеллюлоза, производное целлюлозы, является водорастворимым полимером.
Но также известна нормативная документация (НД 42-1623-05) на препарат ПРЕДУКТАЛ MB заявителя «Лаборатории Сервье», Франция. Согласно НД пролонгированное высвобождение контролируют с использованием гидроксиэтилцеллюлозы, которая является водонерастворимым полимером. При подаче документов на экспертизу в Федеральное государственное учреждение «Научный центр экспертизы средств медицинского применения» Федеральной службы по надзору в сфере здравоохранения и социального развития (ФГУ НЦЭСМП) для последующей регистрации лекарственного средства Триметазидина дигидрохлорид с модифицированным высвобождением препарат ПРЕДУКТАЛ MB был выбран ЗАО «ВЕРТЕКС» в качестве препарата сравнения. Экспертиза ФГУ НЦЭСМП проводит сравнение составов и свойств поданного на регистрацию лекарственного средства по показателям, приведенным в НД уже зарегистрированного препарата. Поэтому и в качестве наиболее близкого аналога заявленного изобретения - прототипа, выбран состав препарата ПРЕДУКТАЛ MB, описанный в НД 42-1623-05.
Присутствие в составе ядра как гидроксипропилметилцеллюлозы, так и гидроксиэтилцеллюлозы, имеющих малую насыпную плотность (0,3 и 0,35 г/см3 соответственно), уменьшает сыпучесть и прессуемость таблеток, что несколько усложняет технологический процесс приготовления таблетированной формы.
Задача, на решение которой направлено изобретение, состоит в расширении ассортимента качественных доступных отечественных лекарственных средств с модифицированным высвобождением.
Поставленная задача достигается путем разработки новой лекарственной формы на основе триметазидина дигидрохлорида с модифицированным высвобождением в виде таблетки для перорального приема. Таблетка содержит эффективное количество действующего вещества, смесь повидона и поливинилацетата в качестве модификатора высвобождения и фармацевтически приемлемые вспомогательные вещества.
Известно, что эффективное количество триметазидина дигидрохлорида в таблетках с модифицированным высвобождением составляет 35 мг (см., например, Реестр зарегистрированных лекарственных средств на сайте ФГУ НЦЭСМП, страница с адресом http://www.regmed.ru/InstrShow2.asp?InstrLinkNx=a59ba59ba54ba59b).
Очевидно, что кинетика высвобождения активного вещества из таблеток зависит от модификатора высвобождения. Как оказалось, смесь повидона и поливинилацетата является подходящим модификатором высвобождения для триметазидина дигидрохлорида. Повидон является водорастворимым полимером, а поливинилацетат - водонерастворимым. Ранее данная смесь в таблетках триметазидина дигидрохлорида с модифицированным высвобождением не использовалась. В качестве смеси повидона и поливинилацетата возможно использование Коллидона SR, свойства которого описаны в V. Buhler, Kollidon®, Polyvinylpyrrolidone for the pharmaceutical industry (Поливинилпирролидон для фармацевтической промышленности), 233-249, BASF, Ludwigshafen, 2001. Коллидон SR на 80% состоит из поливинилацетата и на 19% из повидона.
При погружении таблетки в воду водорастворимый полимер растворяется, образуются каналы, которые способствуют выходу активного ингредиента. Водонерастворимый полимер набухает, образуя гелеобразующий слой, через который постепенно выходит действующее вещество. Тем самым регулируется скорость высвобождения действующего вещества из таблетки. Насыпная плотность смеси повидона и поливинилацетата, как и Коллидона SR, составляет 0,5 г/см3, что оказалось достаточным для высокой прессуемости таблеток триметазидина дигидрохлорида.
Преимущества использования смеси повидона и поливинилацетата, в частности Коллидона SR, в лекарственной форме триметазидина дигидрохлорида по изобретению состоят в том, что такая лекарственная форма имеет высокий эффект пролонгированного высвобождения, профиль высвобождения активного компонента не зависит от рН и легко регулируется от 8 до 24 часов. Таблетки получают сухим смешением компонентов и прямым их прессованием, что заметно упрощает технологический процесс. Таблетки имеют высокую твердость в сочетании с великолепной пластичностью (низкая ломкость таблеток) и стабильность при хранении.
В качестве вспомогательных веществ лекарственная форма может содержать наполнители, скользящие-смазывающие, разрыхлители-дезинтегранты - основные группы веществ, обычно используемые при производстве таблеток.
Предпочтительный качественный и количественный состав лекарственной формы, мас.%: 3,5-70,0 триметазидина дигидрохлорида, 20,0-70,0 смеси повидона и поливинилацетата, 0,2-1,0 скользящего-смазывающего, 7,0-40,5 наполнителя, 1,0-5,0 разрыхлителя-дезинтегранта.
Эффективное количество триметазидина дигидрохлорида в лекарственной форме по изобретению составляет 35 мг. Количество его в процентном соотношении зависит от массы таблетки. При массе таблетки 1,0 г процентное содержание триметазидина дигидрохлорида составит 3,5 мас.%. При массе таблетки 0,05 г процентное содержание триметазидина дигидрохлорида составит 70,0 мас.%.
В качестве наполнителя лекарственная форма содержит одно или несколько веществ из следующих: сахара и их производные (лактоза, модифицированная лактоза, сахароза, глюкоза, маннит, модифицированный маннит, сорбит, фруктоза), полисахариды (целлюлоза и ее производные, крахмал, модифицированный крахмал, декстрин, декстроза, декстрат, мальтодекстрин, кальций и его соли (фосфаты, карбонаты, хлориды), магний и его производные (оксид, карбонат), кросповидон, коповидоны, циклодекстрины, альгиновая кислота и ее соли, сахарин и его соли, натрий и его соли (хлорид, цитрат, фумарат, карбонат), аспартам, молочная кислота и ее соли, янтарная кислота, аскорбиновая кислота, тартаровая кислота, коллоидная двуокись кремния, цикламат, бензойная кислота и ее соли, парабены и их соли.
В качестве скользящего-смазывающего лекарственная форма содержит вещество, выбранное из следующих: крахмал, тальк, полиэтиленоксиды, коллоидная двуокись кремния, стеариновая кислота и ее соли, фумаровая кислота и ее соли, натрий стеарилфумарат.
В качестве разрыхлителя-дезинтегранта лекарственная форма содержит вещество, выбранное из следующих: крахмал и его производные (натриевая соль гликолята крахмала, прежелатинизированный крахмал, амилопектин), натриевая соль кроскармелозы, кросповидоны, полисорбаты, натрий лаурилсульфат, коллоидная двуокись кремния, полиэтиленоксиды, производные целлюлозы.
Для улучшения прочности лекарственная форма может содержать 1,0-5,0 мас.% связующего, которое выбирают из следующих веществ: вода, спирт, сахарный сироп, крахмальный клейстер, растворы эфиров целлюлозы, повидоны, желатин, альгиновая кислота или ее соли, лимонная кислота, шеллак, поливиниловый спирт, растворы метакриловой кислоты и ее сополимеров.
Лекарственная форма по изобретению может быть выполнена с покрытием, что позволит обеспечить большую стабильность препарата при хранении.
Оптимальная массовая доля покрытия составляет от 3,0 до 6,0% от веса ядра таблетки. Покрытие выполнено из пленкообразующего вещества, пластификатора и пигмента - традиционных составляющих покрытий для таблеток.
Предпочтительный качественный и количественный состав покрытия содержит, мас.%; 55,0-65,0 пленкообразующего вещества, 9,0-11,0 пластификатора и 25,0-45,0 пигмента.
Пленкообразующее вещество для покрытия выбирают из следующих: целлюлоза и ее эфиры, натрий карбоксиметилцеллюлоза и ее производные, повидоны, коповидоны, метакриловая кислота и ее сополимеры, сахароза, шеллак, желатин, ксантановая камедь, гуммиарабик, альгиновая кислота и ее соли.
Пластификатор для покрытия выбирают из следующих: полисорбаты, глицерин и его эфиры, полиэтиленгликоль, пропиленгликоль, дибутилфталат, триэтилцитрат, триацетин, повидон, минеральные масла, растительные масла.
Пигмент для покрытия выбирают из одного или несколько веществ из следующих: тальк, титана диоксид, соли железа, красители, каолин.
Покрытие также может быть выполнено из готовых смесей для покрытия, содержащих в своем составе целлюлозу и ее эфиры, повидоны, сополимеры винилпирролидона с винилацетатом.
Предпочтительными готовыми смесями для покрытия являются Advantia Prime и OpadryII. Advantia Prime представляет собой смесь гипромеллозы (гидроксипропилметилцеллюлозы), макрогола (полиэтиленгликоля), титана диоксида и талька. По заказу ЗАО «ВЕРТЕКС» смесь изготавливает International Specialty Products, США, сайт компании http:// www.ispcorp.com/. Opadry II - это готовое покрытие для таблеток, представляющее собой смесь поливинилового спирта, макрогола, диоксид титана и талька. Данную смесь по заказу ЗАО «ВЕРТЕКС» изготавливает Colorcon Limited, Великобритания, сайт компании http://www.colorcon.com/.
Вспомогательные вещества, их соотношение в предлагаемой лекарственной форме подобрано экспериментальным путем и обеспечивает необходимую прочность и распадаемость в воде.
Кроме того, все вспомогательные вещества, формирующие ядро и оболочку, а также их содержание подобраны таким образом, чтобы обеспечить легкую грануляцию до нужного размера и нетоксичность для организма.
Преимущества использования покрытия таблеток оболочкой на основе готовых смесей состоит не только в упрощении технологического процесса (раствор для покрытия готов через 45 минут, в то время как на приготовление раствора для покрытия из отдельных компонентов требуется 1-2 часа).
Упрощается система взаимодействия с поставщиками вспомогательных компонентов: заказывается одна смесь, а не несколько компонентов, соответственно, входной контроль необходимо осуществить только для одного компонента.
Предлагаемую лекарственную форму триметазидина дигидрохлорида получали следующим образом.
В V-блендер загружают триметазидина дигидрохлорид и Коллидон SR. Смесь перемешивают в течение 5-6 минут при скорости вращения блендера 18-20 об/мин. Затем послойно загружают наполнитель, разрыхлитель-дезинтегрант, связующее (если оно присутствует). Перемешивают смесь в течение 10-15 мин при скорости вращения блендера 18-20 об/мин. Затем остановливают блендер и загрузают скользящее-смазывающее. Перемешивают смесь в течение 1 мин при скорости вращения блендера 18-20 об/мин.
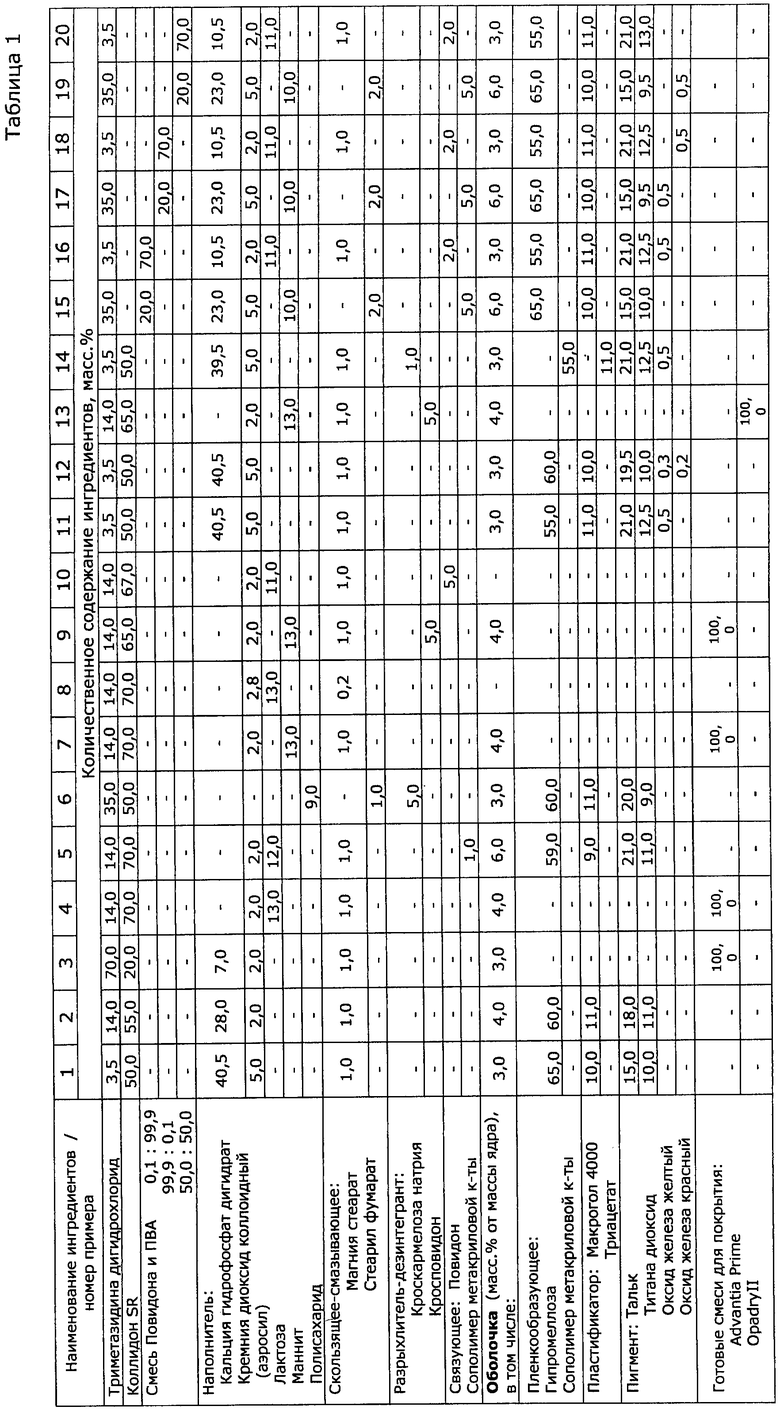
После перемешивания выгружают смесь в емкости, взвешивают. Готовую массу для таблетирования анализируют для определения количественного содержания триметазидина дигидрохлорида. Конкретные составы масс приведены в Таблице 1.
Таблетирование осуществляют на высокоскоростном ротационном таблеточном прессе ECI-SH-31D в соответствии с СОП «Эксплуатация высокоскоростного ротационного таблеточного пресса ECI-SH -31D».
Таблетки - ядра триметазидина дигидрохлорида имеют белый или почти белый цвет, с вкраплениями. Форма таблеток - двояковыпуклая, диаметром 9 мм, радиусом кривизны 0,9Д, средней массой 0,25 г, отклонение в массе отдельных таблеток-ядер от средней массы составляет ±7,5% (0,231-0,269 г), высота таблеток - 4,2-4,3 мм, прочность - 7-8 кг/см2.
Для нанесения пленочной оболочки традиционным способом приготавливают смесь.
Процесс нанесения оболочки из приготовленной на предприятии или готовых смесей Advantia Prime и OpadryII на таблетки-ядра тримектала следует осуществлять на машине для нанесения пленочного покрытия тип BG-80 (коатер).
Процесс покрытия таблеток-ядер пленочной оболочкой ведут при следующих параметрах: температура входящего воздуха - 60°С, скорость вращения барабана в начале процесса - 8 об/мин с постепенным увеличением до 9-12 об/мин, давление сжатого воздуха на иглу форсунки - 0,4 МПа, давление сжатого воздуха на распыление - 0,2 МПа, скорость подачи пленкообразующей суспензии по воде вначале 9 мл/мин с постепенным увеличением до 25-30 мл/мин.
Процесс ведут до полного использования пленкообразующей суспензии, после чего в течение 9-10 мин проводят окончательную сушку таблеток при температуре входящего воздуха 50°С и скорости вращения барабана 5-6 об/мин.
Затем отключают нагрев и охлаждают таблетки до температуры 20-25°С.
Средняя масса таблеток, покрытых оболочкой, составляет 0,258 г. Отклонение в массе отдельных таблеток, покрытых оболочкой, от средней массы составляет ±7,5% (0,238-0,277 г). Прочность ядра таблеток составила 7-8 кгс/см2.
В полученных таблетках-ядрах проверяют растворение. Учитывая, что для большинства препаратов наблюдается корреляция скорости растворения и скорости всасывания, тест «Растворение» является критерием оценки пролонгирующего действия таблеток. Тест «Растворение» проводили на приборе «Лопастная мешалка». В качестве среды растворения использовали 0,05 М фосфатный буферный раствор с рН 6,8. Объем среды составлял 500 мл, скорость вращения мешалки 50 об/мин. Количество высвободившегося триметазидина дигидрохлорида из таблеток по изобретению определяли на спектрофотометре в максимуме поглощения при длине волны 270 нм в кювете с толщиной слоя 10 мм.
При производстве препарата в соответствии с приведенным примером были получены таблетки, соответствующие требованиям фармацевтической статье предприятия (ФСП ЗАО «ВЕРТЕКС»). Согласно ФСП растворение должно составлять: через 1 час - 25-45%, через 2 часа - 43-63%, через 8 часов - не менее 80%, что обеспечит высокую биологическую доступность действующего вещества. Данные по растворению каждого из составов, приведенных в Таблице 1, сведены в Таблицу 2. Из Таблицу 2 следует, что таблетки по изобретению соответствует требованиям ФСП.
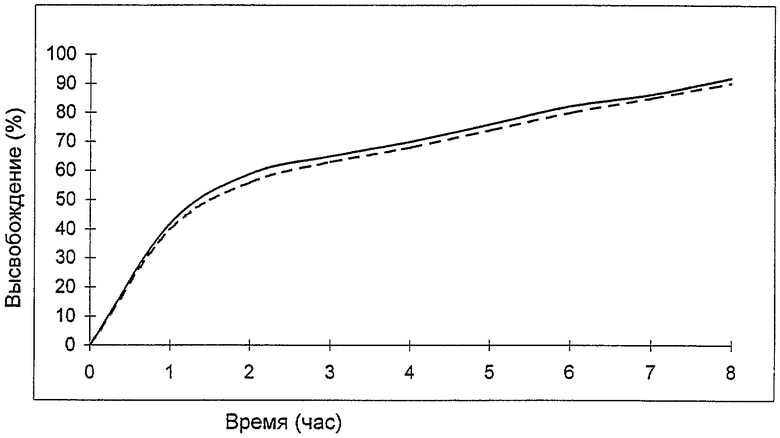
На чертеже представлен график, отражающий профиль растворения в момент изготовления таблеток (сплошная линия) и через три года хранения. Из представленного графика видно, что профиль растворения таблеток по изобретению при хранении не меняется.
Таким образом, проведенные исследования показали, что лекарственная форма по изобретению обладает пролонгированным действием и по своим фармакокинетическим параметрам не уступает препарату сравнения - таблеткам Предуктал MB, о чем свидетельствует заключение по результатам испытаний теста «Кинетика растворения», проведенного ОАО «НИИ Витаминов».
Действующее вещество в новой лекарственной форме триметазидина дигидрохлорида с модифицированным высвобождением равномерно распределено в объеме гидрофильного матрикса, что обеспечивает его замедленное контролируемое высвобождение. Это позволяет увеличить плато концентрации триметазидина в крови в течение суток и дает возможность поддерживать постоянную антиангинальную эффективность триметазидина дигидрохлорида в течение 24 часов. Поскольку новая форма позволяет повысить значение минимальной концентрации на 31% при сохранении максимальной, триметазидин дигидрохлорид обеспечивает лучшую защиту миокарда от ишемии в ранние утренние часы. Лекарственная форма триметазидина дигидрохлорида по изобретению принимается 2 раза в день, что обеспечивает более удобный режим дозирования и повышает приверженность больных лечению.
Предложена новая лекарственная форма триметазидина дигидрохлорида с модифицированным высвобождением в виде таблетки для перорального приема, которая содержит действующее вещество в количестве 3,5-70,0 мас.%, смесь повидона и поливинилацетата в качестве модификатора высвобождения в количестве 20,0-70,0 мас.% и фармацевтически приемлемые вспомогательные вещества. Предпочтительно лекарственная форма триметазидина дигидрохлорида в качестве смеси повидона и поливинилацетата содержит Коллидон SR. Данное изобретение позволит расширить ассортимент качественных доступных отечественных лекарственных средств с модифицированным высвобождением. 17 з.п. ф-лы, 2 табл., 1 ил.
1. Лекарственная форма триметазидина дигидрохлорида с модифицированным высвобождением в виде таблетки для перорального приема, содержащая действующее вещество в количестве 3,5-70,0 мас.%, смесь повидона и поливинилацетата в качестве модификатора высвобождения в количестве 20,0-70,0 мас.% и фармацевтически приемлемые вспомогательные вещества.
2. Лекарственная форма по п.1, отличающаяся тем, что в качестве вспомогательных веществ она содержит наполнители, скользящие-смазывающие, разрыхлители-дезинтегранты.
3. Лекарственная форма по п.2, отличающаяся тем, что она содержит, мас.%: 3,5-70,0 триметазидина дигидрохлорида, 20,0-70,0 смеси повидона и поливинилацетата, 0,2-1,0 скользящего-смазывающего, 7,0-40,5 наполнителя, 1,0-5,0 разрыхлителя-дезинтегранта.
4. Лекарственная форма по п.1, отличающаяся тем, что в качестве смеси повидона и поливинилацетата она содержит Коллидон SR.
5. Лекарственная форма по п.2, отличающаяся тем, что в качестве наполнителя она содержит одно или несколько веществ из следующих: сахара и их производные (лактоза, модифицированная лактоза, сахароза, глюкоза, маннит, модифицированный маннит, сорбит, фруктоза), полисахариды (целлюлоза и ее производные, крахмал, модифицированный крахмал, декстрин, декстроза, декстрат, мальтодекстрин, кальций и его соли (фосфаты, карбонаты, хлориды), магний и его производные (оксид, карбонат), кросповидон, коповидоны, циклодекстрины, альгиновая кислота и ее соли, сахарин и его соли, натрий и его соли (хлорид, цитрат, фумарат, карбонат), аспартам, молочная кислота и ее соли, янтарная кислота, аскорбиновая кислота,тартаровая кислота, коллоидная двуокись кремния, цикламат, бензойная кислота и ее соли, парабены и их соли.
6. Лекарственная форма по п.2, отличающаяся тем, что в качестве скользящего-смазывающего она содержит вещество, выбранное из следующих: крахмал, тальк, полиэтиленоксиды, коллоидная двуокись кремния, стеариновая кислота и ее соли, фумаровая кислота и ее соли, натрий стеарилфумарат.
7. Лекарственная форма по п.2, отличающаяся тем, что в качестве разрыхлителя-дезинтегранта она содержит вещество, выбранное из следующих: крахмал и его производные (натриевая соль гликолята крахмала, прежелатинизированный крахмал, амилопектин), натриевая соль кроскармелозы, кросповидоны, полисорбаты, натрий лаурилсульфат, коллоидная двуокись кремния, полиэтиленоксиды, производные целлюлозы.
8. Лекарственная форма по п.2, отличающаяся тем, что она дополнительно содержит 1,0-5,0 мас.% связующего.
9. Лекарственная форма по п.8, отличающаяся тем, что в качестве связующего она содержит вещество, выбранное из следующих: вода, спирт, сахарный сироп, крахмальный клейстер, растворы эфиров целлюлозы, повидоны, желатин, альгиновая кислота или ее соли, лимонная кислота, шеллак, поливиниловый спирт, растворы метакриловой кислоты и ее сополимеров.
10. Лекарственная форма по п.1, отличающаяся тем, что она выполнена с покрытием.
11. Лекарственная форма по п.10, отличающаяся тем, что массовая доля покрытия составляет от 3,0 до 6,0% от массы ядра таблетки.
12. Лекарственная форма по п.10, отличающаяся тем, что покрытие выполнено из пленкообразующего вещества, пластификатора и пигмента.
13. Лекарственная форма по п.12, отличающаяся тем, что покрытие содержит, мас.%: 55,0-65,0 пленкообразующего вещества, 9,0-11,0 пластификатора и 25,0-45,0 пигмента.
14. Лекарственная форма по п.12, отличающаяся тем, что в качестве пленкообразующего вещества покрытие содержит вещество, выбранное из следующих: целлюлоза и ее эфиры, натрий карбоксиметилцеллюлоза и ее производные, повидоны, коповидоны, метакриловая кислота и ее сополимеры, сахароза, шеллак, желатин, ксантановая камедь, гуммиарабик, альгиновая кислота и ее соли.
15. Лекарственная форма по п.12, отличающаяся тем, что в качестве пластификатора покрытие содержит вещество, выбранное из следующих: полисорбаты, глицерин и его эфиры, полиэтиленгликоль, пропиленгликоль, дибутилфталат, триэтилцитрат, триацетин, повидон, минеральные масла, растительные масла.
16. Лекарственная форма по п.12, отличающаяся тем, что в качестве пигмента покрытие содержит одно или несколько веществ из следующих: тальк, титана диоксид, соли железа, красители, каолин.
17. Лекарственная форма по п.10, отличающаяся тем, что покрытие выполнено из готовых смесей для покрытия, содержащих в своем составе целлюлозу и ее эфиры, повидоны, сополимеры винилпирролидона с винилацетатом.
18. Лекарственная форма по п.17, отличающаяся тем, что покрытие выполнено из готовых смесей для покрытия Advantia Prime на основе гипромеллозы и макрогола или OpadryII на основе поливинилового спирта и макрогола.
| МАТРИКСНАЯ ТАБЛЕТКА С РЕГУЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ ТРИМЕТАЗИДИНА | 2006 |
|
RU2367438C2 |
| Счетная машина | 1927 |
|
SU12297A1 |
| ЛЕКАРСТВЕННАЯ ФОРМА, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2003 |
|
RU2260431C2 |
| ЛЕКАРСТВЕННАЯ ФОРМА, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2005 |
|
RU2281772C1 |
| Центробежный эмульгатор | 1934 |
|
SU40963A1 |
| Устройство для регулирования давления газов в сборных камерах при электролизе воды под давлением | 1932 |
|
SU40964A1 |
| Устройство для питания водой паровых котлов | 1933 |
|
SU41523A1 |
Авторы
Даты
2011-02-27—Публикация
2009-10-08—Подача