Изобретение относится к области экологии, в частности к определению содержания тяжелых металлов в воде.
Известен способ определения тяжелых металлов в воде (заявка РФ № 93019316, G01N 30/06, 20.09.1995), основанный на анализе пробы, в которой устанавливают рН 4-6, обрабатывают комплексоном, полученную суспензию комплексов пропускают через стеклянный фильтр, концентрат растворяют в ацетонитриле и разделяют полученные хелаты металлов в хроматографической колонке, заполненной обращенно-фазным сорбентом, с последующим детектированием в УФ-области (двухволновая детекция).
Недостатком данного способа является значительная трудоемкость подготовки пробы и анализа в хроматографической колонке, а также необходимость наличия дорогостоящей аппаратуры.
Существует способ определения тяжелых металлов в воде (патент РФ № 2071050, G01N 23/223, 27.12.1996) при контроле качества питьевых вод и мониторинге водного бассейна, основанный на введении в анализируемую пробу органического реагента-комплексообразователя 1-(2-тиазолилазо)-нафтол-2 и выделение комплексов тяжелых металлов на мембранных фильтрах.
Недостатком данного способа является необходимость использования дорогостоящей аппаратуры и значительное время определения тяжелых металлов.
Известен способ (патент РФ № 2126151, G01N 33/48, 10.02.1999), сущность которого состоит в том, что при работе с биосубстратом в диагностических целях его смешивают с раствором хлорной меди, при этом в качестве растворителя используют ацетон.
Недостатком данного способа является ограниченное функциональное применение - применение только для диагностики заболеваний.
Наиболее близким к предложенному способу является изобретение (патент РФ № 2184961, G01N 33/18, 10.07.2002), сущность которого состоит в том, что при определении наличия тяжелых металлов в жидкостях в исследуемый раствор добавляют водный раствор белка известной молекулярной массы, затем среду, содержащую раствор белка и исследуемую жидкость, облучают лазерным светом, после этого определяют эффективную массу рассеивающих частиц смеси методом рэлеевского рассеяния света и по изменению этой массы по сравнению с молекулярной массой белка исходного раствора определяют наличие тяжелого металла в исследуемом водном растворе.
Недостатком данного способа является неопределенность практической применимости при различных концентрациях тяжелых металлов в водных растворах, а также значительная трудоемкость.
Задачей изобретения является повышение оперативности определения тяжелых металлов в воде и расширение функциональных возможностей применения.
Поставленная задача решается способом оперативного определения тяжелых металлов в воде, по которому биосубстрат смешивают с раствором, содержащим тяжелые металлы. В отличие от прототипа в качестве растворителя применяют этиловый спирт и воду в соотношении 6:1 и определяют индекс структуры кристаллограмм, полученных в присутствии солей тяжелых металлов: Cu2+, или Fe2+, или Zn2+.
Способ пояснен на фиг.1 - изменение индекса структуры кристаллограммы в зависимости от концентрации Cu2+, фиг.2 - изменение индекса структуры кристаллограммы в зависимости от концентрации Fe2+, фиг.3 - изменение индекса структуры кристаллограммы в зависимости от концентрации Zn2+.
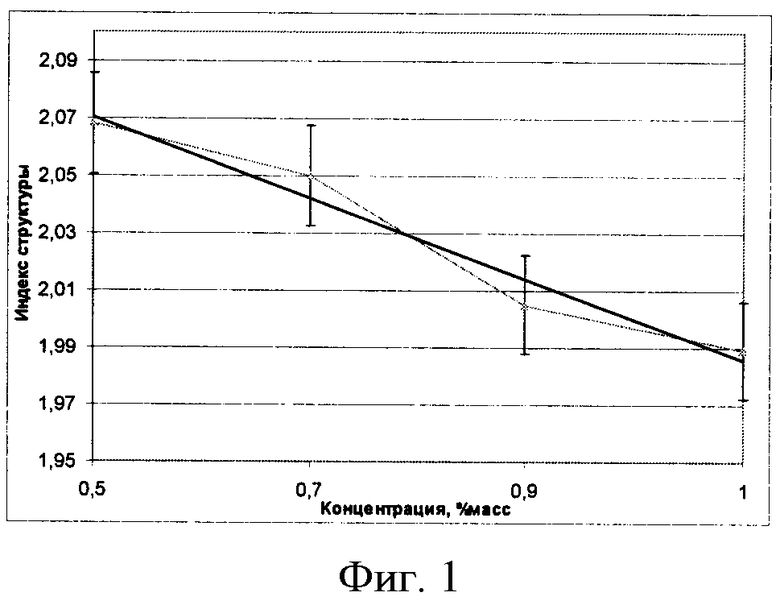
В системах, моделирующих ливневый сток, содержатся тяжелые металлы: Cu2+, или Fe2+, или Zn2+. Кристаллограмма раствора, содержащего Cu2+, характеризуется дендритной структурой кристаллов и наличием ромбической сингонии. Кристаллы имеют характерный зеленоватый оттенок оксида меди. Получены кристаллограммы для раствора, содержащего Cu2+ при различных концентрациях: 0,5…1,0 мас.%.
Изменение индекса структуры кристаллограммы в зависимости от концентрации Cu2+ приведено на фиг 1. Особенностью изменения индекса структуры в зависимости от концентрации Cu2+ является снижение индекса структуры при повышении концентрации Cu2+.
Согласно фиг.1 изменение концентрации Cu2+ (x) в зависимости от индекса структуры кристаллограмм (y) имеет вид:
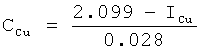 , мас.%
, мас.%
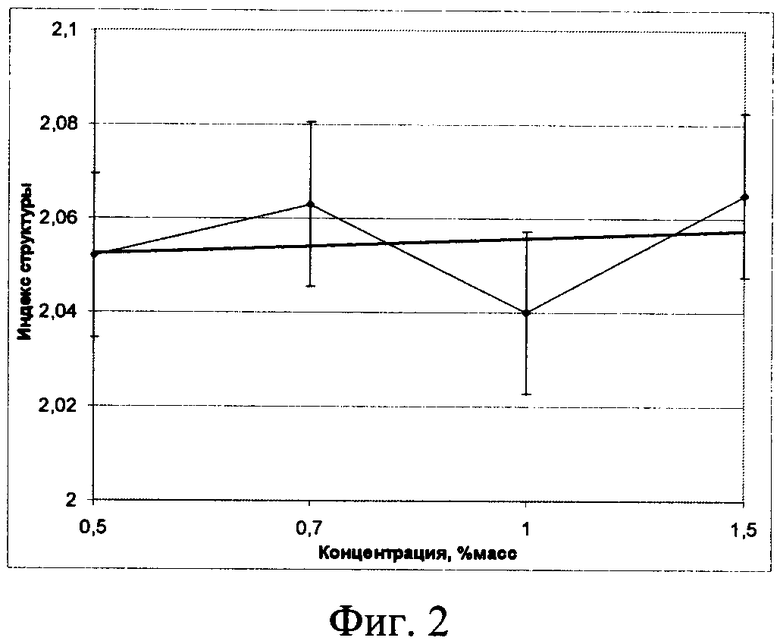
Кристаллограмма раствора, содержащего Fe2+, характеризуется слоистой структурой кристаллов и наличием тетрагональной сингонии. Кристаллы имеют характерный цвет оксида железа. Получены кристаллограммы для раствора, содержащего Fe2+ при различных концентрациях: 0,5…1,5 мас.%.
Изменение индекса структуры кристаллограммы в зависимости от концентрации Fe2+ приведено на фиг.2.
Согласно фиг.2 изменение концентрации Fe2+ (x) в зависимости от индекса структуры кристаллограмм (y) имеет вид:
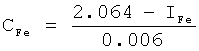 , мас.%
, мас.%
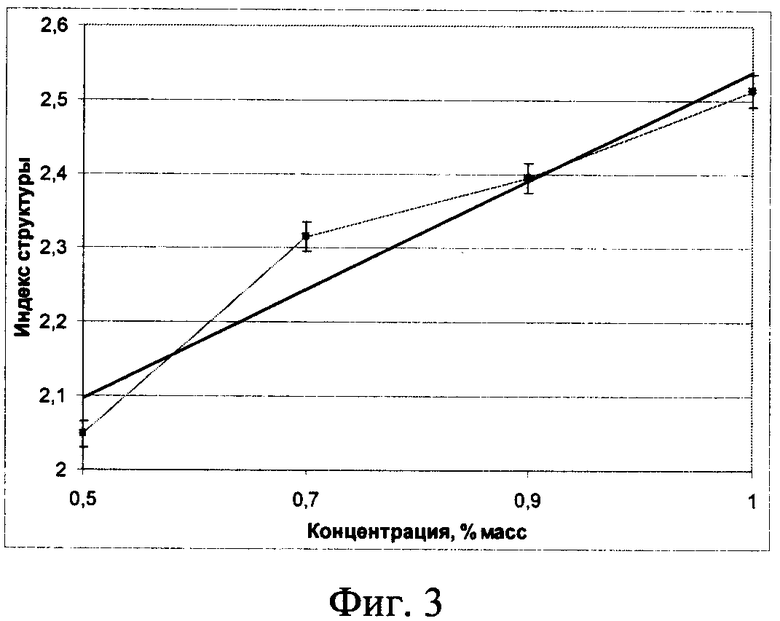
Кристаллограмма раствора, содержащего Zn2+, характеризуется слоистой структурой кристаллов и наличием ромбической сингонии. Кристаллы бесцветны. Получены кристаллограммы для раствора, содержащего Zn2+ при различных концентрациях: 0,5…1,0 мас.%.
Изменение индекса структуры кристаллограммы в зависимости от концентрации Zn2+ приведено на фиг.3.
Особенностью изменения индекса структуры в зависимости от концентрации Zn2+ является увеличение индекса структуры при повышении концентрации Zn2+.
Согласно фиг.3 изменение концентрации Zn2+ (x) в зависимости от индекса структуры кристаллограмм (y) имеет вид:
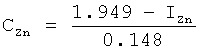 , мас.%
, мас.%
Предложенный способ оперативного определения тяжелых металлов в воде на основе определения индекса структуры кристаллорамм, полученных в присутствии тяжелых металлов: Cu2+, или Fe2+, или Zn2+, являющихся характерными загрязнителями, поступающими в ливневый сток урбанизированной территории, а также биогенных веществ (содержащих NH и СО группы), содержащихся в ливневом стоке с территории города, позволяет в короткие сроки получить информацию о концентрации металлов и при этом не требует сложной аппаратуры и достаточно прост. Величина относительной погрешности индекса структуры составляет 5%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ГАЛЬВАНОСТОКОВ ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2013 |
|
RU2525902C1 |
| ТВЕРДЫЙ РАСТВОР ГИДРОКСИДА МЕТАЛЛА И ТВЕРДЫЙ РАСТВОР ОКСИДА МЕТАЛЛА С ВЫСОКИМИ АСПЕКТНЫМИ ОТНОШЕНИЯМИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2147556C1 |
| СПОСОБ ИОНООБМЕННОЙ ОЧИСТКИ СТОЧНЫХ ВОД И ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ ОТ ИОНОВ МЕТАЛЛОВ | 2013 |
|
RU2550192C2 |
| Способ получения сорбента на минеральной основе | 2017 |
|
RU2682599C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГИДРОГЕЛЯ | 2016 |
|
RU2641111C1 |
| НЕОРГАНИЧЕСКИЙ СФЕРОГРАНУЛИРОВАННЫЙ КОМПОЗИЦИОННЫЙ СОРБЕНТ НА ОСНОВЕ ГИДРОКСИДА ЦИРКОНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2113024C1 |
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ ТЯЖЕЛЫХ МЕТАЛЛОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2592525C2 |
| ТВЕРДЫЙ РАСТВОР ГИДРОКСИДА МЕТАЛЛА, ТВЕРДЫЙ РАСТВОР ОКСИДА МЕТАЛЛА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2196105C2 |
| АМОРФНОЕ ПРОИЗВОДНОЕ КАОЛИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2136593C1 |
| СПОСОБ ОЦЕНКИ ВЛИЯНИЯ НАНОКОМПОНЕНТОВ НА САНИТАРНО-ХИМИЧЕСКИЕ СВОЙСТВА ПОЛИМЕРНЫХ МАТЕРИАЛОВ | 2011 |
|
RU2458345C1 |
Изобретение относится к области экологии применительно к анализу водных сред. В способе оперативного определения тяжелых металлов в воде биосубстрат смешивают с раствором, содержащим тяжелые металлы, причем в качестве растворителя применяют этиловый спирт и воду в соотношении 6:1, и определяют индекс структуры кристаллограмм, полученных в присутствии солей тяжелых металлов Cu2+ Fe2+, Zn2+. Достигается упрощение и ускорение анализа. 3 ил.
Способ оперативного определения тяжелых металлов в воде, по которому биосубстрат смешивают с раствором, содержащим тяжелые металлы, отличающийся тем, что в качестве растворителя применяют этиловый спирт и воду в соотношении 6:1, определяют индекс структуры кристаллограмм, полученных в присутствии солей тяжелых металлов Cu2+, Fe2+, Zn2+, и рассчитывают концентрации металлов CCu, CFe, CZn из соотношений
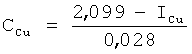 , мас.%,
, мас.%,
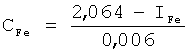 , мас.%,
, мас.%,
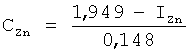 , мас.%,
, мас.%,
где ICu, IFe, IZn - индексы структуры кристаллограмм, полученные в присутствии солеи Cu2+, Fe2+, Zn2+.
| СПОСОБ БИОИНДИКАЦИИ ЗАГРЯЗНЕНИЯ МОРСКОЙ ВОДЫ ТЯЖЕЛЫМИ МЕТАЛЛАМИ | 2003 |
|
RU2264465C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В ВОДНЫХ РАСТВОРАХ | 2000 |
|
RU2184961C2 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ВОДЫ И ПОЧВЫ НА ЗАГРЯЗНЕНИЕ ПОЛЛЮТАНТАМИ | 1997 |
|
RU2135994C1 |
| Способ биоиндикации тяжелых металлов в морской воде | 1987 |
|
SU1479876A1 |
| Способ очистки N-хлоро-нитро-анилина | 1932 |
|
SU31429A1 |
| DE 4122668 A1, 14.01.1993. | |||
Авторы
Даты
2011-06-10—Публикация
2009-12-28—Подача