Введение
Изобретение относится к химической промышленности, а именно к получению нового производного 2,3-дикарбоксиантрахинона как исходного соединения для синтеза металлокомплексов тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина, которые могут быть использованы в качестве красителей и катализаторов.
Уровень техники
Известен 2,3-дикарбоксиантрахинон [K.Sakamoto, E.Ohno. Synthesis of Cobalt Phthalocyanine Derivatives and their Cyclic Voltammograms // Dyes and Pigments. 1997. Vol.35. N 4. P.380]
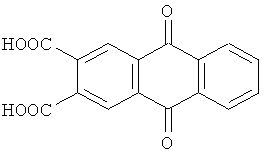
Однако при использовании этого соединения в качестве исходного можно получить лишь тетраантрахинонопорфиразины, которые не обладают красящими свойствами и не проявляют каталитическую активность.
Сущность изобретения
Изобретательская задача состояла в поиске нового соединения, являющегося производным 2,3-дикарбоксиантрахинона, которое при использовании его в качестве исходного продукта дало бы возможность синтезировать металлокомплексы тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина, обладающие свойствами красителей для полимерных материалов и катализаторов различных процессов.
Поставленная задача решена 1-ацетил-5,10-диокси-5,10-дигидро-2H-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновой кислотой формулы
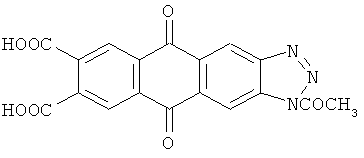
Структура этого соединения доказана данными элементного анализа и ИК спектроскопии.
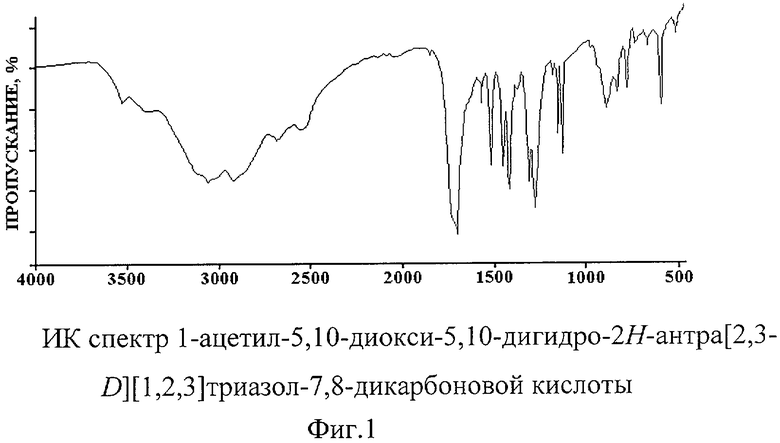
Так, в ИК спектре заявляемого соединения (фиг.1) можно выделить ряд общих полос поглощения с антрахиноном [C.Pecile, B.Lunelli. Polarized Infrared Spectra of Single Crystals of 9,10-Anthraquinone and 9,10-Anthraquinone-ds // J. Chem. Phys. 1967. Vol.46. N 6. P.2109-2118].
Изобретение позволяет получить следующие преимущества: использование 1-ацетил-5,10-диокси-5,10-дигидро-2H-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновой кислоты дает возможность синтезировать металлокомплексы тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина, обладающие способностью окрашивать полимерные материалы и проявляющие каталитические свойства.
Сведения, подтверждающие возможность осуществления изобретения
Для реализации изобретения используют следующие вещества:
бензотриазол - ТУ 6-09-1291-87;
уксусный ангидрид - ГОСТ 21039-75;
диангидрид пиромеллитовой кислоты - ТУ 6-14-786-72;
безводный хлористый алюминий - ОСТ 6-01-300-74;
концентрированная серная кислота - ГОСТ 4204-77.
Целевой продукт получают в три стадии.
Стадия 1. Ацилирование бензотриазола уксусным ангидридом по схеме:
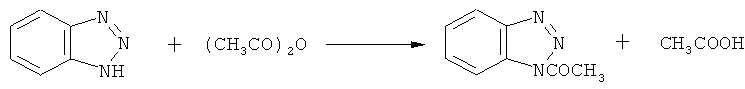
В круглодонной трехгорлой колбе емкостью 100 мл растворяют 11.9 г (0.1 моль) бензотриазола в 20 мл толуола. Колбу соединяют с обратным холодильником и к находящемуся в колбе раствору осторожно в течение 15 минут приливают 11.3 мл (0.12 моль) уксусного ангидрида. При этом реакционная смесь разогревается до кипения. После добавления всего количества уксусного ангидрида смеси дают охладиться. Выпавшие кристаллы игольчатой формы отфильтровывают на воронке Бюхнера, промывают толуолом небольшими порциями до исчезновения запаха уксусной кислоты и сушат на воздухе между листами фильтровальной бумаги.
Выход 1-ацетилбензотриазола - 11 г.
Стадия 2. Ацилирование 1-ацетилбензотриазола диангидридом пиромеллитовой кислоты в присутствии безводного хлористого алюминия по схеме:
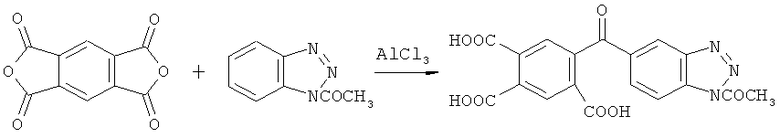
В трехгорловую колбу емкостью 100 мл, снабженную мешалкой, обратным холодильником и термометром, помещают 10.0 г (0.046 моль) диангидрида пиромеллитовой кислоты, 8.21 г (0.051 моль) 1-ацетилбензотриазола и 20 мл гептана. Массу нагревают до 50°С и при перемешивании прибавляют 16.12 г (0.119 моль) безводного хлористого алюминия. Выдерживают 3 часа при кипении реакционной массы (≈100°C), а после отгонки гептана еще 6 часов при 120÷130°С. К охлажденной массе последовательно прибавляют 50 мл воды и 10 мл концентрированной соляной кислоты и перемешивают 12 часов. Осадок отфильтровывают, промывают горячей водой и кипятят 30÷40 минут в 10%-ном растворе соды. Горячий раствор фильтруют, осадок обрабатывают подобным образом еще 3-4 раза. Фильтрат подкисляют соляной кислотой до pH 4 и охлаждают до 10÷15°С. Выпавший осадок отфильтровывают, промывают водой до нейтральной реакции. Сушат при 80°С.
Выход 5-[(1-ацетил-2Н-1,2,3-бензотриазол-5-ил)карбонил]-бензол-1,2,4-трикарбоновой кислоты - 7 г.
Стадия 3. Внутримолекулярная циклизация путем обработки 5-[(1-ацетил-2Н-1,2,3-бензотриазол-5-ил)карбонил]бензол-1,2,4-трикарбоновой кислоты концентрированной серной кислотой (моногидратом) по схеме:
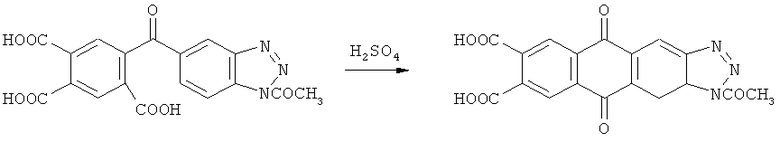
В трехгорлую колбу объемом 100 мл, снабженную мешалкой, обратным холодильником и термометром, помещают 20 мл (0.18 моль) моногидрата и нагревают до 130°С. Затем в течение 15 минут при интенсивном перемешивании вносят 5 г (0.011 моль) полученной 5-[(1-ацетил-2Н-1,2,3-бензотриазол-5-ил)карбонил]бензол-1,2,4-трикарбоновой кислоты, температуру поднимают до 150°С и выдерживают в течение 5 часов. Массу после охлаждения при перемешивании выливают в 200 мл воды, фильтруют, осадок промывают большим количеством ледяной воды, растворяют в содовом растворе и подкисляют соляной кислотой. Осадок отфильтровывают и промывают водой до исчезновения хлорид-ионов. Такую обработку повторяют дважды. Сушат при 100°С.
Найдено, %: С - 57.50; Н - 2.32; N - 11.05. C18H9N3O7.
Вычислено, %: С - 57.00; Н - 2.39; N - 11.08.
Выход: 4.1 г (86%). Температура плавления - 346°С.
Полученный целевой продукт - 1-ацетил-5,10-диокси-5,10-дигидро-2Н-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновая кислота - твердое вещество белого цвета, обладает растворимостью в водно-щелочных растворах, горячей воде, ацетоне, ДМФА.
Пример 1. Использование 1-ацетил-5,10-диокси-5,10-дигидро-2H-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновой кислоты в качестве исходного соединения для синтеза медного и кобальтового комплексов тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)-фталоцианина
В кварцевую ампулу помещают растертую смесь 0.23 г (0.60 ммоль) 1-ацетил-5,10-диокси-5,10-дигидро-2Н-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновой кислоты, 0.24 г (4.00 ммоль) мочевины, 0.036 г (0.18 ммоль) ацетата меди или 0.036 г (0.18 ммоль) ацетата кобальта, 0.02 г (0.40 ммоль) хлорида аммония и 0.002 г (0.01 ммоль) молибдата аммония. Массу медленно нагревают до 180°С в течение часа и выдерживают 3 часа. После охлаждения реакционную массу измельчают, переносят на фильтр Шота, промывают 5%-ной соляной кислотой и водой, пока в промывной жидкости при нанесении ее капли на предметное стекло и выпаривании не остается твердого остатка. Сушат при 100°С. Затем переосаждают из концентрированной серной кислоты и промывают в аппарате Сокслета ацетоном в течение 10 часов. Сушат при 100°С.
Выход тетра[4,5]([6,7] 1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина меди - 0.13 г.
Выход тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина кобальта - 0.12 г.
Эти синтезированные соединения представляют собой сине-зеленые вещества, растворимые в концентрированной серной кислоте, диметилсульфоксиде, диметилформамиде.
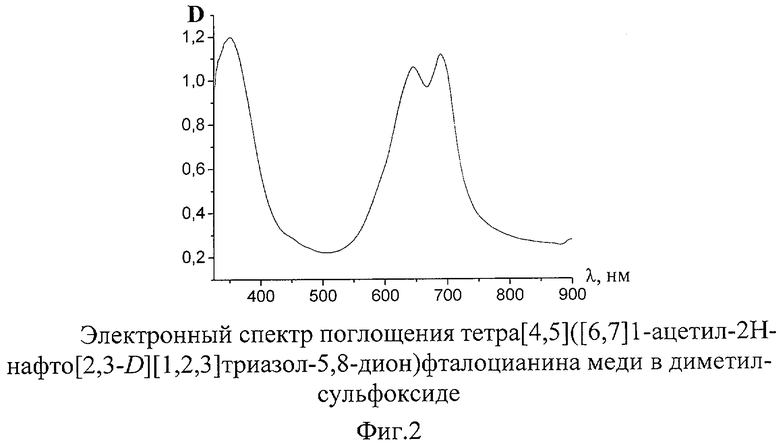
ЭСП тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина меди в диметилсульфоксиде. λmax, нм: 352, 644, 689 (фиг.2).
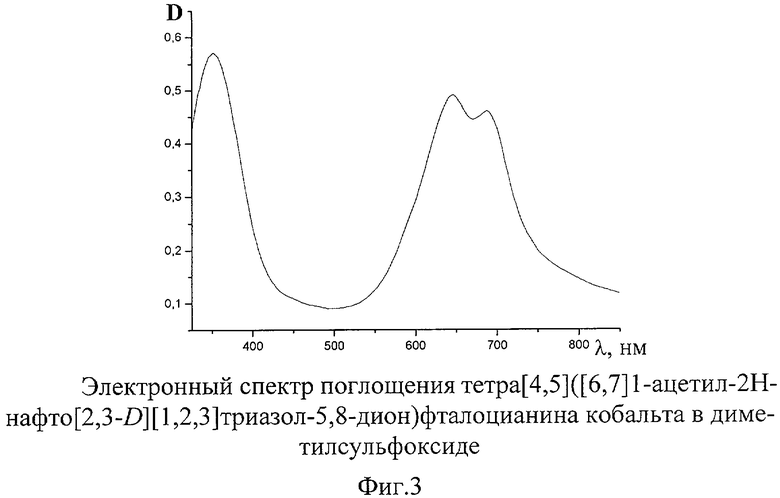
ЭСП тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина кобальта в диметилсульфоксиде. λmax; нм: 352, 646, 688 (фиг.3).
Найдено, %: С 60.53; Н 1.98; N 19.61. C54H28N11O9Cu;
С 60.73; Н 1.98; N 19.67. C54H28N11O9Co.
Вычислено, %: С 60.10; H 1.80; N 19.18. C54H28N11O9Cu;
C 60.97; H 1.75; N 19.52. C54H28N11O9Co.
Пример 2. Использование тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина меди в качестве красителя для крашения полиэтилена и полистирола.
Крашение полиэтилена. 2 г полиэтилена помещают в фарфоровую чашку и нагревают до расплавления, затем вливают 5 мл диметилсульфоксида, в котором растворено 0.003 г тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина меди. Выдерживают при нагревании до полного удаления диметилсульфоксида и выливают полученную массу в форму.
Образец прилагается (см. фиг.5).
Крашение полистирола. 2 г полистирола помещают в фарфоровую чашку и нагревают до расплавления, затем вливают 5 мл диметилсульфоксида, в котором растворено 0.003 г тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина меди. Выдерживают при нагревании до полного удаления диметилсульфоксида и выливают полученную массу в форму.
Образец прилагается (см. фиг.5).
Пример 3. Использование тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина кобальта в качестве катализатора процессов окисления меркаптанов.
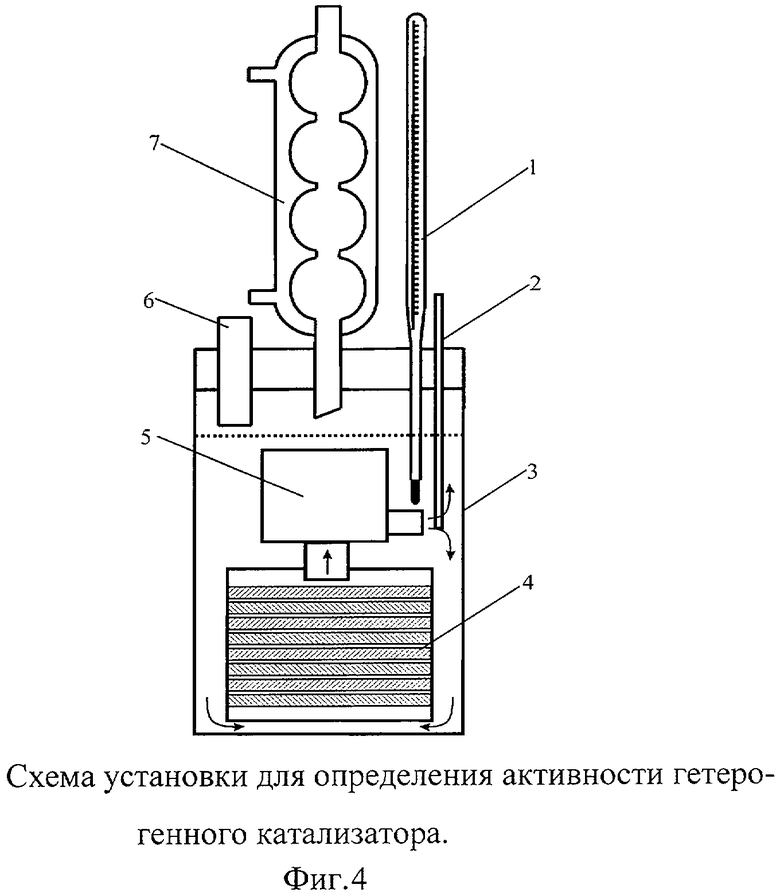
Исследование каталитической активности кобальтового комплекса тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-1)][1,2,3]триазол-5,8-дион)фталоцианина проводили на 0.02 М растворе диэтилдитиокарбомата натрия (ДЭДТК) на установке, изображенной на фиг.4. Установка содержит: 1 - термометр, 2 - барботер, 3 - стеклянный стакан, 4 - образцы гетерогенного катализатора, 5 - насос, 6 - пробоотборник, 7 - обратный холодильник.
Для приготовления гетерогенного катализатора в 50 мл раствора кобальтового комплекса тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина в ДМФА с концентрацией 0.01 моль/л погружают и полностью пропитывают образец нетканого полипропилена массой 2 г. Затем образец извлекают и погружают в воду для удаления органического растворителя. При этом происходит быстрая кристаллизация и осаждение кобальтового комплекса на поверхности полипропиленовых волокон. Концентрация комплекса на поверхности нетканого материала при такой обработке составляет 1.9·10-5 моль на 1 г полипропилена. Полученный таким образом гетерогенный катализатор помещают в стакан с ДЭДТК, снабженный насосом CIRCULATOR 650 производительностью 600 л/ч для подачи воздуха, необходимого для окисления, с постоянной скоростью 2 л/мин. После установления в реакционной смеси в стакане постоянной температуры отбирают пробу 2 мл для определения начальной концентрации ДЭДТК и пропускают воздух. Момент подачи воздуха принимают за начало реакции. В ходе реакции через определенные промежутки времени отбирают пробы по 2 мл для спектрометрического определения текущей концентрации ДЭДТК.
Эффективная константа скорости окисления ДЭДТК составляет 3.2±0.3 сек-1
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕТРА[4,5]([6,7]1-АЦЕТИЛ-2Н-НАФТО[2,3-D][1,2,3]ТРИАЗОЛ-5,8-ДИОН)ФТАЛОЦИАНИНЫ МЕДИ И КОБАЛЬТА | 2009 |
|
RU2411246C1 |
| Способ получения 1-(2-пропаргил)-1Н-нафто[2,3-d][1,2,3]триазол-4,9-дион-4-оксим-2-оксида | 2022 |
|
RU2791249C1 |
| 1,2,4-ТРИАЗОЛО[4,3-C]-10,10-ДИМЕТИЛ-8,10-ДИГИДРО-11Н-ПИРАНО- [4′, 3′:4,5]- ПИРРОЛО [2,3-D] ПИРИМИДИН | 1983 |
|
SU1116712A1 |
| МНОГОКОМПОНЕНТНАЯ СИСТЕМА ДЛЯ ИЗМЕНЕНИЯ, РАЗЛОЖЕНИЯ ИЛИ ОТБЕЛИВАНИЯ ЛИГНИНА, СОДЕРЖАЩИХ ЛИГНИН МАТЕРИАЛОВ ИЛИ УГЛЯ И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 1995 |
|
RU2142479C1 |
| СПОСОБ ПОЛУЧЕНИЯ (СО)ПОЛИМЕРА ВИНИЛХЛОРИДА | 1985 |
|
RU2012565C1 |
| Производные 4,11-диоксиантра [2,3-в] фуран-5,10-диона в качестве дисперсных красителей для полиэфирного волокна и способ их получения | 1981 |
|
SU973577A1 |
| ТРИЦИКЛИЧЕСКИЕ ДИКАРБОНИЛЬНЫЕ ПРОИЗВОДНЫЕ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1995 |
|
RU2145606C1 |
| СПОСОБ ПОЛУЧЕНИЯ КУБОВЫХ КРАСИТЕЛЕЙ И ПИГМЕНТОВ, СОДЕРЖАЩИХ ПЕРИЛЕНОВЫЙ ФРАГМЕНТ | 1997 |
|
RU2128200C1 |
| ЗАМЕЩЕННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ КОНДЕНСИРОВАННОЕ ЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2815814C1 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ IkB-КИНАЗЫ ПРИ ОБЕЗБОЛИВАЮЩЕМ ЛЕЧЕНИИ | 2003 |
|
RU2320338C2 |

Описывается новое соединение - 1-ацетил-5,10-диокси-5,10-дигидро-2Н-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновая кислота формулы

которое может быть использовано в качестве исходного соединения для синтеза металлокомплексов тетра[4,5]([6,7]1-ацетил-2Н-нафто[2,3-D][1,2,3]триазол-5,8-дион)фталоцианина; последние могут быть использованы в качестве красителей или катализаторов. 5 ил.
1-Ацетил-5,10-диокси-5,10-дигидро-2Н-антра[2,3-D][1,2,3]триазол-7,8-дикарбоновая кислота формулы

| ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ | 2001 |
|
RU2185378C1 |
| Способ получения производных триазола | 1980 |
|
SU925952A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Chem | |||
| Abs | |||
| Переходная площадка пассажирского вагона | 1982 |
|
SU1135681A1 |
Авторы
Даты
2011-06-20—Публикация
2009-11-23—Подача