Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики заболеваемости гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма вируса гриппа А, семейства Orthomyxoviridae, рода Influenzavirus A, А/17/Калифорния/2009/38 (H1N1).
В конце апреля 2009 года Всемирная организация здравоохранения (ВОЗ) объявила о появлении в циркуляции среди людей нового вируса гриппа A(H1N1). Новый вирус А/Калифорния/07/2009 (H1N1) имеет генетическое родство по определенным генам с вирусами, вызывающими грипп свиней, птиц и человека, и никогда ранее не циркулировал среди людей. Вирус с легкостью передается от человека к человеку и более контагеозен, чем сезонные штаммы.
11 июня 2009 г. ВОЗ было объявлено о начале пандемии гриппа. К этому времени было подтверждено около 30000 случаев заболеваний в 74 странах. [World Health Organization. Statement by WHO Director-General, Dr. Margaret Chan 11 June 2009. World now at the start of 2009 influenza pandemic. http://www.who.int/mediacentre/news/statements/2009/h1n120090429/en/index.html].
В связи с тем, что изоляты от заболевших гриппом антигенно и генетически родственны новому вирусу А/Калифорния/07/2009 (H1N1), ВОЗ рекомендует использовать этот штамм, как прототип для подготовки актуальной противогриппозной вакцины [World Health Organization. Characteristics of the emergent influenza A(H1N1) viruses and recommendations for vaccine development. http://www.who.int/csr/resources/publications /swineflu/vaccine recommendations/en/index.html].
В результате появления в циркуляции нового шифтового варианта вируса гриппа известный вакцинный штамм вируса гриппа А/17/Новая Каледония/99/145 серотипа A(H1N1) [Патент РФ №2183672. - Опубл. 20.06.2002] - утратил антигенную актуальность и вследствие этого не может вызвать защитную реакцию во время пандемии гриппа. Он является прототипом данного изобретения.
Задачей, на решение которой направлено заявляемое изобретение, является получение антигенно актуального вакцинного штамма для взрослых и для детей на основе холодоадаптированного донора аттенуации А/Ленинград/134/17/57 (H2N2) и нового пандемического вируса А/Калифорния/07/2009 (H1N1).
Применяемые в настоящее время штаммы для живых гриппозных вакцин получают методом генетической реассортации эпидемически актуальных вирусов с холодоадаптированными штаммами - донорами аттенуации [Александрова Г.И. Применение метода генетической рекомбинации для получения вакцинных штаммов вируса гриппа // Вопр. Вирусол. - 1977. - №4, - с.387-395].
Донор аттенуации А/Ленинград/134/17/57 (H2N2) - холодоадаптированный (са) температурочувствительный (ts) штамм вируса гриппа, разрешенный для получения безвредных живых интраназальных вакцин для взрослых и детей [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. Л., 1968. - С.66-83].
Цель реассортации - получить штамм с вакцинной формулой генома 6:2. Гены, кодирующие поверхностные белки вируса гриппа гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального циркулирующего эпидемического (пандемического) штамма, а шесть генов, кодирующих внутренние и неструктурные белки (РВ2, РВ1, PA, NP, M, NS), от безвредного донора аттенуации. На основе донора аттенуации А/Ленинград/134/17/57 (H2N2) был создан вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) - прототип.
Получение вакцинного штамма.
Вакцинный штамм А/17/Калифорния/2009/38 (H1N1) получен методом генетической реассортации пандемического вируса А/Калифорния/07/2009 (H1N1) с донором аттенуации А/Ленинград/134/17/57 (H2N2) посредством инфицирования развивающихся куриных эмбрионов (РКЭ) смесью родительских вирусов в эквивалентных инфекционных дозах, с последующей селекцией клонов с заданными свойствами при пониженной до 25°С температуре инкубации в присутствии антисыворотки к донору аттенуации. Клоны дополнительно очищены трехкратным клонированием методом предельных разведений под прессом антисыворотки к донору при пониженной (25°С) и оптимальной (33°С) температурах инкубации. Чистые клоны проверены по фенотипическим характеристикам (ts-, са-фенотип) и по формуле генома на соответствие вакцинному штамму.
Антигенная характеристика вакцинного штамма. Ответственный за антигенную специфичность поверхностный белок вакцинного штамма - гемагглютинин (НА) - в РТГА идентичен вирусу А/Калифорния/07/2009 (H1N1), антисывороткой к которому полностью нейтрализуется.
Формула генома.
Формула генома (6:2) вакцинного штамма А/17/Калифорния/2009/38 (H1N1) подтверждена методом RT-PCR с помощью специфических праймеров. На чертеже представлены результаты определения формулы генома вакцинного штамма А/17/Калифорния/2009/38 (H1N1) с помощью электрофореза амплифицированных фрагментов генов в 1,7% агарозном геле, содержащем 0,5 мкг/мл этидиума бромида. Обозначения: Лен - амплифицированный фрагмент комплементарной ДНК, соответствующий определенному белку, донора аттенуации А/Ленинград/134/17/57 (H2N2). Sw - амплифицированный фрагмент комплементарной ДНК, соответствующий определенному белку, пандемического вируса А/Калифорния/07/2009 (H1N1). Дорожки 1, 2, 3, 5, 7, 8 - фрагменты генов вакцинного штамма А/17/Калифорния/2009/38 (H1N1), амплифицированные с праймерами, специфичными только для донора аттенуации А/Ленинград/134/17/57 (H2N2) (Лен). Дорожки 4, 6 - фрагменты генов вакцинного штамма А/17/Калифорния/2009/38 (H1N1), амплифицированные с праймерами, специфичными только для пандемического вируса А/Калифорния/07/2009 (H1N1) (Sw).
Формула генома 6:2 соответствует требованиям, предъявляемым к штаммам живой гриппозной вакцины: гены, кодирующие поверхностные белки гемагглютинин (НА) и нейраминидазу (NA) принадлежат пандемическому родительскому вирусу А/Калифорния/07/2009 (H1N1), гены, кодирующие внутренние белки (РВ2, РВ1, PA, NP, M, NS), принадлежат донору аттенуации А/Ленинград/134/17/57 (H2N2).
Фенотипические свойства в экспериментах in vitro.
Фенотипические особенности созданного вакцинного штамма А/17/Калифорния/2009/38 (H1N1) и стабильность его фенотипических признаков изучены сравнением его способности к репродукции при оптимальной температуре (32-33°С) и при температурах за пределами температурного оптимума (25°С и 40°С) до и после его пятикратного пассирования в куриных эмбрионах.
Установлено, что для достижения максимальных инфекционных титров вакцинного штамма требуется его инкубация при 32-33°С в течение 72 часов. В этом случае достигается увеличение титра на 2,8±0,5 Ig ЭИД50/0,2 мл по сравнению с титрами, полученными при инкубации в течение 48 часов (табл.1).
Вакцинный штамм А/17/Калифорния/2009/38 (H1N1) в развивающихся куриных эмбрионах обладает выраженным температурочувствительным и холодоадаптированным фенотипом, идентичным фенотипу донора аттенуации А/Ленинград/134/17/57 (H2N2). Разность в показателях инфекционной активности при температуре инкубации 33°С и 40°С составляет 5,7 Ig ЭИД50/0,2 мл - (RCT40); разность в показателях инфекционной активности (RCT25) при температуре инкубации 33°С и 25°С равна 1,2 Ig ЭИД50/0,2 мл. Фенотипические свойства вакцинного штамма не изменились после его пятикратного пассирования (табл.2).
Генетическая стабильность кодирующих мутаций. Генетическую стабильность вакцинного штамма А/17/Калифорния/2009/38 (H1N1) изучали сравнением сохранности кодирующих мутаций во внутренних генах до и после пятикратного пассирования вакцинного штамма в куриных эмбрионах. Методом рестрикционного анализа ДНК копий генов [Klimov A.I., Сох N.J. PCR restriction analysis of genome composition and stability of cold-adapted reassortant live influenza vaccines // J. Virol. Methods. - 1995. - Vol.52. - №1-2. - P.41-49], основанным на амплификации коротких участков РНК, включающих уникальные нуклеотидные последовательности, характерные только для донора аттенуации А/Ленинград/134/17/57 (H2N2), продемонстрирована идентичность мутаций во всех внутренних генах донора аттенуации А/Ленинград/134/17/57 (H2N2) и вакцинного штамма А/17/Калифорния/2009/38 (H1N1) до и после его пятикратного пассирования, в том числе в генах полимеразного комплекса (РВ2, РВ1, РА), ответственных за аттенуирующий фенотип (табл.3).
тид
кислота
Чувствительность к неспецифическим гамма-ингибиторам сыворотки крови.
Чувствительность вакцинного штамма А/17/Калифорния/2009/38 (H1N1) и его пандемического родителя А/Калифорния/07/2009 (H1N1) к неспецифическим гамма-ингибиторам сыворотки крови оценивали в стандартной реакции РТГА с нормальными (неиммунными) сыворотками крови лошади, морской свинки и кролика. В качестве ингибиторочувствительного контрольного вируса был использован штамм вируса гриппа А/Малайзия/01/04 (H3N2), в качестве ингибитороустойчивого контроля был взят вирус А/Ленинград/134/57 (H2N2). Показано, что вакцинный штамм А/17/Калифорния/2009/38 (H1N1), равно как и его пандемический родитель А/Калифорния/07/2009 (H1N1), высоко устойчивы к гамма-ингибиторам сыворотки крови животных разного происхождения (табл.4).
Безвредность для белых мышей и морских свинок.
Изучение острой токсичности вакцинного штамма А/17/Калифорния/2009/38 (H1N1) проводили в экспериментах на белых мышах и морских свинках обоего пола. Мышам вводили вирус внутрибрюшинно или подкожно однократно в объеме 0,5 мл, морским свинкам - 5 мл внутрибрюшинно. Животным контрольной группы не вводили ничего. Безвредность вакцинного штамма А/17/Калифорния/2009/38 (H1N1) оценивали по выживаемости животных и прибавке в весе. Вирус вводили в дозе 7Ig ЭИД50/0,2 мл. Показана безвредность вакцинного штамма для лабораторных животных при его подкожном и внутрибрюшинном введении. Отмечена прибавка в весе животных при их 100%-ной выживаемости (табл.5).
Аттенуация и нейровирулентность для мышей. Изучение аттенуирующих свойств вакцинного штамма А/17/Калифорния/2009/38 (H1N1) проводили в экспериментах на белых мышах после их интраназального заражения, оценивая степень репродукции вируса в легких по сравнению с уровнем репродукции донора аттенуации А/Ленинград/134/17/57 (H2N2) и его дикого предшественника, вируса А/Ленинград/134/57 (H2N2).
Отсутствие нейровирулентной активности у вакцинного штамма А/17/Калифорния/2009/38 (H1N1) изучали путем интраназального заражения мышей с последующим выделением вируса из ткани мозга. В качестве контроля был использован нейровирулентный штамм вируса гриппа A/WSN/33 (H1N1). Вирусы вводили в дозе 7 Ig ЭИД50/0,2 мл.
Показано, что вакцинный штамм А/17/Калифорния/2009/38 (H1N1) выделялся из легких и носовых ходов мышей в титрах, аналогичных донору аттенуации А/Ленинград/134/17/57 (H2N2). При этом вирусы дикого типа А/Ленинград/134/57 (H2N2) и A/WSN/33 (H1N1) активнее репродуцировались в легких мышей по сравнению с холодоадаптированными вирусами (табл.6), что подтверждает аттенуирующий фенотип вакцинного штамма А/17/Калифорния/2009/38 (H1N1). Показано полное отсутствие проникновения вакцинного штамма А/17/Калифорния/2009/38 (H1N1) в мозг инфицированных животных после их интраназального заражения при активной репродукции в мозговой ткани нейротропного вируса A/WSN/33 (H1N1) (табл.6).
В результате проведенных доклинических исследований установлено, что заявляемый вакцинный штамм живой гриппозной вакцины А/17/Калифорния/2009/38 (H1N1) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью пандемического вируса А/Калифорния/07/2009 (H1N1), структурой генома, оптимальной для реассортантных вакцинных штаммов, температурочувствительностью и холодоадаптированностью, что коррелирует с аттенуацией для человека, характерной для донора аттенуации. Штамм аттенуирован и безвреден для мышей и морских свинок. Морфология штамма полиморфная, типичная для вируса гриппа.
Штамм А/17/Калифорния/2009/38 (H1N1) обладает в опытных проверках статистически достоверным лечебно-профилактическим действием.
Штамм А/17/Калифорния/2009/38 (H1N1) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 32-33°С, характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал гены, кодирующие поверхностные антигены вируса гемагглютинин (НА) и нейраминидазу (NA), от потенциально пандемического вируса и остальные шесть генов, кодирующих внутренние негликозилированные белки, от донора аттенуации.
Штамм А/17/Калифорния/2009/38 (H1N1) ареактогенен для взрослых и для детей при интраназальном введении.
Таким образом, вакцинный штамм А/17/Калифорния/2009/38 (H1N1) по биологическим свойствам и показателям реактогенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 на живую гриппозную вакцину для интраназального применения.
Полученный штамм А/17/Калифорния/2009/38 (H1N1), задепонированный в ФГУН «Государственный НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора) (Россия RU, 119002, г.Москва, Сивцев-Вражек, д.41) под №801, имеет характеристики, представленные в паспорте штамма.
Характеристика штамма
Инфекционная активность штамма А/17/Калифорния/2009/38 (H1N1) при репродукции в развивающихся куриных эмбрионах при 32-33°С в течение 72 часов - 7, 5 Ig ЭИД50/0,2 мл.
Гемагглютинирующая активность - 1:64.
Штамм проявляет генетическую стабильность биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
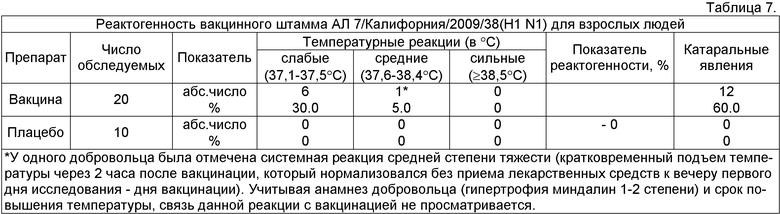
Штамм а/17/Калифорния/2009/38 (h1n1) ареактогенен для взрослых лиц
Пример 1. При вакцинации 20 взрослых человек интраназально реассортантным вакцинным штаммом А/17/Калифорния/2009/38 (H1N1) с инфекционной активностью 6,5 Ig ЭИД50/0,2 мл в объеме 0,5 мл слабые температурные реакции (до 37,5°С) наблюдались у 6 человек (30,0%), Местных и системных реакций сильной степени выраженности отмечено не было ни у одного добровольца. Все местные (60%) и системные (температурные) (30%) реакции были слабой степени выраженности, имели транзиторный характер и исчезали без применения лекарственных средств. У одного добровольца была отмечена системная реакция средней степени тяжести (кратковременный подъем температуры через 2 часа после вакцинации, который нормализовался без приема лекарственных средств к вечеру первого дня исследования - дня вакцинации). Учитывая анамнез добровольца - гипертрофия миндалин 1-2 степени - и срок повышения температуры, связь данной реакции с вакцинацией не просматривается. Катаральные явления (насморк, гиперемия зева и боль в горле) были отмечены у двух человек. Результаты обследования приведены в табл.7.
В получившей плацебо группе из 10 лиц сильных, средних и слабых температурных реакций, а также катаральных явлений не наблюдалось.
Показатель реактогенности (разница в проценте средних реакций у привитых вакциной и получивших плацебо) составил 0%.
Таким образом, вакцинный штамм А/17/Калифорния/2009/38 (H1N1) по показателям реактогенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 на живую сухую гриппозную аллантоисную вакцину для интраназального применения.
Проанализировав результаты оценки переносимости и реактогенности вакцинного штамма А/17/Калифорния/2009/38 (H1N1), был сделан вывод о хорошей переносимости и низкой реактогенности вакцины.
Изобретение относится к медицинской вирусологии. Вакцинный штамм А/17/Калифорния/2009/38 (H1N1) - реассортант, полученный путем скрещивания нового пандемического вируса А/Калифорния/07/2009 (H1N1) с холодоадаптированным температурочувствительным вирусом А/Ленинград/134/17/57 (H2N2) - донором аттенуации, безвредным для людей. Штамм А/17/Калифорния/2009/38 (H1N1) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 32-33°С, характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал гены, кодирующие поверхностные антигены вируса гемагглютинин (НА) и нейраминидазу (NA), от потенциально пандемического вируса и остальные шесть генов, кодирующих внутренние негликозилированные белки, от донора аттенуации. Изобретение может быть использовано в практическом здравоохранении для профилактики заболеваемости пандемическим гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма вируса гриппа А/17/Калифорния/2009/3 8 (H1N1). 1 ил., 7 табл.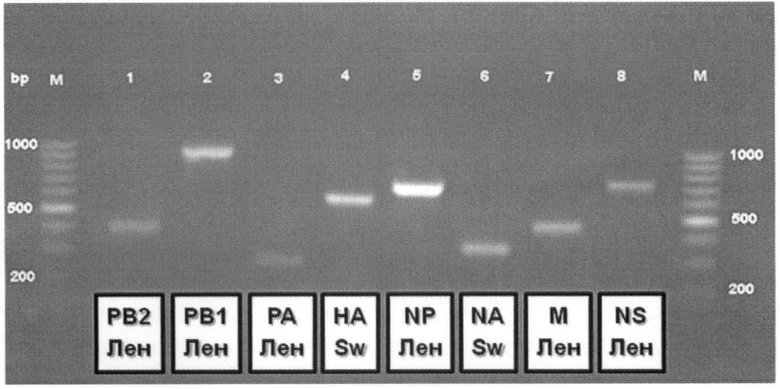
Штамм вируса гриппа А/17/Калифорния/2009/38 (H1N1), задепонированный в ФГУН «Государственный НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора) под №801, используемый для получения живой гриппозной интраназальной пандемической вакцины для взрослых и для детей.
| ШТАММ ВИРУСА ГРИППА A/47/НОВАЯ КАЛЕДОНИЯ/99/156(H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ДЕТЕЙ | 2000 |
|
RU2185437C1 |
| ШТАММ ВИРУСА ГРИППА A/17/НОВАЯ КАЛЕДОНИЯ/99/145(H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 2000 |
|
RU2183672C1 |
| ШТАММ ВИРУСА ГРИППА А/47/ПЕКИН/95/35(H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ДЕТЕЙ | 1999 |
|
RU2159810C1 |
Авторы
Даты
2011-03-10—Публикация
2009-09-16—Подача