Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики эпидемического гриппа среди взрослых живой интраназальной гриппозной вакциной из штамма А/17/Новая Каледония/99/145 (H1N1). Известный вакцинный штамм А/17/Перт/95/29 (H1N1)-прототип [1] - утратил антигенную актуальность и вследствие этого не сможет вызвать защитную реакцию во время эпидемии гриппа, вызванной штаммом, аналогичным вирусу гриппа А/Новая Каледония/20/99 (H1N1).
Задачей, на решение которой направлено заявляемое изобретение, является получение вакцинного штамма актуальной антигенной разновидности на основе эпидемического вируса А/Новая Каледония/20/99 (H1N1).
Вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) получен методом генетической реассортации эпидемического вируса А/Новая Каледония/20/99 (H1N1) с холодоадаптированным штаммом А/Ленинград/134/17/57 (H2N2) - донором аттенуации - с последующей селекцией в присутствии антисыворотки к вирусу А/Ленинград/134/17/57 (H2N2). Донор аттенуации - холодоадаптированный температурочувствительный штамм вируса гриппа А/Ленинград/134/17/57 (H2N2), разрешенный для получения безвредных живых интраназальных вакцин для взрослых [2].
Методом рестрикционного анализа ДНК копий генов вакцинного и родительских штаммов установлено, что вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) унаследовал 6 генов, кодирующих внутренние белки (РВ1, РВ2, PA, NP, M, NS) от донора аттенуации А/Ленинград/134/17/57 (H2N2) и 2 гена, кодирующих поверхностные белки - НА (гемагглютинин) и NA (нейраминидазу) - от эпидемического вируса А/Новая Каледония/20/99 (H1N1). Гемагглютинин в РТГА идентичен вирусу А/Новая Каледония/20/99 (H1N1), антисывороткой к которому полностью нейтрализуется. Штамм является температурочувствительным (разность в показателях инфекционной активности при 33oС и 40oС составляет 6.0 lg ЭИД50/0,2 мл) и холодоадаптированным (разность в показателях инфекционной активности при 33oС и 25oС - 2.0 lg ЭИД50/0,2 мл).
Таким образом, представленный вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью поверхностных белков эпидемического вируса А/Новая Каледония/20/99 (H1N1), структурой генома, оптимальной для реассортантных вакцинных штаммов, температурочувствительностью и холодоадаптированностью, что коррелирует с аттенуацией для человека, характерной для донора атгенуации.
Морфология штамма - полиморфная, типичная для вируса гриппа.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность при репродукции в развивающихся куриных эмбрионах при 33-34oС в течение 48 часов - 8,0-9,0 lg ЭИД50/0,2 мл.
Гемагглютинирующая активность -1:512-1:1024.
Штамм проявляет генетическую стабильность биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
Образец паспорта на вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) прилагается.
ПАСПОРТ ШТАММА
1 Название штамма - А/17/Новая Каледоиия/99/145 (H1N1).
2. Серия - серия 1.
3. Метод получения - рекомбинация; характеристика родительских вирусов:
а) эпидемический вирус - А/Новая Каледония/20/99 (H1N1);
б) донор аттенуации - А/Ленинград/134/17/57 (H2N2).
4. Количество пассажей - 5 в процессе рекомбинации.
5. Характеристика штамма до лиофилизации:
а) оптимальные условия репродукции - 33oС, 48 часов;
б) гемагглютинирующая активность -1:1024;
в) инфекционная активность - 8.5 lg ЭИД50/0,2 мл;
г) чувствительность к ингибиторам - ингибиторорезистентный;
д) разность в показателях инфекционной активности при 33oС и 40oС - 6.0 lg ЭИД50/0,2 мл;
е) разность в показателях инфекционной активности при 33oС и 25oС - 2.0 lg ЭИД50/0,2 мл;
ж) структура генома рекомбинанта:
- гены от эпидемического вируса - НА, NA,
- гены от донора аттенуации - PA, PB1, РВ2, NP, M, NS
6. Характеристика штамма после лиофилизации:
а) дата лиофилизации - 28 февраля 2000 года;
б) объем материала в ампуле -1 мл;
в) количество доз в серии - 3;
г) инфекционная активность - 7.5 lg ЭИД50/0,2 мл;
д) гемагглютинирующая активность -1:256.
7. Рекомендуемое разведение при вакцинации -1:3.
8. Антигенная специфичность
а) гемагглютинина - идентичен вирусу А/Новая Каледония/20/99 (H1N1) по данным РТГА с крысиной антисывороткой;
б) нейраминидазы - идентична вирусу А/Новая Каледония/20/99 (H1N1) по данным ПЦР-рестрикционного анализа ДНК-копий генов.
9. Безвредность для мышей при подкожном и внутрибрюшинном введении - безвреден.
10. Бактериологический контроль лиофилизированного материала: дата проведения - 16 марта 2000 года, результат - стерилен.
11. Контроль на отсутствие посторонних вирусов - посторонние вирусы отсутствуют.
ШТАММ ВИРУСА ГРИППА А/17/НОВАЯ КАЛЕДОНИЯ/99/145 (H1N1) АРЕАКТОГЕНЕН ДЛЯ ВЗРОСЛОГО КОНТИНГЕНТА
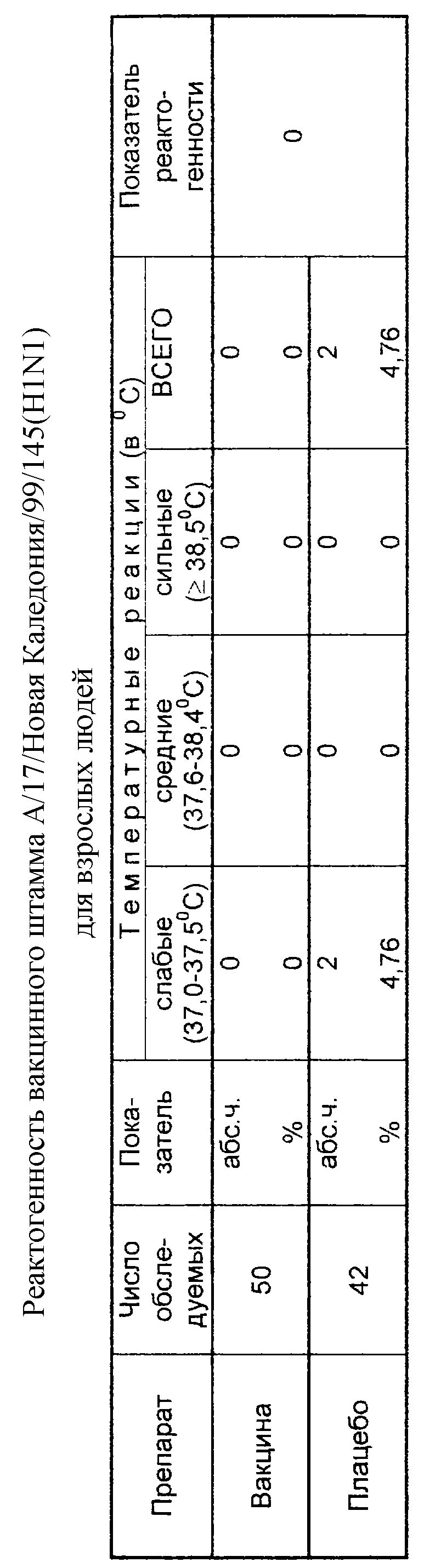
Пример. При вакцинации 50 взрослых лиц интраназально распылителем РДЖ-4М рекомбинантным вакцинным штаммом А/17/Новая Каледония/99/145 (H1N1) с инфекционной активностью 8,5 lg ЭИД50/0,2 мл в разведении 1:3 в объеме 0,5 мл сильных температурных реакций с повышением температуры свыше 38,5oС, средних реакций с повышением температуры в диапазоне 37,6-38,5oС и слабых температурных реакций до 37,5oС не наблюдалось.
В контрольной группе из 42 лиц, получивших плацебо, сильных температурных реакций с повышением температуры свыше 38,5oС и средних реакций с повышением температуры в диапазоне 37,6-38,5oС не наблюдалось. Слабые температурные реакции до 37,5oС наблюдались у двух человек (4,76%) (таблица).
Таким образом, вакцинный штамм А/17/Новая Каледония/99/145 (H1N1) по показателям реактогенности соответствует требованиям, предъявляемым Фармакопейной статьей ФС 42-3569-98 к вакцинным штаммам для живой гриппозной вакцины для интраназального применения для взрослых.
ЛИТЕРАТУРА
1. Киселева И. В. , Александрова Г.И., Руденко Л.Г., Климов А.И. Штамм вируса гриппа А/17/Перт/95/29 (H1N1) для производства живой гриппозной интраназальной вакцины для взрослых. Патент РФ N2144955 от 27.01.00. Опубл. БИ 2000.- N3.
2. Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука.-1994.-151 с.
Вакцинный штамм вируса гриппа А/17/Новая Каледония/99/145 (Н1N1) - реассортант, полученный путем скрещивания эпидемического вируса А/Новая Каледония/20/99 (H1N1) с холодоадаптированным температурочувствительным вирусом А/Ленинград/134/47/57 (Н2N2) - донором аттенуации, безвредным для взрослых людей, свойства которого дают возможность гарантированно получать реассортантные вакцинные штаммы из вновь появляющихся эпидемических вирусов. Штамм А/17/Новая Каледония/99/145 (Н1N1) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 33-34oС, характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал от эпидемического вируса два гена, кодирующих поверхностные белки (гемагглютинин и нейраминидазу), и шесть генов, кодирующих негликозилированные белки от донора аттенуации. Штамм А/17/Новая Каледония/99/145 (Н1N1) ареактогенен для взрослых людей при интраназальном введении. Таким образом, вакцинный штамм А/17/Новая Каледония/99/145 (Н1N1) по биологическим свойствам и показателям реактогенности соответствует требованиям, предъявляемым Фармакопейной статьей ФС 42-3569-98 к вакцинным штаммам для живой гриппозной вакцины для интраназального применения для взрослых. 1 табл.
Штамм вируса гриппа А/17/Новая Каледония/99/145(Н1N1) ГИСК 396/7 (Государственный институт стандартизации и контроля им. Л. А. Тарасевича), используемый для получения живой гриппозной интраназальной вакцины для взрослых.
| ШТАММ ВИРУСА ГРИППА А/17/ПЕРТ/95/29 (Н1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 1998 |
|
RU2144955C1 |
| ШТАММ А(17)ИОГАНЕСБУРГ (94)1 (НЗ N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 1996 |
|
RU2110277C1 |
| АЛЕКСАНДРОВА Г.И., КЛИМОВ А.И | |||
| Живая вакцина против гриппа | |||
| - СПб: Наука, 1994, 151 с. | |||
Авторы
Даты
2002-06-20—Публикация
2000-12-08—Подача