Изобретение относится к области медицины, в частности к неврологии, нейрохирургии и онкологии, и предназначено для лечения опухолей головного и спинного мозга, дегенеративных, гипоксических, ишемических заболеваний и травматических повреждений центральной нервной системы (ЦНС) и других заболеваний человека и животных.
Проблема лечения опухолей, дегенеративных заболеваний и повреждений головного и спинного мозга до настоящего времени остается крайне трудной и практически нерешаемой задачей. Несмотря на значительные достижения современной медицины, выживаемость больных с глиальными опухолями мозга остается на уровне не более 12-15 месяцев. Не получено существенных результатов и в лечении дегенеративных, гипоксических и ишемических заболеваний нервной системы. По-видимому, это связано, с одной стороны, с ограниченными возможностями нервной ткани к регенерации и саногенезу и особенностями нейрогенеза во взрослом мозге, а с другой стороны, со спецификой патогенеза ряда нервных болезней.
Однако за последние два десятилетия представления о возможностях лечения указанных нарушений существенно изменились. Это связано с накоплением научных фактов о регенераторном потенциале ЦНС, открытием механизмов накопления генетических мутаций в нервных клетках головного и спинного мозга при патологии ЦНС и с получением неопровержимых доказательств о возможности управления процессами регенерации, ангиогенеза и синаптогенеза в нервной ткани ([1], с.167, 194).
Концепция раковой (мутантной) стволовой клетки, сформулированная в современной научной литературе, открыла новые горизонты в лечении онкологических болезней и позволяет по-новому рассмотреть патогенетические основы возникновения нейроонкологических заболеваний и ряда нервных болезней [2]. Целая серия открытий конца XX и начала XXI в. в области клеточной и молекулярной биологии, посвященных регуляции клеточных событий в нервной клетке (дифференцировка, апоптоз, пролиферация и т.д.), позволила с новых теоретических позиций взглянуть на проблему патогенеза целого ряда нервных болезней. Раскрыты ключевые механизмы, управляющие супрессией опухолевых генов и сигнальными процессами в нервной клетке, выявлены закономерности нарушения сигнальной системы клеточной регуляции при патологических состояниях мозга [3]. Появление новых производственных технологий для получения широкого спектра химиопрепаратов из сигнальных белков клеточной и межклеточной регуляции и понимание фундаментальных механизмов их действия привели к возможности получения уникальных экспериментальных результатов их применения на животных и человеке. Это открывает огромные перспективы в решении проблемы лечения онкологических и нервных болезней. Разработка и применение новых лекарственных средств, разработанных на базе вне- и внутриклеточных сигнальных белков, дали возможность добиться существенного прогресса в лечении ряда неизлечимых ранее онкологических заболеваний. Доказана возможность прямого воздействия сигнальных белков на раковые и здоровые стволовые клетки. Однако восторженное отношение к клиническому применению сигнальных клеточных энзимов, протеинов и антител к ним для лечения нейроонкологических и ряда неврологических болезней сегодня завершилось разочарованием и неудовлетворенностью полученными результатами. Как показали многочисленные исследования применения препаратов, разработанных на базе сигнальных белков, в терапевтических концентрациях они оказались губительны для здоровой нервной ткани человека, что резко сократило возможности их использования в клинической практике [4].
Надежды на прорыв в лечении заболеваний нервной системы, в том числе и нейроонкологической патологии, в последние 15 лет возлагались на клиническое применение СК [5]. Открытие наличия нейральных стволовых клеток во взрослом мозге дало принципиально новое понимание сущности нейрогенеза [6]. Однако успехи эмпирического и экспериментального применения клеточных технологий для лечения нервных болезней также остаются достаточно скромными, и клиническое использование СК пока ограничено и имеет целый ряд существенных недостатков ([1], с.360).
В конце 90-х годов XX в., с накоплением новых данных о характере и структуре генетических дефектов при целом ряде опухолей мозга и нервных болезней, сформировалась новая научная дисциплина - генотерапия, которая в перспективе также выглядела многообещающим научным направлением в лечении нервных болезней [4]. К сожалению, успехи и генной инженерии, и генной терапии пока остаются скромными и также не увенчались большими достижениями и окончательной победой над нервными болезнями. В настоящее время генная терапия пока технологически не может дать ощутимых результатов, несмотря на широкие возможности и перспективы ее применения в неврологии, нейрохирургии и нейроонкологии.
Возникает резонный вопрос: почему прорыв в фундаментальных областях знаний, клеточной и молекулярной биологии нервной клетки не принес аналогичного биотехнологического прорыва в клинических нейроисследованиях? Ответ на этот вопрос прост, но неоднозначен. С позиций информационного подхода ([1], с.37-58) эти противоречия могут быть объяснены нестыковкой достижений и существующих подходов, полученных на разных информационных уровнях научных исследований. Технологический прорыв в биологии произошел на субклеточном, молекулярном, атомарном уровнях и экстраполировать его результаты на организменный и тканевой уровень довольно трудно и малоперспективно. Именно этим объясняются неудачи клинического применения большого спектра современных рекомбинантных белков клеточного сигналинга семейства цитокинов и нейротрофинов, а также информационных молекул сигнальных белков межклеточного и внутриклеточного взаимодействия. Следует подчеркнуть, что молекулы сигнальных белков и антител к ним крайне нестабильны и работают в микро- и нанодиапазоне. Эффективность их применения при системном (пероральном, парентральном, интратекальном и др.) применении крайне ограничена из-за резкого снижения их концентрации в биологических жидкостях организма при разбавлении в крови, ликворе, лимфатической жидкости. Кроме того, молекулы сигнальных белков имеют очень короткий период длительности своих информационных эффектов и большие возможности воздействия на различные клетки соматических органов при циркуляции их в биологических жидкостях человека и животных [7]. Крайне низкие концентрации сигнальных белков в патологических зонах мозга при системном введении вынуждают исследователей наращивать терапевтическую концентрацию препарата в крови, которая становится токсической для здоровых нейронов, сосудов мозга и соматических органов. Это приводит к тотальному и бесконтрольному воздействию этих сигнальных белков на различных уровнях организма (паренхиматозные органы, железы внутренней секреции и т д.), что вызывает регуляторный дисбаланс функционирования клеток этих органов, сопровождаемый тяжелыми осложнениями такой терапии [4].
Известны работы и исследования, описывающие базовые подходы комплементационной генной терапии опухолей и инфекционных заболеваний, когда в организм больного вводится полноценно работающий ген. Так, создание аутологичных модифицированных Т-лимфоцитов с использованием ретровирусов со встроенными генами позволяет успешно применять генетические конструкции для коррекции иммунодефицита [4]. В роли фармацевтического препарата при подобной генной терапии выступает клонированный ген или искусственно синтезированные молекулы РНК или ДНК. Как правило, в этих исследованиях трансдукция генов в клетках осуществляется ретровирусом (лентивирусом), связанным с определенным геном.
Наиболее близким аналогом (прототипом) настоящего изобретения можно считать техническое решение, заключающееся в использовании астроцитов с целью вызывания апоптоза злокачественной глиомы (Uzzaman M, Keller G., Germano Isabelle M. In vivo Gene Delivery by embryonic stem cell-derived astrocytes for malignant gliomas. Departments of Neurosurgery (MU, IMG) and Gene and Cell Medicine(GK), Mt. Sinai School of Medicine, New York, USA. Neuro Oncol Advance Publication DOI:.1215/15228517-2008-056, публ. 1 августа 2008). В данной работе было показано, что астроциты, полученные из эмбриональных ЭСК, в определенных условиях выделяют гены, которые могут быть использованы с целью вызывания апоптоза клеток злокачественной глиомы in vitro. Было доказано, что ген TRIAL (TNF-зависимый лиганд, индуцирующий апоптоз) вызывает апоптоз в различных опухолевых клетках, в том числе глиомных. Авторы этой работы оценили апоптический эффект от применения трансгенного TRIAL, доставляемого с помощью астроцитов, полученных из эмбриональных СК, в злокачественных глиомах in vivo. Голым мышам были пересажены клетки злокачественной глиомы человека А172, сформировавшие гетеротопный ксенотрансплантат. В эти ксенотрансплантаты были затем введены полученные из эмбриональных СК астроциты, выделяющие TRIAL. Экспрессия TRIAL в ксенотрансплантатах злокачественной глиомы была подтверждена ПЦР-диагностикой с обратной транскрипцией и иммуногистохимией после внешней индукции гена. Через 48 часов после инъекции астроцитов в экспериментальной группе было отмечено значительное снижение объема опухоли - 14% после одинарной дозы астроцитов и 31% после двойной дозы. Окрашивание TUNEL выявило большое количество апоптических клеток опухоли. Через 7 дней после инъекции опухоль подверглась тяжелому некрозу. Экспрессия рецептора смерти (DR4) в экспериментальных группах была значительно выше, чем в контрольных. Авторы этой работы выдвигают предположение о том, что астроциты, полученные из ЭСК и выделяющие TRAIL, могут использоваться как векторы для доставки генов в злокачественные глиомы.
Однако необходимо отметить, что указанное известное техническое решение, как и многие другие подобные способы генотерапии, имеет серьезные ограничения и до настоящего времени не было внедрено в клиническую практику. Применение рекомбинантного вирусного вектора в генной терапии крайне опасно и по данным, представленным Киселевым В.И. [4], уже однажды привело к смерти 18-летнего пациента при проведении первой фазы клинических испытаний. Было доказано, что смерть, вызванная развитием дыхательной недостаточности, отказом почек и отмиранием коры мозга, наступила в ответ на введение генно-инженерной конструкции. Поэтому авторы настоящего изобретения категорически отказались от применения трансгенных конструкций из вирусных плазмид, ретровирусов и лентивирусов, связанных с генами для их трансдукции в патологических клетках.
В настоящее время показано, что при большинстве нервных болезней фактор воспаления и стресса только запускает патологические механизмы в нервных клетках, но доминирующими процессами в патологической нервной ткани являются нарушенные механизмы клеточной регуляции, имеющие точный адрес своего происхождения - генетическую поломку в ядрах нервных клеток. В большинстве неврологических руководств описаны типичные генетические мутации, выявленные в нервных клетках при опухолях мозга, болезни Паркинсона, болезни Альцгеймера, синильных деменциях, боковом амиотрофическом склерозе, энцефалопатиях сосудистого и токсического генеза и целом ряде дегенеративно-атрофических заболеваний ЦНС. Выявление этих генетических поломок в настоящее время не вызывает серьезных технических проблем, если использовать современные методы геномного и протеомного анализа клеток патологического очага. Главной проблемой является интерпретация полученных результатов этих суперсовременных исследований и отсутствие реальной возможности для коррекции выявленных генетических дефектов. Применение генной терапии для коррекции конкретной молекулярной поломки методологически оправдано, но сопряжено с рядом технических и технологических трудностей современного этапа научных исследований. Решение проблемы может быть предложено не в исправлении конкретного генетического «разлома» мутантных генов (генетического дефекта) и замены поврежденного гена, а в задании нового вектора (направления) развития всего клеточного цикла патологической клетки и клеток всей патологической зоны. В этом случае, учитывая блочный характер вовлечения генов клетки в биоуправление и регуляцию, мутации генов (даже в нескольких различных локусах хромосом), приводящие к определенному клеточному циклу, не будут определяющими для жизни и развития всей клетки. Например, если исходом патогенетических процессов в нервной ткани является запуск механизма внутриклеточного апоптоза мутантной нервной СК, то очевидно, что необходимо поменять вектор всех клеточных процессов на индукцию направленной дифференцировки или направленной пролиферации, и наоборот. Это можно сделать, если использовать новый подход - перепрограммирование трансдукции (экспрессии или ингибирования) ключевых генов клетки сигнальными белками. Иллюстрацией этого положения служит работа ключевого гена опухолевой супрессии р53. Снижение экспрессии этого гена ниже нормальных величин запускает работу целого каскада генов в ядре клетки, результатом становятся антиапоптозный эффект, неоангиогенез, пролиферация и клеточное размножение (патогенетические и патофизиологические условия формирования опухоли), а повышение экспрессии р53 приводят к запуску апоптоза, нарушению ангиогенеза, нарушению клеточной миграции и остановке процессов образования новых клеток (патогенетические звенья атрофических и дегенеративных процессов в мозге). Следовательно, управление ключевыми генами может стать основой управления основными клеточными процессами в заданном (репрограммированном) исследователем направлении развития определенных физиологических и алгоритмированных процессов в клетке.
Таким образом, учитывая недостаточность существующей биотехнологической базы генной терапии и отсутствие адекватного носителя генов, в настоящее время целесообразно отказаться от разрушения или приостановки функционирования патологических нервных клеток путем исправления дефектов конкретных мутантных генов и попытаться осуществить биокоррекцию развития клеточных процессов в патологической ткани, задавая программируемый вектор направления развития определенного клеточного цикла. Сегодня созданы все теоретические предпосылки и технологические возможности для осуществления такой биокоррекции (биорегуляции). Достаточно хорошо изучены механизмы клеточного и межклеточного сигналинга, возникновения и динамики развития апоптоза, клеточной дифференцировки, пролиферации и других клеточных процессов. Расшифровано большое количество участвующих в этих процессах сигнальных белков и созданы их рекомбинантные копии и антитела, которые свободно продаются ведущими мировыми биотехнологическими компаниями, например Sigma-Aldrich Corp. (США) и Millipore Corporation (США), а также широко используются различными фармацевтическими компаниями для проведения клинических испытаний в онкологии, неврологии и нейрохирургии.
Однако до настоящего времени не известен универсальный «минибот» для транспортировки сигнальных белков к месту их действия. Современная научная литература в области молекулярных исследований предлагает рассмотреть в качестве кандидатов на эту роль различные модифицированные бактерии, генно-инженерные конструкции и самосборные атомарные нанокострукции (наноботы). Разработаны различные иммунные моноклональные самонаводящиеся антительные бинарные системы со стрептаведином и биотином и иммунолипосомальные наноконструкции, позволяющие осуществить векторный суперселективный транспорт сигнальных молекул к различным клеткам опухоли или патологической зоны [4]. Однако эффекты, достигаемые этими препаратами, очень грубые и разрушающие, поэтому эти препараты не могут претендовать на использование их для целей коррекции клеточного сигналинга и биоуправления процессами в клетке.
Таким образом, возникла необходимость в разработке нового трансферного механизма доставки сигнальной информации, который бы смог обеспечить передачу информационного сигнального воздействия на уровень генома патологической клетки, минуя клетки соматических органов и здоровые клетки мозга, интегрировать взаимодействия на различных информационных уровнях и осуществить систему биоуправления и регуляции патологическим процессом на клеточном и межклеточном уровнях. Нужны новые методология и логистика целевого трансфера сигналов к конкретным генам клеток-мишеней патологической зоны в ЦНС.
Опираясь на фундаментальные принципы теории управления систем [8], можно предположить базовые принципы и механизмы регуляции вне- и внутриклеточного биосигналинга [9]. Для этого необходимо разработать определенные алгоритмы кратковременного управляющего сигнального воздействия (экспрессия, стабилизация, ингибирование) на определенные (ключевые) гены клетки и на основании этих алгоритмов запрограммировать сигнальное управляющее воздействие на объект управления (ОУ). ОУ должен адекватно и постоянно реагировать на клеточный сигналинг. Ответ на воздействие на ОУ необходимо мониторировать и регистрировать, что позволит постоянно осуществлять его коррекцию и управление []. А мощность, периодичность и продолжительность сигналов не должны разрушать управляемую систему, которой и является клетка. Для этих целей существующие технологии иммунолипосомальных конструкций и бинарных систем не подходят, так как обладают очень «жесткими» параметрами воздействия на клетку.
В качестве управляемого «биобота» для трансфера сигналов к патологической клетке авторы настоящего изобретения рассмотрели здоровую СК человека и животных, которая по своей природе является универсальной управляющей системой, генетически запрограммированной на восстановление повреждений и регенерацию в поврежденных органах и тканях. Она обладает уникальной способностью мигрировать в зоны патологии по градиенту концентрации хемокинов и локальных провоспалительных факторов и может в полном объеме выполнить функции трансфера для необходимых сигнальных молекул. Анализ целого ряда научных фактов по функционированию СК в патологической зоне показывает, что при определенных клеточных событиях патологических клеток (например, при апоптозе) здоровая СК получает определенные сигналы от этих клеток, обрабатывает их и посылает обратные сигналы (на «выживание») поврежденным клеткам. Таким образом, СК осуществляют межклеточное и внутриклеточное биоуправление локальным саногенезом и репативными функциями клеток в ткани. В зависимости от степени повреждения патологические клетки реагируют на данные сигналы (каскад цитокинов и нейрофических и других информационных факторов, выделяемых СК) и в них индуктивно запускаются сигнальные системы, способствующие формированию необходимых регенераторных процессов.
Таким образом, основной задачей настоящего изобретения является создание такого препарата стволовых клеток с репрограммированным клеточным сигналингом, который обеспечил бы целевую доставку сигнальных веществ (т.е. сигнальных белков и фармацевтических препаратов, способных к регулированию сигнальных путей) строго в пораженную зону организма млекопитающего, а также запуск в заданное время и длительную поддержку активного сигнального межклеточного воздействия заданного терапевтического характера со стороны здоровой и хорошо управляемой СК на управляющую систему дефектной (мутантной нервной или раковой) клетки.
Решение указанной задачи достигается тем, что согласно настоящему изобретению предложен препарат стволовых клеток с репрограммированным клеточным сигналингом, содержащий базовый препарат стволовых клеток, в мембрану, и/или ядро, и/или цитоплазму которых имплантирован способный к регулированию сигнальных путей стволовых клеток и клеток патологического очага в организме млекопитающего белковый или фармацевтический препарат, предварительно инкапсулированный в наноконтейнеры, полученные из биодеградируемого материала, интактного для органелл и компартаментов стволовых клеток базового препарата и имеющего заданные сроки биодеградации в организме млекопитающего для обеспечения программируемого выхода белкового или фармацевтического препарата во внутри- или межклеточное пространство стволовых клеток и осуществления тем самым перепрограммирования сигнальной трансдукции ключевых генов стволовых клеток в требуемом терапевтическом направлении развития физиологических событий клеточного цикла непосредственно в патологической зоне органа или ткани организма.
В качестве стволовых клеток базового препарата использованы преимущественно аутологичные стволовые клетки.
Размер наноконтейнеров не превышает 100 нм.
В качестве наноконтейнеров могут быть использованы наноконтейнеры на основе биополимерного материала. В качестве биополимерного материала могут быть использованы сополимеры полилактидгликолида и/или полиоксибутиратвалерата.
В качестве наноконтейнеров могут быть использованы также наноконтейнеры на основе липосом или наноэмульсии.
Другой задачей настоящего изобретения является разработка способа получения указанного препарата стволовых клеток с репрограммированным клеточным сигналингом.
Решение указанной второй задачи достигается тем, что согласно настоящему изобретению предложен способ получения препарата стволовых клеток с репрограммированным клеточным сигналингом, включающий в себя выбор базового препарата стволовых клеток, выбор белкового или фармацевтического препарата, способного к регулированию сигнальных путей стволовых клеток и клеток патологического очага в организме млекопитающего, инкапсулирование выбранного белкового или фармацевтического препарата в наноконтейнеры из биодеградируемого материала, интактного для органелл и компартаментов стволовых клеток базового препарата и имеющего заданные сроки биодеградации в организме млекопитающего, и последующую имплантацию наноконтейнеров в мембрану, и/или ядро, и/или цитоплазму стволовых клеток базового препарата.
В качестве базового препарата выбирают преимущественно препарат с аутологичными стволовыми клетками.
Инкапсулирование можно проводить путем ультрадиспергирования смеси биополимерного материала с белковым или фармацевтическим препаратом.
Имплантацию наноконтейнеров можно проводить путем прямых внутриклеточных инъекций суспензии или эмульсии наноконтейнеров в мембрану, цитоплазму или ядро стволовых клеток базового препарата, а также путем эндоцитоза наноконтейнеров в цитоплазму стволовых клеток при экспозиции суспензии или эмульсии наноконтейнеров в базовом препарате.
Преимущественно заявленный способ получения заявленного препарата проводят в стерильных условиях или непосредственно в операционной (ex temporo), или в культуральной лаборатории.
Кроме того, согласно настоящему изобретению предложено применение заявленного препарата СК в качестве средства для внутри- и внеклеточной регуляции сигнальных путей патологических клеток при лечении заболеваний, повреждений и опухолей головного и спинного мозга, а также опухолей и метастатических поражений других органов и систем млекопитающего.
Механизм действия заявленного препарата СК с репрограммированным клеточным сигналингом обусловлен направленной миграцией в патологическую зону мозга или другого органа млекопитающего содержащихся в препарате СК с имплантированными в них сигнальными молекулами белкового или фармацевтического препарата, инкапсулированными в биодеградируемые наноконтейнеры. В результате строго заданной по времени биодеградации наноконтейнеров происходит запрограммированное высвобождение сигнальных молекул из наноконтейнеров в СК или межклеточное пространство патологической зоны и осуществляется заданное воздействие сигнальных молекул на внеклеточные и внутриклеточные сигнальные пути и трансдукцию генов с целью формирования терапевтических индуктивных клеточных процессов (инструктивного апоптоза, управляемой дифференцировки, индуктивной пролиферация и т.д.) в патологической зоне.
Теоретическим и экспериментальным обоснованием создания заявленного клеточного препарата с репрограммированным клеточным сигналингом явились собственные исследования авторов настоящего изобретения, а также убедительные экспериментальные доказательства, опубликованные в литературе [6], где показано, что СК способны мигрировать в опухоль и(или) зоны повреждения мозга по градиенту концентрации воспалительных хемокинов. Отработанные в эксперименте доказательства миграционных способностей НСК и гемопоэтических СК показали универсальность данного феномена для всех типов СК. Способности целевой миграции СК в патологические зоны мозга позволяют использовать СК в качестве универсального транспортного средства для доставки необходимых информационных и сигнальных воздействий в патологические зоны.
Препарат разрабатывался на экспериментальной модели опухоли мозга (глиоме С6), но в процессе создания и экспериментальном применении этого препарата открылись универсальные возможности его использования не только при патологии ЦНС, но и при заболеваниях других органов и систем человека и животных.
Необходимо отметить, что предлагаемое согласно настоящему изобретению использование здоровых СК в качестве средства доставки сигнальных веществ к пораженным зонам в организме возможно только при выполнении определенных условий, а именно:
1. В зоне патологического процесса должна быть завершена острая фаза воспаления и практически снивелировано до минимума действие доминантных локальных воспалительных и деструктивных патогенетических факторов повреждения.
2. Повреждение или патогенное воздействие не должно приводить к необратимой мутации генов в ядре пострадавших клеток.
3. Должны сохраниться возможности обеспечения функционирования микроокружения патологической клетки.
В остальных случаях патологическая клетка становится нечувствительна к управляющим сигналам здоровой СК. Более того, в научной литературе описаны случаи формирования опухолей в тканях после трансплантации в них СК из-за трансформации здоровой СК в мутантную (раковую) СК под воздействием агрессии факторов воспаления и некроза. Поэтому применение первичных и даже культивированных СК без изменения клеточного сигналинга в них вряд ли оправдано при наличии острого воспаления, аутоиммунного процесса, атрофическом процессе, опухолях и в большинстве случаев противопоказано при целом ряде нервных болезней. В этих случаях необходимо усилить природные возможности к биорегуляции и регенерации собственных СК, что возможно при перепрограммировании функциональных возможностей первичных СК на генетическом уровне.
Если руководствоваться фундаментальными принципами теории управления систем, то в соответствии с настоящим изобретением объектом управления (ОУ) становится патологически измененная мутантная клетка, а управление на себя должна взять здоровая управляемая СК. Чтобы лучше понять и спрогнозировать поведение ОУ, можно воспользоваться кибернетическим принципом математической теории колебаний, согласно которому управляющей в системе является более медленная фаза [8]. Экстраполируя математический подход к системе клеточных взаимодействий, можно утверждать, что наиболее медленной фазой в развитии цикла клетки является функционирование самой СК. Нервная СК имеет самую медленную активность биологических процессов в нейрогенезе (полный цикл деления взрослой СК составляет 21 день, а ее предшественников - 12 часов). Мутантная (например, раковая) СК при глиоме имеет еще более медленный цикл деления (28 дней), и соответственно здоровая СК по отношении к ней является управляемой и соподчиненной. Поэтому сигналы здоровой СК не являются управляющими для мутантной (раковой) СК. Именно заторможенность биологических процессов в раковой клетке делает ее малочувствительной к лучевой и химиотерапии, тогда как активно делящиеся клетки полностью отвечают на лучевую нагрузку и химиотерапевтическое воздействие. Наиболее вероятно, что мутантная СК функционирует по принципу разомкнутого управления. Сущность этого принципа состоит в том, что программа управления жестко определена задающим устройством (задающим сигналом). Управление не учитывает влияния возмущений на параметры процесса. Здоровая СК работает по принципу компенсации и принципу обратной связи. Сущность принципа компенсации заключается в возможности коррекции управляющего воздействия при отклонении от заданной величины на входе ОУ путем суммирования сигнала управляющего устройства с корректирующим воздействием, пропорциональным возмущению и компенсирующим его влияние. Принцип обратной связи базируется на том, что управляющее воздействие корректируется в зависимости от выходной величины сигнала. Если значение выходной величины отклоняется от требуемого, то происходит корректировка сигнала с целью уменьшения данного отклонения.
Таким образом, с кибернетических позиций теории управления систем становится понятна глубинная сущность неэффективности лечения нейроонкологической и нейродегенеративной патологии существующими терапевтическими подходами. К решению этих проблем можно подойти с новых методологических позиций. Классической иллюстрацией математического принципа разомкнутого управления в технике является магнитофон, который функционирует в строго заданном режиме воспроизведения звука и не реагирует ни на какие внешние воздействия. Но с помощью сигнального воздействия (реостата сопротивления, вставленного в электрическую цепь) можно замедлить или убыстрить воспроизведение звука. Трансформируя вышеизложенное на биологический язык, соответствующими доминантными сигналами можно ускорить или усилить активность управляющей мутантной СК и сделать ее управляемой в общем континууме изучаемых клеточных систем, подчинить сигналингу здоровой СК и, как следствие, повести в заданном терапевтическом направлении функционирование клеточного цикла. Более того, изменив биологическую функциональную активность раковой СК, можно сделать ее восприимчивой к стандартным режимам лучевой и химиотерапии.
В соответствии с вышеизложенным проблема разработки новых методов лечения нервных и онкологических болезней с использованием настоящего изобретения переходит в плоскость управления взаимодействием двух биологических систем: с одной стороны мутантная (раковая) СК, с другой - здоровая СК.
При решении вышеуказанной задачи, касающейся запуска и длительной поддержки активного сигнального межклеточного воздействия со стороны здоровой СК на управляющую систему дефектной клетки, необходимо обеспечить возможность постоянной генерации сигнала определенной силы внутри здоровой стволовой клетки, учитывая то, что здоровая СК, являясь генетически детерминированным биологическим объектом, способна мигрировать в зону опухоли или патологический очаг пациента. В этой связи запустить работу ключевых генов воздействием на известные сигнальные механизмы не представляет большого труда. Старт репрограммирования СК можно осуществить при химическом, физическом или интервенционном воздействии на СК молекулами сигнальных рекомбинантных белков или антител к ним in vitro перед трансплантацией СК пациенту. Эффект данного воздействия в ряде случаев будет достаточно сильным, но кратковременным и нестойким. Это может привести к разбалансировке функционирования компартаментов СК и нарушить ее миграционные и навигационные способности. Поэтому согласно настоящему изобретению предложено новое техническое решение по репрограммированию трансдукции ключевых генов соматических СК - инкапсулировать белковые и фармацевтические препараты клеточного сигналинга (т.е. препараты, способные к регулированию сигнальных путей стволовых клеток и клеток патологического очага в организме млекопитающего) в наноконтейнеры из биодеградируемого материала, интактного для органелл стволовой клетки, и имплантировать наноконтейнеры с находящимися в них препаратами клеточного сигналинга в мембрану, ядро или цитоплазму СК. Это обеспечивает целевую доставку здоровых СК в пораженную зону организма и активизацию (запуск) терапевтических индуктивных клеточных процессов, таких как апоптоз, пролиферация, дифференцировка, биоактивация клеточных процессов и т.д.) именно в этой пораженной зоне в результате разрушения биодеградируемой оболочки наноконтейнеров в заданный период времени и предотвращение за счет этого нежелательного, а во многих случаях, и опасного действиям указанных препаратов клеточного сигналинга на здоровые клетки других участков организма пациента.
Заданные временные параметры биодеградации материала наноконтейнеров позволяют информационным молекулам цитокинов и нейротрофических факторов выходить из бионейтральной оболочки наноконтейнера (нанокапсулы) в цитоплазму СК через строго определенное время после введения предложенного препарата СК пациенту и осуществлять запрограммированное воздействие сигнальных молекул на необходимые компоненты сигнальных путей и(или) гены ядра клетки, вызывая их экспрессию (индукцию) и направляя развитие клеточного цикла в заранее определенном терапевтическом направлении посредством внутриклеточных или внеклеточных сигналов.
Методология выделения ключевых (управляющих) генов основана на фундаментальных принципах теории управления систем и на результатах транскрипционно-протеомного анализа биоптата патологического участка нервной ткани данного пациента, культуры его мутантных (раковых) СК, выделенных из биоптата, и нативных мобилизованных здоровых СК пациента. Ключевыми генами должны считаться только те гены, экспрессия белков которых значительно ниже показателей нормы. Параметры нормы в каждом конкретном случае определяются на основании изучения экспрессии протеинов здоровых СК пациента при проведении их транскрипционно-протеомного анализа. Количественные показатели экспрессии белков выделенных ключевых генов мутантной (раковой) СК являются базовыми для анализа и подбора сигнальных молекул с целью выбора требуемого белкового или фармацевтического препарата и расчета их безопасной концентрации при имплантации в нативные здоровые СК пациента.
Методология выбора сигнальных молекул для репрограммирования экспрессии (индукции) ключевых генов аутологичных СК должна базироваться на следующих положениях:
1. Сигнальная молекула должна регулировать экспрессию (индукцию) тех сигнальных систем или ключевых генов здоровой СК, функционирование которых обеспечит формирование нового внутриклеточного сигнального пути, результатом чего станет образование внеклеточного или внутриклеточного сигнала, необходимого для развития событий определенного запрограммированного клеточного цикла.
2. В структуре сигнального пути определенного клеточного события сигнальная молекула должна обеспечить строгое развитие клеточных событий по заданному сценарию на разных этапах сигнального пути от ее освобождения до реализации внеклеточного ответа СК.
3. Сигнал внеклеточного ответа СК, запущенный внутриклеточной управляющей сигнальной молекулой, должен изменить биологическую активность клетки и направление ее физиологического функционирования.
При выборе сигнального препарата сигнального вещества (белкового или фармацевтического) целесообразно руководствоваться нижеперечисленными базовыми принципами репрограммирования трансдукции (экспрессии или индукции) ключевых генов здоровых СК.
Принцип разноуровневости сигнального воздействия. Сущность принципа заключается в воздействии внеклеточного сигнала здоровой СК не менее чем на три различных рецептора или сигнальных пути мутантной (раковой) СК, что позволит дублировать управляющий сигнал на внеклеточном и внутриклеточном уровнях.
Принцип одновекторности применения различных сигналов заключается в воздействии различных внеклеточных сигнальных молекул нативной СК на сигнальные пути мутантной (раковой) СК в рамках строго заданного сценария развития событий клеточного цикла (например, развития инструктивного апоптоза).
Принцип доминантности управляющего сигнала здоровой СК предполагает, что запрограммированное сигнальное воздействия здоровой СК на мутантную (раковую) СК должно обеспечить повышение активности экспрессии ее ингибированных ключевых генов (преимущественно не менее чем в 2 раза).
В отличие от известных методов генотерапии, настоящее изобретение не ставит задачу восстановления поврежденных генов, создания мутантных генов, постоянно продуцирующих определенный белок, лизирования генов или блокирования способности к трансляции данного гена. В настоящем изобретении предлагается «блочное» управление экспрессией (индукцией) ключевых генов в конкретном физиологическом направлении развития определенного комплекса клеточных событий. Согласно настоящему изобретению клеткой-мишенью становится не только опухолевая и раковая СК, но и здоровая аутологичная СК, трансплантированная пациенту. В настоящем изобретении показана возможность биоуправления СК за счет интервенционного программируемого воздействия факторов внутриклеточной и внеклеточной регуляции (молекулы сигнальных белков) на гены раковой и здоровой СК с использованием физиологических механизмов клеточного сигналинга.
Транскрипционно-протеомным сравнительным анализом раковой СК и клеток опухоли со здоровыми СК пациента определяются ключевые гены и сохранные звенья генома патологической клетки, а также выявляются нарушения сигнальных путей генома опухолевой клетки [7]. Контролем для сравнения являются показатели экспрессии генов здоровых (гемопоэтических, нейральных или мезенхимальных) СК. Ключевые гены раковой СК определяются как гены с самой низкой экспрессией, а самые высокие показатели экспрессии генов позволяют верифицировать структуру нарушений сигнальных путей. Анализ экспрессии выделяемых ключевых генов раковой СК и опухолевых клеток позволяет выявить патологию основных сигнальных путей клеток патологической зоны в мозге, мониторировать молекулярные процессы, проходящие в патологической клетке при проводимой терапии как in vitro, так и in vivo, а также оценить эффективность и качество проводимой терапии. Последующее лечение с помощью предложенного препарата СК обеспечивает запуск инструктивных индукционных управляемых клеточных процессов в патологических клетках (индукционный инструктивный апоптоз, индукционная направленная дифференцировка и коммитирование клеток в опухоли, индукционная программируемая пролиферация, репрограммируемая активация экспрессии ключевых генов для повышения активности раковых СК с целью усиления эффективности лучевой и химиотерапии и т.д.). Воздействие на трансдукцию генов и сигнальные пути клеток-мишеней осуществляется короткими индукционными сигналами клеточно-межклеточного взаимодействия, поступающими от сигнальных молекул (цитокинов, моноклональных антител, рекомбинантных лиганд, факторов роста, белков теплового шока и т.д.), высвобождающихся из биодеградируемых наноконтейнеров, в результате чего запускается действие промоторов или ингибиторов генов ядра СК. Сигналы начинают поступать внутрь клетки и во внеклеточное пространство по истечении заданного времени после введения предложенного препарата СК в организм пациента. Это время определяется временем начала биодеградации наноконтейнеров и необходимо для того, чтобы СК предложенного препарата в результате своей способности к миграции в патологическую зону организма успели доставить наноконтейнеры с молекулами сигнального вещества в эту зону. При этом необходимо обеспечить многовекторность и многоуровневость воздействия на различные рецепторы одних и тех же клеток-мишеней в терапевтическом направлении.
Настоящее изобретение поясняется чертежами.
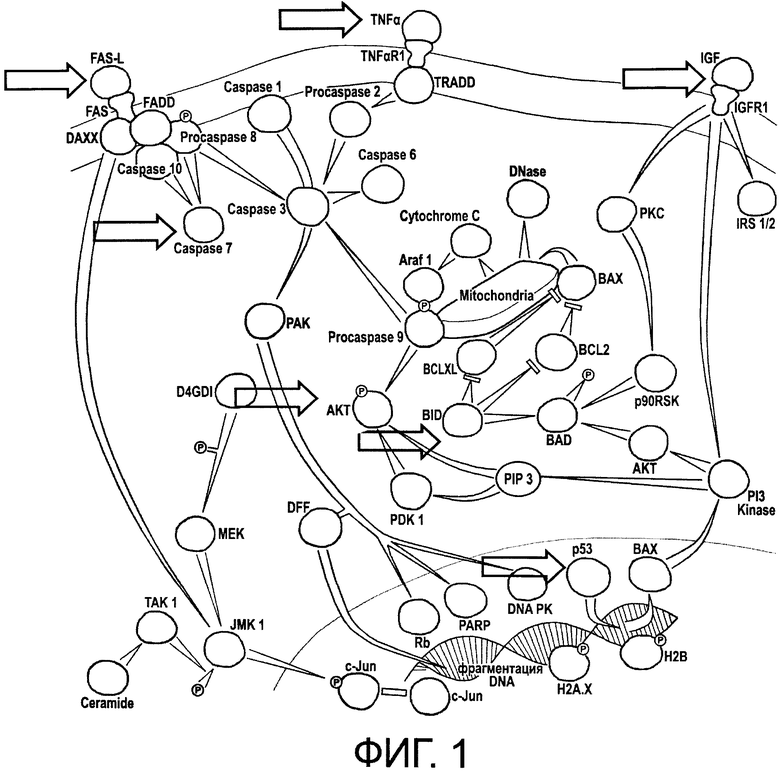
На фиг.1 представлена схема сигнальных путей формирования апоптоза (стрелками показаны возможные точки приложения регуляторного сигнального воздействия для формирования алгоритмированной регуляции апоптоза в аутологичной СК);
на фиг.2 - полученное с помощью электронного микроскопа изображение наноконтейнеров с белковым препаратом (наноконтейнеры получены на основе биополимеров);
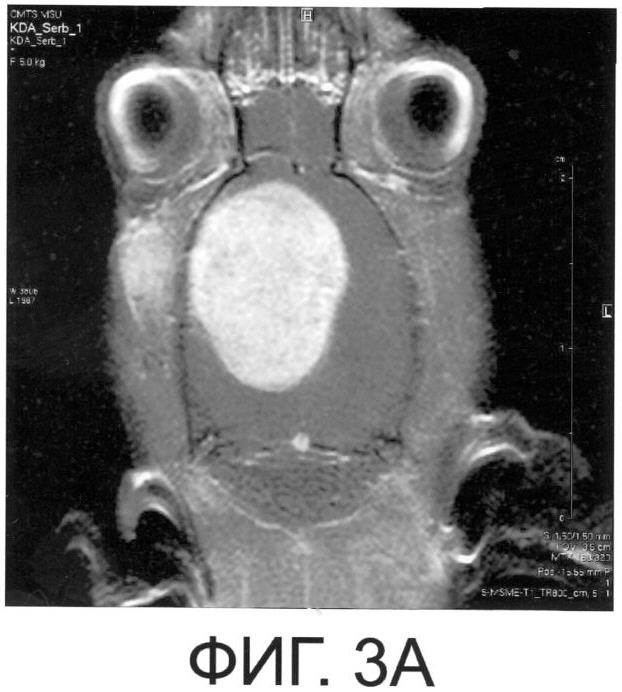
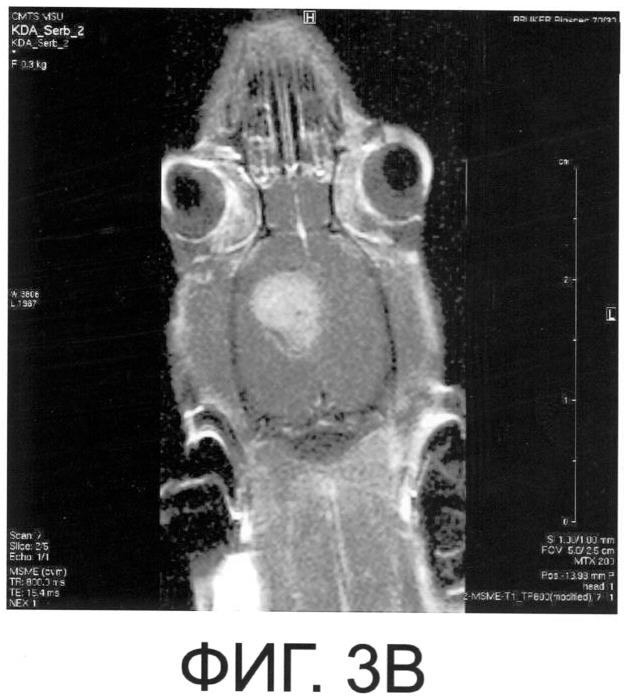
на фиг.3 - МРТ головного мозга крысы с экспериментальной глиомой С6 на восемнадцатые сутки (фиг.3А) и двадцать шестые сутки (фиг.3В) после имплантации предложенного препарата СК с наноконтейнерами, содержащими промоторы апоптоза (аксиальная проекция; Т1 - взвешенное изображение, контрастированное Магневистом).
Ниже описаны преимущественные примеры осуществления способа получения заявленного препарата СК с репрограммированным клеточным сигналингом согласно настоящему изобретению.
Выбор базового препарата СК
Изготовление базового клеточного препарата осуществлялось на основе стандартного препарата гемопоэтических СК, способ приготовления которого описан в патенте RU 2283119 (МПК А61К 35/14, 2006) на «Препарат аутологичных гемопоэтических стволовых клеток, способ его получения, криоконсервации и использования для травматической болезни центральной нервной системы».
Для базового препарата могут использоваться также аутологичные нейральные стволовые клетки (НСК), полученные из обонятельной выстилки слизистой носа пациента. Методика и протокол получения НСК опубликованы [11-14].
Ткань обонятельной выстилки, включающую обонятельный эпителий и слой соединительной ткани (lamina propria), получают от пациентов и обрабатывают по стандартному культуральному протоколу, описанному в научной литературе [15, 16]. Под местной анестезией у пациента берут фрагменты слизистой оболочки размером × 5 мм, которые иссекают из верхнего отдела верхней носовой раковины. Полученную ткань доставляют в лабораторию в охлажденном сбалансированном солевом растворе Хенкса (HBSS) без Са2+ и Mg2+, содержащем антибиотики и антимикотики (1:100; Gibco, Sigma). Время доставки не должно превышать 2 часов. После повторной промывки в том же растворе из слизистой оболочки удаляют кровеносные сосуды, после чего ткань измельчают и инкубируют в течение 40 минут при 36,5°С в растворе трипсина/ЭДТА 0,25%, приготовленном на 0,01 М фосфатном буфере (PBS, рН 7,4). Действие ферментов блокируют средой DMEM (Gibco), содержащей 3% сыворотки. Ткань промывают в трех сменах раствора Хенкса (HBSS) и диссоциируют повторным пипетированием в питательной среде. Состав среды: минимальная среда Игла (MEM, Sigma) 90%, эмбриональная сыворотка телят (FBS, Gibco, Ivitrogen), глюкоза 0,8%, глутамин 2 мМ (Gibco), добавок В27 (Sigma), HEPES 20 мМ, а также ростовые факторы (только для первичных культур) - фактор роста фибробластов (FGF2, 1 нг/мл, Sigma) и нейроростовой фактор (NGF 2 нг/мл, Sigma).
Полученную суспензию клеток центрифугируют (3 мин при 1200 об/мин), а осадок ресуспендируют в питательной среде того же состава.
Количество и жизнеспособность диссоциированных клеток определяют в камере Горяева после окраски 0,1% раствором трипанового синего. Для последующего культивирования используют клеточные суспензии только с 85-95% жизнеспособных клеток.
Диссоциированные клетки (5·105 кл/мл) культивируют в 12-луночных планшетах на полилизин-ламининовом субстрате в течение 14 суток (36,5°С, 5% СО2). Частичную смену 1/3 части питательной среды производят два раза в неделю. Первичную культуру после формирования сливного монослоя снимают с помощью раствора трипсина/ЭДТА. После промывки в HBSS и центрифугирования клетки ресуспендируют в питательной среде. Клеточную суспензию (10000-12000 кл/см2) переносят в 12-луночные планшеты или флаконы (площадь 25 см2). Таким способом культуры пассируют 4 раза до формирования сливного монослоя. Формирующиеся в клеточном монослое прикрепленные к субстрату и свободноплавающие нейросферы отбирают с помощью Пастеровских пипеток и диссоциируют описанным выше методом ферментной обработки. Выделение нейросфер позволяет отделить их от прикрепленных к субстрату обкладочных глиальных клеток, фибробластов и стромальных (опорных) клеток. Клеточную суспензию клеток нейросфер после промывки и центрифугирования ресуспендируют в питательной среде и культивируют в 12-луночных планшетах (10000-12000 кл/см2) и на покровных стеклах (18×18 мм) в чашках Петри до формирования сливного монослоя. Полученные культуры используют для цитологических и иммуноцитохимических исследований. Часть клеток последних пассажей замораживают в среде для криоконсервирования (90% сыворотки, % диметилсульфоксида) и хранят в жидком азоте.
Клеточный монослой фиксируют в 4% растворе параформальдегида, приготовленном на 0,01 М фосфатном буфере (рН 7,4) в течение 30 мин. После промывки в PBS (3 × мин) клетки инкубируют 24 часа при 4°С с первичными антителами к β-тубулину (1:300, Chemicon), нестину (1:100, Chemicon) и нейрональной специфической енолазе (1:100, антитела получены в лаборатории заявителя настоящей заявки). После промывки в PBS клетки последовательно обрабатывают биотинилированными антителами с авидин-биотиновым комплексом (АВС, Vector Laboratories, Inc) и раствором диаминобензидина, приготовленным на фосфатном буфере (DBA 0,5 мг/мл, перекись водорода 0,03%). Препараты обезвоживают и заключают под покровные стекла в синтетическую смолу (Entellan, Merk).
Чтобы исключить возникновение реакций «трансплантат против хозяина», для получения базового препарата необходимо применять только аутологичный биоматериал, например НСК, выделенные из обонятельной выстилки носа пациента или препарат культуры гемопоэтических стволовых клеток (CD34+), выделенных из высокоочищенной смеси мононуклеаров, полученных из лейкоконцентрата мобилизованных СК периферической крови пациента. Могут быть также использованы культуры мезенхимальных СК, полученных из биоптата костного мозга пациента. Однако нельзя полностью исключить возможность использования базового препарата и из алогенных СК.
Выбор белкового или фармацевтического препарата
Сигнальные белки или фармацевтический препарат, способный к регулированию сигнальных путей СК и клеток патологического очага, выбираются в каждом конкретном случае индивидуально в зависимости от задач индукционной клеточной терапии.
В нижеприведенной таблице представлены примеры терапии с использованием известных сигнальных веществ (агентов, влияющих на раковую СК или ее нишу), которые могут быть использованы в настоящем изобретении.
Учитывая, что апоптоз в настоящее время является самым изученным клеточным процессом, было решено отрабатывать новый клеточный препарат с репрограммируемыми свойствами именно на модели этого физиологического клеточного события. Общая схема сигнальных путей формирования апоптоза представлена на фиг.1. Из схемы видно, что процессы апоптоза запускают внеклеточные молекулы сигнальных белков фактора некроза опухоли (TNFa), белки рецепторов смерти (FAS-L), инсулиновый фактор роста (IGF). Активировать процесс можно также и на внутриклеточном уровне, воздействуя на каспазы и ген р53. Таким образом, для целей программирования индукционного инструктивного апоптоза в опухоли мозга в качестве сигнальных белков должны быть выбраны вещества, участвующие в сигнальных цепях апоптоза. Примерами таких веществ могут служить рицин и вискумин.
Авторами настоящего изобретения было организовано проведение экспериментов по проверке цитотоксического действия рицина и вискумина на клетки нейроглиомы С6. Было показано, что эти белки обладают высокой функциональной активностью по отношению к клеткам данной линии. Величина ЛД50 составила 5×10-12 моль для рицина и 5×10-1 моль для вискумина. С использованием четырех специфических методов было показано, что оба белковых токсина вызывают апоптоз клеток нейроглиомы С6. С помощью микроскопических методов удалось выявить фрагментацию ядер и экспозицию фосфатидилсерина на клеточной мембране. Использование проточного цитофлуориметра позволило выявить процент клеток, в которых наблюдается фрагментация ДНК после обработки данными токсинами. Электрофорез выявил специфическую фрагментацию ДНК, характерную для действия каспаза-3-зависимой апоптотической эндонуклеазы CAD.
В качестве примера фармацевтического препарата, используемого в заявленном изобретении, можно указать рапамицин, подавляющий рост раковых СК и стимулирующий рост нормальных СК (см. таблицу).
Инкапсулирование выбранного белкового или фармацевтического препарата в наноконтейнеры из биодеградируемого материала
Авторами настоящего изобретения были разработаны определенные технические условия для производства наноконтейнеров (нанокапсул):
1. Размер нанокапсул не должен превышать 100 нм.
2. Нанокапсула должна внутри себя герметично содержать молекулы сигнального вещества и быть покрытой снаружи биодеградируемой биополимерной или липосомальной оболочкой, биологически нейтральной для организма и имеющей заданные сроки ее биодеградации внутри организма.
3. Нанокапсулы должны быть нейтральными для внутренних компартаментов клетки и не очень сложными в производстве.
4. Процесс биодеградации нанокапсулы должен начинаться в строго заданный период времени после введения препарата СК в организм пациента. В зависимости от конкретных условий и задач лечения этот период может задаваться в очень широком диапазоне - от 1-2 часов до нескольких суток или даже месяцев.
5. По возможности, нанокапсула должна иметь способность к управляемой (программируемой) биодеградации под воздействием методов ионизирующей радиации, лазерного излучения и(или) химических агентов, чтобы иметь при необходимости возможность управлять процессом клеточного сигналинга по заранее определенному алгоритму (программе) в зависимости от конкретных условий и задач лечения.
6. Нанокапсула должна биодеградировать на безопасные для клетки компоненты.
7. Нанокапсула должна быть контрастна для методов лучевой диагностики и легко диагностироваться методами компьютерной и магнитно-резонансной томографии.
8. Находящиеся внутри нанокапсулы молекулы сигнального вещества должны в максимальной степени сохранять свою потенциальную активность, чтобы полностью реализовать ее после выхода из нанокапсулы в результате биодеградации последней.
9. Нанокапсула должна легко имплантироваться через плазматическую мембрану клетки внутрь ее цитоплазмы путем эндоцитоза, путем прямой внутриклеточной инъекции или с использованием физиологических подходов и физико-химических методов воздействия на СК.
10. Биодеградируемый материал оболочки нанокапсул в ряде случаев должен обладать способностью к конъюгированию с липидами для обеспечения возможности прикрепления («заякоривания») нанокапсул на плазматическую мембрану СК.
11. Предлагаемый клеточный препарат с нанокапсулами должен соответствовать критериям безопасности и быть нетоксичным.
Для производства нанокапсул необходимо выбрать биодеградируемый материал. В соответствии с поставленными задачами настоящего изобретения для доставки молекул сигнального белка в клетки-мишени были использованы нанокапсулы трех видов:
1) биодеградируемые нанокапсулы на основе биополимерных материалов (сополимеры полилактидгликолида и сополимеры полиоксибутиратвалерата);
2) биодеградируемые нанокапсулы на основе липосом;
3) наноэмульсии.
Во всех трех указанных случаях нанокапсулирования БАВ получаемый размер наночастиц был в диапазоне от 10 до 100 нм, что делало их способными к пассивной диффузии в СК или к активному захвату клетками путем пиноцитоза, в то время как нанокапсулы с размером более 100 нм способны распространяться только в межклеточном пространстве.
Полученные нанокапсулы с молекулами сигнального белка внутри них помещали в пластиковые пробирки объемом 1,5 мл и хранили при температуре минус 12°С до их дальнейшего анализа и использования.
Биодеградируемые нанокапсулы на основе биополимерных материалов (сополимеры полилактидгликолида и сополимеры полиоксибутиратвалерата)
Инкапсуляцию сигнального белка в биополимерный (полилактидгликолидный или полиоксибутиратвалератный) носитель проводили на экспериментальной установке следующим образом. Навеску лиофилизированного препарата сигнального белка, предварительно перемешанного с мелкодисперсным порошком полилактида (средний размер частиц -20 мкм) загружали в камеру высокого давления с последующим наполнением СO2. Температуру камеры поддерживали на уровне 50°С, а температура сопла составляла около 30°С. Давление сверхкритического СO2 составляло 10 МПа. Содержимое автоклава тщательно перемешивали с помощью магнитного смесителя (150 об/мин) в течение 60 мин с последующим сбросом полученной смеси и диоксида углерода через сопло в приемную камеру. После выдержки полученного продукта в атмосферных условиях в течение 3 часов (это необходимо для полного удаления СО2 из частиц полимера и их окончательного затвердевания) собранные частицы подвергали ультрадиспергированию до размера нанокапсул не более 10 нм. Ультрадиспергирование проводили в погружном диспергаторе Т 18 basic ULTRA-TURRAX. Диспергирующий элемент - S18N-19G (IKA-WERKE GMBH & СО. KG, Германия).
Биодеградируемые нанокапсулы на основе липосом
Предпочтительные методы получения смешанных липосом из нефосфолипидных амфифильных мембранных миметиков и фосфолипидов основаны на фазовом поведении амфифильных липидов и фосфолипидов. Объемное соотношение водного раствора амфифильного мембранного миметика и водного раствора фосфолипида составляло от 5:1 до 20:1. Температура смешивания от 18 до 20°С. Иногда требовалось нагреть амфифильный мембранный миметик и другие ингредиенты, чтобы получить гомогенный водный раствор перед добавлением фосфолипидов. Белковый или фармацевтический препарат сигнального вещества добавляли к ингредиентам в процессе их смешивания.
Получение липосом заданного размера (не более нм) осуществляли двумя способами:
1. Интенсивно перемешивали ингредиенты, добавляемые в определенном порядке, до получения мультиламеллярных везикул. Далее проводили измельчение частиц до получения одноламеллярных или малых мультиламеллярных липосом.
2. С помощью форсунок: (а) впрыскивали раствор фосфолипида на высокой скорости минимум через одно сопло в водную фазу мембранного миметика амфифильной природы, или (б) впрыскивали мембранный миметик амфифильной природы минимум через одно сопло в водную фазу фосфолипида, или (в) впрыскивали раствор фосфолипида на высокой скорости минимум через одно сопло одновременно с впрыском раствора мембранного миметика амфифильной природы также минимум через одно сопло в общий резервуар.
Наноэмульсии
Получение ультрамикроэмульсий (с размером частиц не более нм) осуществляли на основе спонтанно диспергирующихся концентратов фармакологически активных сложных эфиров (АСЭ). В качестве АСЭ можно применять ундеценоаты, лаураты, пальмитаты, стеараты. Спонтанно диспергирующийся концентрат разбавляли фосфатным буфером, содержащим препарат сигнального белка, и получали термодинамически стабильную ультрамикроэмульсию с мицеллами радиусом 1,5-3 нм. Для увеличения времени жизни эмульсии «вода в масле» в водную фазу добавляли эмульгаторы, стабилизаторы и др. Молекулы сигнального белка находились в водной фазе.
При определении задаваемого времени биодеградации нанокапсул внутри клетки следует принимать во внимание, какое конкретное сигнальное вещество будет инкапсулироваться, а также учитывать метод изготовления нанокапсул, что позволит «запрограммировать» время выхода сигнального вещества в аутологичную СК из нанокапсулы в строго заданный период.
Экспериментально доказаны и клинически подтверждены высокие биосовместимые свойства предложенных нанокапсул.
Имплантация наноконтейнеров в СК базового препарата
Имплантация наноконтейнеров (нанокапсул) в СК базового препарата осуществлялась при экспозиции суспензии или эмульсии нанокапсул с находящимися в них молекулами сигнального белка в базовом препарате СК в течение 60 минут или при культивировании аутологичных СК в стандартных условиях в течение 24 часов с добавлением к ним раствора нанокапсул с молекулами сигнального белка.
Кроме того, для имплантации нанокапсул согласно настоящему изобретению имеется принципиальная возможность применять стандартные методы генотерапии, например прямые внутриклеточные инъекции суспензии или эмульсии нанокапсул в мембрану, цитоплазму или ядро СК базового препарата, а также использование конъюгатов нанокапсул с холерным токсином, холестерином, полиэтиленгликолем и асиалгликопротеинами, использование катионных липидов с нанокапсулами, ковалентных липофильных соединений с нанокапсулами, иммунолипосом с нанокапсулами, нейтральных липосом с нанокапсулами, углеводородных энхасер клеточной проницаемости и мембранных фьюжен-генных составляющих.
В ряде случаев изготавливали композитные нанокапсулы, оболочка которых состояла из биодеградируемого биополимера и белков оболочки вируса герпеса. Использование нейротропных белков вируса герпеса для оболочки нанокапсулы имитирует псевдовирусный капсид. В этом случае наружняя оболочка нанокапсулы может сливаться с плазматической мембраной аутологичной СК, и нанокапсулы с молекулами сигнального белка легко проникают в СК путем ее активного эндоцитоза.
Описанные методы инкапсулирования белковых водорастворимых препаратов в наноконтейнеры можно также применять для суперселективного трансфера традиционных химиотерапевтических препаратов, используемых для цитотоксической и циторедукционной терапии. Предложенный препарат аутологичных СК с наноконтейнерами позволит осуществить целевую доставку наноконтейнеров с фармацевтическим препаратом (химиопрепаратом) в зону опухоли, используя миграционные механизмы хоуминга СК в патологическую зону.
Полученный в соответствии с настоящим изобретением препарат СК с репрограммированным клеточным сигналингом может быть введен в организм пациента известными методами, например путем интрацеребральной, интрамедулярной, внутрижелудочковой, интратекальной или внутрисосудистой трансплантации в зависимости от целей лечения, а также путем имплантации в тканево-инженерные конструкции, используемые для закрытия дефектов головного и спинного мозга.
Далее описаны примеры различных препаратов СК с репрограммированным клеточным сигналингом по настоящему изобретению (далее называются также целевыми препаратами), способов их получения и применения для лечения различных заболеваний с получением различных терапевтических эффектов согласно настоящему изобретению.
Пример 1. Получение целевого препарата СК (на основе базового препарата гемопоэтических (CD 34+) СК) с репрограммированным клеточным сигналингом в направлении индуцированного апоптоза для подавления опухолевого роста на модели глиальной опухоли головного мозга (глиомы С6) у крыс in vivo
Получение базового препарата мобилизованных гемопоэтических стволовых клеток (МГСК) человека осуществляли путем внутримышечного применения гранулоцитарного колониестимулирующего фактора (Г-КСФ) в количестве 8 инъекций в течение 4 дней с интервалом 10-12 часов. В первые 3 дня доза Г-КСФ составляла 2,5 мкг на кг, в последний день доза удваивалась. Сбор МГСК осуществляли на 5-й день от начала стимуляции путем стандартной процедуры лейкоцитофереза крови человека на аппарате типа COBA-Spectra (USA). Среднее количестве собранного материала 300-400 мл. Собранный материал оценивался по двум параметрам - по общему количеству ядерных клеток (ЯК) в сепарате и количеству CD34+ клеток на кг веса человека. ЯК в сепарате подсчитывали в камере Горяева. Процент CD34+ клеток оценивали методом проточной цитофлуометриии на приборе FACScan (becton Dickinson, USA). Затем из суспензии ЯК осуществляли магнитосепарацию CD 34+ на магнитных шариках на аппарате типа CliniMax. Количество ГСК CD 34+ наращивали путем их стандартного культивирования в течение 2-х дней.
Затем в клеточную культуру полученного базового препарата добавили раствор нанокапсул из полилактидгликолида размером от 50 до 100 нм со сроком биодеградации полимерной оболочки нанокапсулы до 172 часов. В качестве препарата, способного к регулированию сигнальных путей, нанокапсулы содержали индуктор апоптоза рицин. В течение 12 часов каждая ГСК CD 34+ путем эндоцитоза поглотила не менее 1-2 нанокапсулы с рицином. В дальнейшем полученный таким образом целевой препарат отмывали центрифугированием дважды, криоконсервировали путем программного замораживания с 10% раствором диметилсульфоксида (ДМСО) и полиглюкина (в равных объемах) и хранили в жидком азоте при температуре от минус 80 до минус 120°С. Перед применением целевой препарат разморозили на водяной бане и отмыли двухкратным центрифугированием. Затем препарат стереотаксически имплантировали в семидневную глиому С6, трансплантированную в мозг крысы. За 7 суток меченный флюоресцентным зеленым целевой препарат равномерно распределился по глиоме. При однократном введении данного целевого препарата в опухоль четко верифицировалось подавление роста опухоли больше чем на треть. Контрольное введение индуктора апоптоза рицина интратуморально привело к тотальному глиозу в мозге как в ипсилатеральном, так и контрлатеральном полушарии.
Пример 2. Получение целевого препарата СК (на основе базового препарата гемопоэтических (CD 34+) СК) с репрограммированным клеточным сигналингом в направлении индуцированного апоптоза для стимуляции пролиферации на модели глиальной опухоли головного мозга (глиомы С6) у крыс in vivo
Базовый препарат МГСК человека получали путем, описанным в примере 1. В полученный базовый препарат добавили 1,5 мл раствора нанокапсул из сополимера полиоксибутиратвалерата размером от 50 до 100 нм. В качестве препарата, способного к регулированию сигнальных путей, нанокапсулы содержали индуктор апоптоза рицин. Нанокапсулы имели время биодеградации полимерной оболочки до 44 часов. В течение 6 часов каждая ГСК CD 34+ эндоцитозом поглощала 1-2 нанокапсулы с рицином. Далее полученный целевой препарат криоконсервировали путем программного замораживания с 10% ДМСО и полиглюкина и хранили в жидком азоте при температуре минус 96°С. Перед употреблением целевой препарат разморозили на водяной бане, отмыли 2-кратным центрифугированием индуцированные на апоптоз ГСК и имплантировали в семидневную глиому С6, трансплантированную в мозг крысы. В течение 3 суток меченные красителем Dil индуцированные ГСК погибли в месте трансплантации. При однократном введении данного целевого препарата в опухоль верифицировалась стимуляция роста опухоли больше чем на треть.
Как видно из двух вышеприведенных примеров, один и тот же препарат, индуктор апоптоза рицин, в одних случаях может вызывать подавление (пример 1), а в других (пример 2) - стимуляцию опухолевого роста. Это объясняется различным заданным временем биодеградации нанокапсул, что соответственно приводит к разному времени запрограммированного выхода рицина в цитоплазму СК. СК целевого препарата равномерно по массе всей опухоли распределяются в среднем за 7-10 дней. В примере 1 время биодеградации оболочки нанокапсулы составляло около 7 дней (172 часа). В этом случае гибель значительного количества опухолевых клеток происходила равномерно по всему объему опухоли, что и привело к индуцированному системному процессу программной гибели, так называемому "эффекту листопада" (почти физиологичный процесс). В примере 2 время биодеградации нанокапсул составляло около 2 суток (44 часа), что привело к гибели СК в огромном количестве в очень малом объеме и проявлению "эффекта удаления части ткани", то есть, если все клетки погибают в одном месте, на это опухоль реагирует бурной пролиферацией и соответственно ростом.
Пример 3. Получение целевого препарата СК (на основе базового препарата нейральных стволовых клеток человека) с репрограммированным клеточным сигналингом в направлении индуцированного апоптоза для подавления опухолевого роста на модели глиальной опухоли головного мозга (глиомы Сб) у крыс in vivo
Базовый препарат нейральных стволовых клеток (НСК) получали по методике, которая в настоящем описании приведена выше со ссылками на [11-16].
Перед трансплантацией в глиомы С6 головного мозга крысы базовый препарат размораживали и культивировали 12 часов, как описано ранее. Затем в клеточную культуру базового препарата добавили 1,5 мл раствора нанокапсул с оболочкой из сополимера полиоксибутиратвалерата размером до 80 нм, содержащих индуктор апоптоза вискумин с заданным временем биодеградации полимерной оболочки нанокапсулы до 60 часов. В течение 6-12 часов каждая НСК эндоцитозом поглотила не менее 1-2 нанокапсулы с вискумином. В дальнейшем целевой препарат криоконсервировали путем программного замораживания с 10% раствором ДМСО и полиглюкина (в равных объемах) и хранили в жидком азоте при температуре от минус 80 до минус 120°С. Перед употреблением целевой препарат разморозили на водяной бане, отмыли 2-кратным центрифугированием и имплантировали в семидневную глиому Сб, трансплантированную в мозг крысы. Верифицировали подавление роста опухоли больше чем на треть при однократном введении данного целевого препарата в опухоль. Контрольное введение индуктора апоптоза вискумина интратуморально привело к тотальному глиозу в мозге как в ипсилатеральном, так и контрлатеральном полушарии.
Пример 4. Получение целевого препарата СК (на основе базового препарата алогенных гемопоэтических (CD 34+) СК близкого родственника пациента (брата) с репрограммированным клеточным сигналингом для экспериментального лечения пациента с рецидивирующей глиобластомой левого полушария головного мозга
Пациент К., 30-ти лет, в коматозном состоянии был госпитализирован в отделение реанимации с диагнозом: Рецидивирующей глиобластомы теменно-височной области левого полушария головного мозга с частьми эпилептиформными параксизмами (история болезни), правосторонним гемипарезом и отеком головного мозга. После диагностирования у пациента глиальной опухоли он был оперирован по этому поводу в НИИ нейрохирургии им Н.Н.Бурденко. Прошел стандартный полный курс лучевой терапии (60 грей) и химиотерапию темодалом. Рецидив глиобластомы. Манифестация опухоли проявилась массивными генерализованными эпилептическими припадками, отеком головного мозга. Присоединились осложнения в виде гиперкортицизма (синдром Иценко-Кушинга) вследствие длительного приема высоких доз (до 40 мг в день) кортикостероидных препаратов для купирования внутримозговой гипертензии и отека мозга. В дальнейшем оперативном, лучевом и химиотерапевтическом лечении пациенту отказано в НИИ нейрохирургии РАМН им Н.Н.Бурденко и РОНЦ РАМН им Н.Н.Блохина. Больной был взят в отраслевую программу РАМН «Новые клеточные технологии-медицине» (2003) и включен в подпрограмму «Клеточные технологии в нейроонкологии». Больной подписал информированное согласие на применение новой клеточной технологии. В качестве донора МГСК был взят гистосовместимый по HLA-типированию родной брат пациента К. Базовый препарат МГСК получили согласно примеру 1. Для получения целевого препарата в базовый препарат добавили раствор нанокапсул с оболочкой из сополимера полиоксибутиратвалерата размером 50-100 нм. Нанокапсулы имели срок биодеградации до 170 часов. В качестве препарата, способного к регулированию сигнальных путей, нанокапсулы содержали белок рицин. Перед применением целевой препарат разморозили на водяной бане и отмыли 2-кратным центрифугированием. Проведение экспериментального лечения осуществлялось с разрешения Ученого совета и Этического Комитета РОНЦ РАМН. Учитывая неоперабельность глиобластомы у пациента и высокий риск развития эпилептического статуса пациента, было проведено 20 трансфузий целевого препарата интратекально. По данным контрольных МРТ наблюдалась редукция объема глиобластомы и замещения ее кистой головного мозга в течение 9 месяцев. Клинически у пациента было отмечено уменьшение гидроцефального синдрома, практическая редукция эпилептиформных пароксизмов и снижение порога судорожной готовности по ЭЭГ. По истечении 9 месяцев с начала экспериментального лечения объем глиобластомы по данным МРТ уменьшился в 2 раза за счет замещения ее кистой головного мозга, раскрылись желудочки.
Пример 5. Получение целевого препарата СК (на основе базового препарата гемопоэтических стволовых клеток (ГСК) человека) с репрограммированным клеточным сигналингом в направлении активации пролиферативных процессов в поврежденном спинном мозге у крыс in vivo
Базовый препарат получили согласно примеру 1. Для получения целевого препарата к базовому препарату добавили ультрамикроэмульсии нанокапсул, полученных из ундеценоата и содержащих в себе рекомбинантный белок Вс1-2 в качестве препарата, способного к регулированию сигнальных путей. Предварительные эксперименты были выполнены на модели частичного поврежденного спинного мозга (ПСМ) у крыс линии Вистар. Повреждения Th 10 сегмента спинного мозга у крыс осуществляли путем ламинэктомии на уровне Th8-Thl2, вскрытия твердой мозговой оболочки и 15-минутной компрессии спинного мозга грузом 20 грамм на уровне Тh10 у десяти крыс (контрольная группа 1). Другим десяти крысам в зону аналогичного ПСМ производили интрамедуллярное введение ГСК человека (контрольная группа 2). В опытной группе (10 животных) с аналогичным ПСМ в зону травмы интрамедулярно вводили целевой препарат. Все выжившие животные забивались для проведения иммуногистохимического и гистологического исследования оценки развития апоптоза. Проводились оценка выживания собственных клеток животных и трансплантированных ГСК в экстремальных условиях с использованием стандартного теста с трипановым синим и оценка фрагментации ДНК (признаки апоптоза) путем окрашивания ядерным проточным по методике И.В.Викторова. Было показано, что в опытной группе наличие белка Всl-2 в цитоплазме СК (вследствие выхода молекул этого белка из ультрамикроэмульсии) позволило выжить в неблагоприятных условиях отсутствия кровоснабжения и постоперационного отека ПСМ более 76,2% клеток ПСМ, явления апоптоза и некроза отмечены в 23,8%, в то время как в контрольной группе 2 с имплантацией живых ГСК было отмечено развитие апоптоза и некроза в 53,7%, а в контрольной группе 1 явления апоптоза и некроза в ПСМ были зарегистрированы практически полностью во всех полях зрения (более 90%). Клеточный препарат ГСК человека, использованный для трансплантации в ПСМ контрольной группы 2 и опытной группы, культивировался еще 5 суток и из него были взяты образцы для РНК-анализа. Исследование генной микроматрицы проводилось по каждому из образцов. Реакция на активацию пролиферации ГСК (повышенная регуляция и пониженная регуляция, взятые в виде 2-ступенчатого увеличения или уменьшения) 22 генов на образец изучалась при помощи HG-Focus чипов генома человека (Affimetrix UK Ltd). Данные исследования микроматрицы, полученные из проделанных экспериментов опытной группы, показали, что преобладание в цитоплазме ГСК белка Всl-2 является важным регулятором апоптоза и предотвращает естественную гибель ГСК, способствует их выживанию, приводит к 2-кратной супрессии гена р53 и активации отдельных генов, таких как p21wafl, GADD45, Cyclin В, RTGFb, CDC2. Повышение экспрессии этих генов в целевом препарате ГСК свидетельствует об активации пролиферативных процессов в трансплантированных клетках, а также об усилении процессов дифференцировки и регенеративных свойств для наилучшего обеспечения выживания их в экстремальных условиях.
Пример 6. Получение целевого препарата СК (на основе базового препарата мезенхимальных стволовых клеток (МСК) человека) с репрограммированным клеточным сигналингом в направлении пролиферации для лечения ишемических повреждений мозга на модели ишемического инсульта правого полушария иммунодефицитных мышей in vivo
Для получения базового препарата МСК выделяли из костного мозга человека, а затем культивировали 30 дней. Целевой препарат готовили путем добавления к базовому препарату липосом, изготовленных из нефосфолипидных амфифильных мембранных миметиков и фосфолипидов и содержащих белок CrmA - протеин вируса ветрянки в качестве препарата, способного к регулированию сигнальных путей, и 2-часовой экспозиции с последующим отмыванием клеток путем двухкратного центрифугирования с физиологическим раствором 0,9% на 1500 оборотах. Перед применением целевого препарата его клетки имели фенотип SH2+/SH4+/CD34-/CD45-. В опытной группе мышей целевой препарат применяли через 1 неделю после инсульта путем внутривенного введения в хвостовую вену мышей. Через 3 недели животных забивали для исследования и оценки регенерации в головном мозге. Мышам контрольной группы 1 делали внутривенную трансплантацию нативных МСК, а мышам контрольной группы 2 никакого лечения не проводили. При гистологическом и иммуногистологическом исследовании препаратов, полученных из зоны ишемии головного мозга иммунодефицитных мышей, установлено, что меньшие размеры разрушений, лучшее структурное восстановление поврежденных нейронов и регенерация тканей головного мозга за счет активации регенерации в ишемическом очаге мозга была у животных опытной группы по сравнению двумя контрольными группами. Показана способность целевого препарата более значимо улучшать кровоток в зоне ишемии, уменьшать зону рубца. Доказана способность клеток целевого препарата усиленно пролиферировать и дифференцироваться в нейрональные клетки в 5% (от 2 млн введенных клеток), что подтверждено их возможностью окрашиваться позитивно на нейральные маркеры. В контрольной группе 1 с нативными МСК только 0,03% МСК в зоне ишемии окрашивались нейрональными маркерами. Измененный сигналинг МСК в опытной группе усилил паракринные эффекты стимуляции ангио- и нейрогенеза за счет стимуляции синтеза факторов роста как клетками МСК, так и поврежденными нервными клетками. Данные опыты показали статистическую значимую (р<0,05) выживаемость и восстановление нарушенных моторных, сенсорных и когнитивных (познавательных) функций у мышей с инсультом в опытной группе по сравнению с контрольными группами.
Исходя из вышеизложенного, настоящее изобретение может быть рассмотрено как новое направление в лечении опухолей, ишемических, дегенеративных и травматических повреждений ЦНС и квалифицироваться как высокотехнологичный метод клеточной цитокоррекционной или циторегуляционной терапии опухолей ЦНС, а также терапии других солидных опухолей и соматических заболеваний.
Конкретные примеры осуществления настоящего изобретения и используемые при этом приемы приведены в данном описании только в пояснительных целях и не ограничивают объем и сущность изобретения, которые определяются исключительно нижеизложенной формулой изобретения. Специалистам в данной области техники будут понятны возможные различные варианты и модификации настоящего изобретения, не выходящие за пределы формулы изобретения.
ЛИТЕРАТУРА
1. Брюховецкий А.С. Трансплантация нервных клеток и тканевая инженерия мозга при нервных болезнях. - М.: ЗАО Клиника «Нейровита», 2003.
2. Kobayashi N., Navarro-Alvares N., Soto-Guetierrez A., Kavamoto Hironobu. et al. Cancer Stem Cells Research: Currently Situation and Problems//Cell Transplantation, 2008, Vol.17, p.19-25.
3. Брюховецкий А.С., Чехонин В.П., Менткевич Г.Л. Стволовые клетки в нейроонкологии: здоровые и раковые стволовые клетки, их возможная роль и место в канцерогенезе и современных высокотехнологичных сценариях лечения опухолей мозга. Материалы научно-практической-конференции «Высокие технологии в терапии и реабилитации заболеваний нервной системы». - М., 2008, с.43-44.
4. Введение в молекулярную медицину./ Под ред. А.А.Пальцева. - М.: Медицина, 2006.
5. Цымбалюк В.И., Медведев В.В. Нейрогенные стволовые клетки. Монография. - Киев: Издательство «Коваль», 2005.
6. Zigova T., Snyder E., Sanberg P. Neural Stem Cells for Brain and Spinal Cord Repair, 2003.
7. Пальцев М.А., Иванов А.А., Северин С.Е. Межклеточные взаимодействия. - М.: Медицина, 2003.
8. Неймарк Ю.И., Коган Р.Я., Савельев В.П. Динамические модели теории управления. - М.: Наука, 1985.
9. Гродинз Ф. Теория регулирования и биологические системы. - М.: Мир, 1966.
10. Фокин С.В., Беркинблит М.Б. Математические проблемы в биологии. - М., 1973.
11. Zhang X., Klueber К. М., Guo Z. // Experimental Neurology, - 2004, Vol.186, p.112-123.
12. Zhang X., Cai J., Klueber K.M. et al. // Stem Cells, 2005, Vol.23, p.442-453.
13. Zhang X., Cai J., Klueber K.М. at al. // Stem Cells, 2006a, Vol.24, p.434-442.
14. Zhang X., Klueber K.M., Guo Z. et al. // Brain Res., 2006b, Vol.1073-1074, p.109-119.
15. Marshall C.T., Guo Z., Lu С.et al. // Brain Res., 2005, Vol.1045, p.45-56.
16. Marshall C.T., Lu C., Winstead W. et al. // Histol. HistopatoL, 2006, Vol.21, p.633-643.

Изобретение относится к области медицины и касается препарата стволовых клеток (СК) с репрограммированным клеточным сигналингом, способа получения этого препарата и его применения. Сущность изобретения включает препарат СК с репрограммированным клеточным сигналингом, содержащий базовый препарат СК, в мембрану, и/или ядро, и/или цитоплазму которых имплантирован способный к регулированию сигнальных путей СК и клеток патологического очага в организме млекопитающего белковый или фармацевтический препарат, предварительно инкапсулированный в наноконтейнеры размером до 100 нм, полученные из биодеградируемого материала, интактного для органелл и компартаментов СК базового препарата. Этот материал имеет заданные сроки биодеградации в организме млекопитающего для обеспечения программируемого выхода белкового или фармацевтического препарата во внутри- или межклеточное пространство и осуществления тем самым перепрограммирования сигнальной трансдукции ключевых генов СК в требуемом терапевтическом направлении развития физиологических событий клеточного цикла непосредственно в патологической зоне органа или ткани организма. Преимущество изобретения заключается в обеспечении целевой добавки сигнальных веществ строго в пораженную зону организма. 3 н. и 11 з.п. ф-лы, 3 ил., 1 табл.
1. Препарат стволовых клеток с репрограммированным клеточным сигналингом, содержащий базовый препарат стволовых клеток, в мембрану и/или ядро и/или цитоплазму которых имплантирован способный к регулированию сигнальных путей стволовых клеток и клеток патологического очага в организме млекопитающего белковый или фармацевтический препарат, предварительно инкапсулированный в наноконтейнеры, полученные из биодеградируемого материала, интактного для органелл и компартаментов стволовых клеток базового препарата и имеющего заданные сроки биодеградации в организме млекопитающего для обеспечения программируемого выхода белкового или фармацевтического препарата во внутри- или межклеточное пространство стволовых клеток и осуществления тем самым перепрограммирования сигнальной трансдукции ключевых генов стволовых клеток в требуемом терапевтическом направлении развития физиологических событий клеточного цикла непосредственно в патологической зоне органа или ткани организма.
2. Препарат по п.1, отличающийся тем, что в качестве стволовых клеток базового препарата использованы аутологичные стволовые клетки.
3. Препарат стволовых клеток по п.1, отличающийся тем, что размер наноконтейнеров не превышает 100 нм.
4. Препарат по п.1, отличающийся тем, что в качестве наноконтейнеров использованы наноконтейнеры на основе биополимерного материала.
5. Препарат по п.4, отличающийся тем, что в качестве биополимерного материала использованы сополимеры полилактидгликолида и/или полиоксибутиратвалерата.
6. Препарат по п.1, отличающийся тем, что в качестве наноконтейнеров использованы наноконтейнеры на основе липосом.
7. Препарат по п.1, отличающийся тем, что в качестве наноконтейнеров использованы наноэмульсии.
8. Способ получения препарата стволовых клеток с репрограммированным клеточным сигналингом, включающий в себя выбор базового препарата стволовых клеток, выбор белкового или фармацевтического препарата, способного к регулированию сигнальных путей стволовых клеток и клеток патологического очага в организме млекопитающего, инкапсулирование выбранного белкового или фармацевтического препарата в наноконтейнеры из биодеградируемого материала, интактного для органелл и компартаментов стволовых клеток базового препарата и имеющего заданные сроки биодеградации в организме млекопитающего для обеспечения программируемого выхода белкового или фармацевтического препарата во внутри- или межклеточное пространство стволовых клеток и осуществления тем самым перепрограммирования сигнальной трансдукции ключевых генов стволовых клеток в требуемом терапевтическом направлении развития физиологических событий клеточного цикла непосредственно в патологической зоне органа или ткани организма, и последующую имплантацию наноконтейнеров в мембрану, и/или ядро, и/или цитоплазму стволовых клеток базового препарата.
9. Способ по п.8, отличающийся тем, что выбирают базовый препарат с аутологичными стволовыми клетками.
10. Способ по п.8, отличающийся тем, что инкапсулирование проводят путем ультрадиспергирования смеси биополимерного материала с белковым или фармацевтическим препаратом.
11. Способ по п.8, отличающийся тем, что имплантацию наноконтейнеров проводят путем прямых внутриклеточных инъекций суспензии или эмульсии наноконтейнеров в мембрану, цитоплазму или ядро стволовых клеток базового препарата.
12. Способ по п.8, отличающийся тем, что имплантацию наноконтейнеров проводят путем их эндоцитоза в цитоплазму стволовых клеток при экспозиции суспензии или эмульсии наноконтейнеров в базовом препарате.
13. Способ по п.8, отличающийся тем, что его проводят в стерильных условиях или непосредственно в операционной (ex temporo) или в культуральной лаборатории.
14. Применение препарата стволовых клеток по любому из пп.1-7 в качестве средства для внутри- и внеклеточной регуляции сигнальных путей патологических клеток при лечении заболеваний, повреждений и опухолей головного и спинного мозга, а также опухолей и метастатических поражений других органов и систем млекопитающего.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| REICHARDT W., et al., Impact of mammalian target of rapamycin inhibition on lymphoid homing and tolerogenic function of nanoparticle-labeled dendritic cells following allogenic hematopoietic cell transplantation, J.Immunol., 2008, Oct.1, v.181, (7), pp.4770-4779. | |||
Авторы
Даты
2011-09-10—Публикация
2008-12-30—Подача