Изобретение относится к медицине и фармации, в частности, к лекарственным средствам, используемым для лечения и профилактики заболеваний, характеризующихся повышенной тенденцией к тромбозам (инфаркт миокарда, ишемический инсульт).
Известно лекарственное средство «Ацетилсалициловая кислота» [Машковский М.Д. Лекарственные средства, 15 издание. / М.Д.Машковский // М.: Медицина. - 2005. - T.1. - С.41-42].
Ацетилсалициловая кислота (АСК) является одним из наиболее эффективных нестероидных противовоспалительных лекарственных средств (НПВС). В то же время важной особенностью АСК является ее способность оказывать антиагрегационное действие, ингибировать спонтанную и индуцированную агрегацию тромбоцитов. На сегодня АСК в низких дозах (75-150 мг) однозначно рекомендуется как препарат первого ряда для вторичной профилактики кардиоваскулярных событий и смерти у кардиологических пациентов высокого риска [3]. Современные международные рекомендации по лечению различных категорий кардиологических пациентов высокого риска классифицируют применение ацетилсалициловой кислоты на уровне рекомендаций 1 класса (безусловно доказанная полезность данного терапевтического подхода) и уровня доказательности А (эффективность и безопасность препарата при данных клинических состояниях доказана минимум в двух многоцентровых рандомизированных плацебо контролированных исследованиях).
Побочным негативным действием ацетилсалициловой кислоты является повреждение слизистых оболочек. Использование АСК может привести к возникновению эрозий из язв слизистых оболочек желудочно-кишечного тракта (в первую очередь желудка и 12-перстной кишки), а также к кровотечению. Эти побочные эффекты являются дозозависимыми, и частота их проявления значительно возрастает при использовании высоких доз АСК. Однако даже при использовании низких «кардиологических» доз АСК для антитромбоцитарной терапии нарушения со стороны желудочно-кишечного тракта остаются одними из наиболее распространенных побочных действий. Кроме того, АСК может приводить к развитию реакций гиперчувствительности (бронхоспазм, отек, крапивница и другие кожные реакции), тромбоцитопении, нарушению функций печени и почек.
Известное лекарственное средство тиотриазолин [Тиотриазолин. / [И.А.Мазур, Н.А.Волошин, И.С.Чекман и др.]. - Запорожье, Львов. - 2005. - С.26-40] обладает ярко выраженными антиоксидантными свойствами - реактивирует такие антиоксидантные ферменты, как супероксиддисмутаза и каталаза, снижает степень окислительной модификации белка и липопероксидации, снижает образование супероксидрадикала и пероксинитрита. Кроме этого, тиотриазолин обладает выраженным энерготропным эффектом, что обуславливает улучшение метаболических процессов различных органов и систем. Титриазолин характеризуется наличием гастропротекторного, гепатопротекторного, кардиопротекторного и нейропротекторного действия.
Учитывая широкое применение ацетилсалициловой кислоты в качестве антиагрегантного средства, нами она принята за прототип.
В основу изобретения поставлена задача - разработать лекарственное средство с широким спектром фармакологического действия и низкой частотой развития побочных эффектов, превосходящее прототип по достигаемому антиагрегантному эффекту.
Решение поставленной задачи обеспечивает комбинированное антиагрегантное и антиоксидантное средство, содержащее в качестве активной основы ацетилсалициловую кислоту, за счет того, что активная основа дополнительно содержит тиотриазолин при соотношении ацетилсалициловой кислоты к тиотриазолину 4:1.
Фармакологический эффект от использования изобретения
Использование комбинации ацетилсалициловая кислота + тиотриазолин приводит к усилению антиагрегантных свойств ацетилсалициловой кислоты. Результаты исследований показали, что на фоне введения исследуемой комбинации уменьшались степень и скорость индуцированной агрегации тромбоцитов при использовании основных индукторов агрегации (коллагена, аденозиндифосфата, арахидоновой кислоты). Также было отмечено значительное снижение ульцерогенных свойств ацетилсалициловой кислоты, обусловленных нарушением синтеза гастропротекторных простагландинов в слизистой оболочке желудка. В результате скрининговых исследований удалось выявить, что наиболее удачной комбинацией является использование препаратов ацетилсалициловая кислота + тиотриазолин в соотношении 4:1, при которой каждый из компонентов комбинации использован в своей среднетерапевтической дозе (по антиагрегантной активности).
Использование предложенного комбинированного лекарственного средства, согласно приведенному ниже описанию, позволит повысить его антиагрегантную активность в сравнении с ацетилсалициловой кислотой (табл.1-3), что обусловлено наличием собственной активности титриазолина в отношении ингибирования агрегации тромбоцитов, способностью стабилизировать мембраны тромбоцитов, уменьшая тем самым выделение из них арахидоновой кислоты, в процессе метаболизма которой образуется один из наиболее мощных индукторов агрегации и вазоконстрикторов - тромбоксан А2.
* - различия достоверны по отношению к контрольной группе (Р<0,05);
** - различия достоверны по отношению к группе АСК, 10 мг/кг (Р<0,05).
Влияние препаратов на время максимума индуцированной агрегации тромбоцитов
Для реализации этой задачи имеет значение снижение образования активных форм кислорода и реактивация антиоксидантной системы, а также гастропротекторное действие, присущее тиотриазолину, что подтверждается нашими данными по изучению ульцерогенности (табл.4).
В таблице изменения показателей приведены в процентах от контрольной группы, которые приняты за 100%. (+) - увеличение, (-) - уменьшение.
Суть изобретения объясняется приведенным ниже описанием предлагаемого лекарственного средства и примерами его использования при фиксированном соотношении активных компонентов и лекарственного средства, принятого в качестве прототипа.
В результате исследования были установлены особенности проявлений антиагрегантного и ульцерогенного действия изучаемых препаратов и их влияния на антиоксидантные эффекты. Препараты вводили внутрижелудочно (per os) на 1% крахмальной слизи ежедневно в течение 5 дней в дозах, указанных в таблицах 1-3 и 5. В каждой группе использовалось по 6 животных.
Таким образом, предложенное лекарственное средство, согласно изобретению, проявляет более высокую антиагрегантную активность в сравнении с известным препаратом - ацетилсалициловой кислотой, при этом снижая побочные действия ацетилсалициловой кислоты. В предложенном лекарственном средстве наблюдается увеличение терапевтического эффекта при той же дозе ацетилсалициловой кислоты и с меньшим отрицательным влиянием на показатели физиологической активности организма.
Для иллюстрации приводим следующие примеры изучения внутрижелудочно (per os) введенных препаратов по изобретению.
Пример 1
Изучение действия тиотриазолина и комбинации препаратов на параметры индуцированной агрегации тромбоцитов.
Кровь для исследования индуцированной агрегации тромбоцитов брали у наркотизированных белых нелинейных крыс массой 220-250 г внутрисердечной пункцией. Свертываемость предупреждалась 3,8% раствором цитрата натрия, добавляемого к крови в соотношении 1:9. Для исключения контактной активации тромбоцитов в работе использовалось только пластмассовая посуда (кюветы, пробирки). Вначале кровь центрифугировали на малых оборотах (15 минут при 100 g). При этом отделяется плазма, богатая тромбоцитами (ПБТ), которую отбирали в пластмассовые пробирки. Затем оставшуюся кровь снова центрифугировали, но уже на более высоких оборотах (15 минут при 200 g). Образующийся после повторного центрифугирования верхний слой является бестромбоцитарной плазмой, которую также отбирали в пластмассовые пробирки. ПБТ использовалась для исследования функциональной активности тромбоцитов (изучение агрегации тромбоцитов), бестромбоцитарная плазма - для калибровки шкалы оптической плотности прибора (светопропускание бестромбоцитарной плазмы принималось за 100% агрегации), и, при необходимости, для разведения богатой тромбоцитами плазмы до стандартного содержания клеток, которое должно составлять 200-250×109/л. Допустимый срок хранения ПБТ при комнатной температуре или с использованием водяной бани при 37°С не более 3 часов после взятия пробы крови, поэтому исследование функциональной активности тромбоцитов проводили в течение этого времени.
Исследование агрегационной способности тромбоцитов проводили по методике G.V.Born на анализаторе агрегации тромбоцитов «SOLAR АР 2110» (Беларусь), используя в качестве индукторов растворы аденозиндифосфата (АДФ) в конечных концентрациях 5 и 20 мкМ (НПО «РЕНАМ», Россия), колагена 2 мг/мл (000 «Технология-Стандарт», Россия) и арахидоновой кислоты 1 мМ («Sigma-Aldrich», Германия). Определяли степень максимальной агрегации, время наступления максимума и скорость агрегации за 30 сек. Тромбоциты при исследовании на агрегометре АР 2110 находятся в условиях, приближающихся к физиологическим, в собственном микромире, при стандартной температуре 37°С и постоянной скорости перемешивания, моделирующей кровообращение, в интактной среде (одноразовые пластиковые кюветы). Мерой агрегационного процесса является графически регистрируемое падение оптической плотности плазмы крови в результате потребления тромбоцитов в агрегатах, образующихся под воздействием индукторов агрегации.
После приготовления всех необходимых растворов (ПБТ, бестромбоцитарная плазма, индукторы агрегации), они выдерживались в термостате в течение 3 минут. Затем на агрегометре определялась оптическая плотность бестромбоцитарной плазмы (ее светопропускание в относительной шкале прибора принималась за 100% агрегации). После этого в агрегометр помещалась кювета с ПБТ и измерялось количество тромбоцитов в образце плазмы (при необходимости производили коррекцию содержания кровяных пластинок путем разбавления ПБТ бестромбоцитарной плазмой) и ее оптическую плотность (светопропускание ПБТ в относительной шкале прибора принималось за 0% агрегации). По завершении калибровки агрегометра начинали изучение процесса агрегации тромбоцитов под влиянием различных индукторов (АДФ, коллаген, арахидоновая кислота). В кювету в 450 мкл ПБТ добавляли 50 мкл раствора индуктора агрегации и фиксировали на агрегометре время добавления. После инициации процесса агрегации наблюдали падение оптической плотности исследуемого образца ПБТ, регистрируемого прибором в виде увеличения показателя «степень агрегации» от 0% и выше (максимум до 100%). При этом на графике «степень агрегации - время» определялось 3 показателя: уровень максимального подъема кривой (максимальная степень агрегации); соответствующее ей время (время максимума) и крутизна подъема кривой (скорость агрегации). Время исследования каждого образца составляло 10 минут.
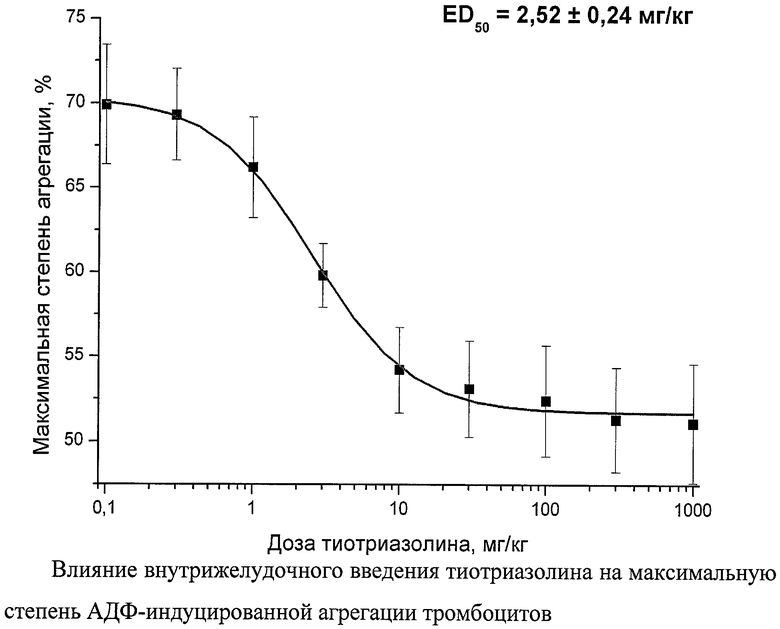
Результаты исследования влияния внутрижелудочного введения тиотриазолина в широком диапазоне доз (0,1; 0,3; 1; 3; 10; 30; 100; 300 i 1000 мг/кг) на АДФ (20 мкмоль/л) - индуцированную агрегацию тромбоцитов показали, что с увеличением дозы величина оказываемого им эффекта также возрастает (табл.5). При этом анализ полученных данных и построение кривой зависимости «доза - эффект» (чертеж) показал, что по данному действию ЕD50 тиотриазолина составляет 2,52±0,24 мг/кг. Поэтому для последующих исследований была взята доза 2,5 мг/кг.
Анализ показателей агрегатограмм выявил, что внутрижелудочное введение крысам ацетилсалициловой кислоты (10 мг/кг) и ее комбинации с тиотриазолином (2,5 мг/кг) приводит к достоверному угнетению агрегации тромбоцитов при использовании всех основных индукторов (АДФ, коллаген и арахидоновая кислота). При этом различные параметры агрегации (максимальная степень, время максимума и скорость за 30 сек) изменялись по-разному, в зависимости от применяемого индуктора.
Так, использование в качестве индуктора раствора коллагена (2 мг/мл) вызывало достоверное снижение максимальной степени агрегации на 20% (Р<0,05) и 36,1% (Р<0,05) у животных, получавших АСК и комбинированный препарат АСК + тиотриазолин соответственно. Время наступления максимума также снижалось на фоне приема препаратов на 23,1% (Р<0,05) и 30,4% (Р<0,05) соответственно. В отношении влияния на скорость агрегации - АСК вызывала небольшое уменьшение этого показателя, которое было недостоверным, а комбинация АСК + тиотриазолин снижало этот показатель на 58,4% (Р<0,05).
Использование в качестве индуктора агрегации раствора архидоновой кислоты (1 ммоль/л) приводило к снижению основного показателя функциональной активности тромбоцитов - степени агрегации 0 на 32,6% (Р<0,05) при применении АСК и АСК + тиотриазолин соответственно. Комбинированный препарат вызывал замедление наступления максимума агрегации на 59,4%, однако эти изменения были недостоверны. Выраженного влияния на скорость агрегации изучаемые препараты в данном случае не оказывали.
АДФ может использоваться в качестве индуктора агрегации в различных концентрациях. Так, использование его в более высокой концентрации (20 мкмоль/л) вызывает однофазную необратимую агрегацию, которая происходит с такой силой и скоростью, что переход первичной во вторичную фазу агрегации различить невозможно.
Под действием малой дозы АДФ (5 мкмоль/л) происходит только первичная (обратимая) агрегация с последующей дезагрегацией. При использовании в качестве индуктора раствора АДФ (20 мкмоль/л) исследуемые препараты (АСК и АСК + тиотриазолин) вызывали достоверное снижение степени максимальной агрегации на 19,9% (Р<0,05) и 50,4% (Р<0,05) соответственно. Скорость агрегации также снижалась на 26,8% (Р<0,05) и 35% (Р<0,05) соответственно. Влияние на время наступления максимума агрегации было недостоверным. При использовании раствора АДФ в более низкой концентрации (5 мкмоль/л) АСК практически не оказывала влияния на параметры агрегации, в то время, как комбинированный препарат АСК + тиотриазолин вызывал достоверное снижение степени и скорости агрегации 31,5% (Р<0,05) и 34,3% (Р<0,05) соответственно.
Результаты исследований предоставлены в таблицах 1-3.
Пример 2
Изучение ульцерогенного действия ацетилсалициловой кислоты и ее комбинации с тиотриазолином
Принцип метода заключается в макроскопичном исследовании слизистой желудков крыс, которые получали препараты на фоне голодания. Исследуемые вещества вводились внутрижелудочно один раз в сутки начиная со второго дня голодания (наличие свободного доступа к воде и отсутствие пищи). После двукратного введения препаратов (на 2 и 3 день эксперимента) животных декапитировали на четвертый день эксперимента (через 24 часа последнего введения исследуемых препаратов), извлекали желудки, рассекали их по малой кривизне и промывали и физиологическом растворе для удаления содержимого. Оценку ульцерогенного эффекта проводили визуально по количеству язвенных дефектов, что отразилось в баллах и язвенном индексе ЯИ.
Была использована 4-балльная шкала для оценки степени поражения слизистой оболочки желудка:
0 - отсутствие изменений;
1 - эрозия;
2 - единичные язвы;
3 - множественные язвы;
4 - прободные язвы.
ЯИ вычисляли по формуле:

Группы животных, которые получали препараты (в каждой группе по 6 животных):
1 - ацетилсалициловая кислота (10 мг/кг);
2 - ацетилсалициловая кислота (10 мг/кг) + тиотриазолин (2,5 мг/кг);
3 - физиологический раствор в адекватном объеме (контрольная группа);
4 - полноценное питание, препараты не вводились. Результаты исследований предоставлены в таблице 4.
Пример 3
Изучение влияния комбинации препаратов на активность перекисного окисления липидов (ПОЛ)
Интенсивность процессов свободно-радикального окисления в структурах мозга (ствол, гиппокамп, кора) и сыворотке крови белых нелинейных крыс оценивали по накоплению продуктов - диеновых конъюгатов (ДК) и малонового диальдегида (МДА).
Состояние антиоксидантной системы оценивали по активности супероксиддисмутазы (СОД) и каталазы.
Препараты вводили внутрижелудочно (per os) на 1% крахмальной слизи ежедневно в течение 5 дней в дозах, указанных в таблицах 6 и 7. В каждой группе использовалось по 6 животных.
Через 60 мин последнего введения препаратов животных подвергали атравматической фиксации и моментальной декапитации. Отдельно выделяли и анализировали следующие участки головного мозга: кора, гиппокамп, ствол.
Замороженные в азоте ткани мозга гомогенизировали в фарфоровых ступках. После центрифугирования при температуре 14°С и 15000g супернатант сливали в чистые пробирки. Определение активности СОД проводили по методу Чевари С. и соавт. по конкуренции с нитросиним тетразолием в системе аэробного взаимодействия НАДН и фенозиметансульфата. Активность каталазы определяли спектрофотометрически по уменьшению концентрации перекиси водорода. Содержимое ДК определяли спектрофотометрически в гептановой фазе после их экстракции смесью гептан - изопропиловый спирт. Содержимое ТБК-зависимых продуктов (МДА) определяли спектрофотометрически по реакции с тиобарбитуровой кислотой.
Анализ полученных результатов показал, что как тиотриазолин, так и ацетилсалициловая кислота обладают антиоксидантным действием. Раздельное введение этих препаратов проводило к уменьшению количества МДА и ДК, и увеличению активности СОД и каталазы. При этом тиотриазолин оказывал намного более выраженное действие по сравнению с АСК. Последняя преимущественно снижала уровень МДА и увеличивала активность СОД, меньше влияя на ДК и каталазу.
Комбинированное введение крысам тиотриазолина и АСК приводило к взаимному усилению их эффектов. При этом в сыворотке крови уровень МДА и ДК снижался на 50,4% (Р<0,05) и 40,6% (Р<0,05), а активность СОД и каталазы увеличилась на 68,8% (Р<0,05) и 36,4% (Р<0,05) соответственно по сравнению с контрольной группой. Данные изменения показателей активности процессов ПОЛ также достоверно отличались от результатов, полученных в группе АСК, что свидетельствует о более высокой антиоксидантной активности комбинированного препарата. Результаты, полученные при исследовании активности процессов ПОЛ в структурах головного мозга, подтверждают выявленные ранее закономерности. На фоне введения комбинированного препарата в стволе, гиппокампе и коре достоверно уменьшились уровни МДА и ДК, и возрастала активность СОД и каталазы.
Результаты исследований представлены в таблицах 6 и 7.
Влияние тиотриазолина, ацетилсалициловой кислоты и их комбинации на показатели перекисного окисления липидов (ПОЛ) в структурах головного мозга крыс
Полученные результаты, анализ эффективности предложенной комбинации и препарата сравнения (прототипа) свидетельствуют, что предложенная комбинация имеет более выраженное антиагрегантное и антиоксидантное действие, ее использование позволяет снизить частоту проявления нежелательных эффектов проводимой фармакотерапии.
Заявляемый объект - комбинация классического антиагрегантного средства ацетилсалициловой кислоты и антиоксидантного препарата тиотриазолина - в условиях экспериментальной медицины способствует более сильному угнетению агрегации тромбоцитов.
Технический результат, который достигается при использовании изобретения, определяется потенцированием эффектов ацетисалициловой кислоты при использовании ее комбинации с тиотриазолином.
Использование предложенной комбинации в одной лекарственной форме уменьшает стоимость лечения, а также повышает комплаенс (склонность больных к лечению) благодаря упрощению введения и соблюдения режима приема.
Таким образом, разработанное решение задачи соответствует изобретательскому уровню и отвечает условию «промышленная пригодность», что позволяет квалифицировать его как изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска снижения эффективности антиагрегантной терапии | 2016 |
|
RU2623051C1 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ И АНТИТРОМБОГЕННУЮ АКТИВНОСТИ | 2010 |
|
RU2453312C1 |
| КОМБИНАЦИЯ, ОБЛАДАЮЩАЯ АНТИАГРЕГАНТНОЙ, ЛИПИДРЕГУЛИРУЮЩЕЙ И ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2453314C1 |
| КАРДИОПРОТЕКТОРНОЕ, АНТИАРИТМИЧЕСКОЕ, ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО | 2007 |
|
RU2366426C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТРОМБОТИЧЕСКОГО ЭФФЕКТА АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ | 2007 |
|
RU2379684C2 |
| Дикалиевая соль N-(3-гидроксибензоил)таурина, обладающая антиагрегантной и антитромботической активностью в сочетании с церебропротективным действием | 2019 |
|
RU2730835C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ АНТИАГРЕГАНТНОГО ПРЕПАРАТА В ОБРАЗЦАХ ЦЕЛЬНОЙ ПЕРИФЕРИЧЕСКОЙ КРОВИ | 2022 |
|
RU2800671C1 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ АКТИВНОСТЬ | 2011 |
|
RU2486182C2 |
| СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ТРОМБОЦИТОВ | 2012 |
|
RU2497520C1 |
| ДИГИДРОХЛОРИД 1-(3-МОРФОЛИНОПРОПИЛ)-2-ФЕНИЛИМИДАЗО[1,2-a]-БЕНЗИМИДАЗОЛА, ПРОЯВЛЯЮЩИЙ СВОЙСТВА АНТАГОНИСТА ПУРИНОВЫХ P2Y-РЕЦЕПТОРОВ, АНТИАГРЕГАНТНУЮ И АНТИТРОМБОТИЧЕСКУЮ АКТИВНОСТЬ | 2008 |
|
RU2391345C2 |
Изобретение относится к лекарственным средствам и касается комбинированного антиагрегантного и антиоксидантного лекарственного средства, содержащего как активную основу ацетилсалициловую кислоту, отличающегося тем, что активная основа дополнительно содержит тиотриазолин. Предложенное комбинированное лекарственное средство обладает более выраженным антиагрегантным и антиоксидантным действием и обеспечивает снижение частоты проявлений нежелательных эффектов длительной фармакотерапии. 1 з.п. ф-лы, 1 ил., 7 табл.
1. Комбинированное антиагрегантное и антиоксидантное лекарственное средство, содержащее как активную основу ацетилсалициловую кислоту, отличающееся тем, что активная основа дополнительно содержит тиотриазолин.
2. Комбинированное антиагрегантное и антиоксидантное лекарственное средство по п.1, отличающееся тем, что оно содержит ацетилсалициловую кислоту в соотношении с тиотриазолином 4:1.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| - М.: Новая волна, 2005, с.164-166 | |||
| МАЗУР И.А | |||
| и др | |||
| Тиотриазолин: фармакологические аспекты и клиническое применение | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ЛЕВИЦКИЙ Е.Л | |||
| и др | |||
| Коррекция поражений ядерного генома антиоксидантами в условиях токсического повреждения печени (обзор)// Современные проблемы | |||
Авторы
Даты
2011-10-10—Публикация
2010-01-12—Подача