Изобретение относится к медицине, а именно к экспериментальной и клинической хирургии и трансплантологии, и может быть использовано при получении тканевых эквивалентов для восстановления полнослойных дефектов слизистых оболочек различной площади в качестве искусственной матрицы-носителя клеточного трансплантата.
Известен способ устранения дефектов слизистых оболочек с использованием активного биологического комплекса для органогенеза, представляющего собой многокомпонентную, объемную, трехмерную структуру, содержащую аллогенные клетки мезенхимы и эпителия человека и, по крайней мере, один слой из биосовместимого полимера в виде сетчатой матрицы внутри коллагеновой структуры (RU 2254146 C2, 20.06.2005).
Данный материал имеет следующие недостатки
1) Наличие в составе комплекса нежного коллагенового геля и ригидной сетки приводит к прорезыванию последней, что нарушает непрерывность клеточных слоев трансплантата.
2) Ригидная полимерная сетка затрудняет механические манипуляции с комплексом, ограничивает возможности придания трансплантату необходимой формы (например, не позволяет свернуть его в трубку небольшого диаметра).
3) Клеточные слои на поверхности нежного коллагенового геля легко травмируются при манипуляциях во время трансплантации комплекса, что ухудшает их приживление.
4) Комплекс имеет недостаточные прочностные характеристики для наложения фиксирующих хирургических швов.
5) Отсутствие пор в материале подложки (комплекс гель-сетка) затрудняет миграцию клеток реципиента в комплекс, а следовательно, процесс его приживления и ремоделирования.
Задачей предлагаемого изобретения является более высокоэффективный, достаточно эластичный и прочный биосовместимый материал.
Поставленная задача решается биологическим материалом подложки тканевых эквивалентов слизистых оболочек, характеризующимся тем, что представляет химико-ферментативно обработанный ксеноперикард, имеющий микроперфорации диаметром 20-400 мкм и плотностью 5-20 перфораций на мм2.
В качестве материала для получения тканевой подложки был использован химико-ферментативно обработанный перикард, полученный по патенту RU 215150, путем последовательной обработки растворами глутарового альдегида перикарда крупного рогатого скота, полученного в первые 6 часов после забоя животных.
Затем после химико-ферментативной обработки ксеноперикард подвергали воздействию импульсного излучения Nd: YAG лазера с длиной волны 1,064 мкм, средней мощностью 10-12 Вт, на промышленном лазерном комплексе JET-Spot, Эквиплюс, РФ, разрешающая способность которого позволила получить до 20 микроперфораций на мм2, диаметром 20-400 мкм.
Химико-ферментативно обработанный ксеноперикард является материалом, широко применяемым в сердечно-сосудистой и абдоминальной хирургии (Иванов А.С., Балоян Г.М., Аль-Азизи М. Истмопластика коарктации аорты. 15-летний опыт клинического применения ксеноперикарда. Клинический опыт и проблемы коллагенопластики. Матер. науч.-практ. конф. М., 1999). Также существуют экспериментальные исследования возможностей применения ксеноперикарда для устранения дефектов уретры, однако результаты оказались неудовлетворительными (Lara RC, Lucon AM, Arap S. Urethroplasty using a bovine pericardium graft: an experimental study using normal urethras from dogs. Braz. J. Med. Biol. Res. 2004 Mar; 37(3):327-3L). Попытки использования нативного материала в качестве подложки тканевого эквивалента слизистой оказались безуспешными.
С целью обеспечения возможности миграции клеток в толщу материала для обеспечения эффективного неоангиогенеза и ремоделирования материала, и как следствие, более полного и быстрого приживления эквивалента, была выполнена перфорация материала.
Существуют различные методики химико-ферментативной обработки биоматериалов (например, RU 2120212 С1, 20.10.1998; RU 2384348 С2, 07.04.2008). Предварительная обработка биоматериалов преследует следующие цели: удаление клеточных элементов и антигенной составляющей (снижение иммуногенности), стабилизация структуры материала.
Микроперфорации могут быть нанесены различными методами, предпочтительно лазером, толщина и энергия пучка которого варьирует в зависимости от толщины и свойств материала. Порозность определена экспериментальным путем и является оптимальной.
На примере химико-ферментативно обработанного ксеноперикарда нами показаны преимущества материала, перфорированного в соответствии с изобретением.
Нижеследующие экспериментальные исследования иллюстрируют биологические свойства материала по изобретению.
Исследовался материал толщиной от 0,2 до 2 мм. Микроперфорации диаметром от 40 до 200 мкм и плотностью до 20 отверстий на мм2 получали с помощью лазера. Ширина и энергия пучка подбирались в зависимости от толщины материала и необходимого размера пор. Тестирование материалов проводили на 40 белых лабораторных крысах. Для этого каждому животному имплантировали под кожу по одному образцу перфорированного и неперфорированного ксеноперикарда. Имплантацию проводили из отдельных кожных разрезов, в сформированные тупым способом карманы. Фиксацию образцов к подлежащим тканям выполняли узловыми швами. Вывод животных из эксперимента и забор материалов для исследования выполняли на сроках 7, 14 дней, 1,3, и 6 месяцев. Выполняли световую микроскопию срезов окрашенных гематоксилин-эозином. По результатам гистологического исследования образцов неперфорированного ксеноперикарда в тканях получены следующие результаты:
- на 7-е сутки по периферии образца наблюдается умеренная клеточная инфильтрация, образование грануляционной ткани,
- на 14-е сутки определяется слабая краевая инфильтрация перикарда, единичные новообразованные сосуды в прилежащих тканях
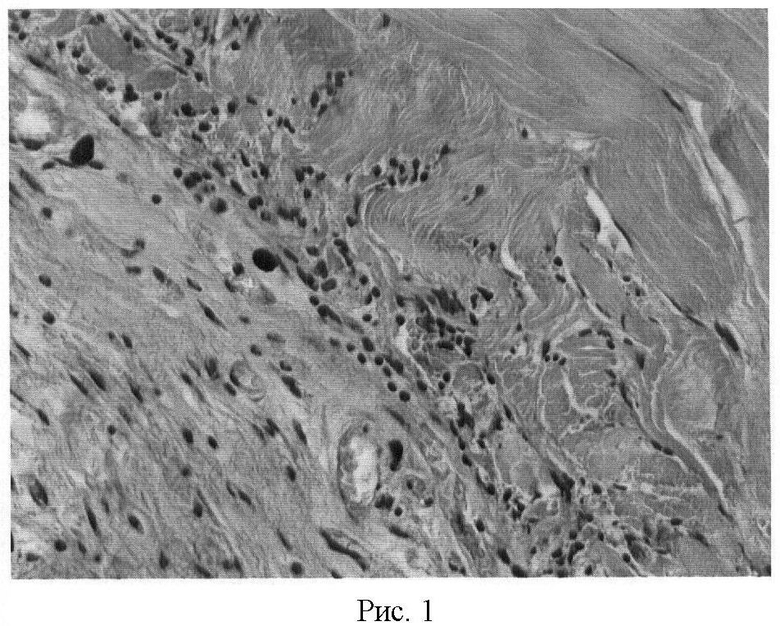
- к концу 1-го месяца наблюдаются признаки ремоделирования материала, клеточные включения определяются до трети толщины перикарда, трансплантат окружен рыхлой соединительной тканью с сформированной сосудистой сетью не проникающей в толщу материала (Рис.1).
По результатам гистологического исследования образцов микроперфорированного ксеноперикарда в тканях получены следующие результаты:
- на 7-е сутки поры полностью заполнены грануляционной тканью
- на 14-е сутки наблюдается прорастание пор рыхлой грануляционной тканью с единичными сосудами на всю глубину трансплантата
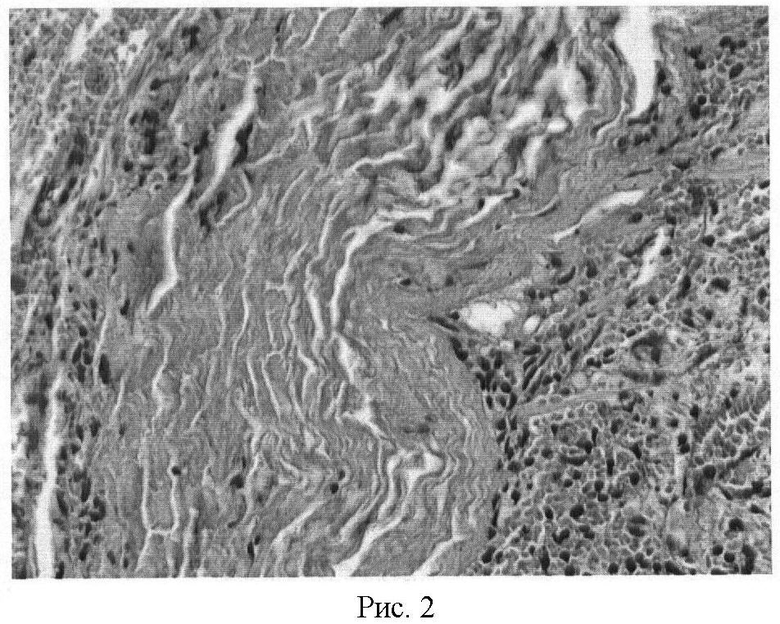
- к концу 1-го месяца трансплантат окружен рыхлой соединительной тканью с сформированной сосудистой сетью, которая проникает на всю толщину перфорированного перикарда (Рис.2).
В ходе эксперимента подтверждена низкая иммуногенность материала, постепенное ремоделирование в тканях, неоангиогенез. Перфорированный ксеноперикард по сравнению с обычным перикардом значительно быстрее интегрируется с окружающими тканями за счет активной миграции клеток в толщу материала сквозь поры и неоангиогенеза в заполняющей поры грануляционной ткани. Также в лабораторных условиях показана возможность закрепления клеток (фибробластов и кератиноцитов) на поверхности материала.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА ПРИ КСЕНОПЛАСТИКЕ | 2011 |
|
RU2472153C1 |
| ТРАНСПЛАНТАТ ДЛЯ ВОССТАНОВЛЕНИЯ ДЕФЕКТОВ СОЕДИНИТЕЛЬНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2330675C2 |
| БИОЛОГИЧЕСКИЙ АКТИВНЫЙ КОМПЛЕКС ДЛЯ ОРГАНОГЕНЕЗА | 2003 |
|
RU2254146C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕЛЛЮЛЯРНОГО ДЕРМАЛЬНОГО МАТРИКСА | 2021 |
|
RU2769248C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ КОЖНОГО ПОКРОВА ПРИ ОБШИРНЫХ ГЛУБОКИХ ОЖОГАХ | 2024 |
|
RU2825747C1 |
| КОМПОЗИЦИОННЫЙ ЭКВИВАЛЕНТ ЖИВОЙ КОЖИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ТЕСТ-НАБОР | 1991 |
|
RU2135191C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ВЕРХНИХ ДЫХАТЕЛЬНЫХ ИЛИ ПИЩЕВАРИТЕЛЬНЫХ ПУТЕЙ | 2012 |
|
RU2523659C1 |
| СПОСОБ ДВУХЭТАПНОЙ БИОИНЖЕНЕРНОЙ РЕКОНСТРУКЦИИ ВЕРХНИХ ПИЩЕВАРИТЕЛЬНЫХ ПУТЕЙ | 2020 |
|
RU2726607C2 |
| Способ восстановления кожного покрова | 2019 |
|
RU2731313C1 |
| Способ одномоментного восполнения объема утраченнной костной ткани и прикрепленной десны | 2023 |
|
RU2818178C1 |
Изобретение относится к области медицины, а именно к экспериментальной и клинической хирургии и трансплантологии. Биологический материал подложки тканевых эквивалентов слизистых оболочек представляет собой химико-ферментативно обработанный ксеноперикард путем последовательной обработки растворами глутарового альдегида перикарда. При этом химико-ферментативно обработанный ксеноперикард имеет микроперфорации диаметром 20-400 мкм и плотностью 5-20 перфораций на мм2. Предложенный материал значительно быстрее интегрируется с окружающими тканями и позволяет повысить эффективность неоангиогенеза. 1 пр., 2 ил.
Биологический материал подложки тканевых эквивалентов слизистых оболочек, характеризующийся тем, что он представляет собой химико-ферментативно обработанный ксеноперикард, имеющий микроперфорации диаметром 20-400 мкм и плотностью 5-20 перфораций на мм2.
| СПОСОБ ПОДГОТОВКИ БИОТКАНИ ДЛЯ КСЕНОПРОТЕЗИРОВАНИЯ | 1999 |
|
RU2151505C1 |
| ПЕРИКАРД ИМПЛАНТИРУЕМОГО АВТОНОМНОГО ИСКУССТВЕННОГО СЕРДЦА | 1990 |
|
SU1783648A1 |
| СПОСОБ ПРОТЕЗИРУЮЩЕЙ ГЕРНИОПЛАСТИКИ СРЕДИННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ | 2009 |
|
RU2400160C1 |
| СПОСОБ ПОЛУЧЕНИЯ КСЕНОТРАНСПЛАНТАТОВ ДЛЯ ОФТАЛЬМОЛОГИИ | 2005 |
|
RU2281061C1 |
| Приспособление для конденсации влаги, выделяющейся из топлива в газогенераторах транспортного типа | 1936 |
|
SU50814A1 |
| Врубовая машина | 1924 |
|
SU2923A1 |
| БИОЛОГИЧЕСКИЙ ПРОТЕЗ КЛАПАНА СЕРДЦА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2007 |
|
RU2355361C2 |
| БАРБАРАШ Л.С | |||
| и др | |||
| Возможности использования лазерных технологий в производстве кардиоваскулярных протезов // Бюллетень СО РАМН, т.30, №5, 2010, статья, | |||
Авторы
Даты
2012-03-20—Публикация
2010-11-25—Подача