Изобретение относится к области биологически активных соединений, касается разработки новых производных класса 1,3,4-тиадиазинов, обладающих антиагрегантным действием и предназначенных для лечения и профилактики таких заболеваний, как инфаркт миокарда, нарушение мозгового кровообращения, отторжение пересаженных органов и тканей, а также могут предотвращать образование тромбозов и эмболий.
Агрегация тромбоцитов играет ведущую роль в возникновении сердечно-сосудистых заболеваний (нарушения коронарного и мозгового кровообращения, патологии сосудов конечностей, брюшной полости и др.) в развитии тромбозов при нарушении кровообращения после хирургических операций. Разработка средств, тормозящих агрегацию тромбоцитов, является важной проблемой современной медицины и позволит значительно улучшить лечение инфаркта миокарда, тромботического инсульта (данные заболевания являются ведущей причиной смертности в развитых странах), тромбозов конечностей, послеоперационных тромбозов, нарушений кровообращения глаз и др.
Наиболее распространенными ингибиторами агрегации являются ацетилсалициловая кислота, дипиридамол, дериваты арахидоновой кислоты (простациклин и его производные, простагландин E1), блокаторы АДФ- и фибриногеновых рецепторов (различные моноклональные антитела, циклические пептиды, соединения непептидной природы), n-3 полиненасыщенные жирные кислоты (ПНЖК). Между тем возможности врача в регуляции тромбоцитарного гемостаза в настоящее время еще недостаточны для оптимального воздействия на данную функцию, т.к. известные лекарственные средства, обладающие антиагрегационным действием, имеют существенные недостатки. Так, ацетилсалициловая кислота оказывает побочное ульцерогенное и гепатотоксическое действие. Широкому клиническому использованию простациклина и простагландина E1 препятствует их крайняя нестабильность и быстрая скорость метаболизма в организме человека. Препараты дипиридамол, пентоксифиллин обладают сравнительно небольшим антиагрегационным действием и сильным сосудорасширяющим эффектом в применяемых дозах. Моноклональные антитела дороги и обладают выраженным иммуногенным действием, что приводит к аллергическим реакциям и тромбоцитопении (что может сопровождаться кровотечением). Полиненасыщенные жирные кислоты обладают антиагрегационным действием, однако оно развивается не сразу, а только при длительном применении.
В последние годы за рубежом разработаны эффективные ингибиторы агрегации тромбоцитов из группы производных тиенопиперидина (клопидогрель). По данным многих авторов клопидогрель является на сегодняшний день наиболее оптимальным из всех имеющихся препаратов. Однако его собственный терапевтический эффект развивается только на второй день и достигает максимума лишь на 4-7-й день лечения. Кроме того, при его применении часто встречаются осложнения в виде диареи, сыпи и лейкопении. Для получения необходимого быстрого антиагрегантного эффекта его часто используют с аспирином, но это иногда приводит к внутренним кровотечениям.
В настоящее время в мире по-прежнему активно разрабатываются способы целенаправленного химического синтеза антиагрегантов нового поколения, обладающих высокой эффективностью и избирательностью действия. Из литературных данных известно, что соединения, принадлежащие к классу тиадиазинов, оказывают выраженное влияние на свертывающую систему крови. Известны различные представители класса тиадиазина, отличающиеся положением гетероатомов в тиадиазиновом кольце, которые обладают выраженным влиянием на свертывающую систему крови. Так, N.Campillo с соавторами [1] констатировал уменьшение агрегации тромбоцитов, индуцированной АДФ, арахидоновой кислотой и коллагеном, как in vitro, так и ex vivo при воздействии фенил- и гетероарилпиразино[2,3-c][1,2,6]тиадиазин-2,2-диоксидов. В работе [Rehse K] показано, что 2-нитрозоимино-3,6-дигидро-2H-1,3,4-тиадиазины также снижают агрегацию тромбоцитов, индуцированную коллагеном [2]. В исследованиях [Ozcelic АВ] установлена антифибринолитическая активность и ингибирование тромбоцитарной агрегации 3-замещенных-5-(4-карбокси-циклогексилметил)-тетрагидро-2H-1,3,5-тиадиазин-2-тионов [3].
В рядах 1,3,4-тиадиазинов нами ранее были найдены вещества, обладающие уникальным сочетанным антикоагулянтным и антиагрегантным действием [4], и эффективные антиагреганты при внутривенном введении [5]. Таким образом, 1,3,4-тиадиазины представляют собой класс соединений, на основе которых возможно создание эффективных препаратов с антиагрегантым действием, действующих на функциональное состояние тромбоцитов.
Такие соединения могут быть использованы в кардиологии и позволят значительно улучшить лечение различных сердечно-сосудистых заболеваний, в том числе инфаркта миокарда и тромботического инсульта.
Техническим результатом предлагаемого изобретения является создание новых химических соединений класса 1,3,4-тиадиазинов, обладающих антиагрегантым действием и пригодных для внутривенного введения.
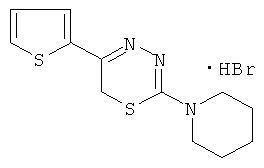
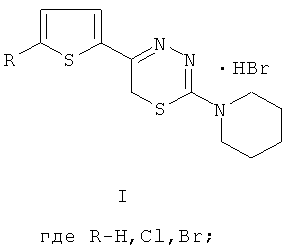
Указанный технический результат достигается тем, что согласно изобретению синтезированы новые 2-пиперидино-5-(тиенил-2)-6H-1,3,4-тиадиазины, гидробромиды (общая формула 1) и 2-пиперидино-5-(тиенил-3)-6H-1,3,4-тиадиазины, гидробромиды (общая формула 2), обладающие антиагрегантной активностью.
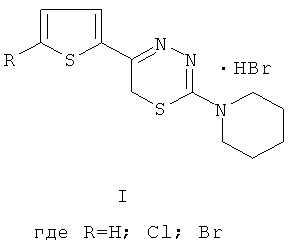

Близкими по структуре (прототип) по отношению к заявляемым 2-циклоалкиламино-5-тиенил-1,3,4-тиадиазинам и обладающими антиагрегантным действием являются 2-циклоалкиламино-5-тиенил-1,3,4-тиадиазины [5] общей формулы III:
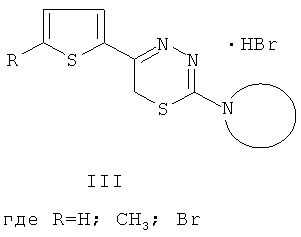
 морфолино-, тиоморфолино-, пирролидино-, 2,6-диметилморфолино-, гексаметиленамино- .
морфолино-, тиоморфолино-, пирролидино-, 2,6-диметилморфолино-, гексаметиленамино- .
Заявляемые соединения формул I и II отличаются от прототипа (формула III) тем, что в положении-2 1,3,4-тиадиазинового кольца находится остаток пиперидина, а в положение-5 - в формуле II кроме заместителя тиенил-2 введен также заместитель - тиенил-3.
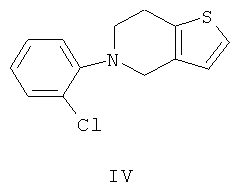
За прототип соединений I и II по биологической активности мы взяли эффективный зарубежный препарат «клопидогрель» [6] (формула IV), принадлежащий к классу тиенопиперидинов. Препараты формулы I, II и формулы IV принадлежат к различным классам гетероциклических соединений, но содержат одинаковые гетероциклы в структуре соединений - пиперидин и тиофен. Такой подход к «конструированию» потенциальных препаратов с антиагрегантной активностью в классе 1,3,4-тиадиазинов оказался результативным: был синтезирован ряд эффективных соединений формулы I и II, обладающих антиагрегантным действием, сравнимым при испытаниях на тромбоцитах крови человека с действием «клопидогреля».
Примеры синтеза и физико-химические характеристики заявляемых соединений
Все соединения получены с выходом 51-61% путем конденсации соответствующих α-бром-2-ацетилтиофенов или α-бром-3-ацетилтиофенов и 4,4-пентаметиленаминотиосемикарбазида при нагревании в абсолютном этаноле и последующим высаживанием (или без высаживания) продуктов реакций абсолютным диэтиловым эфиром из охлажденных растворов. Строение соединений доказано спектральными данными ЯМР 1H на спектрометре «Bruker DRX-400» с рабочей частотой 400,13 Мгц, внутренний стандарт Me4Si. Чистота соединений подтверждена элементным анализом, тонкослойной хроматографией.
Пример 1
2-Пиперидино-5-(тиенил-2)-6H-1,3,4-тиадиазин, гидробромид (1).
К раствору 2,05 г (10 ммоль) α-бром-2-ацетилтиофена в 30 мл абсолютного этанола добавляли 1,59 г (10 ммоль) 4,4-пентаметиленаминотиосемикарбазида в 40 мл абсолютного этанола, 0,5 мл конц. HBr и кипятили на водяной бане в течение 40 мин. После горячего фильтрования к охлажденному реакционному раствору прибавляли 170 мл абсолютного диэтилового эфира. Выпавший осадок тиадиазина 1 отфильтровывали, сушили и перекристаллизовывали из смеси абсолютный этанол: диэтиловый эфир 1:3. Выход 2,1 г (61%). Т.пл. 232-233°C (светло-желтые кристаллы). Rf=0,53 (элюент, бутанол: уксусная кислота: вода 4:1: 5). Найдено, %: C 41,54; H 4,71; N 12,11. C12H16BrN3S2. Вычислено, %: C 41,62; H 4,62; N 12,14. ЯМР 1H (ДМСО-d6), δ, м.д.: 1,77 (c, 6H, пиперидино), 3,89 (c, 4H, пиперидино), 4,45 (c, 2H. CH2S), 7,20 (д.д. 1H тиофена), 7,75 (д. 1H тиофена), 7,85 (д, 1Н тиофена).
Пример 2
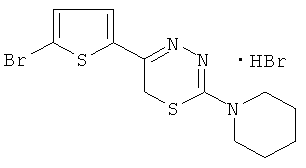
2-Пиперидино-5-(5'-бромтиенил-2)-6Н-1,3-4-тиадиазин, гидробромид (2).
Соединение синтезировано нагреванием 0,56 г (2 ммоль) α-бром-5-бром-2-ацетилтиофена с 0,32 г (2 ммоль) 4,4-пентаметиленаминотиосемикарбазида в 60 мл абсолютного этанола и 0,1 мл конц. HBr 40 мин. К охлажденному реакционному раствору добавляли 70 мл абсолютного диэтилового эфира. Выпавший осадок тиадиазина 2 отфильтровывали, сушили и перекристаллизовывали из абсолютного этанола с добавлением абсолютного эфира в соотношении абсолютный этанол: абсолютный эфир 1:4. Выход 0,44 г (51%). Т.пл. 222-223°C (желтые кристаллы, из смеси этанол: абсолютный эфир 1:4). Rf=0,57 (бутанол: уксусная кислота: вода 4:1:5). Найдено, %: C 33,65; H 3,57; N 9,79. C12H15Br2N3S2. Вычислено, %: 33,88; Н 3,53; N 9,88. ЯМР 1H (ДМСО-d6), δ, м.д: 1,88 (c, 6Н, пиперидино), 3,87 (c, 4Н, пиперидино),4,38 (c, 2Н, CH2S), 7,27 (д., 1Н тиофена), 7,67 (д., 1Н тиофена).
Пример 3
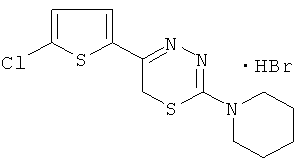
2-Пиперидино-5-(5'-хлортиенил-2)-6Н-1,3-4-тиадиазин, гидробромид (3).
Соединение синтезировано кипячением 3,1 г (13 ммоль) α-бром-5-хлор-2-ацетилтиофена с 2,07 г (13 ммоль) 4,4-пентаметиленаминотиосемикарбазида в 100 мл абсолютного этанола с добавлением 0,5 мл конц. HBr 35 мин. После горячего фильтрования к охлажденному реакционному раствору добавляли 180 мл абсолютного диэтилового эфира, выпавший осадок светло-желтого цвета отфильтровывали, сушили и перекристаллизовывали из абсолютного этанола. Выход 2,5 г (51%). Т пл. 220-222°C (желтые кристаллы, из абсолютного этанола). Rf=0,42 (элюент, бутанол: уксусная кислота: вода 4:1:5). Найдено, %: C 37,81; H 3,97; N 11,15. C12H15BrClN3S2. Вычислено, %: C 37,84; H 3,94; N 11,04. ЯМР 1H (ДМСО-d6), δ, м.д: 1,76 (c, 6Н, пиперидино), 3,88 (c, 4Н, пиперидино), 4,39 (c, 2Н. CH2S), 7,16 (д., 1Н тиофена). 7,72 (д., 1Н тиофена).
Пример 4
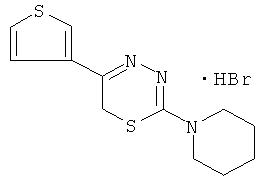
2-Пиперидино-5-(тиенил-3)-6Н-1,3,4-тиадиазин, гидробромид (4).
Соединение синтезировано кипячением 4,1 г (20 ммоль) α-бром-3-ацетилтиофена с 3,18 г (20 ммоль) 4,4-пентаметиленаминотиосемикарбазида в 120 мл абсолютного этанола и 1,0 мл конц. HBr 45 мин. После горячего фильтрования к охлажденному раствору добавляли 150 мл абсолютного диэтилового эфира, выпавший осадок отфильтровывали, сушили и перекристаллизовывали из абсолютного этанола и диэтилового эфира в соотношении абсолютный этанол: эфир 2:1.. Выход 3,6 г (52%). Т пл. 183-184°C. Rf=0,55 (элюент, бутанол: уксусная кислота: вода 4:1:5). Найдено, %: C 41,56; H 4,77; N 12,18. C12H16BrN3S2. Вычислено, %: C 41,62; H 4,62; N 12,14. ЯМР 1H (ДМСО-d6), δ, м.д.: 1,77 (c, 6Н, пиперидино), 3,89 (c, 4H, пиперидино), 4,36 (c, 2Н, CH2S), 7,59 (д, 1Н тиофена), 7,62 (д, 1Н тиофена), 8,33 (д., 1Н тиофена).
Пример 5
2-Пиперидино-5-(2'5'-дихлортиенил-3)-6Н-1,3-4-тиадиазин, гидробромид (5).
Соединение получено кипячением на водяной бане 1,37 г (5 ммоль) α-бром-2,5-дихлор-3-ацетилтиофена с 0,8 г (5 ммоль) 4,4-пентаметиленаминотиосемикарбазида в 80 мл абсолютного этанола. После горячего фильтрования и последующего охлаждения выпавший осадок отфильтровывали, сушили и перекристаллизовывали из смеси абсолютного этанола и абсолютного эфира (абсолютный этанол: абсолютный эфир 1:2). Выход 1,2 г (58%). Т пл. 202-203°C (бесцветные кристаллы). Rf=0,89 (бутанол: уксусная кислота: вода 4:1:5). Найдено, %: C 34,75; H 3,30; N 10,25. C12H14BrCl2N3S2. Вычислено, %: C 34,70; H 3,37; N 10,12. ЯМР 1H (ДМСО-d6), 6, м.д.: 1,77 (c, 6Н, пиперидино), 3,89 (c, 4Н, пиперидино), 4,25 (c, 2Н, CH2S), 7,45 (c, 1Н тиофена).
Примеры исследования антиагрегантной активности заявляемых соединений
Оценка антиагрегантной активности новых соединений была проведена в лаборатории патологии и фармакологии гемостаза Гематологического научного центра РАМН г.Москва. Выявлена высокая способность ингибировать агрегацию тромбоцитов крови человека у пяти растворимых в воде препаратов.
Эксперименты по исследованию антиагрегационной способности соединений были выполнены с использованием венозной крови здоровых доноров (n=50), которую получали путем пункции кубитальной вены и стабилизировали 3,8%-ным раствором цитрата натрия в соотношении 9:1. Для приготовления богатой тромбоцитами плазмы кровь центрифугировали в течение 10 минут при 1000 об/мин, после чего верхний слой плазмы переносили в другую пробирку, а остаток повторно центрифугировали в течение 20 минут при 3000 об/мин для получения плазмы, бедной тромбоцитами.
Агрегацию тромбоцитов исследовали на агрегометре фирмы "Chrono-Log Corporation" (США) по методу G.Born [7]. С этой целью в кювету прибора помещали 250 мкл богатой тромбоцитами плазмы. Оптическим контролем служил такой же объем плазмы, не содержащей тромбоцитов. О степени агрегации судили по максимальной величине падения оптической плотности после окончания реакции (Amax) по сравнению с исходной величиной. Эксперименты проводили следующим образом: в кювету, содержащую 250 мкл богатой тромбоцитами плазмы, добавляли 28 мкл изучаемого препарата и инкубировали полученную смесь в течение 5 мин при температуре 37°C и индуцировали процесс тромбоцитарной агрегации. В контрольных опытах к богатой тромбоцитами плазме добавляли только проагрегант.
В качестве проагрегантов в работе использовали аденозиндифосфорную кислоту (АДФ) (Boehringer Mannheim, Австрия) в конечной концентрации 1×10-5 М и арахидоновую кислоту (АК) в конечной концентрации 1×10-3 M. Арахидоновая кислота (АК), свободная от продуктов окисления, была получена сотрудниками лаборатории оксилипидов Института биоорганической химии им. М.М.Шемякина и Ю.А.Овчинникова РАН.
Статистический анализ полученных данных проводили в соответствии с общепринятыми методами вариационной статистики с использованием t-критерия Стьюдента [8].
Результаты исследования антиагрегационных свойств тиадиазинов приведены в таблицах 1 и 2.
Все исследованные соединения данной группы дозозависимо ингибировали АДФ-индуцированную агрегацию тромбоцитов, при этом они обладали одинаковой антиагрегационной способностью. Максимальное ингибирование агрегации - в 1,5-1,9 раза по сравнению с исходным уровнем отмечалось при использовании этих веществ в конечных концентрациях 1 mM. В минимальной исследованной концентрации (0,001 mM) агрегация уменьшалась на 15-20% по сравнению с исходным уровнем. Следует отметить, что антиагрегационный эффект этих соединений был сравним с действием «клопидогреля», являющегося одним из наиболее сильных антиагрегантов и селективным блокатором АДФ-рецепторов тромбоцитов на АДФ-индуцированную агрегацию in vitro (таблица 1).

В случае АК-индуцированной агрегации (таблица 2) наиболее активными ингибитором АК-индуцированной агрегации оказалось соединение 1, которое практически полностью подавляло тромбоцитарное взаимодействие в диапазоне концентраций 0,01-1 mM. Следует отметить, что антиагрегационный эффект 1 превосходил действие и ацетилсалициловой кислоты, которая является стандартным антагонистом АК-индуцированной агрегации. Все остальные соединения достоверно снижали АК-индуцированную агрегацию в дозах 0,025-1 mM. При этом в концентрации 0,025 mM агрегация уменьшалась в 1,1-1,3 раза и в 2 раза - для соединения 4.
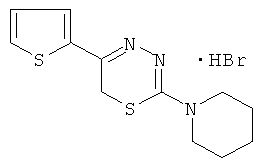

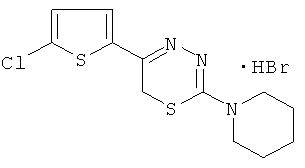

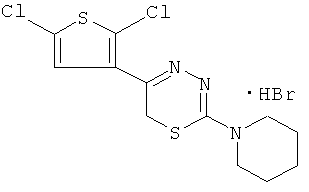
Таким образом, среди всех изученных соединений, содержащих в своей структуре и тиофен, и пиперидин, наиболее эффективным в испытаниях на тромбоцитах крови человека, как в случае АДФ-, так и АК-индуцированной агрегации, является соединение: 2-пиперидино-5-(тиенил-2)-6H-1,3,4-тиадиазин, гидробромид (1)
Промышленная применимость
Данные соединения могут быть использованы в качестве потенциальных фармакологически активных веществ в производстве лекарств сердечно-сосудистого спектра действия, позволяющих ингибировать тромбоообразование.
Источники научно-технической информации
1. Campillo N., García C., Goya P., et al. Novel arylpyrazino[2,3-c][1,2,6]thiadiazine 2,2-dioxides as inhibitors of platelet aggregation. 1. Synthesis and pharmacological evaluation. J. Med. Chem., 42(10), 1698-1704 (1999).
2. Rehse K., Brümmer U., Unsöld E. 2-Nitrosoimino-3,6-dihydro-2H-1,3,4-thiadiazines with antiplatelet and antithrombotic properties. Pharmazie., 53 (12), 820-824 (1998).
3. Ozcelik A.B., Ersan S., Ural A.U., et al. Synthesis of 3-substituted-5-(4-carb oxycyclohexylmethyl)-tetrahydro-2H-1,3,5-thiadiazine-2-thione derivatives as antifibrinolytic and antimicrobial agents. Arzneimittelforschung., 57 (8), 554-559 (2007).
4. Патент РФ №2259371 (2005). Чупахин O.H., Сидорова Л.П., Перова Н.М., Чарушин В.Н., Русинов В.Л. и др. «Замещенные 5R1, 6R2-1,3,4-тиадиазин-2-амины и содержащие их фармацевтические композиции в качестве фармакологически активных средств, обладающих антикоагулянтным и антиагрегантным действием».
5. Патент РФ №2379306 (2010), Чупахин О.Н., Сидорова Л.П., Перова Н.М., Русинов В.Л., Макаров В.Л., Васильева Т.М., Воробьев А.И. «2-Циклоалкиламино-5-тиенил-1,3,4-тиадиазины гидробромиды, обладающие антиагрегантным действием».
6. Chua D, Ignaszewski A. Clopidogrel in acute coronary syndromes. BMJ. 2009 Apr 14; 338:b1180.
7. Born G. Aggregation of blood platelets by adenosine diphosphate and its reversal Nature (London), 194, 927-929 (1962).
8. Лакин Г.Ф. Биометрия: Учеб. пособие для биол. спец. вузов - 4-е изд., перераб. и доп. - М.: Высш. шк., 1990. - 352 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-ЦИКЛОАЛКИЛАМИНО-5-ТИЕНИЛ-1,3,4-ТИАДИАЗИНЫ ГИДРОБРОМИДЫ, ОБЛАДАЮЩИЕ АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2008 |
|
RU2379306C1 |
| 5-(4'-ГИДРОКСИФЕНИЛ)- И 5-(2',5'-ДИГИДРОКСИФЕНИЛ)-6Н-1,3,4-ТИАДИАЗИН-2-АМИНЫ, ГИДРОГАЛАГЕНИДЫ, ИНГИБИРУЮЩИЕ АГРЕГАЦИЮ ТРОМБОЦИТОВ ПРИ ВНУТРИВЕННОМ ВВЕДЕНИИ | 2009 |
|
RU2458060C2 |
| 2-АМИНОПРОПИЛМОРФОЛИНО-5-АРИЛ-6Н-1,3,4-ТИАДИАЗИНЫ, ДИГИДРОБРОМИДЫ И 2-АМИНОПРОПИЛМОРФОЛИНО-4-АРИЛТИАЗОЛЫ, ГИДРОБРОМИДЫ, ОБЛАДАЮЩИЕ АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2456284C1 |
| 2-(1S,2R,5S)-6,6-ДИМЕТИЛБИЦИКЛО[3.1.1]ГЕПТ-2ИЛ]МЕТИЛ}СУЛЬФИНИЛ)ЭТАНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ АНТИАГРЕГАЦИОННЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2522198C2 |
| ЗАМЕЩЕННЫЕ 5R,6R 1,3,4-ТИАДИАЗИН-2 АМИНЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ В КАЧЕСТВЕ ФАРМАКОЛОГИЧЕСКИ АКТИВНЫХ СРЕДСТВ, ОБЛАДАЮЩИХ АНТИКОАГУЛЯНТНЫМ И АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2259371C2 |
| Применение пинанилсульфида с метилмеркаптоацетатным фрагментом - метил 2-({ [(1S, 2R, 5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил]метил} тио)ацетата, обладающий ингибирующим действием на активацию тромбоцитов | 2015 |
|
RU2671567C2 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ АКТИВНОСТЬ | 2011 |
|
RU2486182C2 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ И АНТИТРОМБОГЕННУЮ АКТИВНОСТИ | 2010 |
|
RU2453312C1 |
| ДИГИДРОХЛОРИД 1-(3-МОРФОЛИНОПРОПИЛ)-2-ФЕНИЛИМИДАЗО[1,2-a]-БЕНЗИМИДАЗОЛА, ПРОЯВЛЯЮЩИЙ СВОЙСТВА АНТАГОНИСТА ПУРИНОВЫХ P2Y-РЕЦЕПТОРОВ, АНТИАГРЕГАНТНУЮ И АНТИТРОМБОТИЧЕСКУЮ АКТИВНОСТЬ | 2008 |
|
RU2391345C2 |
| ЗАМЕЩЕННЫЕ 6H-1,3,4-ТИАДИАЗИН-2-АМИНЫ, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНЕСТЕЗИРУЮЩИХ, СЕРДЕЧНО-СОСУДИСТЫХ И ГИПОМЕТАБОЛИЧЕСКИХ СРЕДСТВ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1995 |
|
RU2157210C2 |
Изобретение относится к 2-пиперидино-5-(тиенил-2)-6Н-1,3,4-тиадиазинам, гидробромидам (общей формулы I) и 2-пиперидино-5-(тиенил-3)-6Н-1,3,4-тиадиазинам, гидробромидам (общей формулы II), которые обладают антиагрегантным действием.
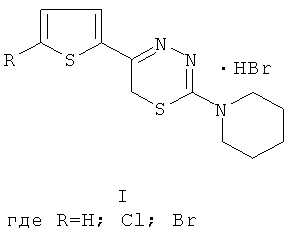

Данные соединения могут быть использованы при создании лекарственных препаратов для кардиологии и позволят значительно улучшить лечение различных сердечно-сосудистых заболеваний, в том числе инфаркта миокарда и тромботического инсульта. 2 табл., 5 пр.
2-Пиперидино-5-(тиенил-2)- и 2-пиперидино-5-(тиенил-3)-6Н-1,3,4-тиадиазины гидробромиды, обладающие антиагрегантным действием

| 2-ЦИКЛОАЛКИЛАМИНО-5-ТИЕНИЛ-1,3,4-ТИАДИАЗИНЫ ГИДРОБРОМИДЫ, ОБЛАДАЮЩИЕ АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2008 |
|
RU2379306C1 |
| ЗАМЕЩЕННЫЕ 5R,6R 1,3,4-ТИАДИАЗИН-2 АМИНЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ В КАЧЕСТВЕ ФАРМАКОЛОГИЧЕСКИ АКТИВНЫХ СРЕДСТВ, ОБЛАДАЮЩИХ АНТИКОАГУЛЯНТНЫМ И АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2259371C2 |
| Гидробромид 2-морфолино-5-(пиридил-2)-6 @ -1,3,4-тиадиазина в качестве реагента для фотометрического определения железа | 1984 |
|
SU1189862A1 |
| US 5137885 A1, 11.08.1992. | |||
Авторы
Даты
2012-03-20—Публикация
2010-04-12—Подача