По настоящей заявке испрашивается приоритет на основании предварительной заявки на патент США (U.S. Provisional Application) No. 60/991169, выданной 29 ноября 2007 года, содержание которой приводится здесь путем ссылки на нее в полном объеме.
Область техники, к которой относится изобретение
Изобретение относится к солям и полиморфам 2-[4-(3-хинолин-6-илметил-3Н-[1,2,3]триазоло[4,5-b]пиразин-5-ил)-пиразол-1-ил]этанола, применяемым при лечении аномального клеточного роста, такого как рак, у млекопитающих. Это изобретение также относится к композициям, включающим такие соли и полиморфы, и к способам применения таких композиций при лечении аномального клеточного роста у млекопитающих, в частности у человека.
Уровень техники
Соединение 2-[4-(3-хинолин-6-илметил-3Н-[1,2,3]триазоло-[4,5-b]пиразин-5-ил)пиразол-1-ил]этанол (называемое здесь также как "соединение 1"), представленное формулой 1
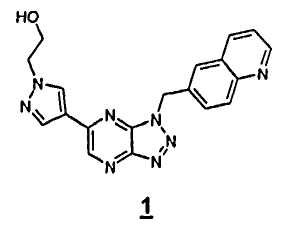
является сильнодействующим синтетическим ингибитором активности c-Met/HGFR (рецептора фактора роста гепатоцитов) киназы и активности ALK (киназы анапластической лимфомы). Соединение 1 обладает противоопухолевыми свойствами, которые фармакологически опосредованы через ингибирование c-Met/HGFR, который вовлечен в регуляцию роста и метастатическое развитие большого разнообразия типов опухолей, и ALK, которая вовлечена в патогенез ALCL (анапластической крупноклеточной лимфомы). Соединение 1 раскрыто в международной заявке No. PCT/IB2007/001142 и в патентной заявке US No. 11/745921, содержание которых приводится здесь путем ссылки на них в полном объеме.
Онкологические заболевания у людей включают разнообразное множество заболеваний, которые в совокупности являются одной из ведущих причин смертности в развитых странах во всем мире (Американское общество борьбы с раковыми заболеваниями, Рак. Факты и цифры. 2005. Атланта: Американское общество борьбы с раковыми заболеваниями; 2005). Развитие онкологических заболеваний вызывается рядом комплексных разнообразных генетических и молекулярных явлений, включающих мутации генов, хромосомные транслокации и кариотипические нарушения (Hanahan D, Weinberg RA. The hallmarks of cancer. Cell 2000; 100: 57-70). Несмотря на то что лежащие в основе рака генетические причины являются и разнообразными, и комплексными, обнаружено, что каждый тип рака проявляет общие черты и приобретенные возможности, которые содействуют его развитию. Эти приобретенные возможности включают неуправляемый клеточный рост, стабильную способность образовывать кровеносные сосуды (то есть способность к ангиогенезу) и способность опухолевых клеток распространяться местно, а также метастазировать во вторичные органы (Hanahan D, Weinberg RA. The hallmarks of cancer. Cell 2000; 100: 57-70). Поэтому возможность выявления новых терапевтических средств, которые 1) ингибируют молекулярные мишени, которые изменяются в процессе развития рака, или 2) нацелены на множество процессов, которые являются общими при развитии рака при различных опухолях, представляет большую важность.
В примере 209 патентной заявки US No. 11/745921 описано получение мезилатной соли соединения 1, которое, как было обнаружено, является кристаллическим полиморфом. Важно иметь соль и полиморфные соли, обладающие улучшенными свойствами, такими как улучшенная кристалличность, характеристики растворения и/или пониженная гигроскопичность, при сохранении свойств химической и энантиомерной стабильности.
Сущность изобретения
В одном варианте осуществления настоящее изобретение предлагает соединение, включающее соль, выбранную из группы, состоящей из гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола и тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В конкретных аспектах этого изобретения соль является безводной. В дополнительном аспекте соль является кристаллической. В дополнительном аспекте соль является кристаллической безводной солью. В дополнительном аспекте соль является практически чистым полиморфом. В дополнительном аспекте соль является соединением, включающим гидрохлоридную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте соль является соединением, включающим малеатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте соль является соединением, включающим фосфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте соль является соединением, включающим сульфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте соль является соединением, включающим тозилатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
В еще одном варианте осуществления настоящее изобретение предлагает фармацевтически приемлемую соль соединения формулы 1.
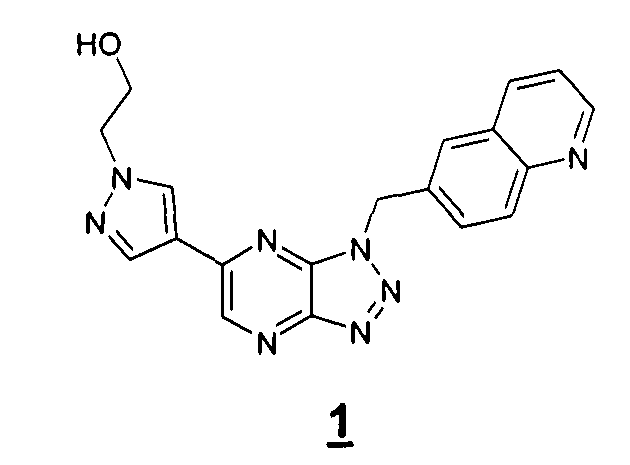
при условии, что фармацевтически приемлемая соль не является мезилатной солью. В дополнительном аспекте фармацевтически приемлемая соль является кристаллической. В дополнительном аспекте фармацевтически приемлемая соль является кристаллической безводной солью. В дополнительном аспекте фармацевтически приемлемая соль является практически чистым полиморфом. В дополнительном аспекте фармацевтически приемлемая соль является гидрохлоридной солью. В дополнительном аспекте фармацевтически приемлемая соль является малеатной солью. В дополнительном аспекте фармацевтически приемлемая соль является фосфатной солью. В дополнительном аспекте фармацевтически приемлемая соль является сульфатной солью. В дополнительном аспекте фармацевтически приемлемой солью является тозилатная соль.
В дополнительном аспекте настоящее изобретение предлагает соединение, представляющее собой кристаллическую гидрохлоридную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, которое характеризуется порошковой рентгенограммой, включающей пик при следующем значении угла дифракции (2θ): 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,7±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,7±0,2, 24,5±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,7±0,2, 24,5±0,2, 26,5±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,7±0,2, 24,5±0,2, 25,6±0,2, 26,5±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 11,6±0,2, 17,7±0,2, 24,5±0,2, 25,6±0,2, 26,5±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 11,6±0,2, 17,7±0,2, 20,3±0,2, 24,5±0,2, 25,6±0,2, 26,5±0,2 и 27,6±0,2. В дополнительном аспекте кристаллическая гидрохлоридная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): практически таких же, как приведенные на фиг.1.
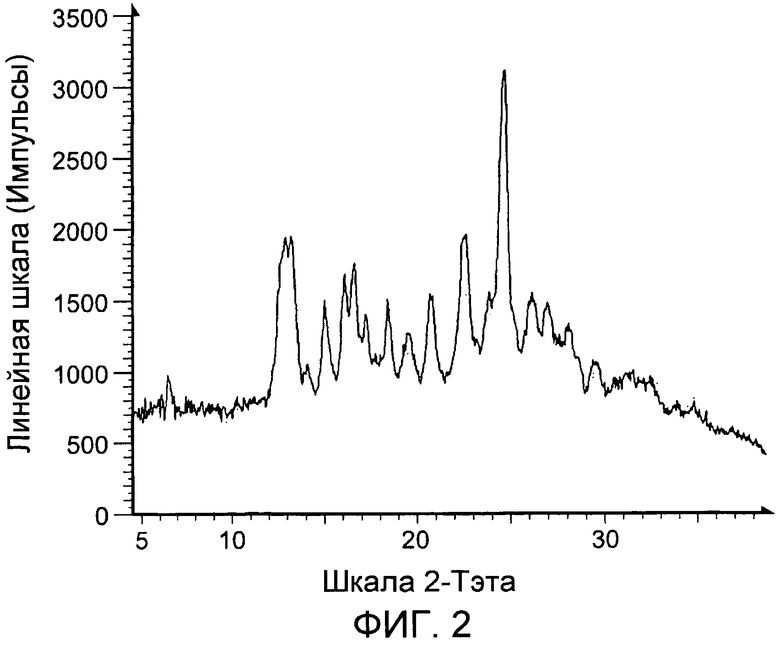
В дополнительном аспекте настоящее изобретение предлагает соединение, включающее кристаллическую малеатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пик при следующем значении угла (2θ): 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 22,6±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло-[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 13,2±0,2, 22,6±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-ил-метил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 12,9±0,2, 13,2±0,2, 22,6±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 12,9±0,2, 13,2±0,2, 16,6±0,2, 22,6±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 12,9±0,2, 13,2±0,2, 16,1±0,2, 16,6±0,2, 22,6±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 12,9±0,2, 13,2±0,2, 16,1±0,2, 16,6±0,2, 22,6±0,2, 23,9±0,2 и 24,6±0,2. В дополнительном аспекте кристаллическая малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): практически таких же, как приведенные на фиг.2.
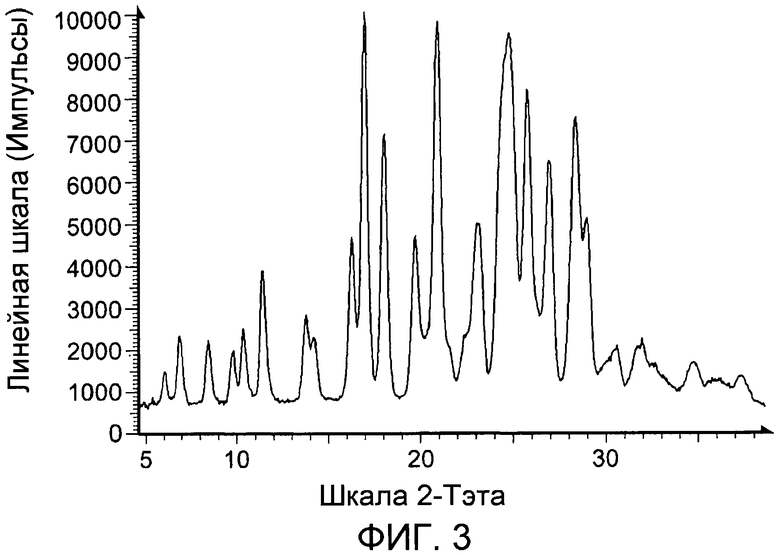
В дополнительном аспекте настоящее изобретение предлагает соединение, включающее кристаллическую фосфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пик при следующем значении угла (2θ): 17,0±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2 и 20,9±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2 и 24,8±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2, 24,8±0,2 и 25,8±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2, 24,8±0,2, 25,8±0,2 и 28,4±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2, 24,8±0,2, 25,8±0,2, 27,0±0,2 и 28,4±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2, 24,8±0,2, 25,8±0,2, 27,0±0,2, 28,4±0,2 и 28,9±0,2. В дополнительном аспекте кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): практически таких же, как приведенные на фиг.3.
В дополнительном аспекте настоящее изобретение предлагает соединение, включающее кристаллическую сульфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пик при следующем значении угла (2θ): 15,2±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2 и 18,0±0.2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2, 18,0±0,2 и 25,0±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2, 18,0±0,2, 25,0±0,2 и 27,2±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло-[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2, 18,0±0,2, 25,0±0,2, 25,7±0,2 и 27,2±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2, 18,0±0,2, 22,0±0,2, 25,0±0,2, 25,7±0,2 и 27,2±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 15,2±0,2, 18,0±0,2, 22,0±0,2, 25,0±0,2, 25,7±0,2, 27,2±0,2 и 27,8±0,2. В дополнительном аспекте кристаллическая сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): практически таких же, как приведенные на фиг.4.
В дополнительном аспекте настоящее изобретение предлагает соединение, включающее кристаллическую полиморфную форму тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пик при следующем значении угла (2θ): 24,4±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 16,5±0,2 и 24,4±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 16,5±0,2, 17,2±0,2 и 24,4±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 14,9±0,2, 16,5±0,2, 17,2±0,2 и 24,4±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 10,7±0,2, 14,9±0,2, 16,5±0,2, 17,2±0,2 и 24,4±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 10,7±0,2, 14,9±0,2, 16,5±0,2, 17,2±0,2, 24,4±0,2 и 27,2±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 10,7±0,2, 14,9±0,2, 16,5±0,2, 17,2±0,2, 24,4±0,2, 26,6±0,2 и 27,2±0,2. В дополнительном аспекте кристаллическая тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола характеризуется порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): практически таких же, как приведенные на фиг.5.
Настоящее изобретение дополнительно предлагает фармацевтическую композицию, включающую кристаллическую гидрохлоридную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Настоящее изобретение дополнительно предлагает фармацевтическую композицию, включающую кристаллическую малеатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Настоящее изобретение дополнительно предлагает фармацевтическую композицию, включающую кристаллическую фосфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Настоящее изобретение дополнительно предлагает фармацевтическую композицию, включающую кристаллическую сульфатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Настоящее изобретение дополнительно предлагает фармацевтическую композицию, включающую кристаллическую тозилатную соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
Настоящее изобретение дополнительно предлагает капсулу, включающую указанную фармацевтическую композицию. В конкретных аспектах этого варианта осуществления капсула включает от 0,2 до 200 мг кристаллической гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте капсула включает от 25 до 150 мг кристаллической гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном варианте осуществления капсула включает от 50 до 100 мг кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В конкретных аспектах этого варианта осуществления капсула включает от 0,2 до 200 мг кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте капсула включает от 25 до 150 мг кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном варианте осуществления капсула включает от 50 до 100 мг кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В конкретных аспектах этого варианта осуществления капсула включает от 0,2 до 200 мг кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте капсула включает от 25 до 150 мг кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном варианте осуществления капсула включает от 50 до 100 мг кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В конкретных аспектах этого варианта осуществления капсула включает от 0,2 до 200 мг кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте капсула включает от 25 до 150 мг кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном варианте осуществления капсула включает от 50 до 100 мг кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В конкретных аспектах этого варианта осуществления капсула включает от 0,2 до 200 мг кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном аспекте капсула включает от 25 до 150 мг кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло-[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В дополнительном варианте осуществления капсула включает 50 до 100 мг кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
В другом варианте осуществления изобретение предлагает способ лечения рака у млекопитающего, включая человека, который включает введение млекопитающему терапевтически эффективного количества фармацевтической композиции настоящего изобретения.
В другом варианте осуществления изобретение предлагает способ лечения рака у млекопитающего, который включает введение млекопитающему, включая человека, капсулы настоящего изобретения.
В другом варианте осуществления настоящее изобретение предлагает способ лечения аномального клеточного роста у млекопитающего, включая человека, если есть необходимость в таком лечении, включающий введение указанному млекопитающему терапевтически эффективного количества кристаллической гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В другом варианте осуществления настоящее изобретение предлагает способ лечения аномального клеточного роста у млекопитающего, включая человека, если есть необходимость в таком лечении, включающий введение указанному млекопитающему терапевтически эффективного количества кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В другом варианте осуществления настоящее изобретение предлагает способ лечения аномального клеточного роста у млекопитающего, включая человека, если есть необходимость в таком лечении, включающий введение указанному млекопитающему терапевтически эффективного количества кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В другом варианте осуществления настоящее изобретение предлагает способ лечения аномального клеточного роста у млекопитающего, включая человека, если есть необходимость в таком лечении, включающий введение указанному млекопитающему терапевтически эффективного количества кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. В другом варианте осуществления настоящее изобретение предлагает способ лечения аномального клеточного роста у млекопитающего, включая человека, если есть необходимость в таком лечении, включающий введение указанному млекопитающему терапевтически эффективного количества кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
В другом варианте осуществления аномальный клеточный рост опосредуется по меньшей мере одной генетически измененной тирозинкиназой. В другом варианте осуществления аномальный клеточный рост опосредуется рецептором фактора роста гепатоцитов (c-Met/HGFR) киназы или киназой анапластической лимфомы (ALK). В другом варианте осуществления аномальный клеточный рост опосредуется рецептором фактора роста гепатоцитов (c-Met/HGFR) киназы. В другом варианте осуществления аномальный клеточный рост опосредуется киназой анапластической лимфомы (ALK).
В другом варианте осуществления аномальным клеточным ростом является рак. В другом варианте осуществления рак выбирают из рака легких, рака кости, рака поджелудочной железы, рака кожи, рака головы и шеи, кожной или внутриглазной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака толстой кишки, рака молочной железы, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, болезни Ходжкина, рака пищевода, рака тонкой кишки, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечника, саркомы мягкой ткани, рака уретры, рака полового члена, рака предстательной железы, хронического или острого лейкоза, лимфоцитарных лимфом, рака мочевого пузыря, рака почки или мочеточника, гипернефроидной опухоли почки, карциномы почечной лоханки, новообразований центральной нервной системы (ЦНС), первичной лимфомы ЦНС, опухолей оси позвоночника, глиомы ствола головного мозга, аденомы гипофиза и их комбинаций.
В еще одном варианте осуществления рак выбирают из группы, состоящей из немелкоклеточного рака легких (NSCLC), плоскоклеточной карциномы, гормон-рефрактерного рака предстательной железы, папиллярной гипернефроидной опухоли почки, колоректальной аденокарциномы, нейробластом, анапластической крупноклеточной лимфомы (ALCL) и рака желудочно-кишечного тракта.
Определения
Используемый здесь термин "аномальный клеточный рост", если не указано иначе, означает, что он не зависит от нормальных регуляторных механизмов (например, отсутствие контактного торможения).
Используемый здесь термин "практически чистая" в отношении конкретной полиморфной или аморфной формы означает, что полиморфная или аморфная форма включает менее чем 10%, предпочтительно, менее чем 5%, предпочтительно, менее чем 3%, предпочтительно, менее чем 1% по массе любой из других физических форм соединения.
Используемый здесь термин "лечение", если не указано иначе, означает обратное течение, облегчение, приостановление развития или предотвращение расстройства или состояния, для которых такой термин применяется, или одного или более симптомов такого расстройства или состояния. Используемый здесь термин "лечение", если не указано иначе, относится к акту "лечения", определенному только что выше.
Используемый здесь термин "практически такой же" относительно расположений пика рентгенограммы означает, что учитываются вариабельность типичного расположения пика и его интенсивности. Например, для специалиста в этой области является очевидным, что расположения пиков (2θ) будут характеризоваться некоторой вариабельностью, свойственной для рентгеновской установки, которая обычно составляет величину вплоть до 0,2°. Кроме того, для специалиста в этой области является очевидным, что относительные интенсивности пиков будут характеризоваться вариабельностью, свойственной для рентгеновской установки, так же как и вариабельностью, связанной со степенью кристалличности, предпочтительной ориентацией, поверхностью приготовленного образца и другими факторами, известными специалистам в этой области, которые следует учитывать только как качественные показатели.
Краткое описание чертежей
На фиг.1 приведена порошковая рентгенограмма кристаллической гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.2 приведена порошковая рентгенограмма кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.3 приведена порошковая рентгенограмма кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.4 приведена порошковая рентгенограмма кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.5 приведена порошковая рентгенограмма кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.6 приведена термогравиметрическая кривая дифференциальной сканирующей калориметрии (DSC) для кристаллической гидрохлоридной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
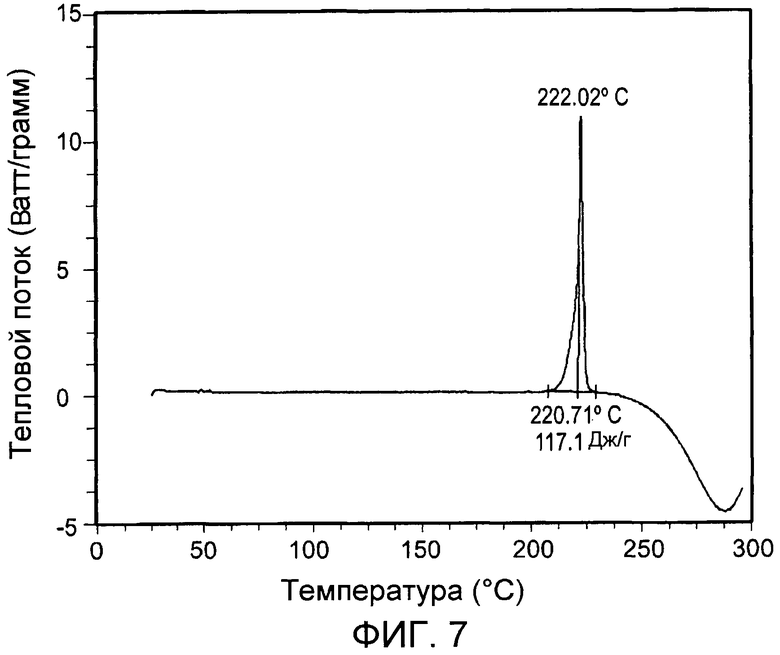
На фиг.7 приведена термогравиметрическая кривая дифференциальной сканирующей калориметрии (DSC) для кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.8 приведена термогравиметрическая кривая дифференциальной сканирующей калориметрии (DSC) для кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.9 приведена термогравиметрическая кривая дифференциальной сканирующей калориметрии (DSC) для кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
На фиг.10 приведена термогравиметрическая кривая дифференциальной сканирующей калориметрии (DSC) для кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола.
Подробное описание изобретения
Были получены несколько индивидуальных кристаллических солей 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Соединение 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанол в форме свободного основания может быть получено в соответствии со способами, описанными в патентном документе United States Patent Application No. 11/745921, содержание которого приводится здесь путем ссылки на него.
Соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло-[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола могут быть получены путем обработки соединения в форме свободного основания подходящим количеством выбранной минеральной или органической кислоты в среде водного растворителя или в среде подходящего органического растворителя, такого как метанол, ацетонитрил, этанол или этилацетат. Требуемую твердую соль получают при осторожном испарении растворителя. Требуемая соль кислоты может быть также осаждена из раствора свободного основания в органическом растворителе путем добавления к раствору соответствующей минеральной или органической кислоты.
Гидрохлоридная соль
HCl соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола может быть получена с хорошей кристалличностью, например, путем перемешивания соединения в форме свободного основания в любом подходящем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, с 2 M HCl при повышенной температуре (например, ~68°C), затем охлаждая до комнатной температуры. После охлаждения раствора осаждается в кристаллической форме образовавшаяся HCl соль, которая может быть выделена фильтрацией.
Порошковая рентгенограмма (PXRD) кристаллической HCl соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола приведена в таблице 1. Термогравиметрическая кривая DSC для HCl соли приведена на фиг.6.
Таблица 1: PXRD табличные данные для кристаллической полиморфной формы 1 гидрохлорида 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола (Пример 1)
Малеатная соль
Малеатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола может быть получена с хорошей кристалличностью, например, путем помещения малеиновой кислоты и 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола в пробирку и расстворения в любом подходящем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, затем добавления подходящего сорастворителя, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, и затем кристаллизации из любого подходящего растворителя, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь.
Порошковая рентгенограмма (PXRD) кристаллической малеатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола приведена в таблице 2. Термогравиметрическая кривая DSC для малеатной соли приведена на фиг.7.
Фосфатная соль
Фосфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола может быть получена с хорошей кристалличностью, например, путем перемешивания 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола с H3PO4 в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, затем перемешивания полученного твердого вещества в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, и затем кристаллизации из соответствующего растворителя, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь.
Порошковая рентгенограмма (PXRD) кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола приведена в таблице 3. Термогравиметрическая кривая DSC для фосфатной соли приведена на фиг.8.
Сульфатная соль
Сульфатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола может быть получена с хорошей кристалличностью, например, путем перемешивания 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола с H2SO4 в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, затем перемешивания полученного твердого вещества в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, и затем кристаллизации из соответствующего растворителя, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь.
Порошковая рентгенограмма (PXRD) кристаллической сульфатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола приведена в таблице 4. Термогравиметрическая кривая DSC для сульфатной соли приведена на фиг.9.
Тозилатная соль
Тозилатная соль 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола может быть получена с хорошей кристалличностью, например, путем перемешивания 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола с пара-толуолсульфоновой кислотой в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь, затем перемешивания полученного твердого вещества в соответствующем растворителе, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метил-трет-бутиловый эфир, метанол, этанол, воду, изопропиловый спирт или их смесь, и затем кристаллизации из соответствующего растворителя, включая, но этим не ограничиваясь, CH2Cl2, ацетон, ТГФ, ацетонитрил, этилацетат, метанол, этанол, воду, изопропиловый спирт или их смесь.
Порошковая рентгенограмма (PXRD) кристаллической тозилатной соли 2-[4-(3-хинолин-6-илметил-3H-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола приведена в таблице 5. Термогравиметрическая кривая DSC для тозилатной соли приведена на фиг.10.
Настоящее изобретение также относится к фармацевтическим композициям, включающим описанные здесь кристаллические полиморфные соли солей соединения 1. Фармацевтические композиции настоящего изобретения могут, например, находиться в форме, подходящей для перорального введения, в виде таблетки, капсулы, пилюли, порошка, составов с замедленным высвобождением, раствора, суспензии, для парентеральной инъекции в виде стерильного раствора, суспензии или эмульсии, для местного введения в виде мази или крема или для ректального введения в виде суппозитория. Фармацевтическая композиция может находиться в виде стандартных лекарственных форм, подходящих для однократного введения точных доз. Фармацевтическая композиция будет включать традиционный фармацевтический носитель или инертный наполнитель и соединение согласно изобретению в качестве активного ингредиента. Кроме того, могут быть включены другие лекарственные или фармацевтические вещества, носители, вспомогательные лекарственные вещества и так далее.
Примеры парентеральных форм введения включают растворы или суспензии активных соединений в стерильных водных растворах, например водных растворах пропиленгликоля или декстрозы. Такие лекарственные формы могут быть, если в этом есть необходимость, соответствующим образом забуферены.
Подходящие фармацевтические носители включают инертные разбавители или наполнители, воду и различные органические растворители. Фармацевтические композиции могут, если в этом есть необходимость, содержать дополнительные ингредиенты, такие как вещества, корригирующие вкус и запах лекарственного средства, связующие, вспомогательные вещества и другие подобные вещества. Таким образом, для перорального введения таблетки, содержащие различные вспомогательные вещества, такие как лимонная кислота, могут применяться вместе с различными разрыхляющими веществами, такими как крахмал, альгиновая кислота и определенные сложные силикаты, и со связующими, такими как сахароза, желатин и аравийская камедь. Кроме того, с целью облегчения процесса таблетирования часто применяют смазывающие вещества, такие как стеарат магния, лаурилсульфат натрия и тальк. Твердые композиции аналогичного типа могут также использоваться в мягких и твердых заполняемых желатиновых капсулах. Предпочтительные материалы включают лактозу или молочный сахар и высокомолекулярные полиэтиленгликоли. Когда для перорального введения требуются водные суспензии или эликсиры, активное соединение может быть объединено в них с различными подсластителями или ароматизаторами, окрашивающими веществами или красителями и, если в этом есть необходимость, эмульгаторами или суспендирующими агентами, вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин, или их комбинациями.
Способы получения различных фармацевтических композиций с конкретным количеством активного соединения являются известными, или они являются очевидными, для специалистов в этой области. Примеры можно найти в монографии Remington's Pharmaceutical Sciences. Mack Publishing Company, Easter, Pa., 15th Edition (1975).
ПРИМЕРЫ
Приводимые далее примеры и препараты дополнительно иллюстрируют и поясняют конкретные аспекты вариантов осуществления изобретения. Следует иметь в виду, что объем настоящего изобретения не ограничивается каким бы то ни было образом объемом следующих примеров.
Методы и материалы
Соли PF-04217903 характеризовали с помощью их порошковых рентгенограмм. Так, порошковые рентгенограммы солей снимали на порошковом рентгеновском дифрактометре марки Bruker D8 Discover с детектором GADDS (детекторная система для регистрации дифракции в полном угловом диапазоне) CS, работающем в режиме отражения при использовании Cu Ka излучения (1,54 Å). Напряжение и силу тока трубки устанавливали 40 кВ и 40 мА, соответственно. Сканы собирали при расстоянии между образцом и детектором, устанавливаемым на 15,0 см. Образцы сканировали в течение 60 секунд, покрывая диапазон от 4,5 до 38,7° в 2θ. Дифрактометр калибровали для положений пиков в 2θ с помощью корундового стандарта. Образцы перемещали в никелевых держателях для образцов, специально изготовленных фирмой Gasser & Sons, Inc (Commack, NY). Все анализы проводили при комнатной температуре, которая обычно составляет 20-30°C. Данные собирали и интегрировали при помощи программного продукта GADDS for WNT version 4.1.14T. Дифрактограммы обсчитывали с помощью программного продукта DiffracPlus, software release 2003, with Eva version 9.0.0.2.
Для снятия рентгенограмм на порошковом дифрактометре марки Bruker D8 Discover с детектором GADDS CS образец обычно помещают в углубление посередине никелевого держателя для образцов. Порошкообразный образец прижимают предметным стеклом или чем-либо подобным для обеспечения произвольной поверхности и соответствующей высоты образца. Держатель для образца затем помещают в прибор Bruker и снимают порошковую рентгенограмму при использовании указанных выше параметров прибора. Разница в измерениях, связанная с таким порошковым рентгеновским анализом, является следствием целого ряда факторов, включающих (a) ошибки при приготовлении образца (например, высоты образца), (b) ошибки прибора, (c) ошибки калибровки, (d) ошибки оператора (включающие ошибки, которые присутствуют при определении положений пика) и (e) природу материала (например, ошибки предпочтительной ориентации). Ошибки калибровки и ошибки высоты образца часто приводят к сдвигу всех пиков в одинаковом направлении. Небольшие различия в высоте образца при использовании плоского держателя могут приводить к большим смещениям положений пиков на порошковой рентгенограмме. Систематическое изучение показало, что различие в высоте образца в 1 мм может привести к сдвигам пика до 1° 2θ (Chen et al.; J Pharmaceutical and Biomedical Analysis, 2001; 26, 63). Эти сдвиги могут быть идентифицированы на дифрактограмме и могут быть устранены путем введения поправки для пика (применения систематического поправочного коэффициента для всех значений положения пиков) или путем повторной калибровки прибора. Как уже упоминалось выше, можно исправить различия в измерениях на различных приборах путем применения систематического поправочного коэффициента для приведения в соответствие положений пиков. Обычно этот поправочный коэффициент может приводить в соответствие положения измеренных пиков с ожидаемыми положениями пиков и может находиться в области ожидаемого 2θ значения ±0,2° 2θ. Значения углов (°2θ) и значения интенсивностей (в виде % от величины самого высокого пика) для каждой формы твердого вещества приведены в таблицах 1-6.
Дифференциальную сканирующую калориметрию (DSC) проводили на приборе марки DSC Q1000 V9.1 Build 296 фирмы TA Instruments. Прибор калибровали для определения постоянной ячейки и теплоемкости при помощи индия и сапфира, соответственно. Образцы готовили путем взвешивания 1-3 мг образца в алюминиевом тигле, который затем накрывали перфорированной алюминиевой крышкой (TA Instruments' part nos. 900786.901 (bottoms) and 900779.901 (top)). Данные анализировали с помощью программного продукта Universal Analysis 2000 for Windows 2000/XP version 4.3A, Build 4.3.0.6. Эксперименты начинали при температуре окружающей среды и нагревали образец со скоростью 10°C/мин до 350°C при продувке газообразным азотом (расход составлял 50 мл/мин). Характеристики термических явлений для каждой соли приведены в таблице 6.
(°C)
перехода
Пример 1: Получение HCl соли
29,5 мг соединения 1 взвешивали в стеклянном сцинтилляционном флаконе объемом 20 мл. Добавляли 1 мл MeOH и раствор перемешивали. Добавляли в раствор из пипетки 38,4 мкл 2 M HCl. Накрытый крышкой и перемешиваемый раствор нагревали до ~68°C в модуле нагреватель-перемешиватель. Нагреватель выключали и раствор продолжали перемешивать. Визуально наблюдали выпадение осадка при охлаждении раствора до ~48°C. Добавляли 500 мкл MeOH и раствор продолжали перемешивать в течение ночи. Твердое вещество выделяли с помощью фильтрации под вакуумом на мембранном фильтре из политетрафторэтилена (PTFE) с размером пор 0,45 мкм. Твердое вещество сушили в вакуум-сушильном шкафу при 60°C в течение ~30 минут.
Пример 2: Получение малеатной соли
6,95 мг малеиновой кислоты и 22,3 мг соединения 1 взвешивали в стеклянном сцинтилляционном флаконе объемом 20 мл. Добавляли ~2 мл ACN и 20 мкл воды. Флакон закрывали и осуществляли перемешивание в течение ~20 минут. Растворитель испаряли путем пропускания слабого потока N2. Добавляли ~3 мл EtOAc и 1 мл IPA и флакон с раствором накрывали крышкой и перемешивали в течение ночи. Твердое вещество извлекали из раствора с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном эксикаторе в течение ~30 минут. Твердое вещество помещали в стеклянный сцинтилляционный флакон объемом 20 мл. Добавляли ~2 мл ацетона и раствор накрывали крышкой и перемешивали при 50°C в течение ~1 часа. Твердое вещество извлекали из раствора с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном эксикаторе в течение ~30 минут.
Пример 3: Получение фосфатной соли
21,12 мг соединения 1 добавляли в стеклянный флакон для ВЭЖХ с завинчивающейся крышкой. С помощью пипетки добавляли во флакон 1 мл MeOH, закрывали его крышкой и осуществляли перемешивание. С помощью пипетки добавляли в раствор 28,357 мкл 2M H3PO4. Добавляли 500 мкл MeOH, закрывали флакон крышкой и осуществляли перемешивание при 60°C в течение ~2 часов. Нагревание прекращали и раствор продолжали перемешивать в течение ночи. Наблюдалось осаждение твердого вещества, и его извлекали из раствора с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном сушильном шкафу при 60°C в течение 30-60 минут. Твердое вещество помещали в стеклянный сцинтилляционный флакон объемом 20 мл и добавляли 5-15 мл IPA, затем флакон закрывали крышкой и осуществляли перемешивание в течение ночи. Твердое вещество отделяли с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм и сушили в вакуумном эксикаторе в течение ~30 минут. Твердое вещество помещали в стеклянный сцинтилляционный флакон объемом 20 мл. Добавляли ~10 мл ACN и флакон с раствором помещали в кожух и перемешивали незакрытым в течение ~48 часов. Твердое вещество извлекали из оставшегося раствора с помощью фильтрации под вакуумом на мембранном фильтре из нейлона с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном эксикаторе в течение ~30 минут.
Пример 4: Получение сульфатной соли
20,92 мг соединения 1 помещали в стеклянный флакон для ВЭЖХ с завинчивающейся крышкой. С помощью пипетки добавляли во флакон 1 мл MeOH, закрывали его крышкой и осуществляли перемешивание. С помощью пипетки добавляли в раствор 28,169 мкл 2 M H2SO4. Затем с помощью пипетки добавляли в раствор 500 мкл MeOH. Раствор нагревали до 60°C и перемешивали при этой температуре в течение ~2 часов. Нагревание прекращали и раствор продолжали перемешивать в течение ночи. Наблюдалось осаждение твердого вещества, и его извлекали из раствора с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном сушильном шкафу при 60°C в течение 30-60 минут. Твердое вещество помещали в стеклянный сцинтилляционный флакон объемом 20 мл. Добавляли 5-15 мл IPA, затем флакон с раствором закрывали крышкой и осуществляли перемешивание в течение ночи. Твердое вещество отделяли с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм и затем сушили в вакуумном эксикаторе в течение ~30 минут. Твердое вещество помещали в стеклянный сцинтилляционный флакон объемом 20 мл. Добавляли ~10 мл ACN и флакон с раствором закрывали крышкой и перемешивали в течение ночи. Твердое вещество извлекали с помощью фильтрации под вакуумом на мембранном фильтре из нейлона с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном эксикаторе в течение ~30 минут.
Пример 5: Получение тозилатной соли
23,79 мг соединения 1 помещали в стеклянный флакон для ВЭЖХ с завинчивающейся крышкой. Добавляли 1 мл MeOH, закрывали флакон с раствором крышкой и подвергали перемешиванию. Добавляли в раствор с помощью пипетки 31,912 мкл 2 M пара-толуолсульфоновой кислоты. Раствор перемешивали при 60°C в течение ~2 часов. Крышку флакона открывали и флакон помещали в поток N2 до тех пор, пока объем раствора не уменьшался до ~500 мкл. Добавляли аликвоты MTBE по 100 мкл до тех пор, пока не начиналось осаждение (суммарно добавляли 300 мкл). Флакон с раствором закрывали крышкой, перемешивали и нагревали до 45°C и затем нагревание прекращали. Продолжали перемешивать раствор в течение ночи. Раствор переносили в стеклянный сцинтилляционный флакон объемом 20 мл. Добавляли ~15 мл IPA и флакон с раствором закрывали крышкой и осуществляли перемешивание в течение ~72 часов. Раствор помещали в поток N2 до тех пор, пока не удалялся растворитель. Добавляли 5-10 мл ацетона. Наблюдалось образование светло-коричневого геля, который прилипал к стенкам стеклянного флакона. Раствор переносили в новый стеклянный сцинтилляционный флакон объемом 20 мл (коричневатая смола оставалась в старом флаконе). Добавляли ~5 мл ацетона и ~1 мл MeOH и раствор перемешивали в незакрытом флаконе в кожухе. Твердое вещество отделяли от раствора с помощью фильтрации под вакуумом на мембранном фильтре из PTFE с размером пор 0,45 мкм. Твердое вещество сушили в вакуумном эксикаторе в течение ~2 часов.
| название | год | авторы | номер документа |
|---|---|---|---|
| C-Анилинохиназолиновые соединения и их использование в лечении рака | 2018 |
|
RU2769694C2 |
| ИНГИБИРОВАНИЕ ЦИКЛИЧЕСКОГО AMP-ЧУВСТВИТЕЛЬНОГО ЭЛЕМЕНТ-СВЯЗЫВАЮЩЕГО БЕЛКА (CREB) | 2020 |
|
RU2831142C2 |
| КРИСТАЛЛИЧЕСКАЯ ТОЗИЛАТНАЯ СОЛЬ (8S,9R)-5-ФТОР-8-(4-ФТОРФЕНИЛ)-9-(1-МЕТИЛ-1Н-1,2,4-ТРИАЗОЛ-5-ИЛ)-8-9-ДИГИДРО-2Н-ПИРИДО[4,3,2-de]ФТАЛАЗИН-3(7Н)-ОНА | 2011 |
|
RU2598606C2 |
| ТОЗИЛАТНАЯ СОЛЬ ТРАНС-N-ИЗОБУТИЛ-3-ФТОР-3-[3-ФТОР-4-(ПИРРОЛИДИН-1-ИЛМЕТИЛ)ФЕНИЛ]ЦИКЛОБУТАНКАРБОКСАМИДА | 2008 |
|
RU2451016C2 |
| Новые производные имидазо[4,5-c] хинолинов и имидазо[4,5-c][1,5] нафтиридинов в качестве ингибиторов LRRK2 | 2016 |
|
RU2722149C1 |
| НЕГИГРОСКОПИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ МАЛЕАТНАЯ СОЛЬ 5-[(Z)-(5-ФТОР-2-ОКСО-1,2-ДИГИДРО-3H-ИНДОЛ-3-ИЛИДЕН)МЕТИЛ]-N-[(2S)-2-ГИДРОКСИ-3-МОРФОЛИН-4-ИЛПРОПИЛ]-2,4-ДИМЕТИЛ-1H-ПИРРОЛ-3-КАРБОКСАМИДА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ РАКА | 2004 |
|
RU2319702C2 |
| НОВАЯ КРИСТАЛЛИЧЕСКАЯ ФОРМА ТРИАЗОЛО (4,5-d) ПИРИМИДИНА | 2005 |
|
RU2418802C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ТРИАЗОЛОПИРАЗИНА И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2643361C2 |
| НОВАЯ КРИСТАЛЛИЧЕСКАЯ И АМОРФНАЯ ФОРМА ТРИАЗОЛО[4,5-d]ПИРИМИДИНА | 2001 |
|
RU2325391C2 |
| Новые производные имидазо[4,5-с]хинолина в качестве ингибиторов LRRK2 | 2018 |
|
RU2773516C2 |







Изобретение относится к полиморфу 2-[4-(3-хинолин-6-илметил-3Н-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, в частности к новой кристаллической фосфатной соли 2-[4-(3-хинолин-6-илметил-3Н-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола. Изобретение также относится к фармацевтической композиции, включающей данную соль, капсуле, включающей фармацевтическую композицию, и применению новой соли при лечении аномального клеточного роста, такого как рак, у млекопитающих. 4 н. и 6 з.п. ф-лы, 10 ил., 6 табл., 5 пр.
1. Кристаллическая фосфатная соль 2-[4-(3-хинолин-6-илметил-3Н-[1,2,3]триазоло[4,5-b]пиразин-5-ил)пиразол-1-ил]этанола, характеризующаяся порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2 и 20,9±0,2.
2. Кристаллическая соль по п.1, характеризующаяся порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2 и 24,8±0,2.
3. Кристаллическая соль по п.1, характеризующаяся порошковой рентгенограммой, включающей пики при следующих значениях угла (2θ): 17,0±0,2, 20,9±0,2, 24,8±0,2 и 25,8±0,2.
4. Фармацевтическая композиция, предназначенная для лечения аномального клеточного роста у млекопитающего, включающая соединение по п.1.
5. Капсула, включающая фармацевтическую композицию по п.4.
6. Применение кристаллической соли по п.1 для получения лекарственного средства, используемого для лечения аномального клеточного роста у млекопитающего, который нуждается в таком лечении.
7. Применение по п.6, где аномальный клеточный рост опосредуется, по меньшей мере, одной генетически измененной тирозинкиназой.
8. Применение по п.6, где аномальным клеточным ростом является рак.
9. Применение по п.8, где рак выбирают из рака легких, рака кости, рака поджелудочной железы, рака кожи, рака головы и шеи, кожной или или внутриглазной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака толстой кишки, рака молочной железы, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, болезни Ходжкина, рака пищевода, рака тонкой кишки, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечника, саркомы мягкой ткани, рака уретры, рака полового члена, рака предстательной железы, хронического или острого лейкоза, лимфоцитарных лимфом, рака мочевого пузыря, рака почки или мочеточника, гипернефроидной опухоли почки, карциномы почечной лоханки, новообразований центральной нервной системы (ЦНС), первичной лимфомы ЦНС, опухолей оси позвоночника, глиомы ствола головного мозга, аденомы гипофиза и их комбинаций.
10. Применение по п.8, где рак выбирают из группы, состоящей из немелкоклеточного рака легких (NSCLC), плоскоклеточной карциномы, гормон-рефрактерного рака предстательной железы, папиллярной гипернефроидной опухоли почки, колоректальной аденокарциномы, нейробластом, анапластической крупноклеточной лимфомы (ALCL) и рака желудочно-кишечного тракта.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2012-03-27—Публикация
2008-11-18—Подача