Предпосылки создания изобретения
Паклитаксел (доступный на рынке как инъекционный препарат Таксол®) является прототипом химиотерапевтических таксанов, которые связываются с β-тубулином, способствует сборке этого белка в микротрубочки и стабилизирует их, в конечном счете, вызывая гибель клетки. Паклитаксел полиглумекс (PPX, химическое название N-(L-пироглутамил)-[поли(L-глутамил)]-L-глутаминовая кислота, частично γ-этерифицированная (2'R,3'S)-3'-бензоиламидо-1'-[[4,10β-бис(ацетокси)-2α-(бензоилокси)-1,7β-дигидрокси-9-оксо-5,20-эпокситакс-11-ен-13α-ил]окси]-1′-оксо-3'-фенилпропан-2'-олом), затем названный PPX, является конъюгатом сложного эфира α-поли-L-глутаминовой кислоты (ПГК) и паклитаксела, причем последний ковалентно связан с ПГК через 2'-гидрокси-положение.
PPX в настоящее время находится на изучении в отношении использования при немелкоклеточном раке легких (НМКРЛ; NSCLC) и раке яичников. Паклитаксел высвобождается после всасывания и протеолитического/гидролитического разложения конъюгата в опухолевой ткани.
Молекулярная формула и молекулярная масса PPX представлены распределениями, так как степень полимеризации α-поли-L-глутаминовой кислоты и число сайтов конъюгации с паклитакселом варьируют в соответствии с процессом производства. Средняя молекулярная масса PPX составляет примерно 40000 Дальтон, при определении неводной гельпроникающей хроматографией с обнаружением по многоугловому рассеянию лазерного излучения. Примерно 35% массы паклитаксела представлено в виде конъюгата в связанной форме, что означает примерно одну сложноэфирную связь паклитаксела на 11 мономерных звеньев. Способы синтеза PPX описаны в публикации РСТ WO 97/33552.
Среди производственных испытаний, которые нужно было выполнить по PPX, как по активному ингредиенту, так и по конечному фармацевтическому продукту, предписаны исследования на количественное содержание конъюгированного паклитаксела и связанных с таксаном примесей. Однако последнее исследование нельзя провести на PPX как таковом, и необходима деэтерификация для высвобождения паклитаксела. В Tetrahedron Letters (1995), 36(12), 2001-2004 описана методика гидролитического расщепления различных сложных эфиров паклитаксела с использованием щелочных смесей перекиси водорода/тетрагидрофурана, причем 2'-ацетат перацетилированного паклитаксела гидролизуется быстрее, чем 10-ацетил-положение. Когда этот способ применяется в отношении паклитаксела, регистрируемым продуктом является 10-дезацетилпаклитаксел (10-ДАТ). Известная процедура, первоначально использованная для количественной оценки конъюгированного паклитаксела и относящихся к таксану примесей в PPX, включает полный водный гидролиз PPX бикарбонатом натрия/пероксидом с сопутствующим экстрагированием паклитаксела и связанных с таксаном примесей в CHCl3 и количественную оценку с помощью ВЭЖХ. Добавление CHCl3 в качестве второй фазы дает возможность экстрагирования высвобожденных таксанов сразу после гидролиза, предотвращая образование большей части 10-ДАТ. Реакция гидролиза, однако, вызывает значительное разложение паклитаксела, главным образом до 10-дезацетилпаклитаксела (10-ДАТ), и 20% уровни 10-ДАТ были обычными при использовании этого метода, так как бифазная система не полностью подавляла гидролиз в 10-м положении. В результате количественно оценивали вместе пики как паклитаксела, так и 10-ДАТ и регистрировали как паклитаксел+10-ДАТ. Чтобы была возможность корректировать количество паклитаксела+10-ДАТ, полученное по методу гидролиза, только по паклитакселу в целом, необходимо осуществлять второй способ с использованием количественного ЯМР для определения количества собственно конъюгированного 10-ДАТ. Таким образом, образование продуктов разложения и изменение кривой конъюгированного таксана является явным недостатком этой процедуры. Кроме того, условия хроматографии не являются специфическими для соединения после разложения.
Поэтому существует потребность в улучшенном способе количественной оценки конъюгированного с ПГК паклитаксела и других конъюгированных с ПГК таксанов.
Подробное описание изобретения
Соответственно, данное изобретение относится к способу определения количества конъюгированного таксана в конъюгатах ПГК-таксан, который включает гидролиз конъюгата в неводной среде с использованием гидразинового производного вместо гидроперокси аниона.
Более подробно, способ данного изобретения включает реакцию конъюгата ПГК-таксан с соединением формулы (I):
R1R2N-NH2, (I)
где R1 и R2 независимо выбраны из С1-С10-алкила, С1-С10-гидроксиалкила, С3-С10-алкенила, С3-С10-гидроксиалкенила, С3-С10-алкинила, С3-С10-гидроксиалкинила, арила, гетероарила; или R1 и R2 вместе с атомом азота, с которым они связаны, образуют 3-8-членное гетероциклическое кольцо, необязательно содержащее до трех гетероатомов, выбранных из O, S и N, и необязательно замещенное не более чем двумя гидроксильными группами;
с получением несвязанных таксанов и ПГК-гидразида с последующим определением несвязанного таксана.
В объеме данного изобретения конъюгат ПГК-таксан является α-поли-L-глутаминовой кислотой (ПГК), причем одна или более из γ-карбоксильных групп повторяющихся элементов глутаминовой кислоты этерифицированы молекулой таксана через 2′-гидроксильную группу последнего. Обычно ПГК содержит от 60 до 310 элементов мономера и имеет молекулярную массу в интервале от 8000 до 40000 Дальтон. ПГК-гидразид является гидразидом, получающимся в результате реакции сложноэфирных групп, связывающих 2′-гидроксильные группы таксана с γ-карбоксильными группами повторяющихся звеньев глутаминовой кислоты ПГК в конъюгате ПГК-таксан с гидразином формулы (I). В ПГК-гидразиде азот первичной аминогруппы соединения формулы (I) связан с карбонилом γ-карбоксильной группы повторяющегося звена глутаминовой кислоты ПГК.
В соответствии с описанием «таксан» означает паклитаксел, доцетаксел или другие таксаны, которые могут быть выделены из природных источников, таких как тис, или из клеточной культуры или получены химическим синтезом, такие как 10-дезацетилпаклитаксел, 7-эпипаклитаксел, цефаломаннин, 7-эпицефаломаннин и N-дебензоил-N-фенилацетилпаклитаксел. Наиболее предпочтительным таксаном является паклитаксел.
В соответствии с описанием термин «С1-С10-алкил» относится к насыщенной углеводородной группе с прямой или разветвленной цепью, содержащей от 1 до 10 атомов углерода, такой как метил, этил, пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, вторичный бутил, трет-бутил), пентил (например, н-пентил, изопентил, неопентил) и тому подобное.
В соответствии с описанием термин «С1-С10-гидроксиалкил» относится к С1-С10-алкильной группе, которая может быть замещена гидроксильными группами числом до трех.
В соответствии с описанием термин «С3-С10-алкенил» относится к алкильной группе, которая содержит от 3 до 10 атомов углерода и имеющей одну углерод-углеродную двойную связь или более таких связей. Примеры алкенильных групп включают этенил, пропенил, бутенил, пентенил, гексенил, бутадиенил, пентадиенил, гексадиенил и тому подобное.
В соответствии с описанием термин «С3-С10-гидроксиалкенил» относится к С3-С10-алкенильной группе, которая может быть замещенной гидроксильными группами, числом до трех, у атомов углерода, не участвующих в углерод-углеродных двойных связях.
В соответствии с описанием «С3-С10-алкинил» относится к алкильной группе, содержащей от 3 до примерно 10 атомов углерода и имеющей одну или более тройных углерод-углеродных связей. Примеры алкинильных групп включают этинил, пропинил, бутинил, пентинил и тому подобное.
В соответствии с описанием термин «С3-С10-гидроксиалкинил» относится к С3-С10-алкинильной группе, которая может быть замещенной гидроксильными группами, числом до трех, у атомов углерода, не участвующих в углерод-углеродных тройных связях.
В соответствии с описанием термин «С1-С3-алкил» относится к прямой или разветвленной насыщенной углеводородной группе, содержащей от 1 атома углерода до 3.
В соответствии с описанием термин «С1-С3-галогеналкил» относится к С1-С3-алкильной группе, замещенной атомами галогена (т.е. F, Cl, Br, I) числом до трех.
В соответствии с описанием термин «С1-С3-алкокси» относится к О-С1-С3-алкильным группам, таким как метокси, этокси, н-пропокси и изопропокси.
В соответствии с описанием термин «С1-С3-тиоалкокси» относится к S-С1-С3-алкильным группам, т.е. метилтио, этилтио, н-пропилтио и изопропилтио.
В соответствии с описанием «арил» относится к ароматическим карбоксильным группам, включая моноциклические или полициклические ароматические углеводороды, такие как фенил, нафтил, антраценил, фенантренил, инданил, инденил и тому подобное, которые могут быть необязательно замещенными галогеном, С1-С3-алкилом, С1-С3-галогеналкилом, С1-С3-алкокси, С1-С3-тиоалкокси или нитрогруппами.
В соответствии с описанием «гетероарильными» группами являются ароматические гетерокарбоциклильные группы, и они включают моноциклические и полициклические ароматические углеводороды, содержащие, по меньшей мере, один гетероатом в кольце, такой как атом серы, кислорода или азота, и которые, необязательно, могут быть замещенными галогеном, С1-С3-алкильными, С1-С3-галогеналкильными, С1-С3-алкокси, С1-С3-тиоалкокси или нитрогруппами. Гетероарильные группы включают пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил, имидазолил, тиазолил, индолил, пирролил, оксазолил, бензофурил, бензотиенил, бензтиазолил, изоксазолил, пиразолил, триазолил, татразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил, пуринил, карбазолил, бензимидазолил и тому подобное.
Примеры соединений формулы (I), которые можно преимущественно использовать для осуществления данного изобретения, включают N,N-диметилгидразин, фенилгидразин, 4-бромфенилгидразин, 4-изопропилфенилгидразин, 4-метоксифенилгидразин, 1-метил-1-фенилгидразин, 1-аминопирролидин, 1-амино-2,6-диметилпиперидин, 1-амино-цис-2,6-диметилпиперидин, (S)-(-)-1-амино-2-(метоксиметил)пирролидин, (R)-(+)-1-амино-2-(метоксиметил)пирролидин, 4-аминоморфолин, 1-аминопиперидин, 1-амино-4-метилпиперазин, 1-амино-4-(2-гидроксиэтил)пиперазин, 1-аминогомопиперидин. Предпочтительными реагентами являются N,N-диметилгидразин, фенилгидразин, 4-аминоморфолин и 1-аминопиперидин, причем наиболее предпочтительным является 4-аминоморфолин.
Реакцию между конъюгатом ПГК-таксан и (I) осуществляют в апротонном органическом растворителе, таком как диметилформамид, диметилсульфоксид, N-метилпирролидинон и тому подобное. В соответствии с предпочтительным воплощением данного изобретения образец PPX или содержащего PPX лекарственного средства растворяют или суспендируют в диметилформамиде или диметилсульфоксиде с получением концентрации PPX от 25 до 52 мг/мл, затем добавляют 4-аминоморфолин или раствор 4-аминоморфолина в трифторуксусной кислоте. Соотношение между раствором PPX и 4-аминоморфолин/трифторуксусной кислотой составляет от 1:0,3 о/о до 1:0,5 о/о. Смесь перемешивают при температуре от примерно 20°С до примерно 42°С в течение срока в интервале от примерно 2 часов до примерно 24 часов.
Определение несвязанного таксана осуществляют с помощью ВЭЖХ или любыми другими методами, известными специалистам в отношении количественного анализа таксанов.
В соответствии с предпочтительным воплощением данного изобретения образец PPX или содержащего PPX лекарственного средства растворяют в диметилсульфоксиде с получением концентрации PPX от 48 до 52 нг/мл, и добавляют раствор 4-аминоморфолина в трифторуксусной кислоте, причем соотношение трифторуксусной кислоты к 4-аминоморфолину составляет 0,017:1 о/о. Отношение раствора PPX к 4-аминоморфолин/трифторуксусной кислоте составляет 1:0,5 о/о. Смесь перемешивают и температуру и время реакции регулируют до примерно тех пор, когда выделяется примерно 2-7% конъюгированного таксана. Предпочтительно, температуру поддерживают в интервале примерно 38-42°С, и время реакции находится в интервале от примерно 1,9 до примерно 2,1 часа. В этих интервалах характеристики чистоты не изменяются как функция превращения. После добавления ацетонитрила раствор подвергают ультрафильтрации путем центрифугирования для удаления непрореагировавшего полимера, а затем непосредственно вводят шприцем в колонку для ВЭЖХ с определением процентной площади паклитаксела и примеси каждого из таксанов. Показатели УФ реакции, указанные в USP или вычисленные, применяют для превращения % площади известных примесей в массовых % по отношению к паклитакселу; количество других неизвестных примесей вместо этого вычисляют в виде % площади. Чистоту паклитаксела рассчитывают путем вычитания суммы всех примесей из 100%.
Мягкие условия реакции по методу данного изобретения снижают степень разложения паклитаксела с примерно 20% до менее 0,5% и дают возможность количественной оценки 10-ДАТ выше 0,2%, устраняя тем самым необходимость количественной оценки с помощью ЯМР.
Данное изобретение теперь будет проиллюстрировано более детально с помощью следующих далее примеров.
ПРИМЕРЫ
Чтобы продемонстрировать точность и чувствительность способа данного изобретения, паклитаксел вводили с помощью шприца в известные количества (10 мас.%) трех химически разных таксанов, а затем конъюгировали с α-поли-(L)-глутаминовой кислотой в количестве 37 мас.%. Два из трех таксанов были примесями от синтеза (цефаломаннин и 7-эпицефаломаннин), третий был примесью от разложения (7-эпипаклитаксел). Исследования проводили при трех разных уровнях введения (1,2%, 9,8%, 28 мас.%) для каждого таксана в интервале предела количественного определения и верхнего предела спецификации. Все три примеси были обнаружены в количестве между 100% и 115%, что считается приемлемым для предназначенного применения данного метода. Типичный пример этого эксперимента представлен в примере 1. Обычный анализ партии с выделением PPX представлен в примере 2.
Пример 1
Раствор конъюгата паклитаксела/7-эпипаклитаксела готовили путем аккуратного отвешивания 350±5 мг конъюгата в 10 мл колбу и растворения в диметилсульфоксиде. Раствор доводили до объема тем же растворителем. Аккуратно отвешивали 250±2,5 мг PPX (фармацевтической степени чистоты) в 5 мл колбу. В ту же колбу добавляли 0,085 мл раствора вводимого раствора (соответствующего уровню введения 1,2 мас.%) и доводили до объема диметилсульфоксидом. Затем выполняли реакцию аминолизиса по общей методике, представленной в примере 2, и анализировали с помощью ВЭЖХ. Выход продукта эпипаклитаксела составил 110,7%.
Пример 2
250 мг PPX (активный фармацевтический ингредиент) аккуратно взвешивали и переносили в 5 мл колбу. После растворения в диметилсульфоксиде образец доводили до объема тем же растворителем. 1,0 мл этого раствора переносили в 5 мл сосуд с коническим дном. В каждый сосуд помещали трехгранный стерженек магнитной мешалки и добавляли 0,5 мл раствора, содержащего трифторуксусную кислоту и 4-аминоморфолин в соотношении 0,017:1 (0,034 мл ТФА добавляли к 2 мл 4-аминоморфолина). Сосуд плотно закрывали пробкой, помещали на термостатированную водяную с перемешиванием баню при 40°С±2°С и перемешивали в течение 2±0,1 часа. В конце реакции сосуду давали медленно остыть до комнатной температуры за примерно 10 минут перед добавлением 0,75 мл ацетонитрила. После перемешивания образец переносили на центрифужные фильтры (граница пропускания по молекулярной массе = 10000 дальтон) и центрифугировали в течение 1 часа при 3000×g. 1 мл образца переносили в сосуд для ВЭЖХ, добавляли 10 мкл ледяной уксусной кислоты и анализировали с помощью ВЭЖХ для определения содержания таксана с использованием колонки Zorbax 300SB-C8, 4,6×100 мм, 3,5 мкм, Agilent Cat. № 861973-906, поддерживаемой при 40°С, и элюированием смесью с градиентом воды/ацетонитрила от 20% ацетонитрила/80% воды до 90% ацетонитрила/10% воды через 60 минут при УФ детекции при 227 нм.
Результаты (среднее по 6 повторам и выраженное в виде % площади, скорректированного по относительному коэффициенту чувствительности детектора (RRF; ОКЧД)) представлены в таблице 1.
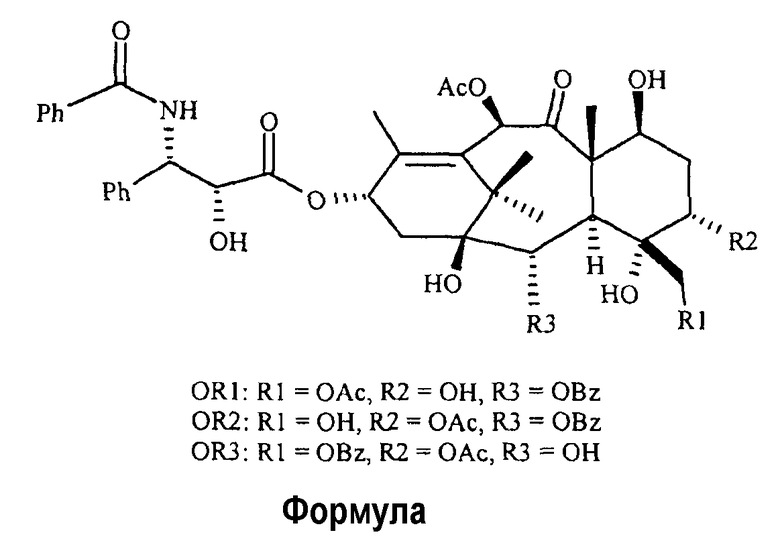
Примеси, показанные как OR1, OR2 и OR3, являются конъюгатами α-поли-(L)-глутаминовой кислотой и таксанов, имеющих следующую формулу:
| название | год | авторы | номер документа |
|---|---|---|---|
| ТАКСАНЫ, КОВАЛЕНТНО СВЯЗАННЫЕ С ГИАЛУРОНОВОЙ КИСЛОТОЙ ИЛИ ПРОИЗВОДНЫМИ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2003 |
|
RU2384593C2 |
| КОНЪЮГАТЫ ПОЛИГЛУТАМАТ-АМИНОКИСЛОТА И СПОСОБЫ | 2006 |
|
RU2472812C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ТАКСАНА, ТВЕРДАЯ КОМПОЗИЦИЯ ТАКСАНА, СПОСОБ ПОЛУЧЕНИЯ ТВЕРДОЙ КОМПОЗИЦИИ ТАКСАНА, КОМПОЗИЦИЯ ДЛЯ СОЛЮБИЛИЗАЦИИ УКАЗАННОЙ ТВЕРДОЙ КОМПОЗИЦИИ ТАКСАНА И КОМПЛЕКТ ЭЛЕМЕНТОВ (НАБОР) ДЛЯ СОСТАВА ТАКСАНА ДЛЯ ИНЪЕКЦИЙ | 2007 |
|
RU2429837C2 |
| МИЦЕЛЛЯРНАЯ КОМПОЗИЦИЯ АМФИФИЛЬНОГО БЛОК-СОПОЛИМЕРА, СОДЕРЖАЩАЯ ТАКСАН, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2449785C2 |
| ТАКСАНЫ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБЫ ИНГИБИРОВАНИЯ | 2001 |
|
RU2265019C2 |
| ПОЛИМЕРНЫЙ КОНЪЮГАТ ГЕКСАКООРДИНИРОВАННОГО КОМПЛЕКСА ПЛАТИНЫ | 2016 |
|
RU2715048C2 |
| ПОЛИМЕРНЫЙ КОНЪЮГАТ КООРДИНАЦИОННОГО КОМПЛЕКСА ПЛАТИНЫ (II) С ПРОИЗВОДНЫМ СУЛЬФОКСИДА | 2016 |
|
RU2721725C2 |
| С-4 КАРБОНАТСОДЕРЖАЩИЕ ТАКСАНЫ | 2000 |
|
RU2243223C2 |
| БЛОК-СОПОЛИМЕРНЫЙ КОНЪЮГАТ ФИЗИОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА | 2016 |
|
RU2732612C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ПРИЕМА, СОДЕРЖАЩАЯ ТАКСАН | 2015 |
|
RU2683326C2 |
Изобретение относится к медицине и описывает способ определения количества конъюгированного таксана в конъюгате полиглутаминовая кислота-таксан, где одна или более молекул таксана связаны через 2'-гидрокси-положение с γ-карбоксильной группой α-поли-L-глутаминовой кислоты, включающий стадии: а) взаимодействия конъюгата полиглутаминовая кислота-таксан с соединением формулы R1R2N-NH2 (I) с получением несвязанного таксана и гидразида полиглутаминовой кислоты и b) определения количества несвязанного таксана. Данное изобретение обеспечивает улучшенный способ определения количества конъюгированного таксана. 8 з.п. ф-лы, 2 пр., 1 табл.
1. Способ определения количества конъюгированного таксана в конъюгате полиглутаминовая кислота-таксан, где одна или более молекул таксана связаны через 2'-гидроксиположение с γ-карбоксильной группой α-поли-L-глутаминовой кислоты,
включающий стадии:
a) взаимодействия конъюгата полиглутаминовая кислота-таксан с соединением формулы (I):

где R1 и R2 независимо представляют С1-С10-алкил, C1-С10-гидроксиалкил, С3-С10-алкенил, С3-С10-гидроксиалкенил, С3-С10-алкинил, С3-С10-гидроксиалкинил, арил, гетероарил; или R1 и R2 вместе с атомом азота, с которым они связаны, образуют 3-8-членное гетероциклическое кольцо, необязательно содержащее до трех гетероатомов, выбранных из О, S и N, и необязательно замещенное не более чем двумя гидроксильными группами;
с получением несвязанного таксана и гидразида полиглутаминовой кислоты; и
b) определения количества несвязанного таксана.
2. Способ по п.1, где количество несвязанного таксана определяют с помощью ВЭЖХ.
3. Способ по п.1 или 2, где таксан выбран из паклитаксела, доцетаксела, 10-дезацетилпаклитаксела, 7-эпипаклитаксела, цефаломаннина, 7-эпицефаломаннина и N-дебензоил-N-фенилацетилпаклитаксела.
4. Способ по п.1, где таксан является паклитакселом.
5. Способ по п.1, где соединение формулы (I) выбрано из N,N-диметилгидразина, фенилгидразина, 4-бромфенилгидразина, 4-изопропилфенилгидразина, 4-метоксифенилгидразина, 1-метил-1-фенилгидразина, 1-аминопирролидина, 1-амино-2,6-диметилпиперидина, 1-амино-цис-2,6-диметилпиперидина, (S)-(-)-1-амино-2-(метоксиметил)пирролидина, (R)-(+)-1-амино-2-(метоксиметил)пирролидина, 4-аминоморфолина, 1-аминопиперидина, 1-амино-4-метилпиперазина, 1-амино-4-(2-гидроксиэтил)пиперазина и 1-аминогомопиперидина.
6. Способ по п.5, где соединение формулы (I) выбрано из N,N-диметилгидразина, фенилгидразина, 4-аминоморфолина и 1-аминопиперидина.
7. Способ по п.6, где соединением формулы (I) является 4-аминоморфолин.
8. Способ по п.7, где стадию а) осуществляют в диметилформамиде или диметилсульфоксиде при температуре в интервале от 20 до 42°С.
9. Способ по п.8, где стадию а) осуществляют в диметилсульфоксиде при температуре от 38 до 42°С.
| Jack W Singer et al | |||
| Машина для удаления мякоти с растений с волокнистыми листьями | 1925 |
|
SU2103A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| WO 9733552 A1, 18.09.1997 | |||
| US 6281368 B1, 28.08.2001. | |||
Авторы
Даты
2012-04-10—Публикация
2008-03-05—Подача