Изобретение относится к области медицины, а именно к композициям на основе цитокинов для профилактики и лечения вирусных заболеваний.
Цитокины - это низкомолекулярные белки, вырабатываемые преимущественно активированными клетками иммунной системы, которые являются медиаторами межклеточных коммуникаций при иммунном ответе, гемопоэзе, воспалении, а также межсистемных взаимодействиях. Обладая широким спектром биологической активности, они определяют не только адекватный уровень иммунореактивности, но и регулируют взаимодействия главных биологических интегративных систем организма: нервной, иммунной и эндокринной. С использованием методов генной инженерии многие цитокины в настоящее время получают в виде рекомбинантных препаратов, полностью идентичных эндогенным молекулам, а количества выделяемых цитокинов достаточны для их клинического применения.
В настоящее время терапия рекомбинантными цитокинами и препаратами на их основе является одним из наиболее перспективных и постоянно расширяющихся направлений фармакологии (Ройт А. Основы иммунологии. - М.: Мир, 1991. 328 с.; Кетлинский С.А., Симбирцев А.С, Воробьев А. А. Эндогенные иммуномодуляторы. - СПб: Гиппократ, 1992. 256 с.; Фрейдлин И.С. Система мононуклеарных фагоцитов. - М.: Медицина, 1984. 272 с.).
Наиболее известными представителями цитокинов являются препараты интерферона и интерлейкинов, используемые в основном для лечения вирусных и иммунных заболеваний в самых различных лекарственных формах (Регистр лекарственных средств России, 2001, М.). Так, известны противовирусные средства, содержащие альфа-, или бета-, или гамма-рекомбинантный интерферон, для профилактики и лечения вирусных заболеваний (RU 2073522, 1997 г.), офтальмологические капли «Локферон» на основе интерферона показаны для лечения целого ряда инфекционно-воспалительных заболеваний глаз, суппозитории «Виферон», «Свеферон» - при урогенитальных заболеваниях вирусной и бактериальной природы, вирусных гепатитов и т.д.
В последнее время широкое применение получили препараты, в состав активного начала которых наряду с цитокинами входят и другие биологически активные компоненты. В частности, лекарственное средство «Интерлизин» (RU 2188665, 2002), содержит раствор лейкоцитарного интерферона и лизоцима. Известны препараты, содержащие интерферон и полиглюкин (RU 2292907, 2006), интерферон и альфа-токоферола ацетат (RU 2057544, 1996).
Наиболее близким по технической сущности и достигаемому результату к заявляемому изобретению является композиция, содержащая смесь интерферона с белками, входящими в состав крови человека, - иммуноглобулинами (применяется смесь IGA, IGМ и IGG, может содержать фармацевтически приемлемые наполнители и представлять собой таблетки, капсулы, сироп и др. лекарственные формы. Препарат растворим в воде при рН около 7,4 и включает 50-500000 ME интерферона на 1 мг иммуноглобулинов (RU 2073522, 1997).
Недостатком указанного, а также иных препаратов, содержащих цитокины, является их недостаточная эффективность и зависимость результатов от особенностей заболевания.
Задачей, решаемой авторами, являлось расширения круга лекарственных средств, обладающих, в частности, воздействием на течение вирусных заболеваний путем создания новой композиции, содержащей цитокины с иными белками сыворотки крови человека.
Было найдено, что технический результат может быть достигнут в результате использования композиции, содержащей цитокин и альфа-фетопротеин (АФП). В качестве цитокинов могут быть использованы, в частности, промышленно выпускаемые препараты, содержащие интерфероны или интерлейкины и вспомогательные вещества, антагонисты рецептора интерлейкина и иные подобные белки. В зависимости от состава композиции содержание в ней альфа-фетопротеина может варьироваться от 0.001 (в случае использования с препаратом АРИЛ) до 99% мас. (при использовании в смеси с препаратом БЕТАЛЕЙКИН).
АФП - представляет собой фетальный гликопротеин с молекулярной массой около 70000 Д. АФП в большом количестве продуцируются клетками печени и брюшной стенки плода. Сырьем для получения АФП служит абортивная, пуповинная и плацентарная кровь, получаемая при медицинских абортах от клинически здоровых женщин, прошедших стандартное обследование. Получаемый материал обязательно тестируется на отсутствие антител к вирусу иммунодефицита человека (ВИЧ) и на отсутствие вируса гепатита В и антител к вирусу гепатита С. Водные растворы АФП нестабильны в процессе хранения, поэтому препарат АФП представляет собой лиофилизат с соответствующими добавками. В настоящее время альфа-фетопротеин (АФП) используют парентерально в онкологии для транспортировки лекарственного средства в зону опухоли (RU 2095084, 1996; RU 2139083, 1998; RU 2097060, 1997; RU 2163139, 2000; RU 2319479, 2005).
Проведенные испытания показали, что заявляемая композиция обладает повышенной эффективностью и может быть рекомендована для лечения широкого круга вирусных заболеваний, в том числе осложненных нарушениями иммунной системы организма. Композицию получают, как правило, простым смешением компонентов в заданных количествах. Наряду с применением такой смеси в ряде случаев возможно введение ее ингредиентов в организм раздельно для образования композиции непосредственно в организме в области их введения.
О влиянии АФП на антивирусную активность цитокинов в просмотренной литературе информации не обнаружено - данное свойство АФП установлено авторами впервые.
Полученные результаты иллюстрируются следующими графическими материалами:
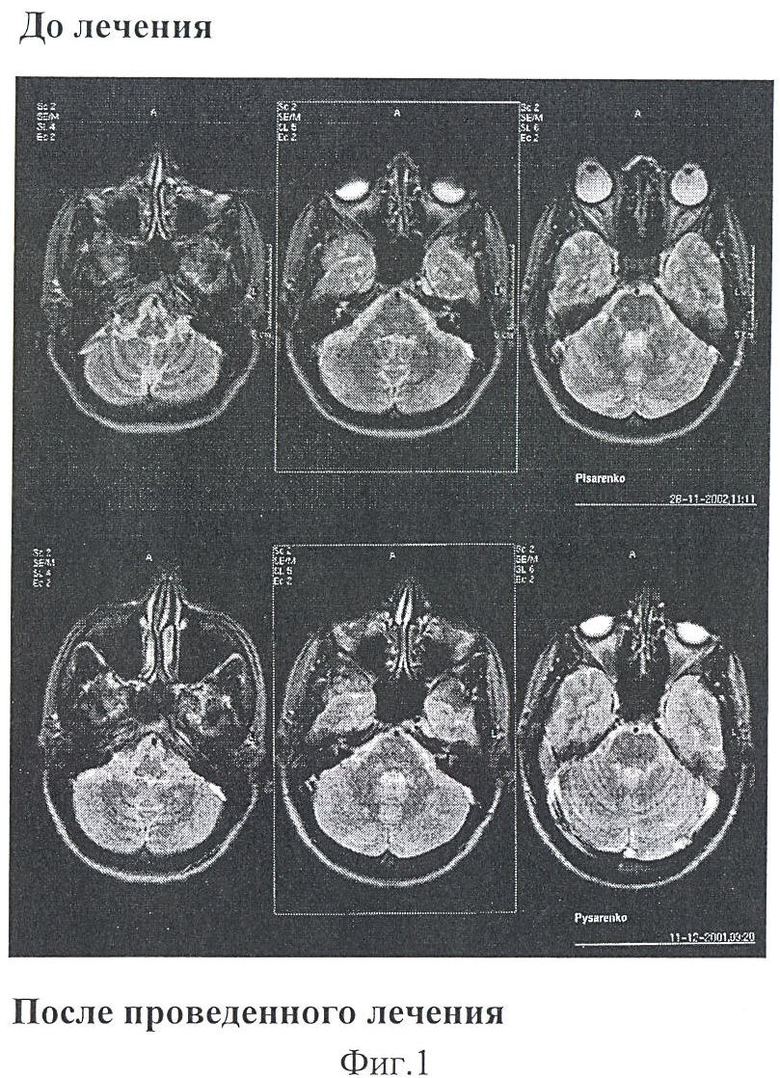
На фиг.1 приведены данные о изменении ЯМРТ при лечении инфекционного процесса, вызванного вирусом Эпштейна-Барра комбинированным препаратом альфа-фетопротеина+интерферон-альфа-2 (пример 3).
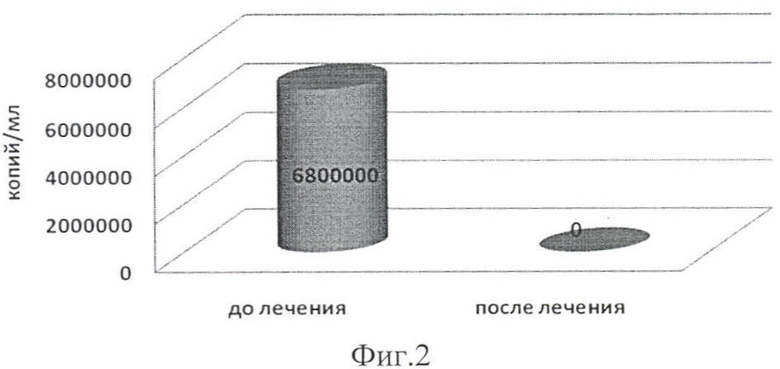
На фиг.2 приведены данные о изменении вирусной нагрузки при лечении хронического вирусного гепатита С, генотип 3а комбинированным препаратом α-фетопротеина и α-интерферон-2 (пример 4).
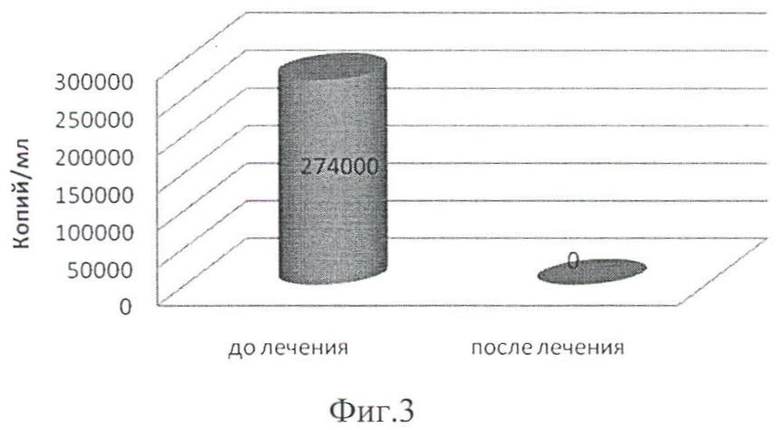
На фиг.3 приведены данные о изменении вирусной нагрузки при лечении хронического вирусного гепатита С, генотип 2а комбинированным препаратом α-фетопротеина+интерлейкин-1 бета (пример 5).
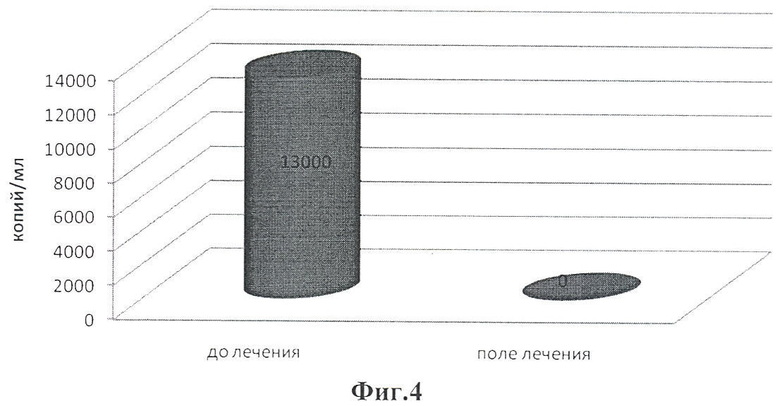
На фиг.4 приведены данные о изменении вирусной нагрузки при лечении хронического вирусного гепатита С, генотип 1в комбинированным препаратом α-фетопротеина+α-интерферон (пример 7).
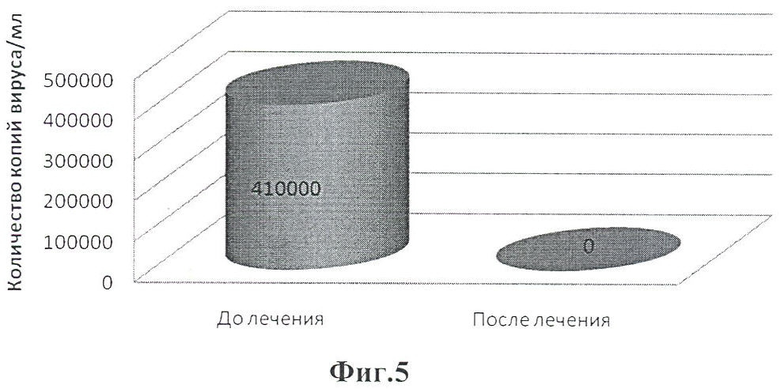
На фиг.5 приведены данные о изменении показателей ПЦР при лечении хронического вирусного гепатита В комбинированным препаратом α-фетопротеина+α-интерферон-2 (пример 8).
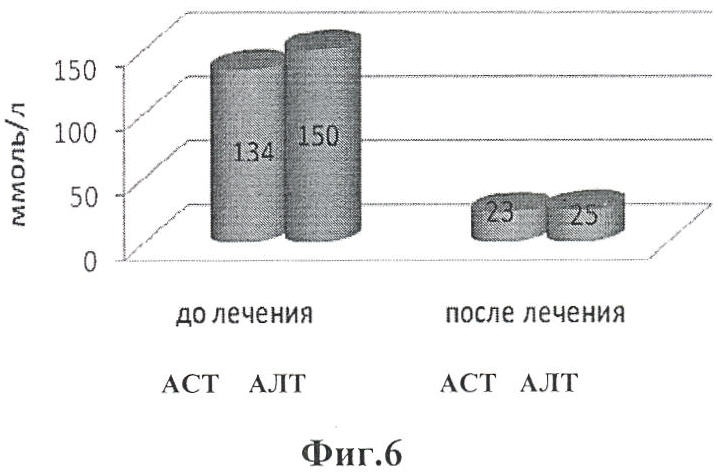
На фиг.6 приведены данные о изменении показателей трансаминаз при лечении хронического вирусного гепатита В комбинированным препаратом α-фетопротеина+α-интерферон-2 (пример 8).
Сущность и преимущества заявляемого изобретения поясняются следующими примерами.
Пример 1. Влияние состава композиции на ее противовирусную активность.
Влияние состава композиции на ее противовирусную активность изучали в тесте оценки противовирусной активности против вируса везикулярного стоматита на клеточной линии Л-68.
Линию диплоидных клеток легкого эмбриона человека Л-68 использовали для определения противовирусной активности, подлинности, токсичности интерферона и определения инфекционного титра вируса. (Посевной банк штамма диплоидных клеток Л-68 аттестован для приготовления иммунобиологических препаратов в МНИИ ВП АМН РФ совместно с ГИСК им. Л.А.Тарасевича МЗ РФ.)
Для эксперимента использовали лиофильно высушенный вирус, стерильно расфасованный в стеклянные запаянные ампулы. В 96-луночный планшет (типа "Costar", кат. №3598) вносили приготовленные клетки линии Л-68 в концентрации 5·104 клеток на лунку в объеме 0,2 мл. После этого планшет инкубировали в течение 1 суток при температуре 37°С в СO2-инкубаторе в атмосфере 5% СО2. За это время клетки распластывались в лунках, образуя сплошной монослой. Через 1 сутки культуральную среду I декантировали в стерильных условиях и в лунки планшета вносили заранее приготовленные разведения вируса в объеме 0,2 мл. По окончании инкубации (через 1 сутки) культуральную среду декантировали и в лунки вносили по 0,05 мл 0,2% раствора кристаллического фиолетового ("Sigma", кат.№С-0775) на 20% метаноле. Через 10 мин краску удаляли, планшет промывали под струей воды и высушивали. Далее в планшет добавляли 0,1 мл лизирующего буфера для элюции красителя в раствор. Интенсивность окрашивания учитывали на ридере для микропланшетов при длине волны 595 нм.
За инфекционный титр вируса принимали максимальное разведение вируса, при котором в течение 1 суток в данных условиях происходило полное разрушение монослоя клеток в лунках.
В культуральной среде готовили двукратные разведения образца рекомбинантного α-интерферона-2в человека или (β-Интерферона-2, активность которого выражена в международных единицах ME (что соответствовало 1 млн ME), и различные дозировки препарата альфа-фетопротеина человека (1 мкг/мл; 10 мкг/мл и 100 мкг/мл). После разведения в планшет вносили приготовленные клетки линии L-68 в концентрации 5·104 клеток на лунку в объеме 0,1 мл. Увеличение оптической плотности соответствовало большей биологической активности интерферона.
В результате проведенных экспериментов значимое усиление защитного действия интерферона от цитопатического действия вируса было выявлено при совместном использовании с препаратом альфа-фетопротеина в двух дозах (см. табл.1). Из таблицы видно, что препарат интерферона обладал дозозависимым защитным противовирусным действием (графы 1 и 5). При совместном внесении образца интерферона в дозе 1 млн МЕ с различными дозами α-фетопротеина отмечаются повышенные значения оптической плотности в опыте по сравнению с контролем, то есть в данных лунках большее количество клеток осталось защищенными от цитопатического действия вируса.
Пример 2. Исследования воздействия введения α-фетокина на противовирусную активность интерлейкинов и их антагонистов.
Специфическую активность композиции оценивали биологическим методом по подавлению пролиферации тимоцитов мышей.
В лунки 96-луночного планшета для культивирования («Flow», Великобритания, кат. №76-008-04 или аналогичного) вносили по 50,0 мкл разведений исследуемого препарата. Каждое разведение вносят не менее чем в три параллельные лунки. В контрольные лунки вносили по 50,0 мкл среды RPMI-1640. Во все лунки прибавляли по 100,0 мкл клеточной взвеси тимоцитов и планшет помещали в СО2-инкубатор на 2 ч при 37°С. После окончания времени преинкубации во все лунки планшета вносили по 25 мкл рабочего раствора конканавалина А и по 25 мкл рабочего раствора ГСО интерлейкина-1 бета.
Одновременно в этом же планшете ставили необходимые контроли:
- контроль клеточной взвеси: к 100 мкл культуральной среды RPMI-1640 добавляют 100 мкл клеточной взвеси тимоцитов;
- контроль действия субоптимальной дозы конканавалина А: к 75 мкл культуральной среды RPMI-1640 добавляют 25 мкл рабочего раствора конканавалина и 100 мкл клеточной взвеси тимоцитов;
- контроль действия интерлейкина-1 бета: к 50 мкл культурной среды добавляют 25 мкл раствора конканавалина А, 25 мкл рабочего раствора ГСО интерлейкина-1 бета и 100 мкл клеточной взвеси тимоцитов.
Культивирование проводили в течение 72 ч в СO2-инкубаторе при 37°С. За 18 ч до окончания культивирования во все лунки планшета вносили по 10 мкл рабочего раствора 3Н-тимидина (40 мкБк). После окончания культивирования тимоцитарные культуры с помощью полуавтоматического харвестера переносили на фильтры для культур клеток («Perkin Elmer», США, кат. №1450), которые затем высушивали. Фильтры помещали в пакеты со сцинтилляционной жидкостью («Perkin Elmer», США, кат. №1205) и определяли включение 3Н-тимидина тимоцитами каждой культуры, используя для этого сцинтилляционный счетчик «Microbeta TriLux» («Perkin Elmer» или аналогичный). Результаты выражали в импульсах в мин. Данные по всем параллельным пробам усредняли.
Достоверность отличий рассчитывали с помощью двухпарного Т-теста Стьюдента с неравными отклонениями, используя программу Microsoft Excel или вручную. Отличия считались достоверными при значениях вероятности Т-теста (р) меньших 0,05.
Для оценки специфической активности анализируемого образца рецепторного антагониста интерлейкина-1 производят расчет достоверности отличий интенсивности включения тимидина в лунках с различными концентрациями препарата и в лунках контроля действия интерлейкина. Далее находят минимальную концентрацию препарата, которая дает достоверное подавление интенсивности включения тимидина по сравнению с контролем действия интерлейкина и оценивают соотношение по массе данной концентрации препарата и используемой в тесте концентрации интерлейкина. Препарат считается активным, если данное соотношение не более чем 100:1. Полученные результаты приведены в таблицах 2 и 3.
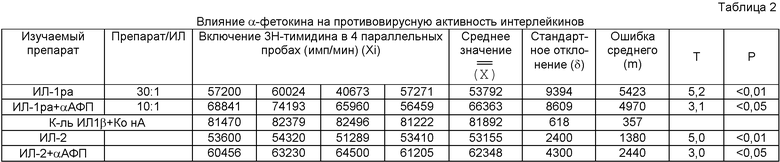
Из приведенных в таблице данных видно, что достоверное снижение включения 3Н-тимидина, стимулированного дозой Кон А и ИЛ или препарата «АРИЛ» наблюдается при меньшем соотношении, чем в случае сочетанного применения цитокина и αАФП. Следовательно, ингибирующий эффект от совместного воздействия достоверно выше.
Пример 3. Лечение инфекционного процесса, вызванного вирусом Эпштейна-Барра комбинированным препаратом альфа-фетопротеина + интерферон-альфа-2.
Больная П., 29 лет поступила в отделение профпатологии МСЧ №2 г.Перми с жалобами на затруднение движений в правой ноге из-за мышечной слабости, вызванной обычной физической нагрузкой, с последующим подволакиванием правой ноги и подворачиванием правой стопы внутрь; неустойчивость в вертикальном положении с открытыми глазами, онемение и гиперестезия кожных покровов верхних конечностей от уровня плечевых суставов до кончиков пальцев обеих кистей, где онемение особенно интенсивно, затруднение при выполнении захвата мелких предметов, онемение и гиперестезию кожных покровов по наружной и внутренней поверхности нижних конечностей с уровня тазобедренных суставов до пальцев стоп одинаковой интенсивности слева и справа; расплывчатость предметов при зафиксированном взгляде, постоянные головокружения.
Анамнез заболевания: Больна с 1991 г. Начало заболевания «классическое» - невралгия лицевого нерва-лечение-ремиссия. В 1992 г. повторная невралгия лицевого нерва-лечение-ремиссия. С 1991 по 1995 гг. нарастала мышечная слабость в нижних конечностях. Зимой 1995 г. отметила появление неустойчивости походки и при очередном осмотре невропатологом был установлен диагноз: рассеянный склероз.
В 1995 г. ЯМР, заключение: левосторонний энцефаломиелит. С 1995 г. несмотря на неоднократное лечение, включая пульс-терапию кортикостероидами, отмечен прогресс заболевания с отягощением неврологической симптоматики.
Клиническое наблюдение: в стационаре больная обследована. Заключение при электрофизиологическом исследовании (до лечения): картина соответствует процессу демиелинизации с 2 сторон, грубее слева с вторичным вовлечением аксонов. Позитивно-негативный комплекс P37-N45, отражающий первичную корковую активность отсутствует, нет ответа на уровне С5 сегмента. Отсутствие ответов на шейном и корковом уровнях свидетельствует о двухстороннем поражении быстрых проводников на уровне шейного утолщения и соматосенсорной зоны коры головного мозга.
На основании проведенного исследования установлен диагноз: рассеянный склероз, цереброспинальная форма, рецидивирующее течение, фаза неустойчивой ремиссии, вирусологическая инвазия (вирус Эпштейна-Барра), вторичный иммунодефицит с проявлениями аутоиммунной агрессии и иммунодепрессии по клеточному звену.
Больной проведено комплексное лечение: патогенетическая терапия, включавшая препарат альфа-фетопротеин человека в дозе 150 мкг совместно с α-интерфероном-2, препарат Интераль, 3 млн ME, в/м №30.
В результате проведенного лечения отмечена положительная динамика.
При ходьбе отсутствует ранее наблюдаемое подворачивание правой стопы внутрь. Исчезла атаксия туловища вправо, отсутствует тенденция к падению. Субъективно пациентка отмечает исчезновение расплывчатости предметов при фиксированном взгляде. Мышечная сила в руках увеличилась с 2 до 4 баллов.
Лабораторная динамика: AT против ВПГ, ЦМВ и токсоплазмозу по (IgM) не определялись. Гипериммуноглобулиемия отсутствует.
При контрольном электрофизиологическом исследовании (после проведенного лечения). Зрительные ВП по большинству показателей имеют положительную динамику. Соматосенсорные ВП n. Medianus - без динамики. Соматосенсорные ВП n. Tibialis характеризуются появлением ранее отсутствовавшего комплекса P37-N45,
что свидетельствует о процессе восстановления поврежденных участков коры головного мозга.
Также отмечалась положительная динамика по ЯМРТ (см. фиг.1).
Пациентка П. Диагноз: рассеянный склероз.
При сравнении данных ЯМРТ от 11.12.2011 г. и 28.11.2002 г. выявлена положительная динамика, заключающаяся в количественных и качественных характеристиках.
Так, в сравнении одинаковых Т2 взвешенных изображений установлено уменьшение очагов демиелинизации в стволе мозжечка перивентрикулярно с 13-15 очагов до 3-5 очагов. Качественные изменения характеризуются уменьшением площади демиелинизированных участков (см. фиг.1).
Пример 4. Лечение хронического вирусного гепатита С, генотип 3а комбинированным препаратом альфа-фетопротеина+интерферон-2-альфа.
История болезни №1053. Пациент Г., 27 лет, находился на лечении в отделении терапии НУЗ ОКБ ст. Пермь II с 17.03.08 по 17.2.08 с диагнозом:
Основной: Хронический вирусный гепатит С, неактивный.
Сопутствующий: хронический гастрит, ремиссия.
При поступлении жалоб активно не предъявлял.
Анамнез заболевания: На очередном профосмотре методом ИФА выявлены антитела к вирусному гепатиту С.
Направлен для обследования и проведения курса терапии альфа-фетопротеин человека+α-интерферон-2.
Клиническое наблюдение:
Выявлена вирусная нагрузка до лечения 6.8×106/мл, генотип 3а.
Назначен α-интерферон-2 в дозе 3000000 ME и альфа-фетопротеин человека 150 мкг, препараты вводились в «одном шприце» в течение 30 дней ежедневно в/м. После проведенного курса терапии RNA HCV методом ПНР не обнаружено (фиг.2).
Пример 5. Лечение полинейропатия, вызванной вирусом краснухи комбинированным препаратом альфа-фетопротеина+интерферон альфа.
История болезни №3830. Пациентка Л., 25 лет находилась на стационарном лечении в НУЗ ОКБ ст. Пермь II с 01.10.07 по 22.10.07 с диагнозом:
Хронический демиелинизирующий полирадикулоневрит. Вялый тетрапарез с выраженным латеральным дефасциитом больше в ногах. Атаксический синдром. Ухудшение.
Анамнез заболевания.
Больна с 1999 г. Заболела остро. На фоне общего здоровья появилось онемение в верхних и нижних конечностях, выраженная слабость. В течение 3-х недель слабость нарастала. Обратилась в поликлинику. Диагноз не был установлен. Направлена в стационар. Диагноз: полинейропатия. Проведен курс лечения без эффекта. Проходила стационарное лечение 3 раза в год, в течение последующих лет состояние не улучшалась. В марте 2007 г. по всей поверхности тела появилась эритематозно-папулезная сыпь, в периферической крови определились повышенные титры антител к краснухе и ВПГ. В связи с этим больной предложено провести курс лечения селективной иммуносупрессивной терапии препаратом альфа-фетопротеин человека в сочетании α-интерфероном.
Клиническое наблюдение: Учитывая прогресс заболевания на фоне проводимого лечения больной предложено стационарное лечение: альфа-фетопротеин человека 75 мкг + альфа-интерферон 3000000 Ед. №20 1 раз в день в/м. В ходе проводимого лечения, после введения препарата альфа-фетопротеина и интерферона, пациентка отметила увеличение мышечной силы в руках и ногах, значительное уменьшение атаксии. Появилась уверенная походка. Самостоятельно стала садиться и вставать со стула. Восстановилась поверхностная и глубокая чувствительность в нижних конечностях. Исчезла эритематозно-папулезная сыпь.
Электрофизиологическое исследование до лечения от 09.10.07: полиневритический характер поражения как моторных (в большей степени), так и сенсорных волокон периферических нервов аксонально-димиелинизирующего типа. Поражены моторные волокна тибиальных нервов на ногах. Электрофизиологическое исследование после лечения в динамике через 6 месяцев: имеется положительная динамика, по сравнению с исследованием от 3.10.07 и 09.10.07 года: увеличилась амплитуда М-ответов с нервов где они ранее не регистрировались, появились М-ответы с перонеальных нервов и с локтевого нерва. Сенсорные ответы не зарегистрированы. При стимуляции локтевого нерва слева регистрируются единичные F-волны (ранее не регистрировались).
Пример 6. Лечение хронического вирусного гепатита С, генотип 2а комбинированным препаратом альфа-фетопротеина + интерлейкин-1 бета.
История болезни №1426. Пациент Д., 54 года, находился на лечении в отделении терапии «НУЗ ОКБ ст. Пермь-II ОАО РЖД» с 10.04.08 по 09.05.08 с диагнозом:
Основной: Хронический вирусный гепатит С, генотип 2а, неактивный, умеренная вирусная нагрузка.
Сопутствующий: Хронический пиелонефрит, неполная ремиссия. Хронический простатит.
При поступлении жалоб активно не предъявлял.
Анамнез заболевания: В ноябре 2007 г. на очередном профосмотре по месту работы методом ИФА выявлены антитела к вирусному гепатиту С.
Направлен для дообследования и проведения курса индивидуальной противовирусной терапии комбинированным препаратом: альфа-фетопротеин, 100 мкг + интерлейкин-1 бета (препарата Беталейкин), 1 мкг. Препараты вводились в «одном шприце» в течение 30 дней ежедневно в/в капельно.
Клиническое наблюдение: Общее состояние удовлетворительное. Объективный статус без особенностей.
Вирусная нагрузка до лечения составляла 2,74·105/мл.
Трансаминазы в норме (ACT 26 ммоль/л, АЛТ 26 ммоль/л).
После проведенного курса терапии трансаминазы сохранялись в пределах нормы.
RNA HCV методом ПЦР не обнаружено (см. фиг.3).
Пример 7. Лечение хронического вирусного гепатита С, генотип 1в комбинированным препаратом альфа-фетопротеина + интерферон альфа.
История болезни №1743. Пациент Л., 54 года, находился на лечении в отделении терапии «НУЗ ОКБ ст. Пермь-II ОАО РЖД» с 05.05.08 по 03.06.08 с диагнозом:
Основной: Хронический вирусный гепатит С, генотип 1b, фаза репликации, неактивный, низкая вирусная нагрузка.
При поступлении жалоб активно не предъявлял.
Анамнез заболевания: В сентябре 2007 г. на очередном профосмотре по месту работы методом ИФА выявлены антитела к вирусу гепатита С.
Направлен для дообследования и проведения курса индивидуальной противовирусной терапии (альфа-фетопротеин человека + α-интерферон).
Клиническое наблюдение: Общее состояние удовлетворительное. Объективный статус без особенностей. Вирусная нагрузка до лечения составила 1,3·103/мл.
Трансаминазы в норме (ACT 25 ммоль/л, АЛТ 28 ммоль/л).
Назначен α-интерферон в дозе 3000000 ME в сочетании с альфа-фетопротеином человека в дозе 150 мкг, препараты вводились в «одном шприце» в течение 30 дней ежедневно внутримышечно.
После проведенного курса терапии трансаминазы сохранялись в пределах нормы.
RNA HCV методом ПНР не обнаружено (см. фиг.4.).
Пример 8. Лечение хронического вирусного гепатита В комбинированным препаратом альфа-фетопротеина + интерферон альфа.
История болезни №4735. Больная Ю., 25 лет находилась на стационарном лечении в отделении терапии НУЗ ОКБ ст. Пермь II г.Перми с 3.12.07 по 21.12.07.
Диагноз: Хронический вирусный гепатит В (HBsAg+), неактивный, фаза репликации, низкая вирусная нагрузка.
Жалобы при поступлении на периодическую тяжесть в правом подреберье, слабость, быструю утомляемость.
Анамнез заболевания: осенью 2006 г. на профосмотре обнаружен HBsAg.
Направлена в гепатоцентр. Проводился 3-недельный курс реаферона, затем получала ПегИнтрон по общепринятой схеме. На фоне лечения наблюдалось увеличение копий вируса в 40 раз.
Направлена для проведения курса терапии: альфа-фетопротеин человека+α-интерферон.
Клиническое наблюдение:
В стационаре назначена терапия α-интерферон по 3000000 ME с альфа-фетопротеином человека по 0,075 мг в/м. Препараты α-интерферон и альфа-фетопротеин человека вводились в «одном шприце».
Больная получала лечение в течение 17 дней, ежедневно.
На 17 день терапии по данным ПЦР диагностики - DNA НВV не обнаружено.
Пример 9. Лечение хронического вирусного гепатита С, генотип 1в на фоне ВИЧ инфекции комбинированным препаратом альфа-фетопротеина + интерферон альфа.
Пациент X, 38 лет, находился на амбулаторном лечении под диспансерным наблюдением в центре профилактики и лечения ВИЧ, гепатоцентре и кафедре инфекционных болезней УГМИ.
Основной: Хронический вирусный гепатит С, генотип 1в, фаза репликации, высокой степени активности, умеренная вирусная нагрузка; хроническая ВИЧ 1 инфекция фаза репликации, вторичный иммунодефицит.
При поступлении жалоб активно не предъявлял.
Анамнез заболевания: В 1995 г. на профосмотре случайно выявлены антитела к НСV и ВИЧ 1, инфекции подтверждены ПЦР исследованием количественно. В течение 6 мес. получал противовирусное лечение. Лечение не закончил из-за осложнений лечения (лейко- и тромбоцитопения, аллопеция).
Вирусная нагрузка не уменьшилась.
В мае 2008 г. направлен для дообследования и проведения курса индивидуальной противовирусной терапии.
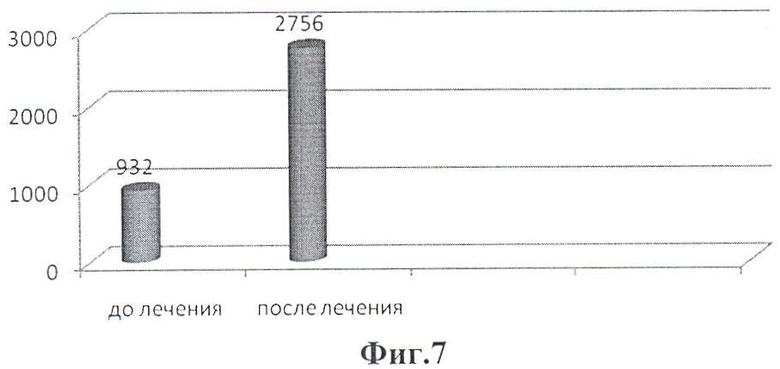
Клиническое наблюдение: Общее состояние удовлетворительное. Объективный статус без особенностей. Вирусная нагрузка RNA НСV до лечения составила 1,46·105 копий/мл. Вирусная нагрузка RNA HIV 2756 копий/мл. CD 4+932 кл.
АЛТ 150 ммоль/л, ACT 134 ммоль/л. Остальные биохимические показатели были в норме.
Назначен α-интерферон в дозе 3000000 ME в сочетании с альфа-фетопротеином человека в дозе 150 мкг, препараты вводились в «одном шприце» в течение 30 дней ежедневно внутримышечно.
После проведенного курса терапии по данным ПЦР диагностики RNA HCV не обнаружено - ранний вирусологический ответ, показатели трансаминаз в пределах физиологической нормы (см. графики). По данным ПЦР RNA HIV - не обнаружено.
После проведенного лечения CD 4+2015 кл. (см. фиг.5, 6).
Пример 10. Лечение ОРВИ комбинированным препаратом альфа-фетопротеина + рецепторный антагонист интерлейкина-1 (препарат РАЛЕЙКИН).
Работа проведена на базе кафедры оториноларингологии ГОУ ВПО Уральской Государственной Медицинской Академии Росздрава в I инфекционном и оториноларингологическом отделении городской клинической больницы №40.
Под наблюдением находились 32 человека с ОРВИ, из них 9 мужчин и 23 женщины в возрасте 38,1±12,0 лет, которые получали препарат рецепторного антагониста интерлейкина-1 (РАЛЕЙКИН) в сочетании с препаратом АФП в виде интраназального введения в каждую половину носа и орошение задней стенки глотки 2 раза в день в течение 5 дней.
Для оценки выраженности катарального синдрома и морфологических изменений слизистой оболочки проводился традиционный инструментальный эндоскопический осмотр ЛОР-органов, включающий переднюю и заднюю риноскопию, фарингоскопию, непрямую ларингоскопию, отоскопию.
При применении комбинированного препарата температура тела нормализовалась на четвертые сутки. Боль в мышцах и суставах регрессировала на третий, а головная боль на четвертый день заболевания. Чувство слабости полностью исчезло на шестые сутки. В этой группе пациентов наблюдалась максимально быстрая элиминация симптомов чихания - на третьи сутки и назальной обструкции на четвертые сутки заболевания. Ринорея и боль при глотании полностью регрессировали на четвертый, а кашель на пятый день наблюдения.
При исследовании концентрации цитокинов в назальных смывах до и после лечения (на 7-й день заболевания) количество интерферона-α на слизистой оболочке носа значимо возросло, достоверных изменений sIgA и ИЛ-6 у пациентов не обнаружено.
Таким образом, приведенные примеры показывают, что комбинированные препараты альфа-фетопротеина с цитокинами эффективны для лечения широкого спектра вирусных инфекций человека (инфекции, вызванные вирусами гепатита В и различных генотипов вируса гепатита С, краснухи, Эпштейна-Барра, сочетаниями вирусов гепатита С и вируса иммунодефицита человека).
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ПРЕПАРАТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВИРУСНЫХ ГЕПАТИТОВ В ИЛИ С И СПИДА | 2010 |
|
RU2440133C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВИРУСНЫХ ГЕПАТИТОВ | 2008 |
|
RU2369403C1 |
| Композиция на основе интерферона I или III типа и гамма-D-глутаминил-L-триптофана для профилактики и лечения инфекционных заболеваний и иммунодефицитных состояний (варианты) | 2014 |
|
RU2672861C2 |
| ЦИТОКИНСОДЕРЖАЩАЯ АЭРОЗОЛЬНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2410082C1 |
| ИНТЕРЛЕЙКИНСОДЕРЖАЩАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2009 |
|
RU2432170C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ И КОМПЛЕКСНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2577299C2 |
| СПОСОБ ИММУНОТЕРАПИИ ГНОЙНОГО РИНОСИНУСИТА | 2010 |
|
RU2457789C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА С | 2010 |
|
RU2429877C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИНТЕРФЕРОНА АЛЬФА-2b И ИНТЕРФЕРОНСОДЕРЖАЩИЙ ПРЕПАРАТ (ВАРИАНТЫ) | 2005 |
|
RU2294372C1 |
| ПРИМЕНЕНИЕ ЦИТОКИНА ИЗ СЕМЕЙСТВА ИНТЕРЛЕЙКИНА-6 ДЛЯ ПОЛУЧЕНИЯ КОМПОЗИЦИИ ДЛЯ КОМБИНИРОВАННОГО ВВЕДЕНИЯ С ИНТЕРФЕРОНОМ-АЛЬФА | 2006 |
|
RU2413529C2 |
Изобретение относится к области медицины, а именно к фармацевтике. Цитокинсодержащая композиция для лечения вирусных заболеваний содержит (% мас.):
альфа-фетопротеин - 0,001-99
препарат цитокина - остальное.
В качестве цитокина могут быть использованы интерферон-2-альфа, интерлейкин-1-бета, рецепторный агонист интерлейкина. Использование заявленной композиции позволяет повысить эффективность лечения заболеваний, вызванных вирусными инфекциями человека (вирусами гепатита В и различных генотипов вируса гепатита С, краснухи, Эпштейна-Барра, сочетаниями вирусов гепатита С и вируса иммунодефицита человека). 3 з.п. ф-лы, 10 пр., 3 табл., 7 ил.
1. Цитокинсодержащая композиция для лечения вирусных заболеваний, содержащая цитокин и иной белок сыворотки крови, отличающаяся тем, что в качестве белка она содержит альфа-фетопротеин человека при следующем соотношении ингредиентов, мас.%:
2. Цитокинсодержащая композиция для лечения вирусных заболеваний по п.1, отличающаяся тем, что в качестве цитокина она содержит интерферон-2-альфа.
3. Цитокинсодержащая композиция для лечения вирусных заболеваний по п.1, отличающаяся тем, что в качестве цитокина она содержит интерлейкин-1-бета.
4. Цитокинсодержащая композиция для лечения вирусных заболеваний по п.1, отличающаяся тем, что в качестве цитокина она содержит рецепторный антагонист интерлейкина.
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ ПРОТИВОВИРУСНОГО ДЕЙСТВИЯ | 1995 |
|
RU2073522C1 |
| ИНТЕРФЕРОНСОДЕРЖАЩАЯ АЭРОЗОЛЬНАЯ КОМПОЗИЦИЯ "НИКОФЕН" | 2004 |
|
RU2277904C2 |
| Вагонеточный скат для поддержки ударного рельса при разгонке рельсовых стыковых зазоров | 1928 |
|
SU7785A1 |
| КОМПОЗИЦИЯ АЛЬФА-ИНТЕРФЕРОНА В ФОРМЕ ВОДНОГО РАСТВОРА | 2000 |
|
RU2232595C2 |
| СПОСОБ ЗАЩИТЫ ЛИМФОИДНЫХ КЛЕТОК КРОВИ ЧЕЛОВЕКА ОТ ВИЧ | 1995 |
|
RU2115125C1 |
| NOMURA H | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Hepatol Res | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2012-04-20—Публикация
2009-03-26—Подача