Предшествующий уровень техники
Настоящее изобретение относится к применению липосомального препарата для изготовления фармацевтической композиции и к применению такой композиции для лечения рака молочной железы, негативного по трем рецепторам.
В настоящее время системное лечение рака молочной железы предлагает три основных различных способа терапевтического воздействия, и возможность применения этих различных вариантов лечения по существу зависит от рецепторного статуса больного (Bernard-Marty et al., 2004). Для проведения эндокринной и биологической терапии требуется наличие соответствующих рецепторов на раковых клетках, тогда как цитотоксическая химиотерапия не зависит от этих специфических рецепторов.
У больных раком молочной железы, положительным по рецепторам гормонов, эндокринная терапия или ее комбинация обычно является предпочтительным методом лечения (Bernard-Marty et al., 2004; Grandishar, 2004). При наличии рецепторов эстрогена (ER) и/или рецепторов прогестерона (PgR) частота ответа на лечение составила выше 80%. В целом, у больных в постменопаузе отмечается повышенная экспрессия ER и PgR по сравнению с больными в пременопаузе.
Золотым стандартом эндокринной терапии является селективный модулятор ER тамоксифен. Он ингибирует связывание эстрогена с рецептором эстрогена, таким образом нарушая серию клеточных механизмов, которые регулируют клеточную репликацию. Несмотря на хорошую переносимость в большинстве случаев тамоксифен вызывает ряд побочных реакций. Хотя этот препарат имеет общую высокую частоту ответа на лечение, у многих больных развивается рецидив заболевания, и возникает устойчивость к препарату. Устойчивость может быть связана с изменением взаимодействия между тамоксифеном и рецептором эстрогена.
Для борьбы с лекарственной устойчивостью были разработаны альтернативные виды эндокринной терапии, которые ставят под сомнение роль тамоксифена (Bernard-Marty et al., 2004; Grandishar, 2004). Ингибиторы ароматазы непосредственно препятствуют биосинтезу эстрогена путем ингибирования фермента ароматазы, преобразующего андростендион в эстрадиол. Последнее поколение этих ингибиторов включает нестероидные препараты, такие как летрозол, анастрозол и вострозол, и стероидные препараты, такие как эксеместан. Лучшая безопасность и частота ответа на лечение в случае этого класса лекарственных средств сделали ингибиторы ароматазы средствами стандартной эндокринной терапии для лечения метастазируемого рака молочной железы у женщин в постменопаузе.
Фулвестрант с противоэстрогенной активностью лишен проблем устойчивости, отмеченных у тамоксифена, благодаря другому механизму действия. Он связывает ER, ингибируя связывание ДНК, и снижает концентрацию ER путем стимуляции его разрушения.
У женщин в пременопаузе, положительных в отношении ER- и PgR, способы эндокринной терапии, кроме применения тамоксифена, включают абляцию яичников хирургическим путем или лучевую терапию и терапию аналогами лютеинизирующего рилизинг фактора гормона (LHRH) (Bernard-Marty et al., 2004). У этих больных яичники являются основным источником синтеза эстрогена, и удаление яичников являлось первоначальной терапией по поводу рака молочной железы. Во избежание побочных реакций при абляции яичников хирургическим вмешательством или облучением функцию яичников можно подавить аналогами LHRH. Аналоги LHRH, такие как госерелин, лейпролид и трипторелин, подавляют продукцию эстрогена яичниками за счет ингибирования гипофизарного высвобождения гонадотропинов посредством их антагонистического воздействия на рецепторы GnRH (гонадолиберина) (Prowell and Davidson, 2004).
По мере все большего понимания и интенсивного исследования в области биологии рака молочной железы в последние годы появились несколько новых мишеней для противоопухолевой терапии. Среди них основной мишенью был определен HER-2/neu. Рецептор эндотелиального фактора роста 2 типа (HER-2) амплифицирован и/или сверхэкспрессирован приблизительно в 30% случаев опухоли молочной железы (Slamon et al., 1987), и на него направленно воздействует ингибирующее антитело трастузумаб. Поскольку трастузумаб представляет собой одно из нескольких средств, приводящих к увеличению общего выживания при метастазируемом раке молочной железы, то оценка статуса HER-2 стала необходимой для оптимально эффективного лечения (Bernard-Marty et al., 2004).
Трастузумаб признан в качестве лекарства второй линии метастазируемого рака молочной железы у больных, имеющих HER-2, которые получали одну или несколько схем химиотерапии, или в качестве лекарства первой линии в комбинации с паклитакселом. Трастузумаб обычно используют до тех пор, пока не происходит прогрессирование заболевания. В целом он хорошо переносится, но самым значимым побочным эффектом является застойная сердечная недостаточность. Применение трастузумаба постоянно оценивается при различных видах моно- и комбинированного лечения в различных популяциях больных и схемах лечения.
Рецепторный статус ER, PgR и HER-2 можно определить стандартными иммуногистохимическими (IHC) или ферментными анализами (Chebil et al., 2003; Yamashita et al., 2006; Schaller et al., 2001). Статус HER-2 также можно оценить амплификацией гена флюоресцентной гибридизацией in situ (FISH) (Kallioniemi et al., 1992).
В целом, способы лечения, зависимые от рецепторного статуса больных, оказались очень эффективным при лечении рака молочной железы.
К сожалению, примерно в 15% случаев рак молочной железы является негативным по ER, PgR и HER-2. В этих случаях прогноз крайне неблагоприятный с частотой рецидива 80% и средней выживания только 6 месяцев.
Для больных, негативных по ER, PgR и HER-2, а также для больных с заболеванием, устойчивым к эндокринной терапии, химиотерапия представляет собой единственный вариант лечения. Химиотерапевтические препараты, обычно используемые при раке молочной железы, представляют собой препараты класса антрациклина, класса таксана и в меньшей степени антиметаболиты, например, капецитабин, гемцитабин, алкилирующие агенты и алкалоиды винки. Эти препараты используют в соответствии с двумя основными схемами лечения. Эти препараты можно использовать как самостоятельные средства последовательным образом или можно использовать в комбинированной терапии. Безусловно, эти два варианта лечения можно в некоторой степени комбинировать.
Было показано, что антрациклины и, в частности, доксорубицин и эпирубицин являются активными средствами при лечении рака молочной железы, а комбинированные схемы с антрациклином представляют собой способы лечения первой линии у больных, которые не получали антрациклины при адъювантной терапии. Простое комбинированное лечение состоит, например, из доксорубицина/эпирубицина плюс циклофосфамида, доксорубицина/эпирубицина плюс циклофосфамида и 5-фторурацила или комбинации антрациклинов и капецитабина или гемцитабина (O'Shaughnessy, 2005).
Однако при обычном использовании антрациклинов на ранних стадиях лечения рака молочной железы повышается вероятность развития устойчивости к антрациклинам у рака молочной железы (Bеrnard-Marty et al., 2004).
Введение таксанов паклитаксела и доцетаксела при лечении обеспечило дополнительную возможность борьбы с заболеванием первой и второй линии. Паклитаксел имеет уникальный механизм действия и широкий спектр антипролиферативной активности, так как связывается с микротрубочками, способствует полимеризации тубулина и стабилизирует собранные микротрубочки. В результате, паклитаксел блокирует клеточный цикл в профазе, приводя к накоплению клеток на фазе G2/M.
К сожалению, паклитаксел имеет крайне низкую растворимость в воде, что затрудняет получение подходящей лекарственной формы. В настоящее время паклитаксел входит в состав и вводится в носителе, в том числе Кремофор EL (полиэтоксилированное касторовое масло) и этанол в соотношении 50:50 (об./об.). Этот раствор разбавляют до 1:10 в солевом растворе перед введением больному. Однако сообщалось о различных тяжелых побочных реакциях композиции Кремофора EL, таких как, например, гиперчувствительность и реакции гиперчувствительности, нефротоксичность и нейротоксичность.
В Патентах США №№ 5648090, 5424073 и 6146659 (Rahman et al.) описан паклитаксел, инкапсулированный в липосому для способа лечения рака у млекопитающих. В этих патентах раскрыт способ введения хозяину терапевтически эффективного количества фармацевтической композиции липосом, которые включают липосому, образующую материал, кардиолипин, и средство, такое как паклитаксел, или антинеопластическое производное паклитаксела, или их смесь, с фармацевтически приемлемым эксципиентом.
Из патента США № 5837283 известно, что катионные липосомы предпочтительно направлены на ангиогенные эндотелиальные клетки в солидных опухолях. Из описания документа WO 2005/0309533 (Teifel et al.) известно, что лечение паклитакселом, инкапсулированным в катионные липосомы, может быть эффективным при различных видах рака. В указанном документе описано использование композиций катионных липосом паклитаксела у больных, страдающих меланомой, раком предстательной железы, поджелудочной железы, желудочно-кишечного тракта, ободочной и прямой кишки и молочных желез. Также описано использование композиций катионных липосом паклитаксела в различных экспериментальных моделях рака поджелудочной железы, саркомы матки, карциномы ободочной кишки и плоскоклеточной карциномы головы и шеи.
Известны также липосомальные композиции для антрациклиновых препаратов. Доксорубицин был инкапсулирован в незаряженных пэгилированных или непэгилированных липосомах для лечения рака молочной железы. Эти композиции использовали в схемах лечения рака молочной железы первой линии (Chan et al., 2004) и второй линии (Keller et al., 2004).
Резюмируя, можно сказать, что большинство вариантов лечения рака молочной железы зависит от рецепторного статуса больных. В частности, эндокринные типы лечения больных подгруппы, негативной по трем рецепторам, неэффективны. Варианты химиотерапевтического лечения ограничены и часто отмечается устойчивость к существующим схемам, подобным антрациклинам. Следовательно, в области медицины существует неудовлетворенная потребность в разработке новых способов лечения для указанного показания.
Таким образом, основной задачей настоящего изобретения является усовершенствование лечения рака молочной железы, негативного по трем рецепторам, в частности, у больных с устойчивостью к лечению антрациклинами.
Описание изобретения
Эта проблема решается благодаря новой фармацевтической композиции для лечения рака молочной железы, негативного по трем рецепторам. Композицию можно использовать в различных схемах или в виде моно- или комбинированной терапии.
Первый аспект настоящего изобретения относится к применению катионного липосомального препарата, содержащего по меньшей мере один катионный липид, антимитотическое средство и необязательно по меньшей мере один нейтральный и/или анионный липид, для получения фармацевтической композиции для лечения рака молочной железы, негативного по трем рецепторам, у человека или животного.
В предпочтительном варианте осуществления катионный липосомальный препарат содержит по меньшей мере один катионный липид в количество от примерно 30 моль% до примерно 99,9 моль%, антимитотическое средство в количестве по меньшей мере примерно 0,1 моль% и необязательно по меньшей мере один нейтральный и/или анионный липид в количестве от примерно 0 моль% до примерно 70 моль%.
Антимитотическим средством предпочтительно является паклитаксел или его производное, такое как доцетаксел. Другие подходящие антимитотические средства представляют собой антрациклины, предпочтительно, доксорубицин или эпирубицин, талидомид, алкалоиды барвинка, подобные винорелбину или винкристину, другие средства, взаимодействующие с микротрубочками, такие как дискодермолид, лаулималид, изолаулималид, элейтеробин, саркодиктин А и В.
Катионный липосомальный препарат можно использовать как монотерапию или в составе комбинированной терапии, например в при комбинированной терапии с терапевтически эффективной дозой по меньшей мере еще одного активного средства, которое можно вводить в виде препарата, который не является катионным липосомальным препаратом, например не является липосомальным препаратом. Дополнительным активным средством может являться химиотерапевтическое средство, такое как антрациклин, и/или дополнительно таксан, например паклитаксел.
Для лечения рака молочной железы, негативного по трем рецепторам, заявители предполагают что использование противоопухолевого средства, например таксана, включенного в катион липосом, обеспечивает улучшенное соотношение между клинической реакцией и побочными эффектами по сравнению с применением антимитотического средства в препаративной форме, отличной от липосомальной. Этот эффект нельзя было спрогнозировать на основании предшествующего уровня техники, поскольку катионные липосомы нацеливают лекарственное средство на эндотелиальные клетки опухоли, которые составляют лишь небольшую часть опухоли.
Кроме того, заявители полагают, что комбинированная терапия антимитотическим средством в липосомальной композиции и дополнительным средством, например антимитотическим средством в композиции, отличной от ее липосомальной, имеет улучшенное соотношение клинической реакции и побочных эффектов, по сравнению с использованием только нелипосомальной композиции, при использовании в аналогичных кумулятивных дозах. Такой синергический эффект нельзя было спрогнозировать на основании предшествующего уровня техники. Как указано выше, различные композиции нацеливают лекарственные препараты на различные участки внутри опухоли. Нельзя было спрогнозировать, что препараты с одинаковым типом действия, подобные антимитотическим лекарственным препаратам, будут проявлять синергический эффект при воздействии на различные клетки внутри опухоли.
Предпочтительные примеры применения фармацевтической композиции, содержащей паклитаксел в катионных липосомах, для лечения различных опухолей у людей описаны в документе WO 2005/0309533 (Teifel et al.).
Особым преимуществом настоящего изобретения является новый способ лечения подтипа рака молочной железы, для которого имелись лишь ограниченные варианты лечения ввиду его биологических свойств. Однако следует отметить, что указанную выше комбинированную терапию можно также использовать при других медицинских показаниях, например для лечения гиперпролиферативных расстройств, например ангиогенных и/или сосудистых расстройств, или рака в целом.
Особое преимущество комбинированной терапии заключается в снижении побочных эффектов активных средств. Следовательно, большим преимуществом является повышение диапазона используемых доз химиотерапевтических средств путем введения комбинации средств в липосомальных и нелипосомальных формах без увеличения побочных эффектов по сравнению с традиционным способом лечения больных раком, негативным по трем рецепторам, или другими расстройствами, комбинированное лечение повышает эффективность лечения и уменьшает побочные эффекты.
Еще один аспект изобретения относится к комбинации
а) катионного липосомального препарата, содержащего по меньшей мере один катионный липид, антимитотическое средство и, необязательно, по меньшей мере один нейтральный и/или анионный липид, и
b) нелипосомального препарата, содержащего антимитотическое средство, для одновременного, раздельного и/или последовательного введения человеку или животному.
Еще один аспект изобретения относится к комбинации
а) катионного липосомального препарата, как описано выше, который предпочтительно содержит по меньшей мере один катионный липид в количестве примерно от 30 моль% до примерно 99,9 моль%, антимитотическое средство, например таксан, в количестве по меньшей мере примерно 0,1 моль% и, необязательно, по меньшей мере один нейтральный и/или анионный липид в количестве от примерно 0 моль% до примерно 70 моль%, и
b) нелипосомального препарата, содержащего антимитотическое средство,
для одновременного, раздельного и/или последовательного введения в организм человека или животного. Предпочтительным является лечение рака.
Еще один аспект изобретения относится к способу лечения рака молочной железы, негативного по трем рецепторам, включающему введение катионного липосомального препарата, содержащего по меньшей мере один катионный липид, антимитотическое средство, и, необязательно, по меньшей мере один нейтральный и/или анионный липид и, предпочтительно, содержащего по меньшей мере один катионный липид в количестве от примерно 30 моль% до примерно 99,9 моль%, антимитотическое средство, например таксан, в количестве по меньшей мере примерно 0,1 моль% и, необязательно, по меньшей мере один нейтральный и/или анионный липид в количестве от примерно 0 моль% до примерно 70 моль%, в терапевтически эффективной дозе индивидууму.
Еще один аспект изобретения относится к способу лечения гиперпролиферативного расстройства, включающему введение комбинации, описанной выше, в терапевтически эффективной дозе индивидууму.
Особенно предпочтительные варианты осуществления по изобретению, относящиеся к катионным липосомальным препаратам, комбинациям катионного липосомального препарата и нелипосомального препарата для лечения рака молочной железы, негативного по трем рецепторам, более конкретно описаны в нижеследующем описании и примерах.
«Примерно» в контексте величин количества относится к среднему отклонению максимум ±20%, предпочтительно ±10% от указанной величины. Например, количество катионного липида примерно 30 моль% относится к 30 моль% ±3 моль% относительно общей молярности липида/амфифила.
«Активное средство» относится к средству, которое является терапевтически эффективным.
«Носитель» относится к разбавителю, адъюванту, эксципиенту или наполнителю, который подходит для введения диагностического или терапевтического средства. Этот термин также относится к фармацевтически приемлемому компоненту (компонентам), который содержит, образует комплексы или иначе ассоциируется со средством для содействия транспорту такого средства к предназначенному участку-мишени. Носители включают те, которые известны в данной области, такие как липосомы, полимеры, липидные комплексы, сывороточный альбумин, антитела, циклодекстрины и декстраны или другие супрамолекулярные сборки.
«Комбинация» или «совместное введение» относится к схеме введения, которая является синхронной, серийной, перекрывающей, чередующейся, параллельной или любой другой схемой лечения, при которой различные препараты или терапевтические средства вводятся как часть одной схемы лечения, назначенного курса или показания, или при которых периоды времени, в течение которых различные вводимые препараты или терапевтические средства частично или полностью совпадают иным образом.
Термин «производное» относится к соединению, полученному из другого соединения, в то же время сохраняющее его общие структурные признаки. Производные можно получить, например, химической функционализацией или дериватизацией.
Термины «липосома» и «липосомальный препарат» используются синонимически по всему настоящему описанию. «Липосома» относится к микроскопическому сферическому, заключенному в мембрану пузырьку (диаметром примерно 50-2000 нм). Термин «липосома» охватывает любой компартмент, заключенный в липидную двухслойную оболочку. Липосомы также называют липидными пузырьками. Для формирования липосомы липидные молекулы включают удлиненные неполярные (гидрофобные) части и полярные (гидрофильные) части. Гидрофобные и гидрофильные части молекулы предпочтительно расположены на двух концах удлиненной молекулярной структуры. Если такие липиды диспергированы в воде, то они спонтанно образуют двухслойные мембраны, именуемые пластинками. Пластинки состоят из двух однослойных листков из липидных молекул с их неполярными (гидрофобными) поверхностями, обращенными друг к другу, и их полярными (гидрофильными) поверхностями, обращенными к водной среде. Мембраны, образованные липидами, заключают в себя часть водной фазы образом, подобным клеточной мембране, заключающей содержимое клетки.
Таким образом, двухслойная оболочка липосомы имеет сходства с клеточной мембраной без белковых компонентов, присутствующих в клеточной мембране. Термин «липосома», используемый в настоящем изобретении, включает многопластинчатые липосомы, которые в целом имеют диаметр в диапазоне примерно от 1 до 10 мкм и состоят из примерно 200 концентрических липидных двухслойных структур, чередующихся со слоями водной фазы, а также включает однопластинчатые пузырьки, которые состоят из одного липидного слоя и в целом имеют диаметр в диапазоне от примерно 20 до примерно 400 нанометров (нм), от примерно 50 до примерно 300 нм, от примерно 300 до примерно 400 нм, от примерно 100 до примерно 200 нм, причем пузырьки можно получить, подвергая многопластинчатые липосомы воздействию ультразвука, экструзией под давлением через мембраны, имеющие поры определенного размера, или гомогенизацией под высоким давлением. Предпочтительными липосомами были бы однопластинчатые пузырьки, которые имеют один липидный слой и диаметр в диапазоне примерно 25-400 нм.
Термин «таксан», используемый в настоящем документе, относится к классу антинеопластических средств, имеющих механизм действия микротрубочек и имеющих структуру, которая включает необычную таксановую кольцевую структуру и стереоскопическую боковую цепь, которая требуется для цитостатической активности. В термин «таксан» также включены разнообразные известные производные, включая и гидрофильные производные, и гидрофобные производные. Производные таксана включают без ограничения производные галактозы и маннозы, описанные в международной патентной заявке № WO 99/18113; пиперазино- и другие производные, описанные в документе WO 99/14209; производные таксана, описанные в документах WO 99/09021, WO 98/22451 и в патенте США 5869680; 6-тио производные, описанные в документе WO 98/28288; сульфенамидные производные, описанные в патенте США № 5821263; и производные таксола, описанные в патенте США № 5415869. И активное средство паклитаксел, и доцетаксел относятся к классу таксана.
«Паклитаксел» (который, как следует понимать, в настоящем документе включает аналоги, препаративные формы и производные, такие как, например, доцетаксел, таксотер (препаративную форму доцетаксела), 10-дезацетиловые аналоги паклитаксела и 3'N-дезбензоил-3'N-трет-бутоксикарбониловые аналоги паклитаксела) можно легко получить, используя методики, известные специалистам в данной области (см. также документы WO 94/07882, WO 94/07881, WO 94/07880, WO 94/07876, WO 93/23555, WO 93/10076; патенты США №№ 5294637; 5283253; 5279949; 5274137; 5202448; 5200534; 5229529; и EP 590267), или получить из разнообразных торговых источников, включая, например, Sigma Chemical Co., St. Louis, Mo. (T7402 от Taxus brevifolia; или T-1912 от Taxus yannanensis). Следует понимать, что паклитаксел относится не только к обычной химически доступной форме паклитаксела, но также к аналогам (например, таксотеру, как указано выше) и конъюгатам паклитаксела (например, паклитакселу-ПЭГ, паклитакселдекстрану или паклитаксел-ксилозе).
«Терапевтически эффективная доза» представляет собой дозу активного средства или фармацевтической композиции, которая достаточна для достижения желаемого терапевтического результата у получающего лечение индивидуума.
Термин «зета-потенциал» относится к измеренному электрическому потенциалу частицы, такой как липосома, измеренному таким прибором, как Zetasizer 3000 с использованием лазерного доплеровского микро-электрофореза в определенных условиях. Зета-потенциал описывает потенциал на границе между объемом раствора и областью гидродинамического сдвига или диффузного слоя. Синонимом этого термина является «электрокинетический потенциал», потому что он представляет собой потенциал частиц, который действует снаружи, и ответственен за электрокинетическое поведение частицы.
Во всех случаях единица мг/м2 п.т. или просто мг/м2 относится к мг активного средства, например паклитаксела, на 1 м2 поверхности тела человека (п.т.).
Предпочтительными катионными липидами липосомального препарата являются соли N-[1-(2,3-диолеоилокси)пропил]-N,N,N-триметиламмония, например метилсульфат (DOTAP). Другие полезные липиды для настоящего изобретения могут включать: DDAB, диметилдиоктадециламмоний бромид; 1,2-диацилокси-3-триметиламмонийпропаны (включая без ограничения: диолеоил, димиристоил, дилауроил, дипальмитоил и дистеароил; также 2 различные ацильные цепи могут быть соединены с глицериновой основной цепью); N-[1-(2,3-диолоилокси)пропил]-N,N-триметиламин (DODAP); 1,2-диацилокси-3-диметиламмонийпропаны (включая без ограничения: диолеоил, димиристоил, дилауроил, дипальмитоил и дистеароил; также 2 различные ацильные цепи могут быть соединены с глицериновой основной цепью); N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмоний хлорид (DOTMA); 1,2-диалкилокси-3-диметиламмонийпропаны (включая без ограничения: диолеил, димиристил, дилаурил, дипальмитил и дистеарил; также 2 различные алкильные цепи могут быть соединены с глицериновой основной цепью); диоктадециламидоглицилспермин (DOGS); 3β-[N-(N',N'-диметиламиноэтан)карбамоил]холестерин (DC-Chol); трифторацетат 2,3-диолеоилокси-N-(2-(сперминкарбоксамидо)этил)-N,N-диметил-1-пропанаминия DOSPA); β-аланилхолестерин; цетилтриметиламмоний бромид (CTAB); диС14-амидин; N-трет-бутил-N'-тетрадецил-3-тетрадециламинопропионамидин; 14Dea2; N-(альфа-триметиламмониоацетил)дидодецил-D-глутамат хлорид (TMAG); O,O'-дитетрадеканоил-N-(триметиламмониоацетил)диэтаноламин хлорид; 1,3-диолеоилокси-2-(6-карбоксиспермил)пропиламид (DOSPER); N,N,N',N'-тетраметил-N,N'-бис(2-гидроксилэтил)-2,3-диолеоилокси-1,4-бутандиаммоний йодид; производные 1-[2-(ацилокси)этил]2-алкил(алкенил)-3-(2-гидроксиэтил)имидазолиний хлорида, как описано Solodin et al. (Solodin et al., 1995), такие как 1-[2-(9(Z)-окстадеценоилокси)этил]-2-(8(Z)-гептадеценил-3-(2-гидроксиэтил)имидазолиний хлорид (DOTIM), 1-[2-(гексадеканоилокси)этил]-2-пентадецил-3-(2-гидроксиэтил)имидазолиний хлорид (DPTIM), производные соединения четвертичного аммония 2,3-диалкилоксипропила, включающие гидроксиалкильную часть на четвертичном амине, как описано, например, Felgner et al. (Felgner et al., 1994), такие как: 1,2-диолеоил-3-диметилгидроксиэтиламмоний бромид (DORI), 1,2-диолеилоксипропил-3-диметилгидроксиэтиламмоний бромид (DORIE), 1,2-диолеилоксипропил-3-диметилгидроксипропиламмоний бромид (DORIE-HP), 1,2-диолеилоксипропил-3-диметилгидроксибутиламмоний бромид (DORIE-HВ), 1,2-диолеилоксипропил-3-диметилгидроксифениламмоний бромид (DORIE-Hpe), 1,2-димиристилоксипропил-3-диметилгидроксиэтиламмионий бромид (DMRIE), 1,2-дипальмитилоксипропил-3-диметилгидроксиэтиламмоний бромид (DPRIE), 1,2-дистерилоксипропил-3-диметилгидроксиэтиламмоний бромид (DSRIE), сложные катионные эфиры ацилкарнитинов, по данным Santaniello et al. [патент США № 5498633]; сложные катионные триэфиры фосфатидилхолина, т.е. 1,2-диацил-sn-глицерин-3-этилфосфохолины, где углеводородные цепи могут быть насыщенными или ненасыщенными и разветвленными или неразветвленными, с длиной цепи от С12 до С24, причем две ацильные цепи необязательно идентичны.
В предпочтительном варианте осуществления липосомальный препарат необязательно включает по меньшей мере один нейтральный и/или анионный липид. Нейтральные липиды представляют собой липиды, которые имеют нейтральный результирующий заряд. Анионные липиды или амфифилы представляют собой молекулы, которые имеют отрицательный результирующий заряд. Они могут быть выбраны из стеринов или липидов, таких как холестерин, фосфолипиды, лизолипиды, лизофосфолипиды, сфинголипиды или пэгилированные липиды с нейтральным или отрицательным результирующим зарядом. Следовательно, полезные нейтральные и анионные липиды включают: фосфатидилсерин, фосфатидилглицерин, фосфатидилинозит (не ограниченный определенным сахаром), жирные кислоты, стерины, включающие группу карбоновой кислоты, например холестерин, 1,2-диацил-sn-глицеро-3-фосфоэтаноламин, включая без ограничения DOPE, 1,2-диацилглицеро-3-фосфохолины и сфингомиелин. Жирные кислоты, связанные с основной цепью глицерина, не ограничены определенной длиной или количеством двойных связей. Фосфолипиды могут также иметь две различных жирные кислоты. Предпочтительно, эти другие липиды находятся в жидком кристаллическом состоянии при комнатной температуре, и они могут смешиваться (т.е. однородная фаза может быть образована и не происходит разделение фаз или образование домена) с использованным катионным липидом, в соотношении, в котором они применяются. В предпочтительном варианте осуществления нейтральный липид представляет собой DOPC.
В еще одном предпочтительном варианте осуществления липосомальный препарат необязательно включает нейтральные и/или анионные липиды, предпочтительно, DOPC, в количестве от примерно 30 моль% до примерно 70 моль%, предпочтительно, от примерно 40 моль% до примерно 60 моль%, а предпочтительнее, от примерно 45 моль% до примерно 55 моль%.
Еще одной целью настоящего изобретения является возможность дегидратировать катионный липосомальный препарат по настоящему изобретению, а также хранить в течение длительных периодов времени в дегидратированном состоянии, а затем регидратировать перед применением, без потери существенной части содержимого во время процессов дегидратации, хранения и регидратации. Для достижения этой цели могут присутствовать один или несколько защитных агентов, таких как криопротекторы. Таким образом, катионный липосомальный препарат по изобретению, предпочтительно, включает криопротектор, который выбран из сахаров или спиртов, или их комбинации. Предпочтительно, криопротектор выбран из трегалозы, мальтозы, сахарозы, глюкозы, лактозы, декстрана, маннита, сорбита или их комбинаций. В предпочтительном варианте осуществления липосомальный препарат включает трегалозу в диапазоне от примерно 5% (масс./об.) до примерно 15% (масс./об.) относительно общего объема препарата.
В предпочтительном варианте осуществления настоящего изобретения таксан представляет собой паклитаксел или его производное. Катионный липосомальный препарат может включать паклитаксел в количестве по меньшей мере от примерно 2 моль% до примерно 8 моль%, предпочтительно, по меньшей мере от примерно 2,5 моль% до примерно 3,5 моль%.
В особенно предпочтительном варианте осуществления катионный липосомальный препарат представляет собой DOTAP, DOPC и паклитаксел в соотношении примерно 50:47:3. Этот состав также обозначается как MBT-0206 или Endo TAG-1. Endo TAG-1 имеет содержание липида 10 мМ в 10% растворе масс./масс. дигидрата трегалозы. Получение такого состава раскрыто в документе WO 2004/002468, который приведен в настоящий документ в качестве ссылки в полном объеме.
Предпочтительно, липосомальный препарат имеет зета-потенциал в диапазоне от примерно 0 мВ до примерно 100 мВ, предпочтительно, в диапазоне от примерно 20 мВ до примерно 100 мВ в примерно 0,05 мМ растворе KCl примерно при рН 7,5.
Описанные липосомы используются для получения фармацевтической композиции для лечения рака молочной железы, лечение эндокринной терапией и терапией, связанной с HER-2, которого неэффективно. Предпочтительно, лечение направлено на рак молочной железы, негативный по трем рецепторам. Показание рак молочной железы, негативный по трем рецепторам, включает рак молочной железы с негативным рецепторным статусом в отношении рецептора эстрогена (ER), рецептора прогестерона (PgR) и рецептора HER-2 (Her-2). Определение рецепторного статуса представляет собой принятую диагностическую процедуру рака молочной железы, хорошо известную в данной области. Статус ER, PgR и HER-2 можно определить стандартными анализами на иммуногистохимической или ферментной основе (IHC) (Chebil et al., 2003; Yamashita et al., 2006), (Schaller et al., 2001). Статус HER-2 можно также оценить генной амплификацией путем флюоресцентной гибридизации in situ (FISH) (Kallioniemi et al., 1992).
Фармацевтическую композицию можно применять как препарат первой, второй и третьей линии. Получающие терапию больные могли быть ранее подвергнуты хирургическому вмешательству для резекции опухоли, лучевой терапии и/или химиотерапии. Используемая химиотерапия при раке молочной железы представляет собой комбинированные схемы на основе антрациклина. Обычно эти комбинированные схемы включают антрациклиновый препарат, например доксорубицин или эпирубицин. Лечение первой линии может включать комбинированную терапию антрациклиновым препаратом и таксановым препаратом. Больные могут быть в пре- или постменопаузе. Рак, на который направлено лечение, может быть на различных клинических стадиях по размеру, распределению и степени образования метастазов.
Фармацевтическую композицию можно вводить больному в терапевтически эффективной дозе. По меньшей мере один раз в неделю, но ее можно также вводить несколько раз в неделю. В предпочтительном варианте осуществления фармацевтическая композиция вводится один или два раза в неделю. Композицию можно также вводить различное число раз в неделю в течение периода лечения.
Во время курса лечения применение композиции можно пропускать по меньшей мере в течение недели. В зависимости от длительности лечения и наблюдаемых побочных эффектов применение можно также пропустить несколько раз в течение периода лечения.
Предпочтительно, липосомальный препарат вводится одиночными дозами от примерно 1 мг/м2 до примерно 50 мг/м2 на введение. В предпочтительном варианте осуществления препарат вводится в дозе от примерно 20 мг/м2 до примерно 50 мг/м2 на введение. В особенно предпочтительном варианте осуществления препарат вводится в дозе от примерно 22 мг/м2 до примерно 44 мг/м2 на введение. В другом особенно предпочтительном варианте осуществления препарат вводится два раза в неделю в дозе примерно 44 мг/м2. В наиболее предпочтительном варианте осуществления изобретения липосомальный препарат вводится в 1, 5, 8, 11, 15, 18, 22, 25, 29, 32, 36 и 39 дни цикла лечения с последующим 14-дневным интервалом без лечения, или в 1, 4, 6, 11, 15 и 18 дни цикла лечения с последующим 10-дневным интервалом без лечения. При желании, циклы лечения могут повторяться несколько раз, например по меньшей мере 2, 3 или 4 раза.
Другим важным аспектом настоящего изобретения является возможность использования катионной липосомальной препаративной формы при одновременной, раздельной или последовательной комбинированной терапии. Комбинированная терапия дополнительно включает введение терапевтически эффективной дозы по меньшей мере еще одного активного средства. В одном из вариантов осуществления еще одно активное средство представляет собой нелипосомальную препаративную форму. Комбинированная терапия может включать одновременное, раздельное и/или последовательное введение человеку или животному. При одновременной комбинированной терапии липосомальный препарат и еще одно активное средство вводятся в один и тот же день.
Липосомальный препарат и еще одно активное средство можно вводить в различные точки времени в один и тот же день или в различные дни. В предпочтительном варианте осуществления липосомальный препарат вводится перед еще одним активным средством, предпочтительно более чем за один час, но не более чем за 12 часов до применения еще одного активного средства.
Еще одно активное средство может быть выбрано из цитотоксических или цитостатических веществ, таких как вещество, обладающее противоопухолевой активностью или активностью против эндотелиальных клеток, соединение, которое снижает или устраняет реакции гиперчувствительности, или химиосенсибилизатор, или их комбинации.
В предпочтительном варианте осуществления еще одно активное средство выбрано из антинеопластического средства, особенно антимитотическое средство, подобное таксану, антрациклин, предпочтительно, доксорубицин или эпирубицин, статин, депсипептид, талидомид, другие средства, взаимодействующие с микротрубочками, такие как дискодермолид, лаулималид, изолаулималид, элейтеробин, саркодиктин А и В, алкилирующие агенты, в частности соединения, включающие платину, подобные цисплатину, карбоплатину, средства, ингибирующие ДНК топоизомеразу, подобные камптотецину, РНК/ДНК антиметаболиты, в частности 5-фторурацил, гемцитабин или капецитабин. В наиболее предпочтительном варианте осуществления оно выбирается из паклитаксела, доцетаксела, кампотецина или любого их производного.
Соединение, которое снижает или устраняет реакции гиперчувствительности, могут быть выбраны из группы, включающей стероиды, антигистамины, антагонисты Н2 рецепторов и их комбинаций в количестве, достаточном для предотвращения фатальных анафилактических реакций. Указанное соединение может также быть выбрано из группы, включающей ранитидин, дексаметазон, дифенгидрамин, фамотидин, гидрокортизон, клемастин, циметидин, преднизолон, хлорфенирамин, хлорфенамин, диметинден малеат и прометазин.
Химиосенсибилизатор может быть выбран из группы, включающей модуляторы клеточного цикла, вещества, которые устраняют лекарственную устойчивость, подобные верапамилу, вазоактивные вещества, подобные антигипертензивным лекарственным препаратам, и вещества, которые модифицируют взаимодействия катионных липосом с компонентами крови, подобные протамину.
Предпочтительным вариантом осуществления изобретения является применение липосомального препарата при комбинированном лечении вместе с нелипосомальным таксаном, таким как паклитаксел или его производное. Предпочтительно, паклитаксел входит в состав Кремофора EL или конъюгата альбумина. В наиболее предпочтительном варианте осуществления липосомальный препарат, содержащий DOTAP, DOPC и паклитаксел, используется при комбинированной терапии вместе с нелипосомальным таксаном, например паклитакселом или его производным.
В еще одном аспекте настоящее изобретение относится к комбинированной терапии, нелипосомальный таксан можно применять в более низкой недельной дозе, по сравнению со стандартной монотерапией. В предпочтительном варианте осуществления липосомальный препарат вводят в недельной дозе от примерно 20 мг/м2 до 50 мг/м2, а препаративную форму нелипосомального таксана вводят в недельной дозе от 25 мг/м2 до 100 мг/м2.
В предпочтительном варианте осуществления липосомальный препарат и нелипосомальный таксан вводятся один раз в неделю.
В современных схемах лечения от 80 до 150 мг/м2 нелипосомального паклитаксела вводят один раз в неделю. Доцетаксел вводят в дозе от 35 мг/м2 до 40 мг/м2 или примерно 70 мг/м2 в схеме введения один раз в неделю (Eniu et al., 2005).
В предпочтительном варианте осуществления изобретения липосомальный препарат вводят один раз в неделю в комбинации примерно с 60 мг/м2 нелипосомального паклитаксела. В другом предпочтительном варианте осуществления изобретения липосомальный препарат вводят один раз в неделю в комбинации примерно с 25-35 мг/м2 нелипосомального доцетаксела.
В наиболее предпочтительном варианте осуществления липосомальный препарат вводится один раз в неделю в дозе примерно 22 мг/м2, а нелипосомальный паклитаксел или производное вводится один раз в неделю в дозе примерно 60 мг/м2 или примерно 70 мг/м2, предпочтительно, в один и тот же день.
В наиболее предпочтительном варианте осуществления композиция используется вместе с нелипосомальной препаративной формой в 1, 8, 15, 22, 29, 36 дни цикла лечения с последующим 14-дневным интервалом без лечения, или в 1, 8, 15 дни цикла лечения с последующим 13-дневным интервалом без лечения. При желании, циклы лечения могут повторяться несколько раз, например по меньшей мере 2, 3 или 4 раза.
Липосомальный препарат можно вводить системно, предпочтительно, внутривенно. Липосомальный препарат можно вводить вместе с физиологически приемлемыми носителями, такими как буфер.
Обычно, фармацевтическая композиция поставляется в дегидратированной форме. Перед применением композицию следует гидратировать в воде с фармацевтической степенью очистки, или солевом растворе, или в другой подходящей жидкости, предпочтительно, включающей физиологически приемлемые носители, такие как буфер.
Описание чертежа
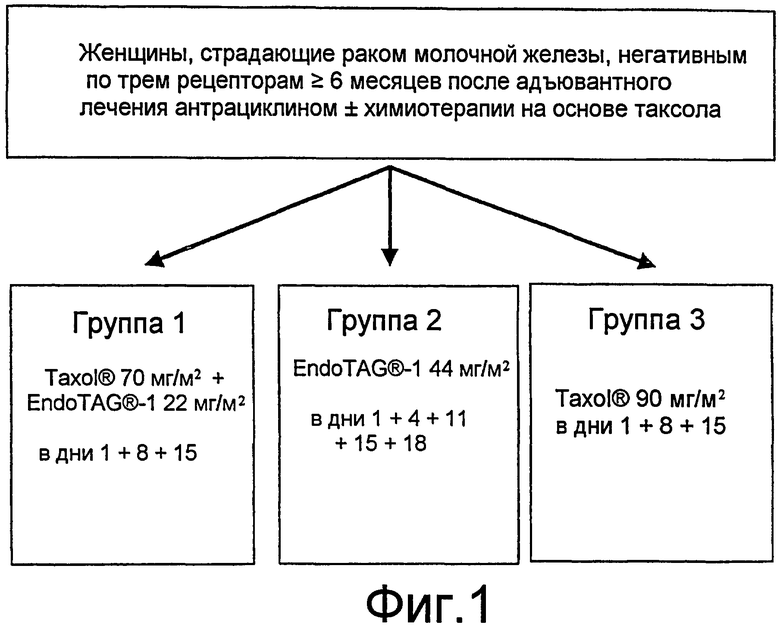
Фиг. 1
Клиническое испытание EndoTAG® при раке молочной железы, негативным по трем рецепторам.
Схематическая диаграмма схемы применения, на которой показано сравнение введения Taxol® с введением EndoTAG®-1 отдельно или в комбинации с Taxol® у женщин, страдающих раком молочной железы, негативным по трем рецепторам, которые по меньшей мере до 6 месяцев до этого получали адъювантное лечение антрациклином. Группа 1: Taxol® (70 мг/м2) в комбинации с EndoTAG®-1 (22 мг/м2 липосомального паклитаксела) вводится в 1, 8, 15 дни каждого цикла. Группа 2: EndoTAG®-1 (44 мг/м2 липосомального паклитаксела) вводится в 1, 4, 8, 11, 15, 18 дни каждого цикла. Группа 3: Taxol® (90 мг/м2) вводится в 1, 8, 15 дни каждого цикла (контрольная группа).
Примеры
Пример 1. Общий протокол лечения людей
Этот пример относится к протоколам для лечения рака молочной железы, негативного по трем рецепторам, у людей.
Катионный липосомальный препарат можно вводить в виде монотерапии или в комбинации с еще одним активным средством. Активное средство липосомального препарата и еще одно активное средство могут быть одинаковыми или различными. Средства выбраны в соответствии с несколькими факторами. Эти факторы связаны с точным физиологическим состоянием больных, лечением, которое ранее получали больные, лекарственной устойчивостью или побочными эффектами любого активного средства.
Различные элементы проведения клинического испытания, включая лечение и мониторинг больных, будут известны специалистам в данной области в свете настоящего описания.
У больных, выбранных для испытания, имеется заболевание, объективно определяемое физикальным обследованием, лабораторными методиками или рентгенологическими процедурами. У таких больных предпочтительно также в анамнезе нет клинически релевантных сердечных или почечных заболеваний, и любую химиотерапию следует прекратить по меньшей мере за 2 недели до включения в исследование.
Раскрытые препаративные формы можно вводить в течение времени вливания от короткого до среднего. Вливание, проводимое на любом уровне дозы, должно зависеть от токсичности, достигаемой после каждого вливания. Так, если после любого однократного вливания или через определенный период времени для вливания с постоянной скоростью достигалась токсичность II степени, то от введения дальнейших доз следует воздержаться, или вливание с постоянной скоростью следует прекратить, пока не снизится токсичность. Возрастающие дозы следует вводить группам больных до тех пор, пока приблизительно у 60% больных не проявится неприемлемая токсичности III или IV степени в любой категории. Дозы, которые составляют 2/3 этой величины, должны быть определены как безопасная доза.
Конечно, физикальное обследование, измерения опухоли и лабораторные тесты следует выполнять перед лечением и через интервалы примерно 3-4 недели. Лабораторные тесты должны включать полный клинический анализ крови, сывороточный креатинин, креатинкиназу, электролиты, мочевину, азот, SGOT (глутамамт-оксалоацетат аминотрансферазу сыворотки крови), билирубин, альбумин и общий сывороточный белок.
Клинические реакции можно определить приемлемой мерой или изменением лабораторных величин, например опухолевых маркеров. Например, полную реакцию можно определить исчезновением всех определяемых признаков заболевания по меньшей мере в течение месяца, тогда как частичную реакцию можно определить по уменьшению на 50% или более.
Некоторое изменение дозировки непременно произойдет, в зависимости от состояния получающего лечение индивидуума. Лицо, ответственное за введение, в любом случае определит соответствующую дозу для отдельного субъекта. Кроме того, для введения людям препараты должны соответствовать стандартам стерильности, апирогенности, общей безопасности и чистоты, как требуется Ведомством Биологических стандартов FDA (Администрации пищевых продуктов и лекарственных средств США).
Перед применением, препаративную форму можно восстановить растворением в водном растворе в случае, если препаративная форма была лиофилизирована. Как подчеркнуто выше, требуемый объем применения рассчитывается по массе тела больной и схеме дозировки. Путь введения предпочтительно включает внутрибрюшинное или парентеральное введение. Обычно введение осуществляется внутривенным путем.
Для применения в настоящем изобретении «терапевтически эффективная доза» композиции или активного средства, вводимого субъекту, будет варьироваться, в зависимости от широкого диапазона факторов. Количество будет зависеть от размера, возраста, пола, массы и состояния больной, а также от активности вводимого вещества. Указав, что имеется значительная вариабельность с точки зрения дозировки, заявители считают, что специалисты в данной области могут, используя настоящее описание, легко определить соответствующую дозировку сначала введением крайне небольших количеств, и пошагово увеличивая дозу до тех пор, пока не будет получен желаемый результат.
Пример 2. II фаза испытания, оценивающего эффективность EndoTAG®-1 у больных, страдающих раком молочной железы, негативным по трем рецепторам
2.1. Описание исследования
В настоящее время у женщин, страдающих раком молочной железы, «негативным по трем рецепторам» в отношении рецепторов эстрогена (ER), прогестерона (PgR) и HER-2/neu (HER-2), имеется небольшое количество вариантов лечения. Статус «опухоли, негативной по трем рецепторам» связан с неблагоприятным прогнозом у больных с ранней стадией рака молочной железы. Термин «опухоль, негативная по трем рецепторам» в настоящее время используется в качестве клинического суррогата «подобного базальному» рака молочной железы: 80% раковых опухолей, негативных по трем рецепторам, являются «подобными базальному». «Подобные базальным» раковые опухоли представляют собой особый подтип раковых опухолей молочной железы, определяемых профилированием генной экспрессии (Brenton et al., 2005; Sotiriou et al., 2003; Sorlie et al., 2001).
2.2. Структура исследования
Всего 135 больных, страдающих раком молочной железы, негативным по трем рецепторам, и соответствующих критериям включения в исследование, методом случайной выборки были включены в одну из следующих групп лечения:
- группа 1: Taxol® (70 мг/м2) в комбинации с Endo TAG®-1 (22 мг/м2 липосомального паклитаксела) на 1, 8, 15 дни каждого цикла с последующим 13-дневным интервалом без лечения.
- Группа 2: монотерапия Endo TAG®-1 (44 мг/м2 липосомального паклитаксела) на 1, 4, 8, 11, 15, 18 дни каждого цикла с последующим 10-дневным интервалом без лечения.
- Группа 3: монотерапия Taxol® (70 мг/м2) на 1, 8, 15 дни каждого цикла с последующим 13-дневным интервалом без лечения (контрольная группа).
Рандомизацию выполняют для достижения соотношения 2:2:1 между группами лечения и стратифицируют по адъювантному лечению одним антрациклином или антрациклином + Taxol®.
Каждый цикл лечения включает 3 недели лечения с последующей 1 неделей отдыха, т.е. всего 4 недели.
Больные будут сначала получать лечение минимально в течение 4 циклов. После оценки реакции опухоли, безопасно реагирующие на лечение (т.е. CR, PR и SD), имеют вариант продолжения лечения до возникновения PD или неприемлемой токсичности.
Всех больных лечат до прогрессирования заболевания или токсичности и наблюдением для определения выживания.
2.3. Цели
Первичная цель: оценить эффективность Endo TAG®-1 + Taxol® (комбинированной терапии) и Endo TAG®-1 (монотерапии) в качестве неотложной терапии больных, страдающих раком молочной железы, негативным по трем рецепторам, устойчивым к лечению антрациклином ± Taxol®.
Вторичная цель: оценить безопасность и переносимость Endo TAG®-1 + Taxol® (комбинированной терапии) и Endo TAG®-1 (монотерапии) у этой популяции больных.
2.4. Исходы
Первичные исходы эффективности:
- частота 4-месячного выживания без выживания (PFS), рассчитанная частотой у рандомизированных больных, у которых не выявляется прогрессирование заболевания, и которые живы через 16 недель после первого вливания исследуемого препарата.
Вторичные исходы эффективности:
- медиана времени PFS.
Реакция опухоли (CR/PR/SD/PD) на 8, 16 и 24 неделе
Количество больных, реагирующих на лечение, т.е. объективная реакция (OR = Полная реакция (CR) + Частичная реакция (PR)).
Количество больных со стабильным заболеванием (SD).
Медиана длительности объективной реакции и стабильного заболевания.
Частота 4-месячного выживания, рассчитанная по частоте рандомизированных больных, живущих через 16 недель после первого вливания исследуемого препарата.
Медиана общего времени выживания (OS)
Оценка боли (VAS)
Средняя величина изменения в неделю от исходного уровня к концу лечения исследуемым лекарственным средством.
Процент больных с улучшением по меньшей мере на 10 мм от исходного уровня во время лечения исследуемым лекарственным препаратом.
Процент больных с ухудшением по меньшей мере на 10 мм от исходного уровня во время лечения исследуемым лекарственным препаратом.
Оценка клинической выгоды по шкале качества жизни (QoL) (Анкета EORTC-QoL-C30)
Средняя величина изменения в неделю от исходного уровня к концу лечения исследуемым лекарственным средством.
Процент больных с улучшением по меньшей мере на 10 пунктов от исходного уровня во время лечения исследуемым лекарственным препаратом.
Процент больных с ухудшением по меньшей мере на 10 пунктов от исходного уровня во время лечения исследуемым лекарственным препаратом.
Исходы безопасности:
Побочные явления: частота и процентная доля больных с побочными эффектами, возникшими в результате лечения.
Лабораторные величины: количество клинически значимых лабораторных величин.
Изменение дозы: процентная доля больных, имеющих высокое снижение дозы, задержек или прекращения введения исследуемого лекарственного средства.
2.5. Количество субъектов/пациенток
135 женщин, страдающих локально рецидивирующим и/или метастатическим, ранее леченным антрациклином ± Taxol® химиотерапией раком молочной железы, негативным по трем рецепторам, рандомизируют в соотношении 2:2:1 (54 больных с комбинированной терапией Endo TAG®-1 + Taxol®, 54 больных с монотерапией Endo TAG®-1 и 27 больных с монотерапией Taxol®).
2.6. Критерии включения
1. Гистологически доказанный биопсией опухоли рак молочной железы, негативный по трем рецепторам.
2. Гормональный статус, отрицательный по эстрогену (ER), прогестерону (PR) и HER2.
3. Возраст ≥18 лет.
4. Опухолевые поражения, в соответствии с критериями RCIT.
5. Отсутствие лактации или беременности у больных.
6. Статус выполнения 0-2 ECOG.
7. Минимум 6 месяцев после предыдущей системной химиотерапии антрациклином при адъювантной схеме отдельно или в комбинации с химиотерапией.
8. Нормальная сердечная функция (оценка LVEF MUGA сканом или эхокардиографией выше нижнего предела нормы для учреждения).
9. Адекватная функция органов (по данным определения нейтрофилов ≥1,5×109/л, тромбоцитов ≥100×109/л, гемоглобина ≥10 г/дкл, общего билирубина ≤1,5 UNL, ASAT (SGOT) и ALAT (SGPT) ≤2,5 UNL, щелочной фосфатазы ≤2,5 UNL, креатинина ≤150 мкмоль/л (1,5 мг/дкл).
10. Отсутствие другого следующего тяжелого заболевания или медицинского состояния: а) отечной сердечной недостаточности или нестабильной стенокардии, предшествующего анамнеза инфаркта миокарда в пределах 1 года от момента включения в исследование, неконтролируемой гипертонии или высокого риска неконтролируемых аритмий; b) анамнеза активного или значительного неврологического расстройства и/или психиатрического расстройства, которое препятствовало бы пониманию и предоставлению информированного согласия, а также помешало бы клинической и рентгенологической оценке центральной нервной системы во время испытания; с) активной неконтролируемой инфекции; d) активной язвенной болезни, нестабильного сахарного диабета.
11. Отсутствие прошлого или текущего анамнеза другого новообразования, кроме излеченных: а) базальноклеточного рака кожи, b) карциномы шейки матки in situ.
12. Отсутствие одновременного лечения другими экспериментальными препаратами. Участие в другом клиническом испытании с каким-либо исследуемым не поступающим в продажу препаратом в пределах 30 дней до включения в исследование.
13. Письменное информированное согласие.
2.7. Введение лекарственного препарата
Endo TAG®-1 + Taxol должны вводиться внутривенно.
Endo TAG®-1 должен вводиться первоначально в дозе 0,5 мл/мин. Через 15 мин скорость введения должна увеличиться до 1,0 мл/мин, и еще через 15 мин скорость введения будет установлена на 1,5 мл/мин.
2.8. Исход первичной эффективности
Первичным исходом является скорость PFS через 16 недель в плече комбинированного лечения Endo TAG®-1 + Taxol®.
Гипотеза H0: p ≤30% в сравнении с H1: p≥50% испытана в плече комбинированного лечения с использованием одноэтапной структуры при уровне значимости α=0,05.
Если действительная реакция опухоли составляет 50% при лечении Taxol® + Endo TAG®-1, то тест будет иметь степень 1-β=0,90.
Такая же гипотеза будет испытана для монотерапии Endo TAG®-1.
Пример 3. Применение Endo TAG-1 в комбинации с Taxotere®
3.1. Обоснование лечения
Женщин, страдающих «негативным по трем рецепторам», местно рецидивирующим и/или метастатическим раком молочной железы, ранее леченным химиотерапией антрациклином ± Taxotere®, лечат еженедельной комбинированной терапией Endo TAG-1 в комбинацией с Taxotere®. Taxotere® включает препарат доцетаксел в качестве активного фармацевтического ингредиента.
3.2. Критерии, определяющие минимальные требования к включению в исследование
- Гистологически доказанный рак молочной железы биопсией опухоли.
- Отрицательный гормональный статус по эстрогенам (ER), прогестерону (PR) и HER2, как показано IHC, ферментным анализом или FISH.
- Отсутствие лактирующих или беременных больных.
- Минимум 6 месяцев после предшествующей системной антрациклиновой химиотерапии по адъювантной схеме.
- Нормальная сердечная функция (оценка LVEF MUGA сканом или эхокардиографией выше нижнего предела нормы для учреждения).
- Адекватная функция органов (по данным определения нейтрофилов 1,5×109/л, тромбоцитов 100×109/л, гемоглобина 10 г/дкл, общего билирубина ≤1,5 UNL, ASAT (SGOT) и ALAT (SGPT) 2,5 UNL, щелочной фосфатазы 2,5 UNL, креатинина 150 мкмоль/л (1,5 мг/дкл).
3.3. Схема лечения
- Endo TAG®-1 вводят в дозе 22 мг/м2 липосомального паклитаксела в 1, 8, 15, 22, 29, 36 дни каждого цикла с последующим 14-дневным интервалом без лечения.
- Taxotere® вводится в дозе 30 мг/м2 доцетаксела в 1, 8, 15, 22, 29, 36 дни каждого цикла с последующим 14-дневным интервалом без лечения.
- Оба препарата вводятся внутривенно.
- Больных лечат до прогрессирования заболевания или развития токсичности.
Все композиции и способы, раскрытые и заявленные в настоящем документе, можно изготовить и провести без ненужного экспериментирования в свете настоящего описания. Хотя композиции и способы по настоящему изобретению были описаны с точки зрения предпочтительных вариантов осуществления, для специалистов в данной области будет очевидно, что в композиции, способы и стадии или в последовательность стадий описанного в настоящем документе способа можно внести изменения без отхода от концепции, сущности и объема изобретения. Конкретнее, будет очевидно, что определенные средства, которые и химически, и физиологически связаны, можно заменить на средства, описанные в настоящем документе, хотя могут достигаться такие же или подобные результаты. Предполагается, что все такие аналогичные замещения и модификации, очевидные для специалистов в данной области, находятся в пределах сущности, объема и концепции изобретения, определенного прилагаемой формулой изобретения.
ССЫЛКИ
Bernard-Marty, С., Cardoso, F., and Piccart, M.J. (2004). Facts and controversies in systemic treatment of metastatic breast cancer. Oncologist 9, 617-632.
Brenton, J.D., Carey, L.A., Ahmed, A.A., and Caldas, C. (2005). Molecular classification and molecular forecasting of breast cancer: ready for clinical application? J Clin Oncol 23, 7350-7360.
Chan, S., Davidson, N., Juozaityte, E., Erdkamp, F., Pluzanska, A., Azarnia, N., and Lee, L.W. (2004). Phase III trial of liposomal doxorubicin and cyclophosphamide compared with epirubicin and cyclophosphamide as first-line therapy for metastatic breast cancer. Ann Oncol 15, 1527-1534.
Chebil, G., Bendahl, P.O., Idvall, I., and Ferno, M. (2003). Comparison of immunohistochemical and biochemical assay of steroid receptors in primary breast cancer-clinical associations and reasons for discrepancies. Acta Oncol 42, 719-725.
Eniu, A., Palmieri. F.M., and Perez, E.A. (2005). Weekly administration of docetaxel and paclitaxel in metastatic or advanced breast cancer. Oncologist 10, 665-685.
Felgner, J.H., Kumar, R., Sridhar, C.N, Wheeler, C.J., Tsai, Y.J., Border, R., Ramsey, P., Martin, M., and Felgner, P.L. (1994). Enhanced gene delivery and mechanism studies with a novel series of cationic lipid formulations. J Biol Chem 269, 2550-2561.
Gradishar, W.J. (2004). Tamoxifen - what next? Oncologist 9, 378-384.
Kallioniemi, O.P., Kallioniemi, A., Kurisu, W., Thor, A., Chen, L.C., Smith, H.S., Waldman, F.M., Pinkel, D., and Gray, J.W. (1992). ERBB2 amplification in breast cancer analyzed by fluorescence in situ hybridization. Proc Natl Acad Sci USA 89, 5321-5325.
Keller, A.M., Mennel, R.G., Georgoulias, V.A., Nabholtz, J.M., Erazo, A., Lluch, A., Vogel, C.L., Kaufmann, M., von Minckwitz, G., Henderson, I.C., et al. (2004). Randomized phase III trial of pegylated liposomal doxorubicin versus vinorelbine or mitomycin C plus vinblastine in women with taxane-refractory advanced breast cancer. J Clin Oncol 22, 3893-3901.
O'Shaughnessy, J. (2005). Extending survival with chemotherapy in metastatic breast cancer. Oncologist 10 Suppl 3, 20-29.
Prowell, Т.M., and Davidson, N.E. (2004). What is the role of ovarian ablation in the management of primary and metastatic breast cancer today? Oncologist 9, 507-517.
Schaller, G., Evers, K., Papadopoulos, S., Ebert, A., and Buhler, H. (2001). Current use of HER2 tests. Ann Oncol 12 Suppl 1, S97-100.
Slamon, D.J., Clark, G.M., Wong, S.G., Levin, W.J., Ullrich, A., and McGuire, W.L. (1987). Human breast cancer: correlation of relapse and survival with amplification of the HER-2/neu oncogene. Science 235, 177-182.
Solodin, I., Brown, C.S., Bruno, M.S., Chow, C.Y., Jang, E.H., Debs, R.J., and Heath, T.D. (1995). A novel series of amphiphilic imidazolinium compounds for in vitro and in vivo gene delivery. Biochemistry 34, 13537-13544.
Sorlie, Т., Perou, C.M., Tibshirani, R., Aas, T., Geisler, S., Johnsen, H., Hastie, Т., Eisen, M.B., van de Rijn, M., Jeffrey, S.S., et al. (2001). Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications. Proc Natl Acad Sci USA 98, 10869-10874.
Sotiriou, C., Neo, S.Y., McShane, L.M., Korn, E.L., Long, P.M., Jazaeri, A., Martiat, P., Fox, S.В., Harris, A.L., and Liu, E.T. (2003). Breast cancer classification and prognosis based on gene expression profiles from a population-based study. Proc Natl Acad Sci USA 100, 10393-10398.
Yamashita, H., Yando, Y., Nishio, M., Zhang, Z., Hamaguchi, M., Mita, K., Kobayashi, S., Fujii, Y., and Iwase, H. (2006). Immunohistochemical evaluation of hormone receptor status for predicting response to endocrine therapy in metastatic breast cancer. Breast Cancer 73, 74-83.
Заявленная группа изобретений относится к медицине, а именно к онкологии, и может быть использована для лечения рака молочной железы, отрицательного по трем рецепторам, а также для изготовления комбинации для его лечения. Для этого вводят катионный липосомальный препарат, содержащий, по меньшей мере, один катионный липид, антимитотическое средство и, по меньшей мере, один нейтральный и/или анионный липид за один или более циклов в общем количестве, эффективном для лечения субъекта. При использовании данных изобретений достигается более эффективное лечения рака за счет синергического эффекта при введении паклитаксела в липосомальной и нелипосомальной формах. 2 н. и 16 з.п., 1 ил., 3 пр.
1. Применение катионного липосомального препарата, содержащего, по меньшей мере, один катионный липид, антимитотическое средство и, необязательно, по меньшей мере один нейтральный и/или анионный липид, для получения фармацевтической композиции для лечения рака молочной железы, негативного по рецептору эстрогена (ER), рецептору прогестерона (PgR) и рецептору эндотелиального фактора роста 2 типа (HER-2) у человека или животного.
2. Применение по п.1, где указанный катионный липосомальный препарат содержит по меньшей мере один катионный липид в количестве примерно от 30 мол.% до примерно 99,9 мол.%, антимитотическое средство в количестве по меньшей мере примерно 0,1 мол.% и, необязательно, по меньшей мере один нейтральный и/или анионный липид в количестве примерно от 0 мол.% до примерно 70 мол.%.
3. Применение по п.1, где указанное антимитотическое средство представляет собой таксан, предпочтительно паклитаксел или его производное.
4. Применение по п.1 или 2, где указанный катионный липосомальный препарат содержит DOTAP (соли N-[1-(2,3-диолеоилокси)пропил]-N,N,N-триметиламмония, например метилсульфат), DOPC (1,2-диолеоил-фосфатидилхолин или 1,2-диолеоил-зп-глицеро-3-фосфатидилхолин) и паклитаксел.
5. Применение по п.1 для введения терапевтически эффективной дозы по меньшей мере один раз в неделю.
6. Применение по п.1 для введения терапевтически эффективной дозы один или два раза в неделю.
7. Применение по п.1 для введения одной дозы от 1 мг/м2 до 50 мг/м2 на введение.
8. Применение по п.1 для введения одной дозы от 20 мг/м2 до 50 мг/м2 на введение, предпочтительно 22 мг/м2 или 44 мг/м2.
9. Применение по п.1 для введения одной дозы 44 мг/м2 дважды в неделю.
10. Применение по п.1, где композиция предназначена для одновременной, раздельной или последовательной комбинированной терапии эффективной дозой по меньшей мере еще одного активного средства и/или теплом, и/или облучением.
11. Применение по п.10, где еще одно активное средство включено в состав композиции в виде нелипосомального препарата.
12. Применение по п.11, где указанное дополнительное активное средство представляет собой цитотоксическое или цитостатическое вещество, такое как вещество, обладающее противоопухолевой активностью или активностью против эндотелиальных клеток, химиотерапевтическое средство, иммунологически активное вещество, соединение, которое снижает или устраняет реакции гиперчувствительности, или хемосенсибилизатор.
13. Применение по п.11, где указанное дополнительное активное средство выбрано из антинеопластических средств, в частности антимитотических средств, подобных таксанам, таким как паклитаксел или его производные, алкилирующие средства, в частности, включающие платину соединения, подобные цисплатину или карбоплатину, средства, ингибирующие ДНК топоизомеразу, подобные камптотецину, антрациклины, подобные доксорубицину, антиметаболиты РНК/ДНК, в частности 5-фторурацил, гемцитабин или капецитабин.
14. Применение по п.10 для введения композиции в еженедельной дозе от 20 мг/м2 до 50 мг/м2 и для введения нелипосомального таксана в еженедельной дозе от 20 мг/м2 до 100 мг/м2.
15. Применение по п.10 для введения композиции и еще одного дополнительного средства один раз в неделю.
16. Применение по п.10 для введения композиции один раз в неделю в дозе примерно 22 мг/м2 и для введения нелипосомального паклитаксела или его производного один раз в неделю в дозе примерно 70 мг/м2.
17. Комбинация
(a) катионного липосомального препарата, содержащего по меньшей мере один катионный липид в количестве примерно от 30 мол.% до примерно 99,9 мол.%, таксан в количестве по меньшей мере примерно 0,1 мол.% и по меньшей мере один нейтральный и/или анионный липид в количестве от примерно 0 мол.% до примерно 70 мол.%, и
(b) нелипосомального препарата, содержащего антимитотическое средтво, для одновременного, раздельного и/или последовательного введения человека или животному, для лечения рака.
18. Комбинация по п.17, в котором указанный катионный липосомальный препарат содержит DOTAP, DOPC и паклитаксел.
| WO 2005039533 A1, 06.05.2005 | |||
| RU 22240319 C2, 10.06.2002 | |||
| ЛОПУХИН Ю.М | |||
| Под ред | |||
| «Хирургия» рук-во для врачей и студентов // М.: ГЭОТАР-Медицина, 1997, с.684, 685 | |||
| CARDOZO F | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2012-04-27—Публикация
2007-03-16—Подача