Изобретение относится к способу получения фосфористой кислоты, которая находит широкое применение в производстве различных фосфорсодержащих соединений, применяемых в качестве комплексонов, восстановителей, стабилизаторов полимеров, биологически активных соединений.
Американской компанией «Монсанто» разработан ряд способов получения фосфористой кислоты из элементного (белого, желтого) фосфора. Описано электролитическое получение фосфористой кислоты из белого фосфора [US 4021321, опубл. 3.05.1977; US 4021322, опубл. 3.05.1977]. Недостатком этого способа является то, что образующаяся в процессе фосфористая кислота загрязнена примесями фосфорной кислоты и хлора и требует дополнительной очистки, а образующаяся при гидролизе в качестве побочного продукта соляная кислота обладает коррозионной активностью. Способ также требует значительной затраты электроэнергии.
Известен способ получения фосфористой кислоты окислением элементного фосфора водяным паром в газовой фазе [CA 2013221, опубл. 1.02.1990] или газовой плазме [CA 2070949, опубл. 11.12.1993]. Недостатками данных методов являются проведение процесса при высоких температурах (более 1000°C, 1500-2500°C), что требует специальных мер предосторожности при работе с элементным (белым) фосфором, а также образование побочных продуктов полимеризации элементного (белого) фосфора - образование красного фосфора.
Известен способ получения фосфористой кислоты из фосфорсодержащего шлама, образующегося при производстве желтого фосфора [RU 2096318, опубл. 20.11.1997]. Недостатком данного метода является использование большого количества концентрированной азотной кислоты и йода.
Известен способ получения фосфористой кислоты по реакции элементного (белого, желтого) фосфора с гидроксидами бария и кальция в присутствии основания и воды [RU 2179152, опубл. 10.02.2002]. Хотя в условиях данного процесса не происходит выделения ядовитого фосфина, образование больших количеств нерастворимых сульфатов кальция и бария и использование избытка коррозионно-опасной разбавленной серной кислоты являются недостатками предлагаемого способа.
Известен способ получения смеси фосфорсодержащих кислот в условиях каталитического окисления элементного (белого, желтого) фосфора под действием благородных металлов, таких как палладий и некоторые другие металлы VIII группы [US 6476256, опубл. 5.11.2002]. Недостатками данного процесса является образование смеси фосфорсодержащих кислот, низкие выходы фосфористой кислоты (до 57.4% в смеси с другими кислотами), образование токсичного фосфина и гетерогенное протекание процесса, так как элементный (белый) фосфор не растворим в водной среде. Для повышения выхода фосфористой кислоты в данном методе необходимо использование специального автоклава и повышение температуры до 90-150°C.
Перечисленные технические решения являются аналогами настоящего изобретения. Наиболее близким к заявляемому изобретению является способ получения фосфористой кислоты взаимодействием органического комплекса палладия - бис(трифенилфосфин) палладийдибромида с элементным (белым) фосфором в присутствии NaBPh4, с последующим гидролизом реакционной смеси [Известия академии наук. Серия химическая, 2010, 59(6), 1094-1096], позволяющий получать фосфористую кислоту из элементного фосфора в выходом до 75%. Однако данный способ требует проведения дополнительного процесса активации используемого комплекса палладия, что приводит к загрязнению полученного продукта примесями бромида натрия. Образующаяся фосфористая кислота загрязнена примесями фосфорной и пирофосфорной кислот, составляющих до 40%, а присутствие трифенилфосфина в реакционной среде приводит к образованию дополнительных фосфорорганических примесей в результате его частичного окисления.
Задачей изобретения является создание нового экологически безопасного, промышленно-приемлемого и селективного способа получения фосфористой кислоты исходя из простых и доступных реагентов (P4, H2O, органический комплекс палладия) с высоким выходом, расширяющего ассортимент известных способов получения фосфористой кислоты.
Технический результат - новый селективный способ получения фосфористой кислоты с выходом до 90%
Технический результат достигается заявляемым способом получения фосфористой кислоты из белого фосфора взаимодействием органического комплекса палладия - трис(дибензилиденацетон)дипалладия с белым фосфором в среде тетрагидрофурана с последующим гидролизом при температуре 20-70°C образовавшихся фосфидов палладия дегазированной водой при следующем мольном соотношении реагентов - комплекс палладия: белый фосфор: вода 1:(1-20):(12-480) и выделением целевого продукта отделением осадка и упариванием фильтрата в вакууме.
На основании данных ЯМР 31Р-спектроскопии установлено, что при реализации заявляемого способа происходит образование одного продукта - фосфористой кислоты. Так, в спектре ЯМР 31Р{-}, снятом с полученного продукта, наблюдается дублет с химическим сдвигом +3.8 м.д. и константой взаимодействия фосфор-водород 1JPH=667 Гц.
Химический процесс, заложенный в основу предлагаемого способа, включает реакцию трис(дибензилиденацетон)дипалладия [Pd2(dbа)3] с белым фосфором в среде тетрагидрофурана с последующим гидролизом образовавшихся фосфидов палладия дегазированной водой (схема 1):
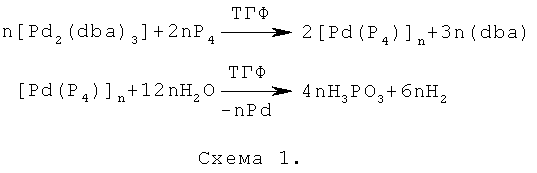
После гидролиза выделение целевого продукта включает отделение осадка соединения палладия, упаривание фильтрата в вакууме масляного насоса и (при необходимости) дополнительную очистку перекристаллизацией [Руководство по неорганическому синтезу. Т.2. Пер. с нем. / Под ред. Г. Брауэра. - М.: Мир. 1985. - С.580-581]. Суммарно процесс получения фосфористой кислоты из элементного фосфора в присутствии комплекса палладия [Pd2(dbа)3] представлен на схеме 2:
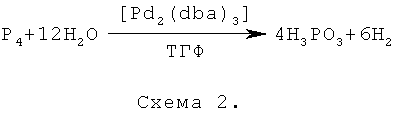
Следующие примеры иллюстрируют осуществление изобретения. Все эксперименты проводились в инертной атмосфере азота при использовании стандартной аппаратуры Шленка. Белый фосфор хранился под слоем воды и непосредственно перед экспериментом промывался последовательно ацетоном, этиловым спиртом и эфиром с последующей осушкой в вакууме, 0.05М раствор белого фосфора в ТГФ готовился растворением навески P4 в соответствующем объеме растворителя. Органический комплекс палладия [Pd2(dbа)3] использован производства фирмы Alfa Aesar (№12760). Спектры ЯМР 31P сняты на ЯМР спектрометре Avance DRX-400 фирмы Bruker на частоте 161.97 МГц. Для наглядности условия получения фосфористой кислоты из белого фосфора по примерам 1-11 обобщены в таблице.
Пример 1.
К раствору, содержащему 54.9 мг (0.06 ммоль) комплекса [Pd2(dbа)3] в 5 мл ТГФ, медленно прикапывают 1.2 мл 0.05М раствора белого фосфора в ТГФ, содержащего 7.4 мг (0.06 ммоль) Р4. После добавления раствора белого фосфора наблюдают образование черного аморфного осадка фосфидов палладия, который при перемешивании в течение 1 часа приобретает кристалличность. После этого к реакционной смеси добавляют 13 мкл (0.72 ммоль) дегазированной воды, перемешивают при комнатной температуре (20°C) в течение 10 часов, отделяют осадок соединения палладия, а фильтрат упаривают в вакууме масляного насоса и получают 12.8 мг фосфористой кислоты H3PO3 в виде бесцветного мелкокристаллического гигроскопичного осадка с температурой плавления 70°C (ЯМР 31P, ТГФ, C6D6-кaпилляp, δ, 3.8 м.д. (д.), 1JPH=667 Гц). Выход - 65%.
Пример 2.
Способ осуществляют в условиях примера 1, но используют 2.4 мл 0.05М раствора белого фосфора, содержащего 14.8 мг (0.12 ммоль) P4 и 26 мкл (1.44 ммоль) дегазированной воды. Получено 20.9 мг H3PO3. Выход - 53%.
Пример 3.
Способ осуществляют в условиях примера 2, но при температуре 50°C. Получено 28.3 мг H3PO3. Выход - 72%.
Пример 4.
Способ осуществляют в условиях примера 1, но используют 12.0 мл 0.05М раствора белого фосфора, содержащего 74.0 мг (0.6 ммоль) Р4 и 0.13 мл (7.2 ммоль) дегазированной воды. Получено 94.5 мг H3PO3. Выход - 48%.
Пример 5.
Способ осуществляют в условиях примера 1, но используют 24.0 мл 0.05М раствора белого фосфора, содержащего 148 мг (1.2 ммоль) P4 и 0.26 мл (14.4 ммоль) дегазированной воды. Получено 173.2 мг H3PO3. Выход - 44%.
Пример 6.
Способ осуществляют в условиях примера 2, но используют 0.26 мл (14.4 ммоль) дегазированной воды. Получено 30.3 мг H3PO3. Выход - 77%.
Пример 7.
Способ осуществляют в условиях примера 6, но при температуре 50°C. Получено 33.1 мг H3PO3. Выход - 84%.
Пример 8.
Способ осуществляют в условиях примера 6, но при температуре 70°C. Получено 35.4 мг H3PO3. Выход - 90%.
Пример 9.
Способ осуществляют в условиях примера 6, но используют 0.52 мл (28.9 ммоль) дегазированной воды. Получено 18.9 мг H3PO3. Выход - 48%.
Пример 10.
Способ осуществляют в условиях примера 9, но при температуре 50°C. Получено 19.3 мг H3PO3. Выход - 49%.
Пример 11.
Способ осуществляют в условиях примера 9, но при температуре 70°C. Получено 22.8 мг H3PO3. Выход - 58%.
Эксперименты проведены при следующих мольных соотношениях реагентов: комплекс [Pd2(dbа)3]: белый фосфор: вода 1:(1-20):(12-480). Указанные соотношения достаточны для получения целевого продукта, и как видно из данных таблицы, наилучшие выходы фосфористой кислоты (примеры 6-8) достигаются при мольном соотношении комплекс [Pd2(dbа)3]: белый фосфор 1:2. Повышение количества используемой воды, т.е. более 120 моль на 1 моль фосфора, приводит к образованию разбавленных растворов и затрудняет выделение продукта и, в конечном счете, к снижению выхода. Установлено, что температура, при которой проводится гидролиз образующихся фосфидов палладия, также влияет на выход целевого продукта. Оптимальные условия осуществления способа таковы:
- молярное соотношение комплекс [Pd2(dbа)3]: белый фосфор: вода 1:2:240;
- гидролиз при температуре 50-70°C.
Таким образом, предлагаемый способ получения фосфористой кислоты из белого фосфора является экологически безопасным, т.к. не происходит образование побочных продуктов, в том числе ядовитого фосфина, экономичным, т.к процесс протекает в гомогенных условиях при комнатной температуре или нагревании до 70°C, является селективным (происходит образование фосфористой кислоты в качестве единственного продукта), основан на простых и доступных исходных реагентах (белый фосфор, H2O, коммерчески доступный комплекс палладия) с выходом целевого продукта до 90%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА КОНЦЕНТРИРОВАННОЙ ФОСФОРИСТОЙ КИСЛОТЫ | 2009 |
|
RU2525424C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРИСТОЙ КИСЛОТЫ (ВАРИАНТЫ) | 2000 |
|
RU2179152C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРИВИТЫХ СИЛОКСАНОВЫХ ПОКРЫТИЙ С СОРБЦИОННЫМИ N-АМИНОДИ(МЕТИЛЕНФОСФОНОВЫМИ) ГРУППАМИ НА ВОЛОКНАХ И МОДИФИЦИРОВАННЫЕ ВОЛОКНИСТЫЕ МАТЕРИАЛЫ | 2014 |
|
RU2556932C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИФОСФОНОВЫХ КИСЛОТ И ИХ СОЛЕЙ | 2007 |
|
RU2425049C2 |
| СПОСОБЫ ИЗВЛЕЧЕНИЯ ОТРАБОТАННЫХ МЕТАНСУЛЬФОНОВОЙ И ФОСФОРИСТОЙ КИСЛОТ И ИХ СУХАЯ СМЕСЬ | 1995 |
|
RU2152950C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ТИЕНОПИРИМИДИНА | 2013 |
|
RU2637309C2 |
| БИ-АРИЛ-МЕТА-ПИРИМИДИНОВЫЕ ИНГИБИТОРЫ КИНАЗ | 2006 |
|
RU2597364C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА ОТЛОЖЕНИЙ МИНЕРАЛЬНЫХ СОЛЕЙ | 1998 |
|
RU2133751C1 |
| СПОСОБ ПОЛУЧЕНИЯ О-ХЛОРАНИЛИНА (ВАРИАНТЫ) | 2014 |
|
RU2556222C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ СТИМУЛИРОВАНИЯ ГЕМОПОЭЗА | 2011 |
|
RU2482869C1 |
Изобретение относится к способу получения фосфористой кислоты и может быть использовано в химической промышленности. Осуществляют взаимодействие органического комплекса палладия - трис(дибензилиденацетон)дипалладия с белым фосфором в среде тетрагидрофурана. Образовавшиеся фосфиды палладия подвергают гидролизу при температуре 20-70°C дегазированной водой. Мольное соотношение реагентов комплекс палладия: белый фосфор: вода составляет 1:(1-20):(12-480). Целевой продукт выделяют отделением осадка и упариванием фильтрата в вакууме. Способ является экологически безопасным, селективным и позволяет получать фосфористую кислоту из простых и доступных реагентов с высоким выходом. 2 з.п. ф-лы, 1 табл., 11 пр.
1. Способ получения фосфористой кислоты из белого фосфора, включающий взаимодействие органического комплекса палладия с белым фосфором в среде тетрагидрофурана с последующим гидролизом образовавшихся фосфидов палладия дегазированной водой и выделение целевого продукта, отличающийся тем, что в качестве органического комплекса палладия используют трис(дибензилиденацетон)дипалладий при следующем мольном соотношении реагентов: комплекс палладия: белый фосфор: вода 1:(1-20):(12-480).
2. Способ получения фосфористой кислоты по п.1, отличающийся тем, что гидролиз проводят при температуре 20-70°C.
3. Способ получения фосфористой кислоты по п.1, отличающийся тем, что выделение целевого продукта включает отделение осадка и упаривание фильтрата в вакууме.
| КАГИРОВ P.M | |||
| и др | |||
| Активация и трансформация молекулы белого фосфора под действием комплексов палладия (II) | |||
| - Известия Академии Наук | |||
| Серия химическая, 2010, 59(6), с.1094-1096 | |||
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРИСТОЙ КИСЛОТЫ (ВАРИАНТЫ) | 2000 |
|
RU2179152C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРИСТОЙ КИСЛОТЫ | 1991 |
|
RU2022918C1 |
| Способ получения фосфористой кислоты | 1980 |
|
SU935476A1 |
| US 3458281 А, 29.07.1969. | |||
Авторы
Даты
2012-09-10—Публикация
2011-02-25—Подача