Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики гриппозной инфекции, вызванной эпидемическим штаммом вируса гриппа. Профилактику осуществляют интраназальной живой гриппозной вакциной (ЖГВ) из штамма вируса гриппа А, семейства Orthomyxoviridae, рода Influenzavirus А - А/17/Новая Каледония/99/76(H1N1).
В настоящее время для получения реассортантных вакцинных штаммов для включения в состав ЖГВ для иммунизации взрослых и детей от 3-х лет применяется холодоадаптированный (ХА) донор аттенуации А/Ленинград/134/17/57(H2N2) [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. - Л., 1986. - С.66-83], который является хорошо охарактеризованным и документировано безвредным для людей. Известен вакцинный штамм А/17/Новая Каледония/99/145(H1N1) на основе донора аттенуации А/Ленинград/134/17/57(H2N2) [патент №2183672, опубл. 20.06.02], предназначенный для производства ЖГВ для взрослых и детей от 3-х лет.
Задачей, на решение которой направлено заявляемое изобретение, является получение нового реассортантного вакцинного штамма А/17/Новая Каледония/99/76(H1N1), предназначенного для иммунизации взрослых и детей, включая детей 1-2-х лет, полученного на основе штамма A/Mocква/21/17/65(H2N2) в качестве ХА донора аттенуации.
Использование в качестве источника поверхностных антигенов эпидемического вируса А/Новая Каледония/20/99(H1N1) и его реассортация с ХА штаммом A/Mocква/21/17/65(H2N2) в качестве донора аттенуации привели к получению вакцинного кандидата антигенной разновидности A(H1N1).
В настоящее время вакцинные штаммы ЖГВ получают методом реассортации современных эпидемических вирусов с холодоадаптированными (ХА) донорскими штаммами, в результате чего образуются реассортанты, имеющие смешанный геном. Гены, кодирующие гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального эпидемического штамма, а шесть генов внутренних и неструктурных белков (РВ2, РВ1, PA, NP, М, NS) - от безвредного ХА донора аттенуации. Донорский штамм A/Mocква/21/17/65(H2N2), использованный для реассортации, был получен после ряда пассажей при пониженной температуре стандартного (пассажного) вакцинного штамма A/Москва/21/65(H2N2) [Александрова Г.И. Дисс.…доктора мед наук. - Л., 1969. - 419 с.]. Штамм A/Mocква/21/17/65(H2N2) характеризуется документированной безвредностью и высокой иммуногенностью для детей от 1 года (2% реактогенности, 60-70% иммуногенности), что было неоднократно подтверждено за время его использования как в виде моновакцины, так и в составе дивакцины в 1960-х годах XX века [Г.И.Александрова. В кн.: Иммунология и специфическая профилактика гриппа у детей. - Л., 1971. - С.21-45].
Проведенный с помощью прямого нуклеотидного секвенирования молекулярный анализ генов внутренних и неструктурных белков штамма A/Mocква/21/17/65(H2N2) показал, что в процессе 17 пассажей при пониженной температуре штамм приобрел 8 нуклеотидных замен в генах внутренних и неструктурных белков по сравнению с вариантом A/Mocква/21/65(H2N2), который до этого пассировали при оптимальной температуре. Из этих восьми нуклеотидных замен шесть являются значащими и приводят к аминокислотным замещениям в РВ2 белке (три) и РВ1, М1 и NS1 белках (по одному). Основные мутации, ответственные за холодовую адаптацию штамма А/Москва/21/17/65, приводят к изменениям в активных функциональных и структурных доменах субъединицы РВ2 вирусной полимеразы (Табл.1).
Для определения инфекционной активности был сделан ряд падающих десятикратных разведений исследуемого вирусного материала, зараженные РКЭ инкубировали при оптимальной (34°C), пониженной до 25°C или повышенной до 40°C температуре. К числу температурочувствительных (имеющих ts фенотип) относили вирусы, которые репродуцировались при повышенной температуре по сравнению с оптимальной с разностью в 5,0-6,0 lg ЭИД50 и более. Если разница титров при оптимальной и пониженной до 25°C температуре не превышала 3,0-3,5 lg ЭИД50, вирусы относили к ХА группе. При изучении репродукции штамма А/Москва/21/17 в куриных эмбрионах было показано, что ХА штамм А/Москва/21/17, в отличие от пассажного предшественника, проявляет высокий уровень репродукции при пониженной до 25°C и плохо репродуцируется при повышенной до 38-39,5°C температуре (Табл. 2).
Таким образом, выявленный множественный характер мутаций во всех генах внутренних и неструктурных белков штамма А/Москва/21/17/65(H2N2) коррелирует с присущими ему фенотипическими признаками холодовой адаптации и аттенуации. Тем не менее, только испытание штамма А/Москва/21/17/65(H2N2) в качестве донора аттенуации могло подтвердить или опровергнуть возможность его использования для этих целей и подтвердить сохранение всех его свойств в процессе реассортации.
Реассортантный вакцинный штамм А/17/Новая Каледония/99/76(H1N1) был получен методом классической генетической реассортации эпидемического вируса А/Новая Каледония/20/99(H1N1) и ХА штамма А/Москва/21/17/65(H2N2) с последующей селекцией при пониженной до 25°C температуре в присутствии иммунной антисыворотки к штамму A/Mocква/21/17/65(H2N2).
Анализ генома полученного вакцинного кандидата был выполнен при посредстве рестрикционного анализа ДНК-копий сегментов РНК, полученных с помощью обратно-транскриптазной полимеразно-цепной реакции (ОТ-ПЦР) [Klimov A.I., J. Virol. Method. - 1995. - №55. - P.445-446] или прямого секвенирования генов. Полученные с помощью ОТ-ПЦР ДНК-копии сегментов NP и М обрабатывали соответственно эндонуклеазами рестрикции Hind III и Bgl II. Было показано присутствие всех нуклеотидных замен, характерных для ХА донорского штамма A/Mocква/21/17/65(H2N2) в генах внутренних и неструктурных белков реассортантного штамма А/17/Новая Каледония/99/76(H1N1). Таким образом, было показано, что реассортант унаследовал 6 генов негликозилированных белков от ХА донора аттенуации A/Mocква/21/17/65(H2N2).
Принадлежность гемагглютинина родительскому эпидемическому вирусу А/Новая Каледония/20/99(H1N1) подтверждена в реакции торможения гемагглютинации (РТГА). РТГА проводили в 96-луночных планшетах для иммунологических реакций, в которые вносили последовательные падающие разведения иммунных антисывороток с шагом 2, соответствующие антигены в стандартной дозе (4 агглютинирующих единицы) и 1% взвесь эритроцитов кур. Титр антигемагглютинирующих антител выражали как величину, обратную наибольшему разведению сыворотки, при котором наблюдалось торможение агглютинации. Было установлено, что вакцинный штамм А/17/Новая Каледония/99/76(H1N1) антигенно идентичен родительскому эпидемическому штамму.
Принадлежность нейраминидазы N1 вакцинного кандидата определяли в ОТ-ПЦР с помощью специфичных праймеров: FN 1-36 (5' ATA АСС ATT GGA ТСА АТС AG 3'), RN1-1230 (5' ТСС GCT GTA CCC TGA CCA AT 3') с последующим секвенированием полученного фрагмента ДНК.
Таким образом, было подтверждено, что реассортант А/17/Новая Каледония/99/76(H1N1) имеет формулу генома 6:2.
Вакцинный штамм А/17/Новая Каледония/99/76(H1N1) проявляет свойства температурочувствительности и холодовой адаптации, характерные для донора аттенуации А/Москва/21/17/65(H2N2).
Пример 1. При культивировании в куриных эмбрионах было показано, что вакцинный штамм А/17/Новая Каледония/99/76(H1N1) плохо репродуцируется при повышенной до 39°C (разность титров при оптимальной температуре 33°C и 39°C составила 8,3 IgЭИД50/мл), то есть является температурочувствительным, подобно аттенуированному донорскому штамму A/Mocква/21/17/65(H2N2). Так же, как и донорский штамм A/Mocква/21/17/65(H2N2), вакцинный кандидат А/17/Новая Каледония/99/76(H1N1) хорошо репродуцировался при пониженной до +25°C температуре (разница в показателях репродукции при пониженной и оптимальной температуре не превышала 3,0 lg ЭИД50/), то есть был холодоадаптированным (Табл. 3) в отличие от пассажного варианта A/Mocква/21/65(H2N2) и эпидемического родительского штамма А/Новая Каледония/20/99(H1N1).
Вакцинный штамм А/17/Новая Каледония/99/76(H1N1) является аттенуированным для мышей и вызывает иммунный ответ при интраназальном введении.
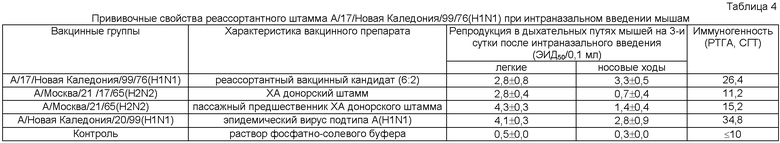
Пример 2. При интраназальном введении мышам в дозе 106 ЭИД50 вакцинный штамм А/17/Новая Каледония/99/76(H1N1) выделялся из легких в среднем в 20 раз слабее, чем эпидемический родительский вирус А/Новая Каледония/20/99(H1N1), что соответствовало уровню репродукции ХА донорского штамма A/Mocква/21/17/65(H2N2) (табл.4). В то же время вакцинный штамм А/17/Новая Каледония/99/76(H1N1) хорошо репродуцировался в носовых ходах мышей, где температура существенно ниже, и вызывал системный иммунный ответ, определяемый по уровню антигемагглютинирующих антител в сыворотках крови в среднегеометрическом титре 26, 4.
Таким образом, представленный вакцинный штамм А/17/Новая Каледония/99/76(H1N1) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму - антигенной специфичностью гемагглютинина эпидемического вируса А/Новая Каледония/20/99(H1N1), структурой генома, оптимальной для реассортантных вакцинных штаммов (6:2), температурочувствительностью, холодоадаптированностью, аттенуацией для лабораторных животных, что коррелирует с документированной безвредностью для детей, характерной для донора аттенуации A/Mocква/21/17/65(H2N2). Штамм депонирован в Государственной коллекции вирусов Научно-исследовательсгого института вирусологии им. Д.И.Ивановского Российской академии медицинских наук под №2417.
Морфология штамма - полиморфная, типичная для вируса гриппа.
ХАРАКТЕРИСТИКА ПОЛУЧЕННОГО ШТАММА
Инфекционная активность при репродукции в развивающихся куриных эмбрионах при 33°C в течение 48 часов - 8,3 lg ЭИД50/мл.
Гемагглютинирующая активность - 1:256.
Штамм проявляет генетическую стабильность биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз). Характеристики штамма отражены в паспорте на вакцинный штамм А/17/Новая Каледония/99/76(H1N1) и табл.4 (стр.7, 8).
ПАСПОРТ ШТАММА
1. Название штамма - А/17/Новая Каледония/99/76(H1N1).
2. Серия - серия 1.
3. Метод получения - реассортация; характеристика родительских вирусов:
а) эпидемический вирус - А/Новая Каледония/20/99(H1N1);
б) донор аттенуации A/Mocква/21/17/65(H2N2).
4. Количество пассажей - 7 в процессе реассортации.
5. Характеристика штамма до лиофилизации:
а) оптимальные условия репродукции - 33°С, 48 часов;
б) гемагглютинирующая активность 1:256;
в) инфекционная активность 7,5 lg ЭИД50/0,2 мл;
г) чувствительность к ингибиторам: ингибиторорезистентный;
д) разность в показателях инфекционной активности при 33°C и 40°C - 6,7 lg ЭИД50/мл;
е) разность в показателях инфекционной активности при 33°C и 25°C - 4,0 lg ЭИД50/мл;
ж) структура генома реассортанта:
- гены от эпидемического вируса - НА, NA,
- гены от донора аттенуации - PA, РВ1, РВ2, NP, М, NS.
6. Характеристика штамма после лиофилизации:
а) дата лиофилизации: 30.05.2005 г.;
б) объем материала во флаконе: 1 мл;
в) количество доз в серии: 4;
г) инфекционная активность - 6,5 lg ИД50/ 0.2 мл;
д) гемагглютинируюшая активность -1:256.
7. Рекомендуемое разведение при вакцинации 1:2.
8. Антигенная специфичность:
а) гемагглютинина - идентичен вирусу А/Новая Каледония/20/99(H1N1) по данным РТГА с крысиной антисывороткой;
б) нейраминидазы - идентична вирусу А/Новая Каледония/20/99(H1N1) по данным секвенирования.
9. Безвредность для мышей при подкожном и интраназальном введении - безвреден.
10. Бактериологический контроль лиофилизированного материала: дата проведения - 30 июня 2005 г.- стерилен.
11. Контроль на отсутствие посторонних вирусов - посторонние вирусы отсутствуют.
Изобретение относится к области микробиологии, биотехнологии и медицинской вирусологии. Предложен реассортантный вакцинный штамм А/17/Новая Каледония/99/76(Н1К1) вируса гриппа А. Данный штамм активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 33°С, характеризуется температурочувствительностью, холодоадаптированностью и аттенуацией для лабораторных животных. Реассортант унаследовал от вируса эпидемического типа A(H1N1) гены, кодирующие поверхностные гликопротеины гемагглютинин и нейраминидазу, а шесть генов, кодирующих негликозилированные белки - от донора аттенуации A/Москва/21/17/65(H2N2). Таким образом, вакцинный штамм А/17/Новая Каледония/99/76(Н1N1) по составу генома и биологическим свойствам удовлетворяет требованиям, предъявляемым к вакцинным штаммам ЖГВ фармакопейной статьей ФСП 42-0417. Изобретение может быть использовано в здравоохранении для профилактики гриппозной инфекции, вызванной эпидемическим штаммом вируса гриппа. 4 табл., 2 пр.
Штамм вируса гриппа А/17/Новая Каледония/99/76(Н1N1), полученный на основе донора аттенуации А/Москва/21/17/65 (H2N2), депонированный в Государственной коллекции вирусов Научно-исследовательского института вирусологии им. Д.И. Ивановского Российской академии медицинских наук под №2417, для получения живой гриппозной интраназальной вакцины.
| ШТАММ ВИРУСА ГРИППА A/17/НОВАЯ КАЛЕДОНИЯ/99/145(H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 2000 |
|
RU2183672C1 |
| АВТОРЕФЕРАТ disserCat | |||
| ДЕШЕВА Ю.А | |||
| Пути усовершенствования живой гриппозной вакцины и тактики ее применения при подготовке к пандемии, 2009. | |||
Авторы
Даты
2012-10-20—Публикация
2011-06-16—Подача