Изобретение относится к области молекулярной биологии и ДНК-технологий, а именно к методам разделения и обнаружения молекул ДНК. В частности, изобретение предназначено для сохранения структурной целостности и функциональных свойств ДНК при ее детекции с использованием УФ-облучения после разделения методом гель-электрофореза для последующего применения при проведении молекулярно-генетических исследований и генно-инженерных манипуляций.
Открытие структуры ДНК [1 - Watson J.D., Crick F.H. Molecular structure of nucleic acids. A structure for deoxyribose nucleic acid. Nature, 171(4356): 737-738 (1953)] и ее главной роли в передаче генетической информации [2 - Crick F.H. Central Dogma of Molecular Biology. Nature, 227: 561-563 (1970)] положили начало молекулярной биологии и ее важнейшим разделам - генной инженерии, генетике человека и медицинской генетике. Важным условием для этого стала разработка методов электрофоретического разделения нуклеиновых кислот в агарозных гелях, после которого фрагменты ДНК разной длины или конформации визуализируют с использованием специфично взаимодействующих с ними флюоресцирующих красителей. В частности, наиболее распространенным подходом стала окраска гелей бромистым этидием, который интеркалирует между азотистыми основаниями ДНК-дуплекса и флюоресцирует при УФ-облучении [3 - Гааль Э., Медьеши Г., Верецкеи Л. Электрофорез в разделении биологических макромолекул: Пер. с англ. - М.: Мир, 1982, 448 с.]. В дальнейшем, помимо визуализации разделенных фрагментов ДНК при электрофорезе, их стали выделять из геля для проведения различных генно-инженерных манипуляций: введения изолированных фрагментов в плазмидные векторы, трансформации бактериальных клеток и т.д. [4 - Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование: Пер. с англ. - М.: Мир, 1984, 403 с.].
Значимая проблема, возникающая при детекции ДНК на источниках УФ-излучения (трансиллюминаторах) с максимумом 254 нм, определяется развитием различных видов ее фотоповреждений: внутри- и межмолекулярных сшивок [5 - Lyamichev V.I., Frank-Kamenetskii M.D., Soyfer V.N. Protection against UV-induced pyrimidine dimerization in DNA by triplex formation. Nature, 344(6266): 568-570 (1990)], а также одно- и двуцепочечных разрывов в молекуле ДНК [6 - Cariello N.F., Keohavong P., Sanderson B.J.S., Thilly W.G. DNA damage produced by ethidium bromide staining and exposure to ultraviolet light. Nuc. Acids Res., 16: 4157-4161 (1988)]. Соответственно, конечным результатом подобных процессов является ухудшение качества препаратов ДНК, что негативно сказывается на результатах последующих генно-инженерных манипуляций [7 - Hartman P.S. Transillumination can profoundly reduce transformation frequencies. BioTechniques, 11: 747-748 (1991)].
Известные из уровня техники способы защиты молекул ДНК от ультрафиолетового излучения на этапах их разделения и детекции могут быть объединены в две основные группы: 1) использование для детекции результатов гель-электрофореза трансиллюминаторов с отличными от 254 нм длинами волн УФ-излучения; 2) введение в систему для гель-электрофореза специальных химических веществ (фотопротекторов), снижающих уровень повреждения ДНК при УФ-облучении.
Первый из названных подходов по своей сути является приборным (аппаратным) решением описанной проблемы. При этом использование длинноволновых трансиллюминаторов [8 - Daum H.A., Meis R., Fiandt М., Hoffman L.M., Seville М. Tutorial: Dark reader transilluminator - maintains biological activity and cloning efficiency when viewing DNA in gels. Genetic Engineering News, 21 (19): 1-3 (2001)] уменьшает повреждение ДНК [9 - Brunk C.F., Simpson L. Comparison of various ultraviolet sources for fluorescent detection of ethidium bromide-DNA complexes in polyacrylamide gels. Anal. Biochem., 82: 455-462 (1977)], но требует замены стандартного оборудования, по сравнению с которым характеризуется относительно более высокой стоимостью.
Вторая группа способов является наиболее близкой к заявляемому изобретению и может рассматриваться в качестве его аналогов. При этом их общим достоинством является то, что использование фотопротекторов во многих случаях является наиболее простым, дешевым и эффективным подходом, позволяющим сохранять структурную целостность и функциональные свойства молекулы ДНК от повреждающего действия УФ-излучения.
Так известен способ защиты ДНК от УФ-облучения при детекции результатов гель-электрофореза путем добавления в электрофоретический буфер нуклеозидов (азотистых оснований, связанных с сахаром): цитидина или гуанозина [10 - Grendemann D., Schumig E. Protection of DNA during preparative agarose gel electrophoresis against damage induced by ultraviolet light. BioTechniques, 21: 898-903 (1996)]. Эффективность данного способа подтверждена результатами последующей транскрипции, трансформации и полимеразной цепной реакции (ПЦР), выделенных из гелей ДНК.
Другим известным способом защиты ДНК от УФ-облучения после проведения гель-электрофореза является ее детекция в присутствии цинк-имидазолевых солей [11 - Hardy E., Sosa A. E., Pupo E., Casalvilla R., Femandez-Patron C. Zinc-imidazole positive: a new method for DNA detection after electrophoresis on agarose gels not interfering with DNA biological integrity. Electrophoresis, 17 (I): 26-29 (1996)]. Сохранение функциональных свойств полученных препаратов ДНК проверено с помощью повторного гель-электрофореза и трансформации.
На этом фоне новизна заявляемого способа определяется использованием в качестве фотопротекторов ДНК принципиально иной группы веществ - алкилоксибензолов (алкилрезорцинов), воспроизводящих естественные природные механизмы защиты микроорганизмов от стрессовых факторов среды обитания [12 - Эль-Регистан Г.И, Мулюкин А.Л., Николаев Ю.А., Сузина Н.Е., Гальченко В.Ф., Дуда В.И. Адаптогенные функции внеклеточных ауторегуляторов микроорганизмов. Микробиология, 75(4): 446-456 (2006)]. Кроме того, из уровня техники данная группа веществ известна как УФ-адсорберы, входящие в состав косметических композиций, предназначенных для снижения пигментации кожи [13 - Ratan К. Chaudhuri. Skin lightening compositions and methods. Patent US 2008/0305059 Al], а также композиций, предотвращающих фотодеструкцию синтетических полимеров - пластмасс и резин [14 - Vagel A., Roo E. Alkylresorcinols - rare chemicals available in bulk. Innov. Pharm. Tech.: 94-95 (2004)].
Однако в доступных источниках научной и патентной литературы не содержатся сведения о возможности использования алкилоксибензолов (алкилрезорцинов) для защиты ДНК от повреждающего действия УФ-облучения, в том числе при детекции результатов гель-электрофореза с сохранением ее структурной целостности и функциональных свойств для последующего использования при проведении генно-инженерных манипуляций.
Таким образом, заявляемый способ не известен из уровня техники, т.е. является новым.
Основной задачей, на решение которой направлен заявляемый способ, является защита ДНК от повреждений, вызываемых ультрафиолетовым излучением при детекции результатов гель-электрофореза, с сохранением ее структурной целостности и функциональной активности.
Сущностью заявляемого способа, сформулированной на уровне функционального обобщения и лежащей в его основе, является следующее: введение в буферный раствор для электрофореза С6-алкилоксибензола (гексилрезорцина) в концентрации 10-3 М (0,194 г/л) с его последующим использованием для разделения молекул ДНК в агарозном геле под действием электрического поля и детекции результатов путем УФ-облучения с длиной волны 254 нм эффективно защищает ДНК от фотоповреждений, предупреждая утрату их структурной целостности, а также сохраняя функциональную активность для последующих манипуляций.
Соответственно, при реализации заявляемого способа характеристика действий, порядок их выполнения и условия осуществления представляются следующим образом:
1) готовится водный раствор одного из стандартных электрофоретических буферов (трис-ацетатного, трис-фосфатного или трис-боратного) с конечной рН=8,0;
2) с использованием данного буфера путем нагревания готовится 0,4-2,0% расплав агарозы;
3) в остуженный до 50°C расплав агарозы вносится краситель бромистый этидий в концентрации, необходимой для последующей визуализации разделенных молекул при УФ-облучении с длиной волны 254 нм;
4) расплав агарозы переливается в горизонтально расположенную кювету, где с помощью гребенки формируются лунки для внесения препаратов ДНК, и оставляется до застывания в гелеобразное состояние;
5) агарозный гель с внесенными в лунки препаратами ДНК переносится в электрофоретическую ванну;
6) готовится навеска С6-алкилоксибензола (гексилрезорцина) категории х.ч., который вносится в электрофоретический буфер до достижения конечной концентрации 10-3 М (0,194 г/л);
7) буфер, содержащий указанные количества С6-алкилоксибензола (гексилрезорцина), переносится в электрофоретическую ванну;
8) ванна подключается к источнику тока, на котором устанавливаются режимы электрофореза;
9) по прошествии времени разделения препаратов ДНК, определяемого размерными характеристиками разделяемых молекул, источник тока отключается и агарозный гель переносится на трансиллюминатор;
10) на трансиллюминаторе под действием УФ-излучения производится визуализация результатов электрофоретического разделения молекул ДНК, в том числе документируемая с использованием цифровых устройств;
11) при необходимости фрагменты агарозного геля, в которых визуализированы разделенные молекулы ДНК, вырезаются из геля и из них выделяется ДНК для последующих генно-инженерных манипуляций.
Таким образом, разделение, визуализация и при необходимости последующее извлечение ДНК из геля проводятся без каких-либо дополнительных действий, а основным отличием описанного выше способа от стандартной процедуры постановки электрофореза является добавление в электрофоретический буфер перед процедурой электрофоретического разделения ДНК С6-алкилоксибензола (гексилрезорцина) в концентрации 10-3 М (0,194 г/л), проявляющего свойства фотопротектора и эффективно сохраняющего структурную целостность и функциональную активность молекул ДНК.
Возможность получения технического результата при выполнении перечисленных действий в указанных интервалах значений определяется следующим комплексом причинно-следственных связей:
1) использование для заявленных целей именно С6-алкилоксибензола (гексилрезорцина) определяется тем, что при проведении сравнительной серии экспериментов с использованием ряда иных алкилоксибензолов, отличающихся длиной алкильного радикала: C1-, C3- и С5-алкилоксибензола, было установлено, что именно он проявляет наибольшие фотопротекторные свойства (табл.1). При этом в качестве критерия эффективности фотопротекции служила остаточная интенсивность флуоресценции фрагментов ДНК под действием УФ-излучения 254 нм с энергетической освещенностью 0,24 В/м2, оцениваемая по уменьшению степени яркости полос на цифровых фотографиях с помощью инструментов универсальной компьютерной программы для анализа и обсчета биологических изображений «Image J»;
2) экспериментальным обоснованием применения Сб-алкилоксибензола (гексилрезорцина) в оптимальной концентрации 10-3М, соответствующей 0,194 г/л, является то, что использование данного вещества в концентрациях выше указанной достоверно не увеличивало защитный эффект по сравнению с контролем (табл.1), а уменьшение приводило к существенному снижению желаемого эффекта;
3) обоснованием использования С6-алкилоксибензола (гексилрезорцина) именно в качестве добавки к электрофоретическому буферу при проведении гель-электрофореза ДНК являются результаты экспериментов с его внесением в различные среды при проведении электрофореза, а именно: добавление в лунки геля к препаратам ДНК, в агарозный гель, а также в электрофоретический буфер. При этом использование последнего пути внесения продемонстрировало свою наибольшую эффективность, обеспечив увеличение сохранности препаратов ДНК в 2,63 раза по сравнению с обычным способом (табл.2), в то время как иные пути внесения увеличивали данный показатель только на 1,63-15,45%.
Таким образом, при разработке заявляемого способа использованы оригинальные экспериментальные данные о наибольшей выраженности фотопротекторных свойств у С6-алкилоксибензола (гексилрезорцина) при оптимальной концентрации 10-3М (0,194 г/л) и его использовании в качестве добавки к электрофоретическому буферу. Соответственно, резюмируя приведенные выше материалы о сущности заявляемого способа, характеристике действий, порядке их выполнения и условиях осуществления, можно констатировать, что заявляемый способ не следует из уровня техники и по этому показателю должен быть оценен как соответствующий критерию «изобретательский уровень».
Заявляемое изобретение иллюстрируется, но никак не ограничивается, следующими примерами.
Пример 1. Реализация способа при визуализации результата разделения продуктов амплификации ПЦР в агарозном геле при различной длительности экспозиции на УФ-трансиллюминаторе
Заявляемый способ использован при детекции результатов полимеразной цепной реакции (ПЦР), проведенной с целью лабораторной ДНК-диагностики хламидийной инфекции.
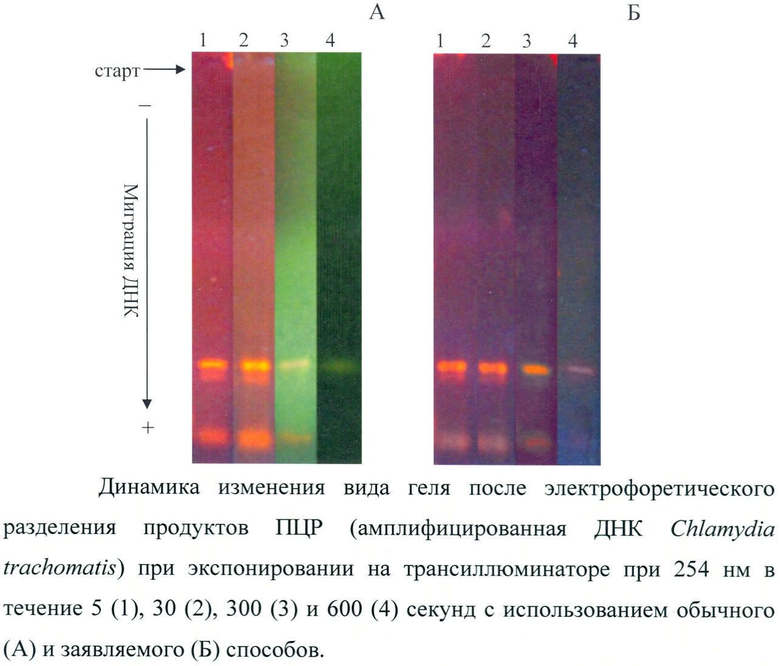
При проведении данного исследования использовались биологические образцы, содержащие ДНК, взятые у лиц, обратившихся по поводу подтверждения или исключения наличия заболевания, сравниваемые с положительными контрольными образцами ДНК Chlamydia trachomatis набора «Полимик-ХЛ» размером 273 п.н. (НПФ «Литех», Россия). Миграцию исследуемых и контрольных продуктов ПЦР после 20 минут электрофореза в 0,8% геле в присутствии 0,5 мкг/мл бромистого этидия в трис-боратном буфере (pH 8,0) при силе тока 100 мА и напряженности электрического поля 5 В/см, задаваемыми источником питания (ДНК-Технология, Россия), оценивали на трансиллюминаторе (Vilber Lourmat, Франция), оснащенном 6 лампами на 254 нм с энергетической освещенностью W=0,24 В/м2. Заключение о наличие заболевания принимали при обнаружении продукта амплификации - молекул ДНК, соответствующих по своему расположению в геле положительному контролю, для чего визуально сравнивали дорожки с внесенными препаратами ДНК при их экспонировании на трансиллюминаторе в течение 5, 30, 300 и 600 секунд (чертеж.). С целью объективизации результата степень сохранения структурной целостности амплифицированных фрагментов ДНК оценивали по уменьшению интенсивности яркости полос на цифровых изображениях гелей агарозы, обработанных с помощью инструментов универсальной компьютерной программы для анализа и обсчета цифровых изображений «ImageJ» (табл.3).
Проведение подобного диагностического исследования обычным и заявляемым способом свидетельствовало о принципиальной идентичности получаемого результата в динамике детекции на трансиллюминаторе, однако имеющего различную стабильность. Так при обычном способе наблюдалась достаточно быстрая деградация фрагментов ДНК под действием УФ-излучения, что проявлялось как снижение интенсивности свечения и последующее исчезновение «полос». Данное обстоятельство существенно затрудняло регистрацию результатов, в том числе при необходимости его представления нескольким специалистам и коллегиальной оценки, тем самым негативно сказываясь на правильности постановки диагноза при диагностике хламидийной инфекции. В свою очередь, положительный эффект от использования заявляемого способа заключался в стабильности картины разделения ДНК (вплоть до 300 секунд УФ-облучения), что представляло условие для принятия правильного диагностического заключения. Кроме того, дополнительным позитивным результатом при реализации заявляемого способа являлось сохранение оптических свойств (прозрачности) геля, обеспечивающих контрастность полос ДНК относительно фона (фиг.).
Пример 2. Реализация способа при сохранении функциональных характеристик молекул плазмидной ДНК для последующей трансформации
Заявляемый способ использован при детекции результатов разделения молекул плазмидной ДНК с их последующим выделением из агарозного геля и трансформации клеток Escherichia coli.
При проведении данного исследования использовались образцы вектора pUC19 размером 2686 н.п. («Сибэнзим», Россия) с клонированными генами luxAB, а также производная от него плазмида. После процедуры электрофоретического разделения в агарозном геле последняя переносилась на трансиллюминатор (Vilber Lourmat, Франция), оснащенный 6 лампами на 254 нм с энергетической освещенностью W=0,24 В/м2, где под визуальным контролем в течение 30 секунд вырезались блоки, содержащие флюоресцирующие «дорожки» плазмидной ДНК. Блоки обрабатывали с использованием набора для извлечения ДНК («Цитокин», Россия), после чего полученные экстракты, а также контрольные образцы исходного вектора pUC19 переносили к заранее подготовленным компетентным клеткам Escherichia coli (выращивание в LB-бульоне до ОП600=0,20-0,30, концентрированно в 25 раз в 100 мМ ледяном растворе CaCl2) и инкубировали при 0°C в течение 15 мин. Комплексы «клетка-ДНК» выдерживали при 42°C в течение 90 секунд и быстро охлаждали во льду. На следующем этапе к клеткам добавляли 1000 мл LB-бульона и инкубировали при 37°C в течение 60 мин, после чего высеивали на LB-агар с селективным маркером - антибиотиком ампициллином (50 мг/мл) для определения числа трансформантов. Эффективность трансформации оценивалась по количеству колоний на поверхности плотной селективной среды после инкубации при 37°C в течение 18-24 ч (табл.4).
Результаты трансформации клеток Escherichia coli исходным вектором pUC19 и плазмидной ДНК свидетельствовали о том, что в последнем случае эффективность трансформации оказывалась более чем на порядок ниже. На этом фоне положительный эффект от использования заявляемого способа заключался в 1,25-кратном увеличении эффективности трансформации: до 9,82% от эффективности трансформации вектором pUC19 по сравнению с аналогичной величиной 7,88% при использовании обычного способа. Таким образом, положительный эффект заявляемого способа защиты ДНК от повреждающего действия УФ-облучения при оценке результатов гель-электрофореза проявлялся в сохранении функциональных характеристик разделенной и детектированной плазмидной ДНК с целью ее последующего применения для процедуры трансформации бактериальных клеток.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ устранения ложноположительных результатов, вызванных контаминацией ДНК-полимераз фрагментами чужеродной ДНК, при индентификации генов blaTEM | 2019 |
|
RU2728317C1 |
| СПОСОБ ДЕТЕКЦИИ ПРОДУКТА ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2000 |
|
RU2169771C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ СИНЕГНОЙНОЙ ПАЛОЧКИ PSEUDOMONAS AERUGINOSA | 2014 |
|
RU2540501C1 |
| Тест-система для определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле | 2019 |
|
RU2726432C1 |
| Набор праймеров для выявления возбудителей бактериальной пневмонии человека методом мультиплексной рекомбиназной полимеразной амплификации | 2023 |
|
RU2813995C1 |
| Способ получения модифицированных комбинаторных ДНК библиотек методом твердофазной реакции удлинения праймера на ПЭТ-микрочастицах | 2018 |
|
RU2734941C2 |
| Способ определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле | 2019 |
|
RU2728660C1 |
| СПОСОБ И НАБОР ДЛЯ ОБНАРУЖЕНИЯ БАКТЕРИЙ РОДА CAMPYLOBACTER У БОЛЬНЫХ С ВОСПАЛИТЕЛЬНЫМИ ЗАБОЛЕВАНИЯМИ КИШЕЧНИКА | 2019 |
|
RU2732923C1 |
| Способ очистки и выделения высокомолекулярных нуклеиновых кислот, гель и устройство для его осуществления | 2023 |
|
RU2828813C1 |
| Лекарственное средство для лечения фиброза печени, способ его получения и способ лечения фиброза печени | 2015 |
|
RU2615445C2 |
Изобретение относится к области молекулярной биологии. Способ предусматривает введение в буфер для гель-электрофореза С6-алкилоксибензола (гексилрезорцина). Изобретение обеспечивает увеличение сроков возможной визуальной детекции разделенных молекул ДНК при их длительном экспонировании на транслюминаторе при 254 нм, усиление контрастных свойств фона и сохранение структурных и функциональных характеристик разделенных молекул ДНК при детекции результатов гель-электрофореза посредством визуализации в ультрафиолетовом излучении. 1 ил., 4 табл., 2 пр.
Способ защиты ДНК от повреждающего действия ультрафиолетового облучения с длиной волны λ=254 нм при детекции результатов гель-электрофореза, заключающийся в том, что перед проведением разделения молекул ДНК в буфер для гель-электрофореза вводят химический фотопротектор С6-алкилоксибензол гексилрезорцин в конечной концентрации 10-3М, что соответствует 0,194 г/л.
| ДАВЫДОВА О.К | |||
| Влияние химических аналогов микробных ауторегуляторов на чувствительность ДНК к УФ-облучению | |||
| - Микробиология, 2006, т.75, №5, с.654-661 | |||
| ДАВЫДОВА О.К | |||
| Длительное сохранение ДНК в водных растворах в присутствии химических аналогов микробных ауторегуляторов | |||
| - Микробиология, 2006, т.75, №5, с.662-669 | |||
| WO 9727322 А2, |
Авторы
Даты
2012-10-27—Публикация
2011-09-19—Подача