ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
В данной заявке испрашивается приоритет согласно разделу 35 Кодекса законов США, §119, на основании предварительной заявки на патент США № 60/863715, поданной 31 октября 2006 г., содержание которой полностью включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение в целом относится к лечению глазных болезней и конкретнее к применению средств, которые снижают ВГД и/или лечат либо предотвращают глаукому.
УРОВЕНЬ ТЕХНИКИ
Первичная открытоугольная глаукома (ПОУГ), также известная как хроническая или простая глаукома, представляет большинство всех случаев глаукомы в США. Большинство форм глаукомы возникает вследствие нарушения оттока водянистой влаги, которое имеет анатомические, биохимические или физиологические причины.
У больных глаукомой в водянистой влаге обнаружен повышенный уровень ингибитора активатора плазминогена-1 (PAI-1) (Dan et al., Arch Opthalmol, 2005). Уровень PAI-1 повышается цитокином TGFβ (Binder et al., News Physiol Sci, 2002), среди прочих эндогенных стимулов. PAI-1 ингибирует активность как тканевого активатора плазминогена (tPA), так и урокиназного активатора плазминогена (uPA). И tPA, и uPA катализируют превращение плазминогена в плазмин - ключевое промежуточное соединение в каскаде фибринолиза (Wu et al., Curr Drug Targets, 2002). Как известно, плазмин стимулирует преобразование определенных матриксных прометаллопротеиназ (MMP) в их активные формы, разрушающих внеклеточный матрикс (ECM) (He et al., PNAS, 1989). PAI-1 также модулирует соединение витронектина, компонента ECM, с интегринами поверхности клетки, которые действуют как рецепторы адгезии (Zhou et al., Nature Structural Biology, 2003). Таким образом, PAI-1 связан и с ослабленной адгезией, и с увеличенным отделением клеток в неглазных тканях.
Лекарственные средства, чья эффективность в снижении внутриглазного давления (ВГД) и/или лечении ПОУГ доказана, включают как агенты, которые уменьшают продукцию водянистой влаги, так и агенты, которые увеличивают ее отток. Такие средства, как правило, вводятся одним из двух возможных путей: местно (непосредственное нанесение на глаз) или перорально. Однако фармацевтические подходы к лечению глазной гипертензии имеют различные нежелательные эффекты. Например, миотические средства, такие как пилокарпин, могут вызвать нечеткость зрения, головную боль и другие отрицательные эффекты, касающиеся зрения. Системно введенные ингибиторы карбоангидразы также могут вызвать тошноту, диспепсию, слабость и метаболический ацидоз. Некоторые простагландины вызывают гиперемию, зуд глаз, а также потемнение ресниц и периорбитальной кожи. Такие отрицательные побочные эффекты могут привести к невыполнению назначений врача пациентом или к отмене терапии, в результате чего зрение продолжает ухудшаться. Кроме того, существуют люди, у которых лечение существующими противоглаукомными препаратами малоэффективно. Поэтому имеется потребность в других терапевтических средствах для лечения глазных болезней, таких как глаукома и глазная гипертензия.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В вариантах осуществления настоящего изобретения признается, что модуляция связывания PAI-1 с витронектином может использоваться для лечения глазного заболевания и/или снижения ВГД. Один вариант осуществления относится к способу лечения глаукомы или повышенного ВГД у пациента, где способ предусматривает введение пациенту эффективного количества композиции, содержащей средство, которое модулирует связывание PAI-1 с витронектином.
Другой вариант осуществления по настоящему изобретению относится к способу лечения глазного заболевания, связанного с PAI-1, где способ предусматривает введение эффективного количества композиции, содержащей средство, которое модулирует связывание PAI-1 с витронектином.
В некоторых из этих вариантов осуществления указанное средство представляет собой ZK4044, PAI-039, WAY-140312, HP-129, T-686, XR5967, XR334, XR330, XR5118, антитела к PAI-1, пептидомиметики PAI-1 и их комбинации.
Еще один вариант осуществления относится к способу производства соединения, которое будет использоваться для лечения глаукомы или повышенного ВГД, где способ предусматривает получение вещества-кандидата, предположительно модулирующего связывание PAI-1, отбор соединения путем оценки способности вещества-кандидата уменьшать количество активного PAI-1 в трабекулярной сети субъекта, страдающего глаукомой или страдающего повышенным уровнем PAI-1; и производство выбранного соединения.
В определенных вариантах осуществления композиции по изобретению дополнительно содержат соединение, выбранное из группы, состоящей из офтальмологически приемлемых консервантов, поверхностно-активных веществ, усилителей вязкости, усилителей проникновения, гелеобразующих средств, гидрофобных оснований, носителей, буферов, натрия хлорида, воды и их комбинаций.
В других вариантах осуществления соединение выбрано из группы, состоящей из β-блокаторов, аналогов простагландинов, ингибиторов карбоангидразы, α2-агонистов, миотических средств, нейропротекторов, ингибиторов киназы rho и их комбинаций, может применяться либо как часть композиции, либо как самостоятельное введение.
Вышеизложенная сущность изобретения в общих чертах описывает особенности и технические преимущества определенных вариантов осуществления настоящего изобретения. Дополнительные особенности и технические преимущества будут описаны ниже в подробном описании изобретения. Новые особенности, которые представляются характерными признаками настоящего изобретения, будет легче понять из подробного описания вместе с любыми сопровождающими его чертежами. Однако подразумевается, что приведенные здесь чертежи предназначены для иллюстрации изобретения или помощи в развитии или понимании изобретения; они не должны рассматриваться как ограничивающие объем изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Более полного понимания настоящего изобретению и его преимуществ можно достичь, обращаясь к следующему описанию вместе с сопровождающим его чертежам, где:
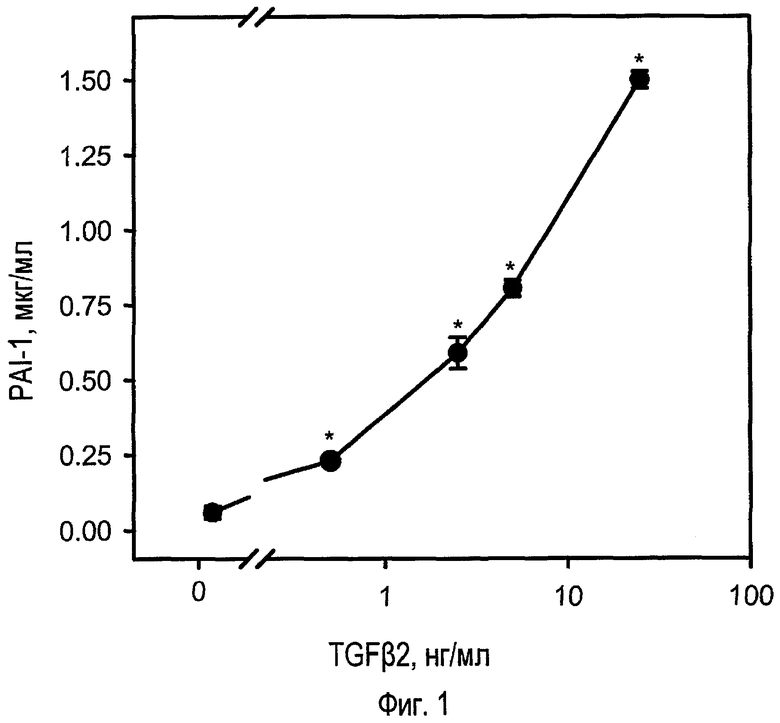
ФИГ.1 - график экспериментальных результатов, демонстрирующий зависящее от концентрации влияние TGFβ2 (24 ч) на уровень PAI-1 в супернатантах клеток трабекулы человека (GTM-3). Данные представлены в виде средних значений и стандартной ошибки среднего (SEM); n = 3. *p<0,05 в отношении соответствующей группы обработки носителя (односторонний дисперсионный анализ [ANOVA], сопровождаемый тестом Dunnett);
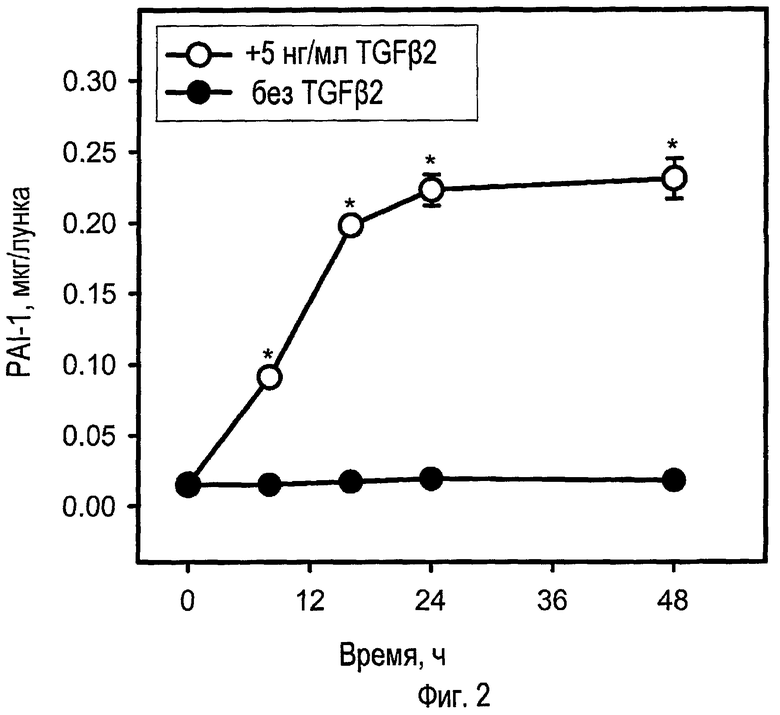
ФИГ.2 - график экспериментальных результатов, показывающий уровни PAI-1 в супернатантах клеток GTM-3 при обработке TGFβ2 (5 нг/мл) или без нее в различные периоды времени. Данные представлены в виде средних значений и SEM; n = 3. *p<0,05 в отношении соответствующей группы обработки носителя в тот же момент (t - критерий Стьюдента);
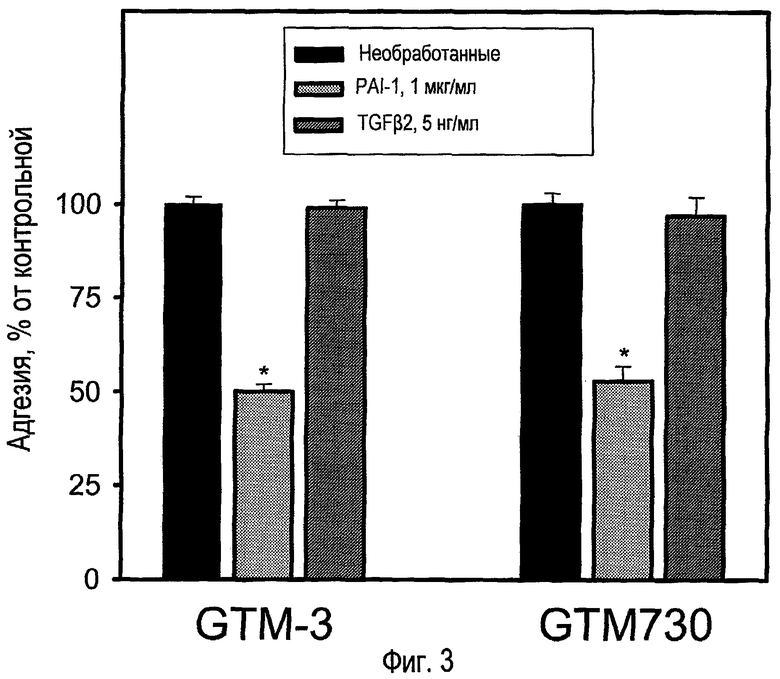
ФИГ.3 - гистограмма, показывающая влияние PAI-1 дикого типа (1 мкг/мл, 2 ч) и TGFβ2 (5 нг/мл, 2 ч) на адгезию трансформированных (GTM-3) и нетрансформированных клеток (GTM730) к субстрату витронектина. Данные представлены в виде средних значений и SEM; n = 12-44. *p<0,05 в отношении соответствующих необработанных групп (односторонний ANOVA, сопровождаемый тестом Dunnett);
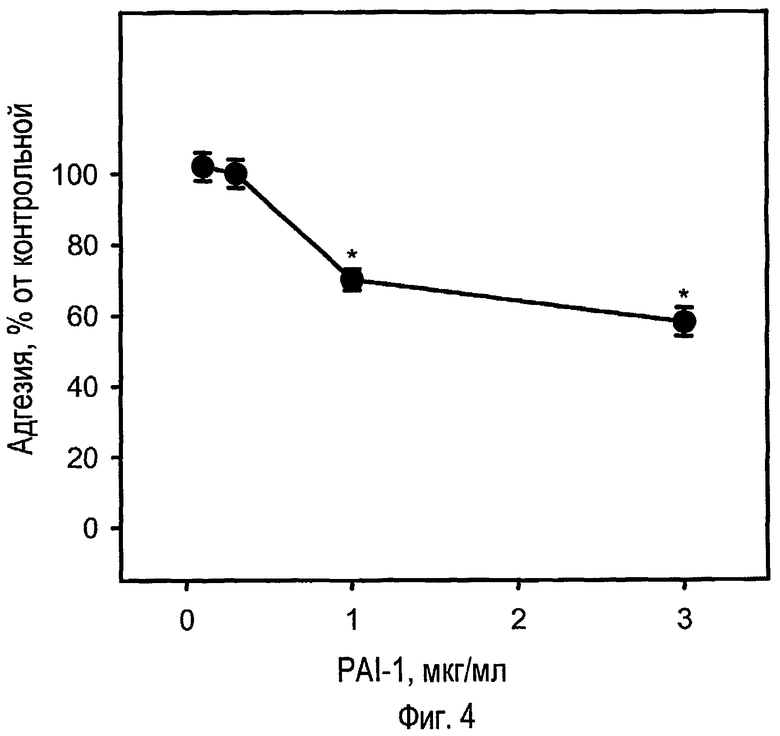
ФИГ.4 - график экспериментальных результатов, демонстрирующий зависящее от концентрации влияние PAI-1 дикого типа (2 ч) на адгезию клеток GTM-3 к субстрату витронектина. Данные представлены в виде средних значений и SEM; n = 4. *p<0,05 в отношении соответствующей группы, обработанной растворителем (односторонний ANOVA, сопровождаемый тестом Dunnett);
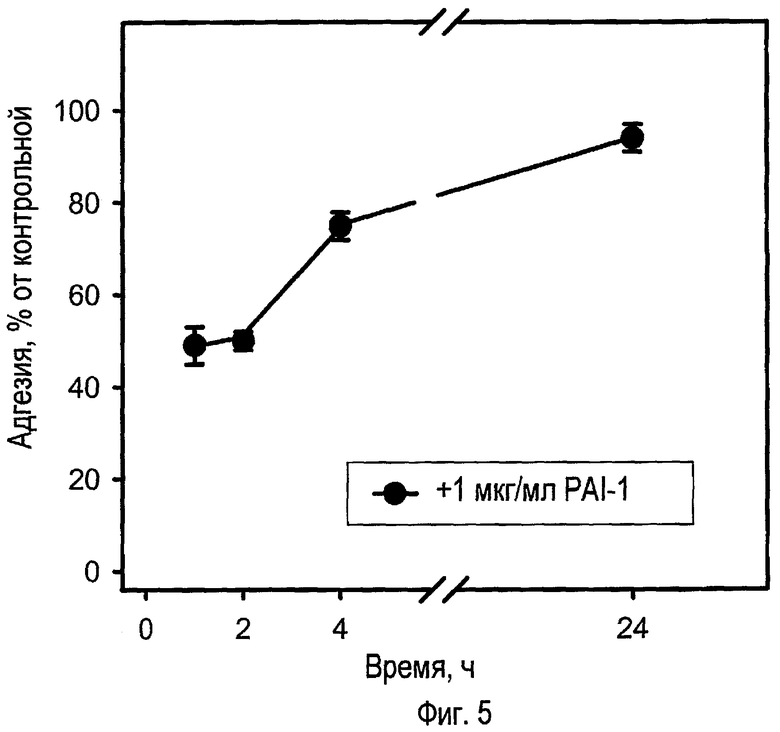
ФИГ.5 - график экспериментальных результатов, показывающий зависящее от времени влияние PAI-1 дикого типа (1 мкг/мл) на адгезию клеток GTM-3 к субстрату витронектина. Данные представлены в виде средних значений и SEM, n = 12-44;
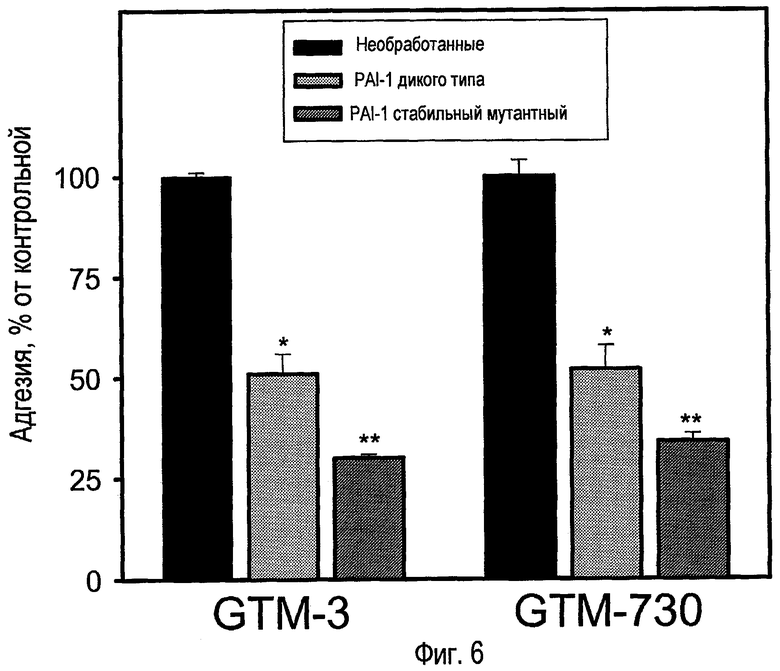
ФИГ.6 - гистограмма экспериментальных результатов, демонстрирующая влияние PAI-1 дикого типа (1 мкг/мл, 1 ч) по сравнению со стабильным, устойчивым к разложению мутантным PAI-1 (1 мкг/мл, 1 ч) на адгезию клеток GTM-3 и GTM730 к субстрату витронектина. Данные представлены в виде средних значений и SEM; n = 4. *p<0,05 в отношении соответствующих необработанных групп (t - критерий Стьюдента); **p<0,05 в отношении соответствующих обработанных групп PAI-1 дикого типа (t - критерий Стьюдента);
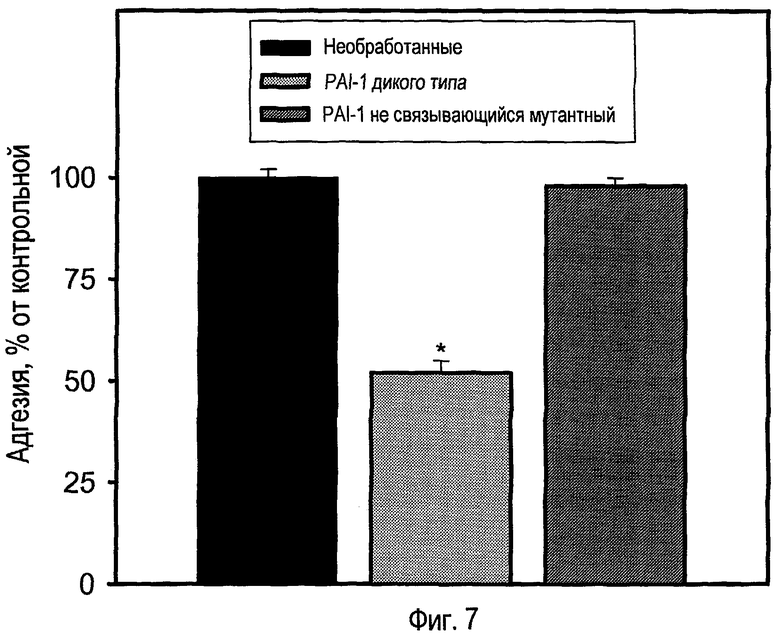
ФИГ.7 - гистограмма экспериментальных результатов, демонстрирующая влияние PAI-1 дикого типа (1 мкг/мл, 2 ч) по сравнению с не связывающим витронектин мутантным PAI-1 (1 мкг/мл, 2 ч) на адгезию клеток GTM-3 к субстрату витронектина. Данные представлены в виде средних значений и SEM, n = 4-24. *p<0,05 в отношении необработанной группы (односторонний ANOVA, сопровождаемый тестом Dunnett); и
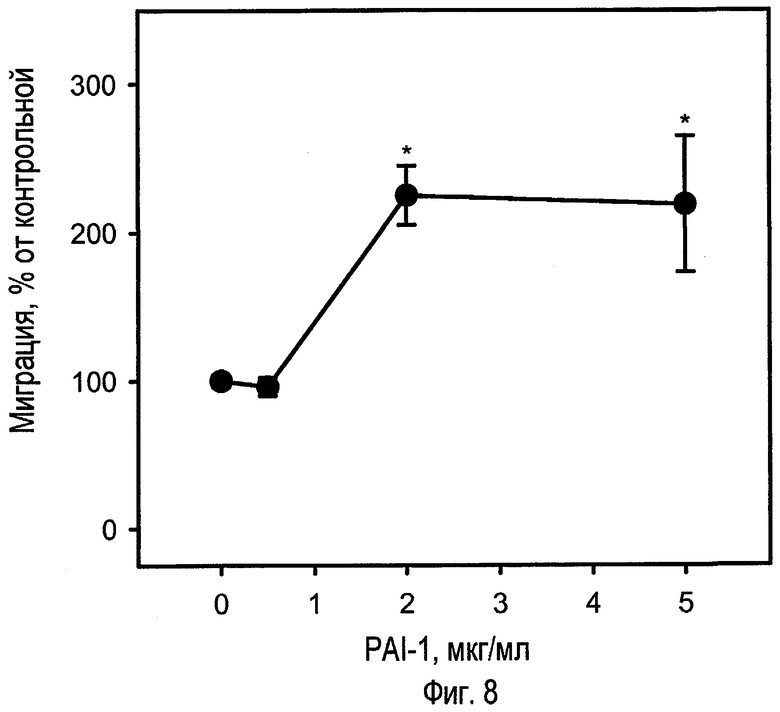
ФИГ.8 - график экспериментальных результатов, показывающий зависящее от концентрации влияние PAI-1 дикого типа (4 ч) на миграцию клеток GTM-3. Данные представлены в виде средних значений и SEM, n = 4-32. *p<0,05 в отношении группы носителя (односторонний ANOVA, сопровождаемый тестом Dunnett).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Показана связь PAI-1 с ослабленной адгезией и с увеличенным отделением клеток в неглазных тканях. Анализ данных, раскрытых в данном документе, заставляет прийти к заключению, что повышенный уровень PAI-1 в водянистой влаге при глаукоме может объясняться действием TGFβ2 на клетки трабекулярной сети. Индуцируемое PAI-1 снижение адгезии TM-клеток происходит, вероятно, из-за того, что PAI-1 вмешивается в прикрепление клеток к компоненту внеклеточного матрикса витронектину. Кроме того, вызываемое PAI-1 ослабление адгезии TM-клеток может облегчать миграцию TM-клеток из ее окружения. Таким образом, вызванные PAI-1 уменьшение адгезии и увеличение миграции TM-клеток могут быть важными факторами в уменьшении TM-клеточности, наблюдаемой в глазах при глаукоме. В определенных вариантах осуществления изобретения признается, что PAI-1 может вызвать такие эффекты в ткани трабекулярной сети (TM).
Циркулирующий PAI-1 в норме существует в латентной форме вследствие способности активного PAI-1 быстро и спонтанно переходить в свою неактивную конформацию. Однако PAI-1, связанный с витронектином, стабилизируется в активной форме, в результате чего его период полувыведения значительно удлиняется. Таким образом, один способ ослабить вредные эффекты активного PAI-1 заключается в использовании средств, которые модулируют взаимодействие PAI-1 и витронектина. Такие средства позволяли бы несвязанному витронектину во внеклеточном матриксе связываться с его рецептором на клеточной поверхности (интегрином), тем самым усиливая адгезию клеток и снижая потерю клеток TM-тканей. Модуляция способности PAI-1 связываться с витронектином может создать эффективный подход к лечению глаукомы.
Определенные варианты осуществления изобретения относятся к способам, направленным на эффекты, осуществляемые при участии PAI-1, при глазных болезнях, таких как глаукома, путем нарушения связывания PAI-1 с витронектином, как показано на следующей схеме.
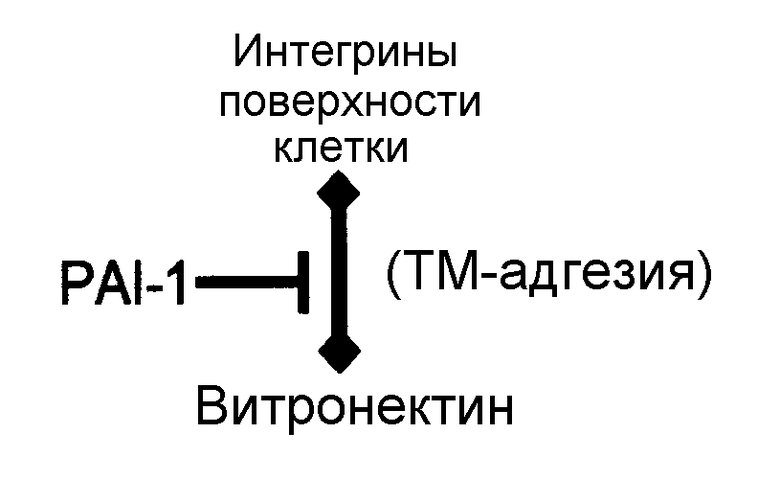
где PAI-1 уменьшает связывание рецепторов адгезии (интегринов), находящихся на поверхности клеток трабекулярной сети, с витронектином, компонентом внеклеточного матрикса. Вследствие этого клетки отделяются от TM и смываются потоком жидкости в юкстаканаликулярный отдел TM. Такое накопление отдельных TM-клеток и их остатков вносит свой вклад в повышенное сопротивление оттоку жидкости и увеличенное ВГД. Модуляция связывания PAI-1 с витронектином может уменьшить отделение TM-клеток и снизить увеличенное сопротивление оттоку и повышенное ВГД. Кроме того, тем самым увеличится клеточность TM-ткани и сохранятся такие жизненные функции, как фагоцитоз.
МОДУЛЯТОРЫ СВЯЗЫВАНИЯ PAI-1
В данной области техники известны различные модуляторы связывания PAI-1. Jensen et al., например, описали открытие малого пептида с высоким сродством к PAI-1 дикого типа, и этот пептид ингибирует связь комплекса uPA-PAI-1 с представителями семейства рецепторов липопротеинов низкой плотности (Jensen et al., Inhibition of plasminogen activator inhibitor-1 binding to endocytosis receptors of the low-density-lipoprotein receptor family by a peptide isolated from a phage display library, Biochem J., 2006, Vol. 399(3):387-396). Агенты, которые нарушают способность PAI-1 ингибировать тканевый активатор плазминогена (tPA) и/или урокиназный активатор плазминогена (uPA), тоже могут модулировать связывание PAI-1. Такие агенты включают, без


Кроме того, ингибиторы PAI-1, такие как описанные Ye (Ye et al., Synthesis and biological evaluation of piperazine-based derivatives as inhibitors of plasminogen activator inhibitor-1 (PAI-1). Bioorg Med Chem Lett., 2004 Feb 9, Vol. 14(3):761-5; Ye et al., Synthesis and biological evaluation of menthol-based derivatives as inhibitors of plasminogen activator inhibitor-1 (PAI-1). Bioorg Med Chem Lett., 2003 Oct 6, Vol. 13(19):3361-5), и ингибиторы на основе антител, как те, что были описаны Verbeke (Verbeke et al., Cloning and paratope analysis of an antibody fragment, a rational approach for the design of a PAI-1 inhibitor. J Thromb Haemost., 2004 Feb, Vol. 2(2):289-97) и van Giezen (van Giezen et al., The Fab-fragment of a PAI-1 inhibiting antibody reduces thrombus size and restores blood flow in a rat model of arterial thrombosis. Thromb Haemost., 1997 May, Vol. 77(5):964-9), также могут модулировать связывание PAI-1. Другие модуляторы связывания PAI-1 могут представлять собой пептидомиметики PAI-1. Содержание всех ссылок, процитированных в этом разделе под заголовком «Модуляторы связывания PAI-1», тем самым включено полностью посредством ссылки.
СПОСОБЫ ВВЕДЕНИЯ
Модуляторы связывания PAI-1 по настоящему изобретению для доставки могут быть включены в различные типы глазных составов. Соединения можно ввести непосредственно в глаз (например, местные глазные капли или мази; устройства с замедленным высвобождением, такие как фармацевтические губки для введения препарата, имплантированные в слепой мешок, или вблизи склеры, или внутрь глаза; инъекции - периокулярные, конъюнктивальные, под тенонову капсулу, внутрикамерные, в стекловидное тело или интраканаликулярные) или системно (например, перорально, с помощью внутривенных, подкожных или внутримышечных инъекций; парентеральная, кожная или назальная доставка) с применением методов, известных обычным специалистам в данной области техники. Также рассматривается, что модуляторы связывания PAI-1 по изобретению могут быть введены во внутриглазные вкладыши или имплантируемые устройства.
Модуляторы связывания PAI-1, раскрытые в данном документе, предпочтительно включены в местные глазные составы для доставки в глаз. Соединения могут быть объединены с офтальмологически приемлемыми консервантами, поверхностно-активными веществами, усилителями вязкости, усилителями проникновения, буферами, натрия хлоридом и водой, чтобы образовать водную стерильную глазную суспензию или раствор. Глазные составы в форме раствора могут быть получены путем растворения соединения в физиологически приемлемом изотоническом водном буфере. Дополнительно глазной раствор может содержать офтальмологически приемлемое поверхностно-активное вещество, способствующее растворению соединения. Кроме того, глазной раствор может содержать средство, увеличивающее вязкость, такое как гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или подобное, чтобы повысить удерживание состава в конъюнктивальном мешке. Также могут использоваться гелеобразующие средства, включая без ограничения геллан и ксантановую камедь. Чтобы получить стерильные глазные составы в форме мази, активный ингредиент объединяют с консервантом в подходящем носителе, таком как минеральное масло, жидкий ланолин или белый вазелин. Стерильные глазные составы в форме геля можно приготовить, суспендируя соединение в гидрофильном основании, полученном при комбинировании, например, карбопола-974 или тому подобного, согласно опубликованным составам для аналогичных глазных препаратов; в состав могут включаться консерванты и средства, регулирующие тоничность.
Предпочтительно из модуляторов связывания PAI-1 готовят местные глазные суспензии или растворы с pH приблизительно 4-8. Соединения содержатся в местных суспензиях или растворах в количестве, достаточном, чтобы снизить ВГД у пациентов с повышенным ВГД и/или сохранить нормальное ВГД у больных глаукомой. Такие количества упоминаются в данном документе как «количество, эффективно контролирующее ВГД» или «эффективное количество». Как правило, количество соединений в этих составах будет составлять 0,01-5% по массе/объему (мас./об.%), но предпочтительно - 0,25-2 мас./об.%. Таким образом, для местного применения 1-2 капли этих составов должны наноситься на поверхность глаза 1-4 раза в сутки по выбору квалифицированного врача.
Модуляторы связывания PAI-1 также могут использоваться в комбинации с другим средствами для лечения повышенного ВГД или глаукомы, например, без ограничения, ингибиторами киназы rho, β-блокаторами, аналогами простагландинов, ингибиторами карбоангидразы, α2-агонистами, миотическими средствами, серотонинергическими средствами и нейропротекторами.
Использованный в данном документе термин «модулятор связывания PAI-1» включает такие модуляторы и их фармацевтически приемлемые соли. Фармацевтически приемлемая соль модулятора связывания PAI-1 - это соль, которая сохраняет активность модулирования связывания PAI-1 и является приемлемой для организма человека. Соли могут представлять собой соли присоединения кислоты или основания, поскольку упомянутые в данном документе соединения могут иметь амино- или карбоксильные заместители. Соль может быть образована с кислотой, такой как уксусная кислота, бензойная кислота, коричная кислота, лимонная кислота, этансульфоновая кислота, фумаровая кислота, гликолевая кислота, бромистоводородная кислота, хлористоводородная кислота, малеиновая кислота, малоновая кислота, миндальная кислота, метансульфоновая кислота, азотная кислота, щавелевая кислота, фосфорная кислота, пропионовая кислота, пировиноградная кислота, салициловая кислота, янтарная кислота, серная кислота, винная кислота, п-толуолсульфоновая кислота, трифторуксусная кислота и тому подобное. Соль может быть образована с основанием, таким как первичный, вторичный или третичный амин, алюминий, аммоний, кальций, медь, железо, литий, магний, марганец, калий, натрий, цинк и тому подобное.
ОПРЕДЕЛЕНИЕ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ
Модуляторы связывания PAI-1 могут быть отобраны с помощью определения связывания или с помощью функциональных исследований, которые также могут использоваться, чтобы определить биологическую активность модуляторов. Такие исследования могут быть разработаны специалистами в данной области техники с использованием ранее описанных способов. Другие исследования существуют или могут быть получены из данных, приведенных ниже, в примерах. Например, анализ миграции клеток трабекулы, описанный далее, может использоваться там, где предполагаемый модулятор связывания PAI-1 добавляют как испытуемое средство.
Определение биологической активности in vivo
Способность определенных модуляторов связывания PAI-1 безопасно снижать ВГД может быть оценена в определенных вариантах осуществления посредством исследований in vivo с использованием новозеландских кроликов-альбиносов и/или макак-крабоедов.
Оценка безопасности для глаз на новозеландских кроликах-альбиносах
В оба глаза новозеландского кролика-альбиноса вводят одну аликвоту объемом 30 мкл испытуемого средства в носителе. За животными непрерывно наблюдают в течение получаса после введения, а затем - каждые полчаса на протяжении 2 ч или до тех пор, пока не исчезнут видимые эффекты.
Острое изменение внутриглазного давления у новозеландских кроликов-альбиносов
Внутриглазное давление (ВГД) определяют с помощью пневмотонометра Mentor Classic 30 после легкой анестезии роговицы, вызванной 0,1% пропаракаина. После каждого измерения глаза промывают одной или двумя каплями физиологического раствора. После измерения исходного ВГД испытуемое соединение в виде одной аликвоты объемом 30 мкл закапывают в один или оба глаза животного либо в один глаз - испытуемое соединение, а во второй - носитель. Последующие измерения ВГД проводят через полчаса, 1, 2, 3, 4 и 5 ч.
Острое изменение внутриглазного давления у макак-крабоедов
Внутриглазное давление (ВГД) определяют пневмотонометром Alcon после легкой анестезии роговицы, вызванной 0,1% пропаракаина, как описано выше (Sharif et al., J. Ocular Pharmacol. Ther., 2001, Vol. 17:305-317; May et al., J. Pharmacol. Exp. Ther., 2003, Vol. 306:301-309). После каждого измерения глаза промывают одной или двумя каплями физиологического раствора. После измерения исходного ВГД испытуемое соединение в виде одной или двух аликвот объемом 30 мкл закапывают в выбранные глаза макака-крабоеда. Последующие измерения ВГД проводят через 1, 3 и 6 ч. Правые глаза всех животных подвергают лазерной трабекулопластике, чтобы вызвать глазную гипертензию. Все левые глаза остаются нормальными и, таким образом, имеют нормальное ВГД.
ПРИМЕРЫ
Следующие примеры включены, чтобы продемонстрировать предпочтительные варианты осуществления изобретения. Специалистами в данной области техники будет ясно, что методы, раскрытые в нижеследующих примерах, представляют собой методы, которые, как обнаружил изобретатель, хорошо функционируют при практическом осуществлении изобретения и, таким образом, могут считаться предпочтительными способами для практического осуществления. Однако в свете настоящего раскрытия специалисты в данной области техники должны понимать, что в конкретных раскрытых вариантах осуществления можно сделать много изменений и тем не менее получить подобный или схожий результат, не отступая от сущности и объема изобретения.
ПРИМЕР 1 - TGFβ2 увеличивает содержание PAI-1 в клетках трабекулы
ФИГ.1 представляет результаты экспериментов, показывающие, что TGFβ2 увеличивает содержание PAI-1 в культурах клеток трабекулы (GTM-3). Опосредуемые PAI-1 эффекты могут содействовать ранее наблюдаемому TGFβ2-опосредованному накоплению вещества внеклеточного матрикса в различных тканях, включая TM-ткани. ФИГ.2 демонстрирует, что такое TGFβ2-опосредованное увеличение уровня PAI-1 постоянно присутствует в культурах клеток, обработанных TGFβ2. Обработка TGFβ2 приводит к зависящему как от концентрации, так и от времени накоплению PAI-1 в супернатантах TM-клеток (ФИГ.1 и 2). Содержание PAI-1 постепенно увеличивается в ответ на TGFβ2, достигая постоянного уровня приблизительно через 24 ч после обработки.
ПРИМЕР 2 - Уменьшение адгезии PAI-1 дикого типа к клеткам трабекулы
ФИГ.3 представляет экспериментальные данные, демонстрирующие способность рекомбинантного PAI-1 человека (2 ч обработки) уменьшать адгезию культивируемых клеток трабекулы человека к субстрату витронектина; на той же самой модели мутантный PAI-1, который не связывается с витронектином, не влиял на адгезию (ФИГ.7). ФИГ.4 показывает влияние увеличивающихся концентраций PAI-1 на адгезию TM-клеток. Влияние PAI-1 на адгезию дозозависимо, оценочный EC50 составляет приблизительно 0,6 мкМ. Такое вмешательство в адгезию TM-клеток может вызвать ускоренную потерю клеток трабекулы, такую как наблюдаемая при глаукоме, в частности ПОУГ. Отделившиеся TM-клетки могут способствовать обструкции оттока водянистой влаги; считается, что этот процесс ведет к повышению сопротивления оттока и увеличению ВГД. Потеря TM-клеток может также привести к ухудшенному клиренсу разрушенного материала в результате сниженной фагоцитарной способности.
Обратимся снова к ФИГ.3: клетки, обработанные TGFβ2 в течение 2 часов, не испытывали измеряемой потери адгезии по сравнению с контрольными. Отсутствие влияния кратковременной обработки TGFβ2 объясняется, вероятно, недостаточной TGFβ2-опосредованной индукцией PAI-1 во время 2-часовой обработки (см. ФИГ.2). Реакции SV40-трансформированных клеток (GTM-3) были очень близки реакциям нетрансформированных клеток (GTM730).
ПРИМЕР 3 - PAI-1 дикого типа постепенно разрушается
ФИГ.5 демонстрирует экспериментальные данные, указывающие, что потеря адгезии, опосредованная PAI-1 дикого типа, преходяща, уровень адгезии приближается к контрольному через 24 ч. ФИГ.6 - гистограмма экспериментальных результатов, показывающая влияние дикого типа PAI-1 (1 мкг/мл, 1 ч) по сравнению со стабильным, устойчивым к разрушению мутантным PAI-1 (1 мкг/мл, 1 ч) на адгезию клеток GTM-3 и GTM730 к субстрату витронектина. В контексте с ФИГ.5 эти данные демонстрируют, что PAI-1 дикого типа, по-видимому, со временем разрушается. Влияние PAI-1 поэтому усилилось при использовании стабильного мутантного PAI-1 (смесь мутаций K154T, Q139L, M354I и H150H), который более устойчив к разложению, чем белок дикого типа.
ПРИМЕР 4 - Влияние PAI-1 дикого типа на адгезию опосредуется витронектином
ФИГ.7 - гистограмма экспериментальных результатов, показывающая влияние PAI-1 дикого типа (1 мкг/мл, 2 ч) по сравнению с мутантным PAI-1 (1 мкг/мл, 2 ч), не связывающим витронектин, на адгезию клеток GTM-3 к субстрату витронектина. Мутант PAI-1, который не связывает витронектин, в других отношениях функционален, но не влияет на адгезию TM-клеток к субстрату витронектина, в то время как связывающий витронектин PAI-1 дикого типа уменьшает адгезию примерно на 50% по сравнению с контрольным уровнем.
ФИГ.8 - график экспериментальных результатов, показывающий зависящее от концентрации влияние PAI-1 дикого типа (4 ч) на миграции клеток GTM-3. PAI-1 дикого типа, при концентрациях, подобных тем, которые ослабляют адгезию TM-клеток, вызывает миграцию TM-клеток.
МЕТОДЫ ДЛЯ ПРИМЕРОВ 1-4
Культура TM-клеток человека. TM-клетки человека выделяли из посмертно полученной донорской ткани человека, определяли их характеристики и культивировали, как ранее описано. Генерирование и определение характеристик трансформированной клеточной линии (GTM-3) тоже осуществляли, как описано ранее (Pang et al. Preliminary characterization of a transformed cell strain derived from human trabecular meshwork. Curr. Eye Res., 1994, Vol. 13:51-63).
PAI-1 ELISA. 24-луночные планшеты с культурами TM-клеток были лишены сыворотки на 24 ч, затем в течение еще 24 ч (или как указано) их инкубировали с TGFβ2 в бессывороточной среде. В аликвотах супернатантов от обработанных культур количественно определяли секретированный PAI-1 с помощью набора ELISA для PAI-1 человека (American Diagnostica).
Адгезия TM-клеток. Адгезию TM-клеток определяли с помощью InnoCyte ECM Cell Adhesion Assay (Calbiochem). TM-клетки (20000 на лунку; бессывороточная среда) помещали на покрытый витронектином 96-луночный планшет. Затем добавляли испытуемые вещества, после чего инкубировали в инкубаторе для культур клеток в течение указанного времени. Неприкрепившиеся клетки после этого удаляли декантацией и осторожной промывкой лунок PBS. Относительное прикрепление клеток определяли посредством поглощения флюоресцентного красителя (calcein-AM).
Миграция TM-клеток. Миграцию TM-клеток оценивали, используя InnoCyte Cell Migration Assay (Calbiochem). TM-клетки (50000 на лунку; бессывороточная среда) помещали в верхние ячейки миграционной камеры, входящей в состав набора. Нижние лунки заполняли растворами испытуемых веществ, затем камеру инкубировали в инкубаторе для культур клеток. Через 4 ч верхнюю часть устройства удаляли и супернатанты осторожно декантировали, чтобы удалить неприкрепившиеся клетки. После этого верхний блок ячеек помещали в свежий нижний планшет, содержащий смесь буфера отделения и calcein-AM. 60 мин спустя аликвоты от каждой нижней лунки были перенесены на свежий, черный, 96-луночный планшет, после чего определяли относительную флюоресценцию.
ПРИМЕРЫ СОСТАВОВ 5-8 ИЗ ПРИМЕРА 5
ПРИМЕР 6
ПРИМЕР 7
ПРИМЕР 8
Настоящее изобретение и его варианты осуществления подробно описаны. Однако не предполагается, что объем настоящего изобретения ограничен конкретными вариантами осуществления любого процесса, производства, композиции, соединений, способов, методов и/или этапов, указанных в описание изобретения. В раскрытом материале могут быть произведены различные модификации, замены и вариации, не отступая от сущности и/или существенных особенностей настоящего изобретения. Соответственно, средний специалист в данной области техники с помощью раскрытия легко поймет, что дальнейшие модификации, замены и/или вариации, выполняющие по существу ту же самую функцию или достигающие по существу того же самого результата, как варианты осуществления, описанные в данном документе, могут быть использованы согласно таким родственным вариантам осуществления изобретения. Таким образом, подразумевается, что объем следующей формулы изобретения включает модификации, замены и вариации процессов, производств, составов вещества, соединений, способов, методов и/или этапов, раскрытых в данном документе.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТАГОНИСТЫ CDK2 В КАЧЕСТВЕ АНТАГОНИСТОВ КОРОТКОЙ ФОРМЫ ФАКТОРА ТРАНСКРИПЦИИ C-MAF ДЛЯ ЛЕЧЕНИЯ ГЛАУКОМЫ | 2004 |
|
RU2370267C2 |
| АГЕНТЫ, КОТОРЫЕ РЕГУЛИРУЮТ, ИНГИБИРУЮТ ИЛИ МОДУЛИРУЮТ АКТИВНОСТЬ И/ИЛИ ЭКСПРЕССИЮ ФАКТОРОВ РОСТА СОЕДИНИТЕЛЬНОЙ ТКАНИ (ФРСТ), В КАЧЕСТВЕ УНИКАЛЬНЫХ СРЕДСТВ ДЛЯ СНИЖЕНИЯ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ И ЛЕЧЕНИЯ ГЛАУКОМАТОЗНЫХ РЕТИНОПАТИЙ/ОПТИЧЕСКИХ НЕВРОПАТИЙ | 2003 |
|
RU2332213C2 |
| ОПОСРЕДОВАННОЕ РНКi ИНГИБИРОВАНИЕ Rho-КИНАЗЫ ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ НАРУШЕНИЙ | 2006 |
|
RU2432165C2 |
| НОВЫЕ АГОНИСТЫ NPR-B | 2010 |
|
RU2557290C2 |
| НОВЫЕ АГОНИСТЫ NPR-B | 2010 |
|
RU2636738C2 |
| ПРИМЕНЕНИЕ ГЕНА СЫВОРОТОЧНОГО АМИЛОИДА А ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ГЛАУКОМЫ И ИДЕНТИФИКАЦИИ АНТИГЛАУКОМНЫХ АГЕНТОВ | 2007 |
|
RU2461378C2 |
| ЛЕЧЕНИЕ ГЛАЗНЫХ БОЛЕЗНЕЙ, ОТЛИЧАЮЩИХСЯ ПОВЫШЕННЫМ ВНУТРИГЛАЗНЫМ ДАВЛЕНИЕМ, С ПОМОЩЬЮ siPHK | 2005 |
|
RU2407531C2 |
| ПРИМЕНЕНИЕ ГЕНА СЫВОРОТОЧНОГО АМИЛОИДА А В ДИАГНОСТИКЕ И ЛЕЧЕНИИ ГЛАУКОМЫ И ОПРЕДЕЛЕНИИ АНТИГЛАУКОМАТОЗНЫХ СРЕДСТВ | 2004 |
|
RU2365379C2 |
| Лечение глазных болезней типа дегенерации желтого пятна, глаукомы и диабетической ретинопатии с помощью лекарственных средств, устраняющих стареющие клетки | 2018 |
|
RU2815482C2 |
| ЛЕЧЕНИЕ ГЛАУКОМЫ | 2018 |
|
RU2759998C2 |
Группа изобретений относится к медицине, а именно к офтальмологии, и может быть использована для лечения глаукомы или повышенного внутриглазного давления (ВГД) у пациента. Для этого пациенту вводят эффективное количество композиции, содержащей средство, которое ингибирует связывание PAI-1 с витронектином. Также предложен способ лечения заболевания глаз, связанного с PAI-1. Группа изобретений обеспечивает лечение глаукомы и ВГД за счет уменьшения отделения клеток ткани трабекулярной сети (ТМ) и снижения увеличенного сопротивления оттоку внутриглазной жидкости, также за счет увеличения клеточности ТМ-ткани и сохранения фагоцитоза. 2 н. и 12 з.п. ф-лы, 8 ил., 8 пр., 4 табл.
1. Способ лечения глаукомы или повышенного ВГД у пациента, предусматривающий:
введение пациенту эффективного количества композиции, содержащей средство, которое ингибирует связывание PAI-1 с витронектином.
2. Способ по п.1, где указанная композиция дополнительно содержит соединение, выбранное из группы, состоящей из:
офтальмологически приемлемых консервантов, поверхностно-активных веществ, усилителей вязкости, усилителей проникновения, гелеобразующих средств, гидрофобных оснований, носителей, буферов, натрия хлорида, воды и их комбинаций.
3. Способ по п.1, дополнительно предусматривающий введение в виде либо части указанной композиции, либо отдельного введения соединения, выбранного из группы, состоящей из:
β-блокаторов, аналогов простагландинов, ингибиторов карбоангидразы, α2-агонистов, мистических средств, нейропротекторов, ингибиторов киназы rho и их комбинаций.
4. Способ по п.1, где указанная композиция содержит от приблизительно 0,01 до приблизительно 5% по массе/объему указанного средства.
5. Способ по п.1, где указанная композиция содержит от приблизительно 0,25 до приблизительно 2% по массе/объему указанного средства.
6. Способ по п.1, где указанное средство выбрано из группы, состоящей из ZK4044, PAI-039, WAY-140312, HP-129, T-686, XR5967, XR334, XR330, XR5118, антител к PAI-1, пептидомиметиков PAI-1 и их комбинаций.
7. Способ лечения заболевания глаз, связанного с PAI-1, у субъекта, которому это необходимо, предусматривающий:
введение пациенту эффективного количества композиции, содержащей средство, которое ингибирует связывание PAI-1 с витронектином.
8. Способ по п.7, где субъект страдает глазной гипертензией или глаукомой либо подвергается риску их развития.
9. Способ по п.7, где указанное введение снижает количество активного PAI-1 у указанного субъекта.
10. Способ по п.7, где указанная композиция дополнительно содержит соединение, выбранное из группы, состоящей из:
офтальмологически приемлемых консервантов, поверхностно-активных веществ, усилителей вязкости, усилителей проникновения, гелеобразующих средств, гидрофобных оснований, носителей, буферов, натрия хлорида, воды и их комбинаций.
11. Способ по п.7, дополнительно предусматривающий введение в виде либо части указанной композиции, либо отдельного введения соединения, выбранного из группы, состоящей из:
β-блокаторов, аналогов простагландинов, ингибиторов карбоангидразы, α2-агонистов, мистических средств, нейропротекторов, ингибиторов киназы rho и их комбинаций.
12. Способ по п.7, где указанная композиция содержит от приблизительно 0,01 до приблизительно 5% по массе/объему указанного средства.
13. Способ по п.7, где указанная композиция содержит от приблизительно 0,25 до приблизительно 2% по массе/объему указанного средства.
14. Способ по п.7, где указанное средство выбрано из группы, состоящей из: ZK4044, PAI-039, WAY-140312, HP-129, T-686, XR5967, XR334, XR330, XR5118, антител к PAI-1, пептидомиметиков PAI-1 и их комбинаций.
Авторы
Даты
2012-11-10—Публикация
2007-10-31—Подача