ОБЛАСТЬ ИЗОБРЕТЕНИЯ
В настоящем изобретении представлен способ ТФЭ/ЖХ-МС/МС для количественного определения ризедроната в пробе мочи.
УРОВЕНЬ ТЕХНИКИ
Бисфосфонаты ингибируют резорбцию костей и являются эффективными средствами лечения метаболических заболеваний костей, в том числе остеопороза и болезни Педжета (I. Elomaa, C. Blomqvist, L. Porkka, T.Holmstrom, T.Taube, C.Lamberg-Allardt, G.H. Borgstrom. Lancet 1985; i:1155; J.P. Kosonen, J. Pharm Biomed Anal. 1992; 10:881; J.A. Cantril, H.M. Buckler, D.C. Anderson, Ann. Rheumatol. Dis. 1986; 45:1012; H.Fleisch, Horm. Metab. Res. 1997; 29:145). Предупреждение резорбции костной ткани является следствием ингибирующего воздействия на функции зрелых остеокластов. Известно несколько биоаналитических методов для бифосфонатов. Как правило, эти методы в основном опираются на ионообменную и ион-парную хроматографию с детектированием по УФ, флуоресценцию (с получением производных до или после колонки), проводимости, селективным по фосфору пламенно-фотометрическим детектором, по показателю преломления и светорассеянию (V. Virtanen, L.H.J. Lajunen, J. Chromatogr. 1993; 617:291; V. Virtanem, L.H.J. Lajunen, Talanta 1993; 40: 661; S.E. Meek, D.J. Pietrzyk Anal. Chem. 1988; 60:1397; M.J. Lovdahl, D.J. Pietrzyk, J. Chromatogr. A 1999; 850:143; R. Niemi, H. Taipale, M. Ahlmark, J. Vepsalainen, T. Jarvinen, J. Chromatogr. B 1997; 701:97; T.L. Chester, Anal. Chem. 1980; 52:1621).
Для определения ризедроната в моче человека использовалась методика ГХ/МС в сочетании с ацилированием и силилированием (D.Y. Mitchell, R.A. Eusebio, L.E. Dunlap, K.A. Pallone, J.D. Nesbitt, D.A. Russell, M.E. Clay, P.J. Bekker, Pharm. Res. 1998; 15:228). Более чувствительный метод для анализа ризедроната в моче человека был разработан на основе твердофазного иммуноферментного анализа (ELISA) (D.Y. Mitchell, M.A. Heise, K.A. Pallone, J.D. Nesbilt, M.E. Clay, J.D. Nesbitt, D.A. Russell, C.W. Melson, J. Clin. Pharmacol. 1999; 48:536). Сообщалось также о количественном определении ризедроната в моче человека с помощью ион-парной ВЭЖХ с переключением колонок и УФ-детектированием (P.T. Vallano, S.B. Shugars, W.F. Kline, E.J. Woolf, B.K. Matuszewski, J. Chromatogr. B 1003; 794:23). Несмотря на то что некоторые из этих методов обеспечивали весьма высокую чувствительность, все они очень сложны и трудоемки.
В последнее время более активно разрабатывались методы ЖХ-МС/МС для ризедроната с последующей экстракцией или получением производных на колонке (L.S. Zhu, V.N. Lapko, J.W. Lee, Y.J. Basir, C. Kafonek, R. Olsen, C. Briscoe, Rapid commun. Mass Spectrom. 2006, 20: 3421; S.Turcotte, J. Couture, F. Vallee, AAPS PharmSci Vol. 5, No. 4, Abstract M1357 (2003).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу количественного определения ризедроната в пробе мочи, включающему:
a) добавление внутреннего стандарта к пробе мочи;
b) нанесение пробы мочи на колонку Oasis HLB, предварительно обработанную метанолом;
c) промывку колонки примерно 1% (об.) TEA в воде и примерно 1% (об.) муравьиной кислоты в метаноле;
d) элюирование ризедроната, по крайней мере однократное, смесью примерно 60% (об.) метанола и примерно 40% (об.) воды, содержащей около 3 мМ EDTA, в вакууме;
e) упаривание элюированного раствора и разбавление смесью 10% (об.) метанола и 90% (об.) 0,05 M NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и внутреннего стандарта; и
f) анализ образца смеси в системе ЖХ-МС/МС.
Упомянутый выше способ ТФЭ/ЖХ-МС/МС для количественного определения ризедроната в пробах мочи относительно прост, обладает высокой чувствительностью, является точным и достоверным и более полно обсуждается ниже с помощью приведенных фигур и подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 - ИЭ/МС спектр ризедроната.
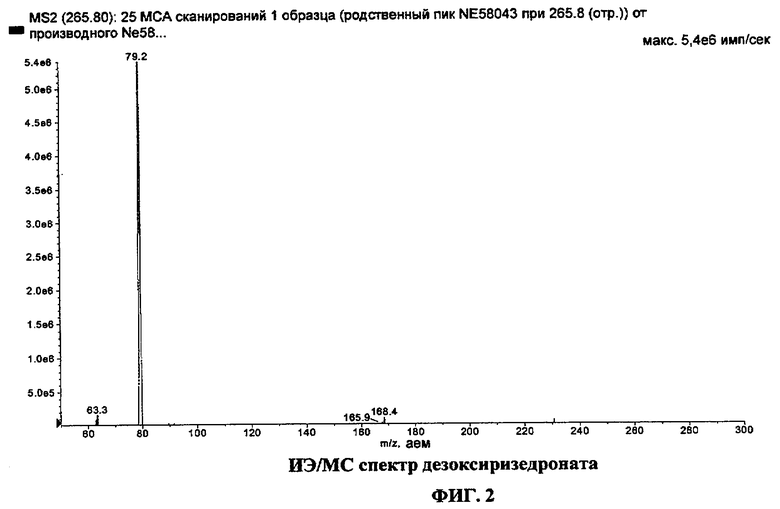
Фиг. 2 - ИЭ/МС спектр дезоксиризедроната.
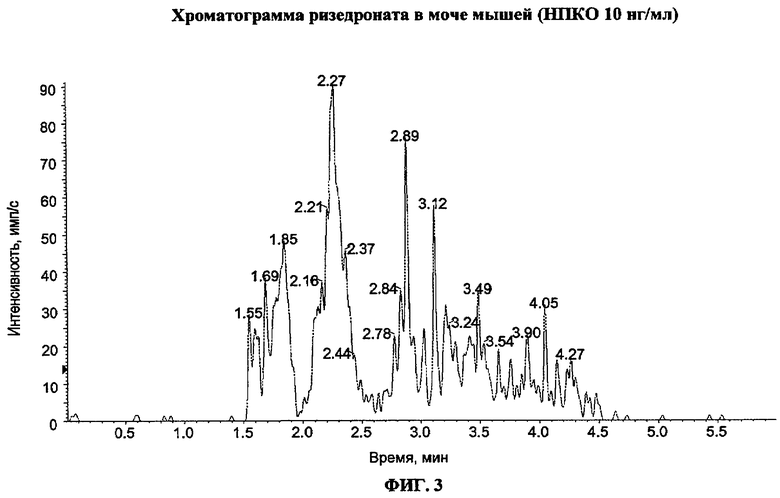
Фиг. 3 - хроматограмма ризедроната в моче мышей (НПКО 10 нг/мл), где интенсивность пика со временем удерживания 2,27 минуты более чем в три раза больше интенсивности того же пика на хроматограмме ВЭЖХ контрольного образца мочи мышей. Это означает, что данный способ позволяет количественно определять концентрацию ризедроната в моче мышей на уровне 10 нг/мл.
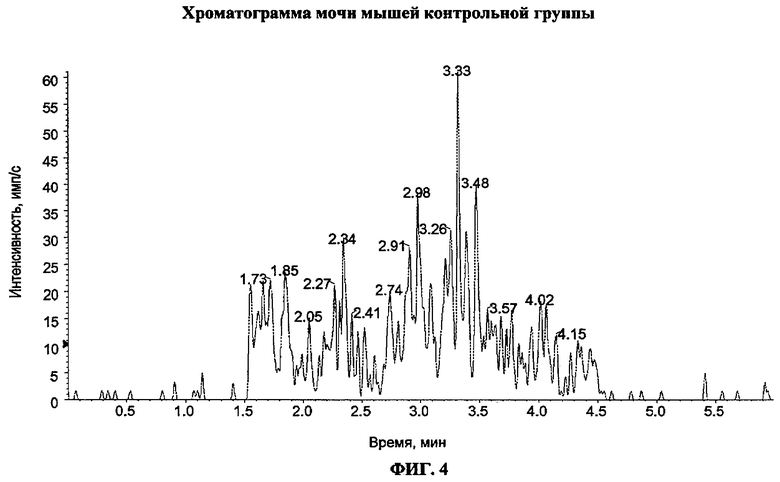
Фиг. 4 - хроматограмма мочи мышей контрольной группы.
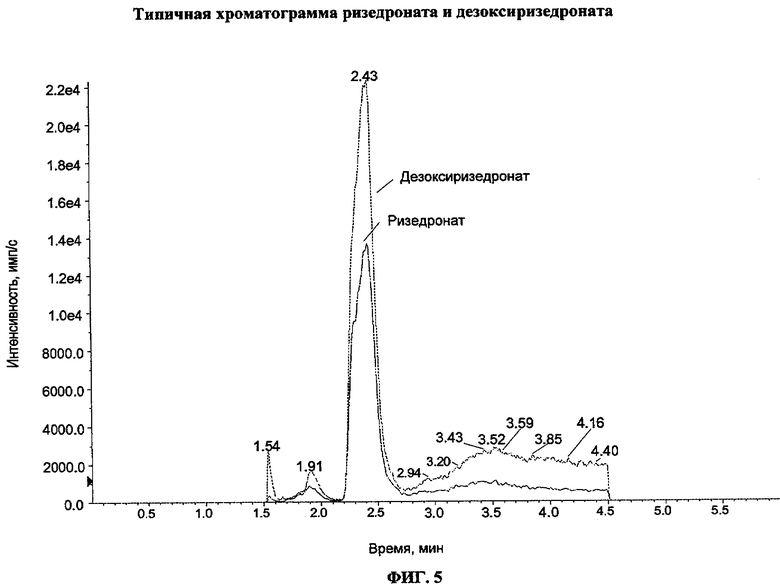
Фиг. 5 - типичная хроматограмма ризедроната и дезоксиризедроната.
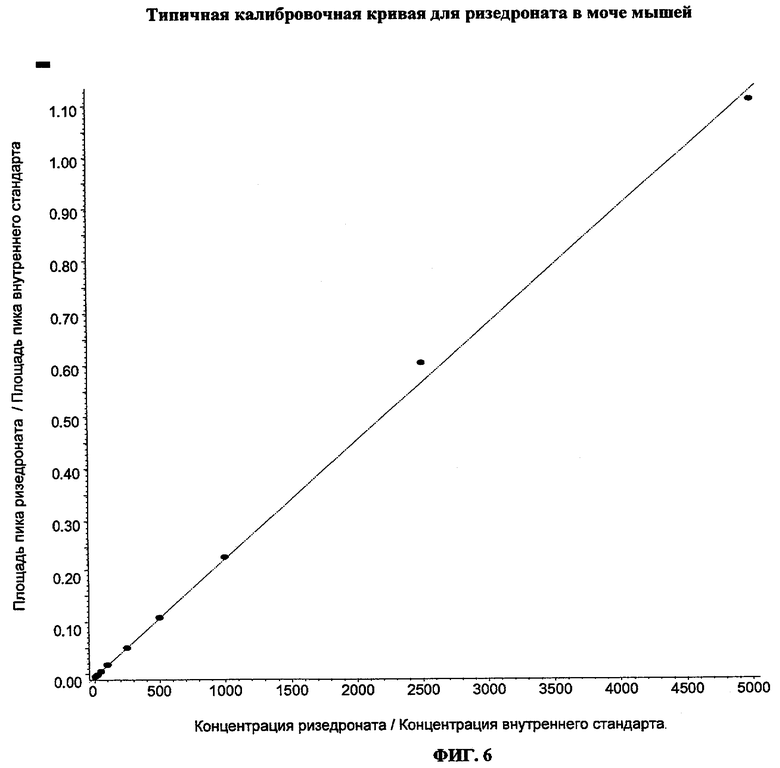
Фиг. 6 - типичная калибровочная кривая для ризедроната в моче мышей.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения и сокращения
Используемые выше и во всем тексте описания изобретения следующие сокращения, если не указано иначе, имеют следующие значения:
аем - атомная единица массы
имп/с - импульсов в секунду
КВ% - коэффициент вариации в процентах
Разн% - разница между теоретической и измеряемой концентрацией в процентах
EDTA - этилендиаминтетрауксусная кислота
ИЭ - ионизация электрораспылением
ВЭЖХ - высокоэффективная жидкостная хроматография
ЖХ/МС - жидкостная хроматография высокого давления/масс-спектрометрия
НПКО - нижний предел количественного определения
КНР - контроль нескольких реакций
МС - масс-спектрометрия
m/z - отношение массы к заряду
NH4Ac - ацетат аммония
NH4OH - гидроксид аммония
СО - стандартное отклонение
ТФЭ - твердофазная экстракция
TEA - триэтиламин
об. - объемное соотношение
Используемые выше и во всем тексте описания изобретения следующие термины, если не указано иначе, имеют следующие принятые значения.
«Дезоксиризедронат» означает (1-фосфоно-2-пиридин-3-илэтил)-фосфоновую кислоту, имеющую следующую химическую структуру:
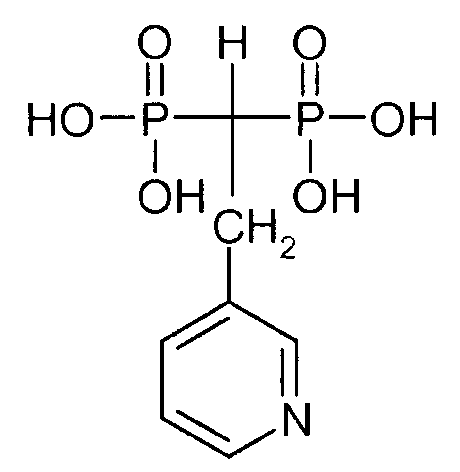
«Колонка Inertsil Phenyl-3 для ВЭЖХ» производится и продается компанией Varian, Inc.
«Внутренним стандартом» называют химическое соединение, которое добавляется в постоянных количествах к образцам, контрольным и калибровочным стандартам для анализа. Данное химическое соединение используется для калибровки посредством построения графика отношения сигнала анализируемого вещества к сигналу внутреннего стандарта как функции от концентрации анализируемого вещества в стандартах. Эта процедура используется для измерения и корректировки с учетом потери анализируемого вещества в процессе подготовки и ввода образца. В частности, внутренним стандартом является соединение, которое по своей химической структуре подобно, но не совпадает с анализируемым веществом.
«Колонка Oasis HLB» производится и продается компанией Waters Corporation. Размер колонки зависит от концентрации ризедроната в пробе мочи. Чем меньше концентрация ризедроната в пробе мочи, тем больше размер колонки, и тем больший объем пробы мочи и раствора для промывки колонки и элюирования ризедроната следует использовать.
«Ризедронат» означает (1-гидрокси-1-фосфоно-2-пиридин-3-илэтил)фосфоновую кислоту, имеющую следующую химическую структуру:
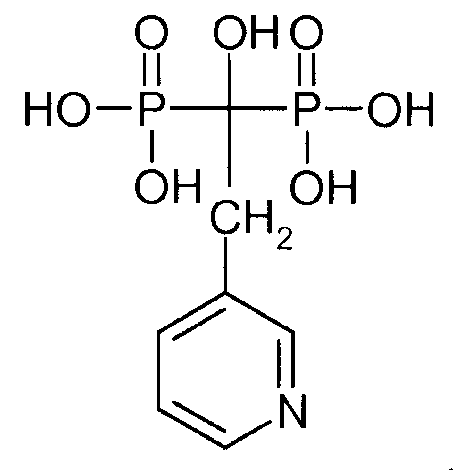
Под «пробой мочи» подразумевают пробу мочи млекопитающих, в том числе пробу мочи человека.
КОНКРЕТНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Одним из конкретных осуществлений настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем под пробой мочи подразумевается проба мочи мыши или крысы.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, где внутренним стандартом является дезоксиризедронат.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, где в качестве колонки Oasis HLB используется колонка Oasis HLB на 30 мг.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, где внутренним стандартом является дезоксиризедронат, который добавляется в виде водного раствора, более точно, в виде водного раствора концентрацией примерно 10 мкг/мл.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем объем пробы мочи составляет примерно 0,4 мл.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, при этом колонку предварительно обрабатывают примерно 1 мл метанола.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, при этом колонку предварительно обрабатывают примерно 1 мл метанола, а затем примерно 0,5 мл 1% (об.) ТЕА в воде.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, при этом колонку промывают примерно 0,5 мл примерно 1% (об.) TEA в воде и примерно 0,5 мл примерно 1% (об.) муравьиной кислоты в метаноле.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем объем смеси примерно 60% (об.) метанола и примерно 40% (об.) воды, содержащей около 3 мМ EDTA, составляет около 1,5 мл.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем ризедронат элюируют дважды примерно 0,75 мл смеси примерно 60% (об.) метанола и примерно 40% (об.) воды, содержащей около 3 мМ EDTA.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем объем смеси примерно 10% (об.) метанола и примерно 90% (об.) 0,05 M NH4Ac-NH4OH буфера составляет около 100 мкл.
Еще одним конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем внутренним стандартом является дезоксиризедронат, и анализ смеси образца в системе ЖХ-МС/МС включает разделение ризедроната и дезоксиризедроната посредством ВЭЖХ на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора A и раствора B, при этом объем раствора A увеличивается примерно с 10% (об.) до примерно 95% (об.), и где раствор A представляет собой примерно 90% (об.) метанола в воде, а раствор B представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2% (об.) триэтиламина.
Другим конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи, причем под пробой мочи подразумевается проба мочи мыши или крысы, включающий:
a) добавление примерно 100 мкл примерно 10 мкг/мл водного раствора дезоксиризедроната к примерно 0,4 мл пробы мочи мыши или крысы;
b) нанесение пробы мочи мышей или крыс на колонку Oasis HLB 30 мг, предварительно обработанную примерно 1 мл метанола, а затем примерно 0,5 мл 1% (об.) ТЕА в воде;
c) промывку колонки примерно 0,5 мл 1% (об.) TEA в воде и примерно 0,5 мл 1% (об.) муравьиной кислоты в метаноле;
d) элюирование ризедроната примерно 1,5 мл смеси примерно 60% (об.) метанола и примерно 40% (об.) воды, содержащей около 3 мМ EDTA, в вакууме;
e) упаривание элюированного раствора и разбавление примерно 100 мкл смеси примерно 10% (об.) метанола и примерно 90% (об.) примерно 0,05 M NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и дезоксиризедроната; и
f) анализ смеси образца в системе ЖХ-МС/МС, где ризедронат и дезоксиризедронат разделяют посредством ВЭЖХ на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора A и раствора B, при этом объем раствора A увеличивается примерно с 10% (об.) до примерно 95% (об.), и где раствор A представляет собой примерно 90% (об.) метанола в воде, а раствор B представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2% (об.) триэтиламина.
Другим конкретным осуществлением настоящего изобретения является способ количественного определения ризедроната в пробе мочи мыши или крысы, включающий:
a) добавление примерно 100 мкл примерно 10 мкг/мл водного раствора дезоксиризедроната к примерно 0,4 мл пробы мочи мышей или крыс;
b) нанесение пробы мочи мышей или крыс на колонку Oasis HLB 30 мг, предварительно обработанную примерно 1 мл метанола, а затем примерно 0,5 мл 1% (об.) ТЕА в воде;
c) промывку колонки примерно 0,5 мл 1% (об.) TEA в воде и примерно 0,5 мл 1% (об.) муравьиной кислоты в метаноле;
d) элюирование ризедроната два раза примерно 0,75 мл смеси примерно 60% (об.) метанола и примерно 40% (об.) воды, содержащей около 3 мМ EDTA, в вакууме;
e) упаривание элюированного раствора и разбавление примерно 100 мкл смеси примерно 10% (об.) метанола и примерно 90% (об.) примерно 0,05 M NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и дезоксиризедроната; и
f) анализ смеси образца в системе ЖХ-МС/МС, где ризедронат и дезоксиризедронат разделяют посредством ВЭЖХ на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора А и раствора B, при этом объем раствора А увеличивается примерно с 10% (об.) до примерно 95% (об.), и где раствор А представляет собой примерно 90% (об.) метанола в воде, а раствор B представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2% (об.) триэтиламина.
Должно быть понятно, что изобретение относится ко всем соответствующим комбинациям конкретных упомянутых при этом вариантов осуществлений.
Осуществления настоящего изобретения будут более очевидны из следующих примеров, которые приводятся только в качестве иллюстрации и не должны рассматриваться как ограничивающие охват изобретения.
ПРИМЕР
Стадия 1: Приготовление стандартных растворов ризедроната в моче с использованием мочи мышей или крыс
Исходный раствор ризедроната 1 мг/мл готовили растворением ризедроната в воде для ВЭЖХ. Стандартные растворы ризедроната в концентрации 250 мкг/мл, 100 мкг/мл и 50 мкг/мл готовили разбавлением 250 мкл, 100 мкл и 50 мкл исходного 1 мг/мл раствора ризедроната до 1 мл водой для ВЭЖХ, соответственно. Соответствующие разбавления стандартных растворов ризедроната 250 мкг/мл, 100 мкг/мл и 50 мкг/мл проводили для того, чтобы получить рабочие растворы ризедроната с концентрацией 25 мкг/мл, 10 мкг/мл, 5 мкг/мл, 2,5 мкг/мл и 1 мкг/мл. Стандартные растворы ризедроната в моче с концентрациями от 10 нг/мл до 2500 нг/мл готовили добавлением 4 мкл каждого рабочего раствора к 0,4 мл мочи контрольных мышей или крыс (то есть мочи мышей или крыс, которые не получали ризедронат).
Стадия 2: Приготовление образца
0,4 мл мочи мыши или крысы, получавшей ризедронат, переносили в стеклянную пробирку размерами 10×75 мм для культивирования тканей. 100 мкл раствора внутреннего стандарта, то есть 10 мкг/мл водного раствора дезоксиризедроната, и 100 мкл 5% ТЕА в воде добавляли ко всем стандартам мочи с ризедронатом и пробам мочи, соответственно.
Экстракцию образца осуществляли на колонке Oasis HLB 30 мг (1 мл, которую производит и продает компания Waters Corporation, № по каталогу: WAT094225). Колонки обрабатывали 1 мл метанола, а затем 0,5 мл 1% TEA в воде. На колонку наносили пробу мочи. Колонку промывали 0,5 мл 1% TEA в воде и 0,5 мл 1% муравьиной кислоты в метаноле, а затем анализируемый раствор и внутренний стандарт элюировали в две последовательные стадии элюирования 0,75 мл смеси 60% метанола в воде, содержащей 3 мМ EDTA. В ходе экстракции образцов для создания потока жидкости через колонки на каждой стадии использовали вакуум (5-15 фунтов на кв. дюйм). Элюированный раствор сушили в атмосфере азота при 37°C в течение 70 минут, а затем остаток разбавляли в 100 мкл смеси 10% метанола/90% 0,05 M NH4Ac-NH4OH буфера (pH 9,26).
Стадия 3: ЖХ-МС/МС анализ
Анализ ризедроната проводили с помощью системы ЖХ-МС/МС API 4000 (продаваемой MDS Sciex), включающей насос Shimadzu LC-10AD, системный контроллер SCL-10A VP, автоматическое устройство ввода пробы Leap Technologies HTS PAL и квадрупольный масс-спектрометр с тройной линзой API 4000.
Ризедронат и внутренний стандарт разделяли на колонке Inertsil Phenyl-3 для ВЭЖХ (3 мкл, 50×030 мм, которую производит и продает компания Varian, Inc., № по каталогу: 0408-050x030) посредством градиентного элюирования смесью раствора A и раствора B в течение 6 минут, при этом объем раствора A увеличивался с 10% до 95%. Раствор A представляет собой 90% метанола в воде, а раствор B - 10 мМ буфер ацетат аммония-уксусная кислота (pH 5,0) с 2% триэтиламина. Расход поддерживали на постоянном уровне 0,2 мл/мин. Образец (10 мкл разбавленного раствора) напрямую вводили в колонку для ВЭЖХ. Масс-спектрометр запрограммирован отслеживать переход m/z 281,9→63,1 для ризедроната в режиме определения отрицательных ионов с энергией столкновения -58 В. Переход m/z 265,8→79,2 используют для измерений внутреннего стандарта дезоксиризедроната. Температура источника установлена на уровне 350°C. Используемое время прогона для анализа составляет 6 минут.
Результаты
Линейность
Зависимость для стандартов ризедроната в моче мышей или крыс является линейной в интервале от 10 до 2500 нг/мл при НПКП 10 нг/мл. Определенная точность при НПКП составляет 14,8% с разбросом 17,8% (n=3). В таблице 1 приводятся параметры регрессии, полученные в ходе проверки. При сопоставлении результатов ежедневного анализа для ризедроната получены коэффициенты корреляции 0,98 или выше. На фиг. 6 приводится характерная калибровочная кривая.
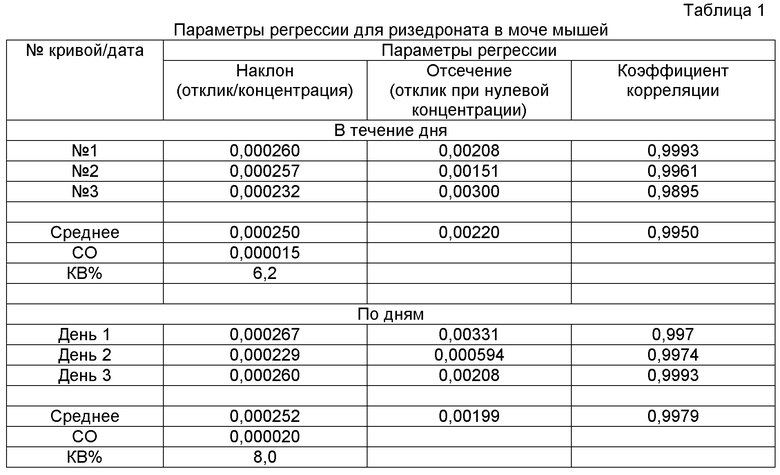
Специфичность
Небольшой пик со временем удерживания 2,27 был зарегистрирован в моче контрольных мышей, но интенсивность пика при НПКП (10 нг/мл) более чем в три раза превышает интенсивность пика в моче контрольных мышей (см. фиг. 3 и фиг. 4). Таким образом, есть возможность количественного определения концентрации ризедроната на уровне 10 нг/мл.
Разброс
Разброс определяется как процент коэффициента вариации измеряемых концентраций для каждого контрольного уровня в ходе исследования. Коэффициент вариации для контрольных образцов мочи мышей в течение одного дня менялся в пределах от 2,2 до 9,6%. Ежедневный разброс для контрольных образцов при 3 уровнях концентрации менялся от 5,2 до 10,3%. Значения разброса для стандартов в течение одного дня и нескольких дней менялись в пределах от 0,3 до 26%.
Точность
Точность анализа выражается как разница в процентах между средней определяемой концентрацией контроля качества и теоретическим значением.
Точность для контрольных образцов мочи мышей в течение одного дня находилась в пределах от -5,3 до 4,4%. Точность в период нескольких дней определяли в течение трех дней анализа с использованием контрольных образцов на 3 уровнях концентрации. Точность в период нескольких дней менялась от -4,0 до 6,0%. Точность обратно рассчитываемых концентраций в стандартах мочи мышей находится в пределах ±15%.
Точность и разброс стандартов калибровки ризедроната
в моче мышей
Точность и разброс образцов контроля качества ризедроната в моче мышей
Выход
Выход ризедроната в экстрагированной моче мышей по сравнению с экстрагированным контролем мочи мышей с добавленным чистым веществом составляет около 51,3%.
Выход ризедроната из проб мочи мышей (250 нг/мл)
Площадь пика пробы с добавленным чистым веществом
Осуществления настоящего изобретения могут принимать другие конкретные формы, которые не будут затрагивать сущности изобретения или его основных положений.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ подготовки пробы мочи для определения монометилфталата, моноэтилфталата, монобутилфталата, монобензилфталата, моноэтилгексилфталата методом высокоэффективной жидкостной хроматографии/масс-спектрометрии | 2019 |
|
RU2687738C1 |
| ВЫСОКОЧУВСТВИТЕЛЬНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВА КОМПОНЕНТОВ, ПОЛУЧЕННЫХ ИЗ ЛЕКАРСТВЕННЫХ ТРАВ | 2011 |
|
RU2558042C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ДИМЕТИЛТЕРЕФТАЛАТА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2010 |
|
RU2425380C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2011 |
|
RU2466406C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ФУМАРОВОЙ И МАЛЕИНОВОЙ КИСЛОТ В ПЛАЗМЕ КРОВИ МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2018 |
|
RU2677341C1 |
| Способ количественного определения антигипертензивных лекарственных веществ в плазме крови | 2022 |
|
RU2803887C1 |
| СПОСОБ ОДНОВРЕМЕННОГО ОПРЕДЕЛЕНИЯ КОМПЛЕКСА АНТИБИОТИКОВ (ТЕТРАЦИКЛИНОВАЯ ГРУППА, ЛЕВОМИЦЕТИН, БАЦИТРАЦИН) В МЯСЕ И МЯСНЫХ ПРОДУКТАХ С ИСПОЛЬЗОВАНИЕМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2019 |
|
RU2729620C1 |
| Способ количественного определения дисульфирама в биологических средах | 2019 |
|
RU2701524C1 |
| Способ количественного определения малонового диальдегида методом ВЭЖХ-МC/МС | 2022 |
|
RU2789058C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БАЦИТРАЦИНА В МЯСЕ И МЯСНЫХ ПРОДУКТАХ С ИСПОЛЬЗОВАНИЕМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2018 |
|
RU2696010C1 |

Изобретение касается способа ТФЭ/ЖХ-МС/МС для количественного определения ризедроната в пробе мочи. Способ включает: a) добавление раствора внутреннего стандарта к пробе мочи; b) нанесение пробы мочи на обработанную хроматографическую колонку, элюирование ризедроната в вакууме; e) упаривание элюированного раствора и разбавление для получения образеца в виде смеси ризедроната и внутреннего стандарта; f) анализ образца смеси в системе жидкостная хроматография высокого давления - масс-спектрометрия/масс-спектрометрия (ЖХ-МС/МС). 3 н. и 13 з.п. ф-лы, 4 табл., 6 ил.
1. Способ количественного определения ризедроната в пробе мочи, включающий:
a) добавление раствора внутреннего стандарта к пробе мочи;
b) нанесение пробы мочи на колонку Oasis® HLB, предварительно обработанную метанолом;
c) промывку колонки примерно 1 об.% триэтаноламина (TEA) в воде и примерно 1 об.% муравьиной кислоты в метаноле;
d) элюирование ризедроната, по крайней мере однократное, смесью примерно 60 об.% метанола и примерно 40 об.% воды, содержащей около 3 мМ этилендиаминтетрауксусной кислоты (EDTA), в вакууме;
e) упаривание элюированного раствора и разбавление смесью 10 об.% метанола и 90 об.% 0,05 М NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и внутреннего стандарта; и
f) анализ образца смеси в системе жидкостная хроматография высокого давления - масс-спектрометрия/масс-спектрометрия (ЖХ-МС/МС).
2. Способ по п.1, в котором пробой мочи является проба мочи мыши или крысы.
3. Способ по п.1, в котором внутренним стандартом является дезоксиризедронат.
4. Способ по п.1, в котором внутренним стандартом является дезоксиризедронат, который добавляется в виде водного раствора.
5. Способ по п.1, в котором внутренним стандартом является дезоксиризедронат, который добавляется в виде водного раствора с концентрацией примерно 10 мкг/мл.
6. Способ по п.1, в котором в качестве колонки Oasis® HLB используется колонка Oasis® HLB на 30 мг.
7. Способ по п.1, в котором объем пробы мочи составляет примерно 0,4 мл.
8. Способ по п.1, в котором колонку предварительно обрабатывают примерно 1 мл метанола.
9. Способ по п.1, в котором колонку предварительно обрабатывают примерно 1 мл метанола, а затем примерно 0,5 мл 1 об.% TEA в воде.
10. Способ по п.1, в котором колонку промывают примерно 0,5 мл 1 об.% TEA в воде и примерно 0,5 мл 1 об.% муравьиной кислоты в метаноле.
11. Способ по п.1, в котором объем смеси примерно 60 об.% метанола и примерно 40 об.% воды, содержащей около 3 мМ EDTA, составляет около 1,5 мл.
12. Способ по п.1, в котором ризедронат элюируют дважды примерно 0,75 мл смеси примерно 60 об.% метанола и примерно 40 об.% воды, содержащей около 3 мМ EDTA.
13. Способ по п.1, в котором объем смеси примерно 10 об.% метанола и примерно 90 об.% 0,05 М NH4Ac-NH4OH буфера составляет около 100 мкл.
14. Способ по п.1, в котором внутренним стандартом является дезоксиризедронат, и анализ смеси образца в системе ЖХ-МС/МС включает разделение ризедроната и дезоксиризедроната посредством высокоэффективной жидкостной хроматографии (ВЭЖХ) на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора А и раствора В, при этом объем раствора А увеличивается примерно с 10 об.% до примерно 95 об.%, и где раствор А представляет собой примерно 90 об.% метанола в воде, а раствор В представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2 об.% триэтиламина.
15. Способ количественного определения ризедроната в пробе мочи мыши или крысы, включающий:
a) добавление примерно 100 мкл примерно 10 мкг/мл водного раствора дезоксиризедроната к примерно 0,4 мл пробы мочи мышей или крыс;
b) нанесение пробы мочи мышей или крыс на колонку Oasis® HLB 30 мг, предварительно обработанную примерно 1 мл метанола, а затем примерно 0,5 мл 1 об.% TEA в воде;
c) промывку колонки примерно 0,5 мл 1 об.% TEA в воде и примерно 0,5 мл 1 об.% муравьиной кислоты в метаноле;
d) элюирование ризедроната примерно 1,5 мл смеси примерно 60 об.% метанола и примерно 40 об.% воды, содержащей около 3 мМ EDTA, в вакууме;
e) упаривание элюированного раствора и разбавление примерно 100 мкл смеси примерно 10 об.% метанола и примерно 90 об.% примерно 0,05 М NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и дезоксиризедроната; и
f) анализ смеси образца в системе ЖХ-МС/МС, где ризедронат и дезоксиризедронат разделяют посредством ВЭЖХ на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора А и раствора В, при этом объем раствора А увеличивается примерно с 10 об.% до примерно 95 об.%, и где раствор А представляет собой примерно 90 об.% метанола в воде, а раствор В представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2 об.% триэтиламина.
16. Способ количественного определения ризедроната в пробе мочи мыши или крысы, включающий:
a) добавление примерно 100 мкл примерно 10 мкг/мл водного раствора дезоксиризедроната к примерно 0,4 мл пробы мочи мышей или крыс;
b) нанесение пробы мочи мышей или крыс на колонку Oasis® HLB 30 мг, предварительно обработанную примерно 1 мл метанола, а затем примерно 0,5 мл 1 об.% TEA в воде;
c) промывку колонки примерно 0,5 мл 1 об.% TEA в воде и примерно 0,5 мл 1 об.% муравьиной кислоты в метаноле;
d) элюирование ризедроната два раза примерно 0,75 мл смеси примерно 60 об.% метанола и примерно 40 об.% воды, содержащей около 3 мМ EDTA, в вакууме;
e) упаривание элюированного раствора и разбавление примерно 100 мкл смеси примерно 10 об.% метанола и примерно 90 об.% примерно 0,05 М NH4Ac-NH4OH буфера, чтобы получить образец в виде смеси ризедроната и дезоксиризедроната; и
f) анализ смеси образца в системе ЖХ-МС/МС, где ризедронат и дезоксиризедронат разделяют посредством ВЭЖХ на колонке Inertsil Phenyl-3 градиентным элюированием смесью раствора А и раствора В, при этом объем раствора А увеличивается примерно с 10 об.% до примерно 95 об.%, и где раствор А представляет собой примерно 90 об.% метанола в воде, а раствор В представляет собой примерно 10 мМ буфера ацетат аммония-уксусная кислота с 2 об.% триэтиламина.
| WO 2006127973 A2, 30.11.2006 | |||
| FABRIZIO BRUNER | |||
| The science of chromatography: lectures | |||
| Urbino, May 27-31, 1985, p.224-225 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2012-11-20—Публикация
2008-03-05—Подача