Область техники, к которой относится изобретение
Настоящее изобретение относятся к продуцирующим инозин микроорганизмам, принадлежащим к роду Corynebacterium, и способу получения инозина, включающему культивирование микроорганизмов, продуцирующих инозин.
Предшествующий уровень техники
Инозин является жизненно важным веществом, участвующим в химическом синтезе и катализируемом ферментами синтеза 5'-инозиновой кислоты, который привлекает усиленное внимание как острая приправа. Кроме того, инозин, который является промежуточным соединением в каскаде реакций биосинтеза нуклеиновой кислоты, играет физиологически значимую роль в организмах животных и растений и широко используется в различных областях, включая пищевую и медицинскую промышленность.
Инозин обычно получают ферментацией с использованием микроорганизмов, таких как Bacillus (Agric. Biol. Chem., 46, 2347 (1992); патент Кореи №27280) или Corynebacterium ammoniagenus (Agric. Biol. Chem., 42, 399 (1978)), или термическим разложением 5'-инозиновой кислоты (патентная публикация с открытой выкладкой №43-3320, Япония). Однако в случае термического разложения 5'-инозиновой кислоты для разложения 5'-инозиновой кислоты требуется большое количество тепла, и поэтому такой способ трудно применять на практике. Для прямой ферментации разработаны и исследованы различные штаммы Е.coli (Biosci. Biotechnol. Biochem., 2001, Mar, 65(3): 570-8). Однако титр продуцирующих инозин штаммов низкий, и поэтому затраты на получение инозина являются высокими. Кроме того, поиск путей получения инозина сосредоточен на штаммах Bacillus и Е.coli.
Таким образом, все еще существует потребность в создании штаммов микроорганизмов, способных продуцировать инозин с высоким выходом и накапливать инозин в высокой концентрации, и способе получения инозина с использованием таких штаммов.
Поэтому авторы продолжили исследование способа получения инозина с высоким выходом/в высокой концентрации, сконцентрировавшись на прямой ферментации с использованием микроорганизмов, и в результате как настоящее изобретение создали микроорганизм, продуцирующий инозин с высоким выходом/в высокой концентрации.
Сущность изобретения
Одно или несколько воплощений настоящего изобретения относятся к микроорганизму рода Corynebacterium, который продуцирует инозин с высоким выходом/в высокой концентрации, в котором путь катаболизма инозина блокируется, и микроорганизм является «текучим» (leaky) ауксотрофом по аденину и также текучим ауксотрофом по гуанину.
Одно или несколько воплощений настоящего изобретения относятся к способу получения инозина с высоким выходом/в высокой концентрации, включающему культивирование микроорганизма.
Краткое описание фигур
Вышеуказанные и другие особенности и преимущества настоящего изобретения станут более явными из подробного описания примеров его воплощения со ссылкой на прилагаемые чертежи, из которых:
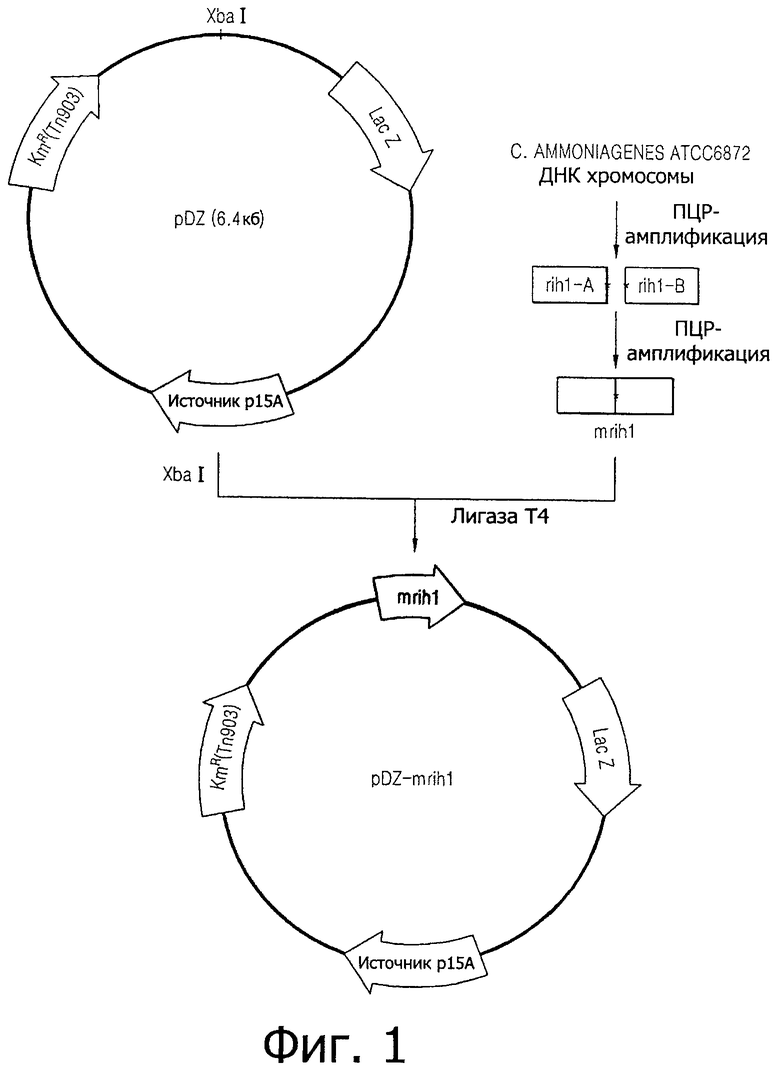
на фиг.1 показана схема конструирования вектора pDZmrih1 для разрыва структуры гена, кодирующего рибонуклеозид-гидролазу 1; и
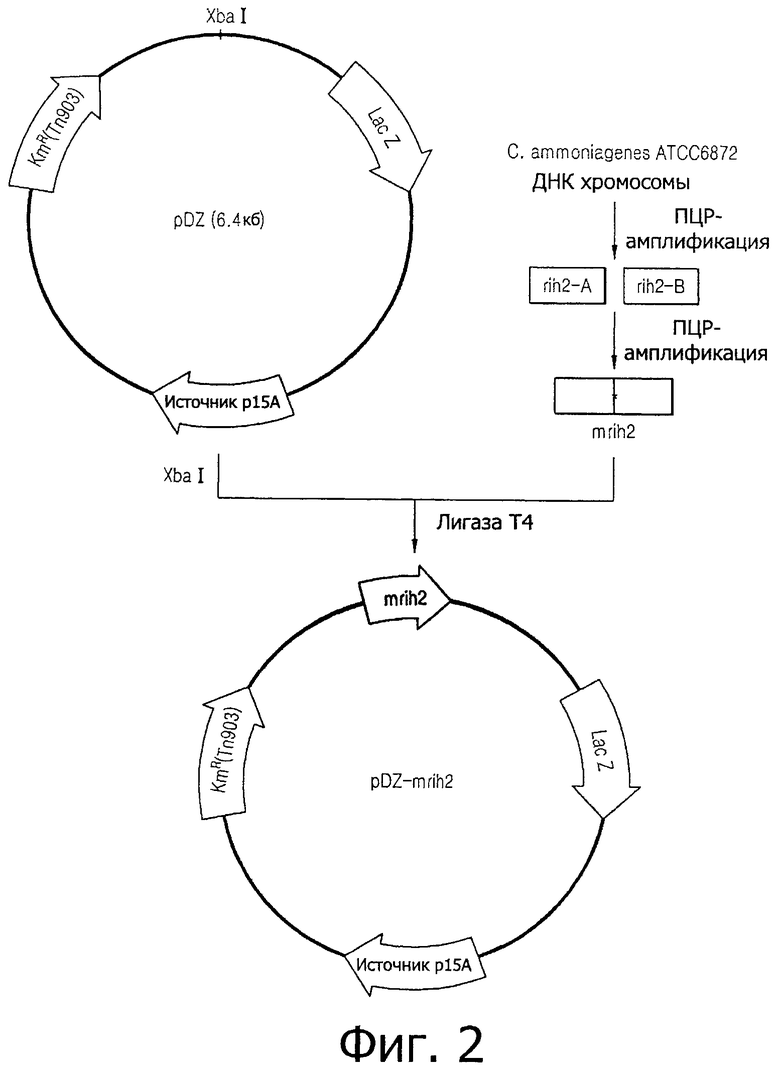
на фиг.2 показана схема конструирования вектора pDZmrih2 для разрыва структуры гена, кодирующего рибонуклеозид-гидролазу 2.
Подробное описание изобретения
Теперь настоящее изобретение будет описываться подробно со ссылками на прилагаемые чертежи.
Настоящее изобретение относится к микроорганизму рода Corynebacterium, имеющему способность продуцировать инозин с высоким выходом/в высокой концентрации, в котором путь катаболизма инозина блокируется, и микроорганизм имеет текучий ауксотрофный фенотип по аденину. Микроорганизм также может иметь текучий ауксотрофный фенотип по гуанину.
В микроорганизме рода Corynebacterium, продуцирующем инозин, каскад реакций катаболизма инозина блокируется генетической рекомбинацией. Иными словами, ген, кодирующий рибонуклеозид-гидролазу (rih) 1, и ген, кодирующий rih 2, инактивируются вариацией последовательности, вызванной встраиванием, делецией или заменой основания. В то же время микроорганизм рода Corynebacterium может иметь текучий ауксотрофный фенотип по аденину и/или текучий ауксотрофный фенотип по гуанину, отобранные искусственным мутагенезом.
Примеры микроорганизма рода Corynebacterium включают Corynebacterium glutamicum, Corynebacterium efficiens, Corynebacterium diphtheriae и Corynebacterium ammoniagenes. Предпочтительно микроорганизм рода Corynebacterium может представлять собой Corynebacterium ammoniagenes, предпочтительнее, Corynebacterium ammoniagenes CN04-0027, происходящий от Corynebacterium ammoniagenes ATCC 6872. Родительский штамм Corynebacterium ammoniagenes ATCC 6872, который является штаммом Corynebacterium ammoniagenes дикого типа, предоставляемым Американской коллекцией типовых культур, не продуцирует инозин.
Corynebacterium ammoniagenes CN04-0027 (KCCM 10905) может накапливать инозин в высокой концентрации с высоким выходом непосредственно в культуре, так как он имеет разорванный ген rih1, кодирующий rih1, и ген rih2, кодирующий rih2, причем посредством этого блокируется путь, разрушающий инозин, и в то же время имеет текучий ауксотрофный фенотип по аденину и текучий ауксотрофный фенотип по гуанину.
Среда, используемая для культивирования микроорганизма рода Corynebacterium, которая описана в подробном описании, включающем примеры, может представлять собой питательную среду, минимальную среду, посевную среду или среду для ферментации в колбах, и пример состава такой среды показан ниже в таблице 1. Однако состав среды не ограничивается примерами, приведенными в таблице 1, и может соответствовать любой среде для культивирования, подходящей для использования при культивировании микроорганизма рода Corynebacterium, которую можно использовать.
Микроорганизм рода Corynebacterium может представлять собой мутантный штамм с усиленной продуктивностью инозина, полученный способом, в котором структуры генов rih1 и rih2, которые кодируют, соответственно, rih1 и rih2, разорваны с целью блокирования пути катаболизма инозина и накопления инозина в культуре организма; к микроорганизму применяют искусственный мутагенез для того, чтобы отобрать текучий ауксотроф по аденину, и затем подтверждают текучий ауксотроф по гуанину.
Микроорганизм рода Corynebacterium может представлять собой рекомбинантный штамм Corynebacterium ammoniagenes ATCC 6872, который получают трансформацией с помощью рекомбинантного вектора, несущего гены rih1 и rih2, которые уже опубликованы одним из специалистов в данной области техники, которым принадлежит настоящее изобретение, с преждевременной мутацией терминации, созданной встраиванием, делецией или заменой основания, где трансляция генов rih1 и rih2 осуществлена не должным образом, что ведет к инактивации рибонуклеозид-гидролазы 1 и рибонуклеозид-гидролазы 2, ферменты rih1 и rih2 инактивируются, и таким образом блокируется путь катаболизма инозина.
В рекомбинантном штамме, в котором каскад реакций катаболизма инозина блокирован, гены rih1 и rih2, которые инактивированы из-за вариации последовательностей, могут иметь последовательность, показанную SEQ ID NO:9 и SEQ ID NO:10, соответственно.
В воплощении настоящего изобретения, кроме того, к рекомбинантному штамму, в котором каскад реакций разрушения инозина блокирован текучим ауксотрофным фенотипом по аденину, можно применить рентгеновское или УФ-излучение или химический мутаген, такой как N-метил-N-нитроN-нитрозогуанин, диэтилсульфид или этиламин. После обработки рекомбинантного штамма химическим мутагеном штамм высевают на минимальную среду состава, показанного в таблице 1, и отбирают отдельные колонии, показывающие текучий ауксотрофный фенотип по аденину, которые растут в среде без аденина, но растут быстрее в среде, включающей аденин. Затем каждую отдельную колонию культивируют в питательной среде с последующим культивированием в посевной среде в течение 24 часов и затем культивируют в среде для ферментации в течение 5-6 суток, и из полученных штаммов штамм с наивысшей продуктивностью по инозину, накопленному в ферментационной культуре, можно отобрать как текучий ауксотрофный штамм по аденину, в котором путь катаболизма инозина блокирован.
Кроме того, отобранный штамм с текучим ауксотрофным фенотипом по аденину можно подвергнуть мутагенезу, описанному выше, в котором штамм обрабатывают химическим мутагеном, причем отбирают штаммы, показывающие текучий ауксотрофный фенотип по гуанину, каждый штамм культивируют в питательной среде, посевной среде и среде для ферментации, и затем штамм с наивысшей продуктивностью по инозину, накопленному в ферментационной культуре, отбирают как продуцирующий инозин микроорганизм с текучим ауксотрофным фенотипом по аденину и гуанину, в котором блокирован путь катаболизма инозина.
Настоящее изобретение также относится к способу получения инозина, который включает культивирование микроорганизма рода Corynebacterium, в котором блокирован путь катаболизма инозина, и который имеет текучий ауксотрофный фенотип по аденину и гуанину и продуцирует инозин в высокой концентрации с высоким выходом, для получения инозина в микроорганизме или культуре; и извлечение инозина из микроорганизма или культуры.
В способе получения инозина микроорганизм рода Corynebacterium могут представлять собой Corynebacterium ammoniagenes CN04-0027 (KCCM 10905).
Способ получения инозина включает культивирование микроорганизма рода Corynebacterium для получения инозина в микроорганизме или культуре.
При культивировании микроорганизма рода Corynebacterium штамм Corynebacterium культивируют в типичной среде, содержащей соответствующие количества источника углерода, источника азота, аминокислоту, витамин или другие питательные вещества, при регулируемых температуре и рН в аэробных условиях.
В этом отношении источник углерода может представлять собой углевод, такой как глюкоза или стерилизованная предварительно обработанная меласса (т.е. меласса, превращенная в редуцирующий сахар), источник азота может представлять собой любой неорганический источник азота, такой как аммиак, хлорид аммония или сульфат аммония; или органический источник азота, такой как пептон, NZ-амин, мясной экстракт, дрожжевой экстракт, кукурузный экстракт, гидролизат казеина, рыба или продукты ее разложения или обезжиренный соевый жмых или продукты его разложения. В качестве минералов можно использовать KH2PO4, K2HPO4, сульфат магния, сульфат железа, сульфат марганца или карбонат кальция (СаСО3), и если желательно, можно добавлять витамины и основания, которые требуются для ауксотрофа.
Культивирование можно осуществлять в аэробных условиях, например, при встряхивании культуры или аэрированном перемешивании культуры при температуре в интервале 28-36°С. Во время процесса культивирования можно поддерживать рН среды при рН 6 - рН 8. Культивирование можно осуществлять в течение 5-6 суток, и инозин, накопленный прямой ферментацией, можно анализировать HPLC.
Одно или несколько воплощений настоящего изобретения теперь будут описываться полнее с обращением к следующим далее примерам. Однако указанные примеры приводятся только в целях пояснения и не предназначены для ограничения объема настоящего изобретения.
Сведения, подтверждающие возможность осуществления изобретения
Пример 1. Создание штамма, в котором структура гена rih разорвана с использованием вектора pDZ для встраивания в хромосому
Для того чтобы гены, кодирующие rih1 и rih2, инактивировать, вызывая изменение последовательности в генах путем встраивания, замены или делеции так, что блокируется путь разрушения инозина, в качестве рекомбинантного вектора используют вектор pDZ, образованный от вектора pACYC177 (New England Biolab, GenBank, инвентарный №X06402), плазмидный клонирующий вектор Е.coli (публикация патента Кореи №07-94433).
На фиг.1 показана схема конструирования вектора pDZmrih1 для разрыва структуры гена, кодирующего rih1. Фиг.2 отображает процесс конструирования вектора pDZmrih2 для разрыва структуры гена, кодирующего rih2.
Для того чтобы амплифицировать ген, кодирующий rih1, и ген, кодирующий rih2, сначала осуществляют ПЦР (PCR) с использованием хромосомной ДНК Corynebacterium ammoniagenes ATCC 6872 в качестве матрицы и праймеров, имеющих последовательности SEQ ID NO:1-4, и праймеров, имеющих последовательности SEQ ID NO:5-8, соответственно.
Подробнее, осуществляют ПЦР гена, кодирующего rih1, с использованием хромосомной ДНК Corynebacterium ammoniagenes ATCC 6872 в качестве матрицы и праймеров, имеющих последовательности SEQ ID NO:1 и 2, и праймеров, имеющих последовательности SEQ ID NOs:3 и 4, соответственно, и получают фрагмент rih1-А и фрагмент rih1-В. Затем осуществляют ПЦР с использованием полученных фрагментов rih1-А и rihl-В в качестве матрицы и использованием праймеров SEQ ID NO:1 и 4, и получают фрагмент мутантного гена с вариацией последовательности, т.е. mrih1. Кроме того, для того, чтобы получить фрагмент мутантного гена mrih2 с изменением последовательности в rih2, осуществляют ПЦР гена, кодирующего rih2, с использованием хромосомной ДНК Corynebacterium ammoniagenes ATCC 6872 в качестве матрицы, и праймеров SEQ ID NO:5 и 6 и праймеров SEQ ID NO:7 и 8, соответственно, и получают фрагмент rih2-А и фрагмент rih2-B, и осуществляют ПЦР с использованием полученных фрагментов rih2-A и rih2-B в качестве матрицы и использованием праймеров SEQ ID NO: 5 и 8. Условия ПЦР, осуществляемой для получения фрагментов rih1-A, rih1-B, rih2-A и rih2-B, следующие: начальная денатурация при 94°С в течение 5 минут; 20 циклов денатурации при 94°С в течение 30 секунд, отжиг при 52°С в течение 30 секунд, и наращивание при 72°С в течение 1 минуты: и заключительное наращивание при 72°С в течение 7 минут. Условия ПЦР, осуществляемой для получения фрагментов мутантных генов путем комбинирования фрагментов rih1 А и В и фрагментов rih2 А и В, соответственно, следующие: начальная денатурация при 94°С в течение 5 минут; 25 циклов денатурации при 94°С в течение 30 секунд, отжиг при 50°С в течение 30 секунд, и наращивание при 72°С в течение 1 минуты: и заключительное наращивание при 72°С в течение 7 минут. Амплифицированные mrih1, mrih2 и вектор pDZ гидролизуют с рестриктазой Xbal и затем для получения рекомбинантного вектора pDZmrih1 и pDZmrih2 лигируют вместе лигазой Т4.
Для того чтобы мутировать последовательность гена rih2 на хромосоме Corynebacterium путем делеции основания, используют сконструированный вектор pDZmrih2 для трансформации Corynebacterium ammoniagenes ATCC 6872 дикого типа посредством электропорации (способ трансформации, раскрытый в Appl. Microbiol. Biotechnol. (1999), 52: 541-545). Затем трансформированные штаммы, в которых вектор pDZmrih2 встроен в хромосому посредством гомологичной рекомбинации с геном rih2, отбирают в среде для отбора, содержащей 25 мг/л канамицина. Успешное встраивание вектора pDZmrih2 в хромосому подтверждают путем оценки того, показывают ли колонии синее окрашивание на твердой среде, содержащей X-gal (5-бром-4-хлор-3-индолил-β-D-галактозид). Каждый штамм, в котором в хромосому посредством гомологичной рекомбинации встроен вектор pDZmrih2, культивируют при встряхивании в питательной среде при 30°С в течение 8 часов, и культивированный штамм серийно разводят от 10-4 до 10-10, и затем разведенную культуру высевают на твердую среду, содержащую X-gal. Большинство колоний показывают синий цвет, но также на небольшом уровне существуют белые колонии. В связи с этим, посредством отбора белых колоний отбирают штаммы, в которых последовательность вектора pDZmrih2 удалена из хромосомы при втором кроссинговере. В результате получают штамм, в котором делетирован 262-ой G гена rih2 в хромосоме Corynebacterium ammoniagenes ATCC 6872. Затем, для того, чтобы мутировать последовательность гена rih1 путем замены основания, используют вектор pDZmrih2 для трансформации штамма, полученного выше, который имеет делецию в последовательности гена rih2, и осуществляют процесс отбора с использованием того же способа, который использовали при отборе мутантного штамма гена rih2, и получают Corynebacterium ammoniagenes CN04-0092, в котором 148-ой G гена rih1 заменен на Т, посредством чего блокируется путь разрушения инозина. Отобранный штамм окончательно идентифицируют испытанием на чувствительность к канамицину и анализом последовательности гена методом ПЦР. Мутированные ген rih1 и ген rih2 штамма соответственно имеют последовательности SEQ ID NO:9 и SEQ ID NO:10.
Пример 2. Отбор мутантного штамма CN04-0093, имеющего текучий ауксотрофный фенотип по аденину
Corynebacterium ammoniagenes CN04-0092, полученный в примере 1, суспендируют в фосфатном буфере (рН 7,0) или цитратном буфере (рН 5,5) в концентрации 107-108 клеток/мл, к полученной суспензии добавляют N-метил-N-ниро-N-нитрозогуанин до конечной концентрации 10-50 мкг/мл, и полученную смесь выдерживают при комнатной температуре или 30-32°С в течение 40-90 минут для того, чтобы вызвать мутацию. Клетки, полученные после центрифугирования, промывают три раза 0,85% солевым раствором, полученные клетки соответствующим образом разводят в минимальной среде состава, показанного в таблице 1, содержащей 2% агара, высевают и культивируют при 30-34°С в течение 4-5 суток, и получают колонии. Полученные колонии переносят в среду без аденина и среду, содержащую 100 мг/л аденина, соответственно, и культивируют в указанных средах в течение 3-4 суток, и затем отбирают колонии, которые растут в среде без аденина и быстрее растут в среде, содержащей 100 мг/л аденина. После того как отобранные колонии идентифицированы как штаммы, имеющие текучий ауксотрофный фенотип по аденину, каждую полученную колонию культивируют в питательной среде, состав которой показан в таблице 1, культивируют в посевной среде в течение 24 часов и культивируют в среде для ферментации в течение 5-6 суток. Через процесс культивирования отбирают штамм, имеющий наивысшую продуктивность по инозину, и называют его Corynebacterium ammoniagenes CN04-0093.
Пример 3. Отбор мутантного штамма CN04-0027 (KCCM 10905), имеющего ликовый гуанинауксотрофный фенотип
Corynebacterium ammoniagenes CN04-0093, полученный в примере 2, суспендируют в фосфатном буфере (рН 7,0) или цитратном буфере (рН 5,5) в концентрации 107-108 клеток/мл, к полученной суспензии добавляют N-метил-N-ниро-N-нитрозогуанин до конечной концентрации 10-50 мкг/мл и выдерживают при комнатной температуре или 30-32°С в течение 40-90 минут для того, чтобы вызвать мутацию. Клетки, полученные после центрифугирования, промывают три раза 0,85% солевым раствором, полученные клетки соответствующим образом разводят в минимальной среде состава, показанного в таблице 1, содержащей 2% агара, высевают и затем культивируют при 30-34°С в течение 4-5 суток, и получают колонии. Полученные колонии переносят в среду без гуанина и среду, содержащую 100 мг/л гуанина, соответственно, и культивируют в указанных средах в течение 3-4 суток, и затем отбирают колонии, которые растут в среде без гуанина и быстрее растут в среде, содержащей 100 мг/л гуанина. Каждую полученную колонию культивируют в питательной среде, состав которой показан в таблице 1, культивируют в посевной среде в течение 24 часов и культивируют в среде для ферментации в течение 5-6 суток. Через процесс культивирования отбирают штамм, имеющий наивысшую продуктивность по инозину. Отобранный Corynebacterium ammoniagenes, в котором блокирован путь разрушения инозина, и который имеет текучий ауксотрофный фенотип по аденину и гуанину и продуцирует инозин в высокой концентрации с высоким выходом, называют Corynebacterium ammoniagenes CN04-0027. Corynebacterium ammoniagenes CN04-0027 депонирован 20 декабря 2007 по Будапештскому договору в Корейском центре культур микроорганизмов, расположенном в Hongje 1-dong, Seodaemun-gu, Seoul, под инвентарным № KCCM 10905.
Пример 4. Титр после ферментации в колбе Эрленмейера
Каждые 3 мл посевной среды состава, указанного в таблице 1, помещают в пробирки диаметром 18 мм каждая и стерилизуют под давлением при 120°С в течение 10 минут. Затем Corynebacterium ammoniagenes ATCC 6872, Corynebacterium ammoniagenes CN04-0092, в котором разорваны гены rih1 и rih2, и который имеет текучий ауксотрофный фенотип по аденину, и Corynebacterium ammoniagenes CN04-0027, в котором разорваны гены rih1 и rih2, и который имеет текучий ауксотрофный фенотип по аденину и гуанину, соответственно вносят в пробирки, и каждый штамм культивируют при встряхивании при 37°С в течение 24 часов для использования в качестве культуры для посева. Каждые 27 мл среды для ферментации состава, указанного в таблице 1, распределяют в 250-мл колбы Эрленмейера и стерилизуют под давлением при 120°С в течение 10 минут, и каждые 3 мл культуры для посева вносят в 250-мл колбы Эрленмейера и культивируют в них при встряхивании в течение 5-6 суток. Число оборотов используемой встряхивающей камеры составляет 220 об/мин, и встряхивающую камеру доводят до температуры 32°С и рН 7,2. В результате культивирования количество инозина, накопленного в среде исходного штамма Corynebacterium ammoniagenes ATCC 6872, составляет 0 г/л, и количество инозина, накопленного в среде Corynebacterium ammoniagenes CN04-0092, составляет 1 г/л. Кроме того, количество инозина, накопленного в среде Corynebacterium ammoniagenes CN04-0093 с текучим ауксотрофным фенотипом по аденину, составляет примерно на 2 г/л больше, чем в случае Corynebacterium ammoniagenes CN04-0092, и Corynebacterium ammoniagenes CN04-0027 с текучим ауксотрофным фенотипом по аденину и гуанину продуцирует примерно 5 г/л инозина, что примерно на 2 г/л больше, чем в случае Corynebacterium ammoniagenes CN04-0093. Продуктивность каждого штамма по инозину приводится ниже в таблице 2.
Как описано выше, согласно одному или нескольким воплощениям настоящего изобретения, когда инозин получают с использованием Corynebacterium ammoniagenes CN04-0027 (КССМ 10905), высокую концентрацию инозина с высоким выходом можно получить прямой ферментацией, и затраты на получение могут быть снижены из-за снижения расхода сахаров.
Хотя настоящее изобретение определенно показано и описано с обращением к примерам его воплощения, специалистам в данной области техники будет понятно, что можно осуществить различные изменения в их форме и деталях без отхода от сущности и объема настоящего изобретения, определенных приведенной далее формулой изобретения.
Представленные изобретения относятся к области биотехнологии и касаются штамма Corynebacterium ammoniagenes, продуцирующего инозин и способа получения инозина при использовании такого штамма. Описанный штамм депонирован в КССМ под номером 10905 и имеет блокированный каскад реакций катаболизма инозина, вследствие инактивации генов, кодирующих рибонуклеозид-гидролазу 1 и 2. Способ получения инозина включает культивирование такого штамма с последующим извлечением. Представленная группа изобретений позволяет получать инозин с высоким выходом и в высокой концентрации. 2 н.п. ф-лы, 2 ил., 2 табл., 4 пр.
1. Штамм микроорганизма Corynebacterium ammoniagenes CN04-0027 (KCCM 10905), продуцирующий инозин.
2. Способ получения инозина, включающий культивирование микроорганизма по п.1 или 2 для получения инозина в микроорганизме или культуре и извлечение инозина из микроорганизма или культуры.
| HYUN-SOO KIM et al., Genes encoding ribonucleoside hyrolase 1 and 2 from Corynebacterium ammoniagenes, Microbiology, 2006, Vol.152, p.p.1169-1177 | |||
| WO 02051984 A1, 04.07.2002. |
Авторы
Даты
2012-12-10—Публикация
2009-01-02—Подача