Изобретение относится к области медицины, конкретно к онкологии, и может быть использовано для повышения эффективности цитостатического лечения больных со злокачественными опухолями.
Применение цитостатиков в высоких дозах сопровождается развитием токсических реакций (угнетение кроветворения, иммунодепрессия, поражение слизистой желудочно-кишечного тракта и т.д.), которые лимитируют их использование. Повышение противоопухолевой и антиметастатической активности противоопухолевых препаратов и тем самым снижение их токсичности на здоровые, неповрежденные опухолевым процессом органы и ткани является актуальной проблемой для клинической онкологии.
Порошок корневищ аира является одним из компонентов препаратов «Викалин» и «Викаир», которые используют для лечения гастритов, а также язвенной болезни желудка и двенадцатиперстной кишки [3].
Задачей, решаемой настоящим изобретением, является расширение арсенала средств, повышающих противоопухолевую и антиметастатическую активность цитостатиков.
Для решения этой задачи применяют галактозосодержащие пектины, полученные из корневищ аира болотного (Acorus calamus L.).
Новым является то, что в качестве средств, повышающих противоопухолевую и антиметастатическую активность цитостатических препаратов, применяют галактозосодержащие пектины из корневищ аира болотного.
Новые свойства явным образом не следуют из уровня техники в данной области и неочевидны для специалистов. В научно-медицинской и патентной литературе не найдено сведений о способности галактозосодержащих пектинов повышать эффективность цитостатической терапии.
Предлагаемое изобретение может быть использовано в онкологической практике с целью повышения эффективности цитостатической терапии.
Исходя из вышеизложенного следует считать предлагаемое изобретение соответствующим условиям патентоспособности: «Новизна», «Изобретательский уровень», «Промышленная применимость».
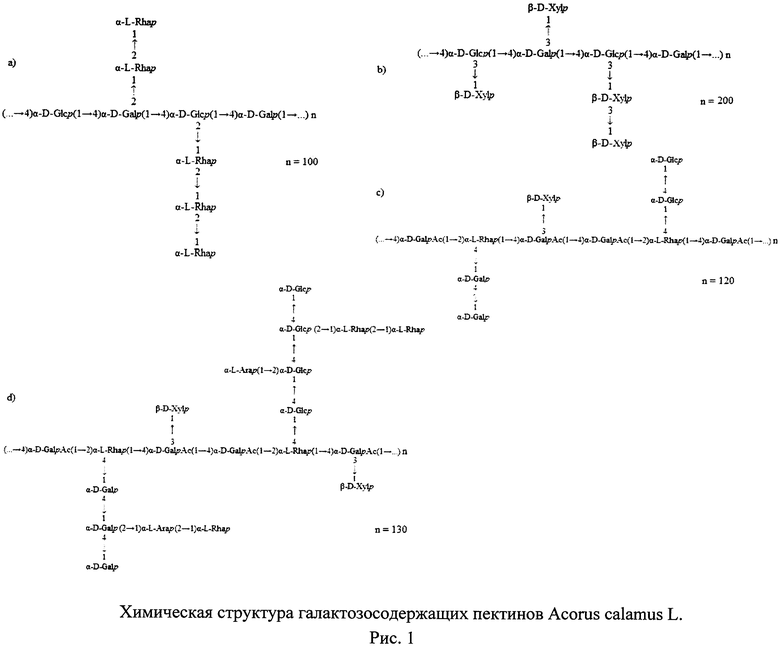
Выделение исследуемых веществ из корневищ аира болотного и определение их химической структуры проводили методами ионообменной хроматографии, ультрафильтрации и порционного осаждения [6]. В результате анализа полученных веществ методом эксклюзионной ВЭЖХ установлено, что они представляют галактозосодержащие пектины с различной химической структорой. Так вещество 1 представляет собой α-D-галакто-(1,4)-α-D-глюкан с разветвлениями, состоящими из остатков α-L-рамнопиранозы (рис.1а); вещество 2 - α(1,2)-L-рамно-α(1,4)-D-галактопиранозилуронан с разветвлениями из остатков нейтральных сахаров (ксилозы, галактозы и глюкозы) (рис.1с); вещество 3 - β-D-ксилопиранозил-α(1,3)-D-галакто-α(1,4)-D-глюкан (рис.1b); вещество 4 - сильноразветвленный рамногалактуронан I (рис.1d).
Новые свойства галактозосодержащих пектинов были обнаружены экспериментальным путем. Исследование проведено на мышах-самках линии C57BL/6 массой 19-20 г в возрасте 3 мес. В качестве модели экспериментального злокачественного роста использовали гематогенно метастазирующую карциному легких Льюис, перевиваемую внутримышечно по 5 млн. опухолевых клеток на мышь. В качестве препарата сравнения использовали суммарный полисахаридный комплекс из корневищ аира болотного, повышающий эффективность противоопухолевой терапии [1, 2].
В конце эксперимента производили выделение опухоли, подсчет метастазов. Эффективность проведенных курсов лечения оценивали по способности повышать противоопухолевое и антиметастатическое действие циклофосфана [5]. В конце эксперимента животных умерщвляли, соблюдая «Правила проведения работ с использованием экспериментальных животных», утвержденные министерством здравоохранения РФ.
Обработку полученных результатов проводили с использованием непараметрических критериев Вилкоксона-Манна-Уитни (u) и углового преобразования Фишера (φ). Различия считали достоверными при Р<0,05 [4].
Пример 1.
Распределение животных на группы:
1. «Контроль» (n=10) - мыши, получавшие ежедневно в течение 14 сут по 0,1 мл ампульной воды для инъекций внутрибрюшинно.
2. «Циклофосфан» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли.
3. «Циклофосфан + вещество 1» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и вещество 1 в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
4. «Циклофосфан + полисахаридный комплекс» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и полисахаридный комплекс из корневищ аира болотного в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
При использовании вещества 1 совместно с циклофосфаном отмечено снижение частоты метастазирования по сравнению с таковой в группе монохимиотерапии (40% против 89%, Р<0,01), тогда как у мышей, получавших в схеме химиотерапии суммарный полисахаридный комплекс, уменьшение этого показателя не было статистически значимым (табл.1).
1-2Р<0,01
1-2Р<0,01
2-3
P<0,01
2-7Р<0,05
Пример 2.
Распределение животных на группы:
1. «Контроль» (n=10) - мыши, получавшие ежедневно в течение 14 сут по 0,1 мл ампульной воды для инъекций внутрибрюшинно.
2. «Циклофосфан» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли.
3. «Циклофосфан + вещество 2» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и вещество 2 в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
4. «Циклофосфан + полисахаридный комплекс» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и полисахаридный комплекс из корневищ аира болотного в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
Вещество 2 обладало наиболее выраженной фармакологической активностью, так как добавление его в схему химиотерапии приводило к повышению как противоопухолевого, так и антиметастатического эффекта цитостатика. Под влиянием вещества 2 отмечено достоверное уменьшение массы основного опухолевого узла в 1,2 раза, показатель торможения роста опухоли составил 36% против 24% в группе мышей, леченных только циклофосфаном. Зафиксировано достоверное снижение количества (в 5,8 раза) и площади (в 15,6 раза) метастазов в легких, частота метастазирования уменьшалась на 49% относительно этих данных у животных, получавших цитостатик (Р<0,01), индекс ингибирования метастазирования оказался наивысшим и составил 99%. При этом у мышей, в схему лечения которых входил полисахаридный комплекс, зафиксировано уменьшение только площади метастатического поражения легких (в 5,1 раза Р<0,05) по сравнению с этим показателем в группе монохимиотерапии (табл.2).
1-2Р<0,05
1-2Р<0,01
1-2Р<0,01
2-4Р<0,05
2-4
Р<0,01
2-4Р<0,01
2-4Р<0,01
2-7Р<0,05
Пример 3.
Распределение животных на группы:
1. «Контроль» (n=10) - мыши, получавшие ежедневно в течение 14 сут по 0,1 мл ампульной воды для инъекций внутрибрюшинно.
2. «Циклофосфан» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли.
3. «Циклофосфан + вещество 3» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и вещество 3 в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
4. «Циклофосфан + полисахаридный комплекс» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и полисахаридный комплекс из корневищ аира болотного в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
Добавление в схему химиотерапии вещества 3 уменьшало площадь метастатического поражения в легких мышей в 2,8 раза относительно таковой у леченных только циклофосфаном животных (Р<0,05), тогда как при комбинированном лечении мышей полисахаридным комплексом и цитостатиком уменьшение площади метастазирования в легких было менее выраженным (табл.3).
1-2Р<0,05
1-2Р<0,01
1-2Р<0,01
2-5Р<0,05
2-7Р<0,05
Пример 4.
Распределение животных на группы:
1. «Контроль» (n=10) - мыши, получавшие ежедневно в течение 14 сут по 0,1 мл ампульной воды для инъекций внутрибрюшинно.
2. «Циклофосфан» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли.
3. «Циклофосфан + вещество 4» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и вещество 4 в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
4. «Циклофосфан + полисахаридный комплекс» (n=10) - мыши, получавшие циклофосфан в дозе 125 мг/кг однократно внутрибрюшинно на 11 сут развития опухоли и полисахаридный комплекс из корневищ аира болотного в дозе 20 мг/кг внутрибрюшинно, начиная с 7 сут после перевивки опухоли ежедневно в течение 14 сут.
Совместное применение вещества 4 и циклофосфана приводило к повышению антиметастатического эффекта последнего: такие показатели как количество метастазов и площадь метастатического поражения снижались в 8,3 и 49,5 раза соответственно (Р<0,01), частота метастазирования достоверно уменьшалась (30% против 89% в группе применения цитостатика) (табл.4). В то же время, при добавлении в схему лечения цитостатиком полисахаридного комплекса такие показатели, как количество метастазов и частота метастазирования, значимо не разнились с таковыми в группе монохимиотерапии, а уменьшение площади метастазов было менее выраженным (табл.4).
1-2Р<0,05
1-2Р<0,01
1-2Р<0,01
2-6Р<0,01
2-6Р<0,01
2-7Р<0,05
Исходя из вышеизложенного галактозосодержащие пектины, выделенные из корневищ аира болотного, в разной степени повышают эффективность цитостатической терапии. Наиболее оптимальной из всех предложенных терапевтических схем оказалась комбинация вещества 2 и циклофосфана. В группе животных, получавших такое лечение, оказался наивысшим как процент торможения роста опухоли, так и индекс ингибирования метастазирования. В то же время, сочетанное использование циклофосфана с суммарным полисахаридным комплексом из корневищ аира болотного не приводило к повышению противоопухолевого эффекта цитостатика, а увеличение антиметастатического действия было менее выраженным, чем в группах мышей, получавших совместно с циклофосфаном галактозосодержащие пектины. Это свидетельствует о том, что терапевтическое действие этих веществ превышает таковое у используемого в качестве средства сравнения полисахаридного комплекса.
Таким образом, разработка лекарственных препаратов на основе галактозосодержащих пектинов для включения их в схемы химиотерапии с целью повышения эффективности цитостатических препаратов является перспективным направлением современной фармакологии.
Список литературы
1. Зуева Е.П., Лопатина К.А., Разина Т.Г., Гурьев A.M. Полисахариды в онкологии. - Томск: «Печатная мануфактура», 2010. - С.64-88.
2. Лопатина К.А. Гурьев A.M., Разина Т.Г. и др. Действие водорастворимых полисахаридов корневищ аира болотного на функциональную активность клеток лимфоузлов в условиях цитостатической терапии перевиваемой опухоли // Сибирский онкологический журнал. - 2006. - Т.19 - №3. - С.59-63.
3. Машковский М.Д. Лекарственные средства. - М.: «Новая волна», 2008. - С.1206.
4. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под ред. Р.У.Хабриева. - 2-изд., перераб. и доп. - М.: ОАО Изд-во «Медицина», 2005. - С.326.
5. Софьина З.П., Сыркин А.Б., Голдин А., Кляйн А. Экспериментальная оценка противоопухолевых препаратов в СССР и США. - М.: «Медицина», 1980. - С.296.
6. Bradford M.M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding // Analyt. Biochem. - 1976. - Vol.72. - P.248-254.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО НА ОСНОВЕ ПОЛИСАХАРИДОВ АИРА БОЛОТНОГО, ПОВЫШАЮЩЕЕ ПРОТИВООПУХОЛЕВУЮ И ПРОТИВОМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ ЦИТОСТАТИЧЕСКИХ ПРЕПАРАТОВ | 2005 |
|
RU2308285C2 |
| Средство, обладающее антиметастатической активностью и повышающее противометастатическое действие циклофосфана | 2016 |
|
RU2657602C1 |
| Средство, повышающее антиметастатическую активность циклофосфана | 2016 |
|
RU2613189C1 |
| АНТИМЕТАСТАТИЧЕСКОЕ СРЕДСТВО | 2017 |
|
RU2657814C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ, ПОВЫШАЮЩЕЕ ПРОТИВОМЕТАСТАТИЧЕСКОЕ ДЕЙСТВИЕ ЦИКЛОФОСФАНА | 2015 |
|
RU2578457C1 |
| СПОСОБ СОЗДАНИЯ БИОЛОГИЧЕСКОЙ МОДЕЛИ УМЕРЕННОГО ТОРМОЖЕНИЯ РОСТА ОПУХОЛИ И МЕТАСТАЗОВ КАРЦИНОМЫ ЛЕГКИХ ЛЬЮИС С ПРОДОЛЖИТЕЛЬНОЙ ЦИКЛОФОСФАНИНДУЦИРОВАННОЙ ЛЕЙКОПЕНИЕЙ У МЫШЕЙ | 2012 |
|
RU2488173C1 |
| СПОСОБ ПОВЫШЕНИЯ ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТИ ЦИКЛОФОСФАНА В ЭКСПЕРИМЕНТЕ | 2004 |
|
RU2270682C2 |
| СРЕДСТВО, ПОВЫШАЮЩЕЕ ПРОТИВООПУХОЛЕВУЮ И АНТИМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ ЦИКЛОФОСФАНА | 2002 |
|
RU2225720C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЗАБОЛЕВАНИЙ В ЭКСПЕРИМЕНТЕ | 2007 |
|
RU2396967C2 |
| КОРРЕКТОР ЦИТОСТАТИЧЕСКОЙ ПОЛИХИМИОТЕРАПИИ | 2007 |
|
RU2353623C1 |
Изобретение относится к области медицины, конкретно к онкологии, и может быть использовано для повышения эффективности цитостатического лечения больных со злокачественными опухолями. Предложено применение галактозосодержащих пектинов, полученных из корневищ аира болотного, в комплексной терапии злокачественных новообразований. Экспериментально показана возможность повышения эффективности химиотерапии с помощью галактозосодержащих пектинов. 1 ил., 4 табл., 4 пр.
Применение галактозосодержащих пектинов, выделенных из корневищ аира болотного (Acorus calamus L.), в качестве средства, повышающего противоопухолевую и антиметастатическую активность цитостатических препаратов.
| ЛОПАТИНА К.А | |||
| и др | |||
| Действие водорастворимых полисахаридов корневищ аира болотного на функциональную активность клеток лимфоузлов в условиях цитостатической терапии перевиваемой опухоли | |||
| - Сибирский онкологический журнал, 2006, т.19, №3, с.59-63 | |||
| ЗУЕВА Е.П | |||
| и др | |||
| Полисахариды в онкологии | |||
| - Томск: Печатная мануфактура, 2010, с.64-88 | |||
| ПИЩЕВАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИММУНОГЛОБУЛИНЫ И ОЛИГОСАХАРИДЫ | 2005 |
|
RU2385714C2 |
| СРЕДСТВО НА ОСНОВЕ ПОЛИСАХАРИДОВ АИРА БОЛОТНОГО, ПОВЫШАЮЩЕЕ ПРОТИВООПУХОЛЕВУЮ И ПРОТИВОМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ ЦИТОСТАТИЧЕСКИХ ПРЕПАРАТОВ | 2005 |
|
RU2308285C2 |
Авторы
Даты
2013-01-10—Публикация
2011-11-17—Подача