Предлагаемое изобретение относится к области аналитической химии и может быть использовано в медицинских, ветеринарных и других исследованиях для определения эстрогена и декспантенола в лекарственных препаратах.
В фармацевтической промышленности продолжает развиваться тенденция к производству лекарственных препаратов, содержащих несколько действующих веществ. Преимущество таких лекарственных препаратов заключается в том, что они вызывают значительный лечебный эффект при отсутствии или минимуме отрицательных влияний на организм. Это свойство обусловлено введением в препарат малых доз отдельных ингредиентов. Проблема обеспечения контроля качества таких препаратов связана, с одной стороны, с малыми дозами, с другой, - с различной химической природой входящих ингредиентов. Решить данную проблему можно с помощью эффективных способов определения количественного состава. К таким способам относится метод высокоэффективной жидкостной хроматографии (ВЭЖХ).
Известен способ определения декспантенола в лекарственных препаратах методом ВЭЖХ в изократическом режиме с использованием хроматографической колонки размером 250×4,0 мм, заполненной сорбентом с размером частиц 5 мкм, со стационарной фазой С4, в качестве подвижной фазы используют смесь 0,01 М раствора ортофосфорной кислоты с ацетонитрилом в соотношении 90:10 (ФСП 8444-07 ЛСР-001794/08-170308).
Известен способ определения декспантенола в лекарственных препаратах методом ВЭЖХ в изократическом режиме с использованием хроматографической колонки размером 150×4,6 мм, заполненной носителем с размером частиц 5 мкм, со стационарной фазой С18, в качестве подвижной фазы используют смесь фосфатного буфера (0,01 М раствор калия фосфата однозамещенного с рН 2,8) с метанолом в соотношении 60:40 (производитель препарата АО «Ядран» Галенский Лабораторий, Хорватия).
Известен способ определения эстрогенов, в частности эстриола, методом ВЭЖХ в изократическом режиме с использованием хроматографической колонки C8 размером 150×4,6 мм, заполненной носителем с размером частиц 5 мкм, в качестве подвижной фазы используется смесь ацетонитрил:метанол:вода в соотношении 35:15:45 (Фармакопея США, 29 изд.).
Известен способ определения эстрогенов, в частности эстрадиола и этилэстрадиола, методом ВЭЖХ в режиме градиентного элюирования с использованием хроматографической колонки C18 размером 150×4,6 мм, в качестве подвижных фаз используется смесь вода:ацетонитрил:ортофосфорная кислота в соотношении от 60:40:0,25 до 100:0,25 ацетонитрил:ортофосфорная кислота (Каталог ЭЛСИКО «Применение колонок для хроматографии», www.HPLC.ru).
Известные способы хорошо себя зарекомендовали и пригодны для качественного и количественного определения декспантенола или эстрогена в однокомпонентных лекарственных препаратах. Однако ни один из известных способов не позволяет количественно определить декспантенол и эстроген в двухкомпонентных лекарственных препаратах.
Задачей предлагаемого изобретения является разработка способа определения декспантенола и эстрогена в составе двухкомпонентного лекарственного препарата.
Поставленная задача решается предлагаемым способом определения содержания эстрогена и декспантенола в двухкомпонентном лекарственном препарате, включающим извлечение эстрогена и декспантенола из анализируемого лекарственного препарата, хроматографирование извлеченных эстрогена и декспантенола методом высокоэффективной жидкостной хроматографии с разделением на колонке С18 размером 50×2,0 мм, заполненной носителем с зернением 2,0 мкм, или размером 150×4,6 мм, заполненной носителем зернением 5,0 мкм, с использованием в качестве подвижных фаз смеси 0,05% раствора кислоты ортофосфорной (рН 2,4) с ацетонитрилом для хроматографии в соотношении от 90:10 до 95:5 и ацетонитрила в режиме линейного градиента на хроматографе с использованием ультрафиолетового детектора, после чего на основании расчетных формул определяют содержание эстрогена и декспантенола в двухкомпонентном лекарственном препарате.
Технический результат от использования предлагаемого изобретения заключается в создании эффективного способа, позволяющего с высокой точностью определить содержание эстрогена и декспантенола в лекарственном препарате. Кроме того, данный способ прост в исполнении и экономичен.
Предлагаемый способ осуществляется следующим образом. Раствор испытуемого препарата и раствор стандартного образца (СО) последовательно хроматографируют на жидкостном хроматографе фирмы Waters, США, с УФ-детектором при длинах волн 206 нм и 280 нм и хроматографической колонкой С18 размером 50×2,0 мм, заполненной обращенно-фазным носителем с зернением 2,0 мкм, или размером 150×4,6 мм, заполненной обращенно-фазным носителем зернением 5,0 мкм, в режиме линейного градиента с использованием в качестве подвижной фазы (ПФ):
- смеси 0,05% раствора кислоты ортофосфорной рН 2,4 с ацетонитрилом для хроматографии в соотношении от 90:10 до 95:5 - фаза А;
- ацетонитрил для хроматографии - фаза В,
получая не менее трех хроматограмм каждого раствора. Находят площади пиков определяемых веществ на хроматограммах испытуемого и стандартного растворов и по формуле рассчитывают их содержание в анализируемом препарате.
Примеры конкретного применения предлагаемого способа
Количественное определение декспантенола и эстрогена-эстриола в лекарственном препарате, выполненном в виде суппозиториев.
Пример 1
Для приготовления испытуемого раствора один суппозиторий, предварительно измельченный и взвешенный с точностью до 0,01 г, растворяют в 50 мл смеси 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) в мерной колбе вместимостью 100 мл при нагревании на водяной бане при температуре 35-45°С в течение 10 мин, затем охлаждают, доводят объем раствора той же смесью до метки, перемешивают и фильтруют через мембранный фильтр, отбрасывая первые порции фильтрата (испытуемый раствор 1).
5 мл испытуемого раствора 1 помещают в мерную колбу вместимостью 50 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр, отбрасывая первые порции фильтрата (испытуемый раствор 2).
Для количественного определения эстриола используют испытуемый раствор 1 для декспантенола раствор 2.
Для приготовления раствора стандартного образца (СО) эстриола берут около 0,05 г (точная навеска) его СО, растворяют в смеси 0,05% раствора ортофосфорной кислоты с ацетонитрилом (3:2) в мерной колбе вместимостью 100 мл, доводят объем раствора той же смесью до метки и перемешивают (раствор А).
Для приготовления раствора стандартного образца (СО) декспантенола берут около 0,05 г (точная навеска) его СО, растворяют в смеси 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) в мерной колбе вместимостью 50 мл, доводят объем раствора той же смесью до метки и перемешивают (раствор Б).
1 мл раствора А и 10 мл раствора Б помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр, отбрасывая первые порции фильтрата (раствор В).
По 40,0 мкл испытуемых растворов 1 и 2 и раствора В СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 150×4,6 мм с обращенно-фазным носителем Puro-spher® STAR RP-18e с размером частиц 5 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 1,0 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстриола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формуле:
Для эстриола 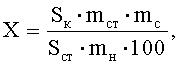
для декспантенола 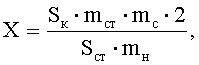
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и СО соответственно;
mст, mс и mн - масса стандарта определяемого вещества в растворе СО, средняя масса суппозитория и масса навески суппозитория, взятой для приготовления испытуемого раствора, соответственно в граммах.
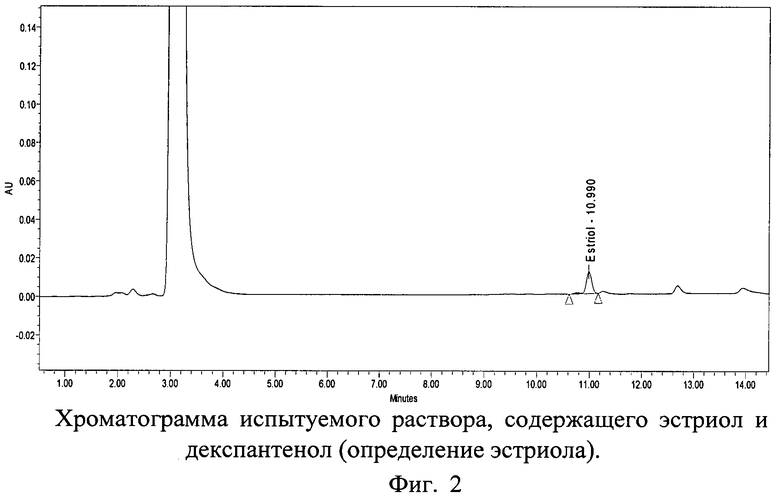
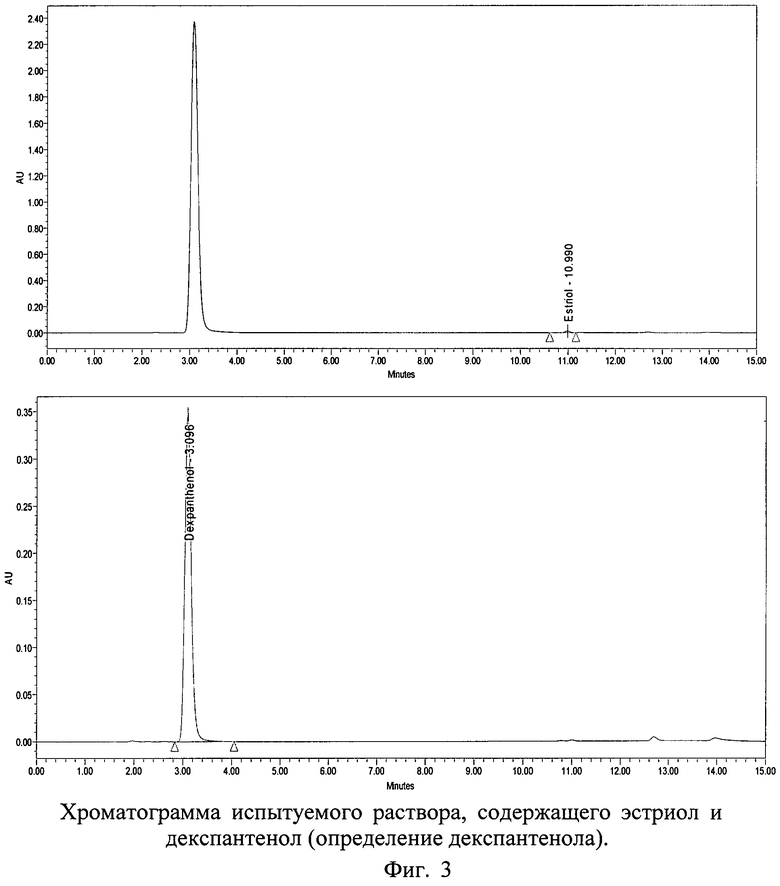
Хроматограммы СО и испытуемого раствора суппозиториев, содержащих декспантенол и эстриол, с использованием колонки 150×4,6 мм с обращенно-фазным носителем Purospher® STAR RP-18e с размером частиц 5 мкм представлены на фиг.1, 2 и 3.
Пример 2
Приготовление испытуемого раствора 1, растворов А и Б СО осуществляется, как в примере 1.
3 мл испытуемого раствора 1 помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки. Перемешивают и фильтруют через мембранный фильтр, отбрасывая первые порции фильтрата (испытуемый раствор 3).
Для количественного определения эстриола используют испытуемый раствор 1, для декспантенола - испытуемый раствор 3.
Для приготовления раствора СО эстриола и декспантенола берут 1 мл раствора А и 3 мл раствора Б, помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки. Перемешивают и фильтруют через мембранный фильтр, отбрасывая первые порции фильтрата (раствор Г).
По 10,0 мкл испытуемых растворов 1 и 3 и раствора Г СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro С18 с размером частиц 2,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 0,6 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстриола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формуле:
Для эстриола 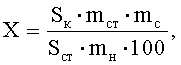
для декспантенола 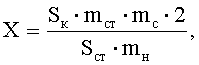
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и СО соответственно;
mст, mс и mн - масса стандарта определяемого вещества в растворе СО, средняя масса суппозитория и масса навески суппозитория, взятой для приготовления испытуемого раствора, соответственно в граммах.
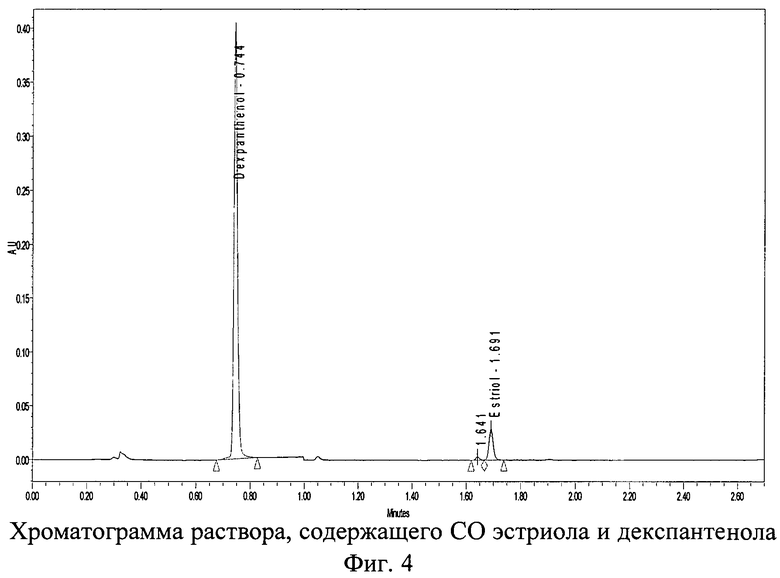
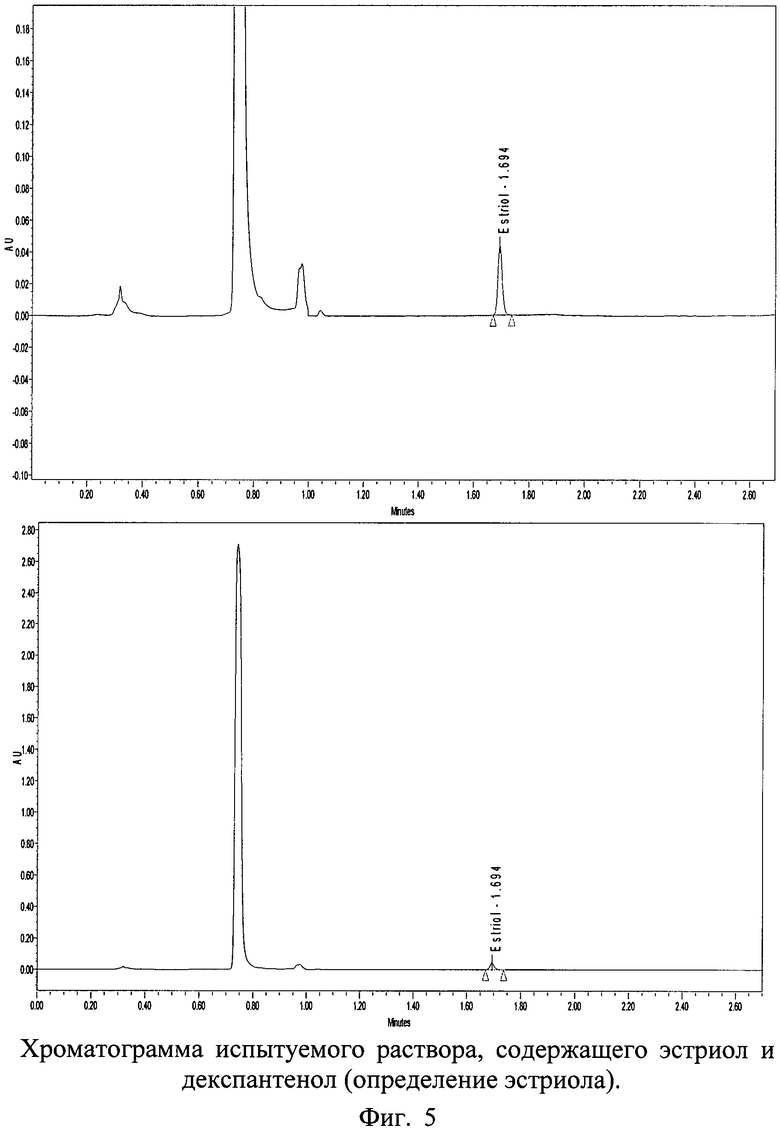
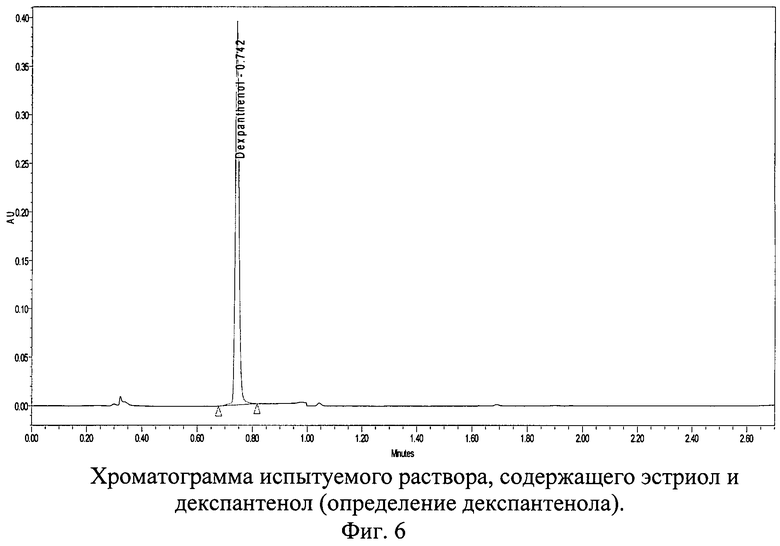
Хроматограммы СО и испытуемого раствора суппозиториев, содержащих декспантенол и эстриол, с использованием колонки 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro С18 с размером частиц 2,0 мкм представлены на фиг.4, 5 и 6.
Количественное определение декспантенола и эстрогена-эстриола в лекарственном препарате, выполненном в виде геля
Пример 3
Для приготовления испытуемого раствора навеску геля массой около 1,0 г, взвешенную с точностью до 0,01 г, помещают в коническую колбу со шлифом вместимостью 100 мл, прибавляют пипеткой 20 мл смеси раствора кальция хлорида с ацетонитрилом (90:10), перемешивают до растворения основы и фильтруют через фильтр «синяя лента», отбрасывая первые порции фильтрата.
5 мл полученного раствора помещают в мерную колбу вместимостью 25 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр (GHP, 0,45 мкм, P/N WAT200514 или аналогичный), отбрасывая первые порции фильтрата (испытуемый раствор 1).
5 мл испытуемого раствора 1 помещают в мерную колбу вместимостью 25 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр (GHP, 0,45 мкм, P/N WAT200514 или аналогичный), отбрасывая первые порции фильтрата (испытуемый раствор 2).
Для количественного определения эстриола используют испытуемый раствор 1, для декспантенола испытуемый раствор 2.
Около 0,05 г (точная навеска) СО эстриола растворяют в смеси 0,05% раствора ортофосфорной кислоты с ацетонитрилом (3:2) в мерной колбе вместимостью 100 мл, доводят объем раствора той же смесью до метки и перемешивают (раствор А).
Около 0,05 г (точная навеска) СО декспантенола растворяют в смеси 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) в мерной колбе вместимостью 50 мл, доводят объем раствора той же смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки и перемешивают (раствор Б).
2 мл раствора А и 10 мл раствора Б помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр (GHP, 0,45 мкм, P/N WAT200514 или аналогичный), отбрасывая первые порции (около 10 мл) фильтрата (раствор В).
По 40,0 мкл испытуемых растворов 1 и 2 и раствора В СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 150×4,6 мм с обращенно-фазным носителем Puro-spher® STAR RP-18e с размером частиц 5 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 1,0 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм - для эстриола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формуле:
Для эстриола 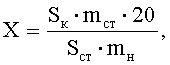
для декспантенола 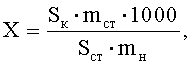
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и СО соответственно;
mст и mн - масса стандарта определяемого вещества в растворе СО и навески геля, взятой для приготовления испытуемого раствора, соответственно в граммах.
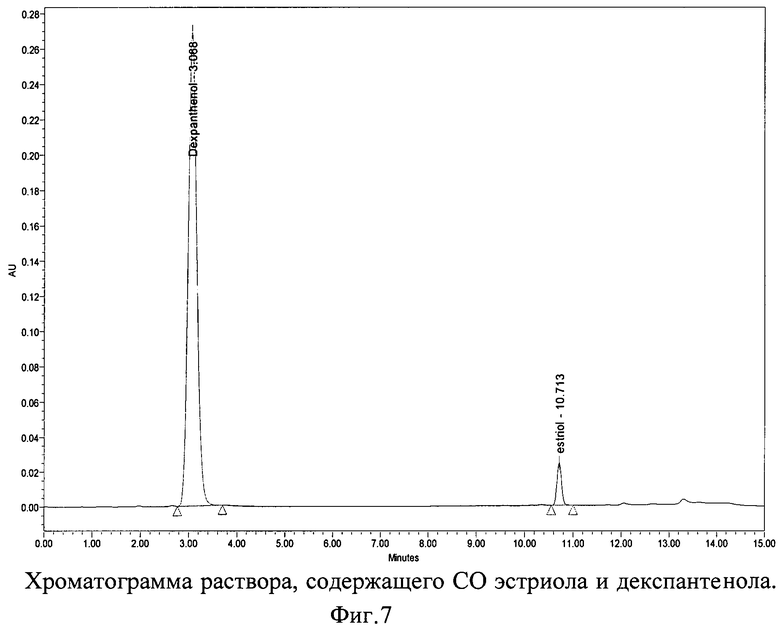
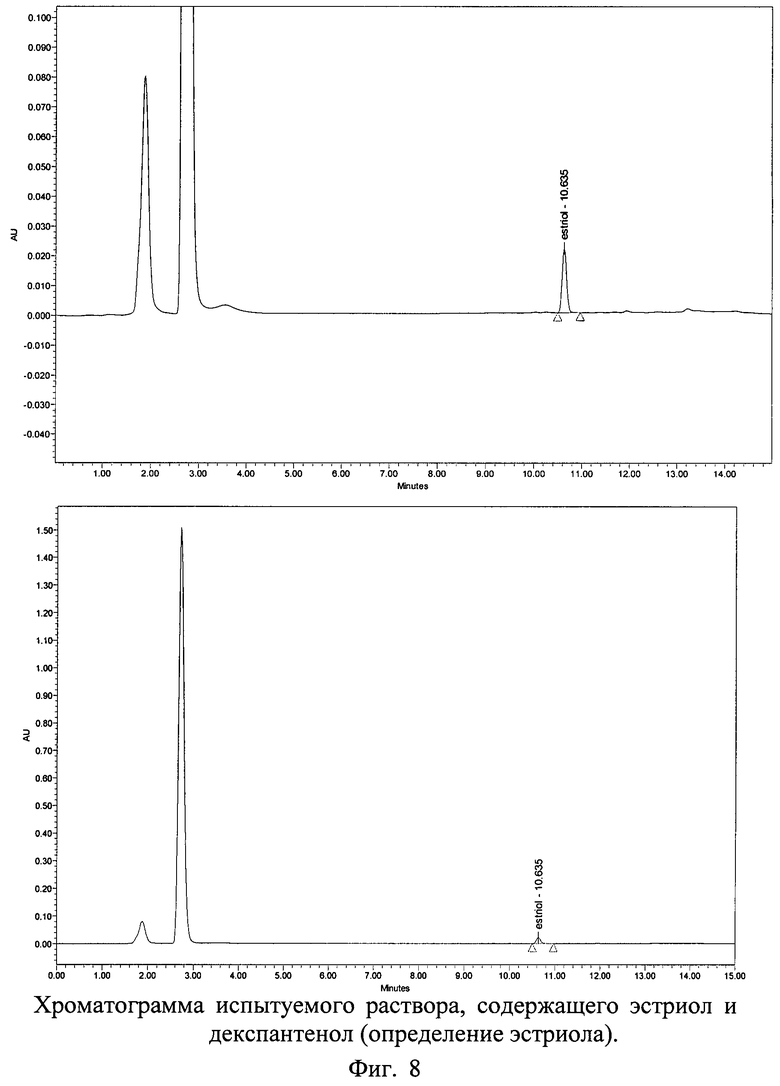
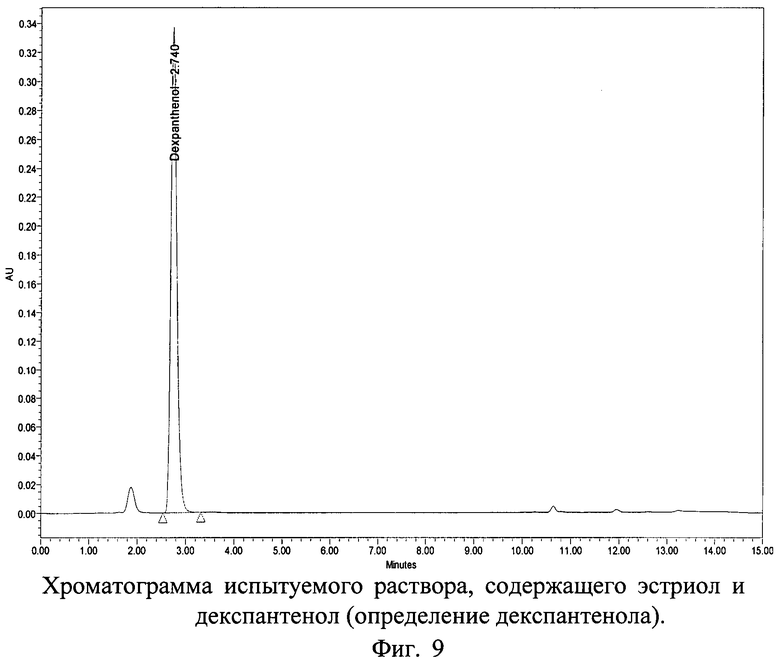
Хроматограммы СО и испытуемого раствора геля, содержащих декспантенол и эстриол с использованием колонки 150×4,6 мм с обращенно-фазным носителем Purospher® STAR RP-18e с размером частиц 5 мкм представлены на фиг.7, 8 и 9.
Пример 4
Приготовление испытуемого раствора 1, растворов А и Б СО осуществляется, как в примере 3.
6 мл испытуемого раствора 1 помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр (GHP, 0,45 мкм, P/N WAT200514 или аналогичный), отбрасывая первые порции фильтрата (испытуемый раствор 3).
2 мл раствора А и 3 мл раствора Б помещают в мерную колбу вместимостью 100 мл, доводят объем раствора смесью 0,05% раствора ортофосфорной кислоты с ацетонитрилом (90:10) до метки, перемешивают и фильтруют через мембранный фильтр (GHP, 0,45 мкм, P/N WAT200514 или аналогичный), отбрасывая первые порции (около 10 мл) фильтрата (раствор Г).
По 10,0 мкл испытуемых растворов 1 и 3 и раствора Г СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro С18 с размером частиц 2,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 0,6 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстриола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формуле:
Для эстриола 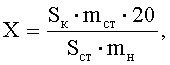
для декспантенола 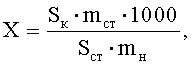
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и СО соответственно;
mст и mн - масса стандарта определяемого вещества в растворе СО и навески геля, взятой для приготовления испытуемого раствора, соответственно в граммах.
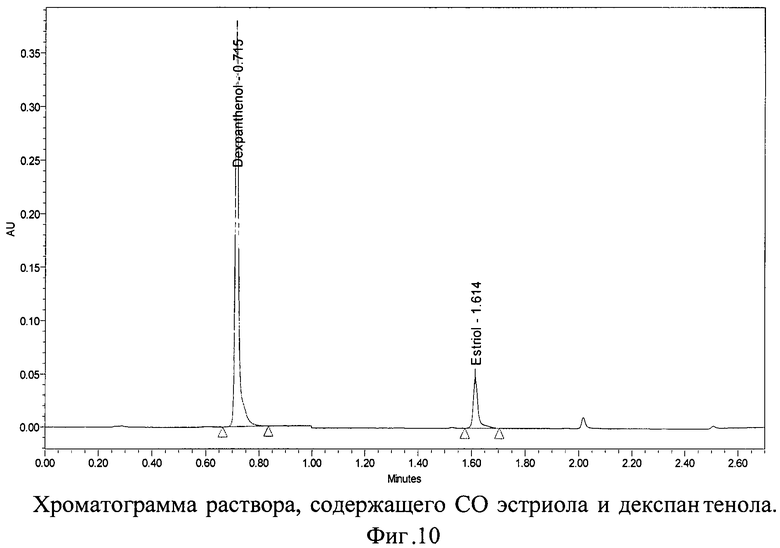
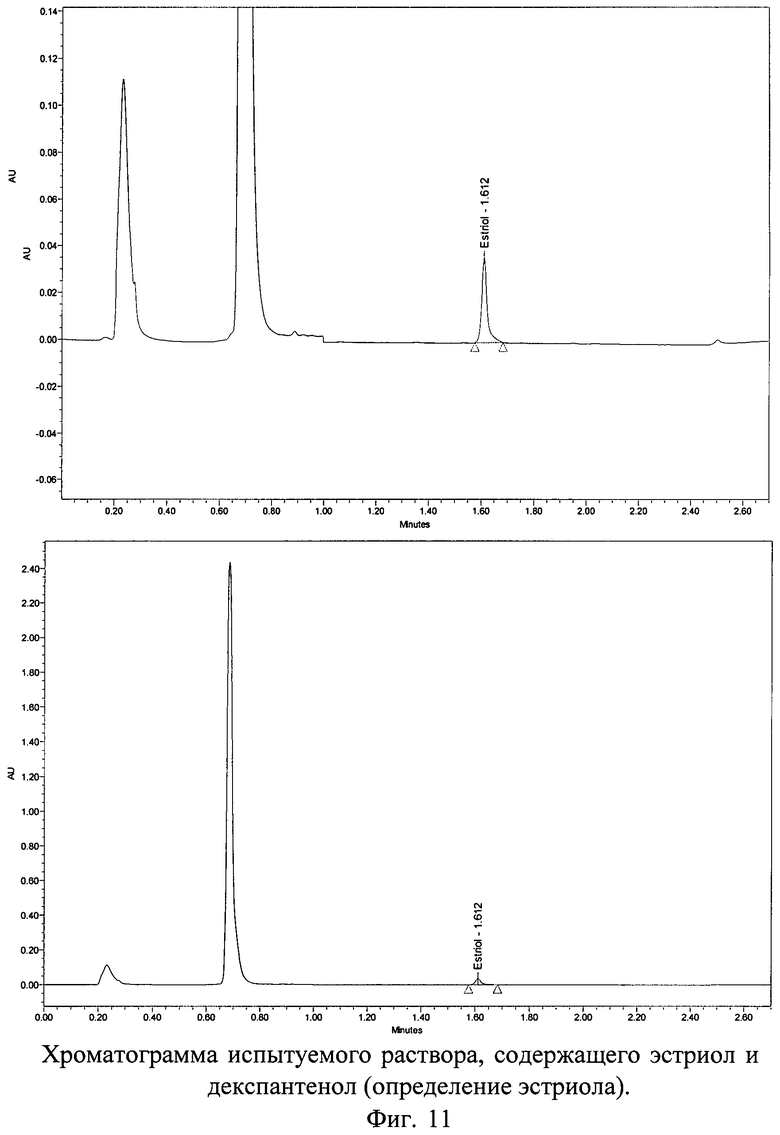
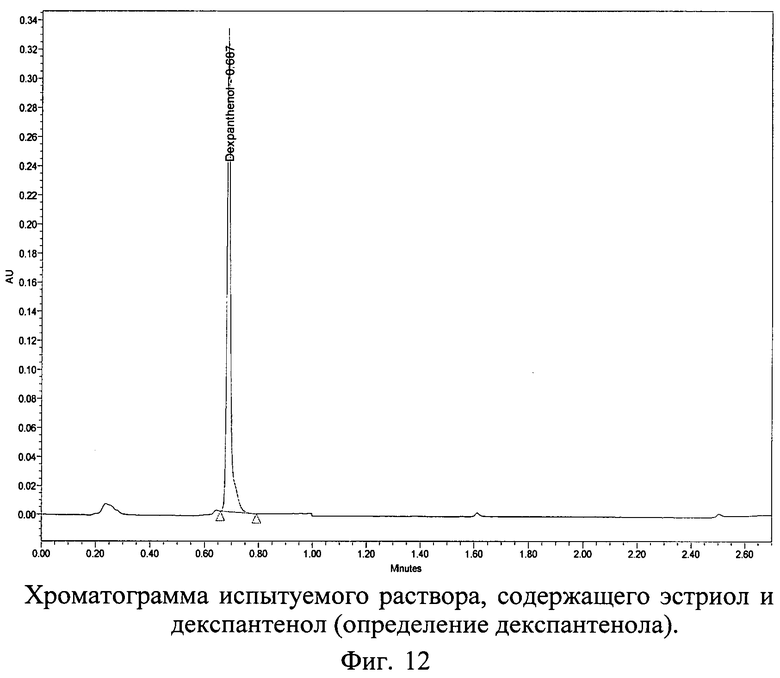
Хроматограммы СО и испытуемого раствора геля, содержащих декспантенол и эстроген (эстриол), с использованием колонки 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro С18 с размером частиц 2,0 мкм представлены на фиг.10, 11 и 12.
Количественное определение декспантенола и эстрогена-эстрона в лекарственном препарате, выполненном в виде суппозиториев или геля
Пример 5
Приготовление растворов испытуемых и СО проводят, как в примерах 1 и 3.
По 40,0 мкл испытуемых растворов 1 и 2 и раствора В СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 150×4,6 мм с обращенно-фазным носителем Puro-spher® STAR RP-18e с размером частиц 5,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 1,0 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстрона.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формулам, описанным в примерах 1 и 3.
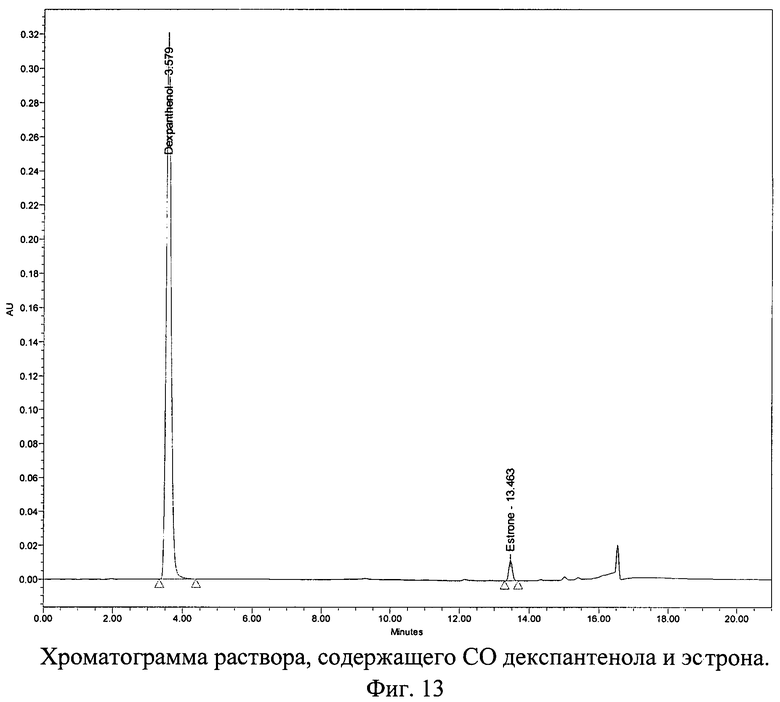
Хроматограмма раствора, содержащего СО декспантенола и эстрогена (эстрон), с использованием колонки 150×4,6 мм с обращенно-фазным носителем Purospher® STAR RP-18e с размером частиц 5,0 мкм представлена на фиг.13.
Пример 6
Приготовление растворов испытуемых и СО проводят, как в примерах 2 и 4.
По 10,0 мкл испытуемых растворов и раствора СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 50×2,0 мм с обращено-фазным носителем YMC-UltraHT Pro C18 с размером частиц 2,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с pH 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 0,6 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстрона.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формулам, описанным в примерах 2 и 4.
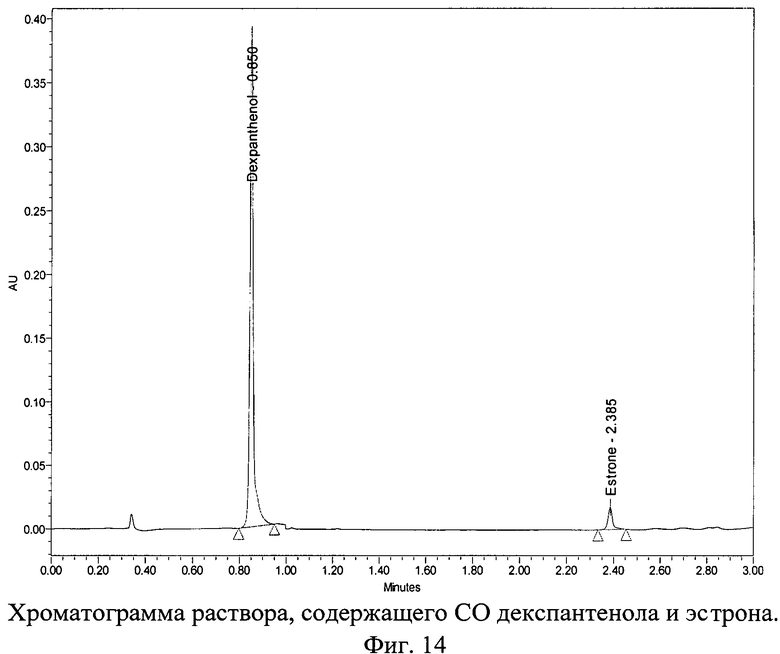
Хроматограмма раствора, содержащего СО декспантенола и эстрогена (эстрон), с использованием колонки 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro C18 с размером частиц 2,0 мкм представлена на фиг.14.
Количественное определение декспантенола и эстрогена-эстрадиола в лекарственном препарате, выполненном в виде суппозиториев и геля
Пример 7
Приготовление растворов испытуемых и СО проводят, как в примерах 1 и 3.
По 40,0 мкл испытуемых растворов 1 и 2 и раствора В СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 150×4,6 мм с обращенно-фазным носителем Puro-spher® STAR RP-18e с размером частиц 5,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 1,0 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстрадиола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формулам, описанным в примерах 1 и 3.
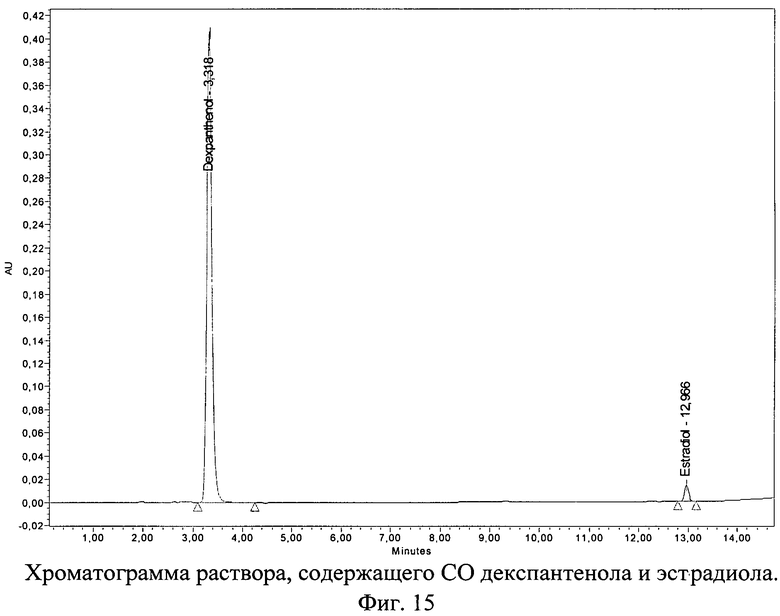
Хроматограмма раствора, содержащего СО декспантенола и эстрогена (эстрадиол), с использованием колонки 150×4,6 мм с обращенно-фазным носителем Purospher® STAR RP-18e с размером частиц 5,0 мкм представлена на фиг.15.
Пример 8
Приготовление растворов испытуемых и СО проводят, как в примерах 2 и 4.
По 10,0 мкл испытуемых растворов и раствора СО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro C18 с размером частиц 2,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси фазы А (с рН 2,4) и фазы В (ацетонитрил для хроматографии). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Скорость потока подвижной фазы 0,6 мл/мин. Длина волны УФ-детектора - 206 нм для декспантенола; 280 нм для эстрадиола.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемом лекарственном препарате по формулам, описанным в примерах 2 и 4.
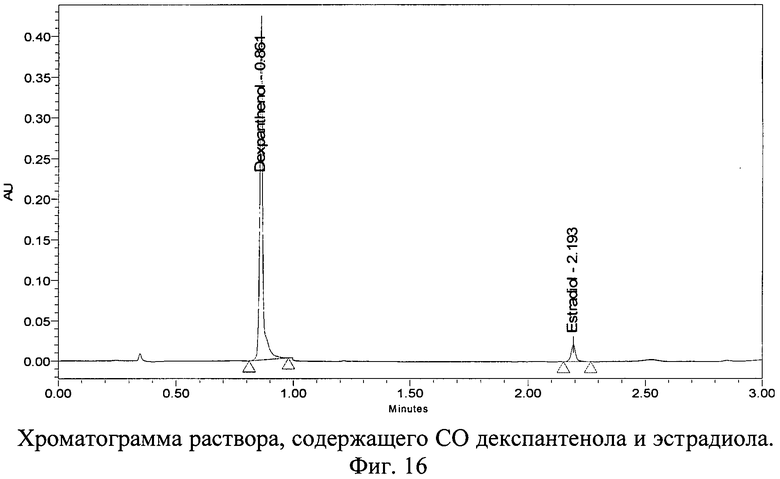
Хроматограмма раствора, содержащего СО декспантенола и эстрогена (эстрадиол), с использованием колонки 50×2,0 мм с обращенно-фазным носителем YMC-UltraHT Pro С18 с размером частиц 2,0 мкм представлена на фиг.16.
Статистическую обработку результатов, полученных при использовании предлагаемого способа, проводили в соответствии с требованиями Государственной фармакопеи СССР, XI изд.
Как видно из полученных результатов, предлагаемый способ позволяет с высокой точностью определить содержание эстрогена и декспантенола в лекарственном препарате.
Предлагаемое изобретение относится к области аналитической химии и может быть использовано в медицинских, ветеринарных и других исследованиях для определения эстрогена и декспантенола в лекарственных препаратах. Способ определения содержания эстрогена и декспантенола в двухкомпонентном лекарственном препарате включает извлечение эстрогена и декспантенола из анализируемого лекарственного препарата. Также способ включает хроматографирование извлеченных эстрогена и декспантенола методом высокоэффективной жидкостной хроматографии с разделением на колонке С18 размером 50×2,0 мм, заполненной носителем с зернением 2,0 мкм, или размером 150×4,6 мм, заполненной носителем с зернением 5 мкм, с использованием в качестве подвижных фаз смеси 0,05% раствора кислоты ортофосфорной (рН 2,4) с ацетонитрилом для хроматографии в соотношении от 90:10 до 95:5 в режиме линейного градиента на хроматографе с использованием ультрафиолетового детектора, после чего на основании расчетных формул определяют содержание эстрогена и декспантенола в двухкомпонентном лекарственном препарате. Техническим результатом изобретения является повышение определения содержания эстрогена и декспантенола в лекарственном препарате. 1 з.п. ф-лы, 16 ил., 4 табл., 8 пр.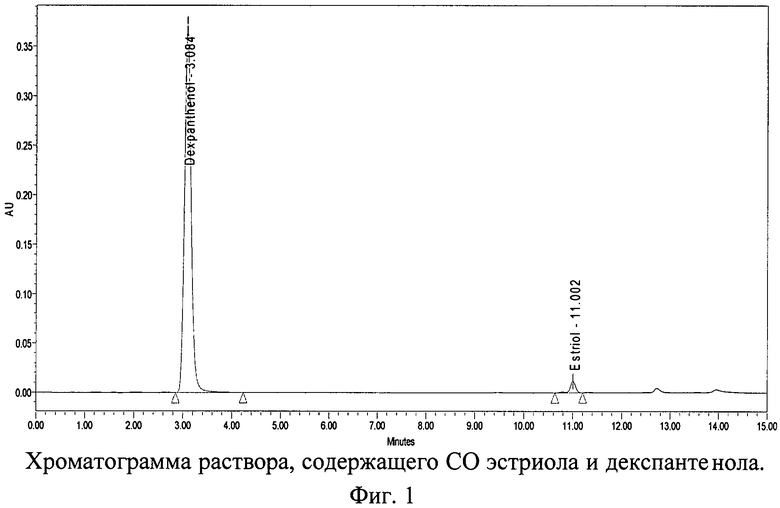
1. Способ определения содержания эстрогена и декспантенола в двухкомпонентном лекарственном препарате, включающий извлечение эстрогена и декспантенола из анализируемого лекарственного препарата, хроматографирование извлеченных эстрогена и декспантенола методом высокоэффективной жидкостной хроматографии с разделением на колонке С18 размером 50×2,0 мм, заполненной носителем с зернением 2,0 мкм, или размером 150×4,6 мм, заполненной носителем с зернением 5 мкм, с использованием в качестве подвижных фаз смесь 0,05%-ного раствора кислоты ортофосфорной (рН 2,4) с ацетонитрилом для хроматографии в соотношении от 90:10 до 95:5, в режиме линейного градиента на хроматографе с использованием ультрафиолетового детектора, после чего на основании расчетных формул определяют содержание эстрогена и декспантенола в двухкомпонентном лекарственном препарате.
2. Способ по п.1, где носитель представляет собой обращенно-фазовый носитель.
| СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ ПРИМЕСИ 4-МЕТИЛАМИНОАНТИПИРИНА В МНОГОКОМПОНЕНТНЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ ЖАРОПОНИЖАЮЩЕГО, АНАЛГЕЗИРУЮЩЕГО, ПРОТИВОПРОСТУДНОГО ДЕЙСТВИЯ | 2007 |
|
RU2338189C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2002 |
|
RU2215288C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИПИРИНА В СЛЮНЕ | 2004 |
|
RU2272286C1 |
| DE 10028548 C1, 30.08.2001. | |||
Авторы
Даты
2013-02-27—Публикация
2011-08-22—Подача