Изобретение относится к высокоэффективной жидкостной хроматографии (ВЭЖХ), а именно, к способам количественного определения состава многокомпонентных лекарственных препаратов жаропонижающего, аналгезирующего, противопростудного действия и может быть использовано в практике контрольно-аналитических лабораторий фармацевтических предприятий и аптечной сети. Способ относится к числу массовых.
Многокомпонентные лекарственные препараты широко распространены в медицинской практике. В состав многих препаратов жаропонижающего, аналгезирующего, противопростудного действия входят, наряду с парацетамолом, кофеином, пропифеназоном, анальгином, наркотические и другие сильнодействующие вещества - кодеина фосфат, эфедрина гидрохлорид, фенобарбитал, фенилэфрина гидрохлорид, хлорфенирамина малеат. В связи с этим проблема обеспечения и контроля качества таких препаратов чрезвычайно актуальна, а ее успешное решение невозможно без эффективных способов определения их количественного состава. В то же время задача разработки таких способов очень сложна, что обусловлено и комплексным составом анализируемых препаратов, и большой разницей в содержании некоторых компонентов. Так, в некоторых препаратах содержание парацетамола превышает количество кодеина фосфата в 37 раз, фенилэфрина гидрохлорида - в 60 раз, а хлорфенирамина малеата - в 75 раз. По этой причине одновременное обнаружение и количественное определение всех действующих компонентов препарата затруднительно, и возникает необходимость в предварительных трудоемких операциях отделения и концентрирования веществ, содержащихся в сравнительно малых количествах, а также в альтернативных способах их определения. Этим можно объяснить и тот факт, что, несмотря на бурное развитие в последние годы новейших методов анализа сложных лекарственных препаратов и, прежде всего, ВЭЖХ, в научной литературе описано очень мало одностадийных способов количественного определения их состава.
Известен способ количественного определения состава таблеток "Спазмовералгин нео", содержащих бромизовал (0,250 г), парацетамол (0,150 г), кофеин (0,050 г), папаверина гидрохлорид (0,030 г), фенобарбитал (0,020 г), кодеина фосфат (0,008 г), эфедрина гидрохлорид и атропина сульфат (содержание в таблетке двух последних компонентов в публикации не указано), методом обращенно-фазовой ВЭЖХ в изократическом режиме элюирования с использованием колонки, заполненной сорбентом с привитыми нитрильными группами, подвижной фазы (ПФ) состава ацетонитрил - 0,05 М фосфатный буферный раствор (рН 4,0) в соотношении 15:85 и детектирования при 230 нм (С.Г.Ларионова, Н.Н.Дементьева, Е.Б.Нечаева, П.В.Назаренко, Г.А.Нестерова. Оптимизация условий анализа таблеток сложного состава аналгезирующего и спазмолитического действия. Фармация. - 2002. - Т.51, №1. - С.16-19). В этой работе авторы одновременно определяют бромизовал, кодеина фосфат (соотношение содержаний 31:1), парацетамол, кофеин, фенобарбитал и папаверина гидрохлорид. Недостаток способа связан с особенностями изократического элюирования и заключается в неудовлетворительном разрешении пиков веществ, элюирующихся из колонки первыми (в интервале коэффициентов емкости k от 0,4 до 1,4 элюируются 7 веществ) и относительно высоком удерживании пика папаверина, элюирующегося последним (k=7,0). Неудовлетворительное разделение пиков определяемых веществ отрицательно влияет и на точность их количественного определения.
Наиболее близким к заявляемому изобретению по составу анализируемых препаратов, поставленной задаче, техническому решению и достигаемым результатам является способ количественного определения состава сложных лекарственных препаратов, содержащих пропифеназон, методом обращенно-фазовой ВЭЖХ (Е.Н.Вергейчик, Н.С.Онегова. ВЭЖХ в анализе сложных лекарственных препаратов, содержащих пропифеназон. Фармация. - 2001. - Т.50, №3. - С.24-26). Авторы публикации предлагают способ количественного определения состава таблеток "Каффетин", содержащих 0,250 г парацетамола, 0,210 г пропифеназона, 0,050 г кофеина и 0,010 г кодеина фосфата в одной таблетке. Поскольку в анализируемых таблетках содержание кодеина фосфата по отношению к пропифеназону и парацетамолу в 21-25 раз меньше, разработчики проводят анализ в 2 стадии. На первой стадии раствор испытуемых таблеток и раствор рабочих стандартных образцов (РСО) хроматографируют в изократическом режиме с использованием в качестве ПФ смеси ацетонитрил - вода - диэтиламин (3:2,2:0,2) и определяют парацетамол (время удерживания 3,08 мин), кофеин (4,0 мин) и пропифеназон (5,73 мин). На второй стадии раствор испытуемых таблеток в воде подкисляют 10% серной кислотой до рН 2,0, трижды проводят экстракцию порциями по 10 мл этилацетата, и экстракты, содержащие парацетамол, кофеин и пропифеназон, отбрасывают. К водному раствору, содержащему кодеина фосфат, добавляют 25% раствор аммиака до рН 9-10 и трижды экстрагируют кодеин порциями по 10 мл хлороформа. Объединенные хлороформные экстракты выпаривают, сухой остаток растворяют в ацетонитриле и в полученном растворе определяют кодеин при описанных выше условиях хроматографирования (время удерживания 4,41 мин). Элюируемые вещества детектируют при 238 и 276 нм.
Недостатками способа являются его многостадийность и, как следствие, трудоемкость, длительность и неудовлетворительная точность определения кодеина фосфата (степень извлечения кодеина из таблеток, по данным авторов способа, 89-93%).
Задачей настоящего изобретения является разработка одностадийного способа количественного определения состава некоторых многокомпонентных лекарственных препаратов жаропонижающего, аналгезирующего, противопростудного действия, в том числе, содержащих действующие вещества в относительно больших и малых количествах.
Поставленная задача достигается методом обращенно-фазовой ВЭЖХ с помощью предлагаемого способа, который заключается в том, что анализ ведут в режиме линейного градиента, наклон и продолжительность которого определяют свойствами компонентов анализируемых препаратов, с использованием в качестве ПФ:
- смеси ацетонитрила с буферным раствором (0,025 М раствор калия фосфата однозамещенного - КН2PO4, рН которого доводят до 3,0 добавлением концентрированной ортофосфорной кислоты);
- смеси ацетонитрила с водой;
- буферного раствора;
- воды.
Способ осуществляется следующим образом: раствор испытуемого препарата и раствор рабочего стандартного образца (РСО) последовательно хроматографируют на жидкостном хроматографе с ультрафиолетовым (УФ) детектором и обращенно-фазовой хроматографической колонкой в режиме линейного градиента с использованием в качестве ПФ:
- смеси ацетонитрила с буферным раствором (0,025 М раствор калия фосфата однозамещенного - КН2PO4 с рН 3,0);
- смеси ацетонитрила с водой;
- буферного раствора;
- воды,
получая не менее трех хроматограмм каждого раствора. Находят площади пиков определяемых веществ на хроматограммах испытуемого и стандартного растворов и по формуле рассчитывают их содержание в анализируемом препарате.
Способ иллюстрируется следующими примерами.
Пример 1.
Количественное определение парацетамола, пропифеназона, кофеина, кодеина фосфата и фенобарбитала в таблетках "Пенталгин Ультра".
Таблетки "Пенталгин Ультра" - аналог таблеток "Каффетин", способ анализа которых описан в прототипе, но имеют еще более сложный состав, так как содержат фенобарбитал.
Для приготовления испытуемого раствора около 0,160 г (точная навеска) тщательно растертых таблеток помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 3,0 и перемешивают в течение 10 минут. Полученный раствор доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм (например, фирмы "Миллипор"), отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,060 г парацетамола и около 0,050 г пропифеназона (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 3,0 и перемешивают до растворения веществ. К полученному раствору добавляют 5,0 мл раствора РСО-2, доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм.
Для приготовления раствора РСО-2 около 0,200 г кофеина, около 0,040 г фенобарбитала и около 0,032 г кодеина фосфата (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 3,0 и перемешивают до растворения веществ. Полученный раствор доводят до метки тем же буферным раствором и перемешивают.
По 5,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 3,9×150 мм с сорбентом Nova-Pak С 18 с размером частиц 4 мкм в режиме линейного градиента с использованием в качестве ПФ смеси элюента А (фосфатный буферный раствор с рН 3,0) и элюента В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 1:1). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 210 нм.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемых таблетках по формуле:
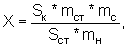
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mст, mc и mн - массы стандарта определяемого вещества в растворе РСО, средняя масса таблетки и масса навески растертых таблеток, взятой для приготовления испытуемого раствора, соответственно, в граммах.
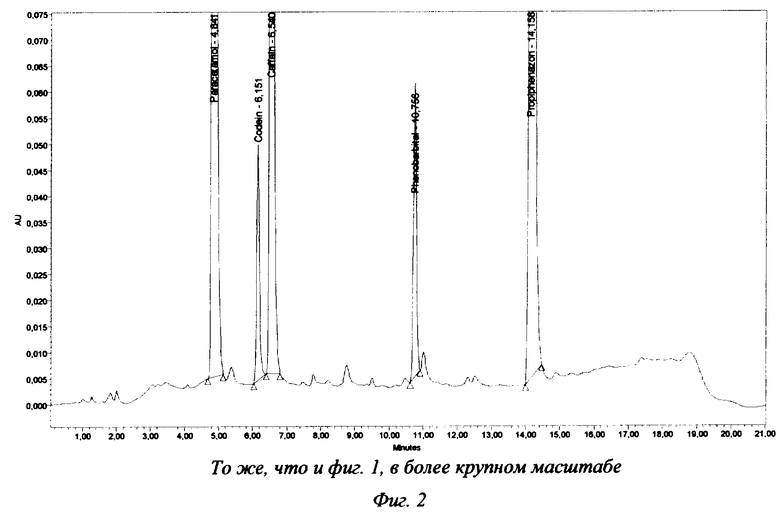
Хроматограммы испытуемого раствора таблеток "Пенталгин Ультра" представлены на фиг.1 и 2. Результаты анализа таблеток (опытная лабораторная работа) представлены в таблице 1.
Пример 2.
Количественное определение аскорбиновой кислоты, парацетамола, кодеина фосфата, фенилэфрина гидрохлорида и хлорфенирамина малеата в таблетках "Пенталгин от простуды".
Для приготовления испытуемого раствора около 0,270 г (точная навеска) тщательно растертых таблеток, предварительно освобожденных от оболочки, и 0,100 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 5 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 7,4 (к 0,025 М раствору К2HPO4·3Н2О добавляют по каплям концентрированную фосфорную кислоту до рН 7,4) и перемешивают в течение 10 минут. Полученный раствор доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,150 г парацетамола, около 0,050 г аскорбиновой кислоты (точные навески) и 0,100 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 5 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 7,4 и перемешивают до растворения веществ. К полученному раствору добавляют 5,0 мл раствора РСО-2, доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм.
Для приготовления раствора РСО-2 около 0,080 г кодеина фосфата, около 0,050 г фенилэфрина гидрохлорида и около 0,040 г хлорфенирамина малеата (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл фосфатного буферного раствора с рН 7,4 и перемешивают до растворения веществ. Полученный раствор доводят до метки тем же буферным раствором и перемешивают.
По 5,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 4,6×150 мм с сорбентом Zorbax SB C8 с размером частиц 3,5 мкм в режиме линейного градиента с использованием в качестве ПФ смеси элюента А (фосфатный буферный раствор с рН 3,0) и элюента В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0) в объемном соотношении 1:1. Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 216 нм.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемых таблетках по формуле:
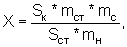
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mст, mc и mн - массы стандарта определяемого вещества в растворе РСО, средняя масса ядра и масса навески растертых ядер, взятой для приготовления испытуемого раствора, соответственно, в граммах.
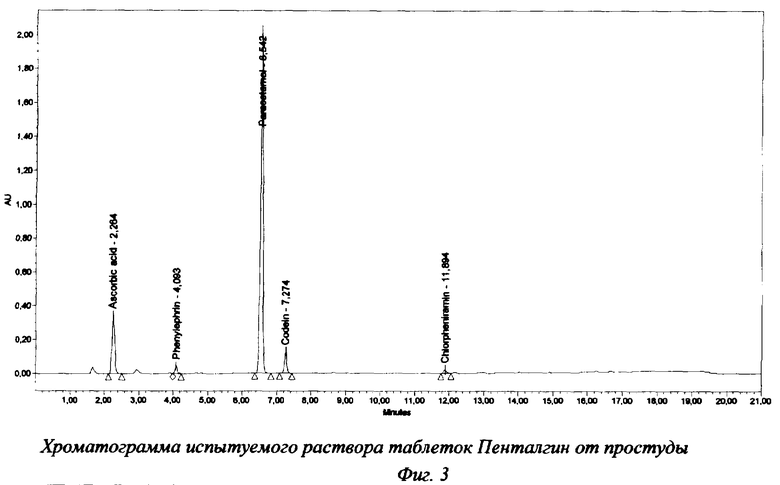
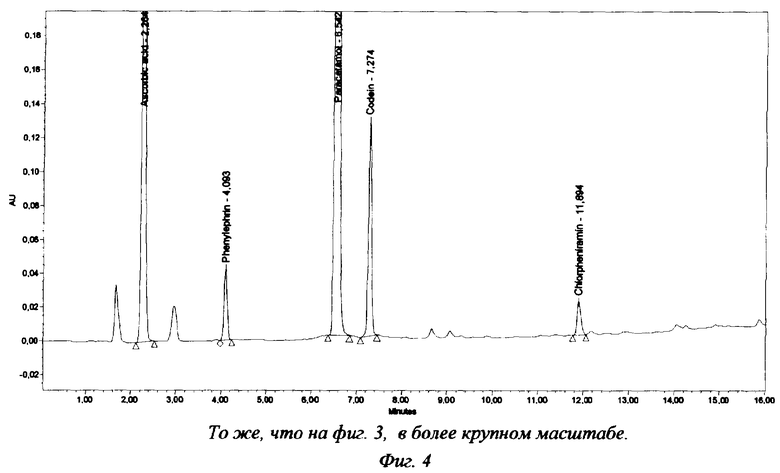
Хроматограммы испытуемого раствора таблеток "Пенталгин от простуды" представлены на фиг.3 и 4. Результаты анализа таблеток (опытная лабораторная работа) представлены в таблице 2.
Пример 3.
Количественное определение аскорбиновой кислоты, парацетамола, кодеина фосфата, фенилэфрина гидрохлорида и хлорфенирамина малеата в гранулированном порошке "Пенталгин от простуды".
Для приготовления испытуемого раствора около 2,5 г (точная навеска) тщательно растертого гранулированного порошка и 0,100 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 5 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 7,4 и перемешивают в течение 10 минут. Полученный раствор доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,150 г парацетамола, около 0,050 г аскорбиновой кислоты (точные навески) и 0,100 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 5 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 7,4 и перемешивают до растворения веществ. К полученному раствору добавляют 5,0 мл раствора РСО-2, доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм.
Для приготовления раствора РСО-2 около 0,080 г кодеина фосфата, около 0,050 г фенилэфрина гидрохлорида и около 0,040 г хлорфенирамина малеата (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл фосфатного буферного раствора с рН 7,4 и перемешивают до растворения веществ. Полученный раствор доводят до метки тем же буферным раствором и перемешивают.
По 5,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 4,6×150 мм с сорбентом Zorbax SB C8 с размером частиц 3,5 мкм в режиме линейного градиента с использованием в качестве ПФ смеси элюента А (фосфатный буферный раствор с рН 3,0) и элюента В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 1:1). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 216 нм.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в одной дозе анализируемого порошка по формуле:
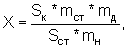
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mст, mд и mн - массы стандарта определяемого вещества в растворе РСО, средняя масса одной дозы гранулированного порошка (5,0 г) и масса навески растертого гранулированного порошка, взятой для приготовления испытуемого раствора, соответственно, в граммах.
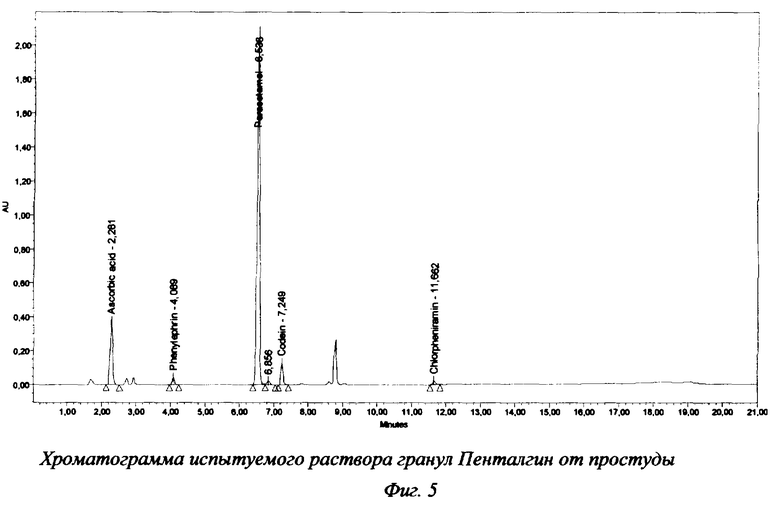
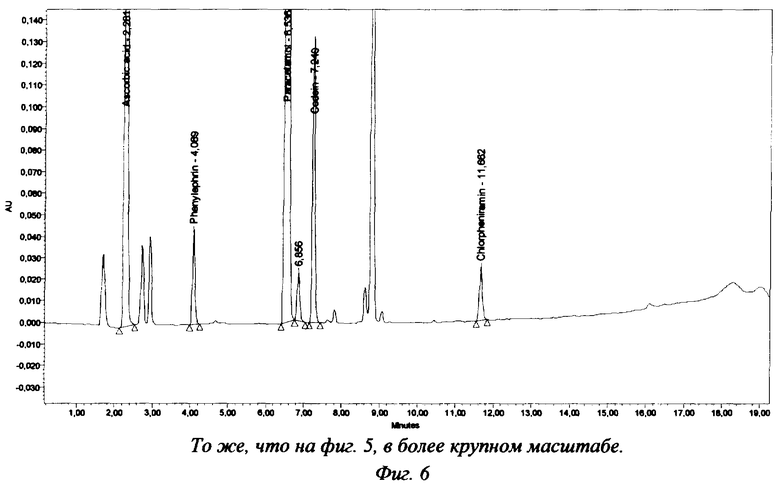
Хроматограммы испытуемого раствора гранулированного порошка "Пенталгин от простуды" представлены на фиг.5 и 6. Результаты анализа гранулированного порошка (опытная лабораторная работа) представлены в таблице 3.
Пример 4.
Количественное определение парацетамола, теофиллина, кофеина, фенобарбитала и эфедрина гидрохлорида в таблетках "Нео-теофедрин".
Для приготовления испытуемого раствора около 0,130 г (точная навеска) тщательно растертых таблеток помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 3,0 и перемешивают в течение 10 минут. Полученный раствор доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,060 г парацетамола и около 0,020 г теофиллина (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл фосфатного буферного раствора с рН 3,0 и перемешивают до растворения веществ. К полученному раствору добавляют 5,0 мл раствора РСО-2, доводят до метки тем же буферным раствором, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм.
Для приготовления раствора РСО-2 около 0,100 г кофеина, около 0,040 г фенобарбитала и около 0,040 г эфедрина гидрохлорида (точные навески) помещают в мерную колбу вместимостью 50 мл, добавляют 5 мл ацетонитрила и 10 мл фосфатного буферного раствора с рН 3,0 и перемешивают до растворения веществ. Полученный раствор доводят до метки тем же буферным раствором и перемешивают.
По 5,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 3,9×150 мм с сорбентом Nova-Pak С 18 с размером частиц 4,0 мкм в режиме линейного градиента, используя в качестве ПФ один из вариантов:
а) смесь элюентов А (фосфатный буферный раствор с рН 3,0) и В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 1:1). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 206 нм.
б) смесь элюентов А (смесь ацетонитрила и воды в объемном соотношении 1:
1), В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 1:1) и С (вода). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 206 нм.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемых таблетках по формуле:
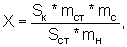
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mст, mс и mн - массы стандарта определяемого вещества в растворе РСО, средняя масса таблетки и масса навески растертых таблеток, взятой для приготовления испытуемого раствора, соответственно, в граммах.
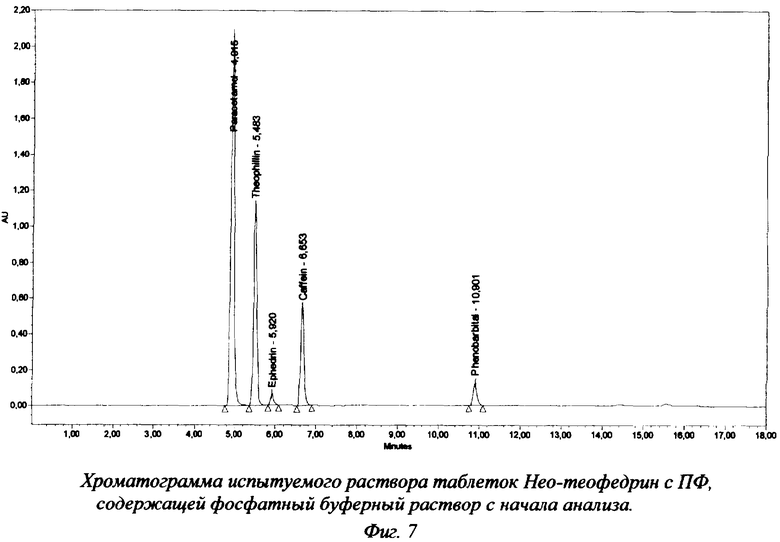
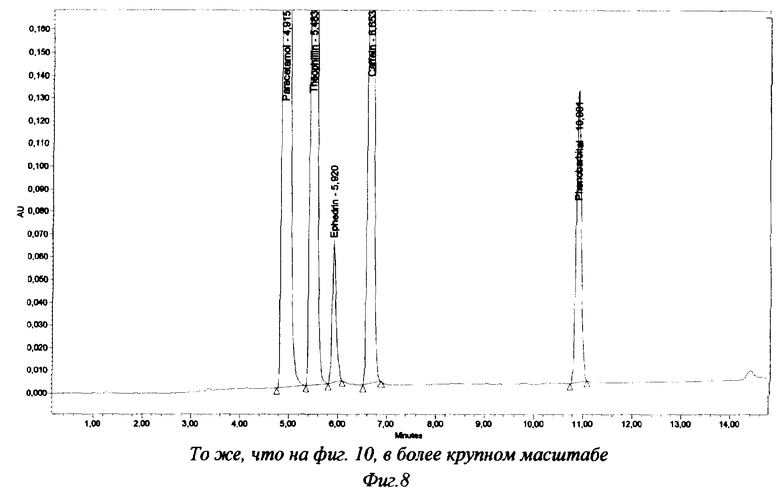
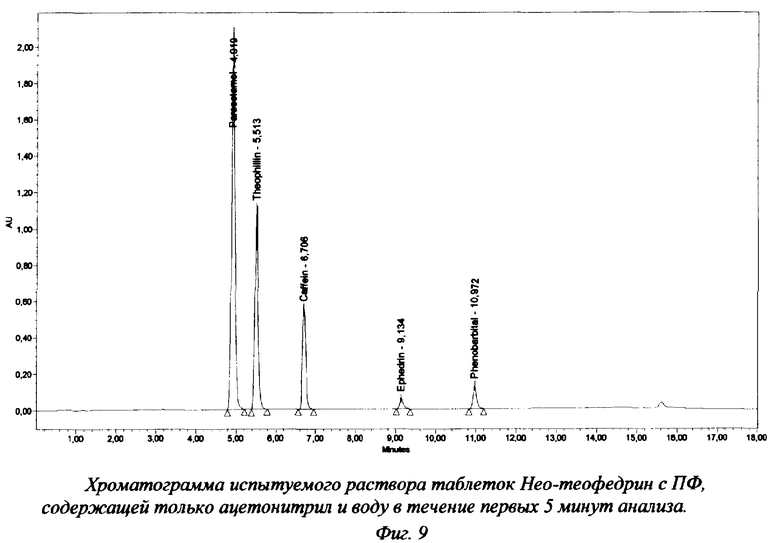
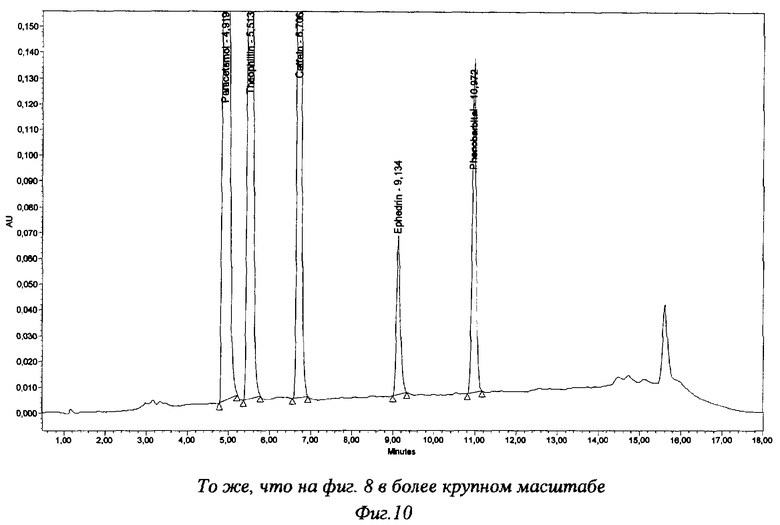
Хроматограммы испытуемого раствора таблеток "Нео-теофедрин" представлены на фиг.7-10. Результаты анализа таблеток (промышленная серия) представлены в таблице 4.
Пример 5.
Количественное определение анальгина, парацетамола, кофеина, фенобарбитала и кодеина фосфата в таблетках "Пенталгин ICN".
Для приготовления испытуемого раствора около 0,160 г (точная навеска) тщательно растертых таблеток и 0,120 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл воды и перемешивают в течение 10 минут. Полученный раствор доводят до метки водой, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,060 г анальгина, около 0,060 г парацетамола (точные навески) и 0,120 г сульфита натрия помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл воды и перемешивают до растворения веществ. К полученному раствору добавляют 5,0 мл раствора РСО-2, доводят до метки водой, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм.
Для приготовления раствора РСО-2 около 0,200 г кофеина, около 0,040 г фенобарбитала и около 0,032 г кодеина фосфата (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл ацетонитрила и 15 мл воды и перемешивают до растворения веществ. Полученный раствор доводят до метки водой и перемешивают.
По 5,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 4,0×150 мм с сорбентом Nucleosil 100 С 18 с размером частиц 5,0 мкм в режиме линейного градиента с использованием в качестве ПФ смеси элюентов А (смесь ацетонитрила и воды в объемном соотношении 1:1), В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 1:1) и С (вода). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 212 нм.
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в анализируемых таблетках по формуле:
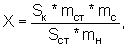
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mст, mс и mн - массы стандарта определяемого вещества в растворе РСО, средняя масса таблетки и масса навески растертых таблеток, взятой для приготовления испытуемого раствора, соответственно, в граммах.
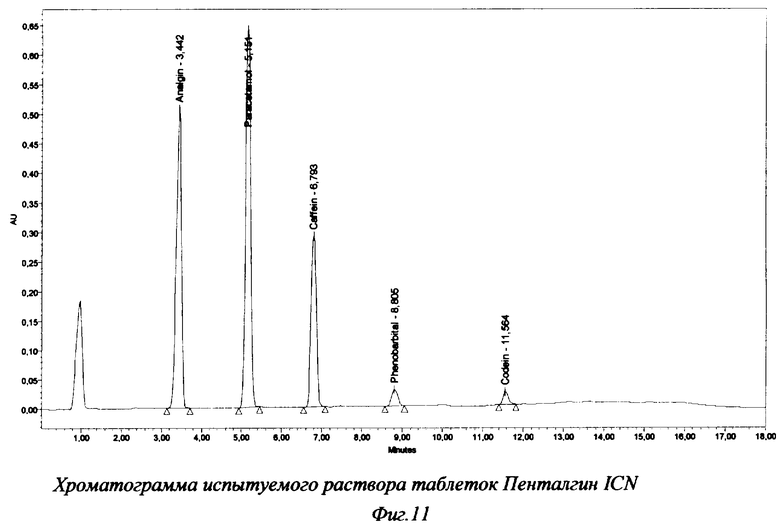
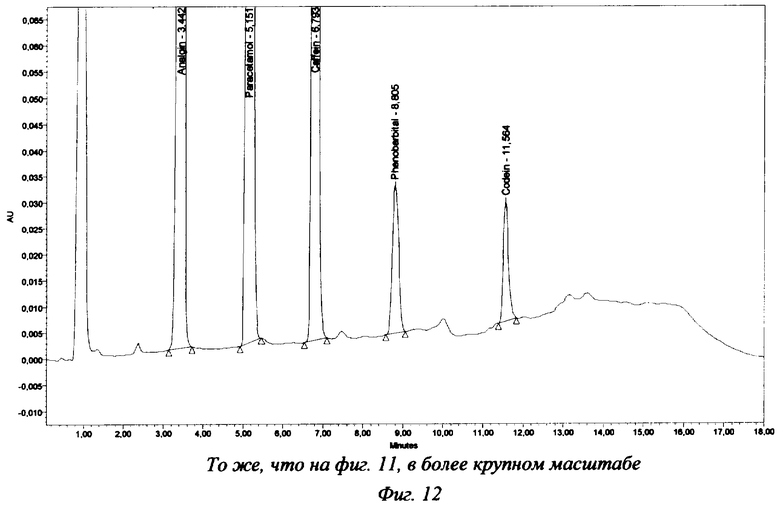
Хроматограммы испытуемого раствора таблеток "Пенталгин ICN" представлены на фиг.11 и 12. Результаты анализа таблеток (промышленная серия) представлены в таблице 5.
Пример 6.
Количественное определение кодеина фосфата, нипагина и нипазола в сиропе "Коделак".
Для приготовления испытуемого раствора около 5,0 мл сиропа помещают в мерную колбу вместимостью 50 мл, добавляют 15 мл смеси ацетонитрила и воды (объемное соотношение 3:7), перемешивают, доводят до метки той же смесью растворителей, перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
Для приготовления раствора РСО около 0,090 г кодеина фосфата, около 0,075 г нипагина и около 0,025 г нипазола (точные навески) помещают в мерную колбу вместимостью 100 мл, добавляют 15 мл смеси ацетонитрила и воды (объемное соотношение 3:7) и перемешивают до растворения веществ. Доводят до метки той же смесью растворителей и перемешивают.
5,0 мл полученного раствора помещают в мерную колбу вместимостью 50 мл, доводят до метки смесью ацетонитрила и воды (объемное соотношение 3:7), перемешивают и фильтруют через гидрофильный мембранный фильтр с размером пор 0,45 мкм, отбрасывая первые 5 мл фильтрата.
По 20,0 мкл испытуемого раствора и раствора РСО последовательно хроматографируют на жидкостном хроматографе с УФ-детектором и колонкой 3,9×150 мм с сорбентом Nucleosil 100 С18 с размером частиц 5,0 мкм в режиме линейного градиента, используя в качестве ПФ один из вариантов:
а) смесь элюентов А (смесь ацетонитрила и воды в объемном соотношении 1:
1), В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 3:2) и С (вода). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Расход подвижной фазы 1,0 мл/мин. Длина волны детектирования - 212 нм.
б) смесь элюента А (фосфатный буферный раствор с рН 3,0) и В (смесь ацетонитрила и фосфатного буферного раствора с рН 3,0 в объемном соотношении 3:
2). Получают не менее 3 хроматограмм каждого раствора.
Состав ПФ в течение анализа изменяется по следующей программе:
Рассчитывают площади пиков определяемых компонентов и находят количество каждого компонента в разовой дозе анализируемого сиропа (5,0 мл) по формуле:
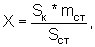
где Sк и Sст - средние значения площадей пиков определяемых компонентов на хроматограммах растворов испытуемого и РСО соответственно;
mс - масса стандарта определяемого вещества в растворе РСО, в граммах.
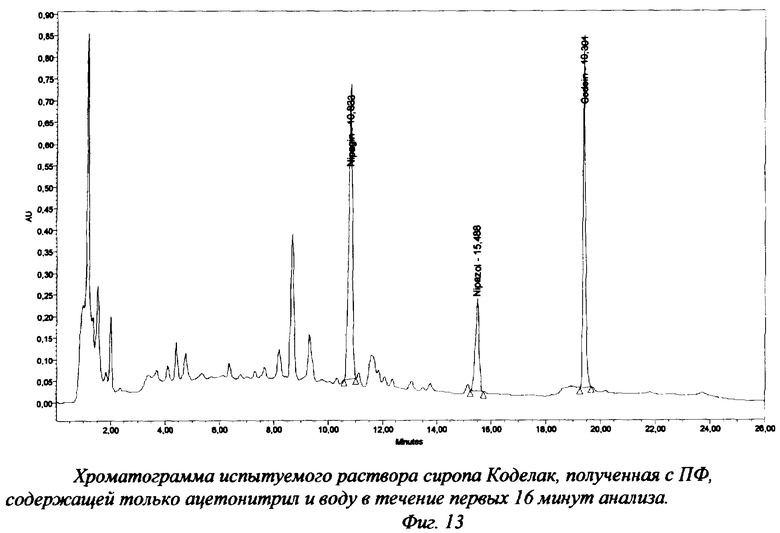
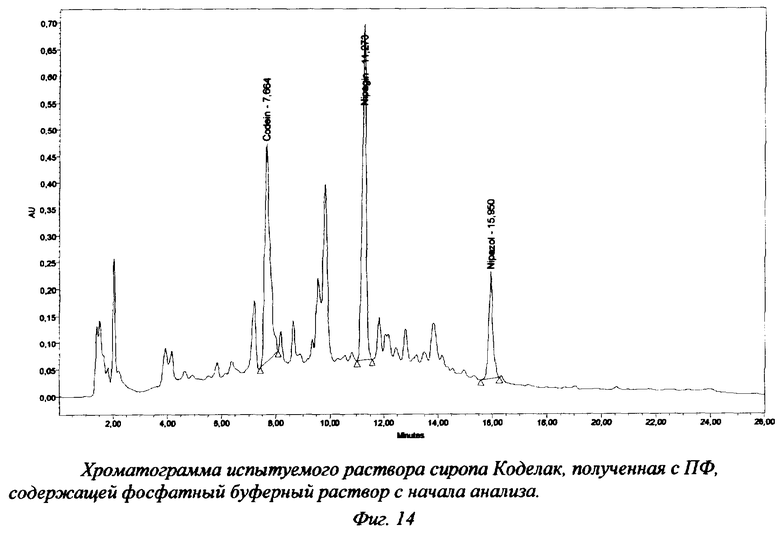
Хроматограммы испытуемого раствора сиропа "Коделак" представлены на фиг.13 и 14. Результаты анализа сиропа (опытная лабораторная работа) представлены в таблице 6.
Сравнительная характеристика предлагаемого и известного способов представлена в табл. 7.
В таблице 8 приведен расчет степени извлечения кодеина фосфата по результатам анализа модельных растворов, содержащих все действующие и вспомогательные вещества таблеток "Пенталгин от простуды".
Как показано в приведенных выше примерах и видно по представленным фигурам, при анализе препаратов, не содержащих анальгин или не идентифицированные компоненты растительного сырья (Коделак сироп), пики всех определяемых и вспомогательных веществ полностью разделяются при изменении состава ПФ от фосфатного буферного раствора с рН 3,0 до смеси ацетонитрила с этим же фосфатным буферным раствором в объемном соотношении 1:1.
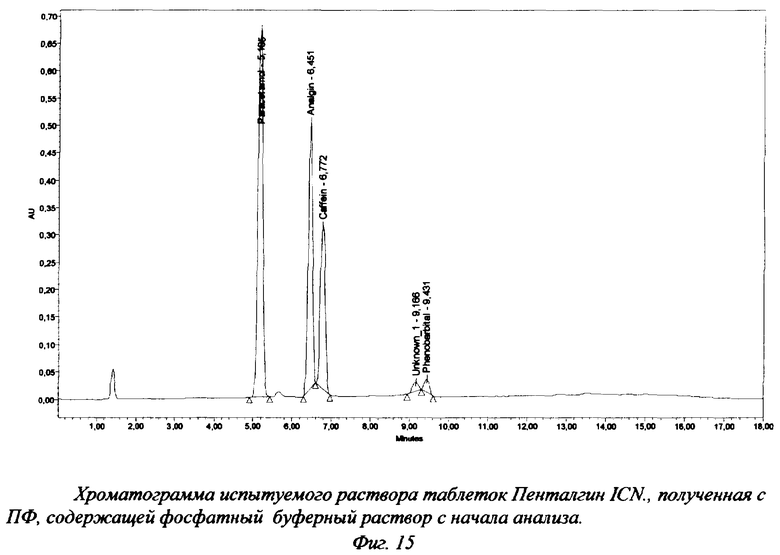
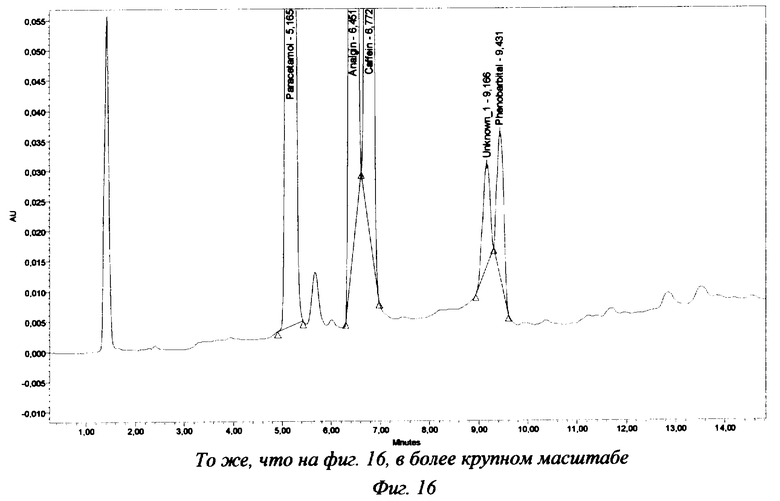
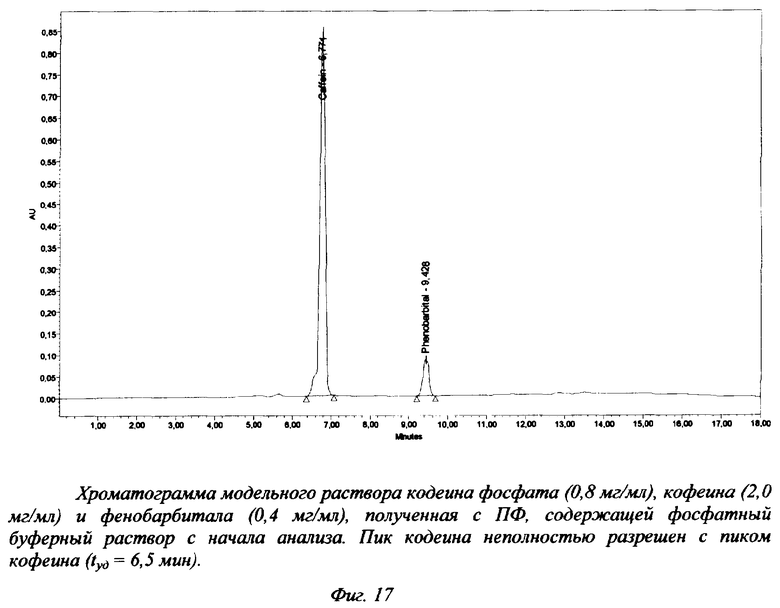
Для препаратов, в состав которых входят анальгин (Пенталгин ICN) или не идентифицированные компоненты растительного сырья (Коделак сироп), применение указанной градиентной программы не дает удовлетворительного результата. В первом случае не удается достичь разделения пиков анальгина и кодеина (фиг.15-17), а во втором наблюдается неполное разделение пиков кодеина и не идентифицированных компонентов растительного сырья (фиг.14).
В предлагаемом способе решение указанной проблемы основано на проведенных нами предварительных исследованиях, которые показали, что с применяемых в работе обращенных фаз типа Нуклеосил 100 С18 и Nova-Pak С18 кодеина фосфат не элюируется смесями ацетонитрил - вода. В соответствии с этим хроматографическим свойством кодеина на начальном этапе градиента вводится ПФ, содержащая только ацетонитрил и воду, а фосфатный буферный раствор с рН 3,0 вводится в ПФ после выхода всех пиков, кроме кодеина. Как видно по фиг.11, 12 (анализ таблеток Пенталгин ICN) и по фиг.13 (анализ сиропа Коделак) такой методический прием позволяет достичь полного разделения пиков всех определяемых и мешающих веществ и кодеина, что позволяет получить точные количественные результаты.
Наши исследования также показали, что аналогичным хроматографическим свойством обладает и эфедрин. В соответствии с этим введение на начальном этапе градиента ПФ, содержащую только ацетонитрил и воду, возможно также и при анализе препаратов, содержащих эфедрин, например, таблеток "Нео-теофедрин" (фиг.9, 10). Но такие таблетки могут быть проанализированы и с введением в ПФ фосфатного буферного раствора с рН 3,0 с начала анализа (фиг.7, 8).
Предложено: способ одновременного количественного определения состава многокомпонентных лекарственных препаратов методом обращенно-фазовой ВЭЖХ с помощью ультрафиолетового детектора. Способ отличает проведение анализа препаратов, содержащих: (1) парацетамол, пропифеназон, кофеин, фенобарбитал, кодеина фосфат или (2) парацетамол, аскорбиновую кислоту, кодеина фосфат, фенилэфедрина гидрохлорид, хлорфениламина малеат или (3) парацетамол, теофиллин, кофеин, фенобарбитал, эфедрина гидрохлорид или (4) кодеина фосфат, нипагин, нипазол - в одну стадию в режиме линейного градиента, при этом состав подвижной фазы изменяется от фосфатного буферного раствора с рН 3,0 до смеси его с ацетонитрилом в объемном соотношении 1:1. Изобретение позволяет достичь полного разделения пиков всех определяемых и мешающих веществ и получить точные количественные результаты. 1 з.п. ф-лы, 17 ил., 8 табл.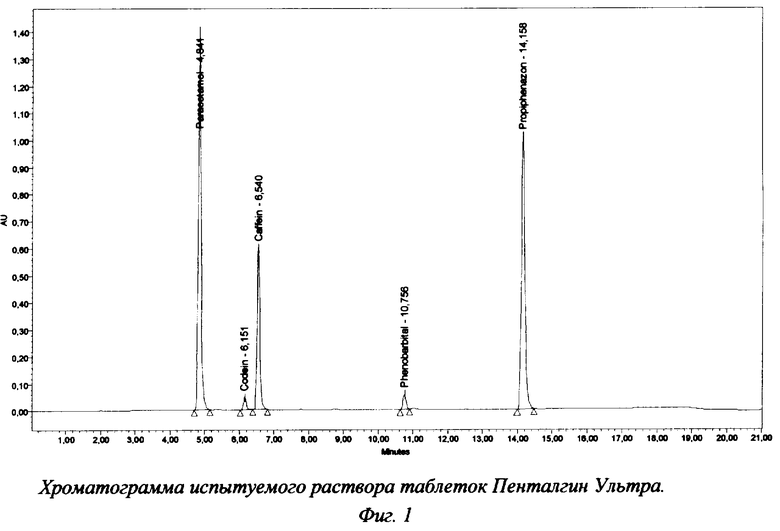
| Реферат из АБД Medline: Senyuva H | |||
| et al | |||
| Simultaneous high-performance liquid chromatographic determination of paracetamol, phenylephrine HCl, and chlorpheniramine maleate in pharmaceutical dosage forms | |||
| J | |||
| Chromatogr | |||
| Sci | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Реферат АБД Medline: Soto-Otero R | |||
| et al | |||
| High performance liquid chromatographic procedure for the | |||
Авторы
Даты
2005-12-27—Публикация
2003-06-23—Подача