Изобретение относится к области медицины, а именно к использованию химических соединений с целью создания лекарственных средств для лечения любых аутоимунных заболеваний, в механизмах патогенеза которых принимает участие фактор некроза опухоли (ФНО), в частности ревматоидного артрита, анкилозирующего спондилоартрита, воспалительных заболеваний кишечника и псориаза.
Наиболее широкое признание среди методов биологического лечения широкого круга аутоимунных заболеваний в наши дни нашла антицитокиновая терапия. Она началась с нейтрализации фактора некроза опухоли (ФНО) (по старой терминологии - ФНО-α), роль которого в развитии и клинических проявлениях аутоиммунных заболевании не вызывает сомнений, моноклональными антителами. Использование данного принципа лечения позволило добиться результатов, значительно превосходящих результаты назначения классических базисных средств (Elliot M.J., Maini R.N., Feldmann M. et al. Treatment of rheumatoid arthritis with chimeric monoclonal antibodies to tumour necrosis factor α. Arthritis Rheum, 1993, v.36, 1681-1690; Maini R., Breedveld F., Kalden J. et al. Therapeutic efficacy of multiple intravenous infusions of anti-tumor necrosis factor a monoclonal antibody combined with low-dose weekly methotrexate in rheumatoid arthritis. Arthr.Rheum., 1998, v.41, p.1552-1563.). Впоследствии эти препараты были с большим успехом использованы также для лечения ряда других воспалительных заболеваний, прежде всего анкилозирующего спондилита и псориатического артрита (Furst D., Keystone E., Breedveld F. et al. Updated consensus statement on tumour necrosis factor blocking agents for the treatment of rheumatoid arthritis and other rheumatic diseases. Ann.Rheum.Dis., 2001, v.60, suppl.III, iii 2-5).
Все эти препараты представляют собой крупные белковые молекулы, полученные методами генной инженерии, что определяет путь их введения (только парентерально - внутривенно или подкожно) и возможные побочные эффекты, в том числе серьезные инфузионные и аллергические реакции. Кроме того, в части случаев к этим белковым препаратам вырабатываются нейтрализующие антитела, что приводит к снижению лечебного действия рассматриваемых средств (Van der Laken C.J., Voskuyl A.E., Roos J.C. et al. Imaging and serum analysis of immune complex formation of radiolabelled infliximab and anti-infliximab in responders and non-responders to therapy for rheumatoid arthritis. Ann.Rheum.Dis., 2007, v.66, p.253-256). В связи со сложностью производства генно-инженерных биологических препаратов их стоимость весьма высока, что заметно ограничивает сферу использования данных препаратов. Поэтому поиск синтетических низкомолекулярных ингибиторов ФНО, которые могли бы применяться внутрь, не были столь дороги и не вызывали указанных нежелательных явлений, представляется очень актуальным
Задачей, на решение которой направлено предлагаемое изобретение, является расширение арсенала средств, которые могут быть использованы в качестве новых эффективных лекарств для нейтрализации токсического действия фактора некроза опухоли при лечении ряда аутоиммунных заболеваний, например, таких как ревматоидной артрит, анкилозирующий спондилоартрит, воспалительные заболевания кишечника и псориаз.
Поставленная задача решается применением гидрированных пиридо ([4,3-b]) индолов формулы (1) в качестве средства для нейтрализации токсического действия фактора некроза опухоли
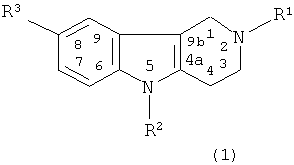
где R1 выбран из группы, содержащей CH3-, CH3CH2-, PhCH3-;
R2 выбран из группы, содержащей H-, PhCH2- или 6-СН3-3-Py-(CH2)2-;
R3 выбран из группы, содержащей H-, CH3- или Br-.
Одним из соединений, которое можно применять в качестве средства для нейтрализации токсического действия фактора некроза опухоли, может быть соединение формулы (1), в котором
R1 соответствует CH3CH2-, R2 соответствует H-, а R3- H-.
Или в котором R1 соответствует PhCH3-, R2 соответствует H-, а R3- H-
Или соединение, где R1 соответствует CH3-, R2 соответствует PhCH2-, a R3-CH3-.
Или соединение, где R1 соответствует CH3-, R2 соответствует 6-СН3-3-Py-(CH2)2-, а R3- Н-.
Или соединение, где R1 соответствует СН3-, R2 соответствует 6- СН3-3-Py-(СН2)2-, а R3-СН3-.
Или соединение, где R1 соответствует СН3-, R2 соответствует Н-, а R3-H-.
Или соединение, где R1 соответствует СН3-, R2 соответствует Н-, а R3-СН3-.
Или соединение, где R1 соответствует СН3-, R2 соответствует Н-, а R3- Br-.
Или дигидрохлорид 2,8-диметил-5-[2-(6-метил-пиридил-3)этил]-2,3,4,5-тетрагидро-1H-пиридо [4,3-b] индола (Димебон).
Указанные в формуле 1 соединения могут представлять собой соли с фармацевтически приемлемыми кислотами.
Соединения формулы 1 являются известными соединениями, широко применяемыми в фармакологической практике, имеющими антиагрессивную, антиаритмическую и другие виды активности.
В последние годы было найдено, что производные гидрированных пиридо[4,3-b] индолов формулы (1), в частности димебон, способны действовать на два основных подтипа ионотропных глутаматных рецепторов ЦНС млекопитающих - АМРА и NMDA рецепторы, что позволяет использовать их в качестве средства для лечения Болезни Альцгеймера и геропротекторного средства. Димебон потенцирует трансмембранные токи, вызываемые активацией АМРА-рецепторов, и одновременно блокирует NMDA-рецепторы (В.В.Григорьев, О.А.Драный, С.О.Бачурин. Сравнительное исследование механизма действия препаратов димебона и мемантина на АМРА и NMDA-подтипы глутаматных рецепторов нейронов головного мозга крыс // Бюлл. Экспер. Биол. мед., 2003, №11, с.535-538).
Авторами изобретения неожиданно было найдено, что соединения формулы (1) обладают способностью нейтрализации токсического действия фактора некроза опухоли, в частности его цитотоксическое действие.
Техническим результатом, который может быть получен при осуществлении изобретения, является значительное снижение инвалидности и летальности больных вышеперечисленными аутоиммунными заболеваниями.
Еще одним аспектом изобретения является фармакологическое средство для нейтрализации токсического действия фактора некроза опухоли, содержащее активное начало и фармацевтически приемлемый носитель, новизна которого заключается в том, что в качестве активного начала оно содержит эффективное количество гидрированного пиридо(4,3-b) индола формулы (1).
Еще одним аспектом изобретения является способ лечения аутоиммунных заболеваний на основе нейтрализации токсического действия фактора некроза опухоли, включающий введение средства по п.1 в дозе 0,001-10 мг/кг массы тела по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта.
Понятие «фармакологическое средство» подразумевает использование любой лекарственной формы, содержащей соединение формулы (1), которая могла бы найти профилактическое или лечебное применение в медицине в качестве средства для лечения АЗ.
Понятие «эффективное количество», используемое в данной заявке, подразумевает использование того количества соединений формулы (1), которое в соединение с его показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме.
Для получения фармакологического средства одно или несколько соединений формулы (1) смешиваются как активный ингредиент с фармацевтически приемлемым носителем, известным в медицине согласно принятым в фармацевтике способам. В зависимости от лекарственной формы препарата носитель может иметь различные формы.
Примерами носителей, которые могут использоваться для изготовления таких композиций, являются лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. Приемлемыми носителями для желатиновых капсул с мягким покрытием являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п.
Кроме того, фармацевтические средства могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, корригенты, соли для изменения осматического давления, буферы, покрывающие агенты или антиоксиданты. Они могут также содержать и другие вещества, обладающие ценными терапевтическими свойствами.
Препаративные формы могут представлять собой обычную стандартную дозу и могут быть приготовлены известными в фармации способами.
В Таблице 1 приведены результаты, демонстрирующие защитный эффект димебона в концентрации 10 мкг/мл от токсического действия ФНО на клетки L929, где * указывает на достоверность разницы между показателями выживаемости клеток при действии на нее ФНО и ФНО + димебон при p≤0.05.
Возможность осуществления изобретения с реализацией заявляемого назначения и получением технического результата подтверждается, но не исчерпывается следующими примерами.
Пример 1. Изучение ингибирующего ФНО действия димебона на модели цитотоксического действия ФНО на клетки мышиных фибробластов L929.
В качестве представителя соединений общей формулы (1) был взят лекарственный препарат «Димебон», дигидрохлорид 2,8-диметил-5-[2-(6-метил-пиридил-3-)этил]-2,3,4,5-тетрагидро-1Н-пиридо[4,3-b]индола формулы (1.1).
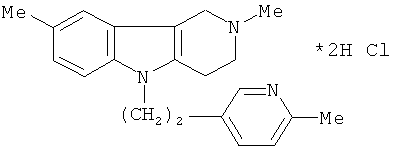
Биологическую активность димебона (IPD) в концентрации 1, 10 и 100 мкг/мл оценивали по его способности модулировать цитотоксическое действие ФНО на клетки мышиных фибробластов L929. Клетки мышиных фибробластов L929 в количестве 2×104 клеток помещали в лунки 96-луночных планшетов (Nunc, Дания) в 100 мкл полной среды 199 (Биолот, Россия), содержащей 10% эмбриональной телячьей сыворотки (Биолот, Россия) и инкубировали 18 часов. Затем удаляли среду и к монослою клеток добавляли по 50 мкл полной среды, содержащей актиномицин Д (2 мкг/мл) (Reanal, Венгрия), димебон, а затем двукратные разведения ФНО (от 100 нг/мл до 0, 1 пкг/мл) (Reanal, Венгрия) и инкубировали при 37º в CO2- инкубаторе (КЕВО Biomed, Швеция). Через 18 часов в каждую лунку добавляли по 10 мкл раствора МТТ (Sigma, США) в PBS (5 мг/мл) и инкубировали 2,5 часа. По истечении указанного времени супернатант удаляли, к оставшимся клеткам добавляли 100 мкл DMSO (Биолот, Россия), оптическую плотность измеряли при 540 нм на приборе Titertek Multiskan MCC (Flow Laboratories, Финляндия). Оценку жизнеспособности вычисляли по формуле C=(A-B):A×100%, где A -светопоглощение в контрольной лунке, B - светопоглощение в тестируемой лунке. Измерения проводили в четырех повторах.
Результаты экспериментов (Таблица 1) показали, что инкубация клеток с димебоном при его концентрации 10 мкг/мл в инкубационной среде с последующим добавлением фактора некроза опухоли вызывала существенный защитный эффект, т.е. сохранение жизни клеток L929. Этот цитопротекторный эффект димебона проявлялся при очень широком диапазоне концентраций ФНО: от 6,25 нг/мл до 0,8 пкг/мл, т.е. в 10000-кратном диапазоне.
Как видно из приведенной таблицы, димебон оказывает прямое защитное действие от цитотоксического действия ФНО на клетки мышиных фибробластов L929, увеличивая выживаемость клеток до 5 раз.
Проведенные дополнительно исследования показали, что при концентрации димебона 1 мкг/мл защитный эффект не обнаруживался, а при концентрации 100 мкг/мл димебон был токсичен для клеток L929 (не проиллюстрировано).
Изложенные факты позволяют нам рекомендовать Димебон для лечения любых аутоимунных заболеваний, в механизмах патогенеза которых принимает участие фактор некроза опухоли. Этот препарат разрешен для повседневного практического применения и хорошо переносится пациентами. Он может рассматриваться как перспективный базисный антиаутоимунный препарат. Его очевидным достоинством является возможность применения внутрь.
Использование Димебона в современной антицитокиновой терапии может уменьшить ее затратность, улучшить переносимость и существенно повысить эффективность лечения наиболее резистентных форм, в частности, ревматоидного артрита, анкилозирующего спондилоартрита, воспалительных заболеваний кишечника и псориаза.
Изобретение относится к области фармацевтики и медицины и касается средства для нейтрализации токсического действия фактора некроза опухоли на основе гидрированных пиридо (4,3-b) индолов формулы (1), фармацевтического средства на его основе и способа лечения аутоиммунных заболеваний на основе нейтрализации токсического действия фактора некроза опухоли. 3 н. и 10 з.п. ф-лы, 1 табл., 1 пр.
1. Средство для нейтрализации токсического действия фактора некроза опухоли на основе гидрированных пиридо (4,3-b) индолов, формулы 1

где R1 выбран из ряда CH3-, CH3CH2- или PhCH3-,
R2 выбран из ряда H-, PhCH2- или 6-СН3-3-Py-(CH2)2-,
R3 выбран из ряда H-, CH3- или Br-.
2. Средство по п.1, где R1 соответствует CH3CH2-, R2 соответствует H-, R3 - H-.
3. Средство по п.1, где R1 соответствует PhCH3-, R2 соответствует H-, R3 - H-.
4. Средство по п.1, где R1 соответствует CH3-, R2 соответствует PhCH2-, R3 - CH3-.
5. Средство по п.1, где R1 соответствует CH3-, R2 соответствует 6-CH3-3-Py-(CH2)2-, R3 - H-.
6. Средство по п.1, где R1 соответствует CH3-, R2 соответствует 6-CH3-3-Py-(CH2)2-, R3 - CH3-.
7. Средство по п.1, где R1 соответствует CH3-, R2 соответствует Н-, R3 - Н-.
8. Средство по п.1, где R1 соответствует CH3-, R2 соответствует H-, R3 - CH3-.
9. Средство по п.1, где R1 соответствует CH3-, R2 соответствует Н-, R3 - Br-.
10. Средство по п.1, где указанное соединение представляет собой дигидрохлорид 2,8-диметил-5-[2-(6-метил-пиридил-3)этил]-2,3,4,5-тетрагидро-1H-пиридо [4,3-b] индола (Димебон).
11. Средство по п.1, где указанные соединения представляют собой соли с фармацевтически приемлемыми кислотами.
12. Фармакологическое средство на основе соединения по п.1, содержащее активное начало и фармацевтически приемлемый носитель, отличающееся тем, что в качестве активного начала оно содержит эффективное количество соединения формулы (1).
13. Способ лечения аутоиммунных заболеваний на основе нейтрализации токсического действия фактора некроза опухоли, включающий введение средства по п.1 в дозе 0,001-10 мг/кг массы тела, по крайней мере, один раз в день в течение периода, необходимого для достижения терапевтического эффекта.
| Антигистаминное средство "димебон | 1963 |
|
SU1138164A1 |
| RU 2006143332 A, 20.06.2008 | |||
| RU 2006142521 A, 20.06.2008 | |||
| RU 2006101999 A, 10.08.2007. | |||
Авторы
Даты
2013-03-10—Публикация
2012-01-17—Подача