Изобретение относится к применению соединений формулы A-R-X или их фармацевтически приемлемых солей для получения фармацевтической композиции для профилактики или лечения заболеваний, соответственно, нежелательных состояний, в частности, у человека, а также к таким композициям.
Чрезмерный стойкий алкоголизм часто приводит к заболеванию печени, так называемому стеатозу (жировая дистрофия печени), который далее может прогрессировать до воспаления печени, соответственно, гепатита, и в поздней стадии до цирроза печени. При этом риск и масштаб соответствующего поражения печени прямо зависят от количества и продолжительности алкоголизма, причем риск индивидуально различен. Обусловленное алкоголем воспаление печени (алкогольный гепатит) представляет собой при известных условиях угрожающее жизни заболевание, которое может протекать с лихорадкой, желтухой, а также с повышением количества лейкоцитов. Такого рода обусловленные алкоголем воспаления печени излечимы путем полной алкогольной абстиненции, за исключением рубцов при циррозе печени.
Наряду с этим, вызываемым алкоголем, так называемом стеатозном гепатите или алкогольном стеатогепатите (ASH) возникают также гепатиты у людей, которым несвойственно никакое злоупотребление алкоголем или которые сами по себе вообще не употребляют никакого алкоголя. Такие гепатиты провоцируются, например, токсинами окружающей среды, например, при работах на лакировальных предприятиях и/или также за счет лекарственных средств.
Известно, что окислительные процессы при обмене веществ протекают с помощью цитохромов. В случае цитохромов речь идет о множестве различных ферментов, активный центр которых имеет гем-структуру. В случае множества реакций окисления и гидроксилирования они катализируют перенос электронов к акцептору.
Важную роль играют, например, цитохромы семейства Р450 (CYP-450). При этом речь идет о монооксигеназах, которые являются убиквитарными и относятся к самым важным ферментам метаболизма гидрофобных, чужеродных организму веществ и модификации гидрофобных гормонов, стероидов.
Одной из главных задач цитохром-Р450-ферментов является солюбилизация чужеродных организму веществ путем гидроксилирования и, таким образом, приведение к почечной экскреции. Поэтому цитохром-Р450-ферменты играют важную роль при детоксикации.
Предполагают, что примерно половина всех современных лекарственных веществ гидроксилируется с помощью цитохром-Р450-ферментов печени. Поэтому длительность пребывания многих лекарственных веществ в организме отчасти значительно снижается за счет активности цитохром-Р450-ферментов. Преобладающее количество цитохрома Р450 у млекопитающих находится в печени, так как она представляет собой центральный орган детоксикации. Цитохром Р450, как правило, находится в форме, связанной с мембраной эндоплазматического ретикулума.
Цитохром-Р450-ферменты также играют ключевые роли в способствовании резистентности насекомых против инсектицидов и растений против гербицидов.
В своей основной структуре цитохром Р450 обладает шестикратно координированной гем-группой, по которой катализируется реакция согласно следующей схеме:
RH+O2+2H++2e-→ROH+H2O
При этом оба необходимых для этой реакции электрона предоставляются, например, NADPH-цитохром-Р450-редуктазой, которые ассоциированы с ферментным комплексом. Таким образом, в случае Р450, возникают также цитотоксические реактивные формы кислорода (ROS).
Известно, что, как в случае алкоголизма, так и также в случае неалкогольного стеатозного гепатита, а также в случае панкреатита, индуцируется синтез цитохрома Р450-2Е1. Функция и способ действия этой, сильно отличающейся от других цитохромов изоформы описывается, например, в М.Н. Wang и др., в Archives of Biochemistry and Biophysics, 317, 299-304 (1995). В соответствии с этим, фермент имеет канал длиной примерно 15 Å, на конце которого находится реакционно-способный центр с обладающим центральным атомом железа гем-циклом.
Уже давно предполагают, что также химиотерапевтические средства, которые используют при лечении раковых заболеваний, разрушаются цитохром-Р450-ферментами.
Однако в недавнем исследовании авторами Jiang и др. («Cytochrome P450 2J2 Promotes the Neoplastic Phenotype of Carcinoma Cells and is Up-regulated in Human Tumors» в Cancer Res., 65, 4707-4715 (2005)) впервые показано, что цитохром Р450 даже может оказывать способствующее раковому заболеванию действие.
Было показано, что экспрессия генов в высокой степени регулируется цитохромом Р450 2J2 в человеческих опухолях. В случае цитохрома Р450 2J2 речь идет об эпоксигеназе, которая превращает субстрат арахидоновую кислоту в четыре различных изомерных эпоксиэйкозатриеновых кислоты (ЕЕТ). При исследовании, далее, показано, что ЕЕТ обладают подавляющим апоптоз действием, так как они защищают опухолевые клетки от воздействия факторов некроза опухоли, и, таким образом, повышают продолжительность жизни раковых клеток. Сверх того, они способствуют митозу, а также пролиферации опухолевых клеток.
Также было показано, что EETs способствуют ангиогенезу, то есть, образованию новых кровеносных сосудов. Этот процесс играет важную роль в случае роста опухолей (Pozzi и др. «Characterization of 5,6- and 8,9-Epoxyeicosatrienoic Acids (5,6- and 8,9-EET) as Potent in “Vivo Angiogenic Lipids”», J. Biol. Chem., 280, 27138-27146 (2005)).
В статье Schattenberg и др. («Hepatocyte CYP2E1 overexpression and steatohepatitis lead to impaired hepatic insulin signalling» в J. Biol. Chem., 280, 9887-9894 (2005)), напротив, впервые связывают сверхпродуцирование цитохрома Р450 с диабетом.
Müller-Enoch и др., в Z. Naturforsch., 56c, 1082-1090 (2001) описывают ингибирование цитохрома Р450 2В1 крысы с помощью лизофосфатидилхолинов, лизофосфатидилинозита, а также арахидоновой и олеиновой кислот, соответственно, с помощью моноацилглицеринов, моноолеилглицеринов и монопальмитоилглицеринов.
Далее, авторами T. Haehner, D. Müller-Enoch и др., в Z. Naturforschung, 50c, 599-605 (2004) описывается влияние одноцепочечных липидных молекул на активность изоформы цитохрома Р450 2В1 крысы.
Задачей настоящего изобретения является предоставить средство для получения фармацевтической композиции, которая пригодна для профилактики или лечения раковых заболеваний, патологических последствий злоупотребления алкоголем, вирусного гепатита, стеатогепатита, острого и хронического панкреатита, токсических заболеваний почек, гепатической резистентности к инсулину при сахарном диабете, поражений печени при болезни Wilson и сидерозах, реперфузионных повреждений при ишемии, для применения в качестве антидота против токсинов окружающей среды и лекарственной интоксикации, для удлинения продолжительности пребывания лекарственных средств в организме или для борьбы против токсических побочных действий при введении химиотерапевтических средств.
Эта задача решается с помощью соединения согласно указанным в формуле изобретения признакам.
А именно, неожиданно найдено, что вышеуказанные заболевания можно лечить с помощью такого рода соединений. Эти соединения ингибируют образование реактивных форм кислорода (ROS), в частности, кислородных радикалов, как супероксид-анион (О2 ·-), а также пероксида водорода (Н2О2), которые не расходуются в прямой окислительно-восстановительной реакции, в случае цитохрома Р450, в частности, изоформ семейства генов 2, конкретно 2Е1, а также 2J2.
Точно так же установлено, что это соединение также ингибирует превращение арахидоновой кислоты в изомерные эпоксиэйкозатриеновые кислоты. Кроме того, было показано, что также гидроксилирование чужеродных организму веществ может подавляться при введении такого соединения.
Используемые согласно изобретению соединения отвечают формуле
A-R-X
Альтернативно можно использовать также их фармацевтичеси приемлемые соли.
При этом R означает алифатический или ароматический углеводородный остаток предпочтительно с 6-40 атомами углерода, который, в частности, имеет концевой остаток А, являющийся гидрофильным или представляющий собой водород, и Х означает остаток, обладающий, по меньшей мере, одной свободной электронной парой у атома углерода или гетероатома и/или з-электронами. Остаток R, в частности, является липофильным.
Обычно остаток R является алкильным остатком. Так, он может быть линейным или разветвленным, может иметь одинарные, двойные или тройные связи и может быть замещенным. Обычно он имеет алифатическую основу с 6-26, в частности, с 8-22 атомами углерода. Предпочтительны, углеводородные цепи с основой из 10-15, в частности, 10-13 атомов углерода. Если R является алициклическим или ароматическим углеводородным остатком, который может быть конденсирован и/или липофильно замещенным, то он обычно содержит по меньшей мере 5, соответственно, 6 атомов углерода и самое большее 40, соответственно, самое большее 25 атомов углерода.
Дальнейшие предпочтительные минимальные длины составляют 7, соответственно, 8 С-атомов и дальнейшие предпочтительные максимальные длины составляют 22, соответственно, 20 С-атомов.
Предпочтительными остатками Х являются гетероциклы, а также алкинильные остатки. Гетероциклы представляют собой, в частности, содержащие азот, кислород и/или серу гетероциклы. Гетероциклы могут быть ароматическими и/или неароматическими и обычно включают 5 или 6 атомов в цикле. В некоторых случаях Х может быть также конденсированным гетероциклом. Примерами такого рода гетероциклов являются имидазол, пиррол, пиразол, пиридин, пиразин, индол, изоиндол, индазол. Предпочтительными гетероциклами являются включающие 6 и, в частности, 5 атомов циклы с одним, двумя или тремя гетероатомами. Другими подходящими гетероциклами являются, например, тиазолы, триазолы, фураны.
Предпочтительные алкины имеют структуру -С≡С-R12, причем R12 означает водород или, в случае необходимости, замещенный С1-С15-, соответственно, максимально С10-алкильный остаток, который, в свою очередь, в случае необходимости может иметь двойные или тройные связи. Обычно, однако, R12 имеет максимально 5 С-атомов, в частности, максимально 3 С-атома. В дальнейшем предпочтительном, предлагаемом согласно изобретению, варианте осуществления остаток Х означает, например,
- первичные, вторичные и третичные амины,
- замещенные или незамещенные диазофункции, как, например, гидразины и гидразоны,
- нитрил, изонитрил,
- S-содержащие функциональные группы, как, например, тио- и изотиоцианаты, алкилсульфиды, сульфоксиды, тиольные группы,
- метилендиоксидную функциональную группу,
- простые алкиловые эфиры и простые алкиловые тиоэфиры.
Остатки Х предпочтительно представляют собой остатки, которые координируются с простетической гем-группой.
Гидрофильным концом А используемой согласно изобретению молекулы может быть любая фармацевтически пригодная гидрофильная функция и, в частности, -ОН, -СООН, фосфатная группа, группа эфира фосфорной кислоты, сульфатная группа, аминогруппа, SH, а также аминокислота или многоатомный спирт, карнитин (γ-N-триметиламино-ß-гидроксимасляная кислота), начальная часть сфингозина (1,3-дигидрокси-2-аминопропильный остаток). Однако, когда А означает водород, А не является никаким гидрофильным концом, и это соединение также можно применять в виде предлагаемой согласно изобретению фармацевтической композиции. Предпочтительными аминокислотами, в частности, с положительно или отрицательно заряженными остатками, являются такие, как, например, лизин, аргинин, гистидин, аспарагиновая кислота, глутаминовая кислота, глутамин, аспарагин, гомоцистеин, серин, гомосерин и/или цитруллин. Предпочтительные многоатомные спирты представляют собой, в частности, глицерин. Как глицерин, так и сахара, в случае необходимости, могут быть замещенными. Предпочтительным замещением является, например, обмен ОН-группы на аминогруппу или SH-группу, соответственно, фосфатную или сульфатную группу. Согласно особенно предпочтительному варианту осуществления, А означает глицериновый остаток формулы
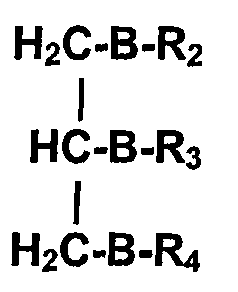
причем, по меньшей мере, один из остатков R2-R4 представляет собой вышеуказанный остаток RX и В означает кислород, серу, селен или селенат, аминогруппу, фосфатную группу или сульфатную группу. Согласно дальнейшему, предлагаемому согласно изобретению, варианту осуществления, другим остатком из R2-R4 является фосфатидилхолиновый остаток, фосфатидилэтаноламино-остаток, фосфатидилсериновый остаток или фосфатидилинозитный остаток. Другими пригодными остатками являются, например, уже указанные выше аминокислоты, в частности таковые с положительно или отрицательно заряженными остатками.
В случае производных 1,2-диацил-sn-глицерин-3-фосфорной кислоты, предлагаемое согласно изобретению применение включает также основную структуру кефалинов, церамидов, лецитинов и соответствующих фосфолипидов, которые имеют конец Х, как указанный выше.
Неразветвленные, насыщенные и незамещенные представители Х-R или BR2-4 отвечают, например, следующим формулам:
а) алканольный остаток: НО-СН2-(СН2)а-Х
b) алкилсульфатный остаток: -O3SO-CH2-(CH2)a-X
с) алкил-СоА-остаток: СоА-S-CO-(CH2)a-X
d) остаток алкановой кислоты: НООС-(СН2)а-Х
причем а означает, предпочтительно, по меньшей мере 6 и, в частности, по меньшей мере 7. Особенно предпочтительно, а означает по меньшей мере 8, причем, в высшей степени предпочтительно, означает 9. Предпочтительные максимальные значения для а представляют собой 40, в частности, 26, причем предпочтительны 22, в частности, 12. Особенно предпочтительными являются 11 и, конкретно, 10.
Соответствующие формулы для разветвленных, ненасыщенных или замещенных представителей сразу ясны специалисту в данной области и поэтому не требуется никакого отдельного представления.
Дальнейшими примерами алифатических остатков R являются, например, додекановый остаток, октадеканольный остаток, ундеканилсульфатный остаток, пальмитил-СоА-остаток или остаток лауриновой кислоты.
Согласно альтернативной форме осуществления, з-электроны остатка Х представляют собой, в частности, таковые из олефиновых, в частности, ацетиленовых, двойных, соответственно, тройных связей, которые обычно являются концевыми. Особенно предпочтительными остатками являются связанный через атом азота имидазольный остаток или этинильный остаток (-С≡С-).
Было обнаружено, что в случае предлагаемого согласно изобретению применения вышеуказанных соединений, в частности таких, которые в качестве Х содержат имидазолированную или этинилированную жирную кислоту и которые in vitro проявляют себя как особенно эффективные, как, например, 17-октадецинил-1-кислота, продолжительность пребывания многих биологически активных веществ в крови может существенно удлиняться за счет того, что карбоксильный конец такой молекулы заменяют, например, сульфатным остатком или близлежащие к карбоксильному концу, то есть, 1-3, С-атома (α,ß,γ-положение) алифатической основы замещают путем присоединения 2 метильных групп или алифатического или ароматического цикла. Таким образом, также улучшается активность in vivo в соответствии с активностью in vitro.
Так, например, 2,2-диметил-11-додециниловая кислота и 10-ундецинилсульфат in vitro проявляют сравнимо высокое ингибирование активности цитохрома-Р450, как 10-ундециниловая кислота, в то время как они in vivo намного превосходят последнюю.
При этом предпочтительно предусматривают, чтобы длина алифатической основы включала 6-26, в частности, 9-20, соответственно, 19, атомов углерода, если в случае R1 речь идет об имидазольном остатке. Представителем этой предпочтительной группы является, например, 12-имидазолилдодеканол или 1-имидазолилдодекан. Относительно структурных формул этих и других веществ следует указать на прилагаемые фигуры.
Согласно предлагаемому согласно изобретению варианту осуществления, далее, предусматривают, чтобы длина алифатической основы включала 6-26 атомов углерода, если в случае R1 речь идет об этинильном остатке. Представителем этой предпочтительной группы является, например, 17-октадецинил-1-кислота.
Согласно дальнейшему варианту осуществления, длина алифатической основы включает 9-13 атомов углерода, если в случае R1 речь идет об этинильном остатке. Представителями этой предпочтительной группы являются, например, 2,2-диметил-11-додециниловая кислота, 10-ундецинилсульфат, 10-ундециниловая кислота или 10-ундецинол.
Эти соединения обладают рядом преимуществ. Прежде всего, во-первых, они непосредственно недоступны для ферментов ß-окислительного метаболизма и поэтому сразу не метаболизируются ими.
Фосфоглицериды, а также триглицериды, согласно вышеприведенному определению, которые замещены в двух положениях глицеринового остатка с помощью остатка формулы -R-X, например, этинилированого или имидазолированного алифатического остатка, после резорбции прежде всего гидролизуются в кишечнике, и именно таким образом, что отщепляется один из обоих алифатических остатков. Таким образом, получаются этинилированные, соответственно, имидазолированные моноглицериды, которые на основании их растворимости также называются лизолипоиды и которые с помощью липопротеинов, соответственно, нековалентных агрегатов из липидов и белков образуют мицеллоподобные частицы и служат для транспорта водонерастворимых липидов в кровь, для доставки к местам действия в организме.
То же самое имеет значение, так же в случае этинилированных, соответственно, имидазолированных моноглицеридов, согласно вышеприведенному определению, которые уже введены как таковые.
Так как определенные патогенные ткани так же, как, например, ткани опухоли, обладают высоким энергообменом и за счет нагрузки факторами роста (VEGF, PDGF) способствуют собственной васкуляризации, нагруженные указанными этинилированными, соответственно, имидазолированными моноглицеридами липопротеины вместе с кровотоком предпочтительно мигрируют в эти ткани. «Упаковка» этинилированных, соответственно, имидазолированных алифатических соединений в форме лизолипидов, делает возможным их целенаправленный транспорт в указанные патогенные ткани.
В случае предлагаемого согласно изобретению применения, соединения обладают активностью при лечении рака, причем, кроме этого, также ингибируется превращение арахидоновой кислоты в эпоксиэйкозатриеновые кислоты. Последние способствуют клеточному делению и клеточной пролиферации и ингибируют апоптоз опухолевых клеток. Точно так же при применении такого соединения ингибируется гидроксилирование химиотерапевтических средств, которое в конечном счете приводит к их экскреции и вместе с тем к их инактивации. Вместе с тем, такое соединение можно применять как для прямой, так и для адъювантной противоопухолевой терапии. На этом основании вышеуказанная предпочтительная форма осуществления, которая делает возможным целенаправленный транспорт в патогенную ткань, является особенно предпочтительной.
Согласно изобретению, дополнительно, предусматривают фармацевтическую композицию, содержащую предлагаемое согласно изобретению соединение в фармацевтически приемлемом носителе.
Возможные показания в отношении предлагаемого согласно изобретению соединения, а также, содержащей его фармацевтической композиции, кроме этого заключаются в лечении последствий злоупотребления алкоголем. Это, в частности, поражения печени или также другие, обусловленные алкоголем воспалительные процессы. Наряду с обусловленными чисто алкоголем поражениями печени, также условия питания и эндокринные факторы, такие как, например, ожирение, а также сахарный диабет и гиперлипидемия, независимо от алкоголя, также вызывают тяжелое поражение печени, которое через стеатозный гепатит (неалкогольный стеатогепатит = NASH) может достигать цирроза печени. Такого рода алкогольные и неалкогольные стеатозные заболевания часто протекают вместе с вирусной инфекцией печени. При этом возможно очень быстрое прогрессирование заболевания. Обнаружено, что все вышеуказанные заболевания, а также их причины или последствия можно лечить с помощью предлагаемых согласно изобретению соединений.
Также найдено, что эти вещества очень хорошо пригодны для лечения воспалений поджелудочной железы. Такого рода воспаления, соответственно, панкреатиты, могут провоцироваться, наряду со злоупотреблением алкоголем, также токсическими веществами. К ним относят, в частности, токсины окружающей среды, как профессиональные химикалии, или также лекарственные средства. Также вирусные инфекции или метаболически-эндокринные факторы могут вызывать такого рода воспаления поджелудочной железы, причем во всех случаях в возникновении болезни и в прогрессировании заболевания принимают участие реактивные формы кислорода.
Предлагаемый согласно изобретению фармацевтический препарат является подходящим также при лечении сахарного диабета, а именно сахарного диабета типа 2 и типа 1.
Токсические заболевания почек, а также другие заболевания, которые провоцируются, например, побочными действиями при введении химиотерапевтических средств, в частности, клеточных токсинов, таких, как металлические комплексы, цисплатин, карбоплатин, титаноцендихлорид или комплексы на основе золота, можно лечить с помощью предлагаемого согласно изобретению лекарственного средства. При этом, в частности, обнаружено, что можно предотвращать органотоксичность металлических комплексов или других токсических средств, таких как галогенированные углеводороды, а именно, моно- и полигалогенированные углеводороды, в том числе дымовые наркотики галотанового типа, а также соответствующие ароматические углеводороды, нитрозамины, акриламид или лекарственные средства, такие как парацетамол, метотрексат, изониазид или амино-гликоридные антибиотики или рентгеновские контрастные средства. Предлагаемое согласно изобретению лекарственное средство, таким образом, также пригодно для лечения органотоксичности токсинов окружающей среды, в частности, в качестве антидота для органов, как печень, почки, центральная нервная система, поджелудочная железа и т.п.
Так, например, становится возможной также более высокая дозировка цитостатических средств в случае терапии раковых заболеваний и на этом основании за счет адъювантной терапии также можно повышать перспективы успеха химиотерапии.
Совершенно неожиданно оказалось пригодным избежание повреждений, которые возникают за счет реперфузии биологических тканей, например, после инфаркта органа, в частности, сердца, а также головного мозга (инфаркт миокарда, инсульт). Так, например, в экспериментах на животных показано, что такого рода реперфузионные повреждения способствуют разрушению ткани на 60-80%, соответственно, что распространение некроза ткани можно уменьшать на этот фактор. Уже давно известно, что основной причиной реперфузионных повреждений являются кислородные радикалы, которые образуются во время ишемии.
Предлагаемое согласно изобретению средство, таким образом, особенно пригодно для избежания реперфузионных повреждений в случае трансплантированных органов. Такого рода органы вплоть до их трансплантации в организм нового реципиента хранят в охлажденном питательном растворе. После трансплантации и последующего присоединения к сосудистой системе реципиента, через них снова проходят жидкости организма, что приводит к реперфузионным повреждениям. Благодаря введению предлагаемого согласно изобретению средства до и во время хранения, а также незадолго до имплантации в организм реципиента, можно решить также и эту важную проблему трансплантации.
Аккумуляция переходного металла железа (соответственно, меди согласно М. Wilson) вызывает потенцирование провоцируемых цитохромом Р450 окислительных повреждений. Наряду с перегрузкой железа в рамках сидерозов известно, что при реперфузионных повреждениях за счет ишемии наступает отчетливое повышение внутриклеточной концентрации свободного железа. Внутриклеточное повышение концентрации железа также возникает за счет токсических соединений, как, например, цисплатин или галогенированные углеводороды, или за счет вирусных гепатитов. Это касается прежде всего печени, а также и почек, например, в случае цисплатина, который выводится ренально. Биохимической основой окислительных повреждений за счет переходного металла железа (соответственно, меди согласно М. Wilson) является реакция Fenton:
Н2О2+Fe2+→Fe3++HO·+HO-
Образующийся в рамках реакционного цикла цитохрома Р450 Н2О2 (окислительно-восстановительный потенциал + 0,32 В) при этом превращается в чрезвычайно сильно окисляющий гидроксильный радикал HO· (окислительно-восстановительный потенциал + 2,31 В).
Повышение концентрации свободного железа в рамках обусловленной цисплатином нефропатии описывается, например, в статье Baliga и др. («Role of cytochrome P450 as a source of catalytic iron in cisplatin-induced nephrotoxicity», Kidney Int., 54, 1562-1569 (1998)). Повышение концентрации железа в случае реперфузионных повреждений за счет ишемии или в случае вирусного гепатита описывается, например, Paller и др. («Cytochrome P450 mediates tissue damaging hydroxyl radical formation during reoxygenation of the kidney», Proc. Natl. Acad. Sci. USA, 91, 7002-7006 (1994); соответственно, Chapoutot и др. («Liver iron excess in patients with hepatotocellular carcinoma developed on viral C cirrhosis», Gut, 46, 711-714 (2000)).
Предлагаемые, согласно изобретению, вещества оказываются, в частности, ингибиторами человеческих изоформ семейства генов 2 цитохрома Р450, а именно, в частности, изоформ 2Е1 и 2J2, и вызываемых ими заболеваний.
Согласно особенно предпочтительному варианту осуществления изобретения, предусматривается, что фармацевтическую композицию включают в липосомы. На основании того факта, что лежащие в основе композиции соединения обладают длинными алифатическими остатками, их включение в липосомы представляет собой очень пригодную форму введения. Такие липосомы пригодны для внутривенного, внутримышечного, интраперитонеального, чрескожного или также перорального введения. В такой же степени также пригодно введение в виде аэрозоля.
Предлагаемые согласно изобретению соединения, однако, можно прямо вводить как таковые. Также в этом случае пригодны вышеуказанные формы введения.
Способы синтеза
Ниже указываются некоторые способы синтеза различных, предлагаемых согласно изобретению, соединений:
1. Синтез 12-имидазолил-1-додекановой кислоты
а) 12-Имидазолил-1-додекановую кислоту синтезируют согласно способу, который описывается в статье Alterman и др. («Fatty acid discrimination and omega-hydroxylation by cytochrome P450 4A1 and a cytochrome P4504A1/NADPH-P450 reductase fusion protein», Archives of Biochemistry and Biophysics, 320, 289-296 (1995)).
Для этого 12-бром-1-додеканол окисляют с помощью реактива Jones до 12-бром-1-додекановой кислоты. Твердую кислоту белого цвета затем этерифицируют с помощью диазометана с получением соответствующего метилового эфира. Сложный метиловый эфир непосредственно смешивают с имидазолом и при температуре 80оС в течение пяти часов превращают в метиловый эфир 12-имидазолил-1-додекановой кислоты. Таким образом, полученную густую массу распределяют между водой и дихлорметаном, органическую фазу сушат над Na2SO4 и выпаривают. Маслянистый остаток очищают хроматографически на силикагеле и затем растворяют в смеси из метанола и тетрагидрофурана (3:4), смешивают с LiOH·H2O и смесь в течение двух часов нагревают при температуре кипения с обратным холодильником. После выпаривания растворителя, остаток белого цвета снова растворяют в воде, экстрагируют дихлорметаном, подкисляют до значения рН 5-6 и снова экстрагируют этилацетатом. Этилацетатный экстракт сушат над Na2SO4, отфильтровывают и выпаривают. Твердый остаток белого цвета перекристаллизуют из смеси этанола с диэтиловым эфиром и получают 12-имидазолил-1-додекановую кислоту.
b) 12-Имидазолил-1-додеканол и 1-имидазолилдодекан синтезируют согласно способу, который описывается в статье Lu и др. («Heme-coordinating analogs of lauric acid as inhibitors of fatty acid ω-hydroxylation», Archives of Biochemistry and Biophysics, 337, 1-7 (1997)).
Для этого 12-бром-1-додеканол и имидазол в молярном соотношении 1:3 нагревают при температуре 80оС в течение 5 часов. Сырой продукт распределяют между водой и дихлорметаном. Органическую фазу сушат над Na2SO4 и выпаривают. 12-Имидазолил-1-додеканол перекристаллизуют из смеси бензола с н-гексаном.
с) 1-Имидазолилдодекан получают из 1-бромдодекана и имидазола в молярном соотношении 1:3 при перемешивании и нагревании при температуре 85°С. Сырой продукт растворяют в дихлорметане и трижды встряхивают с водой. Органическую фазу сушат над Na2SO4, отфильтровывают и выпаривают. Маслянистый остаток после выпаривания выкристаллизовывают из н-гексана и получают 1-имидазолилдодекан.
2. Синтез 12-имидазолил-1-фосфатидилхолина
Фосфатидилхолин в кислых условиях в присутствии дициклогексилкарбодиимида превращают в О-фосфорилизомочевину. К реакционной смеси добавляют 12-имидазолил-1-додеканол, который нуклеофильно воздействует на фосфорильную группу и образует с ней сложноэфирную связь, так что образуется 12-имидазолил-1-фосфатидилхолин. При этом осаждается дициклогексилмочевина. Для успешности этой реакции необходим в качестве катализатора 4-диэтиламинопиридин.
Механизм реакции подобен таковому этерификации по Steglich, при которой используют дициклогексилкарбодиимид, чтобы этерифицировать органическую кислоту с помощью спирта.
3. Синтез 1-пальмитоил-2-имидазолилглицеро-3-фосфатидилхолина
Принцип синтеза фосфатидилхолиндиглицерида, который включает немодифицированную жирную кислоту, а также «меченую» (то есть, в настоящем случае этинилированную или имидазолированную) жирную кислоту, описывается Eibl и др. («Synthesis of labeled phospholipids in high yield», Methods Enzymol., 98, 623-632 (1983)).
3а. Синтез 1,2-дипальмитоил-3-бензилглицерида
Для этого 1,2-изопропилиден-sn-глицерин растворяют в п-ксилоле и при добавлении трет-бутилата калия и бензилхлорида перемешивают. По окончании реакции в равных долях добавляют воду, а также диизопропиловый эфир и осуществляют разделение фаз. Содержащийся в верхней фазе 3-бензил-sn-глицерин получают путем выпаривания и подвергают дальнейшим стадиям очистки.
Затем очищенный 3-бензил-sn-глицерин с жирной кислотой, например, пальмитат, растворяют в тетрахлориде углерода. При добавке 4-диэтиламинопиридина и дициклогексилкарбодиимида образуются сложноэфирные связи между спиртовыми группами 3-бензил-sn-глицерина и карбоксильными группами жирных кислот, причем осаждается дициклогексилмочевина. Механизм реакции также называют как «этерификация по Steglich».
Выпавшую в осадок дициклогексилмочевину удаляют и растворитель выпаривают. После дальнейших стадий очистки получают в качестве продукта 1,2-дипальмитоил-3-бензил-sn-глицерид.
3b. Синтез 1,2-дипальмитоил-sn-глицерида
1,2-Дипальмитоил-3-бензил-sn-глицерид растворяют в тетрагидрофуране и в присутствии катализатора (10% Pd/C) гидрируют с помощью элементарного водорода. При этом бензильный остаток заменяется атомом водорода и образуется 1,2-дипальмитоил-sn-глицерид.
3с. Фосфорилирование 1,2-дипальмитоил-sn-глицерида
Фосфорилтрихлорид смешивают с растворенным в тетрагидрофуране триэтиламином и перемешивают при охлаждении льдом. Затем по каплям добавляют растворенный в тетрагидрофуране 1,2-дипальмитоил-sn-глицерид. При этом сначала образуется 1,2-дипальмитоил-sn-глицерид-3-фосфорилдихлорид.
Затем снова добавляют растворенный в тетрагидрофуране триэтиламин, по каплям добавляют растворенный в тетрагидрофуране бромэтанол и повышают температуру до 25°С. При этом образуется главным образом монохлорид сложного 1,2-дипальмитоил-sn-глицерид-3-фосфорилбромэтилового эфира и только в незначительном количестве в качестве побочного продукта соответствующий сложный дибромэтиловый эфир.
Смесь очищают, охлаждают, смешивают с карбонатом натрия и гексаном и встряхивают. При этом связь между фосфатным остатком и хлоридом гидролизуется. В качестве продукта образуется натриевая соль сложного 1,2-дипальмитоил-sn-глицерид-3-фосфорилбромэтилового эфира.
Подобным образом получают натриевые соли сложного 1,2-дипальмитоил-sn-глицерид-3-фосфорил-(N-бутоксикарбонил)-этаноламиноэфира, а также сложного 1,2-дипальмитоил-sn-глицерид-3-фосфорил-(N-бутоксикарбонил)-трет-бутилсеринового эфира.
3d. Гидролиз сложного 1,2-дипальмитоил-sn-глицерид-3-фосфоалкилового эфира
Сложный 1,2-дипальмитоил-sn-глицерид-3-фосфорилбромэтиловый эфир, или один из указанных, альтернативно полученных сложных фосфоалкиловых эфиров, растворяют в смеси из диэтилового эфира и дистиллированной воды, которая содержит CaCl2·2H2O.
Значение рН устанавливают равным 7,5 путем добавки Palitzsch-буфера. Затем добавляют фермент фосфолипазу А2 и перемешивают в течение 60 минут при температуре 35°С. При этом сложноэфирная связь в положении 2 глицеринового остатка гидролизуется и образуется соответствующий сложный 1-пальмитоил-sn-глицерид-3-фосфоалкиловый эфир, который в положении 2 содержит ОН-группу, а также свободная жирная кислота.
Полученную молекулу теперь в положении 2 глицеринового остатка можно целенаправленно этерифицировать с помощью «меченой» жирной кислоты, например, имидазолированной или этинилированной жирной кислоты. Таким же образом сложный фосфоалкиловый эфир в положении 3 можно переэтерифицировать с помощью пригодного спирта, как, например, холин, серин, этаноламин или инозит.
3е. Этерификация с помощью «меченой» жирной кислоты
в положении 2
Полученный сложный 1-пальмитоил-sn-глицерид-3-фосфоалкиловый эфир растворяют в тетрахлорметане, добавляют имидазолированную или этинилированную жирную кислоту и смесь перемешивают.
В случае добавляемой жирной кислоты речь идет, например, о 17-октадециновой кислоте, которая выпускается фирмой Sigma Aldrich. Точно так же речь может идти о 12-имидазолил-1-додекановой кислоте, которую можно синтезировать, как описывается в п.1.
Затем снова осуществляют «этерификацию по Steglich», в случае которой добавляют смесь 4-диэтиламинопиридина и дициклогексилкарбодиимида. При этом образуется сложноэфирная связь между оставшейся ОН-группой в глицериновом остатке и карбоксильной группой «меченой» жирной кислоты.
Выпавшую в осадок дициклогексилмочевину удаляют и растворитель выпаривают. После дальнейших стадий очистки получают в качестве продукта сложный 1-пальмитоил-2-ацил-sn-глицерид-3-фосфоалкиловый эфир.
3f. Переэтерификация сложного фосфоалкилового эфира в положении 3 глицеринового остатка.
Сложный 1-пальмитоил-2-ацил-sn-глицерид-3-фосфорилбром-этиловый эфир растворяют в хлороформе. Затем добавляют 2-пропанолтриметиламин. Реакционный сосуд инкубируют при температуре 50оС, затем растворитель удаляют с помощью азота. Продукт реакции очищают и таким образом получают «меченый» 1-пальмитоил-2-ацил-sn-глицерид-3-фосфатидилхолин.
Для получения «меченого» 1-пальмитоил-2-ацил-sn-глицерид-3-фосфатидилсерина, полученный, как указано выше, «меченый» сложный 1-пальмитоил-2-ацил-sn-глицерид-3-фосфорил(N-бутоксикарбонил)этаноламиноэфир растворяют в CH2Cl2 и добавляют трифторуксусную кислоту, а также хлорную кислоту. Затем перемешивают при охлаждении и промывают водой и метанолом. После разделения фаз, нижнюю фазу экстрагируют раствором Na2CO3 и выпаривают. После добавления метанола образуются кристаллы, в случае которых речь идет о «меченом» 1-пальмитоил-2-ацил-sn-глицерид-3-фосфатидилэтаноламине.
Поступают подобным образом в целях получения «меченого» 1-пальмитоил-2-ацил-sn-глицерид-3-фосфатидилсерина. В этом случае исходным веществом является полученный, как указано выше, «меченый» сложный 1-пальмитоил-2-ацил-sn-глицерид-3-фосфорил-(N-бутоксикарбонил)-трет-бутилсериновый эфир.
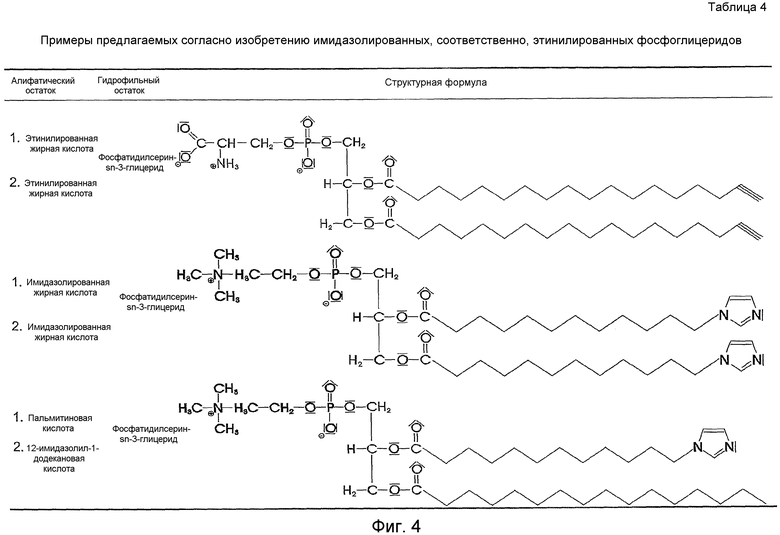
Таблицы
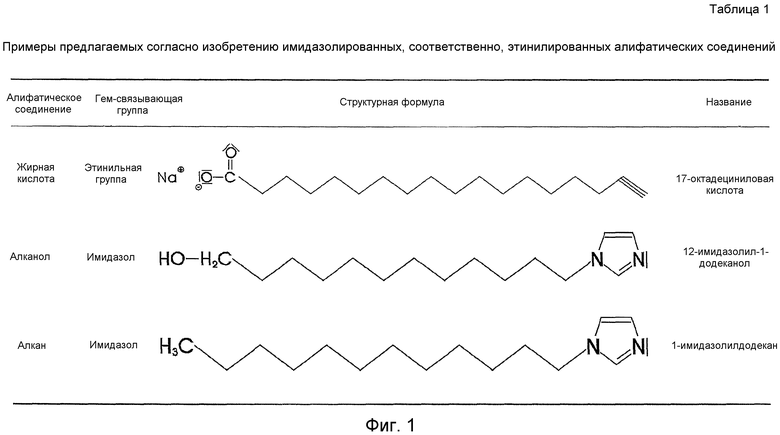
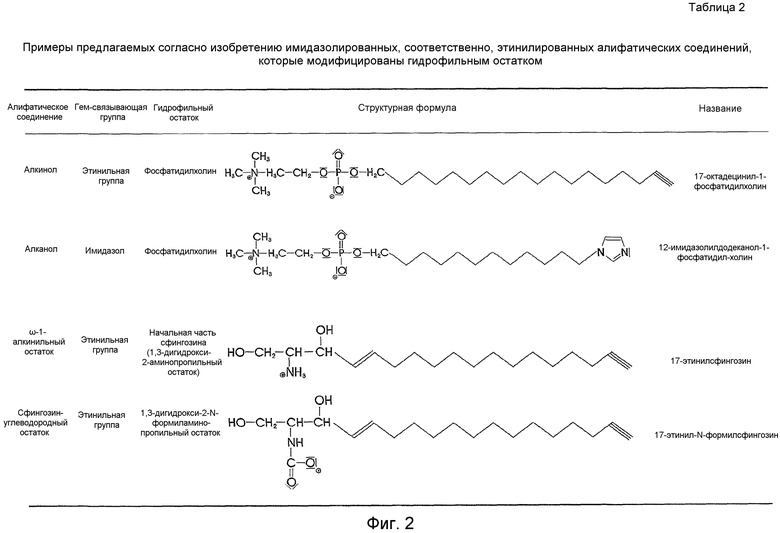
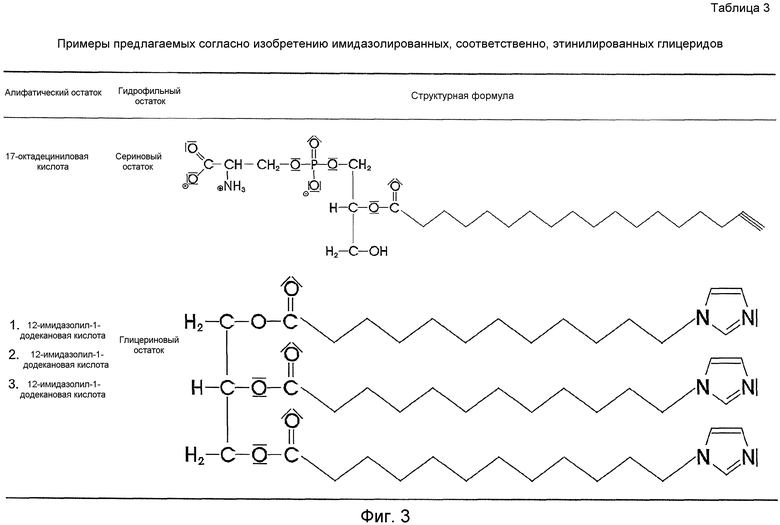
В таблицах 1-4 (см.фиг.1-4) перечислены некоторые типичные, предлагаемые согласно изобретению соединения.
В таблицах 1-3 представлены типичные, применяемые согласно изобретению соединения формулы A-R-X по п.1 формулы изобретения.
При этом специалисту в данной области непосредственно известно, что множество других соединений подпадает под указанную формулу изобретения. Так, алифатические остатки могут быть линейными или разветвленными, могут включать одинарные, двойные или тройные связи и могут быть замещены, и алифатическая основа может иметь 9-19 атомов углерода. Таким же образом углеводородная основа может образовываться с алициклическими и/или ароматическими углеводородами, причем в этом случае из-за циклических структур может быть необходимым вплоть до 40 атомов углерода.
В качестве гидрофильных остатков принимают во внимание также другие спирты, как инозит или этаноламин, соответственно, их глицериды.
Токсичность
Острую токсичность 12-имидазолил-1-додеканола (вещество 1) и 12-(1)-имидазолилдодекана (вещество 2) испытывали на самцах CD-крыс. При этом для 12-имидазолил-1-додеканола получали LD50 (14 дней), равную 1000 мг/кг массы тела, перорально, и для 12-(1)-имидазолил-1-додекана получали LD50 (14 дней), равную 1000 мг/кг массы тела, перорально.
вещество 2: 500 мг/кг массы тела, перорально
дозы:
Определение антинеопластического действия 12-имидазолил-1-додеканола
Для этого четыре линии раковых клеток высевали в, соответственно, «24-луночные планшеты» и культивировали в течение 24 часов. Затем к клеточной суспензии добавляли различные концентрации тестируемого вещества 12-имидазолил-1-додеканола, растворенного в диметилсульфоксиде (ДМСО). Концентрация ДМСО в клеточной среде составляла, соответственно, 0,1%. Эта концентрация ДМСО согласно контрольному опыту оказалась нетоксической, подсчеты клеток осуществляли, соответственно, после времени инкубации в течение четырех суток. Во всех случаях установлено сильное ингибирование пролиферации раковых клеток.
Определены следующие полумаксимальные ингибиторные концентрации, значения IC50, 12-имидазолил-1-додеканола:
В случае всех линий раковых клеток установлен сильный антинеопластический эффект ингибитора.
Оценка цитотоксичности 12-имидазолил-1-додеканола
Полумаксимальную цитотоксичность 12-имидазолил-1-додеканола определяли с помощью теста на цитотоксичность в отношении лактатдегидрогеназы.
При этом определены следующие значения:
Путем сравнения полумаксимальной цитотоксичности 500 мкМ с полумаксимальными ингибиторными константами IC50=50 мкМ для Panc-1 получают дифференциальный фактор 10000. Сверх того, можно сделать вывод, что 12-имидазолил-1-додеканол представляет собой высокоэффективный ингибитор пролиферации раковых клеток с относительно незначительной цитотоксичностью.
Другими словами, предлагаемые согласно изобретению вещества обладают широким терапевтическим «окном».
Ингибирование миграционной активности HepG2-клеток за счет 12-имидазолил-1-додеканола
Миграционные тест-условия: раковые печеночные клетки HepG2 включали в коллагеновый матрикс. Непрерывно в течение 900 минут фотографически контролировали 30 отдельных клеток. Определяли средний процент мигрирующих клеток.
Результат 1: необработанные контрольные HepG2-клетки проявляют среднюю миграционную активность 15%. При добавке 1 мкМ, соответственно, 10 мкМ 12-имидазолил-1-додеканола к матриксной среде миграционная активность клеток снижается на 50%, соответственно, 75%.
Результат 2: так как HepG2-клетки обладают очень сильной экспрессией рецепторов инсулина, определяли влияние инсулина на миграционную активность при использовании 12-имидазолил-1-додеканола и без него.
активность
12-имидазолил-1-додеканола (10 мкМ)
Инсулин вызывает 2,5-кратное увеличение миграционной активности. Активное вещество блокирует это увеличение полностью спустя время наблюдения 450 минут (первая половина времени наблюдения). Спустя 900 минут (вторая половина времени наблюдения) увеличение является отрицательным. Средняя миграционная активность тогда составляет на 13% ниже таковой контроля.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ФОРМУЛЫ А-R-X ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ ДЛЯ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ | 2007 |
|
RU2446801C2 |
| ДЕЙТЕРИРОВАННЫЕ 3-ПИПЕРИДИНОЭТИЛФЕНИЛКЕТОНЫ, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2002 |
|
RU2296755C2 |
| ЛЕЧЕНИЕ ИЛИ ПРОФИЛАКТИКА ПРОЛИФЕРАТИВНЫХ СОСТОЯНИЙ | 2010 |
|
RU2705548C2 |
| ТОПЛИВНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СЫРЬЕВЫЕ МАТЕРИАЛЫ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ | 2007 |
|
RU2441902C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ УВЕЛИЧЕНИЯ БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ АКТИВНОГО ВЕЩЕСТВА С ИСПОЛЬЗОВАНИЕМ ДАННОГО СОСТАВА | 1991 |
|
RU2104715C1 |
| ПРОИЗВОДНЫЕ ТИАЗОЛОХИНОЛИНА, ИХ РАЦЕМАТЫ ИЛИ ОТДЕЛЬНЫЕ ЭНАНТИОМЕРЫ И ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ ГИДРАТЫ И СОЛИ, А ТАКЖЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2138505C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2014 |
|
RU2690377C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МОДИФИЦИРОВАННЫЙ НОСИТЕЛЬ | 2003 |
|
RU2401127C2 |
| ГЕТЕРОЦИКЛИЛ-БЕНЗОИЛ-ГУАНИДИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2152390C1 |
| СПОСОБ ПОЛУЧЕНИЯ СВОБОДНЫХ КИСЛОТ ИЗ ИХ СОЛЕЙ | 2010 |
|
RU2533413C2 |
Изобретение относится к области органической химии, а именно к 12-имидазолил-1-додеканолу или к его фармацевтически приемлемой соли. Технический результат: получено новое производное имидазола, полезное при лечении в т.ч. и раковых патологических состояний. 4 ил.
12-имидазолил-1-додеканол или его фармацевтически приемлемая соль.
| РЕЗЕРВНАЯ СТУПЕНЬ ЗАЩИТЫ ОТ КОРОТКИХ ЗАМЫКАНИЙ | 1990 |
|
RU2016452C1 |
| Способ получения замещенного имидазола или его нетоксичной фармацевтически приемлемой кислотно-аддитивной соли | 1991 |
|
SU1836355A3 |
Авторы
Даты
2013-03-10—Публикация
2007-04-27—Подача