Изобретение относится к дейтерированным 3-пиперидиноэтилфенилкетонам и их физиологически переносимым солям, а также к лекарственным средствам, содержащим эти соединения.
Известными представителями 3-пиперидиноэтилфенилкетонов являются толперизон и эперизон (US-A 3995047, US-A 4638009). Эти соединения применяют в качестве спазмолитических и сосудорасширяющих средств.
Задачей предложенного изобретения является приготовление 3-пиперидиноэтилфенилкетонов, которые в отличие от уже известных соединений обладают лучшие фармакокинетическими и/или фармакодинамическими свойствами.
Неожиданным образом обнаружилось, что заявленные дейтерированные 3-пиперидиноэтилфенилкетоны обладают значительно лучшими фармакокинетическими и/или фармакодинамическими свойствами, чем недейтерированные соединения.
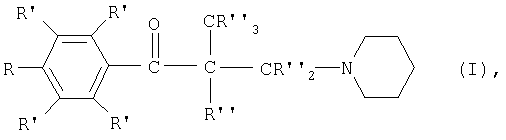
Согласно изобретению задача решается, таким образом, путем приготовления дейтерированных 3-пиперидиноэтилфенилкетонов общей формулы I

где R обозначает недейтерированный, однократно или многократно дейтерированный или пердейтерированный радикал алкила, содержащий до 3 атомов углерода,
все радикалы R' являются водородом или все вместе представляют дейтерий,
радикалы R'' независимо друг от друга являются дейтерием или водородом и причем по меньшей мере один из радикалов R, R' или R'' является дейтерием или содержит дейтерий,
а также их физиологически переносимых солей.
Предпочтительны следующие заявленные дейтерированные 3-пипериди-ноэтилфенилкетоны:
4'-дейтерометил-2-метил-3-пиперидиноэтилфенилкетон,
4'-метил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидиноэтилфенилкетон,
4'-этил-2',3',5',6-тетрадейтеро-2-метил-3-пиперидиноэтилфенилкетон,
4'-изопропил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидиноэтилфенилкетон,
4'-n-пропил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-тридейтерометил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-метил-2-дейтерометил-2-дейтерий-3-пиперидиноэтилфенилкетон,
4'-метил-2-дейтерометил-2-дейтерий-3,3-дидейтеро-3-пиперидино-этилфенилкетон и
4'-тридейтерометил-2',3',5',6'-тетрадейтеро-2-метил-3,3-дидейтеро-3-пиперидино-этилфенилкетон.
Для приготовления лекарственных средств для лечения заболеваний с симптомами в мышечных областях предпочтительным является применение заявленных дейтерированных 3-пиперидиноэтилфенилкетонов, а также их физиологически переносимых солей, при этом заболеваниями с симптомами в мышечной области являются болезненные рефлексно-мускульные напряжения скелетной мускулатуры и/или нервно-мускульных судорог.
Наиболее предпочтительны фармацевтические составы, содержащие заявленные дейтерированные 3-пиперидиноэтилфенилкетоны, а также их физиологически переносимые соли для лечения заболеваний с симптомами в мышечных областях наряду с фармацевтически переносимыми вспомогательными веществами и/или добавками.
Изготовление применяемых согласно изобретению дейтерированных толперизонов само по себе известно. Дейтерированные этилфенилкетоны, применяемые в качестве исходного соединения, получают, используя дейтерированные производные толуола путем ацилирования по Фриделю-Крафту с хлорангидридом пропионовой кислоты (Organikum, 15. Auflage, 1977, S.404-405). При этом использовали имеющиеся в продаже производные толуола тридейтерометилбензол, пердейтеротолуол и известный 2,3,4,5,6-пентадейтеротолуол (A.Borovik et al., Angew. Chem., Int. Ed., 2000, 39(22), 4117-4118).
Превращение в дейтерированные производные толперизона может происходить по аналогии с известным синтезом для 3Н-толперизона (Dietrich, A., Fels, G., J. Labelled Compd. Radiopharm. (1999), 42(12), 1125-1134, а также Dietrich, A., Dissertation 1999, Univ.-GH Paderborn).
A.Dietrich описывает в этих работах, кроме прочего, синтез производных толперизона, тритиированных и дейтерированных в 3'-позиции и в 3',5'-позиции. Эти вещества были использованы для исследования действия и фармакологии толперизона.
Производные толперизона, дейтерированные в 2-позиции и 2-метил-позиции, были получены исходя из известного 2,3-дидегидро-толперизона (Dietrich, A., Dissertation 1999, Univ.-GH Paderbom) в результате реакции обмена с дейтерием. Соединения, дейтерированные в 1-позиции, были получены известным путем с применением дейтерированного параформальдегида в реакции Манниха с соответствующими производными этилфенилкетона.
Обычными физиологически переносимыми неорганическими и органическими кислотами являются, например, соляная, бромистоводородная, фосфорная, серная, щавелевая, малеиновая, фумаровая, молочная, винная, яблочная, лимонная, салициловая, адипиновая и бензойная кислоты. Другие кислоты, которые можно использовать, описаны, например, в издании Fortschritte der Arzneimittelforschung, Bd. 10, S.224-225, Birkhäuser Verlag, Basel und Stuttgart, 1966 и в журнале Journal of Pharmaceutical Sciences, Bd. 66, S.1-5 (1977).
Аддитивный кислые соли получают, как правило, известным образом путем смешивания свободного основания или его растворов с соответствующей кислотой или ее растворами в органическом растворителе, например низшем спирте, таком как метанол, этанол, n-пропанол или изопропанол, или низшем кетоне, таком как ацетон, метилэтилкетон или метилизобутилкетон, или простом эфире, таком как простой диэтиловый эфир, тетрагидрофуран или диоксан. Для лучшего осаждения кристаллов можно использовать также смеси указанных растворителей. Кроме этого, можно получить физиологически переносимые водные растворы аддитивных кислых солей применяемых согласно изобретению соединений в водном кислом растворе.
Аддитивные кислые соли заявленных соединений можно переводить известным образом в свободное основание, например с помощью щелочей или ионообменников. Из свободного основания можно получить другие соли путем реакции обмена с неорганическими или органическими кислотами, в частности такими, которые подходят для образования солей, применяемых в терапии. Эти, а также и другие соли нового соединения, как, например, пикрат, могут служить также для очистки свободного основания, переведя свободное основание в соль, отделив ее и снова выделив из соли основание.
Предметом предложенного изобретения являются также лекарственные средства для орального, ректального, местного (кожного, трансдермального (чрескожного), локального), подкожного, внутривенного или внутримышечного применения, которые наряду с обычными основами и разбавителями содержат в качестве биологически активного вещества соединение общей формулы I или его аддитивную кислую соль.
Заявленные лекарственные препараты получают известным образом с общепринятыми твердыми и жидкими носителями или разбавителями и обычным образом используемыми в фармакологии техническими вспомогательными веществами в соответствии с желаемым видом применения и подходящей дозировкой. Предпочтительно их готовят в такой форме, которая подходит для орального применения. Такими формами являются, например, таблетки, пленочные таблетки, драже, капсулы, пилюли, порошки, растворы или суспензии или депо-формы.
Для местного применения подходят, например, мази, кремы, гели, растворы или пластыри.
Разумеется рассматриваются и парентеральные формы, такие как растворы для инъекций. Кроме того, следует назвать, например, еще свечи.
Соответствующие таблетки можно готовить, например, путем смешивания биологически активного вещества с известными вспомогательными веществами, например инертными разбавителями, такими как декстроза, сахар, сорбит, маннит, поливинилпирролидон, разрыхлителями, такими как кукурузный крахмал или альгиновая кислота, связующими веществами, такими как крахмалы или желатины, технологическими добавками для улучшения переработки, такими как стеарат магния или тальк и/или средствами для достижения эффекта продленного действия, такими как карбоксилполиметилен, карбоксилметилцеллюлоза, ацетофталат целлюлозы или поливинилацетат.
Таблетки могут быть многослойными. Соответственно драже можно получать, покрывая зерна, приготовленные по аналогии с таблетками, такими средствами, которые применяют обычно для оболочек драже, например поливинилпирролидоном или шеллаком, гуммиарабиком, тальком, двуокисью титана или сахаром. При этом можно использовать многослойные оболочки для драже, причем можно применять вспомогательные вещества, упомянутые выше в связи с получением таблеток.
Растворы или суспензии, содержащие биологически активное вещество, используемое в связи с изобретением, могут содержать дополнительно средства для улучшения вкуса, например сахарин, цикламат или сахар, а также, например, ароматические вещества, например ванилин или экстракт апельсина. Они могут содержать, кроме этого, суспендирующие вспомогательные вещества, такие как карбоксиметилцеллюлоза натрия или консерванты, такие как р-гидроксибензоаты. Капсулы, содержащие биологически активные вещества, можно получить, например, смешав это биологически активное вещество с инертным носителем, таким как лактоза или сорбит, и введя его в желатиновую капсулу.
Подходящие свечи можно получить, например, путем примешивания предназначенных для этого носителей, таких как нейтральные жиры или полиэтиленгликоль или их производные.
Получение заявленных лекарственных средств для местного применения специалисту известно. При получении заявленных лекарственных средств для трансдермального (чрескожного) применения используют известные сами по себе вспомогательные вещества и добавки.
Получение заявленных фармацевтических композиций само по себе известно и описано в справочниках, известных специалисту, например в Hager's Handbuch (5.) 2, 622-1045; List et al., Arzneiformenlehre, Stuttgart: Wiss. Verlagsges. 1985; Sucker et al., Pharmazeutische Technologie, Stuttgart: Thieme 1991; Ullmann's Enzyklopädie (5.) A 19, 241-271; Voigt, Pharmazeutische Technologie, Berlin: Ullstein Mosby 1995.
Изготовленные таким образом лекарственные препараты можно применять для лечения заболеваний с симптомами в мышечной области.
Заявленные соединения имеют ряд преимуществ перед известными из уровня техники соединениями, не содержащими дейтерий. Благодаря дейтерированию изменяется, во-первых, обмен веществ в организме. В частности, затрудняется гидроксилирование в радикале фенила, что приводит к уменьшению первичного болевого эффекта. Благодаря этому можно изменять дозировку и получать препараты продленного действия, которые также в депо-форме могут улучшить пластичность мышцы.
Наряду с этим изменяется также фармакодинамика, так как дейтерированные соединения образуют абсолютно другую гидратную оболочку, так что распределение в организме явно отличается от случая с недейтерированными соединениями.
Обмен толперизона и производных от него веществ происходит преимущественно в печени, причем наблюдается сильный первичный эффект. Только пятая часть введенной дозы попадает в неизменном виде в кровь.
Крайне важными для обмена в печени медикаментами или ксенобиотиками являются ферменты цитохрома-Р450 (CYP). Первичные метаболиты при распаде в печени возникают в результате гидроксилирования алкилового заместителя, находящегося на ароматическом кольце, и в результате гидроксилирования самого аромата (Miyazaki, Ishibashi, Takayama; 4th Symposium on Drug Metabolism and Action, 1972, Sendai; Japan: 154-164).
Для получения более подробных сведений об обмене в печени толперизона и заявленных дейтерированных аналогов в лабораторных условиях были проведены фармакокинетические опыты с известным среднему специалисту семейством цитохром-Р450, встречающимся чаще всего в печени (CYP1A1, CYP1A2, CYP2C8, CYP2C19, CYP2D6, CYP2E1, CYP3A4).
Результаты этих исследований представлены на фиг.1-3.
Фиг.1 - расщепление ферментов толперизона с помощью оксидазы цитохрома.
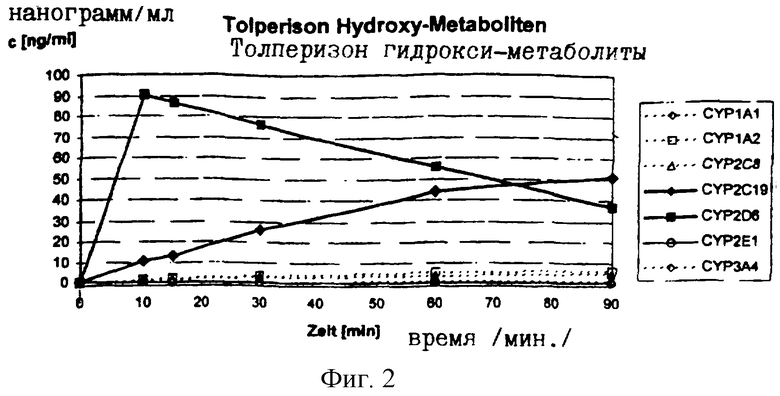
Фиг.2 образование метаболитов гидроксила из толперизона при помощи CYP2D6 и CYP2C19 в сравнении с менее активными цитохромами и
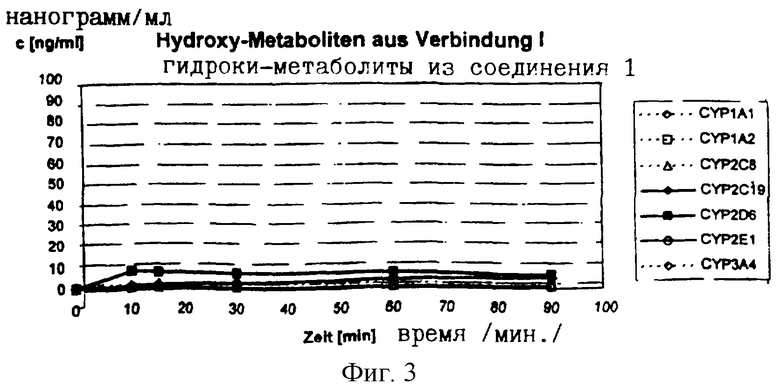
Фиг.3 образование метаболитов гидроксила из соединения I при помощи ферментов цитохром-Р450.
На фиг.1 представлено различное снижение концентрации толперизона в результате расщепления ферментов посредством оксидазы цитохрома по времени.
Таким образом толперизон преобразуется прежде всего благодаря CYP2D6 и CYP2C19. Другие исследованные цитохромы лишь в незначительной степени способствуют биологическому распаду толперизона.
Первичные метаболиты, возникающие в результате гидроксилирования, образуются благодаря CYP2D6 и CYP2C19 в той же степени, как распадается субстрат (см. фиг.2).
Неожиданным образом оказалось, что обмен в печени заявленных дейтерированных соединений при помощи цитохром-Р450-оксидазы четко отличается от обмена соответствующих недейтерированных веществ.
Так, например, ферментное гидроксилирование 1-[4-(тридейтерометил)тетрадейтерофенил]-2-метил-3-пиперидин-1-ил-1-пропанона (I; формула I, где R=CD3, R'=D, R''=Н) благодаря CYP2D6 и CYP2C19 по сравнению с толперизоном эффективно замедляется на 10 порядков (см. фиг.3).
Из этого получается улучшение эффективности, так как нужно исходить из продления срока действия. Польза при терапевтическом лечении заключается в снижении дозировки при применении лекарственных средств, полученных из заявленных дейтерированных этилфенилкетонов, по сравнению с применяемыми до сих пор недейтерированными аналогичными соединениями.
Таким образом можно развивать абсолютно новые препараты.
Изобретение поясняется на основании следующих примеров:
Пример 1
Получение 4'-тридейтерометилэтилфенилкетона
В трехгорлой колбе с мешалкой, капельной воронкой и обратным холодильником с сушильной трубкой с хлористым кальцием к 40 мл дихлорэтана прибавили 16 г безводного мельчайшего порошка хлористого алюминия. При охлаждении льдом добавили по каплям 13,88 г хлорангидрида пропионовой кислоты. 9,5 г тридейтерометилбензола (толуол-d3) добавили по каплям с такой скоростью, чтобы температура реакционного раствора удерживалась постоянно 20°С. По окончании добавления смесь перемешивали в течение 2-х часов, после чего оставили на ночь. Полученный кетонный комплекс с хлористым алюминием распался, когда реакционную исходную смесь осторожно вылили на 50 мл льда. Органическую фазу отделили, а водную фазу трижды экстрагировали с дихлорэтаном. Объединенные органические экстракты промыли водой, 2%-ным раствором натронного щелока, а затем снова водой, после чего сушили с помощью карбоната калия.
Растворитель удалили, а остаток перегнали в вакууме.
Выход: 10,2 г (68%) 4'-тридейтерометилэтилфенилкетона в виде бесцветной жидкости.
С10Н9D3О: 151,223
Рассчитано С 79,43, Н 9,99; найдено С 79,41, Н 10,01.
1H-NMR: при сравнении со спектром 1H-NMR недейтерированного 4'-метилэтилфенилкетона можно было определить в спектре 1H-NMR продукта, при прочих совпадениях, отсутствие резонансного сигнала ароматической группы СН3.
Пример 2
Получение 4'-тридейтерометил-2'3',5',6'-тетрадейтероэтилфенилкетона
По аналогии с примером 1 к 40 мл дихлорэтана прибавили 16 г безводного мельчайшего порошка хлористого алюминия и при охлаждении льдом прибавили 13,88 г хлорангидрида пропионовой кислоты, добавили для реакции 10,02 г тридейтерометил-2',3',4',5',6-тетрадейтеробензола (толуол-d8).
Отличием здесь явилось то, что кетонный комплекс с хлористым алюминием разрушился благодаря вливанию в охлажденный льдом D2O. Дальнейшая обработка происходила так же, как и в примере 1.
Выход: 10,24 г (66%) 4'-тридейтерометил-2',3',5',6'-тетрадейтеро-этилфенилкетона в виде бесцветной жидкости.
C10H5D7O:
Рассчитано С 77,37, Н 12,33; найдено С 77,40, Н 12,31.
1H-NMR: при сравнении со спектром 1H-NMR недейтерированного 4'-метилэтилфенилкетона можно было определить в спектре 1Н-NHR продукта, при прочих совпадениях, отсутствие резонансного сигнала ароматической группы СН3, а также ароматных протонов.
Пример 3
Получение 4'-метил-2',3',5',6'-тетрадейтероэтилфенилкетона
По аналогии с примером 2 к 40 мл дихлорэтана прибавили 16 г безводного мелкого порошка хлористого алюминия и при охлаждении льдом прибавили 13,88 г хлорангидрида пропионовой кислоты, добавили для реакции 9,72 г 2',3',4',5', 6-пентадейтеротолуола (толуол-d5). Обрабатывали так же, как в примере 1.
Выход: 9,59 г (63%) 4'-метил-2',3',5',6'-тетрадейтероэтилфенил-кетона в виде бесцветной жидкости.
С10H8D4О:
Рассчитано С 78,9, Н 10,59; найдено С 79,3, Н 10,53.
1H-NMR: при сравнении со спектром 1H-NMR недейтерированного 4'-метилэтилфенилкетона можно было определить в спектре 1H-NMR продукта, при прочих совпадениях отсутствие резонансного сигнала ароматных протонов.
Пример 4
Получение 4'-тридейтерометил-2-метил-3-пиперидиноэтилфенилкетона
1,15 г 4'-тридейтерометилэтилфенилкетона растворили в 5 мл метанола, после чего добавили, помешивая, 0,3 г параформальдегида и 1,1 г гидрохлорида пиперидина. Реакционную смесь кипятили с обратным холодильником, пока не достигли конечной точки реакции (твердения реакционной смеси). После этого добавили 10 мл хлороформа, органические фазы сушили с сульфатом натрия, фильтровали, а растворитель удаляли в вакууме. Полученное твердое вещество мелко дробили и промывали ацетоном.
Полученные 1,5 г кристаллического сырого продукта переводили в гидрохлорид, который был перекристаллизован из метанола.
Выход: 1,45 г (73%) в форме иголок.
Точка плавления: 167-169°С.
1H-NMR (200 МГц, CDCl3): δ=1,18 (d, 3Н, СН3), 1,25-1,68 (m, 6H, 3×СН2), 2,18-2,45 (m, 4Н, 2×СН2), 2,35 и 2,65 (d и АВ-спектр, J=7,1 Гц, JA,B=12,4 Гц, 2Н, СН2), 3,69 (m, 1H, СН), 7,78 (s, 4H, Ar-H).
13C-NMR (50 МГц, CDCl3): δ=18,00 (Ar-CD3), 20,01 (СН3), 22,15 (СН2), 23,15 (CH2), 34,25 (СН), 52,67 (2 CH2), 58,53 (CH2), 126,73 (Саром), 129,42 (Саром), 131,34 (Cаром), 155,02 (Саром), 204,02 (С:О).
C16H20NOD3·HCl: (284,85)
Рассчитано С 67,47, Н 9,55, N 4,92;
Найдено С 67,45, Н 9,56, N 4,91.
Пример 5
Получение 4'-метил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидиноэтилфенилкетона
По аналогии с примером 4 растворили в 5 мл метанола 1,16 г 4'-метил-2',3',5',6'-тетрадейтероэтилфенилкетона, после чего добавили для реакции 0,3 г параформальдегида и 1,1 г гидрохлорида пиперидина. Продукт изолировали в виде гидрохлорида.
Выход: 1,42 г (71%) в форме иголок.
Точка плавления: 174-176°С.
1H-NMR (200 МГц, CDCl3): δ=1,18 (d, 3Н, СН3), 1,25-1,68 (m, 6H, 3 СН2), 2,18-2,45 (m, 4H, 2 CH2), 2,35 и 2,65 (d и AB-спектр, J=7,1 Гц, JA,B=12,4 Гц, 2Н, СН2), 2,41 (s, 3Н, Ar-СН3), 3,69 (m, 1H, СН).
C16H19NOD4·HCl: (285,85)
Рассчитано С 67,23, Н 9,87, N 4,9;
Найдено С 67,21, Н 9,89, N 4,8.
Пример 6
Получение 4'-тридейтерометил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетона
По аналогии с примером 4 в 5 мл метанола растворили 1,09 г 4'-тридейтерометил-2',3',5',6'-тетрадейтероэтилфенилкетона, после чего добавили для реакции 0,3 г параформальдегида и 1,1 г гидрохлорида пиперидина. Продукт изолировали в виде гидрохлорида.
Выход: 1,46 г (72%) в форме иголок.
Точка плавления: 177-178°С.
C16H16NOD7·HC1: (288,87)
Рассчитано С 66,53, Н 10,81, N 4,85;
Найдено С 66,55, Н 10,84, N 4,87.
1H-NMR (200 МГц, CDCl3): δ=1,18 (d, 3Н, СН3), 1,25-1,68 (m, 6H, 3 CH2), 2,18-2,45 (m, 4H, 2 СН2), 2,35 и 2,65 (d и АВ-спектр, J=7,1 ГЦ, JA,B=12,4 Гц, 2Н, СН2), 3,69 (m, 1H, СН).
IR: Vmax (нуйол) 2721, 2639, 2532, 2408, 1674 (С:O), 1580 (Ar), 1544, 1460, 1411, 1378, 1331, 1298, 1244, 1211, 1159, 1121, 1083, 1081, 1021, 721, 638 см-1.
Пример 7
Получение 4'-метил-2-дейтерометил-2-дейтерий-3-пиперидиноэтилфенилкетона
К раствору 10 г (41 ммоль) 2,3-дидегидро-толперизона в 150 мл этилового эфира уксусной кислоты добавили 100 мг Pd/C (10%) и реакционный сосуд продували газом дейтерия, который затем подключали к аппаратуре. Дейтеризация происходила при давлении 2 атм при комнатной температуре в течение ночи. Реакционную смесь фильтровали через броунмиллерит, а фильтрат сгущали в вакууме. После этого остаток растворяли с 1N NaOH и экстрагировали с простым диэтиловым эфиром, органическую фазу отделяли, сушили с сульфатом натрия, фильтровали и сгущали в вакууме. Полученный амин растворяли в простом диэтиловом эфире и добавляли хлористый ацетил и метанол для получения гидрохлорида.
Выход: 8,6 г (85%) дейтерированного толперизона.
Точка плавления: 178°С.
1H-NMR (200 МГц, CDCl3): δ=1,15 (d, 2Н, CDH2), 1,30-1,72 (m, 6H, 3 CH2), 2,20-2,48 (m, 4H, 2 CH2), 2,48 (s, 3Н, СН3), 2,49 и 2,85 (d и AB-спектр, J=7,2 Гц, JA,B=12,6 Гц, 2Н, CH2), 7,95 (s, 2H, Ar-H).
13C-NMR (50 МГц, CDCl3): δ=19,21 (Ar-СН3), 18,78 (CDH2), 22,20 (СН2), 22,95 (CH2), 35,32 (CD), 52,53 (2 CH2), 58,60 (CH2), 129,33 (Cаром), 130,32 (Саром), 132,15 (Саром), 145,55 (s, Саром), 201,02 (С:О).
C16H21NOD2·HCl: (283,48)
Рассчитано С 67,71, Н 9,23, N 4,93;
Найдено С 67,73, Н 9,21, N 4,95.
Пример 8.
Биологический распад тестируемых веществ при помощи цитохром-Р450-ферментов проводился invitro. Толперизон и детерированный аналог инкубировались с различными Р450 цитохромоксидазами (CYP1A1, CYP1A2, СYP2C8, CYP2C19, CYP2D6, CYP2T1, CYP3F4). Инкубация осуществлялась при температуре 37°С в 200 мл инкубационного раствора, состоящего из 0,1 М фосфорнокислого калия или 0.5 М трис HCl буфер (рН 7,4), 3 мМ NADPH с концентрацией протеина 0,5 мг/мл. Уменьшение концентрации толперизона или дейтерированного аналога измерялось в течение времени при помощи LC/MS/MS (Фиг.1). При помощи LC/MS/MS измерялось, кроме того, образование гидроксиметаболитов (Фиг.2 и 3).
Пример 9.
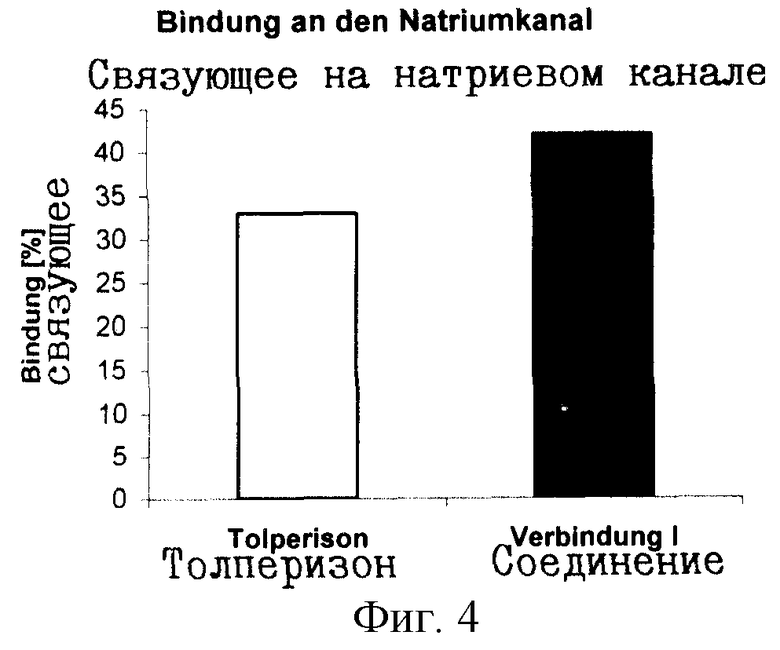
Фармакологическое воздействие тестируемых веществ на натриевый канал тестировалось в vitro при помощи связующею теста на натриевом канале из крысиного мозга (фиг.4). Инкубация осуществлялась при температуре 37°С через 60 минут в инкубационном растворе, состоящем из 50 мМ трис - HCl, рН 7.4 при температуре 25°С, 50 мМ HEPES, 130 мМ Cholin-Cl, 0.8 мМ MgSO4·H2О, 5.5 мМ глюкоза, 40 мг/мл LqTx. Образование толперизона или же дейтерированного аналога определялось количественно при помощи радиосвязующего. В качестве связующею применялось 5 nM [3H] - бетрахотоксинина-А20-альфа-бензоата. Дейтерированное соединение 1 имело более сильное связующее в натриевом канале, чем толперизон.
Пример 10.
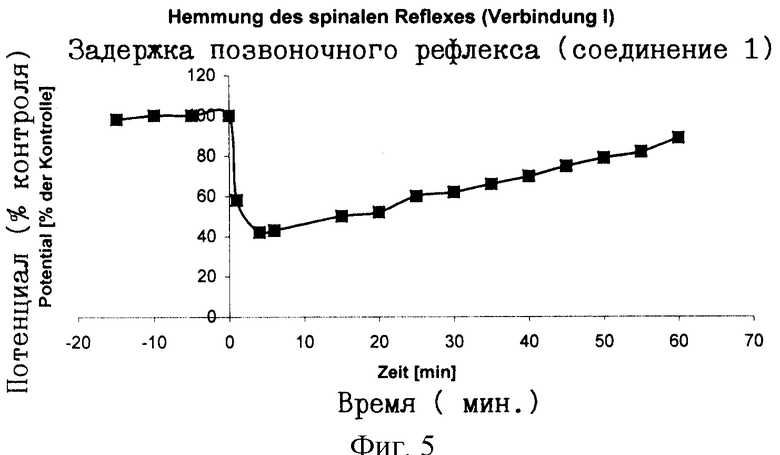
Фармакологическое воздействие тестируемых веществ на позвоночный рефлекс исследовалось па крысах. В результате электрического возбуждения на позвонок L5 вызывался моносинаптический рефлекс, который определялся электромиографически. Внутривенозное введение дейтерированного соединения 1 в момент времени 0 (Фиг.5) блокировало этот рефлекс в одинаковой степени, как и толперизон.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ ДЕЙТЕРИРОВАННОГО ДЕФАКТИНИБА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2761825C1 |
| ДЕЙТРИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ ВИЗУАЛИЗАЦИИ | 2015 |
|
RU2696492C2 |
| ПРОИЗВОДНОЕ СУЛЬФОНИЛБЕНЗАМИДА И ЕГО КОНЬЮГАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2839468C1 |
| ДЕЙТРИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ ВИЗУАЛИЗАЦИИ | 2015 |
|
RU2791900C1 |
| ИНГИБИТОР FAK И КОМБИНАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ С НИМ | 2019 |
|
RU2820555C2 |
| ДЕЙТЕРИРОВАННЫЕ ИНГИБИТОРЫ ПРОТЕАЗЫ ГЕПАТИТА С | 2007 |
|
RU2465264C2 |
| ДЕЙТЕРИРОВАННЫЕ ДИАМИНОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ТАКИЕ СОЕДИНЕНИЯ | 2014 |
|
RU2632907C2 |
| ПРОИЗВОДНОЕ ПАРОКСЕТИНА | 2013 |
|
RU2616610C2 |
| ГАЛОГЕНЗАМЕЩЕННОЕ ФЕНИЛАТНОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЯ | 2020 |
|
RU2820475C2 |
| ИНГИБИТОР, СОДЕРЖАЩИЙ БИЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2820948C2 |
Изобретение относится к 3-пиперидиноэтилфенилкетонам общей формулы (I)
в которой R обозначает недейтерированный, однократно или многократно дейтерированный или пердейтерированный алкил, содержащий до 3 атомов углерода; все радикалы R' являются водородом или все представляют дейтерий; радикалы R" независимо друг от друга являются дейтерием или водородом, причем по меньшей мере один из радикалов R, R' или R'' является дейтерием или содержит дейтерий, а также к их физиологически переносимым солям. Соединения формулы (I) и их соли могут быть использованы для лечения заболеваний с симптомами в мышечной области, таких как болезненные рефлексно-мускульные напряжения скелетной мускулатуры и/или нервно-мускульных судорог. 4 н. и 1 з.п. ф-лы, 5 ил.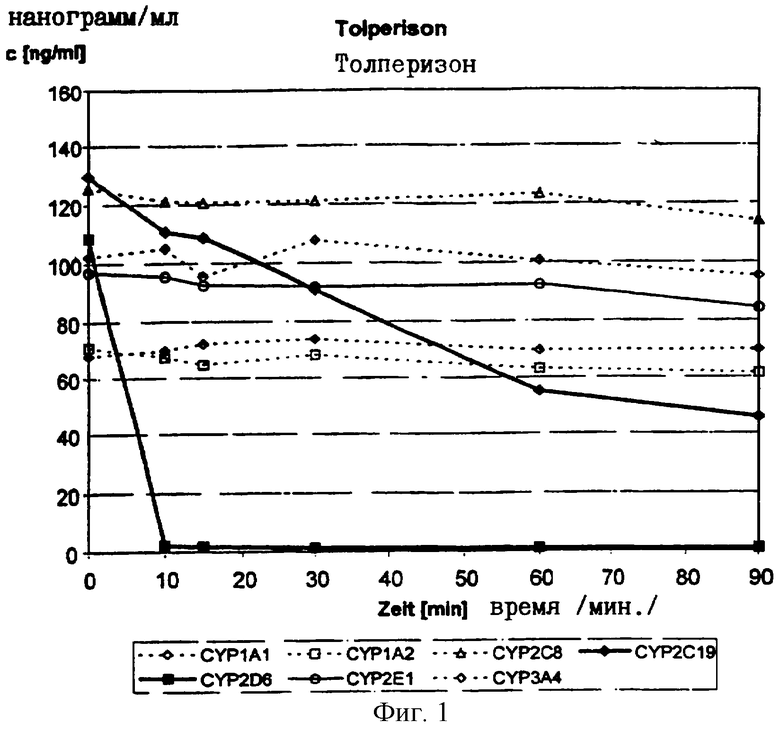
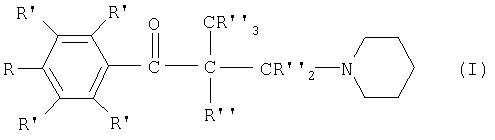
в которой R обозначает недейтерированный, однократно или многократно дейтерированный или пердейтерированный радикал алкила, содержащий до 3 атомов углерода,
все радикалы R' являются водородом или все представляют дейтерий, радикалы R'' независимо друг от друга являются дейтерием или водородом и причем по меньшей мере один из радикалов R, R' или R'' является дейтерием или содержит дейтерий,
а также их физиологически переносимые соли.
4'-тридейтерометил-2-метил-3-пиперидино-этилфенилкетон,
4'-метил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-этил-2',3',5',6-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-изо-пропил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-n-пропил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-тридейтерометил-2',3',5',6'-тетрадейтеро-2-метил-3-пиперидино-этилфенилкетон,
4'-метил-2-дейтерометил-2-дейтерий-3-пиперидино-этилфенилкетон,
4'-метил-2-дейтерометил-2-дейтерий-3,3-дидейтеро-3-пиперидино-этил-фенилкетон и
4'-тридейтерометил-2',3',5',6'-тетрадейтеро-2-метил-3,3-дидейтеро-3-пиперидино-этилфенилкетон.
| СПОСОБ ПОЛУЧЕНИЯ АРИЛОКСИОКСИПРОПИЛЕН-ПИПЕРАЗИНИЛАЦЕТАНИЛИДОВ, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СЛОЖНЫХ ЭФИРОВ, ИЛИ КИСЛОТНОАДДИТИВНЫХ СОЛЕЙ | 1984 |
|
RU2071471C1 |
| US 4638009 А, 20.01.1987 | |||
| US 3995047 А, 30.11.1976. | |||
Авторы
Даты
2007-04-10—Публикация
2002-04-29—Подача