Изобретение относится к аналитической химии, а также может быть использовано в медицине для определения содержания селена в крови и контроля состояний селеновой недостаточности человека и животных.
Известен способ определения селена в крови, основанный на определении интенсивности флуоресценции его соединений (Лебедев П.А., Лебедев А.А. Модификация спектрофлуориметрического метода определения селена в крови. // Химико-фарм. журн. - 1996. - Т.30, №10, с.54-55). Способ заключается в следующем. Пробы сыворотки крови (0.5 мл) обрабатывают в пробирках смесью концентрированных азотной и соляной кислот (3 мл). Пробирки нагревают постепенно от 100°С до 180-190°С в течение 2.5 ч, пока в каждой пробирке не останется примерно 1 мл жидкости. После охлаждения добавляют в каждую пробирку 5 N HCl (0.4 мл) и вновь нагревают при 130-150°С в течение 15 мин для превращения Se (VI) в Se (IV). После охлаждения добавляют маскирующий реактив (2 мл). Он представляет собой смесь из:
1) ЭДТА (комплексон III) 7.6 г, вода 80 мл, 5 N раствор аммиака в количестве, необходимом для растворения осадка;
2) гидроксиламин солянокислый 24 г, вода 500 мл;
3) метиловый оранжевый, 0.05% водный раствор, 40 мл.
Затем добавляют 7.5N раствор аммиака (по каплям) до появления желтого окрашивания и 1N HCl (по каплям) до появления розовой окраски. Затем объем содержимого пробирок доводят до 9 мл дистиллированной водой. Селено-диазоловый комплекс получают добавлением к пробе 1 мл раствора 2,3 - диаминонафталина (ДАН) в 0.1N HCl и последующим выдерживанием на водяной бане при 50°С в течение 30 минут. После охлаждения и добавления 5 мл гептана содержимое перемешивают в миксере 30 мин для экстракции комплекса.
После отстаивания пробы в течение 30 мин отделяют органический слой и измеряют его флуоресценцию на длине волны 525 нм (λвозб=366 нм). Полученные результаты сравнивают с величиной флуоресценции селенодиазоловых комплексов, полученных на основе стандартных растворов, содержащих 50, 100, 150, 200 мкг селена на 1 л воды.
Как отмечают авторы этой работы, стандартные растворы селенистой кислоты, проходящие ту же обработку, что и пробы плазмы и сыворотки крови, не дают воспроизводимых результатов, в отличие от проб крови. Поэтому в качестве вторичного стандарта применяют нормальную лошадиную сыворотку.
Приведенный способ имеет существенные недостатки. В технологии используется маскирующий реактив, а также смесь концентрированных азотной и соляной кислот. Их многократное нагревание и охлаждение для получения четырехвалентного селена значительно усложняют технологический процесс. Сравнение величин флуоресценции селенодиазоловых комплексов с таковой для стандартных растворов может внести существенный вклад в погрешность определяемых величин. Это связано с тем, что интенсивность флуоресценции зависит от многих факторов: параметров возбуждающего излучения и регистрирующей оптической системы, температуры, влажности, давления, освещенности помещения и др. [Паркер С. Фотолюминесценция растворов. М.: Мир, 1972. 504 с.]. Поэтому даже калибровка измерительной аппаратуры не позволяет быть уверенным в точности измерений.
Задачей изобретения является повышение точности определения концентрации селена в крови с помощью специального метода обработки спектральных данных.
Технический результат достигается за счет того, что в способе определения концентрации селена в крови, включающем получение сыворотки крови, превращение Se (VI) в Se (IV), получение селенодиазолового комплекса, его экстракцию и измерение флуоресценции при длине волны возбуждения λвозб=366 нм, построение градуировочного графика, выполненного на основе измерений стандартных растворов, отсутствуют маскирующий реактив и концентрированные азотная и соляная кислоты, для определения концентрации селена измеряются спектры флуоресценции смеси (λрег=480÷600 нм), а обработку спектральных данных производят используя метод Гауссово-Лоренцевых кривых с последующим построением градуировочного графика.
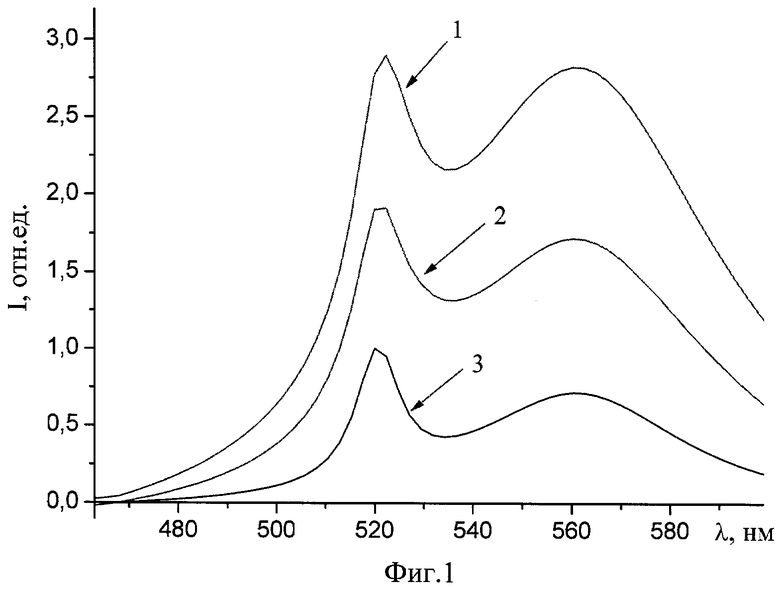
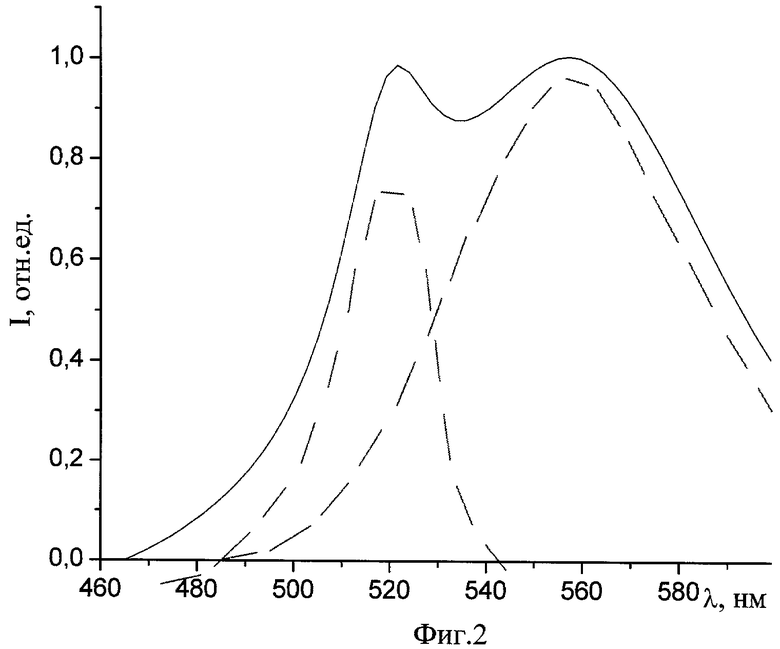
На фиг.1 изображены спектры флуоресценции стандартных растворов при различных концентрациях селена (1-1.05 мМ; 2-2.1 мМ; 3-4.2 мМ). На фиг.2 продемонстрировано разложение спектров флуоресценции смеси на составляющие методом Гауссово-Лоренцевых кривых. На фиг.3 изображен градуировочный график, имеющий линейную функцию в выбранном диапазоне концентраций, учитывающий выход реакции образования СДК, погрешность температуры и концентраций, статистическую обработку спектральных данных мешающих элементов и других факторов.
Способ осуществляют следующим образом.
Кровь предварительно центрифугируют при 8000 об/мин в течение 10 минут для отделения клеточных элементов. К 1 мл полученной сыворотки добавляют 2.5 мл 0.1 N раствора HCl. В течение 30 минут смесь постепенно нагревают до 60°С для перевода селена (VI) в селен (IV), пока объем не достигнет 1 мл. Затем, в предварительно остуженную смесь, добавляют 2.5 мл ДАН, 1 мл ЭДТА и 50 мл 0.1 N HCl. Полученную смесь нагревают при температуре 80°С в течение 20 минут. Затем смесь остужают до температуры 37°С и экстрагируют 10 мл раствора циклогексана. Затем на спектрофлуориметре проводят измерения спектров флуоресценции смеси (λрег=480÷600 нм). Длина волны возбуждения составляет 366 нм, так как находится в максимуме поглощения селендиазолового комплекса (СДК).
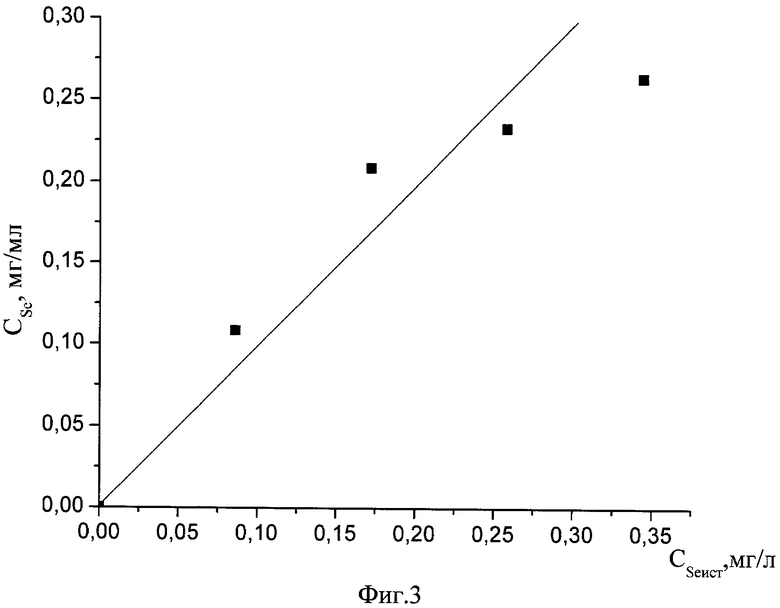
Для построения градуировочного графика приготавливают серию стандартных растворов, для чего берут аликвоту раствора селенистой кислоты H2SeO3 с концентрацией 7.75·10-3 М, добавляют к ней 2.5 мл ДАН, 1 мл ЭДТА и 50 мл 0.1 М HCl. Аликвота раствора селенистой кислоты составляет от 5 до 30 мкл. Смесь нагревают при температуре 80°С в течение 20 минут, затем остужают до температуры 37°С и экстрагируют 10 мл раствора циклогексана. Затем измеряют спектры флуоресценции смеси в фазе циклогексана от 480 до 600 нм (фиг.1).
Обработка результатов спектральных данных. Спектры флуоресценции смеси раскладывают на составляющие методом Гауссово-Лоренцевых кривых (фиг.2), что достаточно просто с помощью современного программного обеспечения. Затем подсчитывают площадь под кривой каждого из составляющих спектра. Количество селена определяют исходя из соотношения
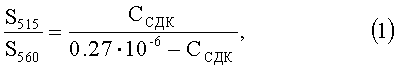
где S515, S560 - площадь под кривой спектров флуоресценции при максимумах 515 и 560 нм, характеризующих флуоресценцию СДК и ДАН соответственно;
0.27·10-6 - концентрация ДАН перед нагреванием при 80°С, М;
ССДК - концентрация СДК, М.
Из (1) получают выражение для концентрации селена
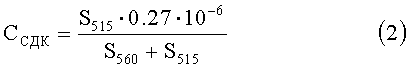
Истинную концентрацию селена в стандартных растворах определяют из закона разбавления растворов
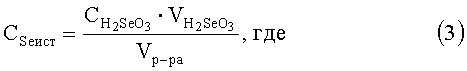
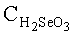 - концентрация селенистой кислоты, равная 7.75·10-3 М;
- концентрация селенистой кислоты, равная 7.75·10-3 М;
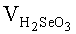 - аликвота селенистой кислоты, л;
- аликвота селенистой кислоты, л;
Vр-ра - объем полученного раствора, л.
После обработки спектров стандартных растворов строят градуировочный график ССДК=f(CSeист), по которому находят концентрацию селена в пробе.
Спектры имеют два четко выраженных максимума (515 и 560 нм), первый из которых (515 нм) характеризуется флуоресценцией СДК, образованный в результате реакции [Паркер С. Фотолюминесценция растворов. М.: Мир, 1972. 520 с.]. Второй (560 нм) - флуоресценцией не израсходованного ДАН. С увеличением концентрации селена наблюдается характерное увеличение интенсивности флуоресценции СДК в выбираемом диапазоне концентраций.
Разложение спектров методом Гауссово-Лоренцевых кривых позволяет разделять флуоресценцию каждого из компонентов смеси, что дает возможность наблюдать существенное различие отношения интенсивностей максимумов каждого из компонентов смеси в спектре флуоресценции от такового после разложения спектров на составляющие (фиг.2). В связи с этим целесообразно использовать разложение спектра на составляющие методом Гауссово-Лоренцевых кривых для более точной обработки экспериментальных данных.
После этого строят градуировочный график ССДК=f(CSeист). Чем больше различий между ССДК и CSeист, тем больше влияние описанных выше факторов. Концентрацию селена в крови находят по градуировочному графику (фиг.3).
| название | год | авторы | номер документа |
|---|---|---|---|
| Модифицированный фотосенсибилизатор на основе наночастиц селена и гидрофильного полимера | 2024 |
|
RU2835425C1 |
| СПОСОБ ФЛУОРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ФЛУНИКСИНА | 2014 |
|
RU2582960C1 |
| Способ люминесцентного определения селена (IV) | 2022 |
|
RU2799799C1 |
| АНТИОКСИДАНТНОЕ СРЕДСТВО С ГЕПАТОПРОТЕКТОРНЫМ ЭФФЕКТОМ НА ОСНОВЕ НАНОСТРУКТУРИРОВАННОГО СЕЛЕНА И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2013 |
|
RU2557992C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ВНУТРИКЛЕТОЧНОЙ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ НИЗКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ, НА ОСНОВЕ НАНОЧАСТИЦ | 2014 |
|
RU2557987C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ В БИОСРЕДАХ | 2010 |
|
RU2445624C2 |
| СОРБЦИННО-ФЛУОРЕСЦЕНТНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ДОКСИЦИКЛИНА В ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ | 2011 |
|
RU2471184C2 |
| Средство, обладающее противоопухолевой активностью на основе нанокомпозитов арабиногалактана с селеном, и способы получения таких нанобиокомпозитов | 2015 |
|
RU2614363C2 |
| 5-[4'-(1'',3''-БЕНЗОКСАЗОЛ-2''-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(4'-СУЛЬФОФЕНИЛ)ПОРФИН В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНОГО СЕНСОРА ДЛЯ ОБНАРУЖЕНИЯ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ АЛЬБУМИНА | 2022 |
|
RU2807912C1 |
| КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ N-ФЕНИЛМАЛЕИНИМИДА | 1997 |
|
RU2149384C1 |
Настоящее изобретение относится к медицине и описывает способ определения концентрации селена в крови, включающий получение сыворотки крови, превращение Se(VI) в Se(IV), получение селено-диазолового комплекса, его экстракцию и измерение флуоресценции при длине волны возбуждения λвозб=366 нм, построение градуировочного графика, выполненного на основе измерений стандартных растворов, где к полученной 1 мл сыворотке крови добавляют 2.5 мл 0.1 N раствора НСl, в течение 30 минут смесь постепенно нагревают до 60°С пока объем не достигнет 1 мл, затем в предварительно остуженную смесь добавляют 2.5 мл 2,3-диаминонафталина (ДАН), 1 мл ЭДТА и 50 мл 0.1 N НСl, полученную смесь нагревают при температуре 80°С в течение 20 минут, затем смесь остужают до температуры 37°С и экстрагируют 10 мл раствора циклогексана, затем проводят измерения спектров флуоресценции смеси (λрег=480÷600 нм) и производят обработку спектральных кривых используя метод Гауссово-Лоренцевых кривых. Способ обеспечивает повышение точности определения селена в крови. 1 пр., 3 ил.
Способ определения концентрации селена в крови, включающий получение сыворотки крови, превращение Se(VI) в Se(IV), получение селено-диазолового комплекса, его экстракцию и измерение флуоресценции при длине волны возбуждения λвозб=366 нм, построение градуировочного графика, выполненного на основе измерений стандартных растворов, отличающийся тем, что к полученной 1 мл сыворотке крови добавляют 2,5 мл 0,1 N раствора НС1, в течение 30 мин смесь постепенно нагревают до 60°С, пока объем не достигнет 1 мл, затем в предварительно остуженную смесь добавляют 2,5 мл 2,3-диаминонафталина (ДАН), 1 мл ЭДТА и 50 мл 0,1 N НСl, полученную смесь нагревают при температуре 80°С в течение 20 мин, затем смесь остужают до температуры 37°С и экстрагируют 10 мл раствора циклогексана, затем проводят измерения спектров флуоресценции смеси (λрег=480÷600 нм) и производят обработку спектральных кривых, используя метод Гауссово-Лоренцевых кривых.
| Голубкина Н.А | |||
| Флуориметрический метод определения селена | |||
| Журнал аналитической химии, т.50, №5, 1995, с.492-497 | |||
| Лебедев П.А., Лебедев А.А | |||
| Модификация спектрофлуориметрического метода определения селена в крови | |||
| Химико-фарм | |||
| журн | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| Лабиринтное уплотнение | 1927 |
|
SU12675A1 |
| Анемограф | 1927 |
|
SU8202A1 |
| КОНДРАХИН И.П | |||
| и др | |||
| Методы | |||
Авторы
Даты
2013-05-20—Публикация
2011-05-20—Подача