ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящая заявка испрашивает преимущество в соответствии с §120 35 U.S.C. на основании предварительной заявки на патент США №11/923727, поданной 25 октября 2007 года, которая полностью включена в описание настоящей заявки посредством ссылки.
Настоящее изобретение относится к сложным эфирам камптотецина и применению сложных эфиров камптотецина для лечения рака, злокачественных опухолей и подобного.
УРОВЕНЬ ТЕХНИКИ
Токсичность (или побочные эффекты), от которых страдают пациенты в результате приема противораковых лекарственных средств, принимаемых в течение процесса химиотерапии, остается самой большой проблемой, связанной с лечением рака. Терапевтический индекс (ТИ) противоракового агента определяют как отношение наиболее допустимой дозы к эффективной дозе. Известно, что большинство противораковых агентов, клинически применяемых в настоящее время, имеет очень узкий диапазон ТИ (от 1 до 1,2). Другими словами, токсические эффекты большинства противораковых агентов у пациентов, получающих химиотерапию, неизбежны при уровнях эффективной дозы вследствие узкого терапевтического индекса, связанного с противораковыми агентами. Различия в токсичности между агентами заключаются в степенях серьезности и типах нарушений. Фторурацил (5-ФУ) представляет собой один из чаще всего используемых химиотерапевтических агентов для системного и паллиативного лечения пациентов с раковыми образованиями, происходящими в желудочно-кишечном тракте, молочной железе, голове и шее. Дигидропиримидиндегидрогеназа (ДПД) представляет собой первоначальный и ограничивающий скорость фермент в катаболизме 5-ФУ. Недостаток ДПД все более признают как важное фармакогенетическое нарушение в этиологии серьезной токсичности, связанной с 5-ФУ. Сообщали, что больные раком, которые были генетически гетерозиготными или гомозиготными для мутирующей аллели гена, кодирующего ДПД, пострадали от серьезной токсичности, включая смерть, после введения 5-ФУ. Van Kuilenburg ABP, Haasjes J, Richel DJ et al. Clinical implications of dihydropyrimidinedehydrogenase (DPD) deficiency in patients with severe 5-fluorouracil-associated toxicity: identification of new mutations in the DPD gene. Clinical Cancer Res 2000, 6: 4705-4712. Van Kuilenburg ABP, Muller EW, Haasjes J et al. Lethal outcome of a complete dihydroprimidine dehydrogenase (DPD) deficiency after administration of 5-florouracil: frequency of the common IVS14+1G>A mutation causing DPD deficiency. Clin Cancer Res 2001, 7: 1149-1153. Платиновые агенты также обычно применяют для лечения. Обширная литература подтверждает побочные эффекты соединений платины. Цисплатин имеет многочисленные токсические эффекты: нефротоксичность, нейротоксичность, ототоксичность, тошнота и рвота. DeVita VT, Hellman S, and Rosenberg SA. Cancer, Principles and Practice of Oncology, 7th Ed, Lippincott Williams & Wilkins 2005, 335. Нефротоксичность цисплатина почти приводила к отказу от него, до введения сильнодействующей гидратации Цвиткови и его сотрудниками, которые предотвратили развитие острой почечной недостаточности. Cvitkovic E, Spaulding J, Bethune V, et al. Improvement of cis-dichlorodiamineplatinum (NSC 119875): therapeutic index in an animal model. Cancer 1977, 39, 1357. Hayes D, Cvitkovic E, Golbey R, et al. High dose cis-platinum diamine dichloride: amelioration of renal toxicity by mamnitol diuresis. Cancer 1977, 39, 1372. Полагали, что токсичность цисплатина была некоторой движущей силой в истории как при поиске менее токсичных аналогов, так и для более эффективного лечения его побочных действий. Миелосупрессия, которая обычно не была вызвана тяжелым действием цисплатина, имеет дозолимитирующую токсичность карбоплатина. Evens B, Raju K. Calvert A, et al. Phase II study of JM8, a new platinum analogue, in advanced ovarian carcinoma. Cancer Treat. Rep., 67, 997, 1983. Дозолимитирующая токсичность оксалиплатина представляет собой сенсорную невропатию - характерную особенность всех DACH-содержащих производных платины. DeVita VT, Hellman S, and Rosenberg SA. Cancer, Principles and Practice of Oncology, 7th Ed, Lippincott Williams & Wilkins 2005, 335. Алкилирующие агенты также играют важные роли при лечении рака. Каждый алкилирующий агент связан с определенной токсичностью и не обсужден индивидуально. Следующие виды токсичности представляют собой типичные для алкилирующих агентов: гематопоэтическая токсичность, желудочно-кишечная токсичность, гонадотоксичность, легочная токсичность, алопеция, тератогенность, канцерогенез и иммуносупрессия. DeVita VT, Hellman S, and Rosenberg SA. Cancer, Principles and Practice of Oncology, 7th Ed, Lippincott Williams & Wilkins 2005, 335. Обычная дозолимитирующая токсичность для алкилирующего агента представляет собой гематопоэтическую токсичность. Агенты, взаимодействующие с топоизомеразой, все более привлекают внимание клинических онкологов за их уникальный механизм действия. Топотекан представляет собой полусинтетический продукт из 10-гидроксикамптотецина природного происхождения и показан к применению при лечении второй линии прогрессирующего резистентного рака яичника и мелкоклеточного рака легкого, и он также был активен при лечении гемобластозов, включая миелодиспластические синдромы и множественные миеломы. Huinink W, Gore M, Carmichael J, et al. Topotecan versus paclitaxol for the treatment of recurrent epithelial ovarian cancer. J Clin Oncol 1997, 15, 2183; Schiller JH, Adak S, Cella D, et al. Topotecan versus observation after cisplatin plus etoposide in extensive-stage small-cell lung cancer: E7593-a phase II trial od the Eastern Cooperative Oncology Group. J Clin Oncol 2001, 19, 2114; von Pawel J, Schiller JH, Shepherd FA, et al. Topotecan versus cyclophosphamide, doxorubicin, and vincristine for the treatment of recurrent small-cell lung cancer. J Clin Oncol 1999, 17, 658, Pizzolato JF, Saltz LB. The camptothecins. Lancet 2003, 361, 2235. Дозолимитирующая токсичность этого агента представляет собой миелосупрессию. Хотя топотекан был комбинирован с различными другими способами лечения, включая ионизирующее излучение, цисплатин, паклитаксел и доксорубицин в клинических испытаниях, ни одна из этих комбинаций не достигла никакого стандартного применения в клинической онкологии. Это может быть отчасти обусловлено многократной миелосупрессивной токсичностью топотекана, которая затрудняет объединение с высокими дозами других агентов, супрессирующих костный мозг. Miller AA, Lilenbaum RC, Lynch TJ, et al. Treatment-related fatal sepsis from topotecan/cisplatin and topotecan/paclitaxol. J Clin Oncol 1996, 14, 1964. Иринотекан также представляет собой полусинтетический продукт из группы камптотецина. Это соединение показано к применению в качестве единичного агента или в комбинации с фторурацилом и лейковорином при лечении пациентов с колоректальными раковыми образованиями и также обнаружен активным при лечении мелкоклеточного рака легкого при введении в комбинации с цисплатином. Эта комбинация также была активной при лечении немелкоклеточного рака легких. Saltz LB, Cox JV, Blanke C, et al. Irinotecan plus florouracil and leucovorin for metastatic colorectal cancer. Irinotecan study group. N Engl J Med 2002, 343, 905; Douillard JY, Cunningham D, Roth AD, et al. Irinotecan combined with florouracil compared with florouracil alone as first-line treatment for metastatic colorectal cancer: a multicenter randomized trial. Lancet 2000, 355, 1041; Pizzolato JF, Saltz LB. The camptothecins. Lancet 2003, 361, 2235. Дозолимитирующие токсичности иринотекана представляют собой нейтропению и диарею замедленного типа, и таким образом, его применение в клинической онкологии также ограничено. Все другие разнообразные противораковые агенты, включая недавно введенные эрбитукс и авастин, могут быть применены для ограниченного числа определенных лечений, что также связано с токсичностью. Таким образом, для исследователей рака и клинических онкологов все еще стоит сложная задача в нахождении лучших агентов с более широким терапевтическим индексом для лечения.
Было показано, что камптотецин, цитотоксический алкалоид, первоначально выделенный из листьев и коры Camptotheca Acuminata (Nyssaceae) Воллом и его сотрудниками (J. Am. Chem. Soc. 88, 3888, 1966), обладает противоопухолевой активностью в отношении системы лейкемии мышей L 1210. Структура камптотецина, алкалоида, который имеет стандартно встречающуюся группу индола алкалоида (Heckendorf et al., J Org. Chem. 41, 2045, 1976), показана ниже в формуле (X).
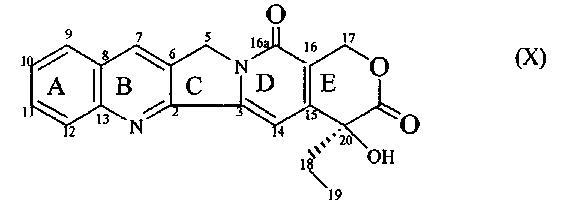
Это соединение («СРТ») имеет пентациклическую кольцевую систему только с одним асимметрическим центром в кольце E с 20(S)-конфигурацией. Пентациклическая кольцевая система включает часть пирроло[3,4-b]хинолин (кольца A, B и C), сопряженный пиридон (кольцо D) и шестичленный лактон (кольцо E) с α-гидроксильной группой. Камптотецин представлял собой большой интерес со времени его первоначального выделения вследствие его заслуживающей внимания активности в отношении системы лейкемии мышей L 1210. Более ранние данные о противоопухолевой активности камптотецина были получены, применяя экспериментально трансплантированные злокачественные опухоли, такие как лейкемия L 1210 у мышей или опухоль Walker 256 у крыс (Chem. Rev. 23, 385, 1973, Cancer Treat. Rep. 60, 1007, 1967). Последующие клинические исследования показали, что это соединение не пригодно к применению в качестве противоракового агента in vivo вследствие его высокой токсичности. Сам камптотецин нерастворим в воде. Следовательно, ранее камптотецин оценивали клинически как растворимую в воде соль карбоксилата натрия. Эта форма камптотецина имела сильную токсичность и, по-видимому, была лишена противораковой активности (Gottlieb et al., Cancer Chemother. Rep. 54, 461, 1970, and 56, 103, 1972, Muggia et al., Cancer Chemother. Rep. 56, 515, 1972, Moertel et al., Cancer Chemother. Rep. 56, 95, 1972, and Schaeppi et al., Cancer Chemother. Rep. 5:25, 1974). Эти результаты вызвали прекращение испытаний фазы II. Продолженная оценка этого агента показала, что соль карбоксилата натрия является только на 10% такой активной, как нативный камптотецин с замкнутым лактонным кольцом в неизмененном виде (Wall et al., In International Symposium on Biochemistry And Physiology of The Alkaloids, Mothes et al., eds., Academie - Verlag, Berlin, 77, 1969, Giovanella et al., Cancer res. 51, 3052, 1991). Кроме того, были установлены важные показатели противоопухолевой активности в группе камптотецина (Wall et al., Ann. Rev., Pharmacol. Toxicol. 17, 117, 1977). Эти результаты показывают, что лактонное кольцо E в неизмененном виде и α-гидроксильная группа являются существенными для противоопухолевой активности.
В середине 1980-х годов было обнаружено, что молекулярная мишень действия камптотецинов представляет собой новый ядерный фермент топоизомеразу I. Hsiang YH, Liu LF. Identification of mammalian DNA topoisomerase I as an intracellular target of anticancer drug camptothecin. Cancer Res1988, 48, 1722. Приблизительно в то же самое время получили и биологически оценили несколько новых растворимых в воде производных камптотецина, включая два соединения (топотекан и иринотекан), обсужденные ранее. Последующие клинические оценки двух соединений показали предсказуемые токсичности и значительную противораковую активность. Takimoto CH, Arbuck SG. Topoisomerase I targeting agents: the camptothecins. In: Chabner BA, Longo DL, eds., Cancer therapy & biotherapy: principles and practice, 3rd ed. Philadelphia: Lippincott Williams & Wilkins 2001, 579. Топотекан был одобрен в 1996 году в качестве лекарственного средства второй линии для лечения прогрессирующего рака яичника, и он позже получил признание для лечения пациентов с резистентным мелкоклеточным раком легкого. В то же самое время иринотекан был зарегистрирован для лечения прогрессирующего 5-фторурацил-резистентного колоректального рака. Он фактически представлял первый новый агент, который получил одобрение для лечения этого заболевания в Соединенных Штатах через почти 40 лет.
В 1989 году Джованелла и др. обнаружили, что некоторые из нерастворимых в воде производных камптотецина имеют высокую противоопухолевую активность в отношении ксенотрансплантатов опухолей человека (Giovanella et al., Science, 246, 1046, 1989). Также было показано, что введение камптотецина с замкнутым лактонным кольцом превосходит введение растворимой в воде соли карбоксилата (Giovanella et al., Cancer Res., 51, 3052, 1991). Эти полученные данные дополнительно подтверждали важность лактонного кольца в неизмененном виде для биологической активности.
Раскрытие кольца 20(S)-камптотецина приводит к гораздо более сильной противораковой активности у мышей, чем у людей. В действительности было доказано, что СРТ, введенный внутримышечно («в/м»), подкожно («п/к») и внутрь в живот («в.ж.»), представляет собой очень сильный противораковый агент в отношении опухолей человека у мышей, то есть при росте в качестве ксенотрансплантатов у голых мышей (Giovanella et al., Cancer Res. 51:3052, 1991). Однако, когда опухоли лечили с помощью СРТ у людей, была показана более низкая степень противораковой активности у людей, чем у мышей (Stehlin et al., In Camptothecins: New Anticancer Agents, 1995, CRC Press, pp. 59-65).
То же самое явление наблюдали с другими производными СРТ. Было показано, что у мышей 9-нитрокамптотецин («9NC») является в 2-3 раза более сильным, чем СРТ в отношении ксенотрансплантатов опухоли человека, вызывая полное уничтожение всех злокачественных опухолей человека, которые лечат (Pantazis et al., Cancer Res. 53:1577, 1993; Pantazis et al., Int. J. Cancer 53:863, 1995).
Раскрытие кольца особенно проблематично в камптотецинах, которые существуют в двух различных формах. Встречающийся в природе камптотецин имеет S-конфигурацию и в 10-100 раз более биологически активен, чем R-изомер. Полагают, что лактон с формой S-конфигурации необходим для противоопухолевой активности, и форма карбоксилата обычно относится к клиническим токсичностям. Молекула находится в равновесии в водном растворе. Это равновесие зависит от pH. При физиологическом pH, то есть 7 или выше, уравнение равновесия выглядит следующим образом:
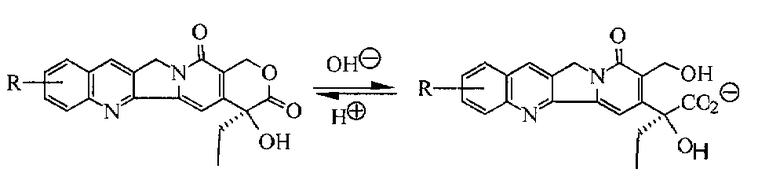
Реакция гидролиза биологического активного лактонного кольца камптотецинов с водой при более высоком pH дает биологически неактивную раскрытую форму. Кроме того, проблема гидролиза с СРТ и его аналогами усугублена в человеческой крови, потому что преобладающий человеческий сывороточный альбумин (HSA) предпочтительно связывается с формой карбоксилата, которая смещает равновесие лактон/карбоксилат к неактивной форме (J. Biochem., 212, 285-287, 1993; Biochemistry, 33, 10325-10336, 1994; Biochemistry, 33, 12540-12545, 19944). Соответственно, сохранение лактонного кольца молекулы в течение достаточного времени для клеток опухоли, чтобы циклически пройти S-фазу, представляет собой главную задачу, и было целью значительного числа исследований.
Множество попыток было сделано для получения производных камптотецина, обладающих большей биологической активностью и повышенной стабильностью. Многие из этих соединений представляют собой продукты модификаций A, B и C кольца молекулы, но немногие из этих модификаций повышали стабильность лактонного кольца при физиологических условиях. Другие подходы были более успешны. Например, ацилирование группы 20-ОН обеспечивает полезный элемент защиты лактонного кольца E/ Wall et al., патент США №4943579, описывает несколько ацилированных соединений камптотецина, имеющих растворимость в воде, хотя лактон может не оставаться в неизменном виде при физиологических условиях. Патент США №5968943 Cao et al. раскрывает производные СРТ, которые представляют собой эффективные противораковые агенты.
В литературе было доложено о множестве различных реакций получения сложных эфиров камптотецина.
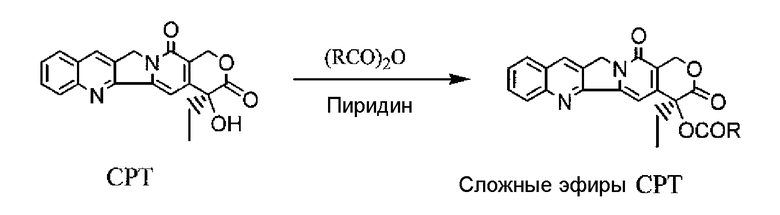
Прямое ацилирование камптотецина ангидридами органических кислот в присутствии пиридина в качестве катализатора применяли для получения сложных эфиров алкил- и алкенилкамптотецина (как показано выше). Эта реакция обычно дает высокие выходы, но доступность ангидридов органических кислот ограничивает возможности реакции.
Следовательно, использовали систему реактивов дициклогексилкарбодиимид (DCC)/диметиламинопиридин (DMAP) для реакций ацилирования карбоксильных кислот со спиртами и тиолами. Предварительно, способ использовали для получения ароматических сложных эфиров камптотецина (как показано ниже).
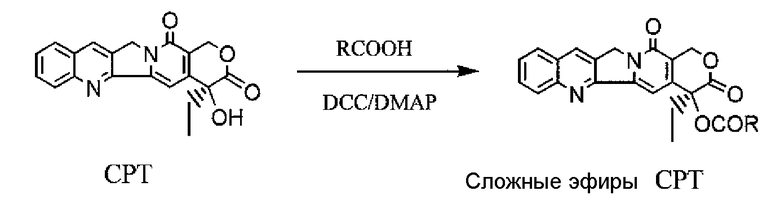
Эта методика, однако, дает хорошие выходы реакции, только когда карбоксильные кислоты являются очень электрофильными. Когда кислоты являются менее электрофильными, реакция дает низкий выход или вообще не получают ожидаемый продукт. Например, используя пропионовую кислоту для получения пропионата камптотецина по этой методике, эфирный продукт по существу не получали и исходный камптотецин возвращался почти на 100%.
Нонановый хлорид также применяли в качестве ацилирующего агента для этерификации камптотецина в присутствии пиридина в качестве агента, улавливающего HCl в метиленхлориде. Реакция (как показано ниже) проходила с низким выходом (6%).
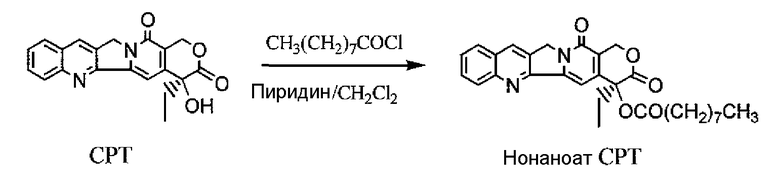
Поскольку изначальные структурные особенности камптотецина обеспечивают для исследователей рака идеальную основу для модификации структуры при получении лучших противораковых агентов, синтезировали и оценили множество различных сложных эфиров камптотецина. Было обнаружено, что продукты этерификации в значительной степени увеличивали биологическую жизнь молекул в теле. Также было показано, что лечение синтетическими сложными эфирами камптотецина опухолей человека, выращенных в ксенотрансплантатах у голых мышей, является эффективным, и токсичность у мышей минимальна. Cao, Z.; Pantazis, P.; Mendoza, J.; Early, J.; Kozielski, A.; Harris, N.; Vardeman, D.; Liehr, J.; Stehlin, J.; Giovanella, B. Ann. N.Y. Acad. Sci. 2000, 922, 122; Cao, Z.; Pantazis, P.; Mendoza, J.; Early, J.; Kozielski, A.; Harris, N.; Giovanella, B. Acta Pharmacologica Sinica 2003, 24, 109.
В то время как существует много способов получения эфиров камптотецина, однако, каждая методика имеет определенные ограничения, как обсуждено выше. Следовательно, все еще есть потребность в открытии сложных эфиров камптотецина, которые сохранят противоопухолевую активность исходного соединения СРТ, будут иметь намного более низкую токсичность, чем СРТ и которые могут быть произведены в соответствии с альтернативной методикой(ами) получения сложных эфиров камптотецина.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соответственно, особенность настоящего изобретения состоит в обеспечении кристаллического гидрата сложного эфира камптотецина, который продемонстрирует широкий спектр противоопухолевой активности и предпочтительно низкую или ненаблюдаемую токсичность.
Другая особенность настоящего изобретения состоит в обеспечении кристаллического гидрата сложного эфира камптотецина, обладающего более широким диапазоном терапевтического индекса, чем большинство противораковых агентов, используемых в настоящее время.
Другая особенность настоящего изобретения состоит в обеспечении безопасного и простого способа получения кристаллического гидрата сложного эфира камптотецина.
Дальнейшая особенность настоящего изобретения состоит в обеспечении кристаллических гидратов сложного эфира камптотецина, которые сохраняют значительную противоопухолевую активность, как исходное соединение СРТ, и имеют намного более низкую токсичность, чем его исходное соединение.
Еще одна особенность настоящего изобретения состоит в обеспечении кристаллических гидратов сложного эфира камптотецина, обладающих хорошей поглотительной способностью в живом организме.
Для достижения особенностей и в соответствии с целями настоящего изобретения, как осуществлено и широко рассмотрено в настоящем описании, настоящее изобретение частично относится к кристаллическим гидратам сложного эфира камптотецина, таким как кристаллические гидраты алифатического сложного эфира камптотецина, как кристаллический гидрат камптотецин-20-O-пропионата («CZ48»), фармацевтическим композициям, включающим кристаллические гидраты алифатического сложного эфира, способам лечения рака или злокачественной опухоли, используя кристаллические гидраты сложного эфира камптотецина, и способам получения гидратированных кристаллических сложных эфиров камптотецина, включающим взаимодействие соединения камптотецина по меньшей мере с одним ацилирующим агентом, протонированным по меньшей мере одной кислотой.
Дополнительные особенности и преимущества настоящего изобретения будут сформулированы частично в описании, которое следует, и частично будут очевидны из описания, или могут быть изучены практикой настоящего изобретения. Задачи и другие преимущества настоящего изобретения будут очевидны и достигнуты посредством элементов и комбинаций, в частности указанных в описании и прилагаемой формуле изобретения.
Все патенты, заявки на патент и публикации, упомянутые во всей заявке, включены полностью посредством ссылки в настоящее описание и являются частью настоящей заявки.
Следует понимать, что как вышеизложенное общее описание, так и следующее подробное описание представляют собой образцовые и только объяснительные и предназначены для обеспечения дальнейшего объяснения настоящего изобретения в формуле изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет собой диаграмму ORTEP одиночной молекулы продукта.
Фиг.2 представляет собой диаграмму ORTEP, изображающую две молекулы кристаллического гидрата камптотецин-20-O-пропионата, соединенные вместе водным мостиком.
Фиг.3 представляет собой диаграмму ORTEP, изображающую трехмерную структуру (a, b координаты положения) кристаллического гидрата камптотецин-20-O-пропионата.
Фиг.4 представляет собой диаграмму ORTEP, изображающую трехмерную структуру (a, c координаты положения) кристаллического гидрата камптотецин-20-O-пропионата.
Фиг.5 представляет собой диаграмму ORTEP, изображающую трехмерную структуру (b, c координаты положения) кристаллического гидрата камптотецин-20-O-пропионата.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Камптотецины («CPT») обладают значительной противоопухолевой и противораковой активностью, но эти соединения подвержены разрушению при нормальных физиологических условиях, и полученные метаболиты часто проявляют токсические свойства. Проведенные в лаборатории исследования метаболизма камптотецина в плазме человека показали, что единственный обнаруженный метаболит представляет собой соль карбоксилата натрия с открытым кольцом, которая является токсичной и неактивной. Измерение фармакокинетики для СРТ в плазме человека указывает, что период полураспада лекарственного средства с лактонным кольцом в неизменном виде представляет собой приблизительно 30 мин. Эти результаты подразумевают, что лекарственное средство теряет 90% его активности, и обнаруживается много токсичностей за очень короткое время после его приема пациентами.
Согласно настоящему изобретению раскрыт СРТ, превращенный в более липорастворимую и гидратированную кристаллическую молекулу сложного эфира, в дальнейшем время от времени называемый пролекарством. При приеме пациентами пролекарства быстро вводятся в кровоток пациентов и легко превращаются в исходное соединение в теле. Отмечено, что само пролекарство может также быть активным и/или может быть частично или полностью превращенным.
Согласно различным вариантам осуществления соединения настоящего изобретения могут включать кристаллические алифатические сложные эфиры СРТ в гидратированной форме, имеющие формулу:
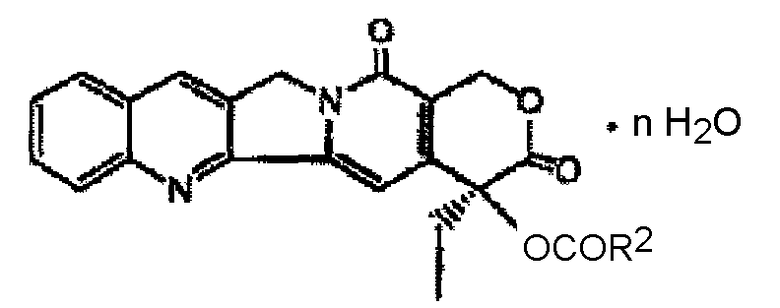
В этой формуле n может представлять собой любое число в пределах от 1 до 10 или более, такое как 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. R2 представляет собой C2-C6 алкильную группу, такую как C2-C4 алкильную группу. В одном или более вариантах осуществления R2 представляет собой -CH2CH3; -CH2CH2CH3; -CH2CH2CH2CH3; или -CH2CH2CH2CH2CH2CH3. В качестве еще одного определенного варианта осуществления n представляет собой 3 и R2 представляет собой -CH2CH3 или -CH2CH2CH3.
Согласно по меньшей мере одному варианту осуществления соединения настоящего изобретения могут включать кристаллический гидрат камптотецин-20-O-пропионата, имеющий формулу, показанную ниже:
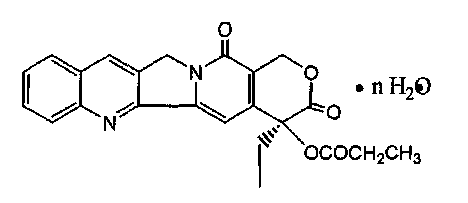
В этой формуле n может представлять собой любое число в пределах от 1 до 10, такое как 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В качестве примера структура кристаллического гидрата камптотецин-20-O-пропионата была определена с помощью рентгеноструктурного анализа монокристалла и показана на фиг.1-5. Фиг.1 изображает диаграмму ORTEP одиночной молекулы продукта. Одна молекула камптотецин-20-O-пропионата и приблизительно 3 молекулы воды соединены через сильные водородные связи. Более одной молекулы камптотецин-20-O-пропионата в кристаллической структуре могут быть связаны друг с другом через мостик, созданный из молекул H2O. Фиг.2 показывает две молекулы камптотецин-20-O-пропионата, соединенные водным мостиком. Фиг.3-5 показывают трехмерные структуры кристалла. Другие сложные эфиры СРТ настоящего изобретения будут иметь ту же самую структуру за исключением длины цепи сложного эфира.
Пролекарства настоящего изобретения могут быть в жидком или твердом состоянии. Согласно настоящему изобретению, соединения представляют собой кристаллические. Согласно по меньшей мере некоторым вариантам осуществления, соединения настоящего изобретения могут быть кристаллическими или твердыми, в которых составляющие атомы, молекулы или ионы упакованы в регулярно упорядоченную, повторяющуюся модель, расположенную во всех трех пространственных направлениях. Кристаллы могут быть моноклинической системой с размерами (от 0,10 до 0,50)×(от 0,01 до 0,10)×(от 0,01 до 0,05) мм3 и объемами от 100 до 5000 Å3, такими объемами, как от 200 до 4500 Å3 или от 500 до 4000 Å3, или от 750 до 3500 Å3, или от 1000 до 3000 Å3, или от 1250 до 2500 Å3, или от 1500 до 2200 Å3.
Используемый в настоящем описании «кристаллический» относится к материалу, который содержит определенное соединение, которое может быть гидратированным и/или сольватированным и имеет достаточное содержание кристаллов, чтобы показать ярко выраженную дифракционную модель с помощью порошковой рентгеновской дифракции (XRPD) или других дифракционных методов. Часто кристаллический материал, который получают из растворителя с помощью прямой кристаллизации соединения, растворенного в растворе, или взаимопревращения кристаллов, полученных при различных условиях кристаллизации, будет иметь кристаллы, которые содержат растворитель, называемый кристаллическим сольватом. Примеры свойств кристаллов включают ориентацию химических частей относительно друг друга в пределах кристалла и преобладание определенной формы соединения, которая предпочтительна в присутствии кислоты в композиции растворителя.
Согласно по меньшей мере одному варианту осуществления, соединения настоящего изобретения могут иметь чистоту от приблизительно 90% до приблизительно 100% по AUC (площадь под кривой). Согласно некоторым вариантам осуществления, соединения настоящего изобретения могут иметь чистоту от приблизительно 95% до приблизительно 100% по AUC. Согласно по меньшей мере одному варианту осуществления, соединения настоящего изобретения могут иметь чистоту от приблизительно 99% до приблизительно 100% по AUC, такую как от 99,3% до 99,999%; от 99,5% до 99,999%; от 99,75% до 99,999%; от 99,85% до 99,999% все по AUC. Согласно по меньшей мере одному варианту осуществления, соединения настоящего изобретения могут иметь точку плавления от приблизительно 240°C до приблизительно 243°C, такую как 242°C или приблизительно 242°C. Эта точка(и) плавления наиболее предпочтительна для кристаллического гидрата сложного эфира, где R2 представляет собой -CH2CH3. Точки плавления соединений настоящего изобретения могут быть ниже или выше, чем упомянутый диапазон, когда R2 представляет собой группу CH3 или C3H7, или C4H9, или C6H13.
Согласно различным вариантам осуществления, настоящее изобретение может включать кристаллические гидраты алифатических сложных эфиров СРТ, имеющие S-конфигурацию, R-конфигурацию и/или рацемические смеси обоих S- и R-изомеров. Согласно некоторым вариантам осуществления, кристаллические гидраты алифатических сложных эфиров СРТ, полученные из природного камптотецина, имеют только S-конфигурацию или главным образом S-конфигурацию, такую как 90% или выше, 95% или выше, 98% или выше, 99% или выше, или от 99% до 99,99%.
Превращение пролекарств в исходное соединение СРТ, может быть опосредовано группой ферментов, называемых эстеразами, присутствующих в крови многих животных, включая людей. С тех пор как пролекарства быстро распределяются по всему телу за короткий промежуток времени после доставки, эти соединения существуют при очень низкой концентрации в то время, когда они подвергаются ферментативному гидролизу, с помощью которого высвобождается исходный камптотецин, который препятствует осаждению СРТ в кровотоке.
Следовательно, настоящее изобретение обеспечивает гидратированные кристаллические производные СРТ или аналоги, которые предпочтительно дольше остаются в неизменном виде в теле человека или животного, особенно в теле человека, таким образом увеличивая противоопухолевые и противораковые эффекты, не производя нежелательных побочных действий.
Настоящее изобретение также обеспечивает фармацевтические композиции, содержащие фармацевтически эффективное количество одного или более соединений настоящего изобретения необязательно в комбинации с одним или более фармацевтически приемлемыми носителями, эксципиентами, разбавителями или вспомогательными веществами. Например, соединения настоящего изобретения могут быть получены в форме таблеток, пилюль, порошковых смесей, капсул, инъецируемых составов, растворов, суппозиториев, эмульсий, дисперсий, добавок в пищу и в других подходящих формах. Они могут также быть получены в форме стерильных твердых композиций, например, высушенных сублимацией и, если желательно, объединенных с другими фармацевтически приемлемыми эксципиентами. Такие твердые композиции могут быть растворены стерильной водой, физиологическим солевым раствором или смесью воды и органического растворителя, такого как пропиленгликоль, этанол и подобные, или некоторой другой стерильной вводимой средой непосредственно перед применением парентерального введения.
Типичные фармацевтически приемлемые носители представляют собой, например, маннит, мочевину, декстраны, лактозу, невосстанавливающие сахара, картофельный и маисовый крахмалы, стеарат магния, тальк, растительные масла, полиалкиленгликоли, этилцеллюлозу, поли(винилпирролидон), карбонат кальция, этилолеат, изопропилмиристат, бензилбензоат, карбонат натрия, желатин, карбонат калия, кремниевую кислоту. Фармацевтическое лекарственное средство может также содержать нетоксичные вспомогательные вещества, такие как эмульгирующие, консервирующие и/или смачивающие агенты и подобные, как, например, сорбитан монолаурат, триэтаноламин олеат, полиоксиэтилен моностеарат, глицерилтрипальмитат, диоктил натрий сульфосукцинат и подобные.
«Фармакологическая композиция» относится к смеси одного или более соединений, описанных в настоящей заявке, или его фармацевтически приемлемых солей с другими химическими компонентами, такими как фармацевтически приемлемые носители и/или эксципиенты. Цель фармакологической композиции состоит в облегчении введения соединения в организм.
Используемая в настоящем описании фраза «фармацевтически приемлемый носитель» обозначает фармацевтически приемлемый материал, композицию или среду для лекарства, такую как жидкий или твердый наполнитель, разбавитель, эксципиент, растворитель или инкапсулированный материал, включенный в перенос или транспортирование испытуемого агента от одного органа или части тела к другому органу или части тела. Каждый носитель должен быть «приемлемым» в значении быть совместимым с другими ингредиентами состава и не вредным для пациента. Некоторые примеры материалов, которые могут служить фармацевтически приемлемыми носителями, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как натрий карбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; (4) порошковый трагакант; (5) солод; (6) желатин; (7) тальк; (8) эксципиенты, такие как какао-масло и воски суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновую кислоту; (16) апирогенную воду; (17) изотонический солончак; (18) раствор Рингера; (19) этиловый спирт; (20) фосфатные буферные растворы; и (21) другие нетоксичные совместимые вещества, используемые в фармацевтических составах. Физиологически приемлемый носитель должен не вызывать значительного раздражения для организма и не отменять биологическую активность и свойства соединения, которое вводят.
«Эксципиент» может относиться к инертному веществу, добавленному к фармакологической композиции для дальнейшего облегчения введения соединения. Примеры эксципиентов включают, но не ограничиваются, карбонат кальция, фосфат кальция, различные сахара и типы крахмала, производные целлюлозы, желатин, жиры, липиды, растительные масла и полиэтиленгликоли.
«Фармацевтически эффективное количество» может также или альтернативно обозначать количество, которое является способным обеспечить терапевтический и/или профилактический эффект. Определенная доза введенного соединения, согласно этому изобретению, для получения терапевтического и/или профилактического эффекта будет, конечно, определена с детальными подробностями, связанная с этим случаем, включая, например, определенное введенное соединение, путь введения, состояние, которое лечат, и человека, которого лечат. Типичная ежедневная доза (введенная в единичной или разделенных дозах) будет содержать уровень дозировки от приблизительно 0,01 мг/кг до приблизительно 50-100 мг/кг веса тела активного соединения изобретения. Ежедневные дозы могут быть от приблизительно 0,05 мг/кг до приблизительно 20 мг/кг или от приблизительно 0,1 мг/кг до приблизительно 10 мг/кг.
В некоторых вариантах осуществления предпочтительный терапевтический эффект представляет собой, в некоторой степени, ингибирование роста характерных клеток пролиферативного заболевания, например, рака молочной железы или рака поджелудочной железы. Терапевтический эффект также обычно, но не в случае необходимости, будет ослаблять в некоторой степени один или более симптомов, кроме роста клетки или размера клеточной массы. Терапевтический эффект может включать, например, один или более из 1) сокращения числа клеток; 2) сокращения размера клеток; 3) ингибирования (то есть замедления, в некоторой степени, предпочтительно, прекращения) клеточной инфильтрации в периферические органы, например, в случае метастаза рака; 3) ингибирования (то есть замедления, в некоторой степени, предпочтительно, прекращения) метастаза опухоли; 4) ингибирования в некоторой степени роста клеток; и/или 5) ослабления в некоторой степени одного или более симптомов, связанных с нарушением.
Фармацевтические композиции, используемые в способах настоящего изобретения, могут также содержать активный ингредиент в форме, подходящей для перорального применения, например, как таблетки, пастилки, таблетки для рассасывания, водные или масляные суспензии, дисперсные порошки или гранулы, эмульсии, твердые или мягкие капсулы, или сиропы, или эликсиры. Композиции, предназначенные для перорального применения, могут быть получены согласно любому способу, известному в данной области техники для получения фармацевтических композиций, и такие композиции могут содержать подсластители, ароматизаторы, красители и/или консерванты. Таблетки могут содержать активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, которые являются подходящими для получения таблеток. Эти эксципиенты могут быть, например, инертными разбавителями, такими как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующими и дезинтегрирующими агентами, такими как микрокристаллическая целлюлоза, кросскармелоза натрия, кукурузный крахмал или альгиновая кислота; связующими агентами, например, крахмал, желатин, поливинилпирролидон или камедь, и смазывающими агентами, например, стеарат магния, стеариновая кислота или тальк. Таблетки могут быть непокрытыми или покрытыми с помощью известных методик, чтобы скрыть вкус лекарственного средства или отложить дезинтегрирование и абсорбцию в желудочно-кишечном тракте и таким образом обеспечить пролонгированное действие за более длительный период. Может быть применен соответствующим образом, например, растворимый в воде материал, скрывающий вкус, такой как гидроксипропилметилцеллюлоза или гидроксипропилцеллюлоза, или материал со временем удерживания, такой как этилцеллюлоза или ацетат бутират целлюлозы.
Составы для перорального применения могут также быть представлены в качестве твердых желатиновых капсул, в которых активный ингредиент смешивают с инертным твердым разбавителем, например, карбонатом кальция, фосфатом кальция или каолином, или в качестве мягких желатиновых капсул, в которых активный ингредиент смешивают с растворимым в воде носителем, таким как полиэтиленгликоль, или масляной средой, например, арахисовым маслом, жидким парафином или оливковым маслом.
Водные суспензии могут содержать активный материал в смеси с эксципиентами, подходящими для получения водных суспензий. Такие эксципиенты могут быть суспендирующими агентами, например, карбоксиметилцеллюлозой натрия, метилцеллюлозой, гидроксипропилметилцеллюлозой, альгинатом натрия, поливинилпирролидоном, трагакантом и аравийской камедью; диспергирующие или смачивающие агенты могут быть фосфатидами природного происхождения, например, лецитином, или продуктами конденсации алкиленоксида с жирными кислотами, например, полиоксиэтилен стеаратом, или продуктами конденсации этиленоксида с алифатическими спиртами с длинной цепью, например, гептадекаэтилен-оксицетанолом, или продуктами конденсации этиленоксида с неполными сложными эфирами, полученными из жирных кислот и гекситола, такими как полиоксиэтилен сорбит моноолеат, или продуктами конденсации этиленоксида с неполными сложными эфирами, полученными из ангидридов жирных кислот и гекситола, например, полиэтилен сорбитан моноолеат. Водные суспензии могут также содержать один или более консервантов, например, этил- или н-пропил-п-гидроксибензоат, один или более красителей, один или более ароматизаторов, и один или более подсластителей, таких как сахароза, сахарин или аспартам.
Масляные суспензии могут быть получены суспендированием активного ингредиента в растительном масле, например, арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как жидкий керосин. Масляные суспензии могут содержать загущающий агент, например, желтый воск, твердый парафин или цетиловый спирт. Подсластители, такие как определено выше, и ароматизаторы могут быть добавлены для обеспечения приятного вкуса пероральному лекарственному средству. Эти композиции могут быть сохранены с помощью добавления антиоксиданта, такого как бутилированный гидроксианизол или α-токоферол.
Дисперсные порошки и гранулы, подходящие для получения водной суспензии с помощью добавления воды, обеспечивают активный ингредиент в смеси с диспергирующим или смачивающим агентом, суспендирующим агентом и одним или более консервантами. Примерами подходящих диспергирующих или смачивающих агентов и суспендирующих агентов являются уже упомянутые выше. Могут также присутствовать дополнительные эксципиенты, например, подсластители, ароматизаторы и красители. Эти композиции могут быть сохранены с помощью добавления антиоксиданта, такого как аскорбиновая кислота.
Соединения и фармацевтические композиции, используемые в способах настоящего изобретения, могут также быть в форме эмульсий «масло-в-воде». Масляная фаза может быть растительным маслом, например, оливковым маслом или арахисовым маслом, или минеральным маслом, например, жидким парафином, или их смесью. Подходящие эмульгирующие агенты могут быть фосфатидами природного происхождения, например, соевым лецитином, и сложными эфирами или неполными сложными эфирами, полученными из ангидридов жирных кислот и гекситола, например, сорбитан моноолеатом, и продуктами конденсации вышеупомянутого неполного сложного эфира с этиленоксидом, например, полиоксиэтилен сорбитан моноолеатом. Эмульсии могут также содержать подсластители, ароматизаторы, консерванты и/или антиоксиданты.
Сиропы и эликсиры могут быть получены с подсластителями, например, глицерином, пропиленгликолем, сорбитом или сахарозой. Такие составы могут также содержать смягчители, консерванты, ароматизаторы, красители и антиоксидант.
Фармацевтические композиции могут быть в форме стерильных инъецируемых водных растворов. Среди приемлемых наполнителей и растворителей, которые могут быть применены, находятся вода, раствор Рингера и изотонический раствор хлорида натрия.
Стерильное инъецируемое лекарственное средство может также быть стерильной инъецируемой микроэмульсией «масло-в-воде», в которой активный ингредиент растворяют в масляной фазе. Например, активный ингредиент может быть сначала растворен в смеси соевого масла и лецитина. Масляный раствор затем вводят в смесь воды и глицерина и обрабатывают с получением микроэмульсии.
Фармацевтические композиции могут быть в форме стерильной инъецируемой суспензии на водной или масляной основе для внутримышечного и подкожного введения. Эта суспензия может быть получена согласно известным в данной области техники способам, используя подходящие диспергирующие или смачивающие агенты и суспендирующие агенты, которые были упомянуты выше. Стерильное инъецируемое лекарственное средство может также быть стерильным инъецируемым раствором или суспензией в нетоксичном парентерально приемлемом разбавителе или растворителе, например, как раствор в 1,3-бутандиоле. Кроме того, стерильные жирные масла стандартно применяют в качестве растворителя или суспендирующей среды. С этой целью может быть применено любое мягкое жирное масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, находят применение в получении инъецируемых лекарственных средств.
Соединения настоящего изобретения, используемые в способах настоящего изобретения, можно также вводить в форме суппозиториев для ректального введения лекарственного средства. Эти композиции могут быть получены, смешивая ингибиторы с подходящим не вызывающим раздражение эксципиентом, который является твердым веществом при обычных температурах, но жидким при ректальной температуре, и следовательно, будет таять в прямой кишке с высвобождением лекарственного средства. Такие материалы включают какао-масло, содержащий глицерин желатин, гидрогенизированные растительные масла, смеси полиэтиленгликоля различных молекулярных масс и сложных эфиров жирных кислот полиэтиленгликоля.
Для местного применения могут быть использованы кремы, мази, желе, содержащие лекарственное средство, растворы или суспензии и т.д., содержащие соединение или композицию изобретения. Используемое в настоящем описании местное применение может включать жидкость для полоскания рта и горла.
Соединения, используемые в способах настоящего изобретения, можно вводить в интраназальной форме через местное применение подходящих интраназальных наполнителей и систем доставки, или через трансдермальные пути введения, используя формы трансдермального пластыря, хорошо известные специалистам в данной области техники. Для введения в форме трансдермальной системы доставки, введение дозировки, конечно, будет непрерывным, а не прерывистым в течение всего режима дозировки.
Способы, соединения и композиции настоящего изобретения можно также применять совместно с другими известными терапевтическими агентами, которые выбраны за их определенную пригодность в отношении состояния, которое лечат. Например, настоящие соединения могут быть пригодными совместно с известными противораковыми и цитотоксическими агентами. Дополнительно, настоящие способы и соединения могут также быть пригодными совместно с другими ингибиторами частей сигнального пути, который связывает рецепторы фактора роста клеточной поверхности с ядерными сигналами, инициирующими клеточную пролиферацию.
Один аспект изобретения представляет собой фармацевтическую композицию, пригодную для лечения рака у теплокровных животных, которая содержит по меньшей мере одно соединение изобретения, как определено в настоящем описании, совместно с фармацевтически приемлемым эксципиентом. Композицию получают в соответствии с известными методиками получения состава композиции, подходящей для перорального, местного, трансдермального, ректального, с помощью ингаляции, парентерального (внутривенного, внутримышечного или внутрибрюшинного) введения и подобного. Подробное методическое руководство для получения композиций изобретения найдено посредством ссылки на 18-й или 19-й выпуск Remington's Pharmaceutical. Sciences, Published by the Mack Publishing Co., Easton, Pa. 18040. Соответствующие части включены в настоящее описание посредством ссылки.
Рассмотрены формы единичных доз или многократных доз, каждые имеющие преимущества в определенных клинических условиях. Единичная доза содержала бы предопределенное количество активного соединения, вычисленного для получения желательного эффекта(ов) при лечении рака. Форма многократной дозы может быть особенно полезной, когда множество единичных доз или дробных доз требуется для достижения желательных эффектов. Обе эти формы дозировки могут иметь описания изобретения, они обусловлены или непосредственно зависят от характерного признака определенного соединения, определенного терапевтического эффекта, который будет достигнут, и любых ограничений, свойственных получению определенного соединения для лечения рака.
Единичная доза может содержать терапевтически эффективное количество, достаточное для лечения рака у объекта, и может содержать от приблизительно 1,0 до 1000 мг соединения, например, от приблизительно 50 до 500 мг.
Соединение может быть введено перорально в подходящем составе, таком как таблетка для глотания, буккальная таблетка, капсула, каплет, эликсир, суспензия, сироп, пастилка, капсула, таблетка для рассасывания и подобные. Обычно наиболее эффективный состав представляет собой таблетку или капсулу (отдельно или вместе определяемый как «пероральная единица дозирования»). Подходящие составы получают в соответствии со стандартными доступными методиками состава, которые соответствуют особенностям соединения к эксципиентам, доступным для получения соответствующей композиции. Таблетка или капсула будет содержать от приблизительно 50 до приблизительно 500 мг соединения настоящего изобретения.
Форма может доставить соединение быстро или может быть лекарственным средством с замедленным высвобождением. Соединение может быть помещено в твердую или мягкую капсулу, может быть спрессовано в таблетки или может быть включено в напитки, продукты питания или иначе в пищу. Процентное содержание окончательной композиции и лекарственного средства может, конечно, варьироваться и может стандартно расположиться между 1 и 90% веса окончательной формы, например, таблетки. Количество в таких терапевтически эффективных композициях представляет собой такое, что будет получена подходящая дозировка. Композиции согласно настоящему изобретению могут быть получены таким образом, чтобы пероральная форма единицы дозирования содержала от приблизительно 5 до приблизительно 50% веса (% вес.) единицы дозирования по весу между 50 и 1000 мг.
Подходящий состав пероральной единицы дозирования может также содержать: связующее вещество, такое как трагакант, камедь, кукурузный крахмал, желатин; подсластители, такие как лактоза или сахароза; дезинтегрирующие агенты, такие как кукурузный крахмал, альгиновая кислота и подобные; смазывающие вещества, такие как стеарат магния; или ароматизаторы, такие как мята перечная, масло грушанки или подобные. Различные другие материалы могут присутствовать в качестве покрытия или иначе модифицировать физическую форму пероральной единицы дозирования. Пероральная единица дозирования может быть покрыта шеллаком, сахаром или обоими веществами. Сироп или эликсир могут содержать соединение, сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консерванта, краситель и ароматизатор. Любой используемый материал должен быть фармацевтически приемлемым и по существу нетоксичным. Подробности типов пригодных эксципиентов могут быть найдены в девятнадцатом выпуске «Remington: The Science and Practice of Pharmacy», Mack Printing Company, Easton, Pa. Для более полного обсуждения смотрите особенно главы 91-93.
Соединение можно вводить парентерально, например, внутривенно, внутримышечно, подкожно или внутрибрюшинно. Носитель, или эксципиент, или смесь эксципиентов могут быть растворителем или дисперсионной средой, содержащей, например, различные полярные или неполярные растворители, их подходящие смеси или масла. Используемый в настоящем описании «носитель» или «эксципиент» обозначает фармацевтически приемлемый носитель или эксципиент и включает любые и все растворители, дисперсионные агенты или среды, покрытие(я), антимикробные агенты, изо/гипо/гипертонические агенты, изменяющие абсорбцию агенты и подобные. Применение таких веществ и агентов для фармацевтически активных веществ хорошо известно в данной области техники. Применение в терапевтических композициях рассматривают за исключением случаев, когда любые стандартные среды или агенты являются несовместимыми с активным ингредиентом. Кроме того, другие или дополнительные активные ингредиенты могут также быть включены в окончательную композицию.
Растворы соединения могут быть получены в подходящих разбавителях, таких как вода, этанол, глицерин, жидкий полиэтиленгликоль(и), различные масла и/или их смеси и другие вещества, известные специалистам в данной области техники.
Фармацевтические формы, подходящие для применения инъекций, включают стерильные растворы, дисперсии, эмульсии и стерильные порошки. Окончательная форма должна быть стабильной при условиях изготовления и хранения. Кроме того, окончательная фармацевтическая форма должна быть защищена от загрязнения и, следовательно, должна быть в состоянии ингибировать рост микроорганизмов, таких как бактерии или грибки. Может быть введена единичная внутривенная или внутрибрюшинная доза. Альтернативно, может быть использована медленная длительная инфузия или многократные краткосрочные ежедневные инфузии, обычно длящиеся от 1 до 8 дней. Можно также применять прием через день, или дозирование один раз каждые несколько дней.
Стерильные инъецируемые растворы получают включением соединения в необходимом количестве в один или более соответствующих растворителей, к которым при необходимости могут быть добавлены другие ингредиенты, упомянутые выше или известные специалистам в данной области техники. Стерильные инъецируемые растворы получают включением соединения в необходимом количестве в соответствующий растворитель при необходимости с различными другими ингредиентами. Затем следуют методики стерилизации, такие как фильтрация. Как правило, дисперсии получают включением соединения в стерильный наполнитель, который также содержит дисперсионную среду и необходимые другие ингредиенты, как показано выше. В случае стерильного порошка, к которому добавляют любые необходимые ингредиенты, предпочтительные способы включают вакуумную сушку или лиофильную сушку.
Отмечено, что во всех случаях окончательная форма должна быть стерильной и должна легко проходить через устройство для инъекции, такое как полая игла. Соответствующая вязкость может быть достигнута и поддерживаться с помощью подходящего выбора растворителей или эксципиентов. Кроме того, может быть приенено использование молекулярных или в форме частиц покрытий, таких как лецитин, соответствующий выбор размера частиц в дисперсиях или использование материалов со свойствами поверхностно-активных веществ.
Предотвращение или ингибирование роста микроорганизмов может быть достигнуто с помощью добавления одного или более антибактериальных агентов, таких как хлорбутанол, аскорбиновая кислота, парабены, тимеросал или подобные. Может также быть предпочтительно включение агентов, которые изменяют тоничность, такие как сахара или соли.
В некоторых случаях, например, где соединение изобретения представляет собой совершенно нерастворимое в воде, может быть целесообразно обеспечить липосомальную доставку. Система ограничивает соединение изобретения введением, инкапсулированием, окружением или включением соединения изобретения в, на или рядом с липидными везикулами, или липосомами, или мицеллами.
В одном или более вариантах осуществления настоящего изобретения настоящее изобретение относится к способам лечения различных форм рака, злокачественных опухолей и/или предраковых состояний или предшественников злокачественных опухолей. Способ может включать лечение рака или злокачественной опухоли у пациента введением соединения или композиции, содержащей соединение настоящего изобретения. Способ может включать введение эффективного количества соединения или композиции, содержащей соединение настоящего изобретения, для лечения рака или злокачественной опухоли, в котором рак или злокачественная опухоль поддаются лечению, используя соединение или композицию, содержащую соединение настоящего изобретения. Ниже дополнительно описано, что различные раковые образования и злокачественные опухоли можно лечить с помощью настоящего изобретения. Соединения настоящего изобретения эффективны при лечении у человека или животных раковых образований, злокачественных опухолей, неоплазм или предраковых состояний. Определенные примеры включают, но не ограничиваются, лейкемию, меланому, рак печени, молочной железы, колоректальный, ректальный, яичника, предстательной железы, желудка, мочевого пузыря, десмопластическую мелкокруглоклеточную опухоль (DSRCT), рак поджелудочной железы, легких, почек, толстой кишки, опухоли центральной нервной системы или их любую комбинацию. Используемый в настоящем описании термин «злокачественная опухоль» предназначен охватить все формы карцином человека или животных, сарком и меланом, которые встречаются в плохо дифференцированных, умеренно дифференцированных и хорошо дифференцированных формах.
Другая важная особенность соединений настоящего изобретения относится к сравнительно низкой или отсутствию очевидной общей токсичности пролекарств, которые вводят в соответствии с идеей настоящего описания. Общая токсичность может быть оценена, используя различные критерии. Например, потерю веса тела объекта более 10% от первоначально зарегистрированного веса тела (то есть перед лечением) можно рассмотреть как один из признаков токсичности. Кроме того, как свидетельство токсичности может также быть интерпретирована потеря общей подвижности и активности и признаки диареи или цистита у объекта.
Кристаллические гидраты алифатических сложных эфиров СРТ демонстрируют широкий спектр активности без заметной токсичности у мышей при различных диапазонах дозы. Терапевтический индекс может быть определен с помощью тестирования на голых мышах, такой как средний терапевтический индекс из испытания на мышах, имеющих ксенотрансплантат опухоли, который представляет собой опухоль мочевого пузыря, молочной железы, толстого кишечника, почки, легкого, меланому, поджелудочной железы, предстательной железы, яичника и/или любое из раковых образований, упомянутых в настоящем описании. Дополнительно терапевтический индекс этого агента значительно улучшен по сравнению с большинством противораковых агентов, клинически используемых в настоящее время онкологами. Терапевтический индекс кристаллических гидратов алифатических сложных эфиров СРТ может находиться в интервале от 2 до 500 (например, от 3 до 500, от 4 до 50, от 3 до 10, от 4 до 15, от 5 до 20, от 8 до 20, от 10 до 20, от 25 до 500, от 50 до 500, от 75 до 500, от 100 до 500, от 150 до 500, от 200 до 500, от 250 до 500, от 300 до 500, от 350 до 500, от 400 до 500, от 450 до 500), при этом полагают, что 2000 мг/кг представляет собой наиболее допустимую дозу. Терапевтический индекс для большинства противораковых агентов, используемых в настоящее время в клинической онкологии, однако, представляет собой приблизительно 1, что является очень узким. Дополнительно, ни один из используемых в настоящее время противораковых агентов невозможно непрерывно применять в течение длительного периода в эффективной дозе. Соединения настоящего изобретения можно непрерывно использовать ежедневно, или еженедельно, или ежемесячно в течение 2 месяцев, от 3 месяцев до 12 месяцев, от 4 месяцев до 15 месяцев, от 5 месяцев до 15 месяцев, от 6 месяцев до 24 месяцев или более.
Согласно различным вариантам осуществления, гидраты кристаллических алифатических сложных эфиров СРТ могут быть введены совместно с фармацевтически приемлемыми носителями или разбавителями. Например, такие фармацевтические композиции могут стандартно содержать, например, фармацевтически приемлемые соли, буферные агенты, консерванты и/или совместимые носители. Как используют в настоящем описании, «фармацевтически приемлемый носитель» относится к одному или более совместимым твердым или жидким наполнителям, разбавителям или инкапсулированным веществам, которые являются подходящими для введения млекопитающим, включая людей. Фармацевтически приемлемый носитель может быть, например, одной или более желатиновыми капсулами, холестериновыми гранулами, микросуспензиями в липиде и в липидоподобных эмульсиях (Интралипид 10, Интралипид 20 или природные масла) или в других подходящих эмульгаторах для липофильных соединений. Количество активного ингредиента (кристаллические гидраты алифатических сложных эфиров СРТ), содержащееся в фармацевтической композиции согласно изобретению, может варьироваться в зависимости от многих факторов, таких как путь введения и типы мишеней (например, типы рака), соединения, которые используют.
При лечении или задерживании роста злокачественных опухолей у млекопитающих, в соответствии с настоящим изобретением вводят соединения или фармацевтические композиции настоящего изобретения с помощью способов, известных специалистам в данной области техники, таких как внутримышечное, внутривенное, трансдермальное или пероральное введение. Обычно можно применять известные способы, например, желатиновые капсулы для перорального введения, а также составы, такие как микросуспензии в липиде и в липидоподобных эмульсиях (например, Интралипид 20, хлопковое масло и арахисовое масло) для внутримышечного введения и включения в холестериновые гранулы для подкожного длительного введения. Другой способ введения соединений настоящего изобретения представляет собой трансдермальный или чрескожный путь. Один пример такого варианта осуществления представляет собой использование пластыря. В частности, пластырь может быть получен с высокодисперсной суспензией соединения, раскрытого в настоящей заявке, например, в диметилсульфоксиде (ДМСО) или смеси ДМСО с хлопковым маслом, и привести в соприкосновение с кожей опухоли млекопитающего от местоположения опухоли внутрь в кожный мешочек. Другие среды или их смеси с другими растворителями и твердыми носителями работали бы одинаково хорошо. Пластырь может содержать гидрат СРТ настоящего изобретения в форме раствора или суспензии. Пластырь может затем быть применен к коже пациента, например, посредством вставки его в кожный мешочек пациента, образованный складыванием и скреплением кожи вместе посредством стежков, зажимов или других удерживающих приспособлений. Этот мешочек следует использовать таким способом, чтобы гарантировать непрерывный контакт с кожей без вмешательства млекопитающего. Помимо использования кожного мешочка может быть применено любое приспособление, которое гарантирует устойчивое размещение пластыря при соприкосновении с кожей. Например, можно применять лейкопластырь, чтобы удерживать пластырь в соответствующем месте на коже.
Используемое в настоящем описании «эффективное количество» соединений настоящего изобретения предназначено обозначать количество соединения, которое будет ингибировать рост, или замедлять рак, или уничтожать злокачественные клетки и вызывать регресс и ослабление злокачественных опухолей, то есть уменьшать объем или размер таких опухолей или устранять опухоль полностью.
Эффективные количества могут быть введены млекопитающим, включая людей, исходя из площади поверхности тела. Взаимозависимость дозировок изменяется для животных различных размеров и видов и для людей (основываясь на мг/м2 поверхности тела) описана E.J. Freireich et al., Cancer Chemother. Rep., 50(4): 219 (1966). Площадь поверхности тела может быть приблизительно определена из роста и веса объекта (см., например, Scientific Tables, Geigy Pharmaceuticals, Ardsley, N.Y. pp.537-538 (1970)). Эффективное количество соединений камптотецина в настоящем изобретении может располагаться от приблизительно 10 до приблизительно 1000 мг/м2 поверхности тела в день.
Предпочтительные эффективные количества или дозировки соединений или пролекарств настоящего изобретения представляют собой от приблизительно 1 до приблизительно 100 мг пролекарства/кг веса тела два раза в неделю при внутримышечном пути введения и от приблизительно 1 до приблизительно 500 мг пролекарства/кг/день при пероральном пути введения. Эффективные количества или дозировки производных СРТ или пролекарств настоящего изобретения представляют собой, например, от приблизительно 1 мг/кг/неделю до приблизительно 100 мг/кг/неделю пролекарства при трансдермальном пути введения. Для всех путей введения точный выбор времени введения дозировок может быть различен для достижения оптимальных результатов. Как правило, при использовании Интралипида 20 в качестве носителя для пролекарства фактическая дозировка пролекарства, достигающая пациента, будет меньше. Это происходит вследствие некоторой потери пролекарств на стенках шприцов, игл и емкостей лекарственного средства, которая является распространенной в случае суспензии Интралипида 20. Когда используют носитель, такой как хлопковое масло, эта вышеописанная потеря не настолько ощущается, потому что пролекарство так сильно не прилипает к поверхности шприцов, игл, емкостей лекарственного средства и подобному. Например, предпочтительно, было обнаружено, что, как правило, приблизительно 2,5 мг пролекарства/кг веса тела два раза в неделю, используя хлопковое масло, которое вводят внутримышечным путем, будет доставлять то же самое количество пациенту как 4,0 мг пролекарства/кг веса тела два раза в неделю, используя Интралипид 20 в качестве носителя. Обычно от приблизительно 1 мг до приблизительно 4 мг пролекарства добавляют к от приблизительно 0,1 мл до приблизительно 1 мл носителя.
В одном или более вариантах осуществления настоящего изобретения одно или более соединений настоящего изобретения (или композиция, содержащая соединение(я) настоящего изобретения) могут быть растворимыми в липосомах. Липосомы могут включать, например, липиды, такие как холестерин, фосфолипиды или мицеллы, состоящие из поверхностно-активного вещества, такого как, например, додецилсульфат натрия, октилфенолполиоксиэтиленгликоль или сорбитан моноолеат. Как правило, пролекарства связываются с липидным бислоем мембраны липосомы с высокой аффинностью. Пролекарство, связанное с липосомой, может предпочтительно вставляться между ацильными цепями липида. Лактонное кольцо производного камптотецина, пролекарство, связанное с мембраной, таким образом удалено от водной окружающей среды внутри и снаружи липосомы и таким образом защищено от гидролиза. Так как лекарственное средство, связанное с липосомой, защищено от гидролиза, противоопухолевая активность лекарственного средства сохраняется. Для пролекарств камптотецина, которые имеют более низкую аффинность с мембраной липосомы и таким образом отделяются от мембраны липосомы, чтобы находится внутри липосомы, pH внутренней части липосом можно уменьшить, таким образом предотвращая гидролиз пролекарств камптотецина.
Группа липосомальных систем доставки, которая может быть использована в соответствии с настоящим изобретением, включает описанные в патентах США №№5552156 и 5736156, которые включены в настоящее описание полностью посредством ссылки. Другие липосомальные системы доставки, которые можно использовать в соответствии с настоящим изобретением, включают липосомы, содержащие активные агенты, соединенные с липидами или поверхностно-активными веществами, как описано в патентах США №№5827533 и 5882679; липидные везикулы, образованные с солями жирных кислот алкиламмония, как описано в патенте США №5874105; липосомы для инкапсулирования композиций сухого порошка активного агента, как описано в патенте США №5783211; липосомальные системы доставки лекарственного средства для локальных пластырей, как описано в патенте США №5718914; липосомы, описанные в патенте США №5631237; композиции липосом и липидных комплексов, описанные в патентах США №№5549910 и 5077057; липосомы, используемые для пролонгированного высвобождения стероидных лекарственных средств, как описано в патенте США №5043165; липосомы, описанные в патенте США №5013556; и липосомы, описанные в патенте США №4663161; все из которых включены в настоящее описание во всей их полноте посредством ссылки.
Однослойные липосомы, также называемые единичными однослойными везикулами, представляют собой сферические везикулы, состоящие из мембраны одного липидного бислоя, которая определяет закрытое пространство. Мембрана бислоя составлена из двух слоев липидов; внутреннего слоя и внешнего слоя. Внешний слой молекул липида ориентирован частями их гидрофильных головок во внешнюю водную среду и их гидрофобными хвостами во внутреннюю часть липосомы. Внутренний слой липида лежит непосредственно ниже внешнего слоя; липиды ориентированы их головками в водную внутреннюю часть липосомы и их хвостами к хвостам внешнего слоя липида.
Многослойные липосомы, также называемые многослойными везикулами, составлены из более, чем одного липидного бислоя мембраны, мембраны которого определяют более одного закрытого пространства. Мембраны представляют собой концентрически устроенные таким образом, чтобы различные мембраны отделяли пространства подобно луковой кожуре.
Используемая в настоящем описании фраза «липосомальные пролекарства» обозначает, что или некоторая часть, или все пролекарство камптотецина расположены в одной или более частях липосомы или мицеллы, или пролекарство камптотецина связано с мембраной липосомы. Системы доставки могут быть липосомой, включающей мембрану липидного бислоя, которая окружает пролекарство камптотецина. Используемая в настоящем описании фраза «связанный с липидной мембраной» обозначает, что по меньшей мере лактонное кольцо некоторой части или всего пролекарства камптотецина связано с липидной мембраной липосомы, и где липосома содержит более одной мембраны бислоя, пролекарство камптотецина связано по меньшей мере с 1 мембраной. Те пролекарства камптотецина, которые имеют высокую аффинность к такой мембране, имеют тенденцию оставаться связанными с мембраной. Пролекарства камптотецина с низкой аффинностью к мембране липосомы по меньшей мере будут частично отделяться от мембраны липосомы и оставаться в пространстве липосомы.
В настоящем описании определено, что мицеллы представляют собой сферические емкости, состоящие из монослоя мембраны, которая определяет закрытое пространство, и мембрана состоит из молекул поверхностно-активного вещества, ориентированных таким образом, что углеводородные хвосты направлены к закрытому пространству, а полярные головки ориентированы к внешней водной среде. Пролекарства камптотецина при связывании с мицеллами находятся или в пространстве связанными с мембраной мицеллы, или связанными с внешней поверхностью мицеллы.
Липосомы успешно применяли для введения лекарственных средств больным раком, и было показано, что они являются клинически подходящими при доставке противораковых лекарственных средств, таких как доксорубицин, даунорубицин и комплексы цисплатина. Forssen, et al., Cancer Res. 1992, 52: 3255-3261; Perez-Soler, et al. Cancer Res. 1990, 50: 4260-4266; и Khokhar, et al. J. Med. Chem. 1991, 34: 325-329, все из которых включены в настоящее описание во всей их полноте посредством ссылки.
Подобным образом мицеллы также применяли для доставки лекарственных средств пациентам (Brodin et al., Acta Pharm. Suec. 19 267-284 (1982)) и мицеллы применяли в качестве носителей лекарственных средств и для направленной доставки лекарственных средств (D. D. Lasic, Nature 335: 279-280 (1992); и Supersaxo et al., Pharm. Res. 8: 1286-1291 (1991)), включая противораковые лекарственные средства (Fung et al., Biomater. Artif. Cells. Artif. Organs 16: 439 et. seq. (1988); и Yokoyama et al., Cancer Res. 51: 3229-3236 (1991)), все из которых включены в настоящее описание во всей их полноте посредством ссылки.
Липосомы и/или мицеллы настоящего изобретения, содержащие пролекарства камптотецина, могут быть введены больному раком обычно внутривенно. Липосомы и/или мицеллы проносятся кровеносной системой к раковым клеткам, где мембрана везикулы соединяется с мембраной раковой клетки, таким образом высвобождая пролекарство камптотецина в раковую клетку, или где липосомы и/или мицеллы остаются смежными с раковыми клетками, пролекарство камптотецина диффундирует от липосом и/или мицелл для попадания в раковые клетки.
Любой липид или смесь липидов, которые образуют липосомы и/или мицеллы, представляют собой подходящие для применения в настоящем изобретении. Подходящими являются фосфатидилхолины, включая, например, L-α-димиристоилфосфатидилхолин (DMPC), L-α-дипальмитоилфосфатидилхолин (DPPC) и L-α-дистеароилфосфатидилхолин (DSPC). Также подходящими являются фосфатидилглицерины, включая, например, L-α-димиристоилфосфатидилглицерин (DMPG). DMPC и DMPG, оба находятся в жидкой фазе при 37°C, в то время как DSPC находится в твердой фазе при 37°C. Учитывая, что присутствие отрицательно заряженного липида в мембране липосомы заставляет липосомы отталкиваться друг от друга, небольшие количества, такие как, например, приблизительно 10%, отрицательно заряженного липида, такого как дистеаролфосфатидилглицерин (DSPG), могут включить в липосомы DSPC. Другие подходящие фосфолипиды включают: фосфатидилэтаноламины, фосфатидилинозитолы и фосфатидные кислоты, содержащие лауриновую, миристиновую, пальмитиновую, гексадециновую, стеариновую, олеиновую, линолевую, арахидоновую, бегеновую и лигноцериновую кислоты. Другой подходящий липид включает холестерин.
Липосомы и/или мицеллы могут быть покрыты полиэтиленгликолем или белком GM1, который помогает частицам избежать ретикулоэндотелиальной системы.
DSPC, поскольку находится в твердой фазе при 37°C (средняя температура людей), ограничивает распространение лекарственного средства камптотецина от липосомы и, таким образом, может использоваться для замедленного высвобождения пролекарства камптотецина.
DMPG, DPPC и DSPC могли получить от Avanti Polar Lipids, Alabaster, Ala. и применить без дополнительной очистки. Все другие химические соединения могут быть химически чистыми и применяться без дополнительной очистки.
Любое поверхностно-активное вещество, или его смеси, которое образует мицеллы, является подходящим для применения в настоящем изобретении. Подходящие поверхностно-активные вещества включают додецилсульфат натрия (ДСН), доступный от Kodak, Rochester, N.Y., октилфенолполиоксиэтиленгликоль, доступный под торговой маркой «Тритон X-100» от Aldrich Chemical Co., Milwaukee, Wis., и сорбитан моноолеат, доступный под торговой маркой «Полисорбат 80» и «Твин 80» от Sigma Chemical Co. Другие подходящие поверхностно-активные вещества включают, например, соль натрия дезоксихолевой кислоты, соль натрия холевой кислоты и полиоксиэтилен-10-цетиловый эфир, доступный под торговой маркой «BRIJ-56»; эти поверхностно-активные вещества доступны от Sigma Chemical Co.
Кроме того, мицеллы могут быть составлены из липида, такого как фосфолипид и смеси липидов. Также мицеллы могут быть составлены из липида и поверхностно-активного вещества.
Суспензии липосом могут быть получены с помощью способа Burke and Tritton Biochemistry 24: 1768-1776 (1985), который включен в настоящее описание во всей полноте посредством ссылки. Липосомы представляют собой предпочтительно маленькие однослойные везикулы (SUV), а не многослойные везикулы (MLV). Однако, как SUV, так и MLV находятся в рамках изобретения. В то время как MLV имеют преимущество ограничения скорости диффузии связанного пролекарства камптотецина, они имеют недостаток в том, что более легко удаляются макрофагами, чем SUV. Могут быть использованы суспензии смеси липидов, содержащие 200 мг/мл липида в фосфатно-солевом буферном растворе (PBS), содержащем 8 мМ Na2HPO4, 1 мМ KH2PO4, 137 мМ NaCl и 3 мМ KCl, имеющем pH 7,4, и полученные с помощью вихревого смешивания в течение 5-10 минут выше температуры фазового перехода гель - жидкий кристалл ТМ липида. Суспензии липида затем обрабатывают ультразвуком в течение 3-4 часов, используя ультразвуковые ванны от Laboratory Supplies Co., Hicksville, N.Y., пока они не станут оптически чистыми. Уменьшение pH от 7,4 до 6,8 можно соблюдать для получения SUV лекарственного средства DMPG; следовательно, pH этих суспензий SUV предпочтительно устанавливают до 7,4, используя небольшие количества 2,5 M NaOH в PBS, и снова обрабатывают ультразвуком. Каждый тип суспензии липосом предпочтительно выдерживают в течение 30 минут при 37°C.
Получения многих липосом и мицелл описаны в патентах США №№5552156, 7244449 и 5736156, которые включены в настоящее описание во всей их полноте посредством ссылки.
«Пролекарства» могут быть производными соединениями, полученными добавлением группы, которая обеспечивает бóльшую растворимость соединению, желательному для доставки. Находясь в теле, на пролекарство обычно действует фермент, например, эстераза, амидаза или фосфатаза, для получения активного соединения.
Термин «алкил», один или в комбинации, относится к необязательно замещенной прямой цепи, необязательно замещенной разветвленной цепи или необязательно замещенному циклическому алкильному радикалу, имеющему от 1 до приблизительно 6 углеродов, более предпочтительно, 2-4 углерода. Примеры алкильных радикалов включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, трет-амил, пентил, гексил и подобные. Термин «циклоалкил» охватывает циклические конфигурации, включает определения алкила и главным образом относится к моноциклическим, бициклическим, трициклическим и более полициклическим алкильным радикалам, в которых каждая циклическая часть имеет от 3 до приблизительно 6 атомов углерода. Примеры циклоалкильных радикалов включают циклопропил, циклобутил, циклопентил, циклогексил и подобные.
«Эффективное количество» или «эффективная доза» может относиться к количеству, необходимому или достаточному для ингибирования нежелательного роста клеток, например, предотвращения нежелательного роста клеток или сокращения существующего роста клеток, такого как рост опухолевых клеток. Эффективное количество может варьироваться в зависимости от факторов, известных специалисту в данной области техники, таких как тип роста клеток, способ и режим введения, размер объекта, интенсивность роста клеток и подобные. Специалист в данной области техники в состоянии рассмотреть такие факторы и определить эффективное количество. Это может быть достигнуто с помощью настоящего изобретения.
«Терапевтически эффективная противоопухолевая терапия» может относиться к терапии, которая является эффективной для поддержания или уменьшения размера, например, объема, первичной опухоли или метастатической опухоли. Это может быть достигнуто с помощью настоящего изобретения.
Согласно одному или более вариантам осуществления настоящего изобретения, обеспечивают способы для создания кристаллических гидратов алифатического сложного эфира камптотецина, которые включают стадию реакции исходного соединения камптотецина по меньшей мере с одним ацилирующим агентом, протонированным по меньшей мере одной кислотой, такой как серная кислота. Ацилирующий агент может содержать группу сложного эфира для образования исходного камптотецина. Полученный сложный эфир камптотецина представляет собой кристаллические гидраты алифатического сложного эфира СРТ. По меньшей мере в одном варианте осуществления полученный сложный эфир камптотецина представляет собой кристаллический гидрат камптотецин-20-O-пропионата (гидрат CZ48). Согласно по меньшей мере одному варианту осуществления, исходное соединение камптотецина представляет собой СРТ.
Количество исходного соединения камптотецина может быть любым желательным количеством, пока присутствует достаточный ацилирующий агент для превращения по меньшей мере части исходного камптотецина в сложный эфир камптотецина, как описано в настоящей заявке. Например, количество исходного соединения камптотецина может быть от приблизительно 1 г до 100 г или более.
Что касается ацилирующего агента, ацилирующий агент обычно в одном или более вариантах осуществления содержит группу сложного эфира для получения исходного камптотецина. Ацилирующий агент может быть производным органической кислоты, таким как ангидрид кислоты. Например, ацилирующий агент может иметь формулу (R1CO)2O, в которой R1 представляет собой органическую группу, и обычно группа R1 представляет собой группу, которая является органической частью присоединения сложного эфира к исходному соединению камптотецина. Более детально, и например, только в целях изобретения, группа R1 может быть алкильной группой, такой как C1-C6 алкильная группа. Определенные примеры групп R1 включают, но не ограничиваются, -CH2CH3; -CH2CH2CH3; -CH2CH2CH2CH3; или -CH2CH2CH2CH2CH2CH3.
Количество ацилирующего агента, используемого в реакциях настоящего изобретения, может быть достаточным количеством таким образом, чтобы группа сложного эфира была образована на исходном соединении камптотецина. Подходящие количества ацилирующего агента включают, но не ограничиваются, от приблизительно 10 мл до приблизительно 1 л, исходя из от 20 г до 30 г исходного камптотецина. Примеры, изложенные ниже, обеспечивают типичные количества ацилирующего агента, который может быть использован в реакции.
Что касается кислоты, используемой в реакциях настоящего изобретения, кислота может быть использована в каталитических количествах так, чтобы ацилирование исходного камптотецина могло произойти с производными органических кислот, такими как ангидрид кислоты. Кислота может быть серной кислотой или другими кислотами, такими как HCl, HNO3 или HClO4. Кислота может быть концентрированной кислотой, такой как концентрированная серная кислота. Кислота может иметь любую молярную концентрацию, такую как от приблизительно 0,0001 до приблизительно 0,02 М или выше. Количество кислоты, используемой в реакции, может быть каталитическим количеством, таким как от приблизительно 0,1 мл до приблизительно 1,0 мл и более предпочтительно, от приблизительно 0,20 мл до приблизительно 0,75 мл или приблизительно 0,5 мл на реакцию с от 20 г до 30 г исходного камптотецина. Количество кислоты, используемой для катализа реакции этерификации, может быть различно в зависимости от веса веществ, вовлеченных в реакцию.
В настоящем изобретении, согласно одному или более вариантам осуществления, различные реагенты могут быть объединены вместе в любом порядке или последовательно в то же самое время или в любой комбинации. Может быть применена любая реакционная емкость. Реакция может проходить при любой температуре выше точки замерзания реагентов, такой как от приблизительно 20°C или выше. Реакция может проходить при температурах окружающей среды или повышенных температурах, таких как от приблизительно 20°C до приблизительно 110°C или выше. Реакция может проходить, не затрачивая много времени, например, от 1 минуты до 1 часа или более. Время реакции зависит от количества используемого реагента и желательного количества превращения исходного СРТ в сложный эфир камптотецина. Реакция может проходить в инертных атмосферах или на воздухе. Примером инертной атмосферы может быть атмосфера азота или атмосфера аргона.
Согласно различным вариантам осуществления, выход реакции может быть по меньшей мере от 95% до 100% вес. исходного соединения камптотецина, которое превращают в сложный эфир камптотецина. По меньшей мере в одном варианте осуществления выход реакции представляет собой от приблизительно 97% до 100% превращения соединения камптотецина в сложный эфир камптотецина.
Чистота и/или концентрация исходного СРТ или реагента является несущественной. Различные чистоты и различные концентрации могут влиять на процент выхода сложных эфиров СРТ, которые образуются в ходе реакции. Предпочтительно, чистота исходного реагента СРТ представляет собой от приблизительно 30% до приблизительно 100%. Более предпочтительно, чистота представляет собой от приблизительно 80% до приблизительно 100% или от 90% до 99,9% или выше. Предпочтительно, количество реагентов СРТ или производного СРТ представляет собой от приблизительно 0,1 до приблизительно 50% общего объема реагентов. Более предпочтительно, количество представляет собой от приблизительно 0,5 до приблизительно 5,0% общего объема реагентов.
pH, концентрация и чистота кислоты не представляются важными, поскольку примеси в кислоте не взаимодействуют с СРТ или ацилирующим агентом. Кислотность кислоты должна быть достаточно сильной для протонирования ацилирующего агента, участвующего в реакции. Этой способностью обладают сильные неорганические кислоты, такие как H2SO4, HCl, HNO3 и HClO4. Для этого типа каталитической реакции этерификации могут быть использованы другие кислоты, такие как AlCl3 и BF3. pH кислоты может быть от приблизительно 0,5 до приблизительно 5. Предпочтительно, кислота является концентрированной и высокоочищенной. Например, концентрация может быть от приблизительно 60% до приблизительно 100%. Предпочтительно, концентрация представляет собой от приблизительно 95% до приблизительно 98%. Чистота кислоты может быть от приблизительно 30% до приблизительно 100%. Предпочтительно, чистота представляет собой от приблизительно 90% до приблизительно 100%. Предпочтительно, количество кислоты, такой как концентрированная серная кислота, представляет собой от приблизительно 0,1 до приблизительно 10% общего объема реагентов. Более предпочтительно, количество представляет собой от приблизительно 0,5% до приблизительно 8,5% общего объема реагентов.
Предпочтительно, кислоту добавляют к смеси СРТ и ангидрида кислоты, в то время как смесь перемешивают. Предпочтительно, количество кислоты, которое может быть добавлено к смеси, является достаточным для действия кислоты в качестве катализатора. Предпочтительно, от приблизительно 4 до приблизительно 8 капель кислоты из стеклянной пипетки могут быть добавлены к приблизительно 70-100 мл ацилгалогенида (подобное количество кислоты можно использовать, когда ацилирующий агент отличается от ацилгалогенида). Однако, в случае необходимости, больше или меньше кислоты может быть добавлено к смеси СРТ и ангидрида кислоты, предпочтительно, в то время как смесь перемешивают.
Смесь СРТ, ангидрида кислоты и кислоты может быть помещена в реактор, который, предпочтительно, содержит инертную атмосферу, такую как N2, и может быть нагрет от приблизительно 80°C до приблизительно 120°C. Предпочтительно, смесь нагревают от приблизительно 90°C до приблизительно 110°C, и более предпочтительно, реактор нагревают до приблизительно 100°C.
Предпочтительно, реакция будет протекать до тех пор, пока не образуется желаемый продукт. Время реакции может быть от короткого, как несколько часов, до долгого, как несколько дней. Предпочтительно, время реакции может быть приблизительно 15 часов при инертной атмосфере, такой как N2.
Пример реакции изображен на схеме 1 ниже.
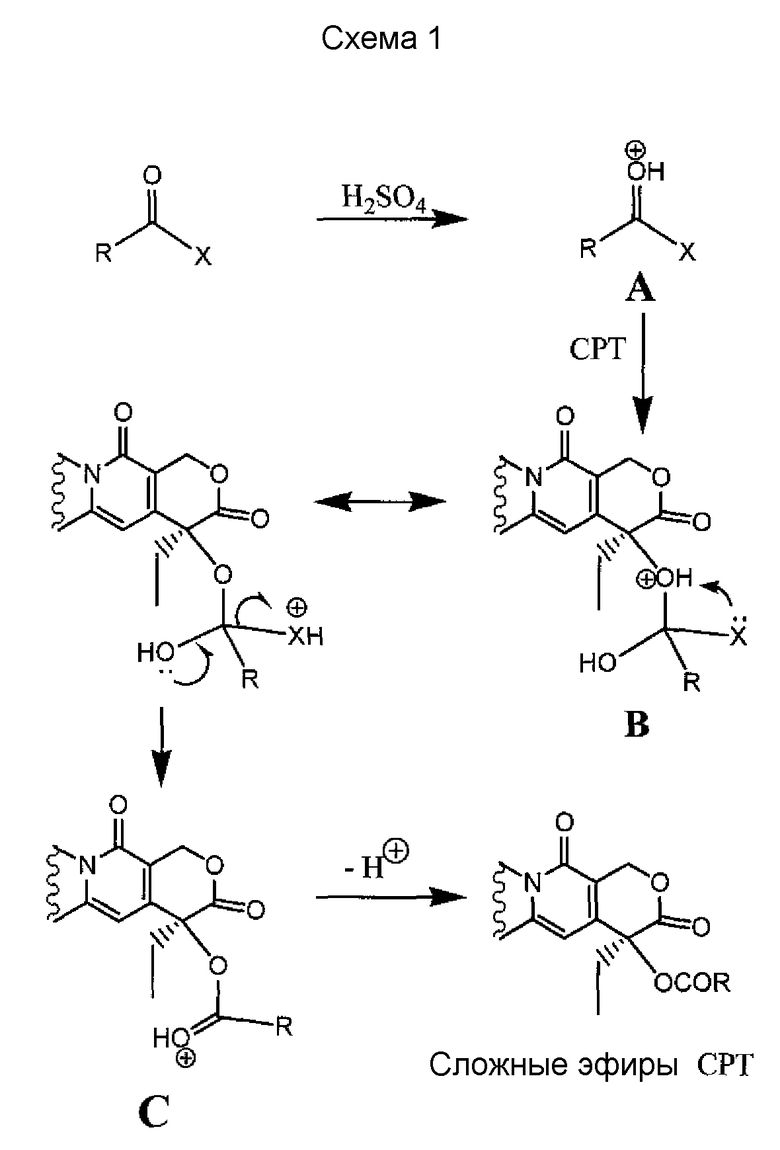
Не желая быть привязанными к любой теории, полагают, что протонирование ацилирующего агента (RCOX) кислотой, такой как серная кислота, образует промежуточное соединение A. Присоединение катионного карбонильного углерода промежуточного соединения А к камптотецину образует промежуточное соединение B. Последующее удаление молекулы ХН из группы B создает окончательные сложноэфирные продукты.
После завершения реакции, которое может быть определено с помощью изменения цвета раствора, раствор может быть охлажден до комнатной температуры. Растворитель может быть удален любыми обычно известными способами разделения, такими как способ выпаривания или способ фильтрации. Неочищенный продукт, полученный после удаления растворителей реакции, может быть очищен с помощью нагревания с обратным холодильником в спиртовых растворителях, таких как этанол. Конечный продукт получают в кристаллической форме после перекристаллизации и/или переосаждения из спирта.
Получали новые сложные эфиры камптотецина со значительно уменьшенной токсичностью, поддерживая противоопухолевую активность, такие как кристаллические гидраты алифатических сложных эфиров СРТ, как кристаллический гидрат камптотецин-20-O-пропионата. Согласно одному или более вариантам осуществления, алифатический сложный эфир СРТ может быть получен с помощью H2SO4-катализируемой реакции ацилирования, изображенной в реакции, как показано ниже:
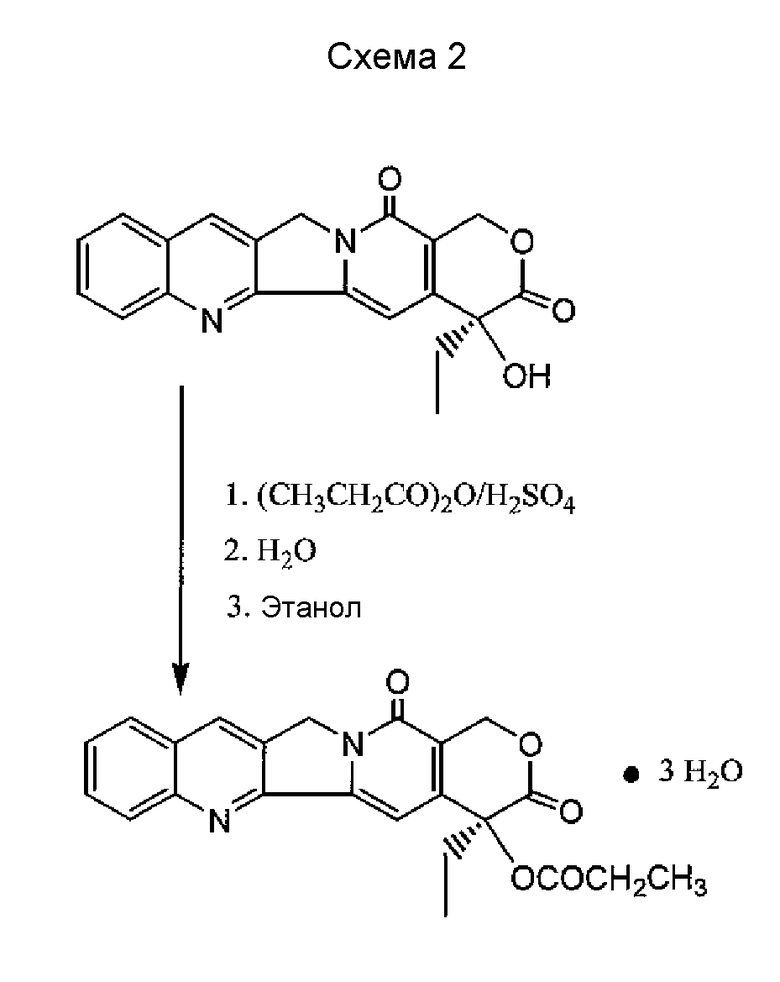
Показано, что исходный камптотецин может взаимодействовать с пропионовым ангидридом при катализации концентратом серной кислоты. Реакционная смесь может затем быть погашена избытком воды для удаления непрореагировавшего пропионового ангидрида и пропионовой кислоты, полученной из реакции. Кристаллизация неочищенного продукта из абсолютного этанола (или других растворителей, как другие спирты) дает окончательный кристаллический гидрат камптотецин-20-O-пропионата в почти количественном выходе. Это также было бы верным для других сложных эфиров СРТ настоящего изобретения. Следует понимать, что фраза «количественный выход», используемая в настоящем описании, может включать выходы 97-100% вес. Чистота продукта, полученного в реакции, представляет собой приблизительно 99-100%. Точка плавления продукта представляет собой приблизительно 240-243°C.
Настоящее изобретение будет дополнительно разъяснено с помощью следующих примеров, которые являются типичными для настоящего изобретения.
ПРИМЕРЫ
Пример 1
Кристаллический гидрат камптотецин-20-пропионата (CZ48) получали следующим образом. Приблизительно 20 г камптотецина (0,05747 моль) и приблизительно 100 мл пропионового ангидрида (97%, Aldrich Chemical Co., Milwaukee, WI) добавляли в 200-мл круглодонную колбу, снабженную магнитной мешалкой и песочной баней. Смесь нагревали с помощью песочной бани, перемешивая. По каплям добавляли несколько капель (от 8 до 10) концентрата серной кислоты (95-98%, реактив A.C.S., Aldrich Chemical Co.), когда температура песочной бани достигала 80°C. Смесь затем перемешивали при 110±10°C в течение ночи (~14 часов). После охлаждения до комнатной температуры, реакционную смесь частями выливали в 1000 мл ледяной воды с перемешиванием. После перемешивания в течение примерно 45 минут, смесь отфильтровывали. Осадок, полученный от фильтрации, высушивали на воздухе в течение 24 часов. Высушенный неочищенный продукт переносили в 500-мл круглодонную колбу, снабженную колбонагревателем.
К этому неочищенному продукту добавляли 200 мл абсолютного этанола (99,5%, 200 proof, Aldrich Chemical Co.). Смесь нагревали с обратным холодильником в течение 2 часов и затем охлаждали до комнатной температуры. Чистый продукт получали в качестве кристаллов после кристаллизации из этанола. Было показано, что чистота составляет 99,8%, используя высокоэффективную жидкостную хроматографию (ВЭЖХ), и было определено, что точка плавления (т.пл.) составляет 242°C. Сухой азот обычно применяли в качестве атмосферы реакции во всех реакциях для лекарственных средств. Всю стеклянную посуду подвергали термической обработке при 70±10°C в течение минимум 2 ч прежде, чем использовать. Точки плавления наблюдали с помощью прибора для определения точек плавления MEL - TEMP® и не исправляли. Камптотецин заказывали из Китайской Народной Республики и использовали в таком виде.
Определение противоопухолевой активности in vivo. Опухоли человека, используемые в экспериментах, обсужденных в настоящем описании, включали 1 линию мочевого пузыря, 3 линии молочной железы, 4 линии толстой кишки, 1 линию DSRCT, 1 линию почек, 2 линии меланомы, 2 линии легкого, 7 линий поджелудочной железы и 1 линию предстательной железы. Гидратированное кристаллическое лекарственное средство CZ48 тонко суспендировали в хлопковом масле и хранили в холодильнике в течение использования. Суспензию перорально вводили мышам, имеющим человеческие опухоли, один раз в день непрерывно в течение 5 дней и 2 свободных дня или один раз в день в течение семи дней в течение целого периода лечения. Период лечения для различных линий опухолей изменяли, в пределах от двух недель до одного года. Из этих проверенных линий опухолей 18 линий достигали положительного ответа, другими словами, более 50% ингибирования роста опухоли с режимом 5 дней и 2 свободных дня, и 2 линии опухоли поджелудочной железы не получали положительный ответ. При непрерывном режиме (ежедневное лечение) одна из тех двух линий опухоли поджелудочной железы при режиме 5/2 с отрицательным ответом достигала положительного ответа. Таблица 1 суммирует результаты.
Противоопухолевая активность гидратированного кристаллического CZ48 в отношении человеческих ксенотрансплантатов у голых мышей
b. Отрицательный ответ обозначает ингибирование роста менее чем на 50%.
В то время как положительный ответ определяли при ингибировании роста по меньшей мере 50%, в действительности достигали полного ингибирования роста для многих линий опухоли. Эффективные дозы, необходимые для достижения положительного ответа, варьируются в зависимости от типов опухолей. Для CLO-карциномы молочной железы, самой чувствительной линии опухоли из тестируемого банка опухолей, полное ингибирование достигали с низкой дозой гидратированного кристаллического CZ48, такой как 4 мг/кг, тогда как для достижения положительного ответа для CAK-почки, PANC1-поджелудочной железы и SU86.86-поджелудочной железы, 3 из менее чувствительных линий, требовалась доза такая высокая, как 1000 мг/кг.
Пример 2
Определение противоопухолевой активности in vivo. Все эксперименты на животных проводили на голых швейцарских мышах NIH, штамм с высокой фертильностью. Их кормили и содержали в лаборатории в строгих стерильных условиях. Для определения противоопухолевой активности опухоль ксенотрансплантата, выращенную в голой мыши, размером приблизительно 1 см3 удаляли хирургическим путем в стерильных условиях, тонко измельчали с помощью ножниц для иридэктомии и суспендировали в среде культуры клеток в отношении 1:10 об./об. Одну половину 1 мл этой суспензии, содержащую приблизительно 50 мг измельченной опухоли во влажном состоянии подкожно вводили в верхнюю часть спинной грудной клетки мыши. Использовали группы из четырех или пяти животных. Гидратированный кристаллический CZ48 тонко суспендировали в хлопковом масле и затем вводили в полость желудка мыши через переднюю брюшную стенку, используя иглу 26 размера. Еженедельный режим, используемый для перорального введения гидратированного кристаллического CZ48, представлял собой один раз в день в течение 7 дней, или пять дней и два свободных дня. Этот режим применяли для всех экспериментов на животных. Лечение начинали, когда опухоль достигала объема приблизительно 200 мм3, то есть хорошо васкуляризированная, поддающаяся измерению и выращенная по экспоненте. Опухоли, выращенные у животных, проверяли и измеряли с помощью циркуля один раз в неделю. Эффективные дозы устанавливали, когда достигали положительный ответ у мышей. Результаты показаны в таблице 2.
Эффективные дозы гидратированного кристаллического CZ48 в линиях опухолей
Как показано в таблице 2, кристаллический гидрат камптотецин-20-O-пропионата имеет широкий терапевтический индекс в пределах от 2 для трех устойчивых линий до 500 для самой чувствительной линии (CLO-грудь), если полагают, что 2000 мг/кг является наиболее допустимой дозой.
Пример 3
Определение токсичности in vivo. Группы из 4 или 5 животных приблизительно одинакового возраста и имеющие подобные веса выбирали и лечили с помощью кристаллического гидрата CZ48 перорально с дозами 1500 мг/кг и 2000 мг/кг, соответственно, непрерывно в течение 60 дней. 3 группы мышей, выбранные для исследования токсичности, были здоровы, одинакового возраста и веса и не имели опухолей. Одну группу использовали в качестве контроля, и другие две группы лечили с помощью лекарственного средства при двух уровнях высокой дозы 1500 мг/кг и 2000 мг/кг соответственно, в течение приблизительно двух месяцев. Изменения веса тела животных в течение лечения регистрировали для группы, которую лечат, относительно группы, которую не лечат, начиная с 0 дня и заканчивая в 60-й день. Результаты показаны в таблице 3.
Токсичность кристаллического гидрата CZ48 у голых мышейа
(1,5 г/кг)b
(2,0 г/кг)b
b. Числа в круглых скобках представляют собой среднеквадратичные отклонения (SD).
Наиболее поразительно, что никакой значимой токсичности у мышей, которых лечат, не наблюдали ни в одном из тестируемых уровней дозы. Потерю веса тела применяли в качестве параметра для измерения токсичности агента. Обычно потерю веса тела 10% или более у мышей в течение лечения считают признаком токсичности. Более значительная потеря веса тела показывает бóльшую токсичность. Лечение не приводило к существенной потере веса тела, которое подразумевало, что применяемые уровни дозы были нетоксичны для мышей и также, что мыши могли переносить дозы еще выше, чем 2000 мг/кг. Непрерывное лечение мышей с помощью кристаллического гидрата камптотецин-20-O-пропионата проявляло более широкий диапазон терапевтического индекса и не приводило ни к какой значимой токсичности.
Пример 4
Определение ФК параметров кристаллического гидрата CZ48. Фармакокинетический профиль кристаллического гидрата камптотецин-20-O-пропионата с единичной дозой 2000 мг/кг регистрировали после перорального введения голым мышам. Соответствующие Cmax и Tmax были 284,86±85,55 нг/мл и 2,0±0,0 ч, соответственно. Камптотецин-20-O-ацетат, аналог CZ48, который не представлял собой кристаллический гидрат, применяли в качестве внутреннего стандарта для определения всех ФК параметров гидрата CZ48. 100 мкл плазмы мыши обрабатывали с помощью кристаллического гидрата CZ48 в дозе 2000 мг/кг, переносили в 2-мл пробирку, и затем 100 мкл рабочего раствора внутреннего стандарта (400 нг/мл) также добавляли в пробирку. К смеси также добавляли 200 мкл 1%-ного раствора уксусной кислота и 1 мл этилового эфира. После вихревого смешивания в течение 10 с, смесь выдерживали при комнатной температуре на шейкере в течение 10 минут и затем центрифугировали при 10000×g в течение 15 минут. Верхний слой, полученный при центрифугировании, переносили в чистую пробирку и выпаривали досуха, используя испаритель, при 40°C в потоке азота. Осадок растворяли в 200 мкл системы растворителей вода/ацетонитрил (50/50, об./об.) и 20-мкл аликвоту вводили в систему ВЭЖХ для анализа. Для исследования 100 мкл плазмы мыши, которая не подвергалась лечению, обрабатывали тем же способом, как и подвергавшуюся лечению. Важные ФК параметры гидрата CZ48 и СРТ на 48 мышах были получены из анализа ВЭЖХ и показаны в таблице 4.
Фармакокинетические параметры гидратированного кристаллического CZ48 и его основного метаболита СРТ у мышей после перорального введения дозы 2000 мг/кг
Пример 5
Определение процентного соотношения абсорбции кристаллического гидрата CZ48 у мыши. Исследования абсорбции также проводили с кристаллическим гидратом камптотецин-20-O-пропионата при использовании методики перфузии мышей на 4 голых мышах. Перед началом методики проведения однократной перфузии in situ готовили буфер HBSS (pH 7,4), состоящий из 9,801 г/л порошков HBSS, 0,372 г/л NaHCO3, 3,502 г/л глюкозы, 5,963 г/л HEPES и 1,164 г/л NaCl, и хранили в холодильнике. Перфузат для методики получали, смешивая определенное количество лекарственного средства, кристаллического гидрата CZ48 с количеством буфера HBSS. Смесь нагревали до 37°C (температура тела) прямо перед применением. Группу из 4 мышей с весом в пределах от 25 до 30 граммов и возрастом в пределах от 9 до 11 месяцев анестезировали и помещали на нагревательную пластину. На пластине поддерживали постоянную температуру 37°C. После установки готовой перфузионной системы с мышью, две части кишечника (тонкая кишка, IS (in situ), и толстая кишка) одновременно перфузировали свежеприготовленным перфузатом. Насос поддерживали при постоянной скорости потока 0,191 мл/мин в течение всей перфузии. Два образца перфузата забирали из каждого выхода (тонкая кишка (SI) или толстая кишка) каждые 30 минут. Концентрации лекарственного средства в перфузате на выходах определяли с помощью ВЭЖХ анализа, и соответствующие процентные соотношения абсорбций вычисляли относительно исходного количества лекарственного средства, и результаты показаны в таблице 5.
Результаты перфузии желудочно-кишечного тракта у мышей
В таблице 5 показано, что значительные абсорбции происходили в тонкой кишке. Отрицательные значения процентного отношения абсорбции, зарегистрированные для толстой кишки, указывают, что количество лекарственного средства, выходящее из толстой кишки, было больше, чем количество, первоначально помещенное в ротовое отверстие двенадцатиперстной кишки мыши. Это можно объяснить накоплениями лекарственного средства в толстой кишке вследствие многократных циклов абсорбция/отток.
Определение кристаллической структуры кристаллического гидрата CZ48. Рентгеноструктурный анализ монокристалла проводили при использовании дифрактометра Siemens SMART, снабженного индикатором площади, управляемым компьютером. Кристалл с размерами 0,4×0,08×0,02 мм помещали в стекловолокно в потоке холодного газа азота при -60°C. Монохроматическое излучение Мо Kα1 (λ=0,71073 Å) применяли для сбора всех полусферических данных с помощью метода узкого кадра. Данные объединяли, используя программу Siemens SAINT, и интенсивности корректировали для фактора Лоренца, поляризации, абсорбции воздуха и абсорбции вследствие изменения длины траектории. Применяли эмпирические поправки и усредняли чрезмерные отклонения. Окончательные параметры клетки уточняли, используя отклонения 1971, имеющие I>10 σ(I). Параметры тетрагональной ячейки представляют собой а=15,008(2) Å, b=6,977(1) Å, c=21,810(3) Å, β=99,959°, V=2249,2(5) Å3, Z=4, ρ=1,354 г/см3, 2θmax=56,66°. Структуру решали прямыми способами с пространственной группой P21 (№4) и уточняли с помощью полноматричного вычисления методом наименьших квадратов F2, тепловое движение всех C, N, O атомов рассматривали анизотропически. Окончательные R показатели [I>2σ(I)], R1=0,0454, wR2=0,0763, R показатели [все данные], R1=0,1105, wR2=0,0933. Все вычисления выполняли с использованием пакета программ Siemens SHELXTL. Данные о кристалле и уточнение структуры для [C23H20N2O5]·3H2O показаны в таблице 7. Атомные координаты (×104) и эквивалентные параметры изотропного смещения (Å2×103) для [C23H20N2O5]·3H2O показаны в таблице 8. Длины связи [Å] и углы [°] для [C23H20N2O5]·3H2O показаны в таблице 9. Параметры анизотропного смещения (Å2×103) для [C23H20N2O5]·3H2O показаны в таблице 10.
Данные о кристалле и уточнение структуры для [C23H20N2O5]·3H2O
Атомные координаты (×104) и эквивалентные параметры изотропного смещения (Å2×103) для [C23H20N2O5]·3H2O
Длины связи [Å] и углы [°] для [C23H20N2O5]·3H2O
Параметры анизотропного смещения (Å2×103) для [C23H20N2O5]·3H2O
-2π2[h2a*2U11+…+2hka*b*U12]
Из этих исследований очевидно, что соединения настоящего изобретения демонстрируют поразительный уровень противораковой активности. Это можно применить как к спектру исследуемых опухолей, так и к качеству ответов. Способ настоящего изобретения способен полностью блокировать рост и полностью регрессировать ксенотрансплантаты карцином человека (например, легких, молочной железы, толстой кишки, желудка, поджелудочной железы, мочевого пузыря, предстательной железы, остеосаркому и яичников) и злокачественных меланом. Это было достигнуто без любой наблюдаемой токсичности. Многие из млекопитающих, которых непрерывно лечили в течение шести месяцев, не показали ни отрицательных эффектов, ни возобновления роста опухоли, которая у них когда-то была. Гидратированные кристаллические алифатические сложные эфиры настоящего изобретения все должны иметь одинаковую степень эффективности и величины терапевтического индекса.
Заявители определенно включают полное содержание всех процитированных ссылок в раскрытии данной заявки. Дополнительно, когда количество, концентрацию или другую величину или параметр показывают в качестве или диапазона, предпочтительного диапазона, или списка верхних предпочтительных величин и нижних предпочтительных величин, следует понимать как особым образом раскрытие всех диапазонов, образованных из любой пары любого верхнего предела диапазона или предпочтительной величины и любого низшего предела диапазона или предпочтительной величины, независимо от того, раскрыты ли диапазоны отдельно. В случае, если диапазон числовых величин перечислен в настоящем описании, если иначе не заявлено, полагают, что диапазон включает его конечные точки, и все целые числа и дроби в пределах диапазона. Полагают, что возможности изобретения не ограничены определенными величинами, перечисленными при определении диапазона.
Другие варианты осуществления настоящего изобретения будут очевидны специалистам в данной области техники из рассмотрения настоящей спецификации и практики настоящего изобретения, раскрытого в настоящем описании. Полагают, что настоящая спецификация и примеры рассматриваются как образцовые только с настоящим объемом и сущностью изобретения, обозначенными в соответствии со следующей формулой изобретения и ее эквивалентами.
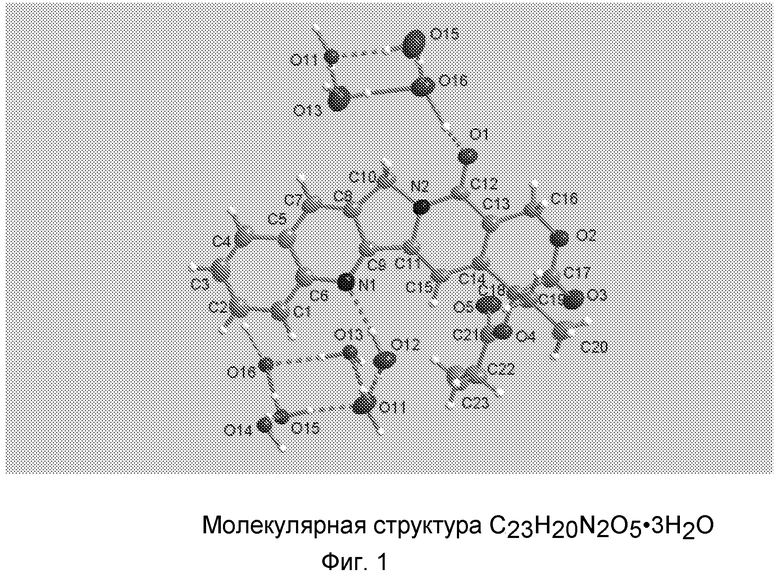
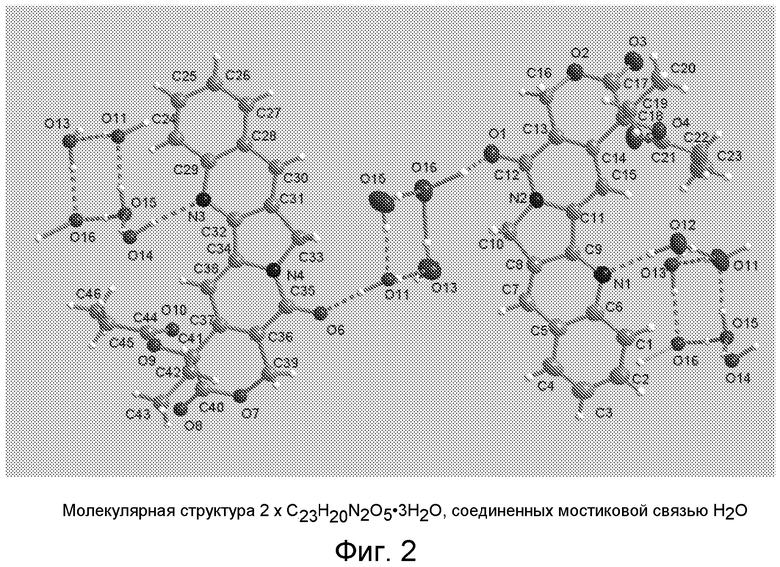
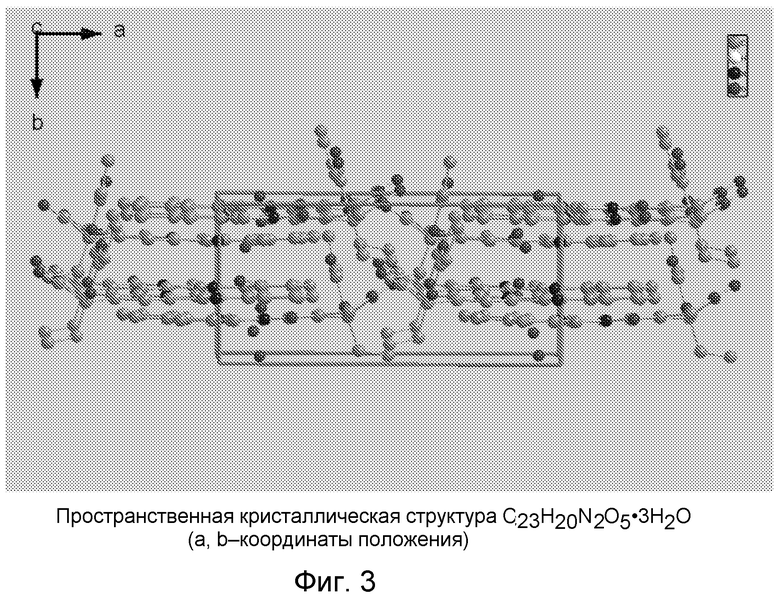
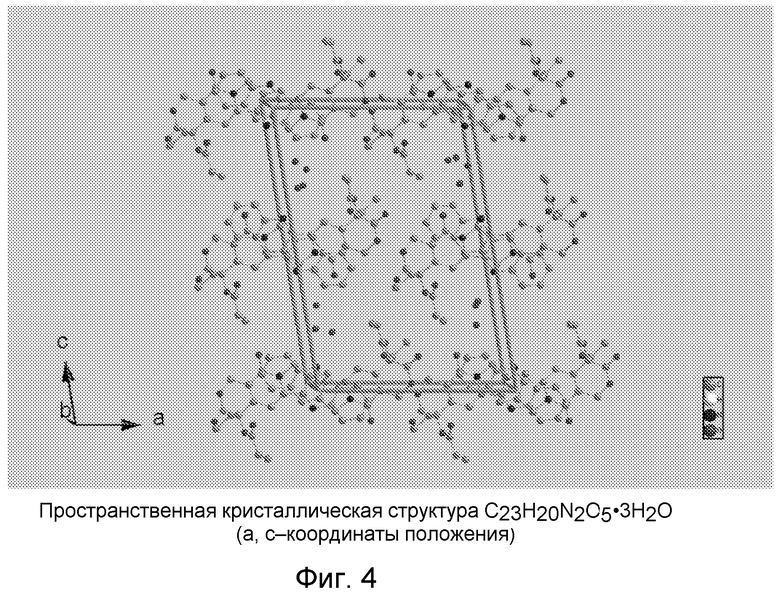
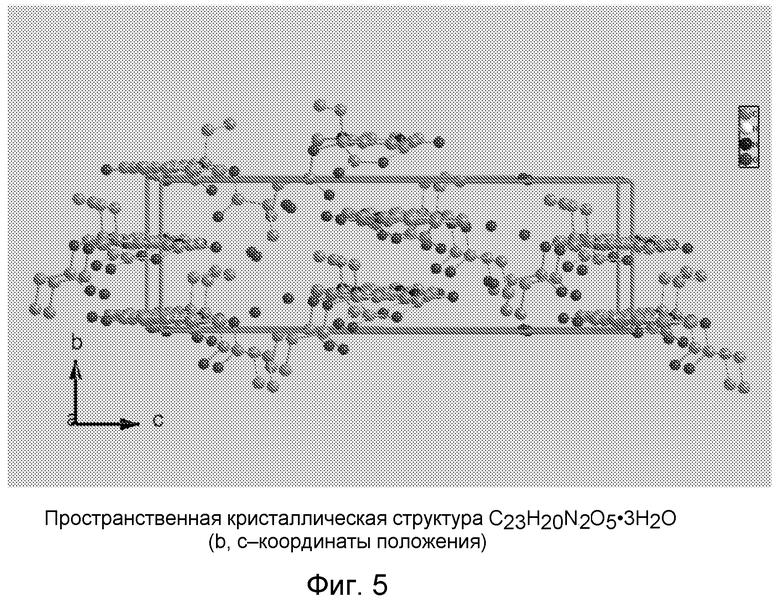
Изобретение описывает кристаллический гидрат сложных эфиров камптотецина, а именно кристаллические гидраты алифатических сложных эфиров камптотецина, фармацевтическую композицию, содержащую кристаллические гидраты алифатических сложных эфиров камптотецина, для лечения рака или злокачественной опухоли, а также способ лечения рака или злокачественной опухоли. Технический результат: получена и описана новая кристаллическая форма гидрата алифатического сложного эфира камптотецина, обладающая низкой токсичностью и хорошей поглотительной способностью в живом организме. 3 н. и 16 з.п. ф-лы, 5 прим., 10 табл., 5 ил.
1. Кристаллический гидрат камптотецина формулы (I):
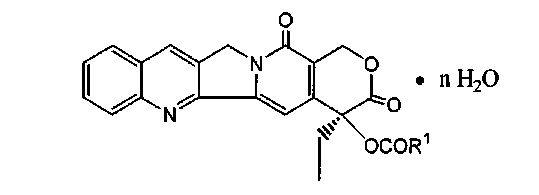
в которой n включает число в пределах от 1 до 10, и R1 представляет собой С2-С6алкильную группу.
2. Кристаллический гидрат камптотецина по п.1, в котором R1 представляет собой линейную С2-С4алкильную группу.
3. Кристаллический гидрат камптотецина по п.1, в котором R1 представляет собой этил.
4. Кристаллический гидрат камптотецина по п.3, в котором кристаллический гидрат камптотецина имеет точку плавления от приблизительно 240°С до приблизительно 243°С.
5. Кристаллический гидрат камптотецина по п.3, в котором соединение имеет точку плавления приблизительно 242°С.
6. Кристаллический гидрат камптотецина по п.1, в котором соединение имеет чистоту от приблизительно 99% до приблизительно 100%.
7. Кристаллический гидрат камптотецина по п.1, в котором n включает число в пределах от 1 до 3.
8. Способ лечения рака или злокачественной опухоли у пациента, включающий введение композиции, содержащей эффективное количество кристаллического гидрата камптотецина по п.1, в котором указанный рак или злокачественная опухоль восприимчивы к указанной композиции.
9. Способ по п.8, в котором R1 представляет собой этил.
10. Способ по п.8, в котором указанный рак представляет собой лейкемию, меланому, рак печени, рак молочной железы, рак яичника, рак простаты, рак желудка, рак мочевого пузыря, десмопластическую мелкокруглоклеточную опухоль (DSRCT), рак поджелудочной железы, рак легкого, рак почки, рак толстой кишки или рак центральной нервной системы.
11. Способ по п.10, в котором R1 представляет собой этил.
12. Способ по п.8, в котором кристаллический гидрат камптотецина вводят внутривенно, внутримышечно или трансдермально.
13. Способ по п.8, в котором кристаллический гидрат камптотецина вводят перорально.
14. Фармацевтическая композиция для лечения рака или злокачественной опухоли, включающая эффективное количество кристаллического гидрата камптотецина по п.1 и фармацевтически приемлемого носителя.
15. Фармацевтическая композиция по п.14, в которой носитель представляет собой липид или липидоподобный эмульгатор.
16. Кристаллический гидрат камптотецина по п.1, в котором указанный кристаллический гидрат камптотецина имеет терапевтический индекс от 2 до 500, как определено при введении указанного кристаллического гидрата камптотецина голым мышам, имеющим опухоль ксенотрансплантата, при использовании дозы 2000 мг/кг в качестве самой высокой допустимой дозы.
17. Кристаллический гидрат камптотецина по п.16, в котором указанный терапевтический индекс представляет собой от 10 до 100.
18. Кристаллический гидрат камптотецина по п.1, в котором кристаллический гидрат камптотецина имеет моноклиническую систему с размерами (от 0,10 до 0,50)×(от 0,01 до 0,10)×(от 0,01 до 0,05) мм3 и объемами от 100 до 5000 Å3.
19. Кристаллический гидрат камптотецина по п.18, в котором указанный кристаллический гидрат камптотецина представляет собой кристаллический гидрат камптотецин-20-пропионата.
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| WASHINGTON, vol.41, no.1, 1998 p.31-37 | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2013-05-27—Публикация
2008-10-24—Подача