Область техники, к которой относится изобретение
Изобретение относится к области биотехнологии, фарамакологии и медицины, конкретно к технологии получения выделенных антител, в особенности человеческих антител, которые связываются с IP-10 с высокой аффинностью, на основе которых предложены фармацевтические композиции и способы лечения различных воспалительных и аутоиммунных заболеваний.
Уровень техники
Индуцируемый интерфероном γ белок 10 (IP-10) (известный также как СХСИО) представляет собой хемокин молекулярной массы 10 кД, который исходно идентифицирован на основе экспрессии гена IP-10 в клетках, обработанных интерфероном γ (ИФН-γ) (см. статью Luster A.D. et al., (1985), Nature, 315:672-676). IP-10 демонстрирует гомологию с белками, обладающими хемотаксической активностью, такими как тромбоцитарный фактор 4 и β-тромбоглобулин, и с белками, обладающими митогенной активностью, такими как пептид III активации соединительной ткани (см. статью Luster A.D. et al., (1987), Proc. Natl. Acad. Sci. USA, 84:2868-2871). IP-10 секретируется множеством клеток, включая эндотелиальные клетки, моноциты, фибробласты и кератиноциты, в ответ на ИФН-γ (см. статью Luster A.D. and Ravetch J.V., (1987), J. Exp. Med., 166:1084-1097). Показано также, что IP-10 присутствует в кожных макрофагах и эндотелиальных клетках при реакциях гиперчувствительности замедленного типа (DTH) в коже человека (см. статью KaplanG. et al., (1987), J. Exp. Med., 166:1098-1108). Несмотря на то, что он исходно идентифицирован на основе того, что индуцируется ИФН-α, IP-10 может также индуцироваться ИФН-α, например, в дендритных клетках (см. статью Padovan E. et al., (2002), J. Leukoc. Biol., 71:669-676). Экспрессия IP-10 может быть также индуцирована в клетках центральной нервной системы, таких как астроциты и микроглия, такими стимулами, как ИФН-γ, вирусы и липополисахариды (см. статьи Vanguri R. and Farber J.M., (1994), J. Immunol., 152:1411-1418; Ren L.Q. et al., (1998), Brain Res. Mol. Brain Res., 59:256-263). Обзор иммунологии IP-10 представлен в статье Neville L.F. et al., (1997), Cytokine Growth Factor Rev., 8:207-219.
Рецептор для IP-10 идентифицирован как CXCR3, седьмой трансмембранный рецептор (см. статью Loetscher М. et al., (1996), J. Exp. Med., 184:963-969). Показано, что CXCR3 экспрессируется на активированных Т-лимфоцитах, но не на покоящихся Т-лимфоцитах, или В-лимфоцитах, моноцитах либо гранулоцитах (Loetscher М. et al., см. выше). Показано, что повышающая регуляция экспрессии CXCR3 происходит на NK (натуральных киллерных) клетках при стимуляции TGF-β 1 (фактором роста Т-клеток β 1) (см. статью Inngjerdingen М. et al., (2001), Blood, 97:367-375).
Идентифицированы также два других лиганда для CXCR3: MIG (Loetscher М. et al., см. выше) и ГАС (см. статью Cole K.Е. et al., (1998), J. Exp. Med., 187:2009-2021).
Показано, что связывание IP-10 с CXCR3 опосредует мобилизацию кальция и хемотаксис в активированных Т-клетках (Loetscher M. et al., см. выше). Хемотаксис и мобилизация внутриклеточного кальция индуцируются также связыванием IP-10 с CXCR3 на активированных NK-клетках (см. статью Maghazachi A.A. et al., (1997), FASEB J., 11:765-774). В тимусе IP-10, как показано, является хемоаттрактантом для Т-клеток TCRαβ+ CD8+, Т-клеток TCRγδ+ и клеток NK-типа (см. статью Romagnani P. et al., (2001), Blood, 97:601-607).
IP-10 или его рецептор CXCR3 идентифицированы при ряде различных воспалительных и аутоиммунных состояний, включая рассеянный склероз (см., например, статью Sorensen T.L et al., (1999), J. Clin. Invest., 103:807-815), ревматоидный артрит (см., например, статью Patel D.D. et al., (2001), Clin. Immunol., 98:39-45), язвенный колит (см., например, статью Uguccioni M. et al., (1999), Am. J. Pathol., 155:331-336), гепатит (см., например, статью Narumi S. et al., (1997), J. Immunol., 158:5536-5544), повреждение спинного мозга (см., например, статьи McTigue D.M. et al., (1998), J. Neurosci. Res., 53:368-376; Gonzalez et al., 2003, Exp. Neurol., 184:456-463), системную красную волчанку (см., например, статью Narumi S. et al., (2000), Cytokine 12:1561-1565), отторжение трансплантата (см., например, Zhang Z. et al., (2002), J. Immunol., 168:3205-3212), синдром Шегрена (см., например, статью Ogawa N. et al., (2002), Arthritis Rheum., 46:2730-2741). Следовательно, необходимы терапевтические агенты, которые ингибируют данную активность, в особенности, агенты, которые пригодны для применения у человека.
Раскрытие изобретения
Настоящее изобретение представляет выделенные моноклональные антитела, в частности, человеческие моноклональные антитела, которые связываются с IP-10 и которые проявляют множество желательных свойств. Данные свойства включают высокую аффинность связывания с человеческим IP-10, а также перекрестную реактивность с IP-10 макаки-резуса, но при отсутствии существенной перекрестной реактивности либо с человеческим MIG, человеческим ITAC, либо мышиным IP-10. Кроме того, антитела ингибируют связывание IP-10 с его рецептором, CXCR3, ингибируют ток кальция, индуцированный IP-10 в клетках, экспрессирующих рецептор, и ингибируют индуцируемую IP-10 миграцию клеток (хемотаксис). К тому же показано, что антитела, соответствующие изобретению, связываются с IP-10 в областях головного мозга человека, у которого диагностирован рассеянный склероз.
В предпочтительных вариантах осуществления изобретения человеческий IP-10 включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:121 [Genbank Регистрационный No. NP_001556];
CXCR3 включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:122 [Genbank Регистрационный No. NP_001495]; IP-10 макаки-резуса включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:123 [Genbank Регистрационный No. AAK95955]; мышиный IP-10 включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:124 [Genbank Регистрационный No. NPJ367249]; человеческий MIG включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:125 [Genbank Регистрационный No. NP_002407] и/или ITAC человека включает полипептид, имеющий последовательность аминокислот, как представлено в SEQ ID NO:126 [Genbank Регистрационный No. NP_005400].
В одном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело специфически связывается с IP-10 и включает вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена зародышевой линии VH человека, выбранного из группы, состоящей из гена VH 3-33 человека, гена VH 3-30.3 человека, гена VH 5-51 человека и гена VH 4-61 человека.
В другом варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело специфически связывается с IP-10 и включает вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена зародышевой линии Vk человека, выбранной из группы, состоящей из гена Vk A27 человека, гена Vk L15 человека, гена Vk L6 человека и гена Vk L18 человека.
В еще одном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело специфически связывается с IP-10 и включает:
(а) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена зародышевой линии VH человека, выбранного из группы, состоящей из гена VH 3-33 человека, гена VH 3-30.3 человека, гена VH 5-51 человека и гена VH 4-61 человека и (b) вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk зародышевой линии человека, выбранного из группы, состоящей из гена Vk A27 человека, гена Vk L15 человека, гена Vk L6 человека и гена Vk L18 человека.
В одном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает:
(a) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена VH 3-33 человека и
(b) вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk человека, выбранную из группы, состоящей из гена Vk A27 человека, гена Vk L15 человека и гена Vk L6 человека, причем антитело специфически связывается с IP-10.
В другом варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает:
(a) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена VH 3-30.3 человека и
(b) вариабельную область легкой цепи, которая представляет собой продукт или выделена из гена Vk L6 человека;
причем антитело специфически связывается с IP-10.
В еще одном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает:
(a) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена VH 5-51 человека и
(b) вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk L18 человека;
причем антитело специфически связывается с IP-10.
В еще одном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает:
(a) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена Vk 4-61 человека и
(b) вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk A27 человека;
причем антитело специфически связывается с IP-10.
В другом аспекте изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающую вариабельную область тяжелой цепи, содержащую последовательности CDR 1, CDR2 и CDR3 и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, причем:
(a) последовательность вариабельной области тяжелой цепи CDR3 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:24-34 и их консервативных модификаций,
(b) последовательность вариабельной области легкой цепи CDR3 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:73-83 и их консервативных модификаций,
(с) антитело специфически связывается с IP-10 и
(d) антитело проявляет по меньшей мере одно из следующих свойств:
(i) антитело ингибирует связывание IP-10 с CXCR3;
(ii) антитело ингибирует индуцированный IP-10 ток кальция;
(iii) антитело ингибирует индуцированную IP-10 миграцию клеток;
(iv) антитело перекрестно реагирует с IP-10 макаки-резуса;
(v) антитело не является перекрестно реактивным с мышиным IP-10;
(vi) антитело не является перекрестно реактивным с человеческим MIG;
(vii) антитело не является перекрестно реактивным с человеческим ITAC.
В предпочтительном варианте осуществления последовательность вариабельной области тяжелой цепи CDR2 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:13-23 и их консервативных модификаций, и последовательность вариабельной области легкой цепи CDR2 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:62-72 и их консервативных модификаций.
В другом предпочтительном варианте осуществления последовательность вариабельной области тяжелой цепи CDR1 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:1-12 и их консервативных модификаций, и последовательность вариабельной области легкой цепи CDR1 включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:51-61 и их консервативных модификаций.
Антитело может представлять собой, например, человеческое антитело, гуманизированное антитело или химерное антитело.
В другом аспекте изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающую вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем:
(a) вариабельная область тяжелой цепи включает последовательность аминокислот, которая по меньшей мере на 80% гомологична последовательности аминокислот, выбранной из группы, состоящей из SEQ ID NONO:35-46,
(b) вариабельная область легкой цепи включает последовательность аминокислот, которая по меньшей мере на 80% гомологична последовательности аминокислот, выбранной из группы, состоящей из SEQ ID NONO:84-94,
(c) антитело специфически связывается с IP-10 и
(d) антитело проявляет по меньшей мере одно следующих функциональных свойств:
(i) антитело ингибирует связывание IP-10 с CXCR3;
(ii) антитело ингибирует индуцируемый IP-10 ток кальция;
(iii) антитело ингибирует индуцируемую IP-10 миграцию клеток;
(iv) антитело перекрестно реагирует с IP-10 макаки-резуса;
(v) антитело не является перекрестно реактивным с мышиным IP-10;
(vi) антитело не является перекрестно реактивным с человеческим MIG;
(vii) антитело не является перекрестно реактивным с человеческим ITAC.
Антитело может представлять собой, например, человеческое антитело, гуманизированное антитело или химерное антитело.
В предпочтительных вариантах осуществления изобретения выделенное моноклональное антитело или его антигенсвязывающая часть включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:1-12,
(b) CDR2 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:13-23,
(c) CDR3 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:24-34,
(d) CDR1 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:51-61,
(e) CDR2 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:62-72, и
(f) CDR3 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:73-83, причем антитело специфически связывает IP-10.
В других предпочтительных вариантах осуществления изобретение представляет выделенное моноклональное антитело, или его антигенсвязывающую часть, включающую:
(a) вариабельную область тяжелой цепи, включающую последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:35-46, и
(b) вариабельную область легкой цепи, включающую последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:84-94, причем антитело специфически связывает IP-10.
В другом аспекте изобретения представлены антитела или их антигенсвязывающие части, которые конкурируют за связывание с IP-10 с любыми из вышеупомянутых антител.
Антитела, соответствующие изобретению, могут быть, например, антителами полной длины, например изотипа IgG1 или IgG4. Альтернативно антитела могут представлять собой фрагменты антител, такие как фрагменты Fab или Fab'2, либо одноцепочечные антитела.
В изобретении представлен также иммуноконъюгат, включающий антитело, соответствующее изобретению, или его антигенсвязывающую часть, связанные с терапевтическим агентом, таким как цитотоксин или радиоактивный изотоп.
В изобретении представлена также биспецифическая молекула, включающая антитело или его антигенсвязывающую часть, соответствующие изобретению, связанные со второй функциональной группой, обладающей другой специфичностью связывания по сравнению с указанным антителом или его антигенсвязывающей частью.
Представлены также композиции, включающие антитело или его антигенсвязывающую часть либо иммуноконъюгат или биспецифическую молекулу, соответствующие изобретению, и фармацевтически приемлемый носитель.
Кроме того, изобретение охватывает молекулы нуклеиновых кислот, кодирующие антитела или их антигенсвязывающие части, соответствующие изобретению, а также экспрессионные векторы, включающие данные нуклеиновые кислоты, и клетки-хозяева, содержащие такие экспрессионные векторы.
Более того, изобретение представляет трансгенную мышь, несущую трансгены тяжелой и легкой цепи человеческого иммуноглобулина, причем мышь экспрессирует антитело, соответствующее изобретению, а также гибридомы, продуцирующие антитело, соответствующее изобретению.
В другом аспекте изобретение представляет способ ингибирования воспалительногоилиаутоиммунногоответа,опосредуемогоактивированными Т-клетками или NK-клетками, заключающийся в контактировании Т-клеток или NK-клеток с антителом или его антигенсвязывающей частью, соответствующими изобретению, таким образом, что происходит ингибирование воспалительного или аутоиммунного ответа.
В еще одном аспекте изобретения представлен способ лечения воспалительного или аутоиммунного заболевания у нуждающегося в лечении субъекта, заключающийся во введении субъекту антитела или его антигенсвязывающей части, соответствующих изобретению, так что осуществляется лечение воспалительного или аутоиммунного заболевания у субъекта.
Заболеванием может быть, например, рассеянный склероз, ревматоидный артрит, воспалительная болезнь кишки (например, язвенный колит, болезнь Крона), системная красная волчанка, диабет типа 1, воспалительные кожные нарушения (например, псориаз, плоский лишай), аутоиммунное заболевание щитовидной железы (например, болезнь Грейвса, тиреоидит Хашимото), синдром Шегрена, легочное воспаление (например, астма, хроническая обструктивная болезнь легких, саркоидоз легких, аутоиммунныйальвеолит), отторжение трансплантата, повреждение спинного мозга, повреждение головного мозга (например, инсульт), нейродегенеративные заболевания (например, болезнь Альцгеймера, болезнь Паркинсона), гингивит, воспаление, вызванное генотерапией, болезни ангиогенеза, воспалительная болезнь почек (например, IgA нефропатия, мембранопролиферативный гломерулонефрит, быстро прогрессирующий гломерулонефрит) и атеросклероз.
В еще одном аспекте изобретение представляет способ лечения вирусной или бактериальной инфекции, влекущие за собой нежелательную активность IP-10 у нуждающегося в лечении субъекта, заключающийся во введении субъекту антитела или его антигенсвязывающей части, соответствующих изобретению, так что осуществляется лечение вирусной или бактериальной инфекции у субъекта. Например, антитела могут быть использованы для лечения вирусного менингита, вирусного энцефалита и бактериального менингита.
Вирусная инфекция, которую предусматривают лечить способом, соответствующим изобретению, может быть опосредована, например, вирусом иммунодефицита человека (ВИЧ), вирусом гепатита С (HCV), вирусом простого герпеса типа I (HSV-1) или вирусом тяжелого острого респираторного синдрома (SARS).
В изобретении представлены также способы получения антител против IP-10 "второго поколения" на основе последовательностей антител против IP-10, предложенных в данном контексте.
Например, изобретение представляет способ получения антитела против IP-10, предусматривающий;
(a) получение: (i) последовательности вариабельной области тяжелой цепи антитела, включающей последовательность CDR1, выбранную из группы, состоящей из SEQ ID NONO:1-12, последовательность CDR2, выбранную из группы, состоящей из SEQ ID NONO:13-23 и/или последовательность CDR3, выбранную из группы, состоящей из SEQ ID NONO:24-34, и (ii) последовательности вариабельной области легкой цепи антитела, включающей последовательность CDR1, выбранную из группы, состоящей из SEQ ID NONO:51-61, последовательность CDR2, выбранную из группы, состоящей из SEQ ID NONO:62-72 и/или последовательность CDR3, выбранную из группы, состоящей из SEQ ID NONO:73-83;
(b) изменение по меньшей мере одного остатка аминокислоты в последовательности вариабельной области тяжелой цепи антитела и/или последовательности вариабельной области легкой цепи антитела с целью создания по меньшей мере одной измененной последовательности антитела, и
(c) экспрессию измененной последовательности антитела в виде белка.
Другие признаки и преимущества данного изобретения будут очевидны из последующего детального описания и примеров, которые не следует истолковывать, как ограничивающие. Содержание всех ссылок, описаний Genbank, патентов и опубликованных патентных заявок, цитируемых во всем материале данной заявки, специально включено в данном контексте в виде ссылки.
Краткое описание чертежей
На Фигуре 1 представлена нуклеотидная последовательность (SEQ ID NO:99) и последовательность аминокислот (SEQ ID NO:35) вариабельной области тяжелой цепи человеческого моноклонального антитела 1D4. Схематически изображены участки CDR1 (SEQ ID NO:1), CDR2 (SEQ ID NO:13) и CDR3 (SEQ ID NO:24) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 2 представлена нуклеотидная последовательность (SEQ ID NO:110) и последовательность аминокислот (SEQ ID NO:84) вариабельной области легкой цепи человеческого моноклонального антитела 1D4. Схематически изображены участки CDR1 (SEQ ID NO:51), CDR2 (SEQ ID NO:62) и CDR3 (SEQ ID NO:73) и указаны отклонения от зародышевой линии V и J.
На Фигуре 3 представлена нуклеотидная последовательность (SEQ ID NO:100) и последовательность аминокислот (SEQ ID NO:36) вариабельной области тяжелой цепи человеческого моноклонального антитела 1Е1. Схематически изображены участки CDR1 (SEQ ID NO:2), CDR2 (SEQ ID NO:14) и CDR3 (SEQ ID NO:25) и указаны отклонения от зародышевой линии V и J.
На Фигуре 4 представлена нуклеотидная последовательность (SEQ ID NO:111) и последовательность аминокислот (SEQ ID NO:85) вариабельной области легкой цепи человеческого моноклонального антитела 1Е1. Схематически изображены участки CDR1 (SEQ ID NO:52), CDR2 (SEQ ID NO:63) и CDR3 (SEQ ID NO:74) и указаны отклонения от зародышевой линии V и J.
На Фигуре 5 представлена нуклеотидная последовательность (SEQ ID NO:101) и последовательность аминокислот (SEQ ID NO:37) вариабельной области тяжелой цепи человеческого моноклонального антитела 2G1. Схематически изображены участки CDR1 (SEQ ID NO:3), CDR2 (SEQ ID NO:15) и CDR3 (SEQ ID NO:26) и указаны отклонения от зародышевой линии V и J.
На Фигуре 6 представлена нуклеотидная последовательность (SEQ ID NO:112) и последовательность аминокислот (SEQ ID NO:86) вариабельной области легкой цепи человеческого моноклонального антитела 2G1. Схематически изображены участки CDR1 (SEQ ID NO:53), CDR2 (SEQ ID NO:64) и CDR3 (SEQ ID NO:75) и указаны отклонения от зародышевой линии V и J.
На Фигуре 7 представлена нуклеотидная последовательность (SEQ ID NO:102) и последовательность аминокислот (SEQ ID NO:38) вариабельной области тяжелой цепи человеческого моноклонального антитела 3С4. Схематически изображены участки CDR1 (SEQ ID NO:4), CDR2 (SEQ ID NO:16) и CDR3 (SEQ ID NO:27) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 8 представлена нуклеотидная последовательность (SEQ ID NO:113) и последовательность аминокислот (SEQ ID NO:87) вариабельной области легкой цепи человеческого моноклонального антитела 3С4. Схематически изображены участки CDR1 (SEQ ID NO:54), CDR2 (SEQ ID NO:65) и CDR3 (SEQ ID NO:76) и указаны отклонения от зародышевой линии V и J.
На Фигуре 9 представлена нуклеотидная последовательность (SEQ ID NO:103) и последовательность аминокислот (SEQ ID NO:39) вариабельной области тяжелой цепи человеческого моноклонального антитела 6А5. Схематически изображены участки CDR1 (SEQ ID NO:5), CDR2 (SEQ ID NO:17) и CDR3 (SEQ ID NO:28) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 10 представлена нуклеотидная последовательность (SEQ ID NO:114) и последовательность аминокислот (SEQ ID NO:88) вариабельной области легкой цепи человеческого моноклонального антитела 6А5. Схематически изображены участки CDR1 (SEQ ID NO:55), CDR2 (SEQ ID NO:66) и CDR3 (SEQ ID NO:77) и указаны отклонения от зародышевой линии V и J.
На Фигуре 11 представлена нуклеотидная последовательность (SEQ ID NO:104) и последовательность аминокислот (SEQ ID NO:40) вариабельной области тяжелой цепи человеческого моноклонального антитела 6А8. Схематически изображены участки CDR1 (SEQ ID NO:6), CDR2 (SEQ ID NO:18) и CDR3 (SEQ ID NO:29) и указаны отклонения от зародышевой линии V и J.
На Фигуре 12 представлена нуклеотидная последовательность (SEQ ID NO:115) и последовательность аминокислот (SEQ ID NO:89) вариабельной области легкой цепи человеческого моноклонального антитела 6А8. Схематически изображены участки CDR1 (SEQ ID NO:56), CDR2 (SEQ ID NO:67) и CDR3 (SEQ ID NO:78) и указаны отклонения от зародышевой линии V и J.
На Фигуре 13 представлена нуклеотидная последовательность (SEQ ID NO:105) и последовательность аминокислот (SEQ ID NO:41) вариабельной области тяжелой цепи человеческого моноклонального антитела 6В10. Схематически изображены участки CDR1 (SEQ ID NO:7), CDR2 (SEQ ID NO:19) и CDR3 (SEQ ID NO:30) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 14 представлена нуклеотидная последовательность (SEQ ID NO:116) и последовательность аминокислот (SEQ ID NO:90) вариабельной области легкой цепи человеческого моноклонального антитела 6В10. Схематически изображены участки CDR1 (SEQ ID NO:57), CDR2 (SEQ ID NO:68) и CDR3 (SEQ ID NO:79) и указаны отклонения от зародышевой линии V и J.
На Фигуре 15 представлена нуклеотидная последовательность (SEQ ID NO:106) и последовательность аминокислот (SEQ ID NO:42) вариабельной области тяжелой цепи человеческого моноклонального антитела 7С10. Схематически изображены участки CDR1 (SEQ ID NO:8), CDR2 (SEQ ID NO:20) и CDR3 (SEQ ID NO:31) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 16 представлена нуклеотидная последовательность (SEQ ID NO:117) и последовательность аминокислот (SEQ ID NO:91) вариабельной области легкой цепи человеческого моноклонального антитела 7С10. Схематически изображены участки CDR1 (SEQ ID NO:58), CDR2 (SEQ ID NO:69) и CDR3 (SEQ ID NO:80) и указаны отклонения от зародышевой линии V и J.
На Фигуре 17 представлена нуклеотидная последовательность (SEQ ID NO:107) и последовательность аминокислот (SEQ ID NO:43) вариабельной области тяжелой цепи человеческого моноклонального антитела 8F6. Схематически изображены участки CDR1 (SEQ ID NO:9), CDR2 (SEQ ID NO:21) и CDR3 (SEQ ID NO:32) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 18 представлена нуклеотидная последовательность (SEQ ID NO:118) и последовательность аминокислот (SEQ ID NO:92) вариабельной области легкой цепи человеческого моноклонального антитела 8F6. Схематически изображены участки CDR1 (SEQ ID NO:59), CDR2 (SEQ ID NO:70) и CDR3 (SEQ ID NO:81) и указаны отклонения от зародышевой линии V и J.
На Фигуре 19 представлена нуклеотидная последовательность (SEQ ID NO:108) и последовательность аминокислот (SEQ ID NO:44) вариабельной области тяжелой цепи человеческого моноклонального антитела 10А12. Схематически изображены участки CDR1 (SEQ ID NO:10), CDR2 (SEQ ID NO:22) и CDR3 (SEQ ID NO:33) и указаны отклонения от зародышевой линии V и J. Альтернативно остаток аминокислоты 32 в CDR1 может быть мутирован из цистеина в серии (SEQ ID NO:11), приводя к последовательности VH SEQ ID NO:45.
На Фигуре 20 представлена нуклеотидная последовательность (SEQ ID NO:119) и последовательность аминокислот (SEQ ID NO:93) вариабельной области легкой цепи человеческого моноклонального антитела 10А12.
Схематически изображены участки CDR1 (SEQ ID NO:60), CDR2 (SEQ ID NO:71) и CDR3 (SEQ ID NO:82) и указаны отклонения от зародышевой линии V и J.
На Фигуре 21 представлена нуклеотидная последовательность (SEQ ID NO:109) и последовательность аминокислот (SEQ ID NO:46) вариабельной области тяжелой цепи человеческого моноклонального антитела 13С4. Схематически изображены участки CDR1 (SEQ ID NO:12), CDR2 (SEQ ID NO:23) и CDR3 (SEQ ID NO:34) и указаны отклонения от зародышевой линии V, D и J.
На Фигуре 22 представлена нуклеотидная последовательность (SEQ ID NO:120) и последовательность аминокислот (SEQ ID NO:94) вариабельной области легкой цепи человеческого моноклонального антитела 13С4. Схематически изображены участки CDR1 (SEQ ID NO:61), CDR2 (SEQ ID NO:72) и CDR3 (SEQ ID NO:83) и указаны отклонения от зародышевой линии V и J.
На Фигуре 23 представлены результаты элайнмента последовательности аминокислот вариабельной области тяжелой цепи 1D4, 1Е1, 2G1, 6А5, 6А8, 7С10 и 10А12 с последовательностью аминокислот человеческой зародышевой линии VH 3-33 (SEQ ID NO:47).
На Фигуре 24 представлены результаты элайнмента последовательности аминокислот вариабельной области тяжелой цепи 6В10 и 8F6 с последовательностью аминокислот человеческой зародышевой линии VH 3-30.3 (SEQ ID NO:48).
На Фигуре 25 представлены результаты элайнмента последовательности аминокислот вариабельной области тяжелой цепи 3С4 с последовательностью аминокислот человеческой зародышевой линии VH 5-51 (SEQ ID NO:49).
На Фигуре 26 представлены результаты элайнмента последовательности аминокислот вариабельной области тяжелой цепи 13С4 с последовательностью аминокислот человеческой зародышевой линии VH 4-61 (SEQ ID NO:50).
На Фигуре 27 представлены результаты элайнмента последовательности аминокислот вариабельной области легкой цепи 1D4, 2G1, 6А5, 6А8, 10А12 и 13С4 с последовательностью аминокислот человеческой зародышевой линии Vk A27 (SEQ ID NO:95).
На Фигуре 28 представлены результаты элайнмента последовательности аминокислот вариабельной области легкой цепи 1Е1, 6В10 и 8F6 с последовательностью аминокислот человеческой зародышевой линии Vk L6 (SEQ ID NO:96).
На Фигуре 29 представлены результаты элайнмента последовательности аминокислот вариабельной области легкой цепи 3С4 с последовательностью аминокислот человеческой зародышевой линии Vk L18 (SEQ ID NO:97).
На Фигуре 30 представлены результаты элайнмента последовательности аминокислот вариабельной области легкой цепи 7С 10 с последовательностью аминокислот человеческой зародышевой линии Vk L15 (SEQ ID NO:98). Осуществление изобретения
Настоящее изобретение относится к выделенным моноклональным антителам, в особенности человеческим моноклональным антителам, которые специфически связываются с IP-10 и которые ингибируют функциональные свойства IP-10.
В ряде вариантов осуществления антитела, соответствующие изобретению, выделены из определенных последовательностей тяжелых и легких цепей зародышевой линии и/или включают определенные структурные признаки, такие как участки CDR, содержащие определенные последовательности аминокислот.
Изобретение представляет выделенные антитела, способы получения данных антител, иммуноконъюгаты и биспецифические молекулы, включающие данные антитела, и фармацевтические композиции, содержащие антитела, иммуноконъюгаты или биспецифические молекулы, соответствующие изобретению.
Изобретение относится также к способам применения антител для подавления воспалительных или аутоиммунных ответов, например, при лечении различных воспалительных или аутоиммунных заболеваний, а также к способам лечения вирусных инфекций, включающих нежелательную активность IP-10.
Чтобы можно было легче понять настоящее изобретение, сначала определяют некоторые термины. Дополнительные определения приведены во всем тексте детального описания.
Термины "белок 10, индуцируемый интерфероном γ", "IP-10" и "CXCL10" используются взаимозаменяемо и включают варианты, изоформы и видовые гомологи человеческого IP-10. Соответственно, человеческие антитела, соответствующие изобретению, в некоторых случаях могут быть перекрестно реактивными с IP-10 видов, отличных от человека. В других случаях антитела могут быть полностью специфическими в отношении человеческого IP-10 и могут не проявлять видовую или другие типы перекрестной реактивности.
Полная последовательность аминокислот человеческого IP-10 имеет регистрационный номер Genbank NP_001556 (SEQ ID NO:121). Полная последовательность аминокислот IP-10 макаки-резуса имеет регистрационный номер Genbank AAK95955 (SEQ ID NO:123). Полная последовательность аминокислот мышиного IP-10 имеет регистрационный номер Genbank NP_067249 (SEQ ID NO:124).
Термин "CXCR3" относится к рецептору для IP-10 (CXCL10). Полная последовательность аминокислот человеческого CXCR3 имеет регистрационный номер Genbank NP_001495 (SEQ ID NO:122).
Термин "MIG" относится к лиганду CXCR3, известному также как монокин, индуцируемый γ-интерфероном, который отличен от IP-10. Полная последовательность аминокислот человеческого MIG имеет регистрационный номер Genbank NP_002407 (SEQ ID NO:125).
Термин "ITAC" относится к лиганду CXCR3, также известному как индуцируемый интерфероном хемоаттрактант Т-клеток α, который отличен от IP-10. Полная последовательность аминокислот человеческого ITAC имеет регистрационный номер Genbank NP_005400 (SEQ ID NO:126).
Термин "иммунный ответ" относится кдействию, например, лимфоцитов, антиген-презентирующих клеток, фагоцитарных клеток, гранулоцитов и растворимых макромолекул, продуцируемых вышеуказанными клетками или печенью (включая антитела, цитокины и комплемент), которое приводит в результате к избирательному повреждению, разрушению или выведению из организма человека инвазивных патогенов, клеток или тканей, инфицированных патогеном, раковых клеток или, в случаях аутоиммунитета или патологического воспаления, нормальных человеческих клеток или тканей.
Термин "путь сигнальной трансдукции" относится к биохимической связи между множеством молекул сигнальной трансдукции, которые играют роль в передаче сигнала из одной части клетки в другую часть клетки. Как используют в данном контексте, выражение "клеточный поверхностный рецептор" включает, например, молекулы и комплексы молекул, способные к приему сигнала и передаче данного сигнала через плазматическую мембрану клетки. Примером "клеточного поверхностного рецептора", соответствующего настоящему изобретению, является рецептор CXCR3, с которым связывается молекула IP-10.
Термин "антитело", как ссылаются в данном контексте, включает целые антитела и любой антигенсвязывающий фрагмент (т.е., "антигенсвязывающую часть") или их отдельные цепи. Термин "антитело" относится к гликопротеину, содержащему по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, связанные друг с другом дисульфидными связями, или его антигенсвязывающей части. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно обозначают в данном контексте как VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно обозначают в данном контексте как VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена CL. Области VH и VL могут быть далее подразделены на участки гипервариабельности, называемые участками, определяющими комплементарность (CDR), между которыми расположены участки, которые являются более консервативными, называемые скелетными (остовными) областями (FR). Каждая из VH и Vk состоит из трех CDR и четырех FR, построенных от аминоконца к карбоксиконцу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (Clq) системы классического комплемента.
Термин "антигенсвязывающая часть" антитела (или просто "часть антитела"), как используют в данном контексте, относится к одному или более фрагментам антитела, которые сохраняют способность специфически связываться с антигеном (например, IP-10). Показано, что антигенсвязывающая функция антитела может осуществляться фрагментами антитела полной длины. Примеры связывающих фрагментов, охватываемых термином "антигенсвязывающая часть" антитела, включают (i) фрагмент Fab, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) фрагмент Р(ab')2, двухвалентный фрагмент, содержащий два фрагмента Fab, связанных дисульфидным мостиком в шарнирной области; (iii) фрагмент Fd, состоящий из доменов VH и СН1; (iv) фрагмент Fv, состоящий из доменов Vk и VH одного плеча антитела, (v) фрагмент dAb (см. статью Ward et al., (1989), Nature, 341:544-546), который состоит из домена VH, и (vi) выделенный участок определяющий комплементарность (CDR). Кроме того, хотя два домена фрагмента Fv, VL и VH, кодируются отдельными генами, они могут быть связаны посредством рекомбинантных методов синтетическим линкером, который дает возможность получить их в виде одной белковой цепи, в которой области Vk и VH спарены с образованием одновалентных молекул (известных как одноцепочечный Fv (scFv); см., например, статьи Bird et al., (1988), Science, 242:423-426; и Huston et al., (1988), Proc. Natl. Acad. Sci. USA, 85:5879-5883). Предусматривается также, что термин "антигенсвязывающая часть" антитела охватывает данные одноцепочечные антитела. Данные фрагменты антитела получают при использовании принятых методик, известных специалистам в области техники, и фрагменты подвергают скринингу на применение таким же образом, как интактные антитела.
Термин "выделенное антитело", как используют в данном контексте, предназначен для обозначения антитела, которое практически не содержит других антител, обладающих отличными антигенными специфичностями (например, выделенное антитело, которое специфически связывает IP-10, практически не содержит антител, которые специфически связывают антигены, отличные от IP-10). Выделенное антитело, которое специфически связывает IP-10, однако, может иметь перекрестную реактивность с другими антигенами, такими как молекулы IP-10 из других видов. Более того, выделенное антитело может практически не содержать другой клеточный материал и/или химические агенты.
Термины "моноклональное антитело" или "композиция моноклональных антител", как используют в данном контексте, относится к препарату молекул антител одного молекулярного состава. Композиция моноклональных антител проявляет одну специфичность связывания и аффинность к определенному эпитопу.
Термин "человеческое антитело", как используют в данном контексте, предусматривает включение антител, имеющих вариабельные области, в которых как скелетные области, так и участки CDR выделены из последовательностей иммуноглобулина зародышевой линии человека. К тому же, если антитело включает константную область, то константная область также происходит из последовательностей иммуноглобулина зародышевой линии человека. Человеческие антитела, соответствующие изобретению, могут включать остатки аминокислот, не кодируемые последовательностями иммуноглобулина зародышевой линии человека (например, мутации, интродуцированные случайным или сайт-специфическим мутагенезом in vitro или посредством соматической мутации in vivo). Однако, термин "человеческое антитело", как используют в данном контексте, не предусматривает включение антител, в которых последовательности CDR, выделенные из зародышевой линии другого виде млекопитающего, например, мыши, привиты на человеческие скелетные последовательности.
Термин "человеческое моноклональное антитело" относится кантителам, проявляющим единственную специфичность связывания, которые имеют вариабельные области, где как скелетные области, так и участки CDR выделены из последовательностей иммуноглобулина зародышевой линии человека. В одном варианте осуществления человеческие моноклональные антитела продуцируются гибридомой, которая включает В-клетку, полученную от трансгенного животного, отличного от человека, например, трангенной мыши, имеющей геном, несущий трансген тяжелой цепи и трансген легкой цепи человека, слитую с иммортализованной клеткой.
Термин "рекомбинантное человеческое антитело", как используют в данном контексте, включает все человеческие антитела, которые получены, экспрессированы, созданы или выделены рекомбинантными средствами, такие как (а) антитела, выделенные у животного (например, мыши), которая является трансгенной или трансхромосомной по генам иммуноглобулина человека, или полученной из него гибридомы (дополнительно описано ниже), (b) антитела, выделенные из клетки-хозяина, трансформированные так, чтобы они экспрессировали человеческое антитело, например, изтрансфектомы, (с) антитела, выделенные из рекомбинантной комбинаторной библиотеки человеческих антител, и (d) антитела, полученные, экспрессированные, созданные или выделенные другими средствами, которые включают сплайсинг последовательностей гена иммуноглобулина человека с другими последовательностями ДНК. Данные рекомбинантные человеческие антитела имеют вариабельные области, в которых скелетные области и участки CDR выделены из последовательностей гена иммуноглобулина человека. Однако, в некоторых вариантах осуществления, данные рекомбинантные человеческие антитела могут быть подвергнуты мутагенезу in vitro (или, когда используют животное, трансгенное по последовательностям 1д человека, соматическому мутагенезу in vivo) и, таким образом, последовательности аминокислот областей VH и VL рекомбинантных антител представляют собой последовательности, которые, будучи выделенными и относящимися к последовательностям VH и VL зародышевой линии человека, могут не существовать в естественных условиях в репертуаре зародышевой линии человеческих антител in vivo.
Как используют в данном контексте, термин "изотип" относится к классу антител (например, IgM или IgGI), которые кодируются генами константной области тяжелой цепи.
Выражения "антитело, распознающее антиген" и "антитело, специфическое в отношении антигена" используют в данном контексте взаимозаменяемо с термином "антитело, которое специфически связывается с антигеном".
Как используют в данном контексте, выражение антитело, которое "специфически связывается с человеческим IP-10" предназначено для обозначения антитела, которое связывается с человеческим IP-10 с KD 5×10-9 М или меньше, более предпочтительно 2×10-9 М или меньше и даже более предпочтительно 1×10-10 М или меньше. Выражение антитело, которое "перекрестно реактивно с IP-10 макаки-резуса", предназначено для обозначения антитела, которое связывается с IP-10 макаки-резуса с KD 0,5×10-8 М или меньше, более предпочтительно 5×10-9 М или меньше и даже более предпочтительно 2×10-9 М или меньше. Выражение антитело, которое "не перекрестно-реактивно с мышиным IP-10" или" не перекрестно-реактивно с человеческим MIG" или "не перекрестно-реактивно с человеческим ITAC" предназначено для обозначения антитела, которое связывается с мышиным IP-10, человеческим MIG или человеческим ITAC с KD 1,5×10-8 М или выше, более предпочтительно KD 5-10×10-8 М или выше и даже более предпочтительно 1×10-7 М или выше. В ряде вариантов осуществления данные антитела, которые не являются перекрестно-реактивными с мышиным IP-10, человеческим MIG и/или человеческим ITAC проявляют по существу неопределяемое связывание в отношении данных белков в стандартных анализах связывания.
Как используют в данном контексте, выражение антитело, которое "ингибирует связывание IP-10 с CXCR3" предназначено для обозначения антитела, которое ингибирует связывание IP-10 с CXCR3 с Ki 1 нМ или меньше, более предпочтительно 0,75 нМ или меньше, даже более предпочтительно 0,5 нМ или меньше и даже более предпочтительно 0,25 нМ или меньше.
Как используют в данном контексте, выражение антитело, которое "ингибирует индуцированный IP-10 ток кальция", предназначено для обозначения антитела, которое ингибирует индуцированный IP-10 ток кальция с IC50 10 нМ или меньше, более предпочтительно 7,5 нМ или меньше, даже более предпочтительно 5 нМ или меньше и даже более предпочтительно 2,5 нМ или меньше.
Как используют в данном контексте, выражение антитело, которое "ингибирует индуцированную IP-10 миграцию клеток", предназначено для обозначения антитела, которое ингибирует индуцированную человеческим IP-10 миграцию клеток с IC50 2 мкг/мл или меньше, более предпочтительно 1 мкг/мл или меньше, даже более предпочтительно 0,5 мкг/мл или меньше и даже более предпочтительно 0,25 мкг/мл или меньше.
Термин "Kassoc" или "Ка", как используют в данном контексте, предназначен для обозначения скорости ассоциации взаимодействия определенное антитело-антиген, тогда как термин "Kdis" или "Kd", как используют в данном контексте, предназначено для обозначения скорости диссоциации взаимодействия определенное антитело-антиген. Термин "KD", как используют в данном контексте, предназначено для обозначения константы диссоциации, которую получают из соотношения Kd к Ka (т.е. Kd/Ka) и выражают как молярную концентрацию (М). Значения KD для антител можно определить, используя способы, хорошо разработанные в области техники. Предпочтительный метод определения KD антитела состоит в использовании поверхностного плазменного резонанса, предпочтительно в использовании системы биосенсоров, такой как система Biacore®.
Как используют в данном контексте, термин "высокоаффинное" для антитела IgG относится к антителу, имеющему KD 10-8 М или меньше, более предпочтительно 10-9 М или меньше и даже более предпочтительно 10-10 М или меньше в отношении антигена-мишени. Однако, "высокоаффинное" связывание может варьировать в отношении других изотипов антитела. Например, "высокоаффинное" связывание в отношении изотипа IgM относится к антителу, имеющему KD 10-7 М или меньше, более предпочтительно 10-8 М или меньше.
Как используют в данном контексте, термин "субъект" включает любого человека или животного, отличного от человека. Термин "животное, отличное от человека" включает всех позвоночных, например, млекопитающих и немлекопитающих, таких как приматы, отличные от человека, овцы, собаки, кошки, лошади, коровы, куры, амфибии, рептилии и т.п.
Различные аспекты изобретения описаны в дальнейших деталях в последующих подразделах.
Антитела против IP-10
Антитела, соответствующие изобретению, характеризуются определенными функциональными признаками и свойствами антител. Например, антитела специфически связываются с человеческим IP-10. Кроме того, антитела могут перекрестно реагировать с IP-10, полученным от одного или более приматов, отличных от человека, таким как макака-резус. Предпочтительно, когда антитела не являются перекрестно реактивными с мышиным IP-10. Более того, хотя MIG и ITAC являются также лигандами для рецептора CXCR3, антитела, соответствующие изобретению, предпочтительно не являются перекрестно реактивными с человеческим MIG или человеческим ITAC.
Предпочтительно, когда антитело, соответствующее изобретению, связывается с IP-10 высокой аффинностью, например, с KD 10-8 М или меньше либо 10-9 М или меньше либо даже 10-10 М или меньше.
Кроме того, антитела, соответствующие изобретению, способны ингибировать одну или более функциональных активностей IP-10. Например, в одном варианте осуществления антитела ингибируют связывание IP-10 с CXCR3. В другом варианте осуществления антитела ингибируют индуцированный IP-10 ток кальция. В еще одном варианте осуществления, антитела ингибируют индуцированную IP-10 миграцию клеток (хемотаксис).
В области техники известны стандартные анализы, направленные на оценку связывающей способности антител в отношении IP-10 различных видов и/или MIG либо ITAC, включая, например, ELISA (твердофазный иммуноферментные анализы), вестерн-блоттинг и RIA (радиоиммунные анализы). Подходящие анализы подробно описаны в Примерах. Кинетика связывания (например, аффинность связывания) антител также может быть оценена стандартными методами анализа, известными в области техники, такими как анализ с использованием Biacore. Анализы, направленные на оценку эффектов антител на функциональные свойства IP-10 (например, связывание рецептора, ток кальция, хемотаксис), описаны более детально в Примерах.
Соответственно, принимается во внимание, что выражение антитело, которое "ингибирует" одно или больше данных функциональных свойств IP-10 (например, биохимическую, иммунохимическую, клеточную, физиологическую или иную биологическую активность или тому подобную), как определено согласно методикам, известным в области техники, и описано в данном контексте, относится к статистически значимому снижению определенной активности относительно уровня, наблюдаемого в отсутствие антитела (или, например, когда присутствует контрольное антитело несоответствующей специфичности). Предпочтительно, когда антитело, которое ингибирует активность IP-10, вызывает такое статистически значимое снижение измеряемого параметра по меньшей мере на 10%, более предпочтительно по меньшей мере на 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90%, и в некоторых предпочтительных вариантах осуществления антитело, соответствующее изобретению, может ингибировать больше, чем 92%, 94%, 95%, 97%, 98% или 99% функциональной активности IP-10.
Моноклональные антитела 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4
Предпочтительными антителами, соответствующими изобретению, являются человеческие моноклональные антитела 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4, выделенные и структурно охарактеризованные, как описано в Примерах 1 и 2. Другим предпочтительным антителом является 10A12S, в котором остаток аминокислоты 32 тяжелой цепи 10А12 (в CDR1 VH) мутирован из цистеина в серин. Последовательности аминокислот Vk 1E1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S и 13С4 представлены в SEQ ID NONO:35-46, соответственно. Последовательности аминокислот Vk 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены в SEQ ID NONO:84-94, соответственно.
Исходя из того, что каждое из данных антител может связываться с IP-10, последовательности VH и VL могут быть "перемешаны и подобраны" для того, чтобы создать другие связывающие молекулы против IP-10, соответствующие изобретению. Связывание IP-10 данных "перемешанных и подобранных" антител можно протестировать, используя анализы связывания, описанные выше и в Примерах (например, ELISA). Предпочтительно, чтобы, когда VH- и VL-цепи перемешивают и подбирают, последовательность VH из определенной пары VH/VL была замещена структурно близкой последовательностью VH. Аналогично является предпочтительным, когда последовательность VL из определенной пары VH/VL замещают структурно близкой последовательностью VL. Например, последовательности VH и Vk 1D4, 2G1, 6А5, 6А8, 10А12 или 10A12S особенно подходят для перемешивания и подбора, поскольку в данных антителах использованы последовательности VH и VL, выделенные из одних и тех же последовательностей зародышевой линии (VH 3-33 и Vk A27) и, таким образом, они проявляют структурную близость. Аналогичным образом последовательности VH и VL 6В10 и 8F6 также являются особенно подходящими для перемешивания и подбора, поскольку в них также использованы последовательности VH и VL, выделенные из одних и тех же последовательностей зародышевой линии (VH 3-30.3 и Vk L6) и, таким образом, они проявляют структурную близость. Альтернативно, например, последовательность VH 1D4, 2G1, 6А5, 6А8, 10А12 или 10A12S можно спарить с VL 13C4, поскольку последовательности VH 1D4, 2G1, 6А5, 6А8, 10А12 и 10A12S исходно спарены с последовательностью Vk зародышевой линии Vk А27 и последовательность Vk 13C4 также происходит из зародышевой линии Vk А27. Аналогично последовательность VL 7C10 или 1Е1 можно спарить с VH 1D4, 2G1, 6А5, 6А8, 10А12 или 10A12S, посколькупоследовательности VL 7С10 и 1Е1 исходно спарены с последовательностью Vk зародышевой линии VH 3-33 и последовательности VH 1D4, 2G1, 6А5, 6А8, 10А12 и 10A12S также выделены из зародышевой линии VH 3-33. Обычному компетентному специалисту будет легко увидеть возможность создания другого спаривания VH/VL структурно близких последовательностей из последовательностей VH и VL, описанных в данном контексте для моноклональных антител 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13C4.
Соответственно в одном аспекте изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающие:
(a) вариабельную область тяжелой цепи, содержащую последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:35-46; и
(b) вариабельную область легкой цепи, содержащую последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:84-94;
причем антитело специфически связывает IP-10.
Предпочтительные комбинации тяжелых и легких цепей включают:
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:35; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:84; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:36; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:85; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:37; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:86; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:38; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:87; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:39; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:88; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:40; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:89; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:41; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:90; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:42; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:91; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:43; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:92; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:44 или 45; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:93; или
(а) вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:46; и (b) вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:94.
В другом аспекте изобретение представляет антитела, которые включают CDR1, CDR2 и CDR3 тяжелой и легкой цепей 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S и 13С4 или их комбинации. Последовательности аминокислот CDR1 VH 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S и 13С4 представлены в SEQ ID NONO:1-12. Последовательности аминокислот CDR2 VH 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены в SEQ ID NONO:13-23. Последовательности аминокислот CDR3 VH 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены с SEQ ID NONO:24-34. Последовательности аминокислот CDR1 Vk 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены в SEQ ID NONO:51-61. Последовательности аминокислот CDR2 Vk 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены в SEQ ID NONO:62-72. Последовательности аминокислот CDR1 Vk 1 D4,1 Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4 представлены в SEQ ID NONO:73-83. Участки CDR схематически представлены с помощью системы Kabat (см. Kabat E. A. et al., (1991), Sequences of Proteins of Immunological Interest (Последовательности белков, представляющих иммунологический интерес), 5 изд., U.S. Department of Health и Human Services, NIH Publication No. 91-3242).
Исходя из того, что данные антитела могут связываться с IP-10 и что антигенсвязывающая специфичность обеспечивается главным образом за счет участков CDR1,2 и 3, последовательности CDR1,2 и 3 VH и последовательности CDR1,2 и 3 VL можно "перемешать и подобрать" (т.е. можно смешать и подобрать CDR из разных антител, при том, что каждое антитело должно включать CDR1,2 и 3 VH и CDR1,2 и 3 VL), чтобы создать другие связывающие молекулы против IP-10, соответствующие изобретению. Связывание IP-10 данных "перемешанных и подобранных" антител можно протестировать, используя анализы связывания, описанные выше и в Примерах (например, ELISA). Предпочтительно, чтобы когда перемешивают и подбирают последовательности CDR VH, последовательность CDR1, CDR2 и/или CDR3 из определенной последовательности VH замещалась структурно близкой последовательностью(ями) CDR. Аналогично, когда перемешивают и подбирают последовательности CDR VL, предпочтительно, чтобы последовательность CDR1, CDR2 и/или CDR3 из определенной последовательности VL замещалась структурно близкой последовательностью(ями) CDR. Например, CDR1 VH 1D4, 1Е1, 2G1, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 10A12S имеют некоторую структурную близость и, вследствие этого, подходят для перемешивания и подбора, тогда как CDR1 VH 3C4 и 13С4 не являются структурно близкими CDR1 VH 1D4, 1Е1, 2G1, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 10A12S и, таким образом, их не следует перемешивать и подбирать вместе с ними. Обычному компетентному специалисту будет легко увидеть, что новые последовательности VH и VL можно создать путем замещения одной или более последовательностей участков CDR VH и/или VL структурно близкими последовательностями из последовательностей CDR, описанных в данном контексте для моноклональных антител 1D4, 1Е1, 2G1, 3C4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4.
Соответственно в другом аспекте изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающую:
(a) CDR1 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:1-12;
(b) CDR2 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:13-23;
(c) CDR3 вариабельной области тяжелой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:24-34;
(d) CDR1 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:51-61;
(e) CDR2 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:62-72; и
(f) CDR3 вариабельной области легкой цепи, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:73-83;
где антитело специфически связывает IP-10.
В предпочтительном варианте осуществления, антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:1;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:13;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:24;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:51;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:62; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:73.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:2;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:14;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:25;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:52;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:63; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:74.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:3;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:15;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:26;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:53;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:64; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:75.
В другом предпочтительном варианте осуществления антитело включает:
(а) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:4;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:16;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:27;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:54;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:65; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:76.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:5;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:17;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:28;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:55;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:66; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:77.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:6;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:18;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:29;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:56;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:67; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:78.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:7;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:19;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:30;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:57;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:68; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:79.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:8;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:20;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:31;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:58;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:69; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:80.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:9;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:21;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:32;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:59;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:70; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:81.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:10 или 11;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:22;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:33;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:60;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:71; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:82.
В другом предпочтительном варианте осуществления антитело включает:
(a) CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:12;
(b) CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:23;
(c) CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:34;
(d) CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:61;
(e) CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:72; и
(f) CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:83.
Антитела, имеющие последовательности определенных зародышевых линий
В ряде вариантов осуществления антитело, соответствующее изобретению, включает вариабельную область тяжелой цепи из гена тяжелой цепи иммуноглобулина определенной зародышевой линии и/или вариабельную область легкой цепи из гена легкой цепи иммуноглобулина определенной зародышевой линии.
Как продемонстрировано в данном контексте, получены человеческие антитела, специфические в отношении IP-10, которые включают вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена человеческой зародышевой линии VH 3-33, гена VH 3-30.3, гена VH 5-51 или гена VH 4-61. Соответственно, изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает вариабельную область тяжелой цепи, которая является продуктом или происходит из гена человеческой зародышевой линии VH, выбранной из группы, состоящей из: VH 3-33, VH 3-30.3, VH 5-51 и VH 4-61. Предпочтительно, когда антитело специфично в отношении полипептида IP-10 человека (например, включающего последовательность Genbank Регистрационный No. NP_001556).
Кроме того, как продемонстрировано в данном контексте, получены человеческие антитела, специфические в отношении IP-10, которые включают вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена человеческой зародышевой линии Vk A27, гена Vk L15, гена Vk L6 или гена Vk L18. Соответственно, изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена человеческой зародышевой линии Vk, выбранной из группы, состоящей из: VkA27, Vk L15, Vk L6 и Vk L18. Предпочтительно, когда антитело специфично в отношении полипептида IP-10 человека (например, включающего последовательность Genbank Регистрационный No. NP_001556).
Предпочтительные антитела, соответствующие изобретению, представлены антителами, включающими вариабельную область тяжелой цепи, которая является продуктом или происходит из одного из вышеперечисленных генов человеческой зародышевой линии VH, а также включающими вариабельную область легкой цепи, которая является продуктом или происходит из одного из вышеперечисленных генов человеческой зародышевой линии Vk. Соответственно, в другом варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело включает:
(a) вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена человеческой зародышевой линии VH, выбранной из группы, состоящей из: VH 3-33, VH 3-30.3, VH 5-51 и VH 4-61; и
(b) вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена человеческой зародышевой линии Vk, выбранной из группы, состоящей из: Vk A27, Vk L15, Vk L6 и Vk L18. Предпочтительно, когда антитело является специфическим в отношении полипептида IP-10 человека (например, содержащего последовательность Genbank регистрационный No. NP_001556).
В изобретении представлены также антитела, включающие предпочтительные комбинации вариабельный областей тяжелой и легкой цепей, которые представляют собой продукт или выделены из генов человеческой зародышевой линии VH и Vk. Например, в предпочтительном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело:
(a) включает вариабельную область тяжелой цепи, которая представляет собой продукт или происходит из гена 3-33 VH человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:47);
(b) включает вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена A27, L15 или L6 Vk человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NONO:95, 98 и 97, соответственно); и
(c) специфически связывается с IP-10.
В одном варианте осуществления, антитело включает вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk A27 человека. Примеры антител, имеющих VH и VK VH 3-33 и Vk A27, соответственно, включают 1D4, 2G1, 6А5, 6А8, 10А12 и 10A12S. В другом варианте осуществления, антитело включает вариабельную область легкой цепи, которая представляет собой продукт или происходит из гена Vk L15 человека. Примером антитела, имеющего VH и VK VH 3-33 и Vk L15, соответственно, является 7С10. В другом варианте осуществления антитело включает вариабельную область легкой цепи гена Vk L6 человека. Примером антитела, имеющего VH и VK VH 3-33 и Vk L6, соответственно, является 1Е1.
В другом предпочтительном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело:
(a) включает вариабельную область тяжелой цепи гена VH 3-30.3 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:48) или выделенную из него;
(b) включает вариабельную область легкой цепи гена Vk L6 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:96) или выделенную из него; и
(c) специфически связывается с IP-10.
Примеры антител, имеющих VH и VK VH 3-30.3 и Vk L6, соответственно, включают 6В10 и 8F6.
В другом предпочтительном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело:
(a) включает вариабельную область тяжелой цепи гена VH 5-51 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:49) или выделенную из него;
(b) включает вариабельную область легкой цепи гена Vk L18 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:97) или выделенную из него; и
(c) специфически связывается с IP-10.
Примером антитела, имеющего VH и VK VH 5-51 и Vk L18, соответственно, является 3С4.
В еще одном предпочтительном варианте осуществления изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, причем антитело:
(a) включает вариабельную область тяжелой цепи гена VH 4-61 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:50) или выделенную из него;
(b) включает вариабельную область легкой цепи гена Vk A27 человека (который кодирует последовательность аминокислот, приведенную в SEQ ID NO:95) или выделенную из него; и
(c) специфически связывается с IP-10.
Примером антитела, имеющего VH и VK VH 4-61 и Vk A27, соответственно, является 13С4.
Как используют в данном контексте, человеческое антитело включает вариабельные области тяжелой и легкой цепи, т.е. "продукт" или "выделенное из" последовательности определенной зародышевой линии, если вариабельные участки антитела получены из системы, в которой используют гены иммуноглобулина человеческой зародышевой линии. Данные системы включают иммунизацию трансгенной мыши, несущей гены человеческого иммуноглобулина, антигеном, представляющим интерес, или скрининг библиотеки генов человеческого иммуноглобулина, представленной на фаге, с помощью антигена, представляющего интерес. Человеческое антитело, т.е. "продукт", или "выделенное из" последовательности иммуноглобулина человеческой зародышевой линии, может быть идентифицировано, как таковое, путем сравнения последовательности аминокислот человеческого антитела с последовательностями аминокислот иммуноглобулинов человеческой зародышевой линии и отбора последовательности иммуноглобулина человеческой зародышевой линии, которая наиболее близка по последовательности (т.е. с самым высоким % идентичности) к последовательности человеческого антитела. Человеческое антитело, которое представляет собой "продукт", или "выделенное из" последовательности иммуноглобулина определенной человеческой зародышевой линии, может содержать отличия аминокислот по сравнению с последовательностью зародышевой линии, обусловленные, например, естественными соматическими мутациями или целевой интродукцией сайт-направленной мутации. Однако, отобранное человеческое антитело, как правило, по последовательности аминокислот по меньшей мере на 90% идентично последовательности аминокислот, кодируемой геном иммуноглобулина человеческой зародышевой линии, и содержит остатки аминокислот, которые идентифицируют человеческое антитело, как являющееся человеческим при сравнении с последовательностями аминокислот иммуноглобулина зародышевой линии других видов (например, последовательностями мышиной зародышевой линии). В ряде случаев человеческое антитело по последовательности может быть по меньшей мере на 95%, или даже по меньшей мере на 96%, 97%, 98% или 99% идентичным последовательности аминокислот, кодируемой геном иммуноглобулина зародышевой линии. Как правило, человеческое антитело, выделенное из последовательности определенной человеческой зародышевой линии, будет обнаруживать не больше, чем 10 отличий аминокислот от последовательности аминокислот, кодируемой геном иммуноглобулина человеческой зародышевой линии. В ряде случаев человеческое антитело может обнаруживать не больше, чем 5, или даже не больше, чем 4, 3, 2 или 1 отличие аминокислот от последовательности аминокислот, кодируемой геном иммуноглобулина человеческой зародышевой линии.
Гомологичные антитела
В еще одном варианте осуществления антитело, соответствующее изобретению, включает вариабельные области тяжелой и легкой цепи, содержащие последовательности аминокислот, которые гомологичны последовательностям аминокислот предпочтительных антител, описанных в данном контексте, и при этом антитела сохраняют желательные функциональные свойства антител против IP-10, соответствующих изобретению.
Например, изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающую вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем:
(а) вариабельная область тяжелой цепи включает последовательность аминокислот, которая по меньшей мере на 80% гомологична последовательности аминокислот, выбранной из группы, состоящей из SEQ ID NONO:35-46;
(b) вариабельная область легкой цепи включает последовательность аминокислот, которая по меньшей мере на 80% гомологична последовательности аминокислот, выбранной из группы, состоящей из SEQ ID NONO:84-94;
(c) антитело специфически связывается с IP-10 и (а) антитело демонстрирует по меньшей мере одно из следующих функциональных свойств:
(i) антитело ингибирует связывание IP-10 с CXCR3;
(ii) антитело ингибирует индуцируемый IP-10 ток кальция;
(iii) антитело ингибирует индуцируемую IP-10 миграцию клеток;
(iv) антитело является перекрестно-реактивным с IP-10 макаки-резуса;
(v) антитело не является перекрестно-реактивным с мышиным IP-10;
(vi) антитело не является перекрестно-реактивным с человеческим MIG;
(vii) антитело не является перекрестно-реактивным с человеческим ITAC. В различных вариантах осуществления антитело может демонстрировать одно или более, два или более, три или более, четыре или более, пять или более либо шесть или более функциональных свойств, перечисленных как пункты (d)-(j) выше. Антитело может быть, например, человеческим антителом, гуманизированным антителом или химерным антителом.
В других вариантах осуществления, последовательности аминокислот VH и/или VL могут быть на 85%, 90%, 95%, 96%, 97%, 98% или 99% гомологичны вышеприведенными последовательностям. Антитело, имеющее области VH и VL, имеющие высокую (т.е. 80% или выше) гомологию с областями VH и VL SEQ ID NONO:35-46 и 84-94, соответственно, могут быть получены посредством мутагенеза (например, сайт-направленного или ПЦР (полимеразной цепной реакцией)-опосредованного мутагенеза) молекул нуклеиновых кислот, кодирующих SEQ ID NONO:35-46 и/или 84-94, с последующим тестированием кодируемого измененного антитела на сохраненную функцию (т.е., функций, приведенных в пунктах (c)-(j) выше) с использованием функциональных анализов, описанных в данном контексте.
Как используют в данном контексте, процент гомологии между двумя последовательностями аминокислот равен проценту идентичности между двумя последовательностями. Процент идентичности между двумя последовательностями представляет собой функцию числа идентичных положений, имеющихся в последовательностях (т.е., % гомологии=число идентичных положений/общее число положений×100), принимая во внимание число гэпов (разрывов) и длину каждого гэпа, которые необходимо вводить для оптимального элайнмента двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно осуществить с использованием математического алгоритма, как описано в неограничивающих примерах ниже.
Процент идентичности между двумя последовательностями аминокислот можно определить с использованием алгоритма, предложенного Е. Meyers и W. Miller (см. Comput. Appl. Biosci., 4:11-17, (1988)), который введен в программу ALIGN (версия 2.0) с помощью таблицы веса остатков РАМ 120, штрафа за длину гэпа 12 и штрафа за гэп 4. Кроме того, процент идентичности между двумя последовательностями аминокислот можно определить, используя алгоритм Needleman и Wunsch (см. J. Mol. Biol., 48:444-453, (1970)), который введен в программу GAP в программном пакете GCG (доступен по адресу http://www.gcg.com) с помощью матрицы Blossum 62 или матрицы РАМ250 и веса гэпов 16, 14, 12, 10, 8, 6, или 4 и веса длины 1, 2, 3, 4, 5, или 6.
Дополнительно или альтернативно, последовательности белка, соответствующие настоящему изобретению, кроме того, могут быть использованы как "последовательность-запрос" для проведения поиска в общедоступных базах данных с целью, например, идентификации родственных последовательностей. Данный поиск можно осуществить с использованием программы XBLAST (версия 2.0), предложенной в статье Altschul, et al. (1990) J. Mol. Biol. 215:403-10. Поиск белка в программе BLAST можно осуществить с помощью программы XBLAST, оценка = 50, длина слова = 3, для получения последовательностей аминокислот, гомологичных молекулам антитела, соответствующих изобретению. Для получения элайнментов с гэпами для целей сравнения, можно использовать программу Gapped BLAST, как описано в статье Altschul et al., (1997), Нуклеиновые кислоты Res., 25(17):3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать параметры умолчания соответствующих программ (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov.
Антитела с консервативными модификациями
В некоторых вариантах осуществления антитело, соответствующее изобретению, включает вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, где одна или более из данных последовательностей CDR включает заданные последовательности аминокислот, в основе которых лежат предпочтительные антитела, описанные в данном контексте (например, 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4), или их консервативные модификации и где антитела сохраняют желательные функциональные свойства антител против IP-10, соответствующих изобретению.
Соответственно, изобретение представляет выделенное моноклональное антитело или его антигенсвязывающую часть, включающие вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3 и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, причем:
(a) последовательность CDR3 вариабельной области тяжелой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:24-34 и их консервативных модификаций;
(b) последовательность CDR3 вариабельной области легкой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательность аминокислот SEQ ID NONO:73-83 и их консервативных модификаций;
(c) антитело специфически связывается с IP-10 и (а) антитело проявляет по меньшей мере одно следующих функциональных свойств:
(i) антитело ингибирует связывание IP-10 с CXCR3;
(ii) антитело ингибирует индуцируемый IP-10 ток кальция;
(iii) антитело ингибирует индуцируемую IP-10 миграцию клеток;
(iv) антитело является перекрестно реактивным с IP-10 макаки-резуса;
(v) антитело не является перекрести о-реактивным с мышиным IP-10;
(vi) антитело не является перекрестно-реактивным с человеческим MIG;
(vii) антитело не является перекрестно-реактивным с человеческим ITAC.
В предпочтительном варианте осуществления последовательность С DR2 вариабельной области тяжелой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:13-23 и их консервативных модификаций; и последовательность CDR2 вариабельной области легкой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:62-72 и их консервативных модификаций. В другом предпочтительном варианте осуществления последовательность CDR3 вариабельной области тяжелой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:1-12 и их консервативных модификаций; и последовательность CDR3 вариабельной области легкой цепи включает последовательность аминокислот, выбранную из группы, состоящей из последовательностей аминокислот SEQ ID NONO:51-61 и их консервативных модификаций.
В различных вариантах осуществления антитело может демонстрировать одно или более, два или более, три или более, четыре или более, пять или более, либо шесть или более функциональных свойств, перечисленных как пункты (d)-(j) выше. Данные антитела могут быть, например, человеческими антителами, гуманизированными антителами или химерными антителами.
Как используют в данном контексте, термин "консервативные модификации последовательности" предназначен для обозначения модификаций аминокислот, которые существенным образом не воздействуют или не изменяют характеристики связывания антитела, содержащего последовательность аминокислот. Данные консервативные модификации включают замены, добавления и делеции аминокислот. Модификации могут быть введены в антитело, соответствующее изобретению, стандартными методиками, известными в области техники, такими как сайт-направленный мутагенеэ и ПЦР-опосредованный мутагенез. Консервативными заменами аминокислот являются такие, в которых остаток аминокислоты замещается остатком аминокислоты, имеющим близкую боковую цепь. Семейства остатков аминокислот, имеющих близкие боковые цепи, определены в области техники. Данные семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными основными цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, серии, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин,метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, один или более остатков аминокислот на участках CDR антитела, соответствующего изобретению, могут быть замещены другими остатками аминокислот из одного и того же семейства боковых цепей, и измененное антитело может быть протестировано на сохраненную функцию (т.е. функции, приведенные в пунктах (c)-(j) выше) с использованием функциональных анализов, описанных в данном контексте.
Антитела, которые связываются с тем же самым эпитопом. что антитела против IP-10, соответствующие изобретению
В другом варианте осуществления изобретение представляет антитела, которые связываются с тем же эпитопом, что различные антитела против IP-10, соответствующие изобретению, представленные в данном контексте, такие как другие человеческие антитела, которые связываются с тем же эпитопом, что антитела 1D4, 1Е1, 2G1, 3C4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4, описанные в данном контексте.
Данные дополнительные антитела можно идентифицировать на основе их способности перекрестие конкурировать (например, конкурентно ингибировать связывание статистически значимым образом) с другими антителами, соответствующими изобретению, такими как 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4, в стандартных анализах связывания.
Способность тест-антитела ингибировать связывание, например, 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4 с человеческим IP-10 показывает, что тест-антитело может конкурировать за связывание с человеческим IP-10; данное антитело может в соответствии с неограничивающей теорией, связываться с тем же или родственным (например, структурно близким или пространственно проксимальным) эпитопом человеческого IP-10, как антитело с которым оно конкурирует.
В предпочтительном варианте осуществления антитело, которое связывается с тем же эпитопом на человеческом IP-10, что 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4, представляет собой человеческое моноклональное антитело. Данные человеческие моноклональные антитела можно получить и выделить, как описано в Примерах.
Сконструированные и модифицированные антитела
Кроме того, антитело, соответствующее изобретению, можно получить при использовании антитела, имеющего одну или более последовательностей VH и/или VL, описанных в данном контексте, в качестве исходного материала для конструирования модифицированного антитело, причем данное модифицированное антитело может иметь измененные свойства относительно исходного антитела. Антитело может быть сконструировано путем модификации одного или более остатков в одной или обеих вариабельных областях (т.е. VH и/или VL), например, на одном или более участков CDR и/или в одной или более скелетных областей. Дополнительно или альтернативно антитело можно сконструировать модификацией остатков в константной области(ях), например, для изменения эффекторной функции(й) антитела.
Одним из типов конструирования вариабельной области, который может быть осуществлен, является прививание CDR. Антитела взаимодействуют с антигенами-мишенями в основном через остатки аминокислот, которые находятся на шести участках определения комплементарности тяжелой и легкой цепи (CDR). По этой причине последовательности аминокислот в CDR более разнообразны у отдельных антител, чем последовательности вне CDR. Поскольку последовательности CDR отвечают за большинство взаимодействий антитело-антиген, возможно экспрессировать рекомбинантные антитела, которые имитируют свойства специфических естественных антител, путем конструирования экспрессионных векторов, которые включают последовательности CDR из специфического естественного антитела, привитые на скелетные последовательности из другого антитела с отличными свойствами (см., например, статьи Riechmann L et al., (1998), Nature, 332:323-327; Jones P. et al., (1986), Nature, 321:522-525; Queen C. et al., (1989), Proc. Natl. Acad. Sci. U.S.A., 86:10029-10033; Патент США No. 5225539, выданный Winter и Патенты США NoNo 5530101; 5585089; 5693762 и 6180370, выданные Queen et al.).
Соответственно, другой вариант осуществления изобретения относится к выделенному моноклональному антителу или его антигенсвязывающей части, включающим вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, включающие последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:1-12, SEQ ID NONO:13-23 и SEQ ID NONO:24-34, соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, включающие последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:51-61, SEQ ID NONO:62-72 и SEQ ID NONO:73-83, соответственно. Таким образом, данные антитела содержат последовательности CDR VH и VL моноклональных антител 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4, хотя могут содержать различные скелетные последовательности из данных антител.
Данные скелетные последовательности можно получить из общедоступных баз данных ДНК или опубликованных ссылок, которые включают последовательности гена антитела зародышевой линии. Например, последовательности ДНК зародышевой линии генов вариабельной области тяжелой и легкой цепи можно найти в базе данных последовательностей человеческой зародышевой линии "VBase" (доступной в Internet по адресу www.mrc-cpe.cam.ac.uk/vbase), а также в работах Kabat E. A., et al. (1991) Sequences of Proteins of Immunological Interest (Последовательности белков, представляющих иммунологический интерес), 5 изд., U.S. Department of Health и Human Services, NIH Publication No. 91-3242; Tomlinson I.M., et al., (1992), "The Repertoire of Human Germline VH Sequences Reveals about Fifty Groups of VH Segments with Different Hypervariable Loops" (Репертуар последовательностей VH человеческой зародышевой линии обнаруживает около пятидесяти групп сегментов VH с различными гипервариабельными петлями) J. Mol. Biol., 227:776-798; и Сох J.P.L. et al., (1994), "A Directory of Human Germline VH Segments Reveals a Strong Bias in their Usage" (Указатель сегментов VH человеческой зародышевой линии показывает важное направление в их применении), Eur. J. Immunol., 24:827-836, содержание каждой из которых специально включено в данном контексте в виде ссылки.
Предпочтительные скелетные последовательности для применения в антителах, соответствующих изобретению, представлены теми, которые структурно близки скелетным последовательностям, используемым в отобранных антителах, соответствующих изобретению, например, близким последовательностям VH 3-33, 3-30.3, 4-61 или 5-51 [SEQ ID NOS:47-50], и/или скелетным последовательностям Vk A27, L6, L18 или L15 [SEQ ID NOS:95-98], используемым в предпочтительных моноклональных антителах, соответствующих изобретению. Последовательности CDR1, 2 и 3 VH и последовательности CDR1, 2 и 3 VL можно привить на скелетные области, которые имеют последовательность, идентичную той, которая обнаружена в гене иммуноглобулина зародышевой линии, из которой происходит скелетная последовательность, или последовательности CDR можно привить на скелетные области, которые содержат одну или более мутаций по сравнению с последовательностями зародышевой линии. Например, показано, что в ряде случаев благоприятно подвергнуть мутации остатки в скелетных областях с целью поддержания или усиления антигенсвязывающей способности антитела (см., например, Патенты США NoNo 5530101, 5585089, 5693762 и 6180370, выданные Queen et al).
Другой тип модификации вариабельной области состоит в мутировании остатков аминокислот на участках CDR 1, CDR2 и/или CDR3 VH и/или VL, чтобы, таким образом, улучшить одну или более характеристик связывания (например, аффинность) антитела, представляющего интерес. Для интродукции мутации(й) можно осуществить сайт-направленный мутагенез или ПЦР-опосредованный мутагенез, и эффект на связывание антитела или другое функциональное свойство, представляющее интерес, можно оценить в анализах in vitro или in vivo, как описано в данном контексте и представлено в Примерах. Предпочтительно, когда интродуцируют консервативные модификации (как описано выше). Мутации могут представлять собой замены, добавления или делеции аминокислот, предпочтительно представляют собой замены. Более того, как правило, изменяют не более, чем один, два, три, четыре или пять остатков.
Соответственно, в другом варианте осуществления изобретение представляет выделенные моноклональные антитела против IP-10 или их антигенсвязывающие части, включающие вариабельную область тяжелой цепи, содержащую: (а) участок CDR1 VH, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:1-12, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению с SEQ ID NONO:1-12; (b) участок CDR2 VH, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:13-23, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению с SEQ ID NONO:13-23; (с) участок CDR3 VH, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:24-34, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению с SEQ ID NONO:24-34; (d) участок CDR1 VL, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:51-61, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению c SEQ ID NONO:51-61; (е) участок CDR2 VL, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:62-72, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению с SEQ ID NONO:62-72; и (f) участок CDR3 VL, включающий последовательность аминокислот, выбранную из группы, состоящей из SEQ ID NONO:73-83, или последовательность аминокислот, имеющую одну, две, три, четыре или пять замен, делеций или добавлений аминокислот по сравнению с SEQ ID NONO:73-83.
Предпочтительной замещающей мутацией, соответствующей изобретению, является замена остатка серина остатком цистеина в положении 32 в CDR1 цепи VH mAb (моноклонального антитела) 10А12. Данную модифицированную форму 10А12 обозначают в данном контексте 10A12S. Последовательность аминокислот цепи VH 10А12 показана в SEQ ID NO:44, и последовательность аминокислот цепи VH 10A12S показана в SEQ ID NO:45.
Сконструированные антитела, соответствующие изобретению, включают те, в которых сделаны модификации в скелетных остатках в VH и/или VL, например, с целью улучшения характеристик антитела. Как правило, данные скелетные модификации делают, чтобы снизить иммуногенность антитела. Например, один подход состоит в "обратном мутировании" одного или более скелетных остатков в соответствующую последовательность зародышевой линии. Более конкретно, антитело, которое было подвергнуто соматической мутации, может включать скелетные остатки, которые отличаются от последовательности зародышевой линии, из которой выделено антитело. Данные остатки можно идентифицировать путем сравнения скелетных последовательностей антитела с последовательностями зародышевой линии, из которой выделено антитело. Например, для 6А5 остаток аминокислоты No 2 (в FR1) VH представляет собой метионин, тогда как данный остаток в соответствующей VH последовательности зародышевой линии 3-33 представляет собой валин (см. Фигуру 23). Для того, чтобы возвратить последовательности скелетной области в конфигурации их зародышевой линии соматические мутации могут быть подвергнуты "обратному мутированию" к последовательности зародышевой линии посредством, например, сайт-направленного мутагенеза или ПЦР-опосреАованного мутагенеза (например, остаток 2 VH 6А5 можно подвергнуть "обратной мутации" из метионина в валин). Предусматривается, что изобретение охватывает также данные антитела, подвергнутые "обратной мутации".
Другой тип скелетной модификации включает мутирование одного или более остатков в скелетной области или даже на одном или более участков CDR с целью удаления Т-клеточных эпитопов, чтобы, таким образом, снизить потенциальную иммуногенность антитела. Данный подход называют также "деиммунизацией", и он более детально описан в Патентной публикации США No. 20030153043, поданной Carr et al.
Вдополнение или альтернативно модификациям, сделанным в скелетных областях или на участках CDR, антитела, соответствующие изобретению, можно сконструировать таким образом, чтобы они включали модификации в области Fc, как правило, с целью изменения одной или более функциональных характеристик антитела, таких как полупериод существования в сыворотке, связывание комплемента, связывание Fc рецептора и/или антигензависимая клеточная цитотоксичность. Более того, антитело, соответствующее изобретению, может быть модифицировано химическим путем (например, к антителу можно присоединить одну или более химических групп) или модифицировано с целью изменения его гликозилирования также с целью изменения одной или более функциональных характеристик антитела. Каждый из данных вариантов осуществления описан более детально ниже. Нумерация остатков в области Fc такая, как в указателе EU Kabat.
В одном варианте осуществления шарнирная область СН1 модифицирована так, что изменено число остатков цистеина в шарнирной области, например, уменьшено или увеличено. Данный подход описан далее в Патенте США No. 5677425, выданном Bodmeret al. Число остатков цистеина в шарнирной области СН1 изменено для того, чтобы, например, облегчить сборку легкой и тяжелой цепей или чтобы повысить или понизить стабильность антитела.
В другом варианте осуществления шарнирная область Fc антитела подвергают мутации с целью снижения биологического полупериода существования антитела. Более подробно, одну или более мутаций аминокислот интродуцируют в область раздела домена СН2-СН3 шарнирного фрагмента Fc, так что у антитела имеется нарушение связывания стафилококкового белка A (SpA) относительно связывания нативного домена шарнира Fc SpA. Данный подход описан более подробно в Патенте США No. 6165745, выданном Ward et al.
В другом варианте осуществления антитело модифицируют, чтобы увеличить его биологический полупериод существования. Возможны различные подходы. Например, можно интродуцировать одну или более из следующих мутаций: T252L, T254S, T256F, как описано в Патенте США No. 6277375, выданном Ward. Альтернативно для увеличения биологического полупериода существования антитело можно изменить в области СН1 или CL для того, чтобы оно содержало эпитоп связывания утилизирующего рецептора, взятого из двух петель домена СН2 области Fc IgG, как описано в Патентах США NoNo. 5869046 и 6121022, выданных Presta et al.
В следующих вариантах осуществления область Fc изменяют замещением по меньшей мере одного остатка аминокислоты другим остатком аминокислоты с целью изменения эффекторной функции(й) антитела. Например, одна или более аминокислот, выбранных из остатков аминокислот 234, 235, 236, 237, 297, 318, 320 и 322, может быть замещена другим остатком аминокислоты так, что антитело имеет измененную аффинность в отношении лиганда эффектора, но сохраняет антигенсвязывающую способность родительского антитела. Лигандом эффектора, к которому изменена аффинность, может быть, например, Fc рецептор или компонент комплемента С1. Данный подход описан более подробно в Патентах США NoNo 5624821 и 5648260, оба из которых выданы Winter et al. В другом примере одна или более аминокислот, выбранных их остатков аминокислот 329, 331 и 322 может быть замещена другим остатком аминокислоты так, чтобы антитело имело измененное связывание C1q и/или пониженную или устраненную комплемент-зависимую цитотоксичность (CDC). Данный подход описан более подробно в Патенте США No 6194551, выданном Idusogie et al.
В другом случае один или более остатков аминокислот в положениях аминокислот 231 и 239 изменены, чтобы таким образом изменить способность антитела связывать комплемент. Данный подход подробно описан в публикации РСТ WO 94/29351, поданной Bodmer et al.
В еще одном случае область Fc модифицирована с целью повышения способности антитела опосредовать антитело-зависимую клеточную цитотоксичность (ADCC) и/или для повышения аффинности антитела к рецептору Fey путем модификации одной или более аминокислот в следующих положениях: 238, 239, 248, 249, 252, 254, 255, 256, 258, 265, 267, 268, 269, 270, 272, 276, 278, 280, 283, 285, 286, 289, 290, 292, 293, 294, 295, 296, 298, 301, 303, 305, 307, 309, 312, 315, 320, 322, 324, 326, 327, 329, 330, 331, 333, 334, 335, 337, 338, 340, 360, 373, 376, 378, 382, 388, 389, 398, 414, 416, 419, 430, 434, 435, 437, 438 или 439.
Данный подход описан далее в Публикации PCT WO 00/42072, поданной Presta. Более того, картированы сайты связывания на человеческом IgG1 для FcγR1, FcγRII, FcγRIII и FcRn и описаны варианты с улучшенным связыванием (см. статью Shields R.L.et al., (2001), J. Biol. Chem., 276:6591-6604). Показано, что специфические мутации в положениях 256, 290, 298, 333, 334 и 339 улучшают связывание с FcγRIII. Кроме того, показано, что следующая комбинация мутантов улучшает связывание FcγRIII: T256A/S298A, S298A/E333A, S298A/K224A и S298A/E333A/K334A.
В еще одном варианте осуществления модифицируют гликозилированием антитела. Например, можно получить дегликозилированное антитело (т.е., антитело, не имеющее гликозилирования). Гликозилирование можно изменить для того, чтобы, например, повысить аффинность антитела к антигену. Данные модификации углеводов можно осуществить, например, путем изменения одного или более центров гликозилирования в последовательности антитела. Например, можно сделать одну или более замещений аминокислот, которые в результате приведут к элиминации одного или более центров гликозилирования скелетной части вариабельной области, чтобы таким образом элиминировать гликозилирование в данном центре. Данное дегликозилирование может повысить аффинность антитела к антигену. Такой подход описан более подробно в Патентах США NoNo 5714350 и 6350861, выданных Со et al.
Дополнительно или альтернативно можно получить антитело, которое имеет измененный тип гликозилирования, такое как гипофукозилированное антитело с уменьшенными количествами остатков фукозила или антитело, имеющее структуры GlcNac с повышенным уровнем ветвления. Данные типы измененного гликозилирования, как показано, повышают ADCC способность антител. Такие модификации углеводов можно осуществить, например, путем экспрессии антитела в клетке-хозяине с измененным механизмом гликозилирования. Клетки с измененным механизмом гликозилирования описаны в уровне техники и могут быть использованы в качестве клеток-хозяев для экспрессии рекомбинантных антител, соответствующих изобретению, чтобы таким образом получить антитело с измененным гликозилированием. Например, в ЕР 1176195, поданной Hanai et al., описана клеточная линия с функционально разрушенным геном FUT8, который кодирует фукозилтрансферазу, так что антитела, экспрессируемые в данной клеточной линии, демонстрируют гипогликозилирование. В Публикации РСТ WO 03/035835, поданной Presta, описан вариант клеточной линии СНО, клетки Lec13 с пониженной способностью присоединять фукозу к Asn(297)-связанным углеводам, что приводит также к гипофукозилированию антител, экспрессируемыхданной клеткой-хозяином (см. также статью Shields R.L et al., (2002), J. Biol. Chern., 277:26733-26740). В Публикации РСТ WO 99/54342, поданной Umana et al. описаны клеточные линии, сконструированные для экспрессии гликопротеин-модифицирующих гликозилтрансфераз (например, β(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII)), так что антитела, экспрессированные в сконструированных клеточных линиях, демонстрируют повышенный уровень ветвления структур GlcNac, что приводит в результате к повышенной активности ADCC антител (см. также статью Umana et al., (1999), Nat. Biotech., 17:176-180).
Другая модификация антител в данном контексте, которая рассматривается в изобретении, представляет собой пегилирование. Антитело можно пегилировать, чтобы, например, увеличить биологический (например, в сыворотке) полупериод существования антитела. Для того, чтобы пегилировать антитело, как правило, проводят реакцию антитела или его фрагмента с полиэтиленгликолем (ПЭГ), таким как реакционное сложноэфирное или альдегидное производное ПЭГ, в условиях, при которых одна или более групп ПЭГ присоединяются к антителу или фрагменту антитела. Предпочтительно, когда пегилирование осуществляют через реакцию ацилирования или реакцию алкилирования с использованием реакционной молекулы ПЭГ (или аналогичного реакционного водорастворимого полимера). Как используют в данном контексте, термин "полиэтиленгликоль" предназначен для охвата любой из форм ПЭГ, которые были использованы для дериватизации других белков, такую как моно(С1-С10)-алкокси- или арилоксиполиэтиенгликоль или полиэтиленгликоль-малеимид. В ряде вариантов осуществления антитело, предназначенное для пегилирования, представляет собой дегликозилированное антитело. Способы пегилирования белков известны в области техники и могут быть применены к антителам, соответствующим изобретению. См., например, ЕР 0 154 316, поданную Nishimura et al. и ЕР О 401 384, поданную Ishikawa et al.
Способы конструирования антител
Как обсуждалось выше, антитела против IP-10, имеющие последовательности VH и VL, описанные в данном контексте, могут быть использованы для создания новых антител против IP-10 путем модификации последовательностей VH и/или VL либо присоединенной к ним константной области(ей). Таким образом в другом аспекте изобретения структурные характеристики антитела против IP-10, соответствующего изобретению, например, 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4, используют для создания структурно близких антител против IP-10, которые сохраняют по меньшей мере одну функциональное свойство антител, соответствующих изобретению, такое как связывание с человеческим IP-10 и IP-10 макаки-резуса, но не мышиного IP-10 или человеческого MIG либо человеческого ITAC, а также ингибирование одного или более функциональных свойств IP-10 (например, связывание CXCR3, ток кальция, хемотаксис). Например, один или более участков CDR 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12, 10A12S или 13С4 или их мутаций можно скомбинировать рекомбинантным путем с известными скелетными участками и/или другими CDR с целью создания дополнительных сконструированных рекомбинантным путем антител против IP-10, соответствующих изобретению, как обсуждалось выше. Другие типы модификаций включают те, которые описаны в предшествующем разделе. Исходным материалом для способа конструирования являются одна или более из последовательностей VH и/или VL, представленных в данном контексте, или один или более их участков CDR. Для создания сконструированного антитело, не является необходимым действительно получать (т.е. экспрессировать в виде белка) антитело, имеющее одну или более из последовательностей VH и/или VL, представленных в данном контексте, или один или более их участков CDR. Точнее, информацию, содержащуюся в последовательности(ях), используют в качестве исходного материала для создания последовательности(ей) "второго поколения", полученных из исходной последовательности(ей), а затем получают последовательность(и) "второго поколения" и экспрессируют в виде белка.
Соответственно, в другом варианте осуществления изобретение представляет способ получения антитела против IP-10, предусматривающий:
(a) получение (i) последовательности вариабельной области тяжелой цепи антитела, включающей последовательность CDR 1, выбранную из группы, состоящей из SEQ ID NONO:1-12, последовательность CDR2, выбранную из группы, состоящей из SEQ ID NONO:13-23, и/или последовательность CDR3, выбранную из группы, состоящей из SEQ ID NONO:24-34; и (ii) последовательности вариабельной области легкой цепи антитело, включающей последовательность CDR1, выбранную из группы, состоящей из SEQ ID NONO:51-61, последовательность CDR2, выбранную из группы, состоящей из SEQ ID NONO:62-72, и/или последовательность CDR3, выбранную из группы, состоящей из SEQ ID NONO:73-83;
(b) изменение по меньшей мере одного остатка аминокислоты в последовательности вариабельной области тяжелой цепи антитела и/или последовательности вариабельной области легкой цепи антитела для создания по меньшей мере одной измененной последовательности антитела; и
(с) экспрессию измененной последовательности антитела в виде белка.
Для получения и экспрессии измененной последовательности антитела можно использовать стандартные методики молекулярной биологии.
Предпочтительно, когда антитело, кодируемое измененной последовательностью(ями) антитела, представляет собой антитело, сохраняющее одно, несколько или все функциональные свойства антител против IP-10, описанных в данном контексте, причем данные функциональные свойства включают, но без ограничения перечисленным:
(i) специфически связывается с человеческим IP-10;
(ii) ингибирует связывание IP-10 с CXCR3;
(iii) ингибирует индуцируемый IP-10 ток кальция;
(iv) ингибирует индуцируемую IP-10 миграцию клеток;
(v) перекрестно реагирует с IP-10 макаки-резуса;
(vi) не является перекрестно-реактивным с мышиным IP-10;
(vii) не является перекрестно-реактивным с человеческим MIG; и (viii) не является перекрестно-реактивным с человеческим ITAC. Измененное антитело может демонстрировать одно или более, два или более, три или более, четыре или более, пять или более, шесть либо семь или более функциональных свойств, перечисленных как пункты (i)-(viii) выше.
Функциональные свойства измененных антител можно оценить с использованием стандартных анализов, имеющихся в области техники и/или описанных в данном контексте, таких как приведены в Примерах (например, ELISA, анализы тока кальция, анализа хемотаксиса).
В некоторых вариантах осуществления способов конструирования антител, соответствующих изобретению, мутации могут быть случайным образом или селективно интродуцированы на протяжении всей или части последовательности, кодирующей антитело против IP-10, и полученные в результате модифицированные антитела против IP-10 могут быть подвергнуты скринингу на активность связывания и/или другие функциональные свойства, как описано в данном контексте. Мутационные способы описаны в уровне техники. Например, в Публикации РСТ WO 02/092780, поданной Short, описаны способы создания и скрининга мутаций антител с помощью насыщающего мутагенеза, сборки путем синтетического лигирования или их комбинации. Альтернативно в Публикации РСТ WO 03/074679 Lazar et al. описывают способы использования компьютеризированных методов скрининга с целью оптимизации физико-химических свойств антител.
Молекулы нуклеиновых кислот, кодирующие антитела, соответствующие изобретению
Другой аспект изобретения относится к молекулам нуклеиновых кислот, которые кодируют антитела, соответствующие изобретению. Нуклеиновые кислоты могут находиться в целых клетках, в клеточном лизате или в частично или практически чистой форме. Нуклеиновая кислота является "выделенной" или "полученной практически чистой", когда она очищена от других клеточных компонентов и иных примесей, например, других клеточных нуклеиновых кислот или белков, стандартными методиками, включая обработку щелочью/SDS (додецилсульфатом натрия), разделение на полосы в CsCl, колоночную хроматографию, электрофорез в агарозном геле и другие, известные в области техники. См. монографию под ред. F. Ausubel et al., (1987), Current Protocols in Molecular Biology (Современные методики в молекулярной биологии), Greene Publishing и Wiley Interscience, New York. Нуклеиновая кислота, соответствующая изобретению, может быть представлена, например, ДНК или РНК и может содержать или не содержать интронные последовательности. В предпочтительном варианте осуществления нуклеиновая кислота представляет собой молекулу кДНК.
Нуклеиновые кислоты, соответствующее изобретению, могут быть получены с использованием стандартных молекулярно-биологических методик. Для антител, экспрессируемых гибридомами (например, гибридомами, полученными из трансгенных мышей, несущих гены иммуноглобулина человека, как подробно описано ниже), кДНК, кодирующие легкие и тяжелые цепи антитела, созданные с помощью гибридомы, можно получить стандартными методами ПЦР-амплификации или клонирования кДНК. Для антител, полученных из библиотеки генов иммуноглобулина (например, при использовании методик представления на фагах), нуклеиновая кислота, кодирующая антитело, может быть получена из библиотеки.
Предпочтительные молекулы нуклеиновой кислоты, соответствующие изобретению, представляют собой молекулы, кодирующие последовательности VH и VL моноклональных антител 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 или 13С4. Последовательности ДНК, кодирующие последовательности VH 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4, представлены в SEQ ID NONO:99-109, соответственно. Последовательности ДНК, кодирующие последовательности VL 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4, представлены в SEQ ID NONO:110-120, соответственно.
После получения фрагментов ДНК, кодирующих сегменты Vk и VL, с данными фрагментами ДНК могут быть проведены дальнейшие манипуляции с помощью стандартных технологий рекомбинантной ДНК, например, с целью превращения генов вариабельной области в гены цепи антитела полной длины, в гены фрагмента Fab или ген scFv.
В данных манипуляциях фрагмент ДНК, кодирующий VL или VH, функционально связан с другим фрагментом ДНК, кодирующим другой белок, такой как константная область антитела или гибкий линкер. Термин "функционально связанный", как используют в данном контексте, предназначен для обозначения того, что два фрагмента ДНК соединены так, что последовательности аминокислот, кодируемые двумя фрагментами ДНК, остаются в рамке считывания.
Выделенную ДНК, кодирующую область VH, можно превратить в ген тяжелой цепи полной длины посредством функционального связывания ДНК, кодирующей VH, с другой молекулой ДНК, кодирующей константные области тяжелой цепи (СН1, СН2 и СН3). Последовательности генов константной области тяжелой цепи человека известны в области техники (см., например, работу Kabat E. A. et al., (1991), Sequences of Proteins of Immunological Interest (Последовательности белков, представляющих иммунологический интерес), 5 изд., U.S. Department of Health и Human Services, NIH Publication No. 91-3242), и фрагменты ДНК, охватывающие данные области, можно получить с помощью стандартной ПЦР-амплификации. Константная область тяжелой цепи может быть представлена константной областью IgG1, IgG2, IgG3, IgG4, IgA, IgE, IgM или IgD, но наиболее предпочтительно является константной областью IgG1 или IgG4. Для гена фрагмента Fab тяжелой цепи ДНК, VH -кодирующая ДНК может быть функционально связана с другой молекулой ДНК, кодирующей только константную область СН1 тяжелой цепи.
Выделенную ДНК, кодирующую область Vk, можно превратить в ген легкой цепи полной длины (а также в ген Fab легкой цепи) посредством функционального связывания ДНК, кодирующей Vk, с другой молекулой ДНК, кодирующей константную область легкой цепи CL. Последовательности генов константной области легкой цепи человека известны в области техники (см., например, работу Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest (Последовательности белков, представляющих иммунологический интерес), 5 изд., U.S. Department of Health и Human Services, NIH Publication No. 91-3242) и фрагменты ДНК, охватывающие данные области, можно получить с помощью стандартной ПЦР-амплификации.
Константная область легкой цепи может быть представлена каппа- или λ-константной областью, но наиболее предпочтительно является каппа-константной областью.
Для создания гена scFv фрагменты ДНК, кодирующие VH и VL, функционально связываютс другим фрагментом, кодирующим гибкий линкер, например, кодирующим последовательность аминокислот (Gly4-Ser)3, так, чтобы последовательности VH и VL можно было экспрессировать как непрерывный одноцепочечный белок с областями VL и VH, соединенными с гибким линкером (см., например, статьи Bird et al., (1988), Science, 242:423-426; Huston et al., (1988), Proc. Natl. Acad. Sci. USA, 85:5879-5883; McCafferty et al., (1990), Nature, 348:552-554).
Получение моноклональных антител, соответствующих изобретению
Моноклональные антитела (mAbs), соответствующие настоящему изобретению, можно получить множеством методик, включая принятую методику получения моноклональных антител например, стандартный метод гибридизации соматических клеток, предложенный Kohler и Milstein, (1975), Nature, 256: 495. Хотя предпочтительны способы гибридизации клеток, в принципе могут быть использованы другие методики получения моноклонального антитела, например, вирусная или онкогенная трансформация В-лимфоцитов.
Предпочтительной системой с использованием животных для получения гибридом является система на мышах. Получение гибридомы в мышах представляет собой очень хорошо разработанную методику. Протоколы иммунизации и методики выделения иммунизированных спленоцитов для слияния известны в области техники. Известны также партнеры для слияния (например, клетки мышиной миеломы) и способы слияния.
Химерные или гуманизированные антитела, соответствующие настоящему изобретению, можно получить на основе последовательности мышиного моноклонального антитела, полученного, как описано выше. ДНК, кодирующую тяжелую и легкую цепи иммуноглобулина, можно получить из мышиной гибридомы, представляющей интерес, и сконструировать, чтобы они включали последовательности немышиного (например, человеческого) иммуноглобулина, используя стандартные молекулярно-биологические методики. Например, для создания химерного антитела мышиные вариабельные области могут быть связаны с человеческими константными областями при использовании способов, известных в области техники (см., например, Патент США No. 4816567, выданный Cabilly et al.). Для создания гуманизированного антитела мышиные участки CDR могут быть введены в человеческий скелет при использовании способов, известных в области техники (см., например, Патент США No. 5,225,539, выданный Winter, и Патенты США NoNo. 5530101, 5585089, 5693762 и 6180370, выданные Queen et al.).
В предпочтительном варианте осуществления антитела, соответствующие изобретению, представляют собой человеческие моноклональные антитела. Данные человеческие моноклональные антитела, направленные против IP-10, можно генерировать, используя трансгенных или трансхромосомных мышей, несущих части человеческой иммунной системы, а не мышиной системы. Данные трансгенные или трансхромосомные мыши включают мышей, называемых в данном контексте мыши HuMAb и мыши КМ, соответственно и совместно называемых в данном контексте "мыши с человеческим Ig". Мышь HuMAb® (Medarex, Inc.) несет минилокусы гена человеческого иммуноглобулина, которые кодируют переаранжированные последовательности тяжелой (µ и γ) и каппа-легкой цепей человеческого иммуноглобулина вместе с направленными мутациями, которые инактивируют эндогенные локусы µ- и каппа-цепей (см., например, статью Lonberg et al., (1994), Nature, 368(6474):856-859). Соответственно, мыши демонстрируют пониженную экспрессию мышиного IgM или каппа, и в ответ на иммунизацию в интродуцированных трансгенах человеческой тяжелой и легкой цепей происходит переключение класса и соматическая мутация, направленные на генерацию высокоаффинных человеческих моноклональных IgGкаппа (см, статью Lonberg N. et al., (1994), выше; обзор Lonberg N., (1994), Handbook of Experimental Pharmacology (Справочник по экспериментальной фармакологии), 113:49-101; статьи Lonberg N. и Huszar D., (1995), Intern. Rev. Immunol., 13:65-93, а также Harding F. и Lonberg N., (1995), Ann. N.Y. Acad. Sci., 764:536-546). Получение и применение мышей HuMab и геномных модификаций, которые несут данные мыши, подробно описано в статьях Taylor L. et al., (1992) Nucleis Acids Research, 20:6287-6295; Chen, J. et al., (1993), International Immunology, 5:647-656; Tuaillon et al., (1993), Proc. Natl. Acad. Sci. USA, 90:3720-3724; Choi et al., (1993), Nature Genetics, 4:117-123; Chen J. et al., (1993), EMBO J. 12:821-830; Tuaillon et al., (1994), J. Immunol., 152:2912-2920; Taylor L et al., (1994), International Immunology, 6:579-591 и Fishwild D. et al., (1996), Nature Biotechnology, 14:845-851, содержание всех из них таким образом специально включено в данном контексте в виде ссылки во всей их полноте. Кроме того, см. Патенты США NoNo 5545806, 5569825, 5625126, 5633425, 5789650, 5877397, 5661016, 5814318, 5874299 и 5770429, все из которых выданы Lonberg и Kау; Патент США No. 5545807, выданный Suraniet al.; Публикации РСТ NoNo WO 92/03918, WO 93/12227, WO 94/25585, WO 97/13852, WO 98/24884 и WO 99/45962, все из которых поданы Lonberg и Kау, и Публикацию РСТ No. WO 01/14424, поданную Korman et al.
В другом варианте осуществления человеческие антитела, соответствующие изобретению, можно получить с использованием мыши, которая несет последовательности человеческого иммуноглобулина на трансгенах и трансхромосомах, например, мышь, которая несет трансген человеческой тяжелой цепи и трансхромосому человеческой легкой цепи. Данные мыши, называемые в данном контексте "мыши КМ", детально описаны в Публикации РСТ WO 02/43478, поданной Ishida et al.
Кроме того, альтернативные системы трансгенных животных, экспрессирующие гены человеческого иммуноглобулина, имеются в уровне техники и могут быть использованы для стимуляции образования антител против IP-10, соответствующих изобретению. Например, можно использовать альтернативную трансгенную систему, называемую Xenomouse (Abgenix, Inc.), данные мыши описаны, например, в Патентах США NoNo 5939598, 6075181, 6114598, 6150584 и 6162963, выданных Kucherlapati et al.
Более того, альтернативные системы трансхромосомных животных, экспрессирующие гены человеческого иммуноглобулина, имеются в уровне техники и могут быть использованы для стимуляции образования антител против IP-10, соответствующих изобретению. Например, можно использовать мышей, несущих как трансхромосому человеческой тяжелой цепи, так и трансхромосому человеческой легкой цепи, называемых "мыши ТС", данные мыши описаны в статье Tomizuka et al., (2000), Proc. Natl. Acad. Sci. USA, 97:722-727. Кроме того, коровы, несущие трансхромосомы человеческих тяжелой и легкой цепей (см. статью Kuroiwa et al., (2002), Nature Biotechnology, 20:889-894), описаны в уровне техники и могут быть использованы для стимуляции образования антител против IP-10, соответствующих изобретению.
Человеческие моноклональные антитела, соответствующие изобретению, можно также получить, используя способы представления на фагах для скрининга библиотек генов человеческого иммуноглобулина. Данные способы представления на фагах с целью выделения человеческих антител разработаны в уровне техники. См., например: Патенты США NoNo. 5223409, 5403484 и 5571698, выданные Ladner et al., Патенты США NoNo. 5427908 и 5580717, выданные Dower et al., Патенты США NoNo. 5969108 и 6172197, выданные McCafferty et al. и Патенты США NoNo. 5885793, 6521404, 6544731, 6555313, 6582915 и 6593081, выданные Griffiths et al.
Человеческие моноклональные антитела, соответствующие изобретению, могут быть также получены с использованием мышей SCID, у которых человеческие иммунные клетки восстановлены так, что путем иммунизации можно генерировать ответ человеческих антител. Данные мыши описаны, например, в Патентах США NoNo 5476996 и 5698767, выданных Wilson et al.
Иммунизация мышей с человеческим Ig
Когда мышей с человеческим Ig используют для стимуляции образования человеческих антител, соответствующих изобретению, данных мышей можно иммунизировать очищенным или обогащенным препаратом антигена IP-10 и/или рекомбинантного IP-10 или слитым белком IP-10, как описано в статьях Lonberg N. et al., (1994), Nature, 368(6474):856-859; Fishwild D. et al., (1996), Nature Biotechnology, 14:845-851 и Публикациях РСТ WO 98/24884 и WO 01/14424. Предпочтительно, когда возраст мышей составляет 6-16 недель при первой инфузии. Например, для внутрибрюшинной иммунизации мышей с человеческим Ig можно использовать очищенный или рекомбинантный препарат (5-50 мкг) антигена IP-10.
Детальные методики генерации полностью человеческих моноклональных антител к IP-10 описаны ниже в Примере 1. Накопленный с различными антигенами опыт показал, что трансгенные мыши реагируют, когда их исходно иммунизируют внутрибрюшинно (IP) антигеном в полном адъюванте Фрейнда с последующими IP иммунизациями через неделю (всего до 6 раз) антигеном в неполном адъюванте Фрейнда. Однако, показано также, что эффективны другие адъюванты, кроме Фрейнда. Кроме того, обнаружено, что целые клетки в отсутствие адъюванта являются высокоиммуногенными. Иммунный ответ можно мониторировать в ходе протокола иммунизации с использованием образцов плазмы, получаемых при ретроорбитальном отборе крови. Плазму можно исследовать с помощью ELISA (как описано ниже), и мыши с достаточными титрами человеческого иммуноглобулина против IP-10 могут быть использованы для слияний. Мышам можно сделать внутривенное бустерное введение антигена за 3 дня до умерщвления и удаления селезенки. Ожидают, что для каждой иммунизации может быть необходимо провести 2-3 вливания. Для каждого антигена, как правило, иммунизируют от 6 до 24 мышей. Обычно используют оба штамма, НСо7 и НСо12. Кроме того, оба трансгена, НСо7 и НСо12, могут быть гибридизованы друг с другом в одной мыши, несущей два различных трансгена человеческой тяжелой цепи (НСо7/НСо12).
Генерация гибридом, продуцирующих человеческие моноклональные антитела, соответствующие изобретению
Для генерации гибридом, продуцирующих человеческие моноклональные антитела, соответствующие изобретению, можно выделить спленоциты и/или клетки лимфатических узлов иммунизированных мышей и слить с подходящей линией иммортализованных клеток, таких как клеточная линия мышиной миеломы. Полученные в результате гибридомы могут быть подвергнуты скринингу на продукцию антигенспецифических антител. Например, одноклеточные суспензии лимфоцитов поджелудочной железы иммунизированных мышей могут быть слиты с одной шестой числа несекретирующих клеток мышиной миеломы Р3Х63-Ag8.653 (АТСС, CRL 1580) при использовании 50% ПЭГ. Клетки помещают приблизительно по 2×105 в плоскодонные чашки для микротитрования с последующим двухнедельным инкубированием в селективной среде, содержащей 20% эмбриональной клональной сыворотки, 18% кондиционированной среды 653, 5% оригена (IGEN), 4 мМ L-глутамина, 1 мМ пирувата натрия, 5 мМ HEPES, 0,055 мМ 2-меркаптоэтанола, 50 единиц/мл пенициллина, 50 мг/мл стрептомицина, 50 мг/мл гентамицина и 1Х HAT (Sigma; HAT добавляют через 24 часа после слияния). Приблизительно через две недели клетки можно культивировать в среде, в которой HAT заменяют на НТ. Затем может быть проведен скрининг отдельных клеток с помощью ELISA на человеческие моноклональные антитела IgM и IgG. После того, как произойдет обширный рост гибридомы, среду обычно исследуют через 10-14 дней. Гибридомы, секретирующие антитело, могут быть перенесены на другие чашки, снова подвергнуты скринингу и, если они еще положительны по человеческому IgG, моноклональные антитела могут быть субклонированы по меньшей мере дважды путем ограничивающего разведения. Стабильные субклоны затем можно культивировать in vitro для генерации маленьких количеств антитело в среде для тканевой культуры с целью характеризации.
Для очистки человеческих моноклональных антител отобранные гибридомы могут быть выращены в двухлитровых роллерных колбах для очистки моноклональных антител. Супернатанты можно отфильтровать и концентрировать перед проведением аффинной хроматографии с белок А-сефарозой (Pharmacia, Piscataway, N.J.). Элюированные IgG можно проверить с помощью гель-электрофореза и высокоэффективной жидкостной хроматографии для того, чтобы удостовериться в их чистоте. Буферный раствор можно заменить на PBS (забуференный фосфатом солевой раствор), и концентрацию можно определить по OD280 (оптической плотности), используя коэффициент экстинкции 1,43. Можно взять аликвоты моноклональных антитела и хранить при -80°С. Генерация трансфектом. продуцирующих моноклональные антитела. соответствующие изобретению
Антитела, соответствующие изобретению, можно также получить в трансфектоме клетки-хозяина, используя, например, комбинацию технологий рекомбинантной ДНК и способы трансфекции генов, как хорошо известно в области техники (см., например, статью Morrison S., (1985), Science, 229:1202).
Например, для экспрессии антител, или их фрагментов ДНК, кодирующие частичные или полной длины легкие и тяжелые цепи, могут быть получены с помощью стандартных молекулярно-биологических методик (например, ПЦР-амплификации или клонирования кДНК с использованием гибридомы, которая экспрессирует антитело, представляющее интерес), и ДНК могут быть введены в экспрессионные векторы так, чтобы гены были функционально связаны с последовательностями контроля транскрипции и трансляции. В данном контексте, термин "функционально связанный" предназначен для обозначения того, что ген антитела лигирован в вектор таким образом, что последовательности контроля транскрипции и трансляции в векторе осуществляют предназначенную им функцию регуляции транскрипции и трансляции генов антитела. Экспрессионный вектор и последовательности контроля экспрессии выбирают так, чтобы они были совместимы с используемой клеткой-хозяином экспрессии. Ген легкой цепи антитела и ген тяжелой цепи антитела можно ввести в отдельный вектор или, более типично, оба гена вводят в один и тот же экспрессионный вектор. Гены антител вводят в экспрессионный вектор стандартными методами (например, лигирование комлементарных рестрики ценных сайтов на фрагменте гена антитела и вектора или лигирование тупых концов при отсутствии каких-либо рестрикционных сайтов). Вариабельные области легкой и тяжелой цепей антител, описанные в данном контексте, можно использовать для создания генов антитела полной длины любого изотипа антитела путем их инсерции в экспрессионные векторы, уже кодирующие константные области тяжелой цепи и константные области легкой цепи желательного изотипа, так, чтобы сегмент VH был функционально связан с сегментом(ами) CL в векторе и сегмент VL был функционально связан с сегментом CL в векторе. Дополнительно или альтернативно рекомбинантный экспрессионный вектор может кодировать сигнальный пептид, который способствует секреции цепи антитела из клетки-хозяина. Ген цепи антитела может быть клонирован в вектор так, чтобы сигнальный пептид был связан в рамке считывания с аминоконцом гена цепи антитела. Сигнальный пептид может представлять собой сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (т.е., сигнальный пептид из неиммуноглобулинового белка).
Кроме генов цепей антитела рекомбинантные экспрессионные векторы, соответствующие изобретению, несут регуляторные последовательности, которые контролируют экспрессию генов цепей антитела в клетке-хозяине. Термин "регуляторная последовательность" предусматривает включение промоторов, энхансеров и других элементов, контролирующих экспрессию (например, сигналов полиаденилирования), которые контролируют транскрипцию и трансляцию генов цепей антитела. Данные регуляторные последовательности описаны, например, в монографии Goeddel (Gene Expression Technology. Methods in Enzymology 185 (Технология экспрессии генов. Методы энзимологии 185), Academic Press, San Diego, CA (1990)). Специалисты в области техники должны иметь в виду, что конструирование экспрессионного вектор, включая отбор регуляторных последовательностей, может зависеть от таких факторов, как выбор клетки-хозяина, предназначенной для трансформации, уровень экспрессии желательного белка и т.п. Предпочтительные регуляторные последовательности для экспрессии в клетке млекопитающего-хозяине включают вирусные элементы, которые направляют высокие уровни экспрессии белка в клетках млекопитающих, такие как промоторы и/или энхансеры, выделенные из цитомегаловируса (CMV), вируса Simian 40 (SV40), аденовируса, (например, аденовирусный главный поздний промотор (AdMLP)) и полиомы. Альтернативно могут быть использованы невирусные регуляторные последовательности, такие как убиквитиновые промотор и промотор β-глобина. Кроме того, используют регуляторные элементы, состоящие из последовательностей из различных источников, такие как промоторная система SRα, которая включает последовательности из раннего промотора SV40 и длинного концевого повтора вируса Т-клеточного лейкоза человека типа 1 (см. статью Takebe Y. et al., (1988), Mol. Cell. Biol., 8:466-472).
Кроме генов цепей антитела и регуляторных последовательностей, рекомбинантные экспрессионные векторы, соответствующие изобретению, могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, ориджины репликации) и гены селектируемых маркеров. Ген селектируемого маркера облегчает отбор клеток-хозяев, в которые интродуцирован вектор (см., например, Патенты США NoNo. 4399216, 4634665 и 5179017, все из которых выданы Axel et al.). Например, как правило, ген селектируемого маркера обусловливает устойчивость к лекарственным препаратам, таким как 0418, гигромицин или метотрексат, клетки-хозяина, в которую интродуцирован вектор. Предпочтительные гены селектируемых маркеров включают ген дигидрофолатредуктазы (DHFR) (для использования в клетках-хозяевах dhfr- при селекции/размножении на фоне метотрексата) и ген neo (для селекции на фоне G418).
Для экспрессии легких и тяжелых цепей экспрессионным вектором(ами), кодирующим тяжелую и легкую цепи, трансфицируют клетку-хозяин с помощью стандартных методик. Предусматривают, что различные формы термина "трансфекция" охватывают широкий круг методик, обычно используемых для интродукции экзогенной ДНК в прокариотическую или эукариотическую клетку-хозяин, например, электропорацию, осаждение фосфатом кальция, трансфекцию с использованием DEAE-декстрана (диэтиламиноэтилдекстрана) и т.п. Хотя теоретически возможно экспрессировать антитела, соответствующие изобретению, либо в прокариотических, либо в эукариотических клетках-хозяевах, экспрессия антител в эукариотических клетках и, наиболее предпочтительно, в клетках млекопитающих-хозяевах является наиболее предпочтительной, поскольку данные эукариотические клетки и в особенности клетки млекопитающих с большей вероятностью, чем прокариотические клетки собирают и секретируют надлежащим образом уложенное и иммунологически активное антитело. Показано, что прокариотическая экспрессия генов антител неэффективна в плане продукции активного антитела с высоким выходом (см. статью Boss M.A. и Wood C.R., (1985), Immunology Today, 6:12-13).
Предпочтительные клетки млекопитающих-хозяева для экспрессии рекомбинантных антител, соответствующих изобретению, включают клетки яичников китайского хомячка (клетки СНО) (включая клетки СНО dhfr-, описанные в статье Uriaub and Chasin, (1980) Proc. Natl. Acad. Sci. USA 77:4216-4220, используемые сселектируемым маркером DHFR, например, как описано в статье R.J.Kaufman и Р.А.Sharp, (1982), Mol. Biol., 159:601-621), клетки миеломы NSO, клетки COS и клетки SP2. В частности, для использования с клетками миеломы NSO другой предпочтительной экспрессионной системой является система экспрессии гена GS, описанная в WO 87/04462, WO 89/01036 и ЕР 338841. Когда рекомбинантные экспрессионные векторы, кодирующие гены антитела, интродуцируют в клетки млекопитающих-хозяев, антитела получают путем культивирования клеток-хозяев в течение периода времени, достаточного для того, чтобы обеспечить экспрессию антитела в клетках-хозяевах или, более предпочтительно, секрецию антитела в культуральную среду, в которой растут клетки-хозяева. Антитела можно выделить из культуральной среды, используя стандартные методы очистки белков.
Характеризация связывания антитела с антигеном
Антитела, соответствующие изобретению, можно протестировать на связывание с IP-10 с помощью, например, стандартного ELISA. Вкратце, планшеты для микротитрования покрывают очищенным IP-10 в концентрации 0,25 мкг/мл в PBS и затем блокируют 5% бычьим сывороточным альбумином в PBS. Разведения антитела (например, разведения плазмы, полученной от иммунизированных IP-10 мышей) добавляют в каждую лунку и инкубируют в течение 1-2 при 37°С. Планшеты промывают PBS/Твин и затем инкубируют с вторичным реагентом (например, для человеческих антител используют козий Fc-специфический поликлональный реагент против IgG человека), конъюгированным с щелочной фосфатазой, в течение 1 часа при 37°С. После промывания планшеты проявляют субстратом pNPP (1 мг/мл) и анализируют при OD (оптической плотности) 405-650. Предпочтительно, когда для слияния используют мышей, у которых развиваются самые высокие титры.
Анализ ELISA, как описано выше, может быть также использован для скрининга гибридом, которые демонстрируют положительную реактивность с иммуногеном IP-10. Гибридомы, которые связываются с высокой аффинностью с IP-10, субклонируют и дополнительно характерзуют. Один клон из каждой гибридомы, который сохраняет реактивность родительских клеток (по данным ELISA), может быть выбран для получения банка клеток из 5-10 флаконов, сохраняемых при -140°С и для очистки антитела.
Для очистки антител против IP-10 отобранные гибридомы можно вырастить в двухлитровых роллерных колбах для очистки моноклональных антител. Супернатанты можно отфильтровать и сконцентрировать перед аффинной хроматографией с использованием белок А-сефарозы (Pharmacia, Piscataway, NJ). Элюированные IgG можно проверить с помощью гель-электрофореза и высокоэффективной жидкостной хроматографии, чтобы подтвердить чистоту. Буферный раствор можно заменить на PBS, и концентрацию можно определить по OD280, используя коэффициент экстинкции 1,43. Можно отобрать аликвоты моноклональных антитела и хранить при -80°С.
Для того, чтобы определить, связываются ли отобранные моноклональные антитела против IP-10 с уникальными эпитопами, каждое из антител может быть биотинилировано с использованием коммерчески доступных реагентов (Pierce, Rockford, IL). Могут быть проведены конкурентные исследования с использованием немеченых моноклональных антител и биотинилированных моноклональных антител с помощью плат для ELISA, покрытых IP-10, как описано выше. Связывание биотинилированных mAb можно определить в помощью зонда стрел (стрептомицин)-авидин-щелочная фосфатаза.
Для определения изотипа очищенных антител могут быть проведены ELISA изотипов с использованием реагентов, специфических в отношении антител определенного изотипа. Например, для определения изотипа человеческого моноклонального антитела лунки планшетов для микротитрования могут быть покрыты 1 мкг/мл агента против человеческого иммуноглобулина в течение ночи при 4°С. После блокирования 1% BSA (бычьим сывороточным альбумином) проводят реакцию планшетов с 1 мкг/мл или меньше тест-моноклональных антител или очищенных контролей изотипов при комнатной температуре в течения одного или двух часов. Затем в лунках может быть проведена реакция либо с человеческим IgG1, либо с зондами, конъюгированными со щелочной фосфатазой, специфической в отношении человеческого IgM. Планшеты проявляют и анализируют, как описано выше.
Человеческие IgG против IP-10 можно далее тестировать на реактивность с антигеном IP-10 посредством вестерн-блоттинга. Вкратце, IP-10 может быть получен и подвергнут электрофорезу в полиакриламидном геле с использованием додецилсульфата натрия. После электрофореза отделенные антигены переносят на нитроцеллюлозные мембраны, блокируют 10% сывороткой телячьих эмбрионов и зондируют с помощью тестируемых моноклональных антител. Связывание человеческого IgG можно определить при использовании щелочной фосфатазы против человеческих IgG и проявить с помощью таблеток субстрата BCIP/NBT (Sigma Chem. Co., St. Louis, Mo.).
Иммуноконъюгаты
В другом аспекте настоящее изобретение характеризует антитело против IP-10 или его фрагмент, конъюгированные с терапевтической молекулой, такой как цитотоксин, лекарственный препарат (например, иммунодепрессант) или радиотоксин. Данные конъюгаты в данном контексте называют "иммуноконъюгатами". Иммуноконъюгаты, которые включают один или более цитотоксинов, называют "имунотоксинами". Цитотоксин или цитотоксический агент включает любой агент, который вреден (например, убивает) клетки. Примеры включают таксол, цитохалазин В, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин и их аналоги или гомологи. Терапевтические агенты в ключа ют также, например, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин 5-фторурацил, декарбазин), алкилирующие агенты (например, мехлорэтамин, тиотепа, хлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромоманнит, стрептозотоцин, митомицин С и цис-дихлордиаминплатина (II) (DDP), цисплатин), антрациклины (например, даунорубицин (ранее дауномицин) идоксорубицин), антибиотики (например, дактиномицин (ранее актиномицин),блеомицин, митрамицин и антрамицин (АМС)) и антимитотические агенты (например, винкристин и винбластин).
Другие предпочтительные примеры терапевтических цитотоксинов, которые могут быть конъюгированы с антителом, соответствующим изобретению, включают дуокармицины, каличеамицины, мейтанзины и ауристатины и их производные. Примером конъюгата каличеамицин-антитело является является коммерчески доступный Mylotarg™; Wyeth-Ayerst.
Цитотоксины могут быть конъюгированы с антителами, соответствующими изобретению, с использованием линкерной технологии, имеющейся в уровне техники. Примеры типов линкеров, которые были использованы для конъюгирования цитотоксина с антителом, включают, но без ограничения перечисленным, гидразоны, тиоэфиры, сложные эфиры, дисульфиды и пептид-содержащие линкеры. Можно выбрать линкер, который, например, чувствителен к расщеплению при низком значении рН в лизосомном отделении или чувствителен к расщеплению протеазами, такими как протеазы, предпочтительно экспрессирующимися в опухолевой ткани, такими как катепсины (например, катепсины В, С, D).
В плане дальнейшего обсуждения типов цитотоксинов, линкеров и способов конъюгирования терапевтических агентов с антителами см. также статьи Saito G. et al., (2003), Adv. Drug Deliv. Rev., 55:199-215; Trail P.A. et al., (2003), Cancer Immunol. Immunother., 52:328-337; PayneG., (2003), CancerCell, 3:207-212; Alien T.M., (2002), Nat. Rev. Cancer, 2:750-763; Pastan I. and Kreitman R.J., (2002), Curr. Opin. Investig. Drugs, 3:1089-1091; Senter P.D. and Springer C.J., (2001), Adv. Drug Deliv. Rev., 53:247-264.
Антитела, соответствующие настоящему изобретению, могут быть также конъюгированы с радиоактивным изотопом с целью генерации цитотоксических радиофармацевтических агентов, называемых также радиоиммуноконъюгатами. Примеры радиоактивных изотопов, которые могут быть конъюгированы с антителами для применения диагностически или терапевтически, включают, но без ограничения перечисленным, йод131, индий111, иттрий90 и лютеций177. В области техники разработан способ получения радиоиммуноконъюгатов. Примеры радиоиммуноконъюгатов коммерчески доступны, включая Zevalin™ (IDEC Pharmaceuticals) и Bexxar™ (Corixa Pharmaceuticals), и подобные способы можно использовать для получения радиоиммуноконъюгатов с использованием антител, соответствующих изобретению.
Конъюгаты антител, соответствующих изобретению, могут быть использованы для модификации заданного биологического ответа, и молекулу лекарственного вещества не следует рассматривать, как ограниченную классическими химическими терапевтическими агентами. Например, молекула лекарственного вещества может представлять собой белок или полипептид, обладающий желательной биологической активностью. Данные белки могут включать, например, ферментативно активный токсин или его активный фрагмент, такой какабрин, рицин А, эндотоксин Pseudomonas или дифтерийный токсин; белок, такой как фактор некроза опухолей или интерферон-γ; либо модификаторы биологического ответа, такие как лимфокины, интерлейкин-1 ("ИЛ-1"), интерейкин-2 ("ИЛ-2"), интерейкин-6 ("ИЛ-6"), гранулоцитарно-макрофагальный колониестимулирующий фактор ("GM-CSF"), гранулоцитарный колониестимулирующий фактор ("G-CSF") или другие факторы роста.
Методики конъюгирования данной терапевтической молекулы с антителами хорошо известны, см., например, раздел Arnonet al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy" (Моноклональные антитела для иммунонаправленности лекарственных препаратов в терапии рака), в монографии Monoclonal Antibodies And Cancer Therapy (Моноклональные антитела и терапия рака), под ред. Reisfeld et al., с.243-56 (Alan R. Liss, Inc. 1985); раздел Hellstrom et al., "Antibodies For Drug Delivery" (Антитела для доставки лекарственных препаратов), в монографии Controlled Drug Delivery (Контролируемая доставка лекарственных препаратов) (2 изд.), под ред. Robinson et al., с.623-53 (Marcel Dekker, Inc. 1987); обзор Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review" (Антитела-носители цитотоксических агентов в терапии рака), в сборнике Monoclonal Antibodies '84: Biological And Clinical Applications (Моноклональные антитела '84, биологическое и клиническое применение), под ред. Pinchera et al., с.475-506 (1985); "Analysis, Results и Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy" (Анализ, результаты и будущие перспективы терапевтического применения антител с радиоактивной меткой в терапии рака), в монографии Monoclonal Antibodies For Cancer Detection And Therapy (Моноклональные антитела для выявления и терапии рака), под ред. Baldwin et al., с.303-16 (Academic Press 1985) и статью Thorpe et al., "The Preparation And Cytotoxic Properties Of Antibody-Toxin Conjugates" (Получение и цитотоксические свойства конъюгатов антитело-токсин), Immunol. Rev., 62:119-58 (1982).
Биспецифические молекулы
В другом аспекте настоящее изобретение характеризует биспецифические молекулы, включающие антитело против IP-10 или его фрагмент, соответствующее изобретению. Антитело, соответствующее изобретению, или его антигенсвязывающие части могут быть дериватизированы или связаны с другой функциональной молекулой, например, другим пептидом или белком (например, другим антителом или лигандом для рецептора) с целью генерации биспецифической молекулы, которая связывается с по меньшей мере двумя различными центрами связывания или молекулами-мишенями. Антитело, соответствующее изобретению, в действительности может быть дериватизировано или связано с больше, чем одной функциональной молекулой с целью генерации мультиспецифических молекул, которые связываются с более, чем двумя различными центрами связывания и/или молекулами-мишениями; предусматривают, что термин "биспецифическая молекула", как используют в данном контексте, охватывает данные мультиспецифические молекулы. Для создания биспецифической молекулы, соответствующей изобретению, антитело, соответствующее изобретению, можетбытьфункциональносвязано (например, путем химического связывания, генетического слияния, нековалентной ассоциации или иным образом) с одной или более других связывающих молекул, таких как другое антитело, фрагмент антитела, пептид или связывающий миметик, так что в результате образуется биспецифическая молекула.
Соответственно, настоящее изобретение включает биспецифические молекулы, содержащие по меньшей мере одну первую специфичность связывания в отношении IP-10 и вторую специфичность связывания в отношении второго эпитопа-мишени. В конкретном варианте осуществления изобретения второй эпитоп-мишень представляет собой Fc рецептор, например, человеческий FcγRI (CD64) или человеческий Fco рецептор (CD89). Вследствие этого изобретение включает биспецифические молекулы, способные связываться с эффекторными клетками, экспрессирующими как FcfR, так и FcorR или РсэпсилонР (например, моноцитами, макрофагами или полиморфонуклеарными клетками (PMNs)) и с клетками-мишенями, экспрессирующими IP-10. Данные биспецифические молекулы направлены на IP-10-экспрессирующие клетки, эффекторные клетки и активности переключения эффекторных клеток, опосредуемые Fc рецептором, такие как фагоцитоз IP-10-экспрессирующих клеток, антитело-зависимая опосредованная клетками цитотоксичность (ADCC), выход цитокинов или генерация аниона супреоксида.
В варианте осуществления изобретения, в котором биспецифическая молекула является мультиспецифической, молекула может дополнительно включать третью специфичность связывания кроме специфичности связывания против Fc и специфичности связывания против IP-10. В одном варианте осуществления третья специфичность связывания представляет собой часть против усиливающего фактора (EF), например, молекулу, которая связывается с поверхностным белком, участвующим в цитотоксической активности, и, таким образом, повышает иммунный ответ против клетки-мишени. "Часть против усиливающего фактора" может представлять собой антитело, функциональный фрагмент антитела или лиганд, который связывается с заданной молекулой, например, антиген или рецептор, и, таким образом, обусловливает усиление эффекта детерминант связывания для Fc рецептора или антигена клетки-мишени. "Часть против усиливающего фактора" может связывать Fc рецептор или антиген клетки-мишени. Альтернативно часть против усиливающего фактора может связываться с элементом, который отличен от элемента, в которым связываются первая и вторая специфичности. Например, часть против усиливающего фактора может связывать цитотоксическую Т-клетку (например посредством CD2, CDS, CD8, CD28, CD4, CD40, 1САМ-1) или другую иммунную клетку, что приводит в результате к повышенному иммунному ответу против клетки-мишени.
В одном варианте осуществления, биспецифические молекулы, соответствующие изобретению, включают в качестве специфичности связывания по меньшей мере одно антитело, или фрагмент данного антитела, в том числе, например, Fab, Fab', F(ab')2, Fv или одноцепочечный Fv. Антитело может также представлять собой димер легкой цепи или тяжелой цепи или их любой минимальный фрагмент, такой как Fv или одноцепочечная конструкция, как описано Ladner et al. в Патенте США No. 4946778, содержание которого специально введено в виде ссылки.
В одном варианте осуществления специфичность связывания для Рек рецептора обеспечена моноклональным антителом, связывание которого не блокировано человеческим иммуноглобулином G (IgG). Как используют в данном контексте, термин "рецептор IgG" относится к любому из восьми генов γ-цепи, находящихся на хромосоме 1. Данные гены кодируют в целом двенадцать изоформ трансмембранного или растворимого рецептора, которые разбиты на три класса рецепторов Fcγ: FcγRI (CD64), FcγRII(CD32) и FcγRIII (CD16). В одном предпочтительном варианте осуществления рецептор Feγ представляет собой молекулы молекулярной массы 72 кД, которая демонстрирует высокую аффинность к мономерному IgG (108-109 М-1).
Получение и характеризация некоторых предпочтительных моноклональных антител против Fey представлены Fangeret al. в Публикации РСТ WO 88/00052 и в Патенте США No 4954617, описание которых полностью включено в данном контексте в виде ссылки. Данные антитела связываются с эпитопом FcγRI, FcγRII или FcγRIII в центре, отличном от центра связывания рецептора с Fcγ и, таким образом, их связывание не блокируется существенным образом физиологическими уровнями IgG. Специфическими антителами против FcγRI антитела, используемыми в данном изобретении, являются mAb 22, mAb 32, mAb 44, mAb 62 и mAb 197. Гибридома, продуцирующая mAb 32 имеется в Американской коллекции типовых культур (American Type Culture Collection), ATCC Регистрационный No. HB9469. В других вариантах осуществления антитело против рецептора Fey представляет собой гуманизированную форму моноклонального антитела 22 (Н22). Получение и характеризация антитела Н22 представлены с статье Graziano R.F. et al., (1995), J. Immunol, 155(10):4996-5002 и Публикации РСТ WO 94/10332. Клеточная линия, продуцирующая антитело Н22, депонирована в Американской коллекции типовых культур (American Type Culture Collection) с обозначением HA022CL1 и имеет регистрационный no. CRL 11177.
В следующих предпочтительных вариантах осуществления специфичность связывания для рецептора Fc обусловлена антителом, которое связывается с рецептором человеческого IgA, например, рецептором Fc-α (FcorRI (CD89)), связывание которого предпочтительно не блокируется человеческим иммуноглобулином А (IgA). Предусматривают, что термин "рецептор IgA" включает генный продукт одного α-гена (FcαRI), находящегося на хромосоме 19. Известно, что данный ген кодирует ряд альтернативно сплайсированных трансмембранных изоформ молекулярной массы 55-110 кД. FcaRI (CD89) конститутивно экспрессируется на моноцитах/макрофагах, эозинофильных и нейтрофильных гранулоцитах, но не на популяциях неэффекторых клеток. FarRI обладает средней аффинностью (~5×107 М-1) к обоим, IgA1 и IgA2, которая повышается при воздействии цитокинов, таких как G-CSF или GM-CSP (см. статью Morton H.C. et al., (1996), Critical Reviews in Immunology, 16:423-440). Описаны четыре FcoRI-специфические моноклональные антитела, идентифицированные как A3, А59, А62 и А77, которые связывают FcorRI вне домена связывания лиганда IgA (см. статью Monteiro R.C. et al., (1992), J. Immunol., 148:1764). FcαRI и FcγRI являются предпочтительными переключающими рецепторами для применения в биспецифических молекулах, соответствующих изобретению, поскольку они (1) экспрессируются в основном на иммунных эффекторных клетках, например, моноцитах, PMN (мононуклеарных клетках периферической крови), макрофагах и дендритных клетках; (2) экспрессируются на высоких уровнях (например, 5000-100000/клетку); (3) являются медиаторами цитотоксическихактивностей (например, ADCC, фагоцитоза); (4) опосредуют повышенный уровень презентации антигенов, включая собственные антигена, направленные на них.
Хотя предпочтительны человеческие моноклональные антитела, другие антитела, которые можно использовать в биспецифических молекулах, соответствующих изобретению, представляют собой мышиные, химерные и гуманизированные моноклональные антитела.
Биспецифические молекулы соответствующие настоящему изобретению, можно получить путем конъюгирования составляющих специфичностей связывания, например, специфичностей связывания против FcR и против IP-10, при использовании способов, известных в области техники. Например, каждую специфичность связывания биспецифической молекулы можно генерировать отдельно, а затем конъюгировать друг с другом. Когда специфичности связывания представляют собой белки или пептиды, для ковалентного конъюгирования может быть использовано множество связывающих или перекрестно связывающих агентов. Примеры перекрестно связывающих агентов включают белок А, карбодиимид, N-сукциимидил-S-ацетил-тиоацетат (SATA), 5,5'-дитиобис(2-нитробезойную кислоту) (DTNB), о-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и сульфосукцинимидил 4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-3МСС) (см., например, статьи Karpovsky et al., (1984), J. Exp. Med., 160:1686; Liu M.A. et al., (1985), Proc. Natl. Acad. Sci. USA, 82:8648). Другие способы включают описанные в статьях Paulus, (1985), Behring Ins. Mitt., No. 78, 118-132; Brennan et al., (1985), Science, 229:81-83 и Glennie et al., (1987), J. Immunol., 139: 2367-2375). Предпочтительными конъюгационными агентами являются SATA и сульфо-SMCC, оба из которых производятся фирмой Pierce Chemical Co. (Rockford, IL).
Когда специфичности связывания представляют собой антитела, они могут быть конъюгированы через сульфгидрильное связывание С-концевых шарнирных областей двух тяжелых цепей. В особенно предпочтительном варианте осуществления шарнирную область модифицируют так, чтобы она перед конъюгированием включала нечетное число сульфгидрильных остатков.
Альтернативно обе специфичности связывания могут кодироваться в одном и том же векторе и экспрессироваться и собираться в одной и той же клетке-хозяине. Данный способ особенно эффективен, когда биспецифическая молекула представляет собой слитый белок mAb x mAb, mAb x Fab, Fab x F(ab')2 или ligand x Fab. Биспецифическая молекула, соответствующая изобретению, может быть одноцепочечной молекулой, включающей одно одноцепочечное антитело и детерминанту связывания, или одноцепочечной биспецифической молекулой, содержащей одно одноцепочечное антитело и две детерминанты связывания. Биспецифические молекулы могут включать по меньшей мере две одноцепочечные молекулы. Способы получения биспецифических молекул описаны, например, в Патенте США No 5260203; Патенте США No 5455030; Патенте США No 4881175.
Патенте США No 5132405; Патенте США No 5091513; Патенте США No 5476786; Патенте США No 5013653; Патенте США No 5258498 и Патенте США No 5482858.
Связывание биспецифических молекул с их специфическими мишенями может быть подтверждено, например, с помощью твердофазного иммуноферментного анализа (ELISA), радиоиммуноанализа (RIA), анализа FACS (с использованием флуоресцентного клеточного сортера), биоанализа (например, ингибирования роста), или вестерн-блоттинга. Каждый изданных анализов в основном определяет присутствие комплексов белок-антитело, представляющих особый интерес при использовании меченого реагента (например, антитела), специфического в отношении комплекса, представляющего интерес. Например, комплексы FcR-антитело можно определить, используя, например, связанное с ферментом антитело или фрагмент антитела, которое распознает и специфически связывается с комплексами антитело-FcR. Альтернативно комплексы можно определить с использованием множества других иммуноанализов. Например, антитело можно пометить радиоактивной меткой и использовать в радиоиммуноанализе (RIA) (см., например, работу Weintraub, В., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, март, 1986 г., (Принципы радиоиммуноанализов, Седьмые курсы по методикам анализа с использование радиолигандов, Эндокринологическое общество, март 1986 г.), которая включена в данном контексте в виде ссылки). Радиоактивный изотоп можно определить такими средствами, как применение γ-счетчика или сцинтилляционного счетчика или с помощью авторадиографии.
Фармацевтические композиции
В другом аспекте настоящее изобретение представляет композицию, например, фармацевтическую композицию, содержащую одно или комбинацию моноклональных антител или ихантигенсвязывающей части(ей), соответствующих настоящему изобретению, приготовленных вместе с фармацевтически приемлемым носителем. Данные композиции могут включать одно или комбинацию (например, два или более различных) антител или иммуноконъюгаты либо биспецифические молекулы, соответствующие изобретению. Например, фармацевтическая композиция, соответствующая изобретению, может включать комбинацию антител (или иммуноконъюгатов либо биспецифических молекул), которые связываются с различными эпитопами на антигене-мишени или которые обладают комплементарными активностями.
Фармацевтические композиции, соответствующее изобретению, можно также применять в комбинированной терапии, т.е. комбинированными с другими агентами. Например, комбинированная терапия может включать антитело против IP-10, соответствующее настоящему изобретению, в сочетании с по меньшей мере одним другим противовоспалительным или иммунодепрессивным агентом. Примеры терапевтических агентов, которые могут быть использованы в комбинированной терапии, описаны более подробно ниже в разделе, посвященном применению антител, соответствующих изобретению.
Как используют в данном контексте, "фармацевтически приемлемый носитель" включает любые и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и замедляющие всасывание агенты и т.п., которые являются физиологически совместимыми. Предпочтительно, когда носитель подходит для внутривенного, внутримышечного, подкожного, парентерального, спинального или эпидермального введения (например, путем инъекции или инфузии). В зависимости от способа введения активное соединение, т.е. антитело, иммуноконъюгат или биспецифическая молекула, могут быть покрыты материалом для защиты соединения от действия кислот и других естественных условий, которые могут инактивировать соединение.
Фармацевтические соединения, соответствующее изобретению, могут включать одну или более фармацевтически приемлемых солей. Термин "фармацевтически приемлемая соль" относится к соли, которая сохраняет желательную биологическую активность родительского соединения и не дает никаких нежелательных токсикологических эффектов (см., например, статью Berge S.M. et al., (1977), J. Pharm. Sci., 66:1-19). Примеры данных солей включают кислотно-аддитивные соли и основно-аддитивные соли. Кислотно-аддитивные соли включают соли, полученные из нетоксичных неорганических кислот, таких какхлористоводородная, азотная, фосфорная, серная, бромистоводородная, йодистоводородная, фосфористая и т.п., а также нетоксичные органические кислоты, такие как алифатические моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты и т.п. основно-аддитивные соли включают соли, полученные из щелочноземельных металлов, таких как натрий, калий, магний, кальций и т.п., а также из нетоксичных органических аминов, таких как N,N'-дибензилэтилендиамин, N-метилглюкамин, хлоропрокаин, холин, диэатноламин, этилендиамин, прокаин и т.п.
Фармацевтическая композиция, соответствующая изобретению, может также включать фармацевтически приемлемый антиоксидант. Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфат натрия, сульфит натрия и т.п.; (2) растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, α-токоферол и т.п., а также (3) металл-хелатирующие агенты, такие как лимонная кислота, этилендиаминтетрауксусная кислота (ЭДТА), сорбит, винная кислота, фосфорная кислот и т.п.
Примеры подходящих водных и неводных носителей, которые могут быть использованы в фармацевтических композициях, соответствующих изобретению, включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и т.п.) и их подходящие смеси, растительные масла, такие как оливковое масло, и инъекционные органические сложные эфиры, такие как этилолеат. Надлежащую текучесть можно поддерживать, например, при использовании покрывающих материалов, таких как лецитин, путем поддержания требующегося размера частиц в случае дисперсий и путем использования поверхностно-активных веществ.
Данные композиции могут также содержать вспомогательные агенты, такие как консерванты, смачивающие агенты, эмульгаторы и диспергирующие агенты. Предупреждение присутствия микроорганизмов может быть обеспечено как процессами стерилизации, см. выше, так и включением различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенола, сорбиновой кислоты и т.п. Может быть также желательным включение в композиции изотонических агентов, таких как сахара, хлорид натрия и т.п. Кроме того, пролонгированное всасывание инъекционной фармацевтической формы может быть осуществлено включением агентов, которые замедляют всасывание, таких как моностеарат алюминия и желатин.
Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления для немедленного введения стерильных инъекционных растворов или дисперсии. Применение данных сред и агентов для фармацевтически активных субстанций известно в области техники. Исключая какие-либо принятые среды или агент по причине их несовместимости с активным соединением, предусматривают их применение в фармацевтических композициях, соответствующих изобретению. В композиции могут быть также включены дополнительные активные соединения.
Терапевтические композиции, как правило, должны быть стерильными и стабильными в условиях изготовления и хранения. Композиция может быть приготовлена в виде раствора, микроэмульсии, липосомы или другой упорядоченной структуры, подходящей для высокой концентрации лекарственного препарата. Носитель может быть представлен растворителем или дисперсионной средой, содержащей, например, воду, этанол, полиол (например глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.) и их подходящие смеси. Надлежащую текучесть можно поддерживать, например, при использовании покрытия, такого как лецитин, путем поддержания требующегося размера частиц в случае дисперсий и путем использования поверхностно-активных веществ. Во многих случаях будет предпочтительным включить в композицию изотонические агенты, например сахара, многоатомные спирты, такие как маннит, сорбит, или хлорид натрия и т.п. Пролонгированное всасывание инъекционных композиций может быть осуществлено включением в композицию агента, который замедляет всасывание, например солей моностеаратов и желатина.
Стерильные инъекционные растворы могут быть приготовлены путем введения активного соединения в необходимом количестве в соответствующий растворитель с одним или комбинацией вышеперечисленных ингредиентов, как требуется, с последующей стерилизацией микрофильтрацией. Как правило, дисперсии готовят введением активного соединения в стерильный носитель, который содержит базовую дисперсионную среду и другие необходимые ингредиенты из вышеперечисленных. В случае стерильных порошков для приготовления стерильных инъекционных растворов предпочтительными способами получения являются вакуумная сушка и сублимационная сушка (лиофилизация), которые дают порошок активного ингредиента с любым дополнительным требующимся ингредиентом из его предварительно простерилизованного фильтрацией раствора.
Количество активного ингредиента, которое можно скомбинировать с материалом носителя для получения одной дозированной формы, будет варьировать в зависимости от субъекта, которого предполагают лечить, и конкретного способа введения. Количество активного ингредиента, которое можно скомбинировать с материалом носителя для получения одной дозированной формы, будет, как правило, таким количеством композиции, которое дает терапевтический эффект. Обычно из ста процентов данное количество будет лежать в интервале от приблизительно 0,01 процента до приблизительно девяноста девяти процентов активного ингредиента предпочтительно от приблизительно 0,1 процента до приблизительно 70 процентов, наиболее предпочтительно от приблизительно 1 процента до приблизительно 30 процентов активного ингредиента в комбинации с фармацевтически приемлемым носителем.
Схемы дозирования подбирают так, чтобы обеспечить оптимальный желательный ответ (например, терапевтический ответ). Например, может быть введен один болюс, может быть введено несколько раздельных доз в течение времени или доза может быть пропорционально уменьшена или увеличена, как обусловлено требованиями терапевтической ситуации. Особенно благоприятно готовить парентеральные композиции в дозированной унифицированной дозе для удобства введения и унификации дозирования. Термин дозированная унифицированная доза, как используют в данном контексте, относится к физически дискретным единицам, соответствующим однократным дозам, предназначенным для субъектов, которых предполагают лечить; каждая единица содержит заданное количество активного соединения, рассчитанного так, чтобы получить желательный терапевтический эффект, в сочетании с необходимым фармацевтическим носителем. Спецификация для дозированных унифицированных форм, соответствующих изобретению, продиктована и непосредственно зависит от (а) уникальных характеристик активного соединения и конкретного терапевтического эффекта, который предполагают достигнуть, и (b) ограничений, принятых в области рецептирования такого активного соединения для лечения чувствительности у субъектов.
Для введения антитела дозировки лежат в интервале от приблизительно 0,0001 до 100 мг/кг и более обыкновенно от 0,01 до 5 мг/кг массы тела хозяина. Например, дозировки могут составлять 0,3 мг/кг массы тела, 1 мг/кг массы тела, 3 мг/кг массы тела, 5 мг/кг массы тела или 10 мг/кг массы тела или лежать в интервале 1-10 мг/кг. Иллюстративная схема лечения предусматривает введение один раз в неделю, один раз каждые две недели, один раз каждые три недели, один раз каждые четыре недели, один раз в месяц, один раз каждые три месяца или один раз каждые 6 месяцев. Предпочтительные схемы дозирования антитела против IP-10, соответствующего изобретению, включают 1 мг/кг массы тела или 3 мг/кг массы тела путем внутривенного введения, при этом антитело дают, используя одну из следующих схем дозирования: (i) каждые четыре недели по шесть доз, затем через каждые три месяца; (ii) каждые три недели; (iii) 3 мг/кг массы тела однократно, а затем по 1 мг/кг массы тела каждые три недели.
В некоторых способах два или более моноклональных антител с различными специфичностями связывания вводят одновременно, в данном случае доза каждого вводимого антитела снижается в рамках указанного интервала. Антитело обычно вводят за множество приемов. Интервалы между однократными дозами могут составлять, например, неделю, месяц, каждые три месяца или год. Интервалы могут также быть неравномерными, как показывает измерение уровней антител к антигену-мишени в крови пациента. В некоторых способах дозы подбирают для достижения концентрации антитела в плазме приблизительно 1-1000 мкг/мл и в некоторых способах приблизительно 25-300 мкг/мл.
Альтернативно антитело можно ввести как препарат с замедленным высвобождением, причем в таком случае требуется менее частое введение. Доза и частота варьируют в зависимости от полупериода существования антитела в организме пациента. Как правило, человеческие антитела демонстрируют самый длинный полупериод существования, за ними следуют гуманизированные антитела, химерные антитела и нечеловеческие антитела. Доза и частота введения могут варьировать в зависимости от того, является ли лечение профилактическим или терапевтическим. При профилактическом применении вводят относительно низкую дозу через относительно нечастые интервалы в течение длительного периода времени. Некоторые пациенты продолжают получать лечение в течение всей последующей жизни. При терапевтическом применении иногда требуется относительно высокая доза при относительно коротких интервалах до тех пор, пока заболевание не уменьшится или не закончится, и предпочтительно до тех пор, пока у пациента не обнаружат частичное или полное ослабление симптомов болезни. После этого пациенту можно делать введения по профилактической схеме.
Действительные уровни доз активных ингредиентов в фармацевтических композициях, соответствующих настоящему изобретению, могут варьировать так, чтобы получить количество активного ингредиента, которое эффективно для достижения желательного терапевтического ответа для конкретного пациента, композиции и способа введения без проявления токсичности в отношении пациента. Выбранный уровень дозировки будет зависеть от ряда фармакокинетических факторов, включая активность используемых конкретных композиций, соответствующих настоящему изобретению, или их сложного эфира, соли или амида, способ введения, время введения, скорость выведения используемого конкретного соединения, продолжительность лечения, другие лекарственные препараты, соединения и/или материалы, используемые в комбинации с используемой конкретной композицией, возраст, пол, масса, состояние, общее состояние здоровья и предшествующая история болезни пациента, которого предполагают лечить, и подобные факторы, хорошо известные в области медицины.
"Терапевтически эффективная доза" антитела против IP-10, соответствующего изобретению, предпочтительно приводит в результате к снижению тяжести симптомов заболевания, увеличению частоты и продолжительности периодов без симптомов заболевания или предупреждению повреждения или нетрудоспособности вследствие физических недостатков, связанных с болезнью. В случае ревматоидного артрита (РА) предпочтительно, когда терапевтически эффективная доза предупреждает дальнейшее усугубление физических симптомов, ассоциированных с РА, таких как, например, боль, утомление, утренняя ригидность (продолжающаяся больше одного часа), диффузные мышечные боли, потеря аппетита, слабость, боль в суставах, сопровождающаяся жаром, опухание, болезненность и ригидность суставов после периода неподвижности. Предпочтительно, когда терапевтически эффективная доза также предупреждает или задерживает развитие РА, как это может быть желательно, когда появляются ранние или предшествующие признаки заболевания. Аналогичным образом она включает задержку хронического прогрессирования, ассоциированного с РА. Лабораторные тесты, используемые для диагноза РА включают химические анализы (в том числе измерение уровней IP-10), гематологические, серологические и радиологические исследования. Соответственно, любой клинический или биохимический анализ, который мониторирует любой из вышеперечисленных параметров, может быть использован для определения, соответствует ли конкретное лечение терапевтически эффективной дозе для лечения РА. Обычный специалист в области техники смог бы определить данные количества на основе таких факторов, как размеры субъекта, тяжесть симптомов у субъекта и выбранные конкретная композиция и способ введения.
Композицию, соответствующую настоящему изобретению, можно ввести одним или более способами введения при использовании методов, известных в уровне техники. Как должен иметь в виде компетентный специалист, способ и/или методика введения будут варьировать в зависимости от требующихся результатов. Предпочтительные способы введения антител, соответствующих изобретению, включают внутривенный, внутримышечный, внутрикожный, внутрибрюшинный, подкожный, спинальный и другие парентеральные способы введения, например посредством инъекции или инфузии. Выражение "парентеральное введение", как используют в данном контексте, означает методики введения, отличные от энтерального и наружного введения, обычно путем инъекции, и включает без ограничения перечисленным внутривенную, внутримышечную, внутриартериальную, интратекальную, внутрикапсульную, внутриглазничую, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, субкапсульную, субарахноидальную, интраспинальную, эпидуральную и внутригрудинную инъекцию и инфузию.
Альтернативно антитело, соответствующее изобретению, можно ввести непарентеральным путем, таким как наружный, эпидермальный и путь введения через слизистую оболочку, например, интраназально, перорально, вагинально, ректально, подъязычно и наружно.
Активные соединения можно приготовить с носителями, которые будут защищать соединение от быстрого высвобождения, например, препарат с контролируемым высвобождением, включая имплантаты, чрескожные пластыри и микроинкапсулированные системы доставки. Могут быть использованы биоразлагаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие способы получения таких препаратов запатентованы и, как правило, известны специалистам в области техники. См., например, монографию Sustained и Controlled Release Drug Delivery Systems (Системы доставки лекарственных препаратов с замедленным и контролируемым высвобождением), под ред. J.R. Robinson, Marcel Dekker, Inc., New York, 1978.
Терапевтические композиции можно вводить с помощью медицинских устройств, известных в уровне техники. Например, в предпочтительном варианте осуществления терапевтическая композиция, соответствующая изобретению, может быть введена с помощью безигольного гиподермического инъекционного устройства, такого как устройства, раскрытые в Патентах США NoNo 5399163, 5383851, 5312335, 5064413, 4941880, 4790824 или 4596556. Примеры хорошо известных имплантатов и модулей, используемых в настоящем изобретении, включают: Патент США No. 4487603, который раскрывает имплантируемый насос для микроинфузий для распределения лекарственного средства с контролируемой скоростью; Патент США No. 4486194, который раскрывает терапевтическое устройство для введения лекарственных препаратов через кожу; Патент США No. 4447233, который раскрывает насос для инфузии лекарственного средства для доставки лекарственного средства с точной скоростью инфузии; Патент США No. 4447224, который раскрывает имплантируемый инфузионный аппарат с изменяющимся потоком для непрерывной доставки лекарственного препарата; Патент США No. 4439196, который раскрывает осмотическую систему доставки лекарственного препарата, имеющую многокамерные отделения, и Патент США No. 4475196, который раскрывает осмотическую систему доставки лекарственного препарата. Данные патенты включены в данном контексте в виде ссылки. Специалистам в области техники известны многие другие подобные имплантаты, системы доставки и модули.
В некоторых вариантах осуществления человеческие моноклональные антитела, соответствующие изобретению, могут быть изготовлены так, чтобы обеспечить надлежащее распределение in vivo. Например, гематоэнцефалический барьер (ВВВ) исключает многие соединения с высокой гидрофильностью. Чтобы гарантировать, что терапевтические соединения, соответствующее изобретению, преодолевают ВВВ (если это требуется), они могут быть изготовлены, например, в липосомах. Относительно способов получения липосом см., например, Патенты США 4522811, 5374548 и 5399331. Липосомы могут содержать одну или более групп, которые избирательно транспортируются в специфические клетки или органы, усиливая, таким образом, направленную доставку лекарственного препарата (см., например, статью V.V. Ranade, (1989), J. Clin, Pharmacol., 29:685). Иллюстративные направляющие группы включают фолат и биотин (см., например, Патент США 5416016, выданный Lowet al.); маннозиды (см. статью Umezawa et al., (1988), Biochem. Biophys. Res. Commun., 153:1038); антитела (см. статьи P.O.Bloeman et al., (1995), FEBS Lett., 357:140; M.Owais et al., (1995), Antimicrob. Agents Chemother., 39:180); рецептор поверхностно-активного белка A (Briscoe et al., (1995), Am. J. Physiol., 1233:134); p120 (см. статью Schreier et al., (1994), J. Biol. Chem., 269:9090), см. также статьи K.Keinanen, M.L.Laukkanen, (1994), FEBS Lett., 346:123; J.J.Killion; I.J.Fidler, (1994), Immunomethods, 4:273. Применения и способы, соответствующее изобретению
Антитела (и иммуноконъюгаты, а также биспецифические молекулы), соответствующие настоящему изобретению, имеют диагностическое и терапевтическое применение in vitro и in vivo. Например, данные молекулы могут быть введены в клетки в культуре, например in vitro или ex vivo, либо субъекту, например in vivo, с целью лечения, предупреждения или диагностики ряда нарушений. Термин "субъект", как используют в данном контексте, предусматривает включение человека и животных, отличных от человека. Животные, отличные от человека, включают всех позвоночных, например млекопитающих и немлекопитающих, таких как приматы, отличные от человека,, овцы, собаки, кошки коровы, лошади, куры, амфибии и рептилии. Способы особенно подходят для лечения пациентов-людей с нарушениями, ассоциированными с патологической экспрессией IP-10. Когда антитела к IP-10 вводят вместе с другим агентом, данные два компонента могут быть введены в любом порядке или одновременно.
Водном варианте осуществления, антитела (и иммуноконъюгаты, а также биспецифические молекулы), соответствующие изобретению, могут быть использованы для детекции уровней IP-10 или уровней клеток, которые содержат IP-10. Это может достигаться, например, посредством контактирования образца (такого как образец in vitro) и контрольного образца с антителом против IP-10 в условиях, которые обеспечивают образование комплекса антитела и IP-10. Любые комплексы, образованные антителом и IP-10, определяют и сравнивают в образце и в контроле. Например, стандартные способы детекции, хорошо известные в уровне техники, такие как ELISA и проточные цитометические анализы, можно осуществить с использованием композиций, соответствующих изобретению.
Соответственно, в одном аспекте изобретение далее представляет способы детекции присутствия IP-10 (например, антигена человеческого IP-10) в образце или измерения количества IP-10, заключающиеся в контактировании образца и контрольного образца с антителом, соответствующим изобретению, или его антигенсвязывающей частью, которая специфически связывается с IP-10 в условиях, которые обеспечивают образование комплекса антитела или его части и IP-10. Затем определяют образование комплекса, причем разница в образовании комплекса между образцом в сравнении с контрольным образцом является показателем присутствия IP-10 в образце.
Кроме того, в объем изобретения входят наборы, содержащие композиции (например, антитела, человеческие антитела, иммуноконъюгаты и биспецифические молекулы), соответствующее изобретению, и инструкции по применению. Набор может далее включать по меньшей мере один дополнительный реагент или одно или более дополнительных антител, соответствующих изобретению (например, антитело обладающее комплементарной активностью, которое связывается с эпитопом на антигене-мишени, отличном от первого антитела). Наборы, как правило, включают этикетку, указывающую на предполагаемое применение содержимого набора. Термин этикетка включает любую надпись или записанный материал, поставляемый на или вместе с набором, или иным образом сопровождающий набор.
Известно, что IP-10 обладает эффектом хемоаттрактанта в отношении активированных Т-клеток и МК-клеток, а также рекрутирует данные клетки в очаги воспаления и аутоиммунных ответов. Соответственно, антитела против IP-10 (и иммуноконъюгаты и биспецифические молекулы), соответствующее изобретению, могут быть использованы для подавления воспалительного или аутоиммунного ответа, опосредованного активированными Т-клетками и/или NK-клетками при ряде клинических показаний. Изобретение, вследствие этого, представляет способ подавления воспалительного или аутоиммунного ответа, опосредованного активированными Т-клетками и/или МК-клетками, заключающийся в контактировании Т-клеток или NK-клеток с антителом или его антигенсвязывающей часть, соответствующими изобретению (или иммуноконъюгатом либо биспецифической молекулой, соответствующими изобретению) так, что происходит подавление воспалительного или аутоиммунного ответа. Конкретные примеры воспалительных или аутоиммунных состояний, при которых могут быть использованы антитела, соответствующие изобретению, включают, но не ограничены следующими:
А. Рассеянный склероз и другие демиелинизирующие заболевания
Показано, что экспрессия мРНК IP-10 повышена при мышином экспериментальном аллергическом энцефаломиелите (ЕАЕ), модели рассеянного склероза на мышах (см. статью Godiska R., et al., (1995), J. Neuroimmunol., 58:167-176). Более того, повышенные уровни IP-10 обнаружены в спинно-мозговой жидкости больных PC (рассеянного склероза) во время острых демиелинизирующих событий (см. статьи SorensenT.L et al., (1999), J. Clin. Invest., 103:807-815; Franciotta et al., (2001), J. Neuroimmunol., 115:192-198). Показано также, что IP-10 экспрессируется астроцитами в очагах поражения PC, но не в непораженном белом веществе (см. статью Balashov, K.E. et al., (1999), Proc. Natl. Acad. Sci. USA, 96:6873-6878) и экспрессируется макрофагами в бляшках PC и реактивными астроцитами в окружающей паренхиме (см. статью Simpson J.E. et al., (2000), Neuropathol. Appl. Neurobiol., 26:133-142). В Патентной публикации РСТ WO 02/15932 показано, что введение антител против IP-10 на модели PC с использованием мышиного вируса гепатита (MHV) дает в результате пониженную инвазию Т-лимфоцитов и макрофагов, подавленное развитие демиелинизации, повышенный уровень ремиелинизации и улучшенную неврологическую функцию (см. также статью Liu М.Т. et al. (2001) J. Immunol. 167:4091-4097). Введение мышиных антител против IP-10, как показано, снижает долю клинических и гистологических случаев и тяжесть заболевания при мышином (ЕАЕ) (см. статью Fife В.Т. et al., (2001), J. Immunol., 166:7617-7624).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении PC и других демиелинизирующих заболеваний путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами против PC, такими как интерферон β-1а (например, Avonex®, Rebif®), интерферон β-1b (например, Betaseron®), глатирамер ацетат (например, Сорахопе®) и/или митоксантрон (например, Novantrone®).
В. Ревматоидный артрит
Показано, что уровни IP-10 существенно повышены в синовиальной жидкости, синовиальной ткани и сыворотке пациентов с ревматоидным артритом (РА) (см. статьи Patel D.D. et al., (2001), Clin. Immunol., 98:39-45; Hanaoka R. et al., (2003), Arthritis Res. and Therapy, 5:R74-R81). Рецептор IP-10, CXCR3, как показано, предпочтительно экспрессируется на тучных клетках (мастоцитах) в синовиальной ткани, полученной от пациентов с РА (см. статью Ruschpler P. et al., (2003), Arthritis Res. Ther., 5:R241-R252). В модели артрита, вызываемого адъювантом, на крысах (АА) описан определяемый ответ аутоантител против собственного IP-10 (см. статью Salomon I. et al., (2002), J. Immunol., 169:2685-2693). Более того, введения ДНК-вакцины, кодирующей IP-10, повышало уровень продукции нейтрализующих антител против IP-10 у крыс, и данные аутоантитела к IP-10 могли адоптивно переносить устойчивость кАА непримированным (наивным) крысам (см. статью Salomon I. et al., выше).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении ревматоидного артрита путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами против РА, такими как нестероидные противовоспалительные лекарственные препараты (NSAIDs), анальгетики, кортикостероиды (например, преднизон, гидрокортизон), ингибиторы ФНО (фактора некроза опухолей) (включая адилимумаб (Humira®), этанерцепт (Enbrel®) и инфликсимаб (Remicade®), модифицирующими заболевание антиревматическими лекарственными препаратами (включая метотрексат, циклофосфамид, циклоспорин, ауранофин, азатиоприн, тиомалат золота натрия, гидроксихлороквин сульфат, лейлуномид, миноциклин, пеницилламин и сульфасалазин), лекарственными средствами против фибромиалгии, лекарственными средствами против остеопороза и лекарственными средствами против подагры.
С. Воспалительная болезнь кишки
Показано, что экспрессия IP-10 существенно повышена в клетках, инфильтующихся в собственную пластинку слизистой оболочки биоптатов толстой кишки, взятых у пациентов с язвенным колитом (см. статью Uguccioni М. et al., (1999), Am. J. Pathol., 155:331-336). Кроме того, показано, что нейтрализация IP-10 защищает мышей от изъязвления эпителия при остром колите и повышает выживаемость клеток крипт (см. статью Sasaki S. et al., (2002), Eur. J. Immunol., 32:3197-3205). Кроме того, у мышей ИЛ-10 -/-, у которых развивается колит, аналогичный болезни Крона у человека, лечение антителами против IP-10 привело к улучшению состояния воспаления (см. статью Singh U.P. et al., (2003), J. Immunol., 171:1401-1406).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении воспалительной болезни кишки (IBD), включая язвенный колит и болезнь Крона, путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами против IBD, такими как лекарственные препараты, содержащие месаламин (включая сульфасалазин и другие агенты, включающие 5-аминосалициловую кислоту (5-ASA), такие как олсалазин и балалазид), нестероидные противовоспалительные лекарственные препараты (NSAIDs), анальгетики, кортикостероиды (например, преднизон, гидрокортизон), ингибиторы ФНО (включая адилимумаб (Humira®), энатерцепт (Enbrel®) и инфликсимаб (Remicade®), иммунодепрессанты (такие какб-меркаптопурин, азатиоприн и циклоспорин А) и антибиотики.
D. Системная красная волчанка
Показано, что уровни сывороточного IP-10 заметно повышены у пациентов с системной красной волчанкой (SLE) и показано, что данные уровни коррелируют с активностью заболевания (см., например, статью Narumi S. et al., (2000), Cytokine, 12:1561-1565). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении SLE путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами против SLE, такими как нестероидные противовоспалительные лекарственные препараты (NSAIDs), анальгетики, кортикостероиды (например, преднизон, гидрокортизон), иммунодепрессанты (такие какциклофосфамид, азатиоприн и метотрексат), антималярийные препараты (такие как гидроксихлороквин) и биологические лекарственные препараты, которые ингибируют продукцию антител к dsДНК (например, UP 394).
Е. Диабет типа I
Показано, что уровни сывороточного IP-10 повышены у пациентов с диабетом типа I, в частности, с недавним началом болезни, и показано, что данные уровни коррелируют с числом реактивных с GAD продуцирующих γ-интерферон Т-клетоку пациентов, положительных по аутоантителам к GAD (см. статью Shimada A. et al., (2001), Diabetes Care, 24:510-515). В отдельном исследовании обнаружено, что уровни сывороточного IP-10 повышены у пациентов с недавно диагностированным заболеванием и у пациентов с высоким риском заболевания и концентрации IP-10 коррелируют с уровнями ИФН-γ (см. статью Nicoletti F. et al., (2002), Diabetologia, 45:1107-1110). Более того, продемонстрировано, что β-клетки секретируют IP-10, приводя к хемоаттрактации Т-клеток, и у мышей с дефицитом CXCR3, как показано, бывает задержанное развитие диабета типа I (см. статью Frigerio S. et al., (2002), Nature Medicine, 8:1414-1420).
Соответственно в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении диабета типа I путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими антидиабетическими агентами, такими как инсулин.
F. Воспалительные кожные нарушения
Показано, что экспрессия IP-10 ассоциирована с рядом воспалительных кожных нарушений. Например, IP-10 определен в кератиноцитах и кожном инфильтрате из активных псориазных бляшек (см. статью Gottlieb А.В. et al., (1988), J. Exp. Med., 168:941-948). Более того, CXCR3 экспрессируется кожными лимфоцитами CD3+, давая возможность предположить, что CXCR3 участвует в транспорте Т-лимфоцитов в псориазную дерму (см. статью Rottman J.B. et al., (2001), Lab. Invest., 81:335-347). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении псориаза путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами или препаратами, такими как наружные препараты (например, стероиды, деготь, кальципотриен, тазаротен, антралин, салициловая кислота), фототерапия, системные лекарственные средства (например, метотрексат, пероральные ретиноиды, циклоспорин, сложные эфиры фумаровой кислоты) и/или биологические лекарственные препараты (например, алефасепт, эфалицумаб).
Показано, что плоский лишай, хроническое воспалительное заболевание кожи и слизистой оболочки полости рта, ассоциировано с инфильтрацией Т-клеток CD4+ и CD8+, которые экспрессируют CXCR3 и, более того, показано, что инфильтрирующиеся цитолитические Т-клетки CD8+ несут IP-10 в своих цитолитических гранулах, и кератиноциты в области поражения, как показано, характеризуются сверхэкспрессией IP-10 (см. статью lijima W. et al., (2003), Am. J. Pathol., 163:261-268). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении плоского лишая путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами или препаратами, такими как противовоспалительные агенты, антигистамины, кортикостероиды и светотерапия.
Показано, что экспрессия IP-10 повышена при других воспалительных кожных нарушениях, таких как хроническая дискоидная красная волчанка и лимфоцитарная инфильтрация кожи Джесснера (см. статью Flier J. et al., (2001), J.Pathol., 194:398-405). Соответственно антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении данных воспалительных кожных нарушений путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами или препаратами, как описано выше.
G. Аутоиммунное заболевание щитовидной железы
Показано, что как IP-10, так и CXCR3 экспрессируются в щитовидной железе пациентов, страдающих от болезни Грейвса (GD), но не экспрессируются (или слабо экспрессируются) в нормальной ткани щитовидной железы, и экспрессия находится на самом высоком уровне у пациентов с недавним началом GD (см. статью Romagnani P. et al., Am. J. Pathol., 161:195-206). IP-10, как также показано, экспрессируется в щитовидной железе пациентов, страдающих от тиреоидита Хашимото (см. статью Kemp E.H. et al., (2003), Clin. Endocrinol., 59:207-213). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении аутоиммунного заболевания щитовидной железы, включая болезнь Грейвса и тиреоидит Хашимото, путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами или препаратами, такими как лекарственные препараты против щитовидной железы, радиоактивный йод и субтотальная тиреоидэктомия.
Н. Синдром Шегрена
Показано, что экспрессия мРНК1Р-10 в значительной мере регулируется повышающим образом в слюнных железах пациентов с синдромом Шегрена (S3), причем экспрессия наиболее заметна в дуктальном эпителии, прилежащем климфоидным инфильтратам (см., например, статью Ogawa N. et al., (2002), Arthritis Rheum., 46:2730-2741). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении синдрома Шегрена путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами против СШ, такими как искусственные смазывающие компоненты (например, не содержащие консервант искусственные слезы, искусственная слюна, неароматизированные кожные лосьоны, солевые спреи для носа и вагиналные смазывающие агенты), Lacriserts® для лечения сухих глаз, пилокарпин гидрохлорид (Salagen®) и цейемелин (Еуохас®) для лечения сухости во рту, нестероидные противовоспалительные лекарственные препараты (NSAIDs), стероиды и иммунодепрессивные лекарственные
препараты.
I. Легочное воспаление
Экспрессия IP-10 исследована на модели аллергической астмы на мышах, причем результаты демонстрируют, что IP-10 регулируется повышающим образом в легких после введения аллергена и что сверхэкспрессия IP-10 ассоциирована с повышенной гиперактивностью дыхательных путей, эозинофилией, повышенными уровнями ИЛ-4 и рекрутированием лимфоцитов CD8+ (см. статью Medoff B.D. et al., (2002), J. Immunol., 168:5278-5286). Более того, показано, что в бронхиолярном эпителии у курящих, у которых развивается хроническая обструктивная болезнь легких (COPD), экспрессируется IP-10 (см. статью Saetta M. et al., (2002), Am. J. Respir. Crit. Care Med., 165:1404-1409). К тому же высокие уровни IP-10 продемонстрированы в жидкости бронхоальвеолярного лаважа пациентов с легочным саркоидозом и лимфоцитарным альвеолитом (см. статью Agostini С. et al., (1998), J. Immunol., 161:6413-6420).
Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении заболевания, характеризующегося воспалением легких, таким как астма, COPD, легочный саркоидоз или лимфоцитарный альвеолит, путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами для уменьшения воспаления легких, такими как хромолин натрия, недокромил натрия, ингаляционные кортикостероиды, системные (например, пероральные) кортикостероиды, β-антагонисты короткого действия, бронходилататоры короткого действия, β-антагонисты или агонисты длительного действия (пероральные и ингаляционные), модификаторы лейкотриенов, теофиллин и кислородная терапия.
J. Отторжение трансплантата
Показано, что IP-10 играет роль в отторжении транплантированной ткани. Например, лечение мышей нейтрализующими антителами против IP-10 повышает выживаемость маленьких кишечных аллотрансплантатов и снижает уровень накопления Т-клеток и NK-клеток хозяина в собственной пластинке слизистой оболочки (см. статью Zhang Z. et al., (2002), J. Immunol., 168:3205-3212). Кроме того, у мышей, получающих аллотрансплантаты островков поджелудочной железы, лечение антителом против IP-10 также приводит в результате к повышенной выживаемости аллотрансплантата и пониженной инфильтрации лимфоцитов в трансплантат (см. статью Baker M.S. et al., (2003), Surgery, 134:126-133). Кроме того, показано, что сердечные аллотрансплантаты, но не нормальные сердца, экспрессируют IP-10 и CXCR3, и повышенные уровни IP-10 ассоциированы с васкулопатией сердечных аллотрансплантатов (см. статью Zhao D.X. et al., (2002), J. Immunol., 169:1556-1560). Показано также, что CXCR3 и IP-10 экспрессируются воспалительными клетками, инфильтрирующимися в аллотрансплантаты легкого (см. статью Agostini, С. et al., (2001), Am J. Pathol., 158:1703-1711). Нейтрализация CXCR3 или IP-10 in vivo, как показано на модели мышиного легочного трансплантата, ослабляет синдром облитерирующего бронхиолита (BOS), основного ограничивающего фактора выживаемости реципиентов легочного трансплантата (см. статью Belperio J.A. et al., (2002), J. Immunol., 169:1037-1049).
В свете вышеизложенного, в изобретении представлен также способ подавления отторжения транспланата путем введения антитела против IP-10, соответствующего изобретению, реципиенту трансплантата, нуждающемуся в лечении. Примеры тканевых трансплантатов, которые можно лечить, включают, но без ограничения перечисленным, печень, легкое (например, лечение BOS), почку, сердце, тонкую кишку и клетки островков поджелудочной железы. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами для подавления отторжения трансплантата, таким как иммунодепрессанты (например, циклоспорин, азатиоприн, метилпреднизолон, преднизолон, преднизон, микофенолят мофетил, сирилимус, рапамицин, такролимус), противоинфекционные агенты (например, ацикловир, клотримазол, ганцикловир, нистатин, триметопримсульфаметоксазол), диуретики (например, буметанид, фуросемид, метолазон) и противоязвенные средства (например, циметидин, фарнотидин, лансопразол, омепразол, ранитидин, сукралфат).
К. Повреждение спинного мозга Травматическое повреждение спинного мозга ведет к инфильтрации воспалительных клеток. Показано, что IP-10 играет главную роль во вторичной дегенерации после повреждения спинного мозга (см. статью Gonzalez et al., (2003), Exp. Neurol., 184:456-463; см. также Патентную публикацию РСТ WO 03/06045). Уровень IP-10, как показано, существенно повышен при ушибах спинного мозга крыс через 6 и 12 часов после повреждения (см. статью McTigue D.M. et al., (1998), J. Neurosci. Res., 53:368-376) и в поврежденном спинном мозге мышей через 6 часов после повреждения (см. Gonzalez et al., (2003), выше). Соответственно, ингибирование активности IP-10 после повреждения спинного мозга, как показано, эффективно в плане снижения инфильтрации воспалительных клеток и, таким образом, уменьшает вторичное повреждение тканей вследствие воспаления. Ингибирование может также уменьшить инфильтрацию воспалительных клеток, снизить вторичную дегенерацию иулучшить восстановление после травматического повреждения головного мозга и инсульта. Таким образом, в изобретении представлен также способ лечения повреждения спинного мозга и повреждения головного мозга (например, инсульта) у нуждающегося в лечении субъекта, заключающийся во введении субъекту антитела против IP-10, соответствующего изобретению. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами, такими как другие противовоспалительные агенты.
L Нейродегенеративные заболевания
Обнаружено, что экспрессия IP-10 и CXCR3 в центральной нервной системе регулируется повышающим образом в связи с патологическими изменениями, ассоциированными с болезнью Альцгеймера (AD) (см. статью Xia M.Q. and Hyman D.T., (1999), J. Neurovirol., 5:32-41). В головном мозге, пораженном (AD), CXCR3, как показано, конститутивно экспрессируется на нейронах и в нейронных процессах в различных кортикальных и субкортикальных областях, и IP-10, как показано, экспрессируется в астроцитах, и его уровень заметно повышен по сравнению в нормальным головным мозгом (см. статью Xia M.Q. et al., (2000), J. Neuroimmunol., 108:227-235). Соответственно, антитела, соответствующие изобретению, могут быть использованы при лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера и болезнь Паркинсона, путем введения субъекту, нуждающемуся в лечении антителом против IP-10, в виде монотерапии или в комбинации с другими терапевтическими агентами. Примеры агентов, с которыми может быть скомбинировано антитело против IP-10 для лечения болезни Альцгеймера, включают ингибиторы холинэстеразы (донепецил, ривастигмин, галантамин, такрин) и витамин Е. Примером агента, с которым может быть скомбинировано антитело против IP-10 для лечения болезни Паркинсона, является леводопа.
М. Гингивит
Пограничный периодонтит связан с воспаленной тканью десны. В воспаленной ткани десны человека обнаружены клетки, продуцирующие IP-10, а также клетки, экспрессирующие рецептор CXCR3 (см. статью Kabashima Н. et al., (2002), Cytokine, 20:70-77). Соответственно, в другом варианте осуществления антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении гингивита путем введения антитела субъекту, нуждающемуся в лечении. Антитело может быть использовано в виде монотерапии или в комбинации с другими агентами или способами лечения, такими как полоскания для рта против гингивита (например, полоскания для рта с антибиотиками), снятие отложений с периодонта и выравнивание корней, а также периодонтальная хирургия.
N. Воспаление, ассоциированное с генотерапией
Репликационно-дефицитные аденовирусы, используемые как аденовирусные векторы в генотерапии, могут вызывать острое нарушение и воспаление в тканях, инфицированных вирусными векторами. Данные аденовирусные векторы, как показано, индуцируют экспрессию IP-10 посредством капсид-зависимой активации NFkB (см. стать Borgland S.L et al., (2000), J. Virol., 74:3941-3947). Соответственно, антитела против IP-10, соответствующие изобретению, могут быть использованы для ингибирования индуцированного IP-10 нарушения и/или воспаления во время генотерапевтического лечения, в котором используют вирусный вектор, такой как аденовирусный вектор, который стимулирует нежелательную продукцию IP-10.
О. Заболевания, связанные с ангиогенезом
Показано, что IP-10 ингибирует ангиогенез in vitro и in vivo (см. статьи Stricter et al., (1995), Biochem. Biophys. Res. Commun., 210:51-57; Angiolillo et al., (1995), J. Exp. Med., 182:155-162; Luster et al., (1995), J. Exp. Med., 182:219-231). Ангиогенез играет решающую роль во многих болезненных процессах, таких как реакция заживления при травме. Например, сосудистая сеть в поврежденном спинном мозге остается в состоянии активного ремоделирования по меньшей мере до 28 дней после повреждения (см. статью Popovich et al., (1997), J. Сотр. Neurol., 377:443-464).
IP-10, как полагают, проявляет свои ангиостатические эффекты посредством ингибирования роста и хемотаксиса эндотелиальных клеток. Он осуществляет это через свой гепарин-связывающий мотив, а также посредством рецептор-опосредованного механизма. Через свой гепарин-связывающий мотив он препятствует связыванию ангиогенных факторов FGF-2 и VEFG165 со своими рецепторами. Он также проявляет свои эффекты через рецептор-опосредованный процесс. Рецептор для IP-10, CXCR3, альтернативно сплайсируется для образования двух известных вариантов CXCR3A и CXCR3B. Связывание IP-10 с рецептором CXCR3A приводит к пролиферации и хемотаксису клетки-мишени, тогда как связывание IP-10 с рецептором CXCR3B имеет противоположный эффект ингибирования роста и хемотаксиса. IP-10 действует именно через рецептор CXCR3B какангиостатический фактор (см. статью Lasagni et al., (2003), J. Exp. Med., 197:1537-1549).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении заболеваний, с участием ангиогенеза, например, когда ангиостатическое поведение IP-10 задерживает или препятствует заживлению или обостряет болезненный процесс. Данные заболевания включают: 1) аберрантную физиологическую неоваскуляризацию, которая может оказывать воздействие на заживание раны, цикл эструса у женщин, беременность, гипертрофию, вызываемую физическими нагрузками и т.п.; 2) показания, при которых может требоваться стимуляция неоваскуляризации, включая индукцию формирования коллатеральных сосудов (включая ишемию миокарда, периферическую ишемию, церебральную ишемию), заболевание коронарных артерий, заболевание периферических сосудов, инсульт, заживление ран, приживление трансплантата после трансплантации органа, такой кактрансплантация клеток островков, перелом и повреждение связок, восстановительная хирургия, конструирование тканей, рестеноз, выпадение волос, пролежни и варикозные язвы, желудочно-кишечные язвы, плацентарная недостаточность, асептический некроз, легочная и системная гипертензия, сосудистая деменция, болезнь Альцгеймера, церебральная аутосомная доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатия (CADASIL); псевдокиста щитовидной железы и лимфатический отек, и 3) показания, при которых может требоваться сосудистое ремоделирование, включая злокачественное образование сосудов, псориаз и преэклампсию. Антитела, соответствующие изобретению, могут быть использованы в виде монотерапии или в комбинации с другими агентами, вызывающими ангиогенез.
Р. Воспалительное заболевание почек
Показано, что рецептор CXCR3 экспрессируется мезангиальными клетками пациентов с IgA нефропатией, мембранопролиферативным гломерулонефритом или быстро прогрессирующим гломерулонефритом (см. статью Romagnani P. et al., (1999), J. Am. Soc. Nephrol., 10:2518-2526). Кроме того, на модели нефротоксического нефрита на мышах уровни мРНК IP-10 были повышены в шесть раз к корковом веществе пораженных нефритом почек через 7 дней после индукции нефрита (см. статью Schadde E. et al., (2000), Nephrol. Dial. Transplant., 15:1046-1053). К тому же высокие уровни экспрессии IP-10 отмечены в образцах биоптатов почек людей, больных гломерулонефритом по сравнению с нормальными почками (см. статью Romagnani P. et al., (2002), J. Am. Soc. Nephrol., 13:53-64). Соответственно, антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении воспалительного заболевания почек, включая IgA нефропатию, мембранопролиферативный гломерулонефрит или быстро прогрессирующий гломерулонефрит. Антитела, соответствующие изобретению, могут быть использованы в виде монотерапии или в комбинации с другими агентами или способами терапии, применяемыми при лечении гломерулонефрита, такими как антибиотика, диуретики, лекарственные средства против высокого давления и диализ.
Q. Атеросклероз Показано, что IP-10 представляет собой митогенный и хемотактический фактор гладкой мускулатуры сосудов, что является важными свойствами клеток гладкой мускулатуры в плане их участия в патогенезе атеросклероза (см. статью Wang X. et al., (1996), J. Biol. Chem., 271:24286-24293). Индукция IP-10, как показано, происходит в клетках гладкой мускулатуры после лечения LPS (липополисахаридами) или интерфероном у, а также в сонной артерии крыс после баллонной ангиопластики (см. статью Wang X. et al., (1996), выше). Более того, продемонстрировано, что IP-10 экспрессируется в эндотелиальных клетках, клетках гладкой мускулатуры и макрофагах, ассоциированных с атеромой, позволяя предположить роль IP-10 в рекрутировании и удерживании активированных Т-клеток, которые были отмечены в областях повреждения стенки сосудов в процессе атерогенеза (см. статью Mach F. et al., (1999), J. Clin. Invest., 104:1041-1050). Соответственно, антитела против IP-10, соответствующие изобретению, могут быть использованы для лечения или предупреждения атеросклероза. Антитела могут быть использованы в виде монотерапии или в комбинации с другими агентами или способами терапии, применяемыми при лечении атеросклероза, такими как лекарственные средства против высокого кровяного давления и лекарственные препараты, снижающие уровень холестерина.
R. Вирусные инфекции
IP-10 может регулироваться повышающим образом при различных вирусных инфекциях и может играть положительную роль в рекрутировании актививрованных Т-клеток при борьбе с вирусной инфекцией. Однако, в ряде случаев продукция IP-10 во время вирусной инфекции может привести к вредным эффектам и, таким образом, активность IP-10 может быть нежелательной и может потребоваться ингибировать активность IP-10 при данных вирусных инфекциях с помощью антитела против IP-10, соответствующего изобретению.
Например, показано, что IP-10 стимулирует репликацию вируса иммунодефицита человека (ВИЧ) в макрофагах моноцитарной природы и лимфоцитах периферической крови (см. статью Lane B.R. et al., (2003), Virology, 307:122-134). Кроме того, уровни IP-10 повышены в спинно-мозговой жидкости и головном мозге ВИЧ-инфицированных пациентов и в центральной нервной системе мышей, трансгенных по др120 ВИЧ (см. статью Asensio V.С. et al., (2001), J. Virol., 75:7067-7077).
Показано также, что уровни IP-10 повышены у пациентов с хроническим персистирующим вирусом гепатита С (HCV) и у пациентов с хроническим активным гепатитом (см. статью Narumi S. et al., (1997), J. Immunol., 158:5536-5544). В инфицированной HCV печени IP-10, как показано, экспрессируется гепатоцитами, но не другими типами клеток, и в печени обнаружена существенно более высокая доля СХСР3-положительныхТ-клеток по сравнению в кровью (см. статью Harvey С.Е. et al., (2003), J. Leukoc. Biol., 74:360-369). Показано, что повышенный уровень секреции IP-10 ассоциирован с воспалительным ответом на острую глазную инфекцию вируса простого герпеса типа I (HSV-1) у мышей, лечение инфицированных HSV-1 мышей антителами против IP-10, как показано, уменьшает инфильтрацию мононуклеарных клеток в строму роговицы, снижает патологию роговицы и подавляет распространение вируса из стромы роговицы с сетчатку при острой инфекции (см. статью Carr D.J. et al., (2003), J. Virol., 77:10037-10046).
Показано также, что экспрессия IP-10 осуществляется при вирусном менингите. IP-10, как продемонстрировано, присутствует в CSF (спинно-мозговой жидкости) больных вирусным менингитом и отвечает за хемотаксическую активность нейтрофилов, мононуклеарных клеток периферической крови и активированных Т-клеток (см. статьи Lahrtz F. et al., (1997), Eur.J. Immunol., 27:2484-2489; Lahrtz F. et al., (1998), J. Neuroimmunol., 85:33-43).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении вирусных инфекций, включающих нежелательную активность IP-10, путем введения антитела субъекту, нуждающемуся в лечении. Неограничивающие примеры вирусных инфекций, которые можно лечить, включают ВИЧ (например, ВИЧ-индуцированный энцефалит), HCV, HSV-1, вирусный менингит и тяжелый острый респираторный синдром (SARS). Антитело может быть использовано в виде монотерапии или в комбинации с другими антивирусными агентами, такими как в случае ВИЧ-инфекции нуклеозидные/нуклеотидные ингибиторы обратной транскриптазы, ненуклеозидные ингибиторы обратной транскриптазы и/или ингибиторы протеазы (и их комбинации), в случае инфекции HCV интерферон а 2а, пегилированный интерферон а 2а и/или рибавирин и в случае инфекции HSV-1 ацикловир, валацикловир и/или фамцикловир.
S. Бактериальные инфекции.
Бактериальные инфекции индуцируют образование IP-10 в пораженных клетках (см. статью Gasper N.A. et al., (2002), Infect Immun., 70:4075-82). Бактериальный менингит, как, в частности, известно, способствует экспрессии IP-10 (см. статью Lapinet J.A. et al., (2000), Infect Immun., 68:6917-23). IP-10 образуется также соматическими клетками семенных канальцев яичка в модели бактериальной инфекции, решительно указывая на вероятную роль данных хемокинов в кумуляции нейтрофилов и Т-лимфоцитов при воспалении яичка, которая классически наблюдается в патогенезе бактериальных инфекций (см. статью Aubry F. et al., (2000), EurCytokine Netw., 11:690-8).
В свете вышеизложенного антитела против IP-10, соответствующие изобретению, могут быть использованы при лечении бактериальных инфекций, включающих нежелательную активность IP-10, путем введения антитела субъекту, нуждающемуся в лечении. Примеры бактериальных инфекций включают, но без ограничения перечисленным, бактериальный менингит и бактериальную пневмонию. Антитело может быть использовано в виде монотерапии или в комбинации с другими антибактериальными агентами, такими как антибиотики.
Настоящее изобретение далее иллюстрируют следующими примерами, которые не следует истолковывать, как дальнейшее ограничение. Содержание всех фигур и всех ссылок, патентов и опубликованных патентных заявок, цитируемых на протяжении данной заявки, специально введено в данном контексте в виде ссылки.
Пример 1: Генерация человеческих моноклональных антител против IP-10
Антиген
Очищенный рекомбинантный человеческий IP-10, выделенный из E.coli (фирма PeproTech, Inc., Номер по каталогу: 300-12), или очищенный рекомбинантный человеческий IP-10, конъюгированный с гемоцианином блюдечка (KLH), используют как антиген.
Мыши. трансгенные по HuMab. и мыши КМ
Полностью человеческие моноклональные антитела к IP10 получают, используя линии НСо7, НСо12 и НСо17 мышей, трансгенных по HuMab, и линию КМ трансгенных трансхромосомных мышей, каждая из которых экспрессирует гены человеческого антитела. В каждой из данных линий мышей эндогенный ген мышиной каппа-легкой цепи разрушен, как описано в статье Chen et al., (1993), EMBO J., 12:811-820 и эндогенный ген мышиной тяжелой цепи разрушен, как описано в Примере 1 Публикации РСТ WO 01/09187. Каждая из данных линий мышей несет трансген человеческой каппа-легкой цепи КСо5, как описано в статье Fishwild et al., (1996), Nature Biotechnology, 14:845-851. Линия НСо7 несет трансген НСо7 человеческой тяжелой цепи, как описано в Патентах США NoNo 5545806, 5625825 и 5545807. Линия НСо 12 несет трансген НСо12 человеческой тяжелой цепи, как описано в Примере 2 Публикации РСТ WO 01/09187. Линия НСо17 несет трансген НСо17 человеческой тяжелой цепи, как описано в Примере 8 ниже.
Линия КМ содержит трансхромосому SC20, как описано в Публикации PCTWO 02/43478.
Иммунизации HuMab и КМ:
Для генерации полностью человеческих моноклональных антител к 1Р10 мышей HuMab и мышей КМ иммунизируют очищенным рекомбинантным 1Р10, выделенным из E.coli, или конъюгатом IP10-KLH в качестве антигена. Общие схемы иммунизации для мышей HuMab описаны в статьях Lonberg N. et al., (1994), Nature, 368(6474):856-859; Fishwild D. et al., (1996), Nature Biotechnology, 14: 845-851 и Публикации РСТ WO 98/24884. При первой инфузии антигена возраст мышей составляет 6-16 недель. Для иммунизации мышей HuMab и мышей КМ внутрибрюшинно, подкожно (Sc) или посредством инъекции в подушечку лапы используют очищенный рекомбинантный препарат (5-50 мкг) антигена 1Р10 (например, очищенный из трансфицированных клеток Е, coli, экпрессирующих 1Р10).
Трансгенных мышей иммунизируют дважды антигеном в полном адъюванте Фрейнда или адъюванте Риби либо внутрибрюшинно (IP), либо подкожно (Sc) или через подушечку лапы (FP), с последующей иммунизацией IP, Sc или FP через 3-21 день (в целом до 11 иммунизации) антигеном в неполном адъюванте Фрейнда или адъюванте Риби. Иммунный ответ мониторируют с помощью ретроорбитальных (заглазничных) заборов крови. Плазму подвергают скринингу с помощью ELISA (как описано ниже), и мышей с достаточными титрами человеческого иммуноглобулина против 1Р10 используют для слияний. Мышам делают внутривенное бустерное введение антигена за 3 и 2 дня до умерщвления и удаления селезенки. Как правило, для каждого антигена проводят 10-35 слияний. Для каждого антигена иммунизируют несколько дюжин мышей. В целом 1Р10 иммунизируют 82 мыши линий мышей НСо7, НСо12, НСо17 и КМ. Селекция мышей HuMab или КМ. продуцирующих антитела против 1Р10:
Для отбора мышей HuMab или КМ, продуцирующих антитела, которые связывают 1Р10, сыворотки иммунизированных мышей тестируют с помощью ELISA, как описано в статье Fishwild D. et al., (1996). Вкратце, планшеты для микротитрования покрывают очищенным рекомбинантным 1Р10 из Е.coli в концентрации 1-2 мкг/мл в PBS (забуференном фосфатом солевом растворе), 50 мкл/лунку, инкубируют при 4°С в течение ночи, затем блокируют 200 мкл/лунку 5% куриной сыворотки в PBS/Твин (0,05%). Разведения плазмы, полученной от иммунизированных 1Р10 мышей, добавляют в каждую лунку и инкубируют в течение 1-2 час при комнатной температуре. Планшеты промывают PBS/Твин и затем инкубируют с козьим поликлональным антителом против Fc IgG человека, конъюгированным с пероксидазой хрена (HRP), в течение 1 часа при комнатной температуре. После промывания планшеты проявляют с помощью субстрата ABTS (Sigma, A-1888, 0,22 мг/мл) и анализируют на спектрофотометре при OD 415-495. Мышей, у которых развиваются самые высокие титры антител против 1Р10, используют для слияний. Слияния проводят, как описано ниже, и супернатанты гибридом тестируют на активность против 1Р10 с помощью ELISA.
Генерация гибридом. продуцирующих человеческие моноклональные антитела к IP10:
Мышиные спленоциты, выделенные у мышей HuMab и мышей КМ, сливают с помощью ПЭГс клеточной линией мышиной миеломы, основываясь на стандартных протоколах. Затем полученные в результате гибридомы подвергают скринингу на продукцию антиген-специфических антител. Одноклеточные суспензии лимфоцитов поджелудочной железы от иммунизированных мышей сливают с одной четвертой частью несекретирующих клеток мышиной миеломы SP2/0 (АТСС, CRL 1581) с помощью 50% ПЭГ (Sigma). Клетки помещают с густотой приблизительно 1×105/лунку в плоскодонный планшет для микротитрования с последующим инкубированием в течение приблизительно двух недель в селективной среде, содержащей 10% сыворотки телячьих эмбрионов, 10% кондиционированной среды P388D1 (АТСС, CRLTIB-63), 3-5% оригена (IGEN) в DMEM (Mediatech, CRL 10013, с высоким содержанием глюкозы, L-глутамина и пирувата натрия), а также 5 мМ HEPES, 0,055 мМ 2-меркптоэтанола, 50 мг/мл гентамицина и 1хНАТ (Sigma, CRL P-7185). Через 1-2 недели клетки культивируют в среде, в которой HAT заменяют НТ. Затем отдельные лунки подвергают скринингу с помощью ELISA (описано выше) на человеческие моноклональные антитела IgG против 1Р10. После достижения обширного роста гибридомы среду обычно мониторируют через 10-14 дней. Гибридомы, секретирующие антитело, пересевают, снова подвергают скринингу и, если они все еще положительны по человеческим IgG, моноклональные антитела против 1Р10 субклонируют по меньшей мере дважды путем ограничивающего разведения. Стабильные субклоны затем культивируют in vitro для генерации маленьких количеств антитела в среде для тканевых культур с целью дальнейшей характеризации.
Для дальнейшего анализа отбирают гибридомные клоны 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4.
Пример 2: Структурная характеризация человеческих моноклональных антител против IP-10
Последовательности кДНК, кодирующие вариабельные области легкой и тяжелой цепи моноклональных антител 1D4, 1Е1, 2G1, 3С4, 6А5, 6А8, 6В10, 7С10, 8F6, 10А12 и 13С4, получают из соответствующих гибридом, используя стандартные методики ПЦР, и секвенируют с использованием стандартных методик секвенирования ДНК. В случаях, когда только секвенирования ДНК недостаточно для однозначного определения структуры антитела, проводят также анализ белка (например, анализ N-концевых аминокислот и масс-спектроскопию) и результаты сравнивают с анализом последовательности ДНК, чтобы таким образом определить правильную структуру антитела. Получены следующие результаты структурного анализа:
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 1D4 представлены на Фигуре 1 и в SEQ ID NONO:99 и 35, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 1 D4 представлены на Фигуре 2 и в SEQ ID NONO:110 и 84, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 1Е1 представлены на Фигуре 3 и в SEQ ID NONO:100 и 36, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 1 Е1 представлены на Фигуре 4 и в SEQ ID NONO:111 и 85, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 2G1 представлены на Фигуре бив SEQ ID NONO:101 и 37, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 2G1 представлены на Фигуре бив SEQ ID NONO:112 и 86, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 3С4 представлены на Фигуре 7 и в SEQ ID NONO:102 и 38, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 3С4 представлены на Фигуре 8 и в SEQ ID NONO:113 и 87, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 6А5 представлены на Фигуре 9 и в SEQ ID NONO:103 и 39, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 6А5 представлены на Фигуре 10 и в SEQ ID NONO:114 и 88, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 6А8 представлены на Фигуре 11 и в SEQ ID NONO; 104 и 40, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 6А8 представлены на Фигуре 12 и в SEQ ID NONO:115 и 89, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 6В10 представлены на Фигуре 13 и в SEQ ID NONO:105 и 41, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 6В10 представлены на Фигуре 14 и в SEQ ID NONO:116 и 90, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 7С10 представлены на Фигуре 15 и в SEQ ID NONO:106 и 42, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 7С10 представлены на Фигуре 16 и в SEQ ID NONO:117 и 91, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 8F6 представлены на Фигуре 17 и в SEQ ID NONO:107 и 43, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 8F6 представлены на Фигуре 18 и в SEQ ID NONO:118 и 92, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 10А12 представлены на Фигуре 19 и в SEQ ID NONO:108 и 44, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 10А12 представлены на Фигуре 20 и в SEQ ID NONO:119 и 93, соответственно.
Последовательности нуклеотидов и аминокислот вариабельной области тяжелой цепи 13С4 представлены на Фигуре 21 и в SEQ ID NONO:109 и 46, соответственно. Последовательности нуклеотидов и аминокислот вариабельной области легкой цепи 13С4 представлены на Фигуре 22 и в SEQ ID NONO:120 и 94, соответственно.
Сравнение последовательностей тяжелой цепи иммуноглобулина 1D4, 1Е1, 2G1, 6А5, 6А8, 7С10 и 10А12 с известными последовательностями тяжелых цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в тяжелых цепях данного антитела использован сегмент VH из человеческой зародышевой линии VH 3-33. Элайнмент последовательностей VH 1D4, 1Е1, 2G1, 6А5, 6А8, 7С10 и 10А12 с последовательностями зародышевой линии VH 3-33 (SEQ ID NO:47) показан на Фигуре 23. Последующий анализ последовательностей VH 1D4, 1Е1, 2G1, 6А5, 6А8,7С10 и 10А12 с использованием системы определения участков CDR Kabat приводит к построению схемы участков CDR1, CDR2 и CD3 тяжелой цепи, как показано на Фигурах 1, 2, 5, 9, 11, 15 и 19, соответственно.
Сравнение последовательностей тяжелой цепи иммуноглобулина 6В10 и 8F6 с известными последовательностями тяжелых цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в данных тяжелых цепях антитела использован сегментVH из человеческой зародышевой линии VH 3-30.3. Элайнмент последовательностей Vk 6B10 и 8F6 с последовательностью зародышевой линии VH 3-33 (SEQ ID NO:48) представлен на Фигуре 24. Последующий анализ последовательностей VH 6B10 и 8F6 с использованием системы определения участков CDR Kabat приводит к построению схемы участков CDR1, CDR2 и CDR3 тяжелой цепи, как показано на Фигурах 13 и 17, соответственно.
Сравнение последовательности тяжелой цепи иммуноглобулина 3С4 с известными последовательностями тяжелых цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в данных тяжелых цепях антитела использован сегмент VH из человеческой зародышевой линии VH 5-51. Элайнмент последовательности VH 3С4 с последовательностью зародышевой линии VH 5-51 (SEQ ID NO:49) представлен на Фигуре 25. Последующий анализ последовательности VH 3С4 с использованием системы определения участков CDR Kabat приводит к построению схемы участков тяжелой цепи CDR1, CDR2 и CDR3, как показано на Фигуре 7.
Сравнение последовательности тяжелой цепи иммуноглобулина 13С4 с известными последовательностями тяжелых цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в данных тяжелых цепях антитела использован сегмент VH из человеческой зародышевой линии VH 4-61. Элайнмент последовательности VH 13С4 с последовательностью зародышевой линии VH 4-61 (SEQ ID NO:50) представлен на Фигуре 26. Последующий анализ последовательности VH 13С4 с использованием системы определения участков CDR Kabat приводит к построению схемы участков тяжелой цепи CDR1, CDR2 и CDR3 как показано на Фигуре 21.
Сравнение последовательностей легкой цепи иммуноглобулина 1D4, 2G1, 6А5, 6А8, 10А12 и 13С4 с известными последовательностями легких цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в легких цепях данного антитела использован сегмент VL из человеческой зародышевой линии Vk A27. Элайнмент последовательностей VL 1D4, 2G1, 6А5, 6А8, 10А12 и 13С4 с последовательностью зародышевой линии VK A27 (SEQ ID NO:95) представлен на Фигуре 27. Последующий анализ последовательностей VL 1D4, 2G1, 6А5, 6А8, 10А12 и 13С4 с использованием системы определения участков CDR Kabat приводит к построению схемы участков CDR1, CDR2 и CDR3 легкой цепи, как показано на Фигурах 2, 6, 10, 12, 20 и 22, соответственно.
Сравнение последовательностей легкой цепи иммуноглобулина 1Е1, 6В10 и 8F6 с известными последовательностями легких цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в легких цепях данных антител использован сегмент VL из человеческой зародышевой линии Vk L6. Элайнмент последовательностей VL 1E1, 6В10 и 8F6 с последовательностью зародышевой линии VK L6 (SEQ ID NO:96) представлен на Фигуре 28. Последующий анализ последовательностей VL 1 Е1, 6В10 и 8F6 с использованием системы определения участков CDR Kabat приводит к построению схемы участков CDR1, CDR2 и CDR3 легкой цепи, как показано на Фигурах 4, 14 и 18, соответственно.
Сравнение последовательностей легкой цепи иммуноглобулина 3С4 с известными последовательностями легких цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в легкой цепи 3С4 использован сегмент VL из человеческой зародышевой линии Vk L18. Элайнмент последовательностей VL 3C4 с последовательностью зародышевой линии Vk L18 (SEQ ID NO:97) представлен на Фигуре 29. Последующий анализ последовательности VL 3С4 с использованием системы определения участков CDR Kabat приводит к построению схемы участков CDR1, CDR2 и CDR3 легкой цепи, как показано на Фигуре 8.
Сравнение последовательностей легкой цепи иммуноглобулина 7С10 с известными последовательностями легких цепей иммуноглобулина человеческой зародышевой линии демонстрирует, что в легкой цепи 7С10 использован сегмент VL из человеческой зародышевой линии Vk L15. Элайнмент последовательностей VL 7С10 с последовательностью зародышевой линии Vk L15 (SEQ ID NO:98) представлен на Фигуре 30. Последующий анализ последовательности VL 7С10 с использованием системы определения участков CDR Kabat приводит к построению схемы участков легкой цепи CDR1, CDR2 и CDR3, как показано на Фигуре 16.
Пример 3: Характеризация специфичности связывания и кинетики связывания человеческих моноклональных антител против IP-10
В данном примере аффинность связывания, кинетику связывания и специфичность связывания антител против IP-10 исследуют с помощью анализа Biacore. Кроме того, специфичность связывания и перекрестную конкуренцию исследуют с помощью ELISA.
Анализ Biacore
Антитела против IP-10 характеризуют по аффинности и кинетике связывания посредством анализа Biacore (Biacore AB, Uppsala, Sweden). Экспрессируемый Е.coli очищенный рекомбинантный человеческий IP-10 (R& D Systems) связывают с сенсорным чипом СМ5 @ 97 RU, используя протокол связывания EDC/NHS, представленный Biacore AB. Связывание измеряют, пропуская антитело в потоке буфера HBS ЕР (представленном Biacore AB) в концентрациях 33-267 нМ при скорости потока 40 мкл/мин. За кинетикой ассоциации антигена с антителом следят в течение 5 минут и за кинетикой диссоциации следят в течение 8 минут. Кривые ассоциации и диссоциации приводят в соответствие модели связывания Langmuir 1:1, используя программу BIAevaluation (Biacore AB). Данные, соответствующие изначальным нескольким дюжинам секунд, отдельно для фаз ассоциации и диссоциации рассматривают при приведении в соответствие кривых с целью сведения к минимуму эффекта авидности. Эксперименты проводят как при 25°С, так и при 37°С. Значения KD, kon и koff, которые определяют, приведены в Таблице 1 для связывания при 25°С и в Таблице 2 для связывания при 37°С:
Характеризация связывания при 37°С с человеческим IP-10
Полупериод существования антител (в часах), как определяют по времени, необходимому для диссоциации половины комплекса антитело-антиген во время фазы диссоциации, измеряют при 25°С и 37°С. Значения определяют по расширению кривых диссоциации до достижения времени, требующегося для 50% уменьшения оси Y сенсограммы диссоциации. Результаты представлены ниже в Таблице 3:
Перекрестная реактивность антитела при 25°С с IP-10 макаки-резуса, человеческим MIG, человеческим ITAC и мышиным IP-10 определяют посредством анализа Biacore, используя такие же способы, как описано выше для человеческого IP-10. Человеческий MIG, человеческий IP-10 и мышиный IP-10 получают коммерческим путем (PeproTech, Rocky Hill, NJ), тогда как IP-10 макаки-резуса получают путем рекомбинантной экспрессии и очищают стандартными методами. Антигены конъюгируют с сенсорным чипом СМ5 @ 140 RUs (IP-10 макаки-резуса), 457 RUs (человеческий MIG), 206 RUs (человеческий ITAC) и 150 RUs (мышиный IP-10). Сенсограммы ассоциации получают пропусканием потока антител с буфере HBS ЕР при концентрации 133 нМ в течение 5 минут. Затем поток останавливают и мониторируют диссоциацию в течение 5 минут. Кривые ассоциации и диссоциации приводят в соответствие с моделью связывания Langmuir, используя программу BIAevaluation (Biacore АВ). Результаты экспериментов по перекрестно реактивности суммируют в Таблице 4:
Анализ ELISA
Дополнительные эксперименты проводят, используя анализ ELISA для исследования антигенной перекрестной реактивности антител против IP-10 в отношении человеческого MIG, IP-10 макаки-резуса или мышиного IP-10. Методики, используемые для ELISA, такие же, как описано выше в Примере 1 за исключением того, что планшеты для микротитрования покрывают 1 мкг/мл либо рекомбинантного человеческого IP-10, человеческого MIG (PeproTech, No по каталогу 300-26), мышиного IP-10 (PeproTech, No no каталогу 250-16), либо рекомбинантного IP-10 макаки-резуса. Результаты, выраженные как значения EC50 (в нг/мл) суммированы ниже в Таблице 5:
Исследования перекрестной конкуренции между различными антителами против IP-10 проводят с помощью ELISA, используя биотинилированные формы 6А5 и 2G1, чтобы определить, распознают ли антитела различные эпитопы на IP-10. Методика конкурентных ELISA аналогична ELISA, описанному выше в Примере 1. Вкратце, планшеты для микротитрования покрывают очищенным рекомбинантным IP-10 из Е. coli в концентрации 0,2 мкг/мл в PBS, 50 мкл/лунку и инкубируют при 4°С в течение ночи. Затем лунки блокируют 200 мкл/лунку 5% куриной сыворотки в PBS/Твин (0,05%). Разведения очищенных человеческих антител против IP-10 человека (от 2 мкг/мл до 3,91 нг/мл) добавляют в каждую лунку и инкубируют в течение 30 минут при комнатной температуре. Планшеты промывают РВ3/Твин и затем инкубируют с 0,1 мкг/мл биотин-6А5 или биотин-201 в течение 30 минут. Затем планшеты трижды промывают PBS/Твин. После промывания в каждую лунку добавляют фосфатазу, меченную страптавидином (KPL, No по каталогу: 15-30-00), в разведении 1:2000 в 5% куриной сыворотке и инкубируют в течение 1 часа при комнатной температуре. После промывания планшеты проявляют субстратом p-NPP (Moss, Inc, партия 10274021) и анализируют на спектрофотометре при OD 405. Как ожидают, немеченые 2G1 могут конкурировать с биотин-201 за связывание с IP-10 и, более того, каждое из немеченых 6А5, 7С10, 10А12, 10A12S, 6В10, 8F6 и 1D4 способны конкурировать за связывание биотин-201 с человеческим IP-10. Аналогично немеченые 6А5 могут конкурировать с биотин-6А5 за связывание с IP-10 и, более того, каждое из немеченых 2G1, 7С10, 10А12, 10A12S, 6В10, 8F6 и 1D4 способны конкурировать за связывание биотин-6А5 с человеческим IP-10. Данные результаты показывают, что каждое из данных антител обладает специфичностью связывания с одним и тем же эпитопом (или группой эпитопов) человеческого IP-10.
Пример 4: Ингибирование связывания IP-10 с CXCR3
В данном примере исследуют способность антител против IP-10 ингибировать связывание человеческого IP-10 со своим рецептором, CXCR3, на экспрессирующих рецептор клетках. Во-первых, проводят анализ по Скетчарду связывания 125Р-10 с клетками 300.19, трансфицированными так, чтобы они экспрессировали CXCR3. Клетки выращивают в средах RPMI, содержащих 10% FCS и селективный фон G418. Перед использованием клетки дважды промывают сбалансированным солевым раствором Хенка (HBSS) при 4°С и подводят до густоты 4×107 клеток/мл. Стекловолоконные планшеты (Millipore Multiscreen®, No по каталогу MAFBNOB50) блокируют 200 мкл 0,1% раствора полиэтиленимина за один день до проведения эксперимента. Вдень проведения исследования блокирующий буфер отсасывают с помощью коллектора Millipore. Планшеты промывают три раза 200 мкл связывающего буфера (50 мМ HEPES, рН 7,2, 1 мМ CaCl2, 5 мМ MgCl2, 0,5% BSA). В каждую лунку добавляют двадцать пять микролитров связывающего буфера, а затем либо 25 мкл 1000-кратного избытка немеченого IP-10, либо связывающего буфера. Добавляют двадцать пять микролитров 125-IP-10 (Amersham, No no каталогу IM332-25 мкКи) с повышающимися концентрациями, а затем 25 мкл клеток с густотой 1×106 клеток/лунку. Планшеты инкубируют на встряхивающем устройстве для планшет в течение 60 минут при комнатной температуре и промывают три раза буфером для промывания (10 мМ HEPES, рН 7,2, 0,5 М NaCl, 0,5% BSA) при объеме 200 мкл/промывание. Планшеты сушат, добавляют 25 мкл сцинтилляционного агента, и подсчитывают планшеты на счетчике Wallac Microbeta Counter. Данные анализируют при использовании программы Prism и вычисляют KD. Для связывания рецептора определяют среднее KD 0,231 нМ.
Затем исследуют способность антител против IP-10 ингибировать связывание 100 пМ 125I-hlP-10 с клетками, экспрессирующими CXCR3. Конкурентные анализы проводят аналогично вышеописанному эксперименту. Вкратце, в стекловолоконные планшеты для фильтрования добавляют 25 мкл связывающего буфера, а затем 25 мкл повышающихся концентраций антител против IP-10. Двадцать пять микролитров 125I-IP-10 добавляют до конечной концентрации 0,100 нМ. Наконец, добавляют 25 мкл клеток с густотой 1×106 лунку и планшеты инкубируют на встряхивателе для планшетов в течение 60 минут при комнатной температуре, промывают и подсчитывают, как описано выше. Значения EC50 вычисляют, используя программу Prism. Значения К, (в нМ) определяют, используя формулу:
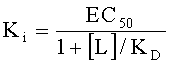
Результаты суммированы ниже в Таблице 6:
Пример 5: Ингибирование индуцированного IP-10 потока кальция
В данном примере исследуют способность антител против IP-10 ингибировать индуцируемый IP-10 ток кальция с использованием либо клеток 300.19, трансфицированных таким образом, что они экспрессируют CXCR3, либо активированных против CD3 человеческие лимфоцитов периферической крови (PBLs), которые экспрессируют CXCR3. Для получения PBL нормальную человеческую кровь очищают стандартным разделением в фиколле. Очищенные человеческие PBL стимулируют нанесением клеток на чашки, покрытые 3 мкг/мл антитела против CD3 и выращивают в среде RPMI с добавлением 10% FBS. Следующие три дня инкубирования клетки поддерживают в среде для роста, содержащей 500 ед./мл ИЛ-2. В день проведения исследования клетки промывают и ресуспендируют в средах с густотой 2,5×107 клеток/мл. Клетки 300.19, трансфицированные таким образом, что они экспрессируют CXCR3, выращивают в RPMI, содержащей 10% FBS. Клетки 300.19 ресуспендируют в среде для роста с густотой 2×106 клеток/мл.
Для проведения анализа 100 мкл клеточной суспензии добавляют в 96-луночный планшет с черными боковыми стенками и прозрачным дном, который покрыт поли-О-лизином (Corning/Costar, No по каталогу 3667). 100 микролитров набора нагружающего красителя Calcium 3 (FlexStation™, Molecular Devices, Inc., Sunnyvale, CA) добавляют в каждую лунку, планшеты центрифугируют при 1100 об./мин в течение 4 минут и инкубируют при 37°С в течение 30 минут. Используя 96-луночный планшет с реагентом человеческий IP-10 (Peprotech, No по каталогу 300-12) разводят в сбалансированном солевом растворе Хенка 20 мМ HEPES и 1% FBS (800 пМ для клеток 300.19 и 1200 пМ для человеческих PBL). Антитела серийно разводят в планшетах для реагента, содержащих IP-10. Включают контрольные лунки, содержащие только буфер или только IP-10. В планшеты, содержащие меченные красителем клетки, добавляют двадцать два микролитра раствора IP-10/антитело/лунку и определяют ток кальция мониторированием флуоресценции Calcium 3 при использовании устройства FlexStation™ в соответствии с инструкциями изготовителя с течение 200 секунд. Площадь под кривой (AUC) вычисляют интергированием тока кальция в интервале 20-100 секунд согласно стандартным протоколам (см., например, статью Smart D. et al., (1999), Br. J. Pharmacol., 128:1-3). Данные анализируют с использованием программы Prism™ (Molecular Devices, Inc.) и определяют значения IC50 (в нМ). Результаты суммируют ниже в Таблице 7:
Пример 6: Ингибирование индуцируемой IP-10 миграции клеток
Способность антител против IP-10 ингибировать миграцию клеток, индуцируемую IP-10, исследуют в анализе хемотаксиса in vitro. В данных экспериментах используют клетки 300.19, экспрессирующие CXCR3 и стимулируют их либо: (i) 100 нг/мл рекомбинантного человеческого IP-10 (rhlP-10); (ii) супернатантом клеток ТНР-1, стимулированных ИФН-γ (который индуцирует секрецию нативного IP-10 и MIG), причем IP-10, выделенный из ТНР-1, используют в концентрации 16 нг/мл, и активность MIG блокируют добавлением анти-MIG (R&D Systems) в концентрации 2,5 мкг/мл, либо (iii) 100 нг/мл рекомбинантного IP-10 макаки-резуса (rrmlP-10). Ингибирование миграции клеток оценивают при использовании различных концентраций антител и определяют хемоткасический индекс.
В частности, Ингибирование хемотаксиса оценивают с использованием стандартного анализа на 96-луночных планшетах (Multiscreen MIC plates (Millipore)). Для трансфицированных клеточных линий используют фильтр 5 мкм и для первичных клеток используют фильтр 3 мкм. Реагирующие клетки (300.19 CXCR3+; МВР-специфические человеческие клетки РВМС) ресуспендируют в буфере для хемотксиса (RPMI+1% BSA или FBS) с густотой 1×106 клеток/мл. 100 мкл клеточной суспензии добавляют в верхнюю лунку и оставляют для инкубирования в течение 30 минут при 37°С. Перед добавлением в нижнюю лунку вводят 5% CO2.
IP-10 человека и макаки-резуса готовят в концентрации 100 нг/мл для IP-10, полученного из ТНР-1, клетки ТНР-1 стимулируют ifn-k (0,2 нг/мл) и собирают супернатант; IP-10 из PC CSF используют очищенным. Лиганд получают в 150 мкл буфера для хемотаксиса и помещают в нижнюю камеру.
Для анализов ингибирования хемотаксиса лиганд предварительно инкубируют с различными концентрациями указанного антитела против IP-10 (5 мкг/мл, 2,5 мкг/мл, 1,25 мкг/мл, 0,613 мкг/мл, 0,3 мкг/мл, 0,015 мкг/мл) в течение 30 минут при 37°С в 5% CO2 перед проведением анализа. Верхнюю камеру помещают на лунками и инкубируют лунки в течение 2 часов при 37°С в 5% СО2. В конце инкубирования реагирующие клетки отсасывают из верхней камеры. Верхнюю камеру осторожно удаляют. Клетки подсчитывают в 4 случайных полях/лунку при увеличении 400х. Данные усредняют по трем лункам и представляют как индекс хемотаксиса (т.е. снижение миграции в ответ на лиганд относительно одной среды).
Результаты, выраженные как значения IC50, суммируют в Таблице 8 ниже:
Исследуют также способность антител против IP-10 ингибировать миграцию экспрессирующих CXCR3 клеток 300.19 в ответ на спинномозговую жидкость (CSF) больных рассеянным склерозом (PC). Снова антитело против MIG в концентрации 2,5 мкг/мл добавляют к образцу С3Рдля нейтрализации активности MIG. Результаты двух экспериментов, выраженные как значения IC50, суммированы в Таблице 9:
Исследования миграции клеток проводят, используя экспрессирующие CXCR3 клетки 300.19 и рекомбинантный человеческий MIG (R&D Systems) в концентрации 200 нг/мл с целью изучения способности антител против IP-10 ингибировать индуцируемую MIG миграцию клеток. Антитела против IP-10 6В10, 8F6, 1D4, 6А5 образец 2, 10А12 и 10A12S тестируют индивидуально в концентрации 1 мкг/мл и обнаруживают, что они не ингибируют индуцируемую MIG миграцию клеток.
Пример 7: Связывание антител со срезом головного мозга больных PC
В данном примере исследуют способность антител против IP-10 окрашивать срезы головного мозга, полученные от больных рассеянным склерозом (PC). Срезы головного мозга больной PC женщины в возрасте 57 лет получают через 19,8 часов после смерти и показывают наличие перивентрикулярных бляшек неправильной формы (1,3 см×1,0 см) с множеством дополнительных бляшек меньшего размера, присутствующих в остальной части белого вещества. Окрашивание LFB демонстрирует полную демиелинизацию. Проводят иммуногистохимический анализ срезов, используя антитела 6А5 (образец 2) и 10A12S против IP-10, а также агенты против GFAP и против CD68 в качестве положительных контролей и антитело для отрицательного контроля.
Для окрашивания срезов против IP-10 используют стандартный иммуногистохимический метод. Срезы блокируют, используя 2%-10% сыворотку. Добавляют 100 мкл/срез первичного антитела (например, 6А5), разведенного 1:100 в 2% сыворотке, затем инкубируют в течение 1 часа при комнатной температуре. Срезы необязательно инкубируют в течение ночи при 4°С и промывают. Затем добавляют вторичное биотинилированное антитело против человека (разведенное в 2% сыворотке (100 мкл/срез)) и инкубируют 30-60 минут при комнатной температуре. Эндогенные пероксидазы удаляют добавлением разбавленной H2O2 в MeOH. Затем добавляют раствор АВС (Vector Labs), 100 мкл/срез и инкубируют в течение 30 минут при комнатной температуре. Раствор субстрата DAB готовят непосредственно перед использованием. На предметные стекла наносят 100 мкл/срез перед инкубированием в темноте в течение 10-20 минут (как требуется для проявления). Затем проводят контрастное окрашивание предметных стекол ядерным красителем гематоксилином в течение 3 минут (проявление проверяют через 1 мин.). Наконец, предметные стекла инкубируют в 2% бикарбонате натрия в течение 45 секунд для проявления окрашивания.
Результаты показывают, что как 6А5, так и 10A12S могут связываться с IP-10 in situ в срезах головного мозга больного PC, причем связывание 6А5 более интенсивно, чем связывание 10A12S.
Пример 8: Конструирование линии трансгенных мышей НСо17
Линию трансгенных мышей НСо17 генерируют совместной инъекцией инсерта 80 т.п.н. рНС2 (см. статью Taylor et al., (1994), Int. Immunol., 6:579-591), инсерта 25 т.п.н pVX6 и фрагмента искусственной хромосомы дрожжей ~460 т.п.н. хромосомы yIgH24. Сама конструкция рНС2 полностью способна к реаранжировке in vivo с образованием функциональных локусов тяжелой цепи иммуноглобулина человека; pVX6 и yIgH24 вводят для участия с создании дополнительного разнообразия VH зародышевой линии. Отдельные компоненты смеси ДНК, используемой для получения НСо17, описаны ниже.
Вышеописанный инсерт рНС2 включает четыре функциональных сегмента гена VH человеческой зародышевой линии: 1-69 (DP-10), 5-51 (DP-73), 4-34 (DP-63) и 3-30.3 (DP-46). Кроме того, данная конструкция содержит также человеческие геномные последовательности, включающие 15 функциональных D-сегментов, все 6 J-сегментов, а также сегменты µ и γ1 константной области и функциональную область переключения µ-γ1.
Инсерт pVX6 содержит 3 сегмента VH человеческой зародышевой линии, VH1-18 (DP-14), VH5-51 (DP-73) и VH3-23 (DP-47). Фрагмент ДНК 8,5 т.п.н. Hindlll/Sall, включающий ген VH1-18 (DP-14) человеческой зародышевой линии, вместе с приблизительно 2,5 т.п.н. 5'-фланкирующей и 5 т.п.н. 3'-фланирующей геномной последовательностью субклонируют в плазмидный вектор р8Р72 (Promega, Madison, Wis.) для генерации плазмиды р343.7.16. Фрагмент ДНК BamHI/Hindlll 7 т.п.н., включающий ген человеческой зародышевой линии VH5-51 (DP-73), вместе с приблизительно 5 т.п.н. 5'-фланкирующей и 1 т.п.н. 3'-фланирующей геномной последовательностью, клонируют в плазмидный клонирующий вектор pGP1f на основе pBR322 (см. статью Taylor et al., (1992), Nucleic acids Res., 20:6287-6295), для генерации плазмиды p251f. Новый клонирующий вектор, полученный из pGP1f, pGP1k, разрезают с помощью EcoRV/BamHI и лигируют во фрагмент ДНК 10 т.п.н. EcoRV/BamHI, включающий ген VH3-23 (DP47) человеческой зародышевой линии вместе с приблизительно 4 т.п.н. S'-фланкирующей и 5 т.п.н. 5'-фланирующей геномной последовательностью. Полученную в результате плазмиду p112.2RR.7 разрезают BamHI/Sall и лигируют с очищенным инсертом BamHI/Sall p251f 7 т.п.н. Полученную в результате плазмиду pVx4 разрезают Xhol и лигируют в инсерт Xhol/Sall p343.7.16 8,5 т.п.н. Получают клон с геном VH1-18 в той же самой ориентации, что два других V-гена. Данный клон, названный pVx6, затем разрезают Notl для получения инсерта.
Исходную хромосому дрожжей (YAC)yIgH24 изначально идентифицируют скринингом с помощью ПЦР при использовании семейства специфических праймеров VH3 и VH4 и картируют на хромсоме 14 человека по содержанию VH. Установлено, что yIgH24 содержит сегменты VH, включающие представителей семейств VH VH1, VH2, VH3, VH4 и VH5 и, в частности, по меньшей мере VH1-24, VH1-45, VH1-46, VH2-26, VH3-30, V 3-30.5, VH3-30.3, VH3-33, VH3-43, VH3-48, VH3-49, VH3-53, VH4-28, VH4-30, VH4-30.4, VH4-30.3, VH4-31, VH4-34, 4-39 и VH5-51.
Очищенные инсерты из pVX6 (26 т.п.н.), рНС2 (80 т.п.н.) и yIgH24 (прибл.460 т.п.н.) комбинируют в молярном соотношении 1:1:1 и микроинъекцией вводят в пронуклеусы полудневных эмбрионов F2 (C57BL/6J×DBA/2J), как описано Hogan et al. (см. монографию В. Hogan et al., Manipulating the Mouse Embryo, A Laboratory Manual (Лабораторное руководство по манипуляциям с мышиными эмбрионами), 2 изд., 1994, Cold Spring Harbor Laboratory Press, Plainview, N.Y.). Исходная линия трансгенных мышей, содержащая последовательности из pVx6, HC2 и yIgH24, создана из мышей, которые развиваются из инъецированных эмбрионов. Данная линия названа (НСо17) 25950.
Затем линию (НСо17) 25950 скрещивают с мышами, несущими мутацию CMD (описаны в Примере 1 Публикации РСТ WO01/09187), мутацию JKD (см. статью Chen et al., (1993), EMBO J., 12:811-820) и трансген (КСо5)9272 (см. статью Fishwild et al., (1996), Nature Biotechnology, 14:845-851). Полученные в результате мыши экспрессируют трансгены тяжелой и каппа-легкой цепей иммуноглобулина человека на фоне, гомозиготном по разрушению эндогенных локусов тяжелой и каппа-легкой мышиных цепей.
Эквивалентные решения
Компетентные специалисты в области техники узнают или способны установить при использовании не более чем рутинного экспериментирования много эквивалентных решений конкретных вариантов осуществления изобретения, описанных в данном контексте. Предусматривается, что последующая формула изобретения охватывает данные эквивалентные решения
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА РЕЦЕПТОРА 1 ИНТЕРФЕРОНА АЛЬФА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2600884C2 |
| ВЫДЕЛЕННОЕ АНТИ-CD30 АНТИТЕЛО (ВАРИАНТЫ), ХОЗЯЙСКАЯ КЛЕТКА, СПОСОБ ПОЛУЧЕНИЯ ХИМЕРНОГО ИЛИ ГУМАНИЗИРОВАННОГО ВАРИАНТА АНТИ-CD30 АНТИТЕЛ (ВАРИАНТЫ), СПОСОБ ИНГИБИРОВАНИЯ РОСТА КЛЕТОК CD30+ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛЕВЫХ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ CD30 | 2006 |
|
RU2492186C2 |
| АНТИ-C5 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2774716C2 |
| АНТИТЕЛА РЕЦЕПТОРА 1 ИНТЕРФЕРОНА АЛЬФА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2412202C2 |
| ВЫДЕЛЕННОЕ АНТИТЕЛО ПРОТИВ СПЕЦИФИЧЕСКОГО МЕМБРАННОГО АНТИГЕНА ПРОСТАТЫ (PSMA) И СПОСОБ ИНГИБИРОВАНИЯ РОСТА КЛЕТОК, ЭКСПРЕССИРУЮЩИХ PSMA | 2006 |
|
RU2421466C2 |
| МОЛЕКУЛЫ АНТИТЕЛ С УЛУЧШЕННЫМИ СВОЙСТВАМИ | 2009 |
|
RU2430111C1 |
| Молекулы, связывающиеся с 4-1ВВ | 2011 |
|
RU2710717C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, СОДЕРЖАЩИЙ МОЛЕКУЛЫ АНТИТЕЛ С УЛУЧШЕННЫМИ СВОЙСТВАМИ | 2010 |
|
RU2565809C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ЧЕЛОВЕКА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1 (PD-1) И СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТИ-PD-1-АНТИТЕЛ САМОСТОЯТЕЛЬНО ИЛИ В КОМБИНАЦИИ С ДРУГИМИ ИММУНОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ | 2016 |
|
RU2732924C2 |
| МОДИФИЦИРОВАННЫЙ ЭКЗОТОКСИН А ПСЕВДОМОНАД | 2014 |
|
RU2687143C2 |
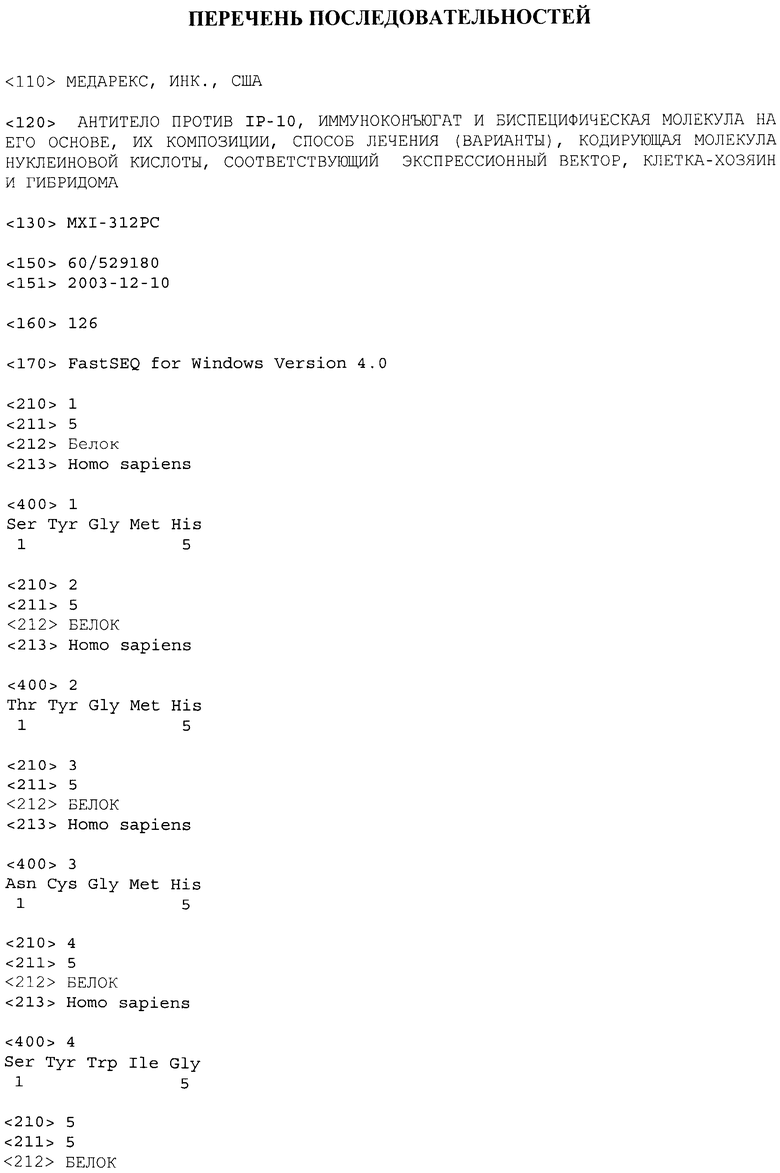






























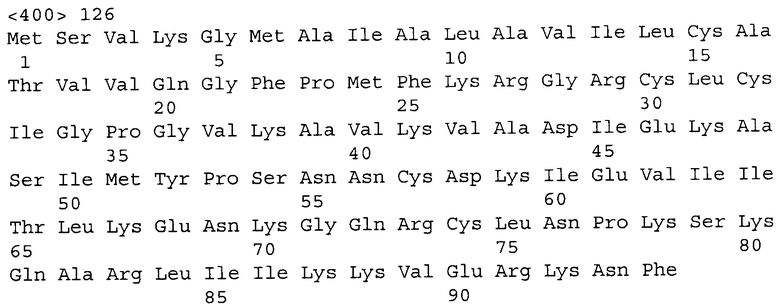
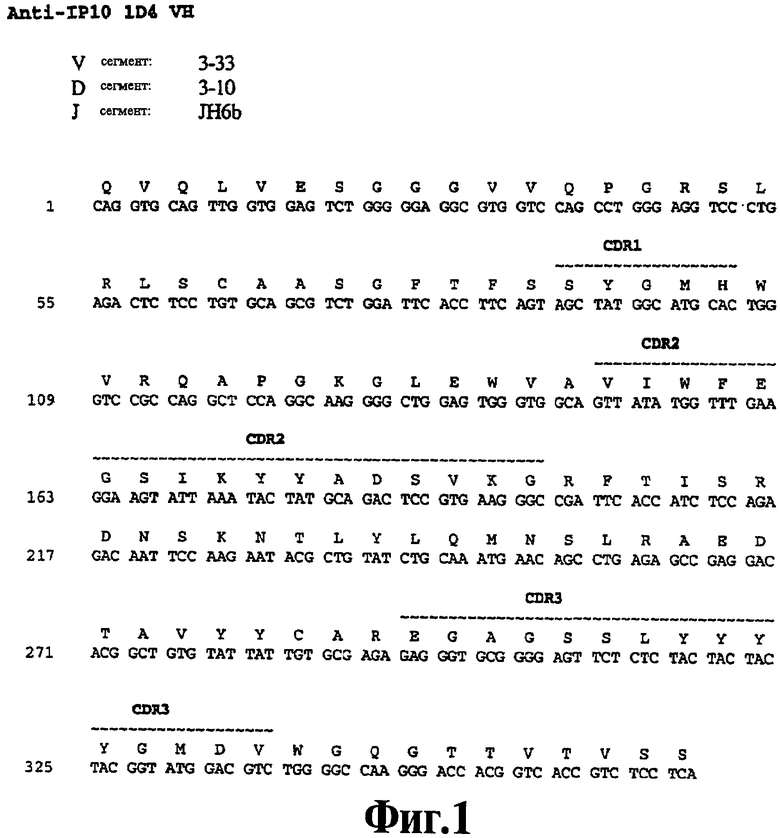


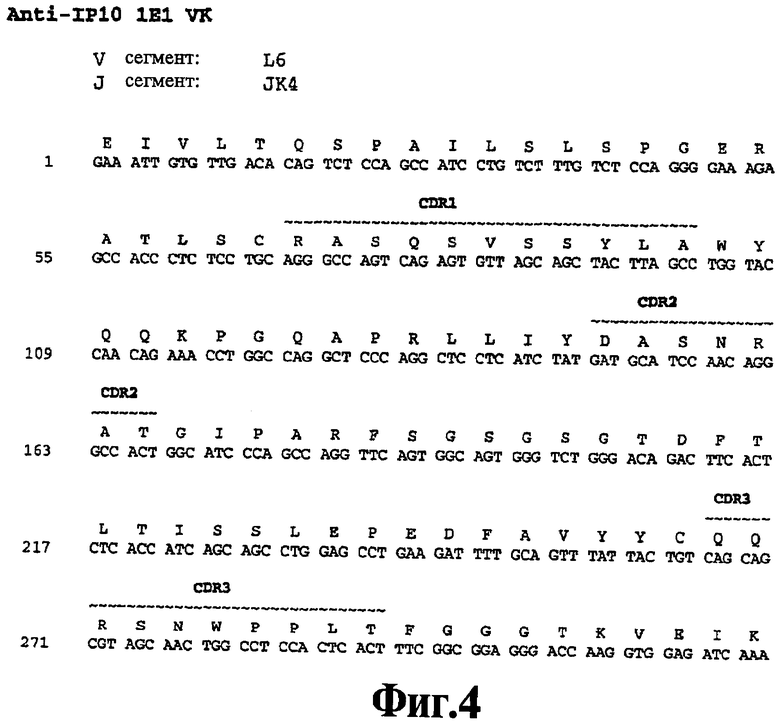


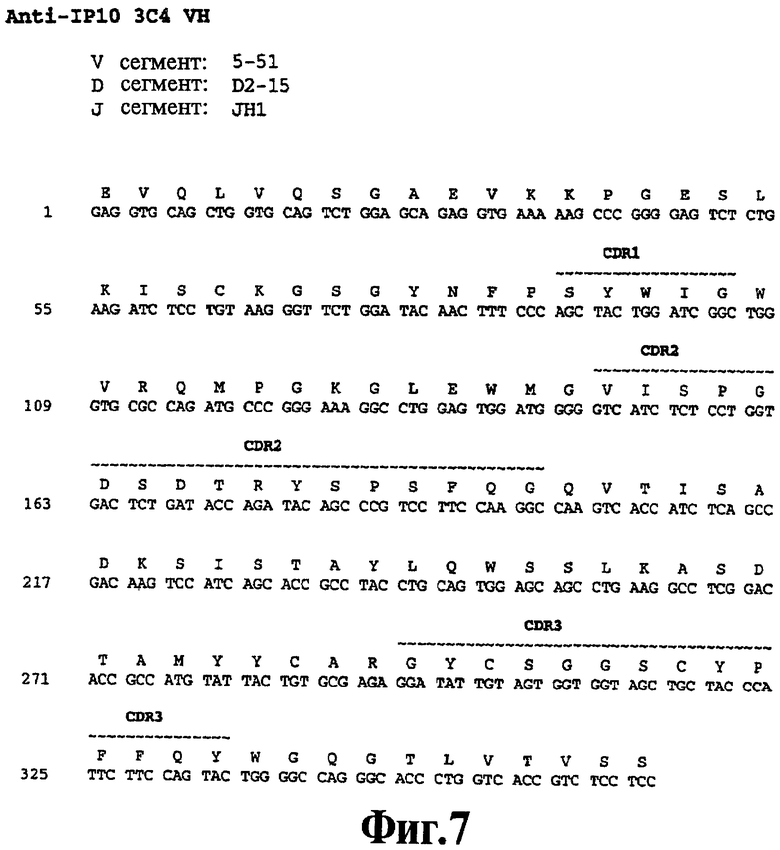
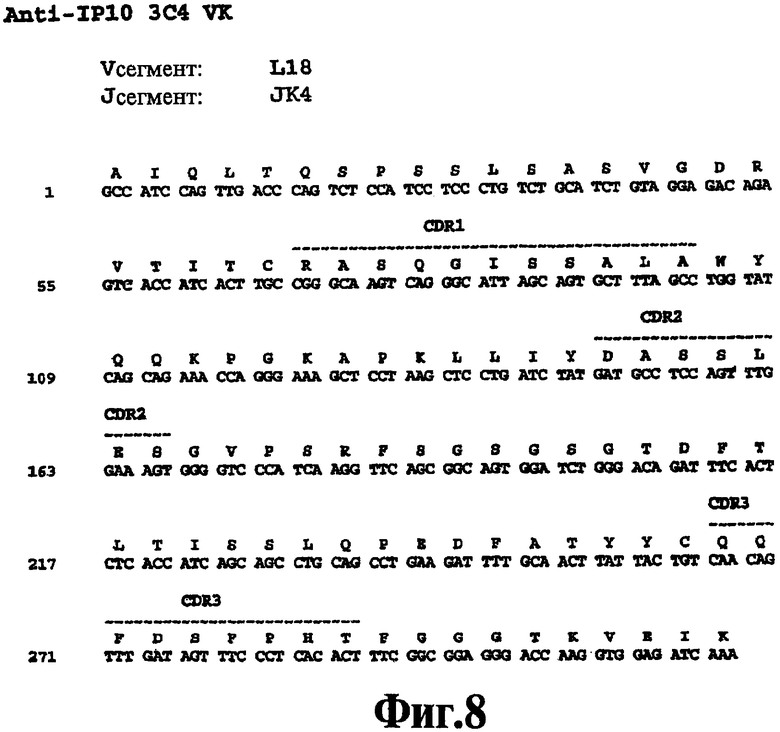
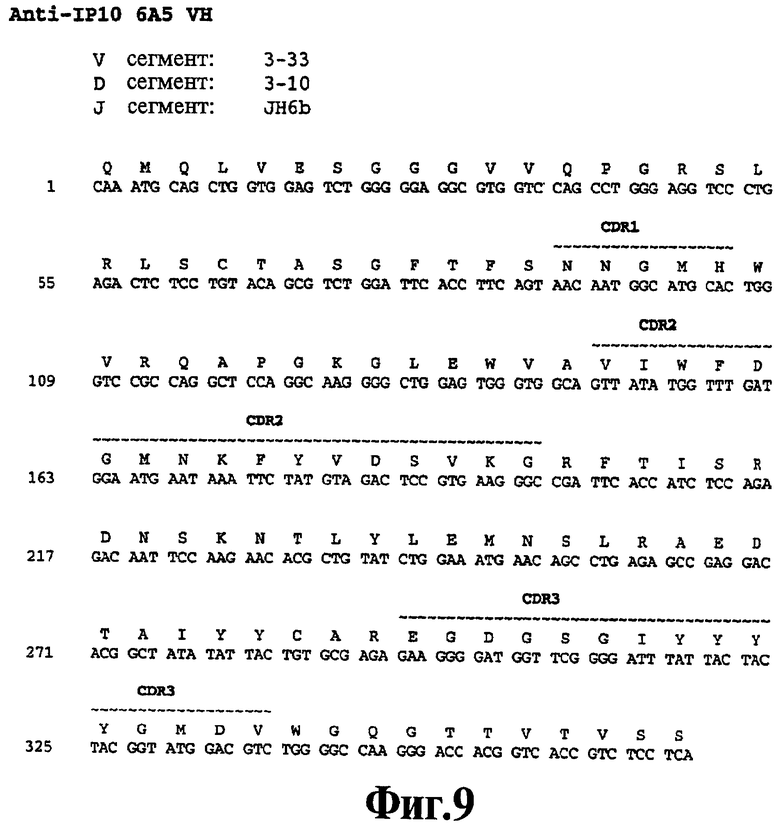
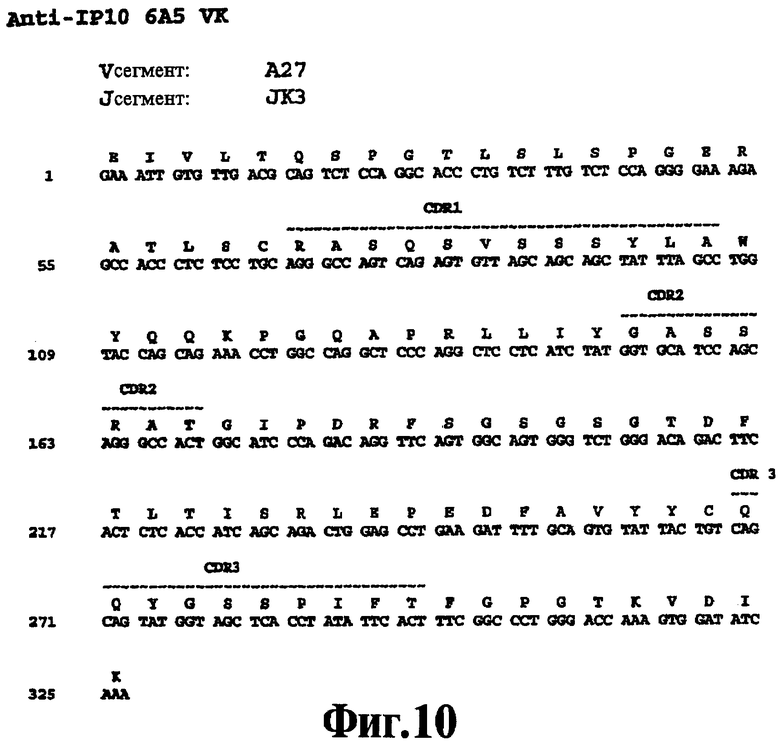

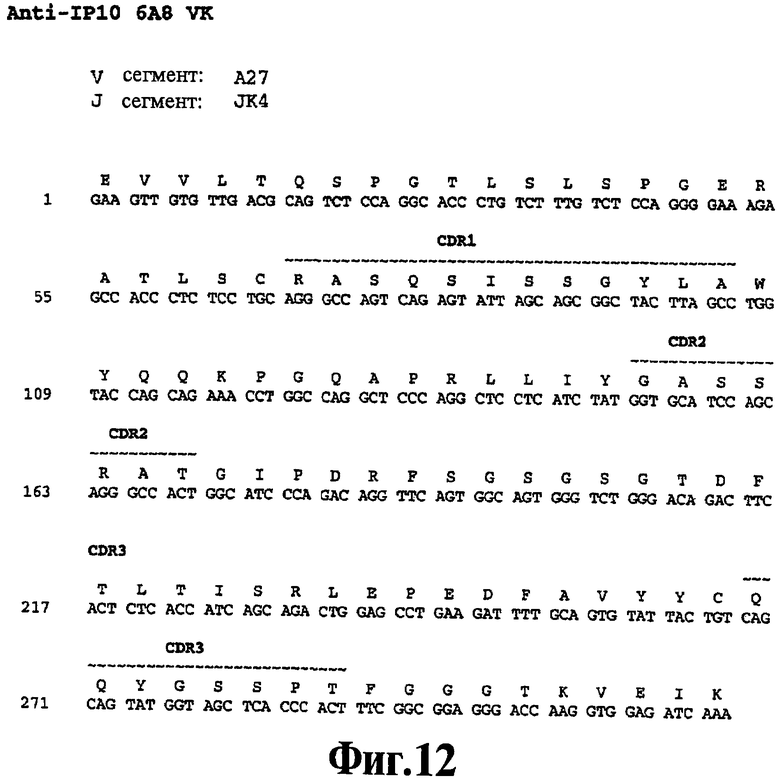
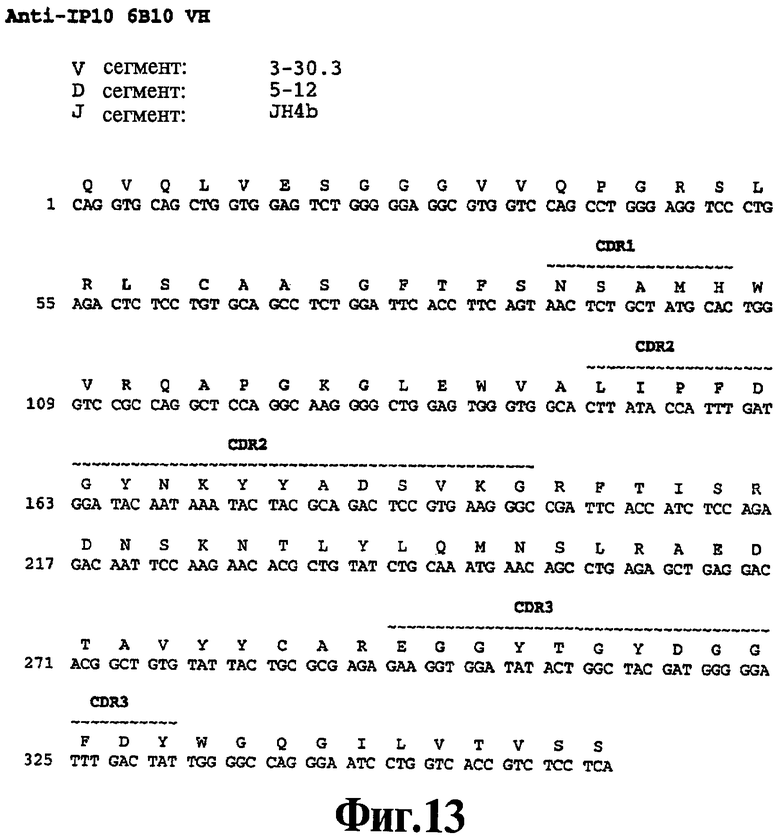
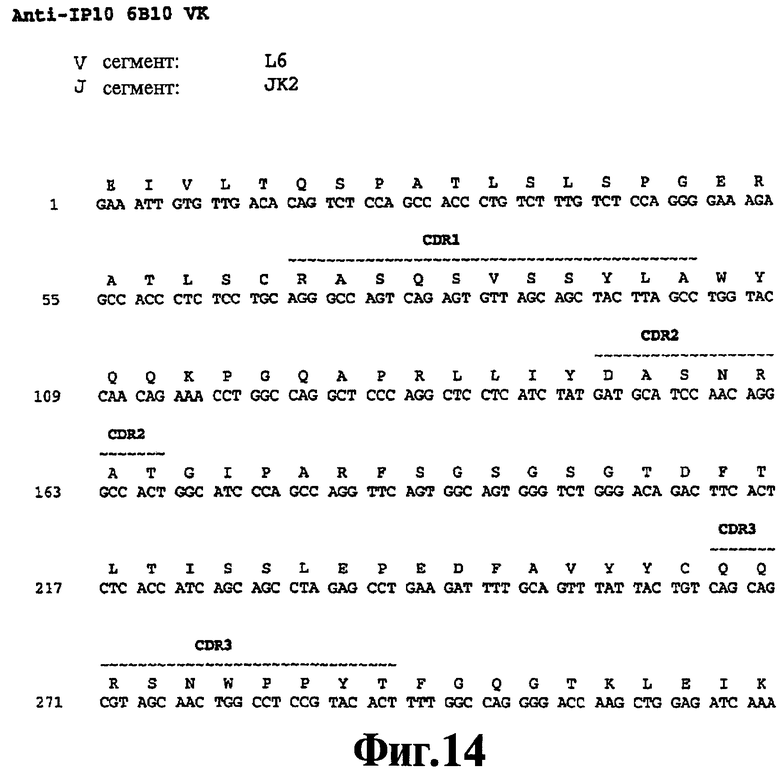


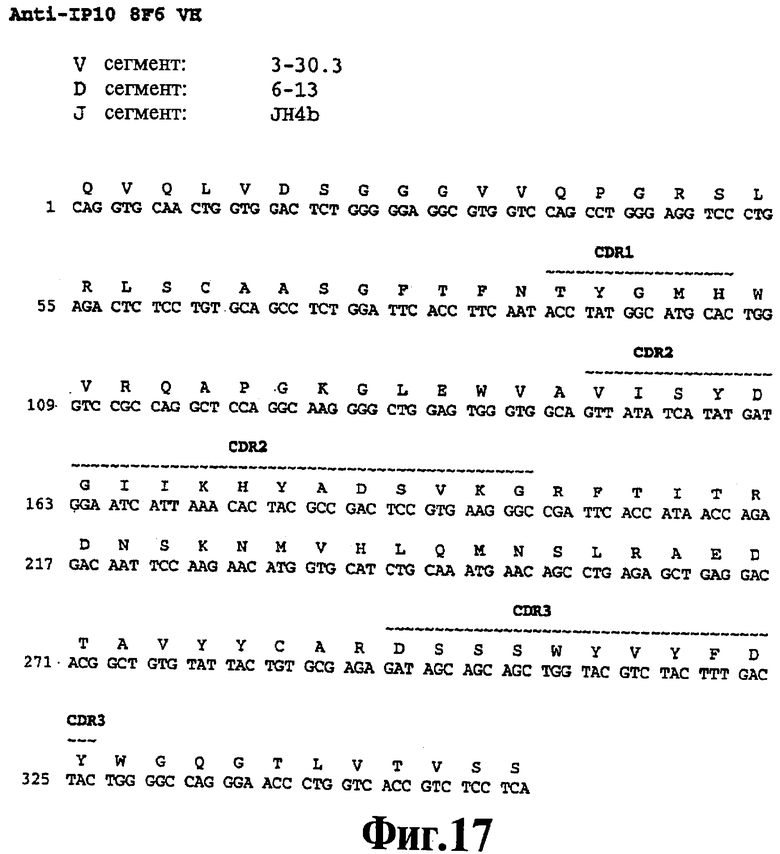

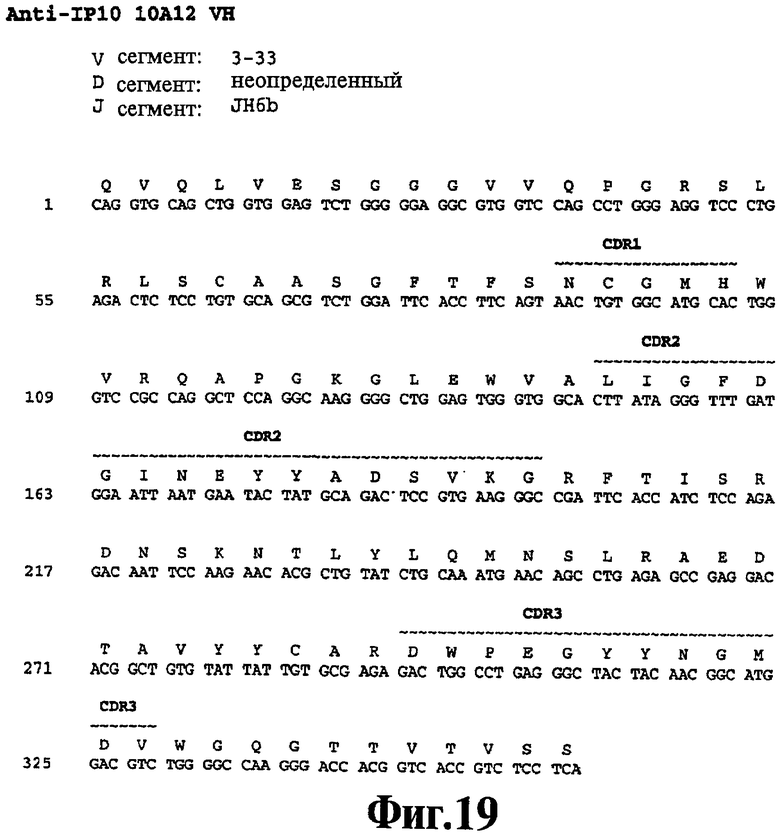


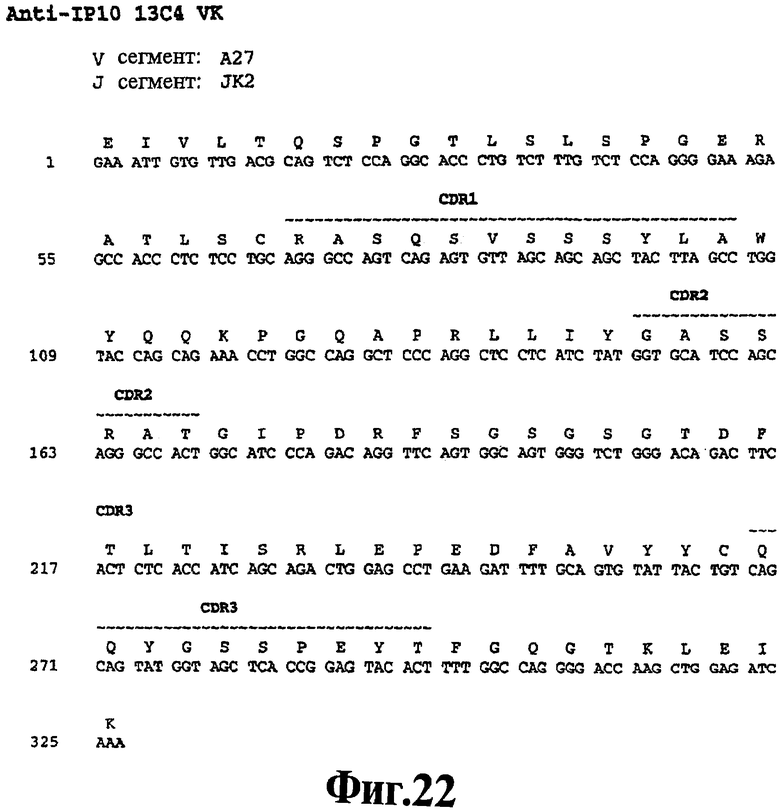
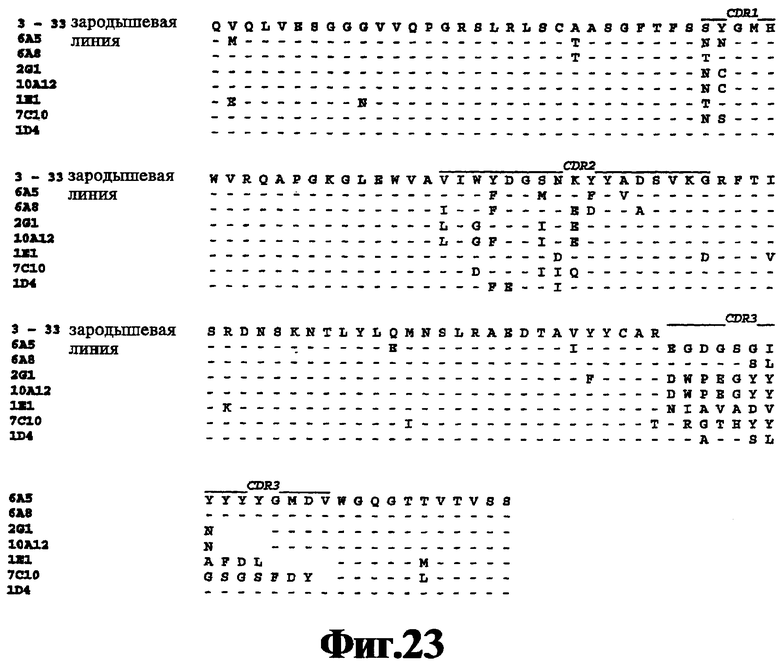
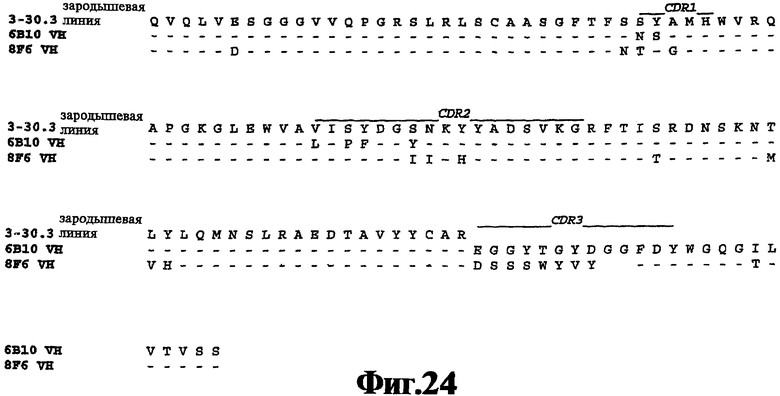
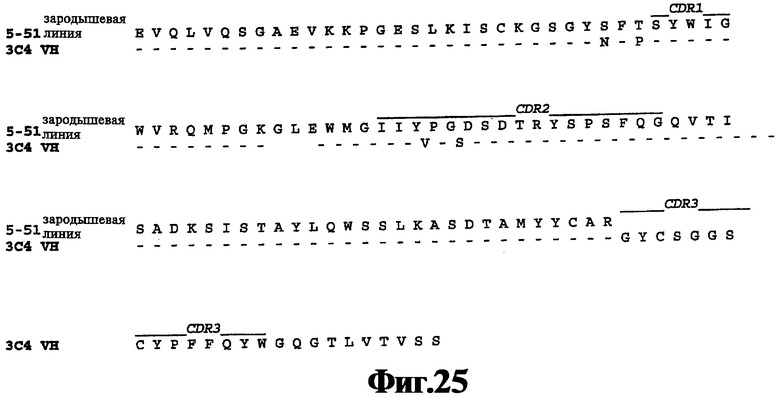
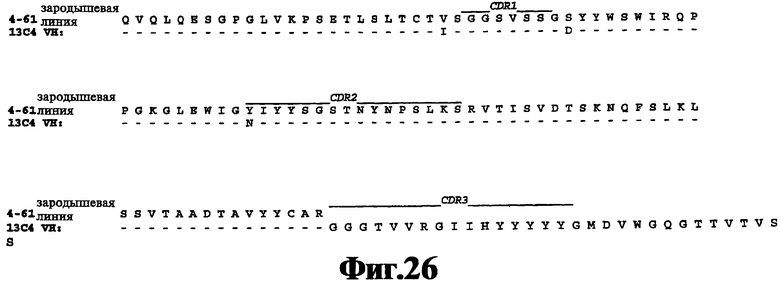
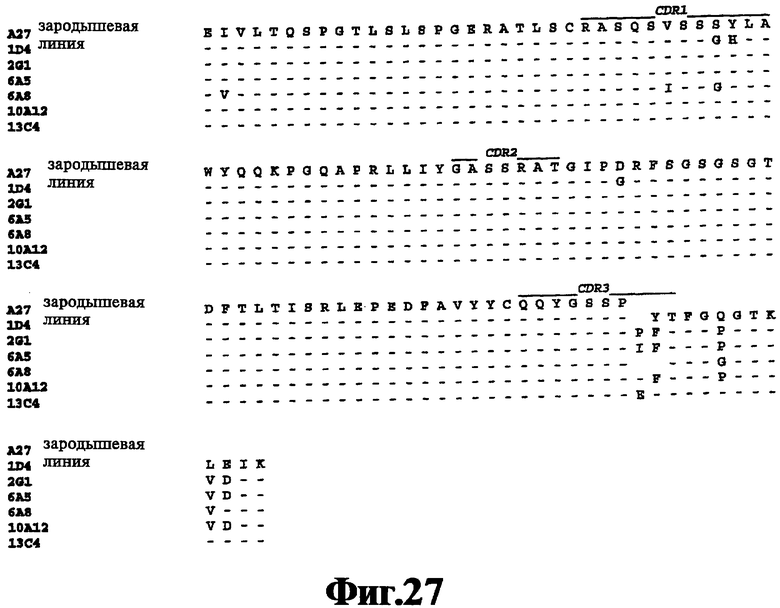
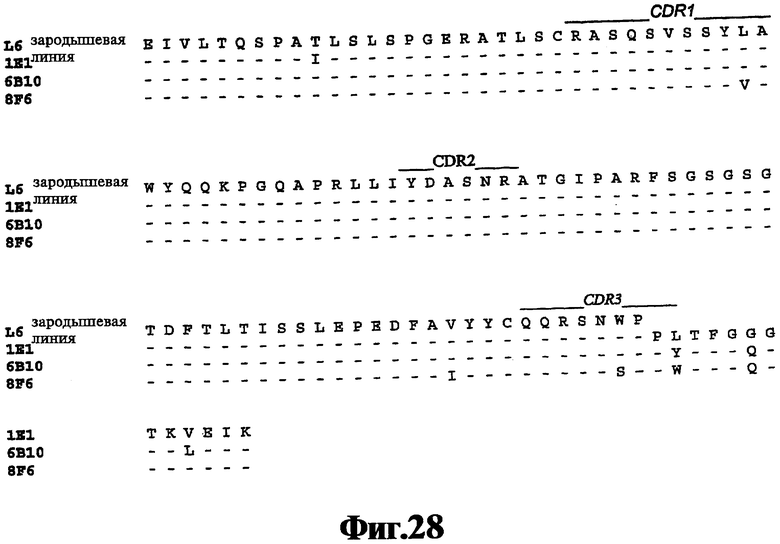
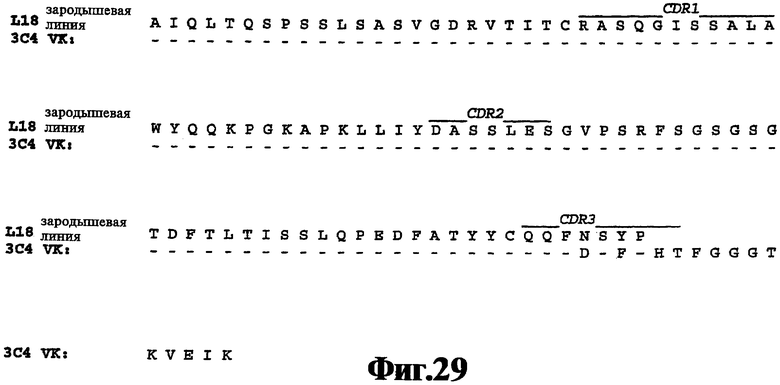
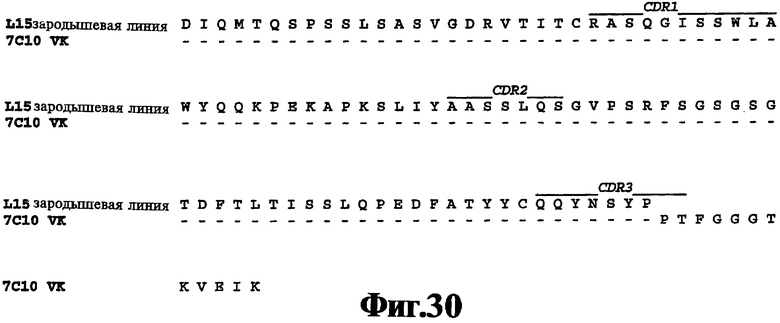
Изобретение относится к иммунологии. Предложены варианты выделенных моноклональных антител или антигенсвязывающей части, специфичных к IP-10 человека. Описаны: иммуноконъюгат, биспецифическая молекула на их основе, а также варианты композиции на основе антитела, иммуноконъюгата или биспецифической молекулы - для лечения аутоиммунных и воспалительных заболеваний. Также раскрыты: кодирующая нуклеиновая кислота, экспрессионный вектор на ее основе и клетка-хозяин, несущая такой вектор, для получения антитела. Описано применение антитела или антигенсвязывающей части для получения лекарственного средства для лечения: либо вирусной или бактериальной инфекции, влекущей за собой нежелательную активность IP-10, либо аутоиммунных и воспалительных заболеваний, вызванных нежелательной активностью IP-10. Предложена гибридома, продуцирующая антитело, полученная из спленоцита трансгенной мыши, сшитого с иммортализованной клеткой. Использование изобретения обеспечивает новые антитела, которые могут найти применение в медицине для лечения различных заболеваний, связанных с активностью IP-10. 12 н. и 10 з.п. ф-лы, 30 ил., 9 табл., 8 пр.
1. Выделенное моноклональное антитело или его антигенсвязывающая часть, обладающее способностью специфически связываться с IP-10 человека, причем указанное антитело или его антигенсвязывающая часть включает:
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:1,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:13,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:24,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:51,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:62 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:73;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:5,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:17,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:28,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:55,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:66 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:77;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:9,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:21,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:32,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:59,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:70 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:81;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:2,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:14,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:25,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:52,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:63, и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:74;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:3,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:15,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:26,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:53,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:64, и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:75;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:4,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:16,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:27,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:54,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:65 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:76;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:6,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:18,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:29,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:56,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:67 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:78;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:7,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:19,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:30,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:57,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:68 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:79;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:8,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:20,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:31,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:58,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:69, и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:80;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:10 или 11;
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:22,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:33,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:60,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:71, и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:82;
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:12,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:23,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:34,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:61,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:72, и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:83.
2. Антитело или его антигенсвязывающая часть по п.1, которое содержит:
CDR1 вариабельной области тяжелой цепи, включающий SEQ ID NO:5,
CDR2 вариабельной области тяжелой цепи, включающий SEQ ID NO:17,
CDR3 вариабельной области тяжелой цепи, включающий SEQ ID NO:28,
CDR1 вариабельной области легкой цепи, включающий SEQ ID NO:55,
CDR2 вариабельной области легкой цепи, включающий SEQ ID NO:66 и
CDR3 вариабельной области легкой цепи, включающий SEQ ID NO:77.
3. Антитело или его антигенсвязывающая часть по п.1, которое включает:
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:35 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:84;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:39 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:88;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:43 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:92;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:36 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:85;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:37 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:86;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:38 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:87;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:40 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:89;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:41 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:90;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:42 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:91;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:44 или 45 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:93;
вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:46 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:94.
4. Антитело или его антигенсвязывающая часть по п.2, которое включает вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO:39 и
вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO:88.
5. Выделенное моноклональное антитело или его антигенсвязывающая часть по любому из пп.1-4, которое обладает по меньшей мере одним из следующих свойств:
ингибирует связывание IP-10 с CXCR3;
ингибирует индуцируемый IP-10 ток кальция;
ингибирует индуцируемую IP-10 миграцию клеток;
является перекрестно-реактивным с IP-10 макаки-резуса;
не является перекрестно-реактивным с мышиным IP-10;
не является перекрестно-реактивным с человеческим MIG;
не является перекрестно-реактивным с человеческим ITAC.
6. Антитело или его антигенсвязывающая часть по п.1, которое представляет собой антитело полной длины изотипа lgG1 или lgG4.
7. Антитело или его антигенсвязывающая часть по п.1, которое представляет собой фрагмент антитела или одноцепочечное антитело.
8. Композиция для лечения воспалительных и аутоиммунных заболеваний на основе специфического связывания IP-10 человека, включающая терапевтически эффективную дозу антитела или его антигенсвязывающей части по любому из пп.1-7 и фармацевтически приемлемый носитель.
9. Иммуноконъюгат для лечения воспалительных и аутоиммунных заболеваний на основе специфического связывания IP-10 человека, включающий антитело или его антигенсвязывающую часть по любому из пп.1-7, связанные с терапевтическим агентом.
10. Иммуноконъюгат по п.9, в котором терапевтический агент представляет собой цитотоксин.
11. Иммуноконъюгат по п.9, в котором терапевтический агент представляет собой радиоактивный изотоп.
12. Композиция для лечения воспалительных и аутоиммунных заболеваний на основе специфического связывания IP-10 человека, включающая терапевтически эффективную дозу иммуноконъюгата по любому из пп.9-11 и фармацевтически приемлемый носитель.
13. Биспецифическая молекула для лечения воспалительных и аутоиммунных заболеваний на основе специфического связывания IP-10 человека, включающая антитело или его антигенсвязывающую часть, обладающее способностью специфически связываться с IP-10 человека, по любому из пп.1-7, связанные со второй функциональной группой, имеющей другую специфичность связывания, чем указанное антитело или его антигенсвязывающая часть.
14. Композиция для лечения воспалительных и аутоиммунных заболеваний на основе специфического связывания IP-10 человека, включающая терапевтически эффективную дозу биспецифической молекулы по п.13 и фармацевтически приемлемый носитель.
15. Выделенная молекула нуклеиновой кислоты, кодирующая антитело или его антигенсвязывающую часть по любому из пп.1-7.
16. Экспрессионный вектор, включающий молекулу нуклеиновой кислоты по п.15.
17. Клетка-хозяин для получения антитела по любому из пп.1-7, содержащая экспрессионный вектор по п.16.
18. Гибридома, продуцирующая антитело по любому из пп.1-7, полученная из спленоцита, который выделен из трансгенной мыши, содержащей трансген или трансхромосому тяжелой цепи человека и трансген или трансхромосому легкой цепи человека, и сшит с иммортализованной клеткой.
19. Применение антитела или его антигенсвязывающей части по любому из пп.1-7 в качестве компонента для получения лекарственного средства для лечения воспалительного или аутоиммунного заболевания, вызванного нежелательной активностью IP-10.
20. Применение по п.19, в котором заболевание выбрано из группы, состоящей из рассеянного склероза, ревматоидного артрита, воспалительной болезни кишки (например, язвенного колита, болезни Крона), системной красной волчанки, диабета типа I, воспалительных кожных нарушений (например, псориаза, плоского лишая), аутоиммунного заболевания щитовидной железы (например, болезни Грейвса, тиреоидита Хашимото), синдрома Шегрена, легочного воспаления (например, астмы, хронической обструктивной болезни легких, саркоидоза легких, аутоиммунного альвеолита), отторжения трансплантата, повреждения спинного мозга, повреждения головного мозга (например, инсульта), нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона), гингивита, воспаления, вызванного генотерапией, болезней ангиогенеза, воспалительной болезни почек (например, IgA нефропатии, мембранопролиферативного гломерулонефрита, быстро прогрессирующего гломерулонефрита) и атеросклероза.
21. Применение антитела или его антигенсвязывающей части по любому из пп.1-7 в качестве компонента для получения лекарственного средства для лечения вирусной или бактериальной инфекции, влекущей нежелательную активность IP-10.
22. Применение по п.21, в котором вирусная инфекция опосредована вирусом иммунодефицита человека (ВИЧ), вирусом гепатита С (HCV), вирусом простого герпеса типа I (HSV-1) или вирусом тяжелого острого респираторного синдрома (SARS).
| US 20030166589 A1, 04.09.2003 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГЕПТАДИЕН-3,5-ОНА-2 | 1966 |
|
SU215932A1 |
| CARR et al., "Effect of Anti-CXCL10 Monoclonal Antibody on Herpes Simplex Virus Type 1 | |||
| Keratitis and Retinal Infection", J | |||
| Virol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| РОЙТ и др | |||
| Иммунология, пер | |||
| с англ | |||
| - М.: Мир, 2000, с.107-112, 150. | |||
Авторы
Даты
2013-06-27—Публикация
2004-12-10—Подача