Область техники, к которой относится изобретение
Изобретение относится к медицине, в частности к получению дефукозилированных антител к фактору CD30 человека, демонстрирующих повышенную зависящую от антител клеточную цитотоксичность по отношению к клеткам, экспрессирующим фактор CD30, которые не лизируются фукозилированными формами. Изобретение направлено также на хозяйские клетки, экспрессирующие анти-CD30 антитела без фукозильных остатков. Предлагаются также способы ингибирования роста клеток, экспрессирующих CD30, включая опухолевые клетки.
Уровень техники
Молекула клеточной поверхности CD30 входит в состав подсемейства рецепторов фактора некроза опухолей (TNF-R). Члены этого семейства характеризуются вариабельной гомологией, в него входят рецептор фактора роста нервов (NGFR), CD120(a), CD120(b), CD27, CD40 и CD95. Эти молекулы, обычно, характеризуются наличием множественных обогащенных цистеином повторов в экстрацитоплазматической области (de Bruin, Р.С., et al. Leukemia 9:1620-1627 (1995)). Считается, что члены этого семейства играют решающую роль в регуляции пролиферации и дифференциации лимфоцитов. CD30 представляет собой трансмембранный гликопротеин типа I с шестью (для людей) или тремя (для мышей и крыс) обогащенными цистеином повторами в последовательности центральной петли. CD30 существует в виде молекулы весом 120 кДа, образующейся из внеклеточного протеина-предшественника весом 90 кДа. Он уходит ("слущивается") с клеточной поверхности в виде растворимого протеина (sCD30) весом, приблизительно, 90 кДа. Слущивание sCD30 представляет собой активный процесс живой клетки, а не просто вызывается высвобождением белка из умирающей или мертвой клетки. Кодирующие протеин CD30 кДНК (cDNA) удалось клонировать из библиотек экспрессии линии HLTV-1 человеческих Т-клеток HUT-102 методом иммуноскрининга с моноклональными антителами Ki-1 и Ber-H2 (Schwab, U., et al. Nature 299:65 (1982)). Обнаружено, что мышиные и крысиные кДНК CD30 кодируют последовательности аминокислот длиной 498 и 493 остатка, соответственно. Человеческая кДНК CD30 кодируют дополнительно еще 90 аминокислотных остатков, частично дублирующихся из одного из обогащенных цистеином доменов. Ген CD30 был картирован на 1р36 у людей и 5q36.2 у крыс.
Преимущественно, CD30 экспрессируется в активированных лимфоидных клетках. В частности, показано, что стимуляция CD30 в лимфоидных клетках индуцирует плейотропные биологические эффекты, включая пролиферацию, активацию, дифференциацию и смерть клеток, в зависимости от типа клеток, стадии дифференциации и наличия других стимулов (Gruss, H.J. et al., Blood 83:2045-2056 (1994)). Первоначально CD30 идентифицировали с помощью моноклонального антитела Ki-1, которое реагирует с антигенами, экспрессирующимися в клетках Ходжки на (Hodgkin) и Рид-Стернберга (Reed-Stern berg) болезниХоджкина. Соответственно, CD30 широко используются как клинический маркер лимфомы Ходжкина и родственных гематологических злокачественных заболеваний (Froese et al., J. Immunol. 139:2081 (1987); Carde et al., Eur. J. Cancer 26:474 (1990)).
Показано, что CD30 экспрессируется в подмножестве лимфом, не являющихся лимфомами Ходжкина (NHL), включая лимфому Буркитта, анапластические крупноклеточные лимфомы (ALCL), кожные лимфомы Т-клеток, узелковые лимфомы мелкорасщепленных клеток, лимфомы лимфоцитов, лимфомы периферических Т-клеток, лимфомы Леннерта, лимфомы иммунобластов, лейкемии/лимфомы Т-клеток (ATLL), лейкемия взрослых Т-клеток (T-ALL) и фолликулярные лимфомы энтеробластов/центроцитов(cb/сс) (Stein et al., Blood 66:848 (1985); Miettinen, Arch. Pathol. Lab. Med. 116:1197 (1992); Piris et al., Histopathology 17:211 (1990); Burns et al., Am. J. Clin. Pathol. 93:327(1990); и Eckert et al., Am. J. Dermatopathol. 11:345 (1989)), а также в нескольких клеточных линиях, трансформированных вирусами, таких как Т-клетки, трансформированные Т-клеточным лимфотропным вирусом I или II и в В-клетках, трансформированных вирусом Эпштейна-Барра (Stein et al., Blood 66:848 (1985); Andreesen et al., Blood 63:1299 (1984)). Кроме того, экспрессия CD-30 документирована в эмбриональных и неэмбриональных карциномах, злокачественных меланомах, мезенхимных опухолях, а также в миелоидных клеточных линиях и макрофагах на поздней стадии дифференциации (Schwarting et al., Blood 74:1678 (1989); Pallesen et al., Am J. Pathol. 133:446 (1988); Mechtersheimer et al., Cancer 66:1732 (1990); Andreesen et al., Am. J. Pathol. 134:187 (1989)).
Поскольку процентное содержание CD30-пoлoжитeльныx клеток у нормальных индивидуумов весьма мало, экспрессия CD30 в раковых клетках делает их важной мишенью опосредуемой антителами терапии, осуществляемой специфическими целевыми терапевтическими агентами против CDSO-положительных неопластических клеток (Chaiarle, R., et al. Clin. Immunol. 90(2): 157-164 (1999)). Показано, что опосредуемая антителами терапия усиливает цитотоксичность CD30-положительных клеток путем как комплементарной активации, так и зависящей от антител клеточной цитотоксичностью (ADCC) (Pohl С., et al. Int J Cancer 54:418 (1993)). Однако, хотя полученные на сегодняшний день результаты ясно показывают, что CD30 является полезной мишенью для иммунотерапии, они также демонстрируют, что доступные на настоящее время мышиные антитела не являются идеальными терапевтическими агентами. В случае пациентов с рефракторной болезнью Ходжкина пассивная терапия антителами не показала эффективности in vitro или in vivo. Клинические испытания анти-CD30 антител Ber-Н2 позволили определить локализацию антител, но не продемонстрировали ответов (Falini В. et al. (1992) Brit J Haematol. 82:38-45; Koon, H.B. et al. (2000) Curr Opin in Oncol. 12:588-593). В ходе лечения человеческой болезни Ходжкина на мышиной модели SCID совместное использование анти-CD30 антител и дегликозилированного цепного токсина Ricin toxin-A привело к развитию цитотоксичности, токсичность третьей степени наблюдалась также и у людей (Schell, R. et al. (2002) Annals of Oncology 13:57-66).
Таким образом, в настоящее время существует потребность в улучшенных терапевтических антителах против CD30, более эффективных (по сравнению с имеющимися аналогами) при лечении и/или профилактике болезней, опосредуемых CD30.
Раскрытие изобретения
Настоящее изобретение направлено на изолированные дефукозилированные антитела (то есть, на антитела без остатков фукозы), которые связываются с CD30 человека и демонстрируют улучшенную опосредованную (направляемую) антителами клеточную цитотоксичность (ADCC) по отношению к клеткам, экспрессирующим CD30, по сравнению с недефукозилированной формой антител (то есть, сантителами, содержащими остатки фукозы). Изобретение направлено также на методы лечения разнообразных заболеваний, при которых наблюдается экспрессия CD30, с использованием антител и композиций настоящего изобретения.
В соответствии с одним своим аспектом, изобретение направлено на выделенные дефукозилированные моноклональные антитела, или их антиген-связывающие фрагменты, где эти антитела связываются с человеческим белком CD30 с KD 10×10-8 М или меньше, более предпочтительно 1×10-8 М, еще более предпочтительно 5×10-9 М или меньше, наиболее предпочтительно 1×10-9 или меньше.
Дефукозилированные антитела настоящего изобретения связываются с CD30 и ингибируют рост клеток, экспрессирующих CD30, усиливая зависящую от антител клеточную цитотоксичность (ADCC) в присутствии человеческих клеток-эффекторов (например, моноцитов или моноядерных клеток), по сравнению с фукозилированной формой антител. В соответствии с одним аспектом изобретения, дефукозилированные антитела опосредуют повышение ADCC экспрессирующих CD30 клеток в присутствии человеческих эффекторных клеток, но не мышиных эффекторных клеток.
В соответствии с предпочтительным аспектом изобретения, дефукозилированные антитела настоящего изобретения индуцируют ADCC клеток L1236 in vitro, а фукозилированная форма антител не индуцирует ADCC, при условии концентрации антитела 0,1 мкг/мл и отношения целевых клеток к клеткам-эффекторам, составляющего 1:50. В соответствии с другим предпочтительным аспектом, дефукозилированные антитела настоящего изобретения усиливают ADCC клеточных лини и L540, L428 и Karpas in vitro, no сравнению с фукозилированной формой антител, при условии концентрации антител 0,1 мкг/мл и отношения целевых клеток к клеткам-эффекторам, составляющего 1:50. Соответственно, антитела настоящего изобретения представляют собой усовершенствованные средства лечения заболеваний, характеризующихся экспрессией CD30.
Предпочтительно, если дефукозилированные антитела настоящего изобретения представляют собой моноклональные антитела. В соответствии с одним своим аспектом, изобретение направлено на гуманизированные или химерные моноклональные антитела. Предпочтительно, если человеческие или химерные антитела готовятся из мышиных анти-CDSO антител, выбранных из группы, содержащей АС 10, HeFi-1, Ber-H2, Ki-1, Ki-4, HRS-3, Irac, HRS-4, M44, M67, Ber-H8. В соответствии с другим своим аспектом, изобретение направлено на человеческие моноклональные антитела.
В соответствии с одним воплощением изобретения, человеческие моноклональные антитела содержат:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, содержащей SEQ ID NO:1, 2 и 3; и
(b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, содержащей SEQ ID NO:4, 5 и 6.
Где антитела связывают CD30 и не содержат остатков фукозы.
Предпочтительная комбинация содержит:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:1; и
(b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:4.
Еще одна предпочтительная комбинация содержит:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:2; и
(b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:5.
Еще одна предпочтительная комбинация содержит:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:3; и
(b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:6.
В соответствии с другим аспектом, изобретение направлено на дефукозилированные анти-CD30 антитела, содержащие:
вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2, и CDR3; и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2, и CDR3, где:
(a) последовательность вариабельной области тяжелой цепи CDR1 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:7, 8 и 9;
(b) последовательность вариабельной области тяжелой цепи CDR2 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:10, 11 и 12;
(c) последовательность вариабельной области тяжелой цепи CDR3 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:13, 14 и 15;
(a) последовательность вариабельной области легкой цепи CDR1 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:16, 17 и 18;
(b) последовательность вариабельной области легкой цепи CDR2 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:19, 20 и 21; и
(c) последовательность вариабельной области легкой цепи CDR3 содержит аминокислотную последовательность выбранную из группы, включающей аминокислотные последовательности SEQ ID NO:22, 23 и 24;
Где антитела связываются с CD30 и не содержат остатков фукозы.
Предпочтительная комбинация включает:
(a) вариабельную область тяжелой цепи человека CDR1, содержащую SEQ ID NO:7;
(b) вариабельную область тяжелой цепи человека CDR2, содержащую SEQ ID NO:10;
(c) вариабельную область тяжелой цепи человека CDR3, содержащую SEQ ID NO:13;
(d) вариабельную область легкой цепи человека CDR1, содержащую SEQ ID NO:16;
(e) вариабельную область легкой цепи человека CDR2, содержащую SEQ ID NO:19; и
(f) вариабельную область легкой цепи человека CDR3, содержащую SEQ ID NO:22.
Еще одна предпочтительная комбинация включает:
(a) вариабельную область тяжелой цепи человека CDR1, содержащий SEQ ID NO:8;
(b) вариабельную область тяжелой цепи человека CDR2, содержащую SEQ ID NO:11;
(c) вариабельную область тяжелой цепи человека CDR3, содержащую SEQ ID NO:14;
(d) вариабельную область легкой цепи человека CDR1, содержащую SEQ ID NO:17;
(e) вариабельную область легкой цепи человека CDR2, содержащую SEQ ID NO:20; и
(f) вариабельную область легкой цепи человека CDR3, содержащую SEQ ID NO:23.
Еще одна предпочтительная комбинация включает:
(a) вариабельную область тяжелой цепи человека CDR1, содержащую SEQ ID NO:9;
(b) вариабельную область тяжелой цепи человека CDR2, содержащую SEQ ID NO:12;
(c) вариабельную область тяжелой цепи человека CDR3, содержащую SEQ ID NO:15;
(d) вариабельную область легкой цепи человека CDR1, содержащую SEQ ID NO:18;
(e) вариабельную область легкой цепи человека CDR2, содержащую SEQ ID NO:21; и
(f) вариабельную область легкой цепи человека CDR3, содержащую SEQ ID NO:24.
В соответствии с еще одним аспектом, изобретение направлено на дефукозилированные анти-CD30 антитела человека, содержащие вариабельную область тяжелой цепи, которая представляет собой продукт или производное гена VH 4-34 или VH 3-07 человека. Изобретение также направлено на дефукозилированные анти-CD30 антитела человека, содержащие вариабельную область легкой цепи, которая представляет собой продукт или производное гена Vk L15, А27 или L6 человека. Кроме того, изобретение направлено на дефукозилированные анти-CD30 антитела человека, содержащие вариабельную область тяжелой цепи, которая представляет собой продукт или производное гена VH 4-34 или VH 3-07 человека, и вариабельную область легкой цепи, которая представляет собой продукт или производное гена Vk L15, А27 или L6 человека.
В соответствии с еще одним аспектом, изобретение направлено на хозяйскую клетку, содержащую гены тяжелых и легких цепей иммуноглобулина, кодирующие анти-CD30 антитела, где указанная клетка не содержит фукозил трансферазу, так что экспрессируемые указанной клеткой анти-CD30 антитела не содержат остатков фукозы. Предпочтительно, чтобы гены тяжелых и легких цепей иммуноглобулина представляли собой гены тяжелых и легких цепей иммуноглобулина человека. Предпочтительно, если фукозил трансфераза - это FUT8. Предпочтительно, чтобы клетка относилась к линии СНО.
В соответствии с еще одним аспектом, изобретение направлено на метод ингибирования роста клеток CD30+. Метод включает приведение клеток в контакт с дефукозилированными анти-CD30 антителами в условиях, достаточных для индукции опосредуемой антителами клеточной цитотоксичности (ADCC) указанных клеток. Клетки могут быть, например, опухолевыми клетками. Предпочтительно, чтобы анти-CD30 антитела представляли собой антитела человека.
Изобретение направлено также на метод ингибирования роста экспрессирующих CD30 опухолевых клеток субъекта. Указанный метод включает назначение субъекту дефукозилированных анти-CD30 антител в количестве, эффективном для ингибирования роста опухолевых клеток субъекта, экспрессирующих CD30. Предпочтительно, чтобы анти-CD30 антитела представляли собой антитела человека. В соответствии с предпочтительными аспектами, опухолевые клетки представляют собой опухолевые клетки болезни Ходжкина (Hodgkin's Disease (HD)) или анапластической крупноклеточной лимфомы (anaplastic large-cell lymphoma (ALCL)).
Другие аспекты и преимущества настоящего изобретения станут очевидны из следующего далее подробного описания и примеров, которые не ограничивают область изобретения. Содержание всех ссылок, записей генетического банка (Genbank), патентов и опубликованных патентных заявок, процитированных в настоящей заявке, явным образом включены в нее по ссылке.
Краткое описание чертежей
На Фиг.1 показана нуклеотидная последовательность (SEQ ID NO:30) и аминокислотная последовательность (SEQ ID NO:1) вариабельной области тяжелой цепи человеческого моноклонального антитела 5F11. Отмечены области CDR1 (SEQ ID NO:7), CDR2 (SEQ ID NO:10) и CDR3 (SEQ ID NO:13), указаны зародышевые производные V, D и J.
На Фиг.2 показана нуклеотидная последовательность (SEQ ID NO:33) и аминокислотная последовательность (SEQ ID NO:4) вариабельной области легкой цепи человеческого моноклонального антитела 5F11. Отмечены области CDR1 (SEQ ID NO:16), CDR2 (SEQ ID NO:19) и CDR3 (SEQ ID NO:22), указаны зародышевые производные V и J.
На Фиг.3 показана нуклеотидная последовательность (SEQ ID NO:31) и аминокислотная последовательность (SEQ ID NO:2) вариабельной области тяжелой цепи человеческого моноклонального антитела 17G1. Отмечены области CDR1 (SEQ ID NO:8), CDR2 (SEQ ID NO:11) и CDR3 (SEQ ID NO:14), указаны зародышевые производные V и J.
На Фиг.4 показана нуклеотидная последовательность (SEQ ID NO:34) и аминокислотная последовательность (SEQ ID NO:5) вариабельной области легкой цепи человеческого моноклонального антитела 17G1. Отмечены области CDR1 (SEQ ID NO:17), CDR2 (SEQ ID NO:20) и CDR3 (SEQ ID NO:23), указаны зародышевые производные V и J.
На Фиг.5 показана нуклеотидная последовательность (SEQ ID NO:32) и аминокислотная последовательность (SEQ ID NO:3) вариабельной области тяжелой цепи человеческого моноклонального антитела 2Н9. Отмечены области CDR1 (SEQ ID NO:9), CDR2 (SEQ ID NO:12) и CDR3 (SEQ ID NO:15), указаны зародышевые производные V, D и J.
На Фиг.6 показана нуклеотидная последовательность (SEQ ID NO:35) и аминокислотная последовательность (SEQ ID NO:6) вариабельной области легкой цепи человеческого моноклонального антитела 2Н9. Отмечены области CDR1 (SEQ ID NO:18), CDR2 (SEQ ID NO:21) и CDR3 (SEQ ID NO:24), указаны зародышевые отклонения V и J.
Фиг.4 представляет собой график, на котором показано цитотоксическое убивающее клетки действие фукозилированной и дефукозилированной форм 5F11 на клеточную линию L540 лимфомы Ходжкина человека, по сравнению с изотипно соответствующим контрольным антителом (1D4).
Фиг.5 представляет собой график, на котором показано цитотоксическое убивающее клетки действие фукозилированной и дефукозилированной форм 5F11 на клеточную линию L428 лимфомы Ходжкина человека, по сравнению с изотипно соответствующим контрольным антителом (1D4).
Фиг.6 представляет собой график, на котором показано цитотоксическое убивающее клетки действие фукозилированной и дефукозилированной форм 5F11 на клеточную линию L1236 лимфомы Ходжкина человека, по сравнению с изотипно соответствующим контрольным антителом (1D4).
Фиг.7 представляет собой график, на котором показано цитотоксическое убивающее клетки действие фукозилированной и дефукозилированной форм 5F11 на клеточную линию лимфомы Karpas Т-клеток человека, по сравнению с изотипно соответствующим контрольным антителом (1D4).
На Фиг.11-12 показаны аминокислотные последовательности человеческих зародышевых линий VH 3-11, VK L15, VK A27, и VK L6 (SEQ ID NOs:25-29, соответственно), отмечены области CDR.
Фиг.9 представляет собой график, на котором показана блокада активности ADCC анти-CD16 антителами.
Фиг.10 представляет собой график, на котором показано цитотоксическое убивающее клетки действие фукозилированной и дефукозилированной форм 5F11 в присутствии мышиных (левая панель) или человеческих (правая панель) эффекторных клеток.
Фиг.11 представляет собой график, демонстрирующий эссэй (анализ) ADCC с использованием крови мартышек cynomolgus.
Осуществление изобретения
Настоящее изобретение направлено на усовершенствованные композиции антител, ассоциированные с CD30 и/или клетками, экспрессирующими CD30. Антитела настоящего изобретения не содержат фукозильных остатков на своих углеводородных цепях. Более того, антитела демонстрируют улучшенную направляемую антителами клеточную цитотоксичность (ADCC), связанную с уничтожением клеток CD30+. В соответствии с конкретным аспектом изобретения, антитела настоящего изобретения способны убивать клетки CD30+ в таких условиях, в которых фукозилированная форма антител эффективно убивать клетки CD30+ не может. В соответствии с другим аспектом, антитела настоящего изобретения усиливают уничтожение клеток CD30+, по сравнению с фукозилированной формой этих антител. В соответствии с одним аспектом, антитела настоящего изобретения представляют собой полностью гуманизированные антитела и особенно полезны для терапевтического лечения заболеваний людей, связанных с CD30-экспрессирующими клетками. Методы применения анти-CD30 антител без фукозильных остатков для терапевтического лечения (то есть, для лечения и/или профилактики заболеваний, связанных с экспрессией CD30) также охватываются настоящим изобретением.
Чтобы лучше понять настоящее изобретение, необходимо определить некоторые термины. Это сделано далее. В подробном описании будут введены также дополнительные определения.
Термины "CD30" и "антиген CD30" используются здесь взаимозаменяемо и включают любые варианты, изоформы и межвидовые гомологи человеческого CD30, естественно экспрессирующиеся клетками. Выданный Генбанком номер полной аминокислотной последовательности человеческого белка CD30 - это NPJ301234. Полная последовательность кДНК, кодирующая человеческий белок CD30, получила номер Генбанка NM_001243.
В настоящем изобретении термины "антитела без остатков фукозы" и "дефукозилированные антитела" используются взаимозаменяемо и означают антитела, углеводные фрагменты которых не содержат фукозильных остатков, или у которых фукозильные остатки были удалены. Антитела без фукозильных остатков можно получить, например, экспрессией антитела в клетке или системе экспрессии, которая не прикрепляет фукозильные остатки к углеводной цепи антитела или минимизирует прикрепление, или путем химической модификации антитела, удаляющей фукозильные остатки с углеводной цепи (например, обработкой антитела фукозидазой). Термины "без остатков фукозы" и "дефукозилированные" не ограничены механизмами получения антител с измененной углеводной структурой.
В настоящем изобретении термины "антитела, экспрессирующие остатки фукозы" и "фукозилированные антитела" используются взаимозаменяемо и означают антитела, углеводные фрагменты которых содержат фукозу.
Термин "иммунный ответ" означает действие, например, лимфоцитов, антиген представляющих клеток, фагоцитирующих клеток, гранулоцитов и растворимых макромолекул, образующихся в упомянутых выше клетках или в печени (включая антитела, цитокины и комплементы), которое приводит к селективному повреждению, разрушению или выведению из человеческого организма внешних патогенов, клеток или тканей, инфицированных патогенами, раковых клеток или, в случае аутоиммунного заболевания или патологического воспаления, нормальных человеческих клеток или тканей.
В настоящем изобретении термин "эффекторные клетки" означает иммунные клетки, вовлеченный в эффекторную фазу иммунного ответа, а не в когнитивную фазу или фазу активации иммунного ответа. Примеры иммунных клеток включают клетки миелоидного или лимфоидного происхождения, например, лимфоциты (например, В- и Т-клетки, в том числе цитолитические Т-клетки (CTL)), клетки-киллеры, клетки-природные киллеры, макрофаги, моноциты, эозинофилы, нейтрофилы, полиморфоядерные клетки, гранулоциты, тучные клетки и базофилы. Некоторые эффекторные клетки экспрессируют специфические рецепторы Fc и выполняют специфические иммунные функции. В соответствии с предпочтительными аспектами, эффекторная клетка способна индуцировать зависящую от антител опосредованную клетками цитотоксичность (ADCC), например, такой способностью обладают нейтрофилы. Например, экспрессирующие FcR моноциты и макрофаги принимают участие в специфическом уничтожении клеток-мишеней и представлении антигенов другим компонентам иммунной системы или в связывании с клетками, которые представляют антигены. В соответствии с другими аспектами, эффекторная клетка может фагоцитировать антиген-мишень или клетку-мишень. Экспрессия конкретного FcR эффекторной клеткой может регулироваться гуморальными факторами, такими какцитокины. Например, показано, что экспрессия FcαRI усиливается под действием G-CSF или GM-CSF. Такая усиленная экспрессия усиливает эффекторную функцию клеток-носителей FcαRI по отношению к мишеням. Эффекторная клетка может фагоцитировать или лизировать антиген-мишень или клетку-мишень.
"Клетка-мишень" или "целевая клетка" означает любую клетку или патоген, чье уничтожение было бы благоприятно для субъекта (например, человека или животного), и на которое может быть направлена композиция (например, антитела) настоящего изобретения. Например, клеткой-мишенью может быть клетка, экспрессирующая или сверх-экспрессирующая CD30.
Термин "зависящая от антител клеточная цитотоксичность" или "ADCC" означает опосредуемую клетками цитотоксическую реакцию, когда клетка-мишень CD30+ со связанным анти-CD30 антителом распознается эффекторной клеткой с Fc рецепторами и затем лизируется без обязательного участия комплемента.
В контексте настоящего изобретения термин "усиливает ADCC" (например, применительно к клеткам) означает любое заметное усиление лизиса клеток при их взаимодействии с анти-CD30 антителами без фукозильных остатков, по сравнению с уничтожением этих клеток при взаимодействии с фукозилированными анти-CD30 антителами в присутствии эффекторных клеток (например, при отношении клетки-мишени: эффекторные клетки=1:50), например усиление лизиса клеток по меньшей мере, приблизительно, на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 150%, 200%, 250%, 300% или 325%.
Термин "антитело" в контексте настоящего изобретения включает целые антитела и их любые антиген-связывающие фрагменты (антиген-связывающие участки) или отдельные цепи. "Антитело" означает гликопротеин, содержащий по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, связанные между собой дисульфидными мостиками, или его антиген-связывающий участок. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (обозначается VH) и постоянную (константную) область тяжелой цепи. Постоянная область тяжелой цепи состоит из трех доменов, CH1, СH2 и СH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (обозначается VL) и постоянной области легкой цепи. Постоянная область легкой цепи состоит только из одного домена, СL. Регионы VH и VL можно также разделить на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), и перемежающимися с более консервативными областями, так называемыми каркасными областями (FR). Каждый VH и VL состоит из трех CDR и четырех FR, расположенными в следующем порядке, начиная от амино-конца и до карбоксильного конца: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелых и легких цепей содержат домен связывания, взаимодействующий с антигеном. Три постоянных области антитела могут опосредовать связывание иммуноглобулина с тканями или факторами носителя, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (Clq) классической системы комплемента.
Термин "антиген-связывающий участок антитела" (или просто "участок антитела") здесь означает один или несколько фрагментов антитела, обладающих способностью специфически связываться с антигеном (например, с CD30). Показано, что антиген-связывающая функция антитела может осуществляться фрагментами антитела полной длины. Примеры связывающих фрагментов антитела, подходящих под определение "антиген-связывающихучастков", включают: (i) фрагмент Fab, одновалентный фрагмент, состоящий из доменов VL, VH, СL и СH1; (ii) фрагмент F(ab')2, двухвалентный фрагмент, содержащий два домена Fab, связанных дисульфидными мостиками в области петли, (iii) фрагмент Fd, содержащий домены VH и СH1; (iv) фрагмент Fv, состоящий из доменов VL и VH одного "плеча" антитела; (v) фрагмент dAb (Ward et al., (1989) Nature 341:544-546), содержащий домен VH; и (vi) изолированную область (CDR). Более того, хотя два домена фрагмента Fv, VL и VH, кодируются двумя различными генами, их можно объединить с использованием рекомбинантных методов и синтетического линкера, в результате чего они будут образовываться как одна белковая цепочка, в которой пара областей VL и VH формирует одновалентные молекулы (называемых одноцепочечными Fv (scFv); см, например., Bird et al. (1988) Science 242:423-426; и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Такие одноцепочечные антитела также попадают под определение "антиген-связывающего участка антитела". Фрагменты этих антител получают традиционными методами, известными специалистам в соответствующей области; их проверка на применимость осуществляется так же, как и в случае интактных антител.
Термин "рекомбинантное человеческое антитело" здесь означает все человеческие антитела, которые готовят, экспрессируют, создают или выделяют рекомбинантными методами, в том числе (a) выделенные из животных (например, из мышей) антитела, трансгенные или трансхромосомальные с включением генов иммуноглобулина человека или приготовленные с помощью гибридом (далее этот метод описан подробно), (b) антитела, выделенные из хозяйских клеток, которые были трансформированы так, чтобы экспрессировать антитела человека, например, из трансфертом, (c) антитела, взятые из рекомбинантной комбинаторной библиотеки антител человека, и (d) антитела, приготовленные, экспрессированные, созданные или выделенные другими способами, предполагающими сплайсинг последовательностей гена иммуноглобулина человека на другие последовательности ДНК. Такие рекомбинантные человеческие антитела содержат вариабельные области, в которых области каркаса и CDR являются производными от иммуноглобулина зародышевых линий человека. В соответствии с некоторыми аспектами, однако, рекомбинантные человеческие антитела могут быть подвержены мутагенезу in vitro (или, в случае использования последовательностей животных, трансгенных по отношению к lg человека, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя и производны от человеческих зародышевых последовательностей VH и VL и родственны им, могут и не существовать в репертуаре зародышевых человеческих антител в природе.
Термин "моноклональное антитело" или "композиция моноклональных антител" здесь означает препарат молекул антитела одного молекулярного состава. Композиция моноклональных антител демонстрирует простую (одиночную) специфичность связывания и сродство к конкретному эпитопу.
Термин "антитело человека" здесь означает антитела с вариабельными областями, у которых как область каркаса, так и CDR, производны от последовательностей зародышевых линий иммуноглобулина человека. Более того, если антитело содержит постоянную область, то этот область также будет производным от последовательностей зародышевых линий иммуноглобулина человека. Антитела человека настоящего изобретения могут содержать аминокислотные остатки, не кодируемые последовательностями зародышевых линий иммуноглобулина человека (например, они могут быть результатом мутаций вследствие случайного или сайт-специфического мутагенеза in vitro или соматических мутаций in vivo).
Термин "человеческое моноклональное антитело" означает антитела, демонстрирующие простую специфичность связывания, каркасные и CDR вариабельные области которых производны от последовательностей зародышевых линий иммуноглобулина человека. В соответствии с одним аспектом изобретения, человеческие моноклональные антитела получают из гибридомы, которая содержит В-клетки трансгенного животного, например, трансгенной мыши, геном которых содержит трансген тяжелой цепи и легкой цепи человека, включенные в иммортализованную клетку. Термин "человеческое моноклональное антитело" здесь означает также все антитела человека, которые готовят, экспрессируют, создают или выделяют рекомбинантными методами, в том числе (a) выделенные из животных (например, из мышей) антитела, трансгенные или трансхромосомальные с включением генов иммуноглобулина человека или приготовленные с помощью гибридом (далее этот метод описан подробно), (b) антитела, выделенные из клеток-носителей, которые были трансформированы так, чтобы экспрессировать антитела человека, например, из трансфертом, (c) антитела, взятые из рекомбинантной комбинаторной библиотеки антител человека, и (d) антитела, приготовленные, экспрессированные, созданные или выделенные другими способами, предполагающими сплайсинг последовательностей гена иммуноглобулина человека на другие последовательности ДНК. Такие рекомбинантные человеческие антитела содержат вариабельные области, в которых области каркаса и CDR являются производными от иммуноглобулина зародышевых линий человека. В соответствии с некоторыми аспектами, однако, рекомбинантные человеческие антитела могут быть подвержены мутагенезу in vitro (или, в случае использования последовательностей животных, трансгенных по отношению к lg человека, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител представляютсобой последовательности, которые, хотя и производны от человеческих зародышевых последовательностей VH и VL и родственны им, могут и не существовать в репертуаре зародышевых человеческих антител в природе.
Термин "выделенное (изолированное) антитело" здесь означает антитела, в значительной степени свободные от примесей других антител с другой антигенной специфичностью (например, выделенные антитела, специфически связывающиеся с CD30, в значительной степени не содержат примесей антител, связывающихся с другими антигенами). Выделенные антитела, специфически связывающиеся с эпитопами, изоформами или вариантами человеческого CD30, могут, однако, обладать кросс-реактивностью по отношению к другим родственным антигенам, например, из других видов (например, видовые гомологи CD30). Более того выделенное антитело может быть в значительной степени свободно от примесей других клеточных компонентов и/или химических веществ. В соответствии с одним аспектом настоящего изобретения, комбинацию "выделенных" моноклональных антител с различной специфичностью объединяют в хорошо описанную композицию.
Термин "гуманизированное антитело" здесь означает антитела, у которых последовательности CDR, выделенные у зародышевых линий других млекопитающих, например, мыши, были трансплантированы в каркасные последовательности человека. В каркасные области этих последовательностей человека могут быть внесены дополнительные модификации.
Термин "химерное антитело" здесь означает антитела, вариабельные области последовательностей которых получены у одних видов, а постоянные области - у других видов. Например, у такого антитела вариабельные области могут быть производными от антитела мыши, а постоянные области - от антитела человека.
Термин "эпитоп" означает протеиновый детерминант, способный к специфическому связыванию к или с антителом. Обычно, эпитопы состоят из химически активных групп молекул на своей поверхности, такие как аминокислоты или боковые цепи Сахаров, и, обычно, характеризуются специфической трехмерной структурой и специфическими зарядами. Конформационные эпитопы отличаются от неконформационных тем, что связывание с первыми прекращается в присутствии денатурирующих агентов, а со вторыми - нет.
В настоящей заявке термин "специфическое связывание" означает связывание антитела с предопределенным антигеном. Как правило, при константа диссоциации (KD) комплекса антиген-антитело составляет 10-7 М или меньше, причем KD при связывании антитела с предопределенным антигеном по меньшей мере в два раза меньше KD связывания с неспецифическим антигеном (например, с BSA, казеином), то есть, не с предопределенным или близкородственным ему антигеном. Фразы "антитело, распознающее антиген" и "антитело, специфическое для антигена" используются взаимозаменяемо с термином "антитело, которое специфически связывается с антигеном".
Термин "изотип" означает здесь класс антитела (например, IgM или IgGI), кодирующийся генами постоянной области тяжелой цепи.
Термин "вектор" означает здесь молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она связана. Одним из типов вектора является "плазмида", представляющая собой петлю двухцепочечной ДНК, в которую могут быть встроены дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, дополнительные сегменты ДНК могут быть встроены в вирусный геном. Некоторые векторы способны автономно реплицироваться в клетке-носителе, в которую они были введены (например, бактериальные векторы с бактериальной природой репликации или эписомальные векторы млекопитающих). Другие векторы (например, не-эписомальные векторы млекопитающих) могут интегрироваться в геном клетки-носителя при попадании в нее и, таким образом, реплицируются вместе с геномом носителя. Более того, существуют векторы, способные управлять экспрессией генов, с которыми оперативно связаны. Такие векторы называются здесь "векторы рекомбинантной экспрессии" (или просто "векторы экспрессии"). В общем случае, векторы экспрессии, применимые в технологиях рекомбинантной ДНК, часто существуют в виде плазмид. В настоящей спецификации термины "плазмида" и "вектор" могут использоваться взаимозаменяемо, поскольку плазмида является самой распространенной формой вектора. Однако, настоящее изобретение охватывает также и другие формы векторов экспрессии, такие как вирусные векторы (например, ретровирусы сдефектом репликации, аденовирусы и адено-ассоциированные вирусы), которые выполняют эквивалентные функции.
Термин "рекомбинантная хозяйская клетка" (или просто "хозяйская клетка") в настоящем изобретении означает клетку, в которую был введен вектор рекомбинантной экспрессии. Необходимо понимать, что эти термины относятся не только к конкретной клетке, но и к ее потомству. Поскольку в последующих поколениях могут возникать различные модификации, определяемые либо мутациями, либо влиянием окружающей среды, такое потомство может и не быть идентичным родительской клетке, но, все-таки, оно входит в область действия термина "хозяйская клетка" в настоящей заявке. Рекомбинантные клетки включают, например, клетки СНО, трансфектомы и лимфотические клетки.
Термин "субъект" здесь означает человека или другое животное. Термин "другое животное" включает всех позвоночных, например, млекопитающих и немлекопитающих, таких как приматы (не люди), овцы, собаки, кошки, лошади, коровы, куры, амфибии, рептилии и т.д.
Термин "трансгенное животное" означает здесь животное (не человека), геном которого содержит один или больше трансген или трансхромосому тяжелых или легких цепей человека (интегрированных или неинтегрированных в природную геномную ДНК животного), и которое способно экспрессировать полностью человеческие антитела. Например, трансгенная мышь может содержать трансген легкой цепи человека и либо трансген, либо трансхромосому тяжелой цепи человека, так что такая мышь будет вырабатывать анти-CD30 антитела человека при иммунизации антигеном CD30 и/или экспрессирующими CD30 клетками. Трансген тяжелой цепи человека можно интегрировать в хромосомную ДНК мыши, что имеет место в случае трансгенной мыши, например, мыши HuMAb, а можно ввести его экстрахромосомно, что имеет место для трансхромосомной мыши (например, KM), как описано в патенте WO 02/43478. Такие трансгенные и трансхромосомные мыши способны вырабатывать различные изотипы моноклональных антител человека к CD30 (например, IgG, IgA и/или IgE), если осуществлять рекомбинацию V-D-J и переключать изотипы.
В следующих подразделах более подробно описаны различные аспекты настоящего изобретения.
Анти-CD30 антитела без остатков фукозы, обладающие усиленной активностью ADCC
Настоящее изобретение направлено на дефукозилированные анти-CD30 антитела с усиленной управляемой антителами клеточной цитотоксичностью (ADCC) по отношению к клеткам, экспрессирующим CD30, по сравнению с фукозилированной формой антител. В соответствии с предпочтительным аспектом, дефукозилированные антитела настоящего изобретения индуцируют ADCC клеток L1236 in vitro, а фукозилированная форма антител не индуцирует ADCC, в условиях, когда концентрация антител составляет 0,1 мкг/мл, а отношение количества клеток-мишеней к эффекторным клеткам составляет 1:50. В соответствии с еще одним предпочтительным аспектом, дефукозилированные антитела настоящего изобретения усиливают ADCC клеток L540, L428 и Karpas in vitro, по сравнению с фукозилированной формой антител, в условиях, когда концентрация антител составляет 0,1 мкг/мл, а отношение количества клеток-мишеней к эффекторным клеткам составляет 1:50.
Усиленную активность ADCC дефукозилированных антител настоящего изобретения можно количественно измерить, например, как увеличение процента лизиса клеток, по сравнению с фукозилированной формой антител, причем активность ADCC для фукозилированной и дефукозилированной форм измеряется в одних и тех же условиях (например, одинаковые концентрации антител и одинаковые отношения концентрации клеток мишеней к эффекторным клеткам). Предпочтительно, если дефукозилированные анти-CD30 антитела настоящего изобретения увеличивают процент лизиса CD30+ клеток (по сравнению с фукозилированной формой антител), по меньшей мере, в 1,25 раза (то есть, отношение процента лизиса под действием дефукозилированной формы к проценту лизиса под действием фукозилированной формы составляет по меньшей мере 1,25), более предпочтительно, если по меньшей мере в 2 раза, еще более предпочтительно, если по меньшей мере в 2,5 раза, наиболее предпочтительно, если по меньшей мере в 3 раза. В различных аспектах дефукозилированная форма антител усиливает процент лизиса клеток CD30+ по сравнению с фукозилированной формой от 1,25 до 3,25 раза, предпочтительно, от 1,5 до 3,25 раза, более предпочтительно, от 1,61 до 3,25 раза, еще более предпочтительно, от 2,15 до 3,25 раза, еще более предпочтительно, от 2,63 до 3,25 раза; предпочтительно, если это усиление происходит в условиях, когда концентрация антител составляет 25 мкг/мл, а отношение концентрации клеток мишеней к эффекторным клеткам составляет 1:50.
В дополнение к этому или альтернативно, усиленную активность ADCC дефукозилированных антител настоящего изобретения можно количественно измерить через снижение значения EC50 дефукозилированной формы, по сравнению с фукозилированной. Это снижение можно выразить как отношение EC50 фукозилированной формы к EC50 дефукозилированной формы. Предпочтительно, если указанное отношение для ADCC клеток CD30+ составляет, по меньшей мере, 3 (то есть, EC50 дефукозилированной формы в три раза меньше EC50 фукозилированной формы), более предпочтительно, если составляет, по меньшей мере 4, еще более предпочтительно, если, по меньшей мере, 5, по меньшей мере, 7, по меньшей мере, 10, по меньшей мере, 15 или, по меньшей мере, 20. В различных аспектах отношение EC50 фукозилированной формы к EC50 дефукозилированной формы для ADCC клеток CD30+ колеблется от 2 до 27,1, более предпочтительно, от 4 до 27,1, еще более предпочтительно, от 4,7 до 27,1, еще более предпочтительно, от 7,8 до 27,1, и еще более предпочтительно, от 11,1 до 27,1. Предпочтительно определять значения EC50 в анализах ADCC, когда отношение концентрации клеток мишеней к эффекторным клеткам составляет 1:50, а концентрация антител колеблется от 0,0001 мкг/мл до 10 мкг/мл или выше.
Примеры клеточных линий CD30+, которые могут использоваться в анализах ADCC, и по отношению к которым дефукозилированные антитела настоящего изобретения демонстрируют усиленную активность ADCC, по сравнению с фукозилированной формой антител, включают клетки L540 (человеческая лимфома Ходжкина; DSMZ No. ACC 72), L428 (человеческая лимфома Ходжкина; DSMZ No. ACC 197), L1236 cells (человеческая лимфома Ходжкина; DSMZ No. ACC 530), и клетки Karpas (лимфома Т-клеток человека; DSMZ No. ACC 31). Усиленный дефукозилированными анти-CD30 антителами ADCC эффект может приводить к ADCC-активности клеток CD30+при такой концентрации антител, когда ADCC, вообще, не наблюдается при использовании фукозилированной формы. Например, в анализах ADCC in vitro при отношении концентрации клеток мишеней к эффекторным клеткам 1:50 вызванная дефукозилированными анти-CD30 антителами ADCC наблюдается на L1236 линии клеток CD30+ в концентрации всего лишь 0,005 мкг/мл, в случае фукозилированных анти-CD30 антител никакой ADCC не наблюдается в концентрациях до 0,1 мкг/мл.
Дефукозилирование анти-CD30 антител
Анти-CD30 антитела (например, мышиные, химерные, гуманизированные и человеческие) известны в науке, и они могут применяться в настоящем изобретении. Анти-CD30 антитела настоящего изобретения модифицированы так, что у них отсутствуют фукозильные остатки. Антитела без фукозильных остатков можно получить различными способами. Например, с помощью технологий рекомбинантной ДНК их можно экспрессировать в клетке с измененным механизмом гликозилирования, при котором будет ингибироваться введение остатков фукозы в углеводную цепочку. Кроме того (или в дополнение к этому), антитела можно дефукозилировать, химически удалив фукозильные остатки.
В соответствии с одним аспектом изобретения, антитела экспрессируют в клетках, в которых отсутствует фермент фукозилтрансфераза, так что такая клеточная линия вырабатывает протеины без остатков фукозы в углеводных цепях. Например, ген фукозилтрансферазы FUT8 (альфа(1,6)фукозилтрансфераза) отсутствует в клеточных линиях Ms704, Ms705 и Ms709, так что в углеводных цепочках антител, экспрессирующихся в клетках Ms704, Ms705 и Ms709, отсутствуют остатки фукозы. Линии Ms704, Ms705, и Ms709 FUT8-/- были созданы целевым разрушением гена FUT8 в клетках CHO/DG44 с использованием двух векторов замещения (см U.S. Patent Publication No. 20040110704 by Yamane et al. и Yamane-Ohnuki et al. (2004) Biotechnol Bioeng 87:614-22). В качестве еще одного примера, в работе ЕР 1,176,195 Hanai et al. описывают клеточную линию с функционально поврежденным геном FUT8, кодирующим фукозил трансферазу, так что антитела, экспрессируемые в таких линиях, демонстрируют гипофукозилирование, уменьшая количество или вовсе устраняя фермент, родственный альфа 1,6 связи. Hanai с соавторами описывают клеточные линии, от природы характеризующиеся низкой активностью фермента, присоединяющего фукозу к N-ацетилглюкозамину, который связывается с областью Fc антитела, или не обладающие такой активностью. Например, это может быть линия крысиной миеломы YB2/0 (АТСС CRL 1662). Поданная Presta заявка РСТ Publication WO 03/035835 содержит описание вариантной линии клеток СНО, клеток Lec13 с уменьшенной способностью прикреплять фукозу к Asn(297)-связанным углеводам, что также приводит к гипофукозилированию антител, экспрессирующихся в этих клетках-носителях (см. также Shields, R.L et al. (2002) J. Biol. Chem. 277:26733-26740). В публикации РСТ WO 99/54342 Umana et al. описывает клеточные линии, сконструированные так, чтобы экспрессировать гликопротеин-модифицированные гликозил трансферазы (например, бета(1,4)-N-ацетилглюкозаминилтрансферазу III (GnTIII)), так что экспрессирующиеся в этих сконструированных клеточных линиях антитела демонстрировали повышенное содержание раздвоенных структур GlcNac, что приводило к повышению активности ADCC антител (см. также Umana et al. (1999) Nat. Biotech. 17:176-180).
В соответствии с другим аспектом, после экспрессии анти-СОЗО антител фукозильные остатки отщепляются от них с помощью фермента фукозидазы. Например, удалить фукозильные остатки от антител можно с помощью фукозидазы альфа-L-фукозидазы (Tarentino, A.L et al. (1975) Biochem. 14:5516-23).
Кроме того, в соответствии с другими аспектами, можно приготовить и другие формы гликозилированных антител. Например, можно сделать агликозилированные антитела (то есть, антитела без гликозилирования). Подобные углеводные модификации могут сопровождаться, например, изменением одного или нескольких сайтов гликозилирования последовательности антитела. Например, в результате одной или нескольких аминокислотных замен можно удалить один или несколько каркасных сайтов гликозилирования вариабельную область и, таким образом, этот сайт гликозилироваться не будет. Подобное агликозилирование может повышать сродство антитела к антигену. Подробно этот подход описан в патентах U.S. Nos. 5,714,350 и 6,350,861 Со et al.
Измерение отсутствия фукозильных остатков у анти-CD30 антител
Антитела настоящего изобретения не содержат фукозильных остатков, например, в фрагменте Fc углеводной цепи. Антитела можно проверить на отсутствие фукозильных остатков стандартными методами, известными в соответствующей области, например, капиллярным электрофорезом APTS с индукцией флуоресценции лазерным излучением. Кратко, N-связанные олигосахариды очищенных анти-CD30 антител выделяют, добавляя пептид N-гликаназу (Прозим) с последующей инкубацией в течение одной ночи. Углеводы ресуспендируют и дериватизируют 8-аминопирен-1,3,6-трисульфонатом(8-aminopyrene-1,3,6-trisulfonate(APTS)) в мягких условиях восстановительного аминирования, при которых минимизируется дезалилирование и отщепление фукозильных остатков. Аддукты реакции анализируют капиллярным электрофорезом с детекцией индуцированной лазером флуоресценции на детекторе производства Beckman Coulter. Отсутствие фукозы можно определить по сдвигу в электрофорезе, по сравнению с тем же антителом, содержащим фукозу. Отсутствие фукозы в анти-CD30 антителах можно определить также методом моносахаридного анализа с использованием HPLC. Подходящие для определения связывания CD30 анализы более подробно описаны в разделе примеров.
Измерение опосредованного антителами уничтожения клеток CD30+
Дефукозилированные анти-CD30 антитела можно проверить на способность опосредовать фагоцитоз и убийство клеток, экспрессирующих CD30. В соответствии с одним аспектом изобретения, дефукозилированные анти-CD30 антитела усиливают уничтожение клеток, экспрессирующих CD30, по сравнению с такими же антителами, содержащими фукозу в той же концентрации. В соответствии с другим аспектом, дефукозилированные анти-CD30 антитела индуцируют гибель экспрессирующих CD30 клеток, причем такие же антитела, содержащие фукозу, в той же концентрации не индуцируют эту гибель.
ADCC активность моноклональных антител можно проверить в анализах in vitro. Например, можно воспользоваться анализом ADCC, основанным на высвобождении хрома. Кратко, моноядерные клетки периферической крови (РВМС) или другие эффекторные клетки здоровых доноров очищают центрифугированием в градиенте плотности Ficoll Hypaque с последующим лизисом содержащихся там следовых количеств эритроцитов. Промытые РВМС суспендируют в RPMI с 10% инактивированной нагреванием фетальной телячьей сывороткой и смешивают с клетками, мечеными 51Cr и экспрессирующими CD30. Это делают с различным отношением концентрации эффекторных клеток к клеткам опухолей (эффекторные клетки: опухолевые клетки). После этого в различных концентрациях добавляют анти-CD30 антитела. В качестве отрицательного контроля можно использовать изотипно соответствующие антитела. Анализы выполняют при 37°С в течение 4-18 часов. Цитолиз образцов измеряют, определяя высвобождение 51Cr в культуральный супернатант. Можно также тестировать одновременный эффект различных анти-CD30 моноклональных антител, определяя, не усиливается ли цитолиз в присутствии нескольких форм антител.
Альтернативным анализом, позволяющим определить способность анти-CD30 антител опосредовать фагоцитоз и гибель экспрессирующих CD30 клеток, является разрешенный во времени флуорометрический анализ. Кратко, экспрессирующие CD30 клетки загружают в ацетоксиметильный эфир усиливающего флуоресценцию лиганда (BATDA), проникающего сквозь клеточные мембраны. Внутри клетки эфирные связи гидролизуются, и соединение уже не может проходить сквозь мембраны. После этого в различных концентрациях добавляют анти-CD30 антитела. Затем в систему вводят раствор европия (Perkin Elmer), и все свободные лиганды связываются с европием, формируя высоко флуоресцирующий стабильный комплекс (EuTDA), который можно определять на микропланшетном ридере (Perkin Elmer). Интенсивность измеренного сигнала коррелирует с количеством лизировавшихся клеток.
Анти-CD30 антитела можно тестировать на модели in vivo (например, на мышах), определяя их эффективность в опосредовании фагоцитоза и уничтожении экспрессирующих CD30 клеток, то есть, опухолевых клеток. Эти антитела можно выбирать, например, руководствуясь следующими не ограничивающимися критериями:
1) Связывание с живыми клетками, экспрессирующими CD30.
2) Высокое сродство при связывании CD30.
3) Связывание с уникальным эпитопом на CD30 (чтобы устранить возможную конкуренцию моноклональных антител с комплементарной активностью при совместном использовании).
4) Опсонизация клеток, экспрессирующих CD30.
5) Опосредование in vitro ингибирования роста, фагоцитоза и/или уничтожения клеток, экспрессирующих CD30, в присутствии эффекторных клеток человека.
Предпочтительные антитела настоящего изобретения соответствуют одному или нескольких перечисленным критериям. В конкретном аспекте настоящего изобретения, моноклональные антитела используют совместно, например, в составе фармацевтической композиции, содержащей два или более анти-CD30 моноклональных антитела или их фрагментов. Например, чтобы добиться желаемого терапевтического или диагностического эффекта, в одном составе можно объединить анти-CD30 моноклональные антитела с различной но комплементарной активностью. Иллюстрацией такого подхода является композиция, содержащая анти-CD30 моноклональные антитела, опосредующие высоко эффективное уничтожение клеток-мишеней в присутствии эффекторных клеток, а также еще один тип анти-CD30 моноклональных антител, ингибирующих рост клеток, экспрессирующих CD30.
Измерение связывания с CD30
Связывание антител настоящего изобретения с CD30 можно тестировать, например, стандартными методами анализа, известными в соответствующей области, такими как ELISA, FACS и/или Biacore. Кратко, в типичном анализе ELISA планшеты для микротитрования покрывают очищенным CD30 в концентрации 0.25 мкг/мл в PBS и затем блокируют раствором 5% бычьего сывороточного альбумина в PBS. В каждую ячейку вводят разбавленные до нужной концентрации антитела и инкубируют на 1-2 часа при температуре 37°C. Планшеты промывают после этого системой PBS/Tween и инкубируют с вторичным реагентом (например, Fc-специфическим поликлональным реагентом в случае антител человека или анти-человеческий IgG козы), конъюгированным к щелочной фосфатазе. Промывку осуществляют в течение часа при 37°C. По завершении промывки планшеты инкубируют с субстратом pNPP (1 мг/мл) и анализируют при OD 405-650.
Чтобы продемонстрировать связывание моноклональных антител с экспрессирующими CD30 живыми клетками, можно использовать цитометрию в потоке. В соответствии с типичным протоколом такого метода (не ограничивающим область изобретения), экспрессирующие CD30 клеточные линии (выращенные в стандартных условиях) смешивают с различными концентрациями моноклональных антител в PBS, содержащем 0.1% BSA и 20% мышиной сыворотки, и затем один час инкубируют при 37°C. После последующей промывки клетки реагируют с мечеными флуоресцеином вторичными антителами (например, анти-человеческим IgG) в тех же условиях, что и для первичных антител. Образцы можно анализировать на приборе FACScan, использующего свет и свойства бокового рассеяния, позволяющие регистрировать отдельные клетки. В дополнение или помимо цитометрии в потоке можно использовать также флуоресцентную микроскопию. Клетки окрашивают так, как было описано, и затем изучают методом флуоресцентной микроскопии. Данный метод позволяет увидеть отдельные клетки, но его чувствительность может быть понижена, в зависимости от плотности антигена.
Взаимодействие анти-CD30 антител с антигеном CD30 можно исследовать также методом Вестерн-блоттинга. Например, можно приготовить экстракты клеток, экспрессирующих CD30, и поставить с ними электрофорез в полиакриламидном геле с додецил сульфатом натрия. По окончании электрофореза выделенные антигены переносят на мембрану из микроцеллюлозы, блокируют 20% мышиной сывороткой и анализируют с помощью тестируемых моноклональных антител. Для детекции связывания антител можно использовать анти-специфические специфические вторичные антитела, соединенные со щелочной фосфатазой и поставляемые с субстратными таблетками BCIP/NBT (Sigma Chem. Co., St. Louis, МО). Известны и другие технологии, позволяющие оценить способность антител связываться с CD30, к их числу относятся RIA и анализ Biacore. Подробно подходящие методы определения связывания CD30 описаны в Примерах.
Химерные или гуманизированные анти-CD30 антитела
В соответствии с определенными аспектами, дефукозилированные анти-CD30 антитела настоящего изобретения представляют собой химерные или гуманизированные антитела. Такие антитела получают из доступных мышиных анти-CD30 антител с помощью известных процедур превращения мышиного антитела в химерное или гуманизированное антитело. Неограничивающие примеры таких мышиных анти-CD30 антител включают АС10, HeFi-1, Ber-H2, Ki-1, Ki-4, HRS-3, Irac, HRS-4, M44, M67 и Ber-Н8 моноклональные антитела. Более того, гуманизированные анти-CD30 антитела описаны в патентной публикации РСТ WO 02/4661.
Моноклональные анти-CD30 антитела человека
Предпочтительные антитела настоящего изобретения включают анти-CD30 моноклональные антитела человека. В качестве примеров таких антител можно указать 5F11, 17G1 и 2Н9, они были выделены и структурно охарактеризованы, как описано в WO 03/059282. Аминокислотные последовательности VH антител 5F11, 17G1 и 2Н9 представлены как SEQ ID NOs:1, 2 и 3, соответственно. Аминокислотные последовательности VL антител 5F11, 17G1 и 2Н9 представлены как SEQ ID NOs:4, 5 и 6, соответственно.
Поскольку каждая из этих молекул может связываться с CD30, последовательности VH и VL можно смешивать и спаривать друг с другом, создавая другие анти-CD30 связывающие молекулы настоящего изобретения. Для проверки способности таких "перемешанных" антител связывать CD30 можно воспользоваться анализами для определения связывания, хорошо известными в данной области, такими как анализы FACS и ELISA. Предпочтительно, когда цепи VH и VL смешаны и приведены в соответствие друг с другом, и последовательность VH конкретной пары VH/VL замещена на структурно похожую последовательность VH. Аналогично, предпочтительно, если последовательность VL конкретной пары VH/VL замещена на структурно похожую последовательность VL. Например, очень хорошо поддаются перемешиванию последовательности VH антител 5F11 и 2Н9, так как эта последовательность данных антител получена от одной и той же зародышевой последовательности (VH 4-34) и поэтому демонстрируют структурное сходство.
В соответствии с конкретными аспектами, изобретение направлено на дефукозилированные моноклональные антитела или их антиген-связывающие участки, содержащие:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы SEQ ID NOs:1, 2, и 3; и
(b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы SEQ ID NOs:4, 5, и 6;
Где антитела специфически связывают CD30 человека. Предпочтительные комбинации тяжелых и легких цепей включают:
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:1; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:4; или
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:2; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:5; или
(a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO:3; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO:6.
В соответствии с другим аспектом, изобретение направлено на дефукозилированные антитела, содержащие тяжелой и легкой цепи CDR1, CDR2 и CDR3 антител 5F11, 17G1 и 2Н9, или их комбинацию. Аминокислотные последовательности VH цепей CDR1 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:7, 8 и 9, соответственно. Аминокислотные последовательности VH цепей CDR2 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:10, 11 и 12, соответственно. Аминокислотные последовательности VH цепей CDR3 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:13, 14 и 15, соответственно. Аминокислотные последовательности Vk цепей CDR1 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:16, 17 и 18, соответственно. Аминокислотные последовательности Vk цепей CDR2 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:19, 20 и 21, соответственно. Аминокислотные последовательности Vk цепей CDR3 антител 5F11, 17G1 и 2Н9 представлены номерами SEQ ID NOs:22, 23 и 24, соответственно. Регионы CDR выделены в соответствии с системой Kabat (Kabat, E.A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health и Human Services, NIH Publication No. 91-3242).
Поскольку каждое из этих антител может связываться с CD30, и антиген-связывающая специфичность обеспечивается, в основном, областями CDR1, 2 и 3, цепи VH последовательностей CDR1, 2 и 3 и цепи Vk последовательностей CDR1, 2 и 3 можно смешивать и спаривать (то есть, можно смешивать и спаривать CDR различных антител, хотя каждое антитело должно содержать VH CDR1, 2 и 3 и Vk CDR1, 2 и 3) с получением других анти-CD30 связывающих молекул настоящего изобретения. Для проверки способности таких "перемешанных" антител связывать CD30 можно воспользоваться анализами для определения связывания, хорошо известными в данной области, такими как анализы FACS и ELISA. Предпочтительно, в случае смешивания последовательностей VH CDR, последовательности CDR1, CDR2 и/или CDR3 конкретной последовательности VH замещают на структурно похожие последовательности CDR. Аналогично этому, в случае смешивания последовательностей Vk CDR, последовательности CDR1, CDR2 и/или CDR3 конкретной последовательности Vk замещают на структурно похожие последовательности CDR. Специалисту в данной области понятно, что для создания новых последовательностей VH и VL одну или несколько последовательностей CDR областей VH и/или VL можно заменить на структурно похожие последовательности CDR, описанные здесь для моноклональных антител 5F11, 17G1 и 2Н9.
В соответствии с другим аспектом, настоящее изобретение направлено на дефукозилированные моноклональные антитела или их антиген-связывающие фрагменты, содержащие:
(a) вариабельную область тяжелой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:7, 8 и 9;
(b) вариабельную область тяжелой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:10, 11 и 12;
(c) вариабельную область тяжелой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:13, 14 и 15;
(d) вариабельную область легкой цепи CDR1, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:16, 17 и 18;
(e) вариабельную область легкой цепи CDR2, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:19, 20 и 21; и
(f) вариабельную область легкой цепи CDR3, содержащую аминокислотную последовательность, выбранную из группы, включающей SEQ ID NO:22, 23 и 24;
Где антитело специфически связывается с CD30. В соответствии с предпочтительным аспектом, антитела содержат:
(a) вариабельную область тяжелой цепи CDR1, содержащую SEQ ID NO:7;
(b) вариабельную область тяжелой цепи CDR2, содержащую SEQ ID NO:10;
(c) вариабельную область тяжелой цепи CDR3, содержащую SEQ ID NO:13;
(d) вариабельную область легкой цепи CDR1, содержащую SEQ ID NO:16;
(e) вариабельную область легкой цепи CDR2, содержащую SEQ ID NO:19; и
(f) вариабельную область легкой цепи CDR3, содержащую SEQ ID NO:22.
В соответствии с еще одним предпочтительным аспектом, антитела содержат:
(a) вариабельную область тяжелой цепи CDR1, содержащую SEQ ID NO:8;
(b) вариабельную область тяжелой цепи CDR2, содержащую SEQ ID NO:11;
(c) вариабельную область тяжелой цепи CDR3, содержащую SEQ ID NO:14;
(d) вариабельную область легкой цепи CDR1, содержащую SEQ ID NO:17;
(e) вариабельную область легкой цепи CDR2, содержащую SEQ ID NO:20; и
(f) вариабельную область легкой цепи CDR3, содержащую SEQ ID NO:23.
В соответствии с еще одним предпочтительным аспектом, антитела содержат:
(a) вариабельную область тяжелой цепи CDR1, содержащую SEQ ID NO:9;
(b) вариабельную область тяжелой цепи CDR2, содержащую SEQ ID NO:12;
(c) вариабельную область тяжелой цепи CDR3, содержащую SEQ ID NO:15;
(d) вариабельную область легкой цепи CDR1, содержащую SEQ ID NO:18;
(e) вариабельную область легкой цепи CDR2, содержащую SEQ ID NO:21; и
(f) вариабельную область легкой цепи CDR3, содержащую SEQ ID NO:24.
Антитела с конкретными последовательностями зародышевых линий
В соответствии с некоторыми аспектами, дефукозилированные антитела настоящего изобретения содержат вариабельную область тяжелой цепи из гена тяжелой цепи иммуноглобулина конкретной зародышевой линии и/или вариабельную область легкой цепи из гена легкой цепи иммуноглобулина конкретной зародышевой линии.
Например, в соответствии с предпочтительным аспектом, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающие фрагменты, содержащие вариабельную область тяжелой цепи, который представляет собой продукт или производное гена VH 4-34 человека, причем антитело специфически связывается с CD30 человека. В соответствии с другим предпочтительным аспектом, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающие фрагменты, содержащие вариабельную область тяжелой цепи, который представляет собой продукт или производное гена VH 4-07 человека, причем антитело специфически связывается с CD30 человека. В соответствии с еще одним предпочтительным аспектом, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающиефрагменты, содержащие вариабельную область легкой цепи, который представляет собой продукт или производное гена Vk L15 человека, причем антитело специфически связывается с CD30 человека. В соответствии с еще одним предпочтительным аспектом, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающие фрагменты, содержащие вариабельную областьлегкой цепи, который представляет собой продукт или производное гена Vk A27 человека, причем антитело специфически связывается с CD30 человека. В соответствии с еще одним предпочтительным аспектом, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающие фрагменты, содержащие вариабельную область легкой цепи, который представляет собой продукт или производное гена Vk L6 человека, причем антитело специфически связывается с CD30 человека.
В соответствии с еще одним предпочтительным аспектом, настоящее изобретение направлено на дефукозилированные моноклональные антитела или их антиген-связывающие фрагменты, причем антитело:
(a) содержит вариабельную область тяжелой цепи, представляющую собой продукт или производное генов VH 4-34 или 3-07 человека (которые кодируют аминокислотные последовательности SEQ ID NOs:25 и 26, соответственно);
(b) содержит вариабельную область легкой цепи, представляющую собой продукт или производное генов Vk L15, А27 или L6 человека (которые кодируют аминокислотные последовательности SEQ ID NOs:27, 28 и 29, соответственно); и
(c) специфически связывается с CD30 человека.
Предпочтительная комбинация клеток зародышевых линих VH и Vk представляет собой VH 4-34 и Vk L15. Примером антитела, VH и Vk которых представляют собой VH 4-34 и Vk L15, соответственно, является антитело 5F11. Еще одной предпочтительной комбинацией VH и Vk является VH 3-07 и Vk A27. Примером антитела с VH и Vk, представляющими собой VH 3-07 и Vk A27, соответственно, является 17G1. Еще одной предпочтительной комбинацией VH и Vk является VH 4-34 и Vk L6. Примером антитела с VH и Vk, представляющими собой VH 4-34 и Vk L6, соответственно, является 2Н9.
В настоящей заявке антитело человека содержит вариабельные области тяжелой и легкой цепей, которые представляют собой продукт или производное конкретной зародышевой последовательности, если вариабельные области антитела получаются из системы, в которой используются зародышевые гены иммуноглобулина человека. Такие системы включают трансгенную мышь с генами иммуноглобулина человека, иммунизированную интересующим антигеном, или скрининг библиотеки генов иммуноглобулина человека на фаге с интересующим антигеном. Человеческое антитело, представляющее собой "продукт" или "производное" зародышевой последовательности иммуноглобулина человека, можно идентифицировать, сравнивая аминокислотные последовательности антитела человека с аминокислотными последовательностями зародышевых иммуноглобулинов человека (например, с помощью базы данных Vbase) и выбирая такие зародышевые последовательности иммуноглобулинов человека, которые ближе всего к последовательности антитела человека (то есть, у них наибольший процент идентичности). Антитело человека, представляющее собой "продукт" или "производное" конкретной зародышевой последовательности иммуноглобулина человека, может содержать аминокислотные отличия от этой зародышевой последовательности, вызванные, например, происходящими в природе соматическими мутациями или сайт-направленным мутагенезом. Однако, как правило, аминокислотная последовательность антитела человека по меньшей мере на 90% идентична последовательности, кодируемой зародышевым геном иммуноглобулина человека, и содержит аминокислотные остатки, идентифицирующее ее именно как антитело человека, по сравнению с аминокислотными последовательностями зародышевых иммуноглобулинов других видов (например, мышиными). Иногда аминокислотная последовательность антитела человека может быть, по меньшей мере, на 95%, или даже, по меньше мере, на 96%, 97%, 98% или 99% идентична последовательности, кодируемой зародышевым геном иммуноглобулина человека. Как правило, человеческое антитело, производное от конкретной зародышевой последовательности человека, демонстрирует не больше 10 аминокислотных отличий от аминокислотной последовательности, кодируемой человеческим зародышевым геном иммуноглобулина. В некоторых случаях, антитело человека может демонстрировать не больше 5, или даже не больше 4, 3, 2 или 1 аминокислотного отличия от аминокислотной последовательности, кодируемой геном иммуноглобулина человека.
Гомологичные антитела
В соответствии с еще одним аспектом, дефукозилированные антитела настоящего изобретения содержат вариабельные области тяжелых и легкий цепей, аминокислотные последовательности которых гомологичны аминокислотным последовательностям предпочтительных описанных здесь антител, причем эти антитела сохраняют желательные функциональные свойства анти-CD30 антител настоящего изобретения.
Например, изобретение направлено на дефукозилированные моноклональные антитела или на их антиген-связывающие фрагменты, содержащие вариабельную область тяжелой цепи и вариабельную область легкой цепи, где:
(a) вариабельная область тяжелой цепи содержит аминокислотную последовательность, по меньшей мере, на 80% гомологичную аминокислотной последовательности, выбранной из группы, содержащей SEQ ID NO:1, 2, и 3;
(b) вариабельная область легкой цепи содержит аминокислотную последовательность, по меньшей мере, на 80% гомологичную аминокислотной последовательности, выбранной из группы, содержащей SEQ ID NO:4, 5, и 6; и
(c) антитела специфически связываютс с CD30 человека.
В соответствии с другими аспектами, аминокислотные последовательности VH и/или VL могут быть на 85%, 90%, 95%, 96%, 97%, 98% или 99% гомологичны последовательностям, описанным выше. Антитела, VH и VL области которых характеризуются высокой (то есть, 80% или больше) гомологией с VH и VL областями описанных выше последовательностей, можно получить мутагенезом (то есть, сайт-направленным или PCR- мутагенезом) одной или нескольких молекул нуклеиновых кислот, кодирующих SEQ ID NOs:1-6, с последующей проверкой наличия у кодируемых такой измененной последовательностью антител требуемой функции (то есть, связывания с CD30) с помощью описанных выше анализов. Молекулы нуклеиновых кислот, кодирующие последовательности SEQ ID NOs:1-6, представлены как SEQ ID NOs:30-35.
В настоящей заявке процент гомологии между двумя аминокислотными последовательностями эквивалентен проценту идентичности между ними. Процент идентичности между двумя последовательностями представляет собой функцию от количества идентичных позиций последовательностей (то есть, % гомологии=(число идентичных позиций)/(общее число позиций)×100). При этом необходимо учитывать количество и длину пробелов (gaps), которые требуется ввести для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между ними можно осуществить с помощью математического алгоритма, как описано в приводимых ниже неограничивающих примерах.
Процент идентичности между двумя нуклеотидными последовательностями можно определить с помощью программы GAP программного пакета GCG (доступного на сайте http://www.gcg.com). При этом матрица NWSgapdna. CMP и значение параметра gap weight составляют 40, 50, 60, 70 или 80, а значение параметра length weight составляет 1, 2, 3, 4, 5 или 6. Процент идентичности между двумя нуклеотидными или аминокислотными последовательностями можно определить также с помощью алгоритма, разработанного Е. Meyers и W. Miller (Comput. Appl. Biosci., 4:11-17 (1988)) и включенного в программу ALIGN (версия 2.0). При этом необходимо использовать таблицу весовых остатков РАМ 120, значение параметра дар length penalty равно 12, а значение gap penalty равно 4. Кроме того, процент идентичности между двумя аминокислотными последовательностями можно определить по алгоритму Needleman и Wunsch (J. Mol. Biol. 48:444-453 (1970)), входящего в состав программы GAP программного пакета GCG (доступного на сайте http://www.gcg.com). При этом необходимо использовать либо матрицу Blossum 62, либо матрицу РАМ250, значения параметра gap weight составляют 16, 14, 12, 10, 8, 6 или 4, а значение параметра length weight составляет 1, 2, 3, 4, 5 или 6.
Процент идентичности между двумя аминокислотными последовательностями можно определить по алгоритму Е. Meyers и W. Miller (Comput. Appl. Biosci., 4:11-17 (1988)) и включенного в программу ALIGN (версия 2.0). При этом необходимо использовать таблицу весовых остатков РАМ 120, значение параметра gap length penalty равно 12, а значение gap penalty равно 4. Кроме того, процент идентичности между двумя аминокислотными последовательностями можно определить по алгоритму Needleman и Wunsch (J. Mol. Biol. 48:444-453 (1970)), входящего в состав программы GAP программного пакета GCG (доступного на сайте http://www.gcg.com). При этом необходимо использовать либо матрицу Blossum 62, либо матрицу РАМ250, значения параметра масса пробела (gap weight) составляют 16, 14, 12, 10, 8, 6 или 4, а значение параметра длина пробела (length weight) составляет 1, 2, 3, 4, 5 или 6.
В дополнение или альтернативно, белковые последовательности настоящего изобретения можно использовать также как последовательности запроса для выполнения поиска в публичных базах данных, чтобы, например, обнаружить там родственные последовательности. Такой поиск можно выполнить с помощью программы XBLAST (версия 2.0) автора Altschul, et al. (1990) J. Mol. Biol. 215:403-10. Для поиска протеинов BLAST программой XBLAST необходимо задать значения score=50, wordlength=3. Так можно получить аминокислотные последовательности, гомологичные молекулам антител настоящего изобретения. Чтобы выполнить выравнивание с учетом пробелов (gapped alignments) для сравнения, можно воспользоваться программой Gapped BLAST, как описано в работе Altschul et al., (1997) Nucleic Acids Res. 25(17):3389-3402. При работе с модулями BLAST и Gapped BLAST можно воспользоваться значениями параметров соответствующих программ (например, параметров программ XBLAST и NBLAST), предлагаемыми по умолчанию. Более подробная информация содержится на сайте http://www.ncbi.nlm.nih.gov.
Антитела с консервативными модификациями
В соответствии с некоторыми аспектами, дефукозилированные антитела настоящего изобретения содержат вариабельную область тяжелой цепи, содержащий последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащий последовательности CDR1, CDR2 и CDR3, где одна или более этих CDR последовательностей содержат указанные аминокислотные остатки, основанные на описанных здесь предпочтительных антителах (например, на 5F11, 17G1, и 2Н9), или их консервативные модификации, и где антитела сохраняют требуемые функциональные свойства анти-CD30 антител изобретения. Соответственно, изобретение направлено на дефукозилированные моноклональные антитела или их антиген-связывающие фрагменты, содержащие вариабельную область тяжелой цепи, содержащий последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащий последовательности CDR1, CDR2 и CDR3, где:
(a) последовательность вариабельной области CDR3 тяжелой цепи содержит аминокислотные последовательности SEQ ID NO:9, 12 или 15, и их консервативные модификации;
(b) последовательность вариабельной области CDR3 легкой цепи содержит аминокислотные последовательности SEQ ID NO:18, 21 или 24, и их консервативные модификации; а также
(c) антитела специфически связываются с человеческим CD30.
В соответствии с предпочтительным аспектом, последовательность вариабельной области тяжелой цепи CDR2 содержит аминокислотную последовательность SEQ ID NO:8, 11 или 14 и ее консервативные модификации; а последовательность вариабельной области легкой цепи CDR2 содержит аминокислотную последовательность SEQ ID NO:17, 20 или 23 и ее консервативные модификации. В соответствии с другим предпочтительным аспектом, последовательность вариабельной области тяжелой цепи CDR1 содержит аминокислотную последовательность SEQ ID NO:7, 10 или 13 и ее консервативные модификации; а последовательность вариабельной области легкой цепи CDR1 содержит аминокислотную последовательность SEQ ID NO:16, 19 или 22 и ее консервативные модификации.
В настоящей заявке термин "консервативная модификация последовательности" означает аминокислотные модификации, которые всего лишь незначительно влияют на (изменяют) характеристики связывания содержащего аминокислотную последовательность антитела. Такие аминокислотные модификации включают аминокислотные замены, включения или делеции. Модификации антител настоящего изобретения можно осуществлять стандартными известными методами, такими как сайт-направленный мутагенез или PCR-опосредованный мутагенез. При консервативных аминокислотных заменах аминокислотные остатки заменяют на другие аминокислотные остатки с такими же боковыми цепями. Семейства аминокислотных остатков с одинаковыми боковыми цепями описаны в соответствующей литературе. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), с кислыми боковыми цепями (например, аспарагиновая или глутаминовая кислоты), с незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), с неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), с бета-ветвящимися боковыми цепями (например, треонин, валин, изолейцин) и с ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Так, один или больше аминокислотных остатков CDR областей антител настоящего изобретения можно заменить на другие аминокислотные остатки из того же семейства боковых цепей, после чего измененные антитела проверяют на сохранение у них функции (то есть, функций, описанных в пунктах (i)-(iv) выше) с помощью описанных здесь функциональных анализов.
Альтернативно, в соответствии с другим аспектом изобретения, мутации можно вводить случайным образом по всей кодирующей последовательности анти-CD30 антитела или в ее части, как это происходит при насыщающем мутагенезе, и полученные в результате модифицированные анти-CD30 антитела также затем скринируют на связывание.
Антитела, связывающиеся с тем же эпитопом, что и анти-CD30 антитела настоящего изобретения
В соответствии с другим своим аспектом, настоящее изобретение направлено на дефукозилированные антитела, связывающиеся с тем же эпитопом, что и различные описанные здесь анти-CD30 антитела настоящего изобретения; это могут быть другие антитела человека, связывающиеся с тем же эпитопом, что и описанные здесь антитела 5F11, 17G1 или 2Н9. Такие дополнительные антитела можно идентифицировать по их способности к перекрестной конкуренции (например, к статистически значимому конкурентному ингибированию связывания) с другими антителами настоящего изобретения, такими как 5F11, 17G1 или 2Н9, что определяется стандартными методами определения связывания с CD30. Способность исследуемого антитела ингибировать связывание, например, 5F11, 17G1 или 2Н9 с CD30 человека показывает, что оно может конкурировать с этими антителами за связывание с CD30; в соответствии с неограничивающей настоящее изобретение теорией такое антитело может связываться с тем же или родственным эпитопом (например, структурно или пространственно похожим) CD30 человека, что и антитело, с которым оно конкурирует. В соответствии с предпочтительным аспектом, антитело, связывающееся с таким же эпитопом CD30 человека, что и антитела 5F11, 17G1 или 2Н9, представляет собой моноклональное антитело человека. Методы получения и выделения таких моноклональных антител описаны в публикации РСТ Publication WO 03/059282.
Сконструированные и модифицированные антитела
Дефукозилированные антитела настоящего изобретения могут также быть приготовлены из антител с одной или более описанными здесь последовательностями VH и/или VL как исходный материал, из которого конструируют модифицированное антитело, причем свойства последнего могут отличаться от свойств исходного антитела. Антитело может быть сконструировано путем модификации одного или нескольких аминокислотных остатков одной или нескольких вариабельных областей (то есть, VH и/или VL), например, внутри одной или нескольких областей CDR или одной или нескольких каркасных областей. Дополнительно или альтернативно, антитело может быть сконструировано путем модификации остатков постоянных областей, например, чтобы изменить эффекторные функции антитела.
Одним возможным типом конструирования вариабельной является трансплантация (grafting) CDR. Антитела взаимодействуют с антигенами мишени, предпочтительно, с помощью аминокислотных остатков, расположенных в шести тяжелых и легких цепей областях, определяющих комплементарность (CDR). По этой причине входящие в CDR аминокислотные последовательности различных антител более разнообразны, по сравнению с областями за пределами CDR. Так как CDR последовательности отвечают за большую часть взаимодействий антиген-антитело, для экспрессии рекомбинантного антитела, имитирующего свойства конкретного природного антитела, можно сконструировать векторы экспрессии, включающие CDR последовательности конкретного природного антитела, которые перенесли (пересадили) в каркасные последовательности другого антитела с другими свойствами (см., например, Riechmann, L et al. (1998) Nature 332:323-327; Jones, P. et al. (1986) Nature 321:522-525; Queen, C. et al. (1989) Proc. Natl. Acad. See. U.S.A. 86:10029-10033; U.S. Patent No. 5,225,539 to Winter, и U.S. Patent Nos. 5,530,101; 5,585,089; 5,693,762 и 6,180,370 to Queen et al.).
Соответственно, еще один аспект настоящего изобретения направлен на дефукозилированные моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельные области тяжелой цепи, содержащие последовательности CDR1, CDR2 и CDR3, аминокислотные последовательности которых выбраны из группы SEQ ID NOs:7, 8 и 9, SEQ ID NOs:10, 11 и 12 и SEQ ID NOs:13, 14 и 15, соответственно, и вариабельные области легкой цепи, содержащие аминокислотные последовательности, выбранные из группы SEQ ID NOs:16, 17 и 18, SEQ ID NOs:19, 20 и 21 и SEQ ID NOs:22, 23 и 24, соответственно. Такое антитело содержит VH и VL CDR последовательности моноклональных антител 5F11, 17G1 или 2Н9, но может также содержать каркасные последовательности и других антител.
Такую каркасную последовательность можно получить из публичных баз данных ДНК или из литературных источников, содержащих зародышевые последовательности генов антител. Например, зародышевые последовательности ДНК генов вариабельных областей тяжелых и легких цепей человека можно найти в базе данных зародышевых последовательностей человека "VBase" (доступной на сайте Интернет по адресу www.mrc-cpe.cam.ac.uk/vbase), или в работах Kabat, E.A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health и Human Services, NIH Publication No. 91-3242; Tomlinson, I. M., et al. (1992) "The Repertoire of Human Germline VH Sequences Reveals about Fifty Groups of VH Segments with Different Hypervariable Loops" J. Mol. Biol. 227:776-798; и Сох, J. P. L et al. (1994) "A Directory of Human Germ-line VH Segments Reveals a Strong Bias in their Usage" Eur. J. Immunol. 24:827-836. Содержание всех этих работ явным образом включено сюда по ссылке.
Предпочтительные каркасные последовательности для использования с антителами настоящего изобретения структурно похожи на каркасные последовательности избранных антител настоящего изобретения, например, похожи на последовательности настоящего изобретения VH 4-34 или 3-07 (SEQ ID NO:25 или 26) и/или Vk L15, A27 или на каркасную последовательность L6 (SEQ ID NO:27, 28, или 29). Это последовательности предпочтительных моноклональных антител изобретения. Последовательности VH CDR1, 2 и 3 и последовательности Vk CDR1, 2 и 3 можно перенести в каркасные области, последовательности которых идентичны тем, что представлены в зародышевых генах иммуноглобулина, от которых происходит данная каркасная последовательность, или же CDR последовательности можно перенести в каркасные области, содержащие одну или несколько мутаций, по сравнению с зародышевыми последовательностями. Например, показано, что иногда бывает полезно внести мутации в остатки в каркасных областях, чтобы сохранить или усилить антиген-связывающую способность антитела (см., например U.S. Patent Nos. 5,530,101; 5,585,089; 5,693,762 и 6,180,370 авторов Queen et al).
Еще один тип модификации вариабельной области связан с внесением мутаций в аминокислотные остатки областей VH и/или Vk CDR1, CDR2 и/или CDR3 с тем, чтобы улучшить связывающие свойства (то есть, сродство) интересующих антител. Для осуществления мутаций можно использовать сайт-направленный или PCR-опосредованный мутагенез, а эффект мутаций на связывание антител или другие интересующие функциональные свойства можно проверить различными методами анализа in vitro или in vivo, описанными здесь и приведенными в разделе примеров. Предпочтительно осуществлять консервативные модификации (как описано выше). Мутации могут представлять собой замены, вставки и делеции аминокислот, но предпочтительными мутациями являются замены. Более того, как правило, в области CDR изменяют не более чем один, два, три, четыре или пять остатков.
Таким образом, в соответствии с другим аспектом, настоящее изобретение направлено надефукозилированные анти-CD30 моноклональные антитела или их антиген-связывающие фрагменты, вариабельную область тяжелой цепи которая содержит: (а) VH CDR1 область, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:7, 8 и 9, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делециями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:7, 8 и 9; (b) VH CDR2 область, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:10, 11 и 12, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делециями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:10, 11 и 12; (с) VH CDR3 область, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:13, 14 и 15, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делениями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:13, 14 и 15; (d) Vk CDR1 область, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:16, 17 и 18, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делециями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:16, 17 и 18; (e) Vk CDR2 область, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:19, 20 и 21, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делециями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:19, 20 и 21; и (f) Vk CDR3 область, содержащий аминокислотную последовательность, выбранную из группы, состоящую из SEQ ID NO:22, 23 и 24, или аминокислотную последовательность с одной, двумя, тремя, четырьмя или пятью аминокислотными заменами, делециями или вставками, по сравнению с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:22, 23 и 24.
К числу сконструированных антител настоящего изобретения относятся и такие, модификации у которых были сделаны в аминокислотных остатках каркаса внутри последовательностей VH и/или Vk, например, чтобы улучшить свойства антител. Как правило, такие модификации каркаса делают, чтобы снизить иммуногенность антитела. Например, одним подходом является "обратная мутация" одного или нескольких остатков каркаса для приведение в соответствие с зародышевой последовательностью. Конкретно, подвергавшееся соматической мутации антитело может содержать аминокислотные остатки каркаса, отличающиеся от зародышевой последовательности, из которой оно было получено. Такие остатки идентифицируют, сравнивая каркасную последовательность антитела с зародышевой последовательностью, из которой оно было получено. Например, в случае 5F11, аминокислотный остаток #83 (внутри FR3) последовательности VH представляет собой аспарагин, в то время как остаток соответствующей зародышевой последовательности VH 4-34 - серин. Чтобы вернуть последовательность каркаса в "зародышевую" конфигурацию, можно "обратно мутировать" соматическую мутацию к зародышевому виду, например, с помощью сайт-направленного или PCR-опосредованного мутагенеза (например, остаток 83 последовательности FR3 область VH антитела 5F11 можно "обратно мутировать" из аспарагина в серин). Такие "обратно мутированные" антитела также входят в область действия настоящего изобретения.
Еще один тип каркасной модификации включает мутирование одного или нескольких остатков каркасного область или даже одного или нескольких областей CDR, чтобы удалить эпитопы Т-клеток и, тем самым, снизить потенциальную иммуногенность антитела. Этот подход называется "деиммунизация" и подробно был описан в Carr et al. U.S. Patent Publication No. 20030153043.
В дополнение или альтернативно модификациям в каркасных областях или областях CDR, при конструировании антител настоящего изобретения модификации можно включать в область Fc. Как правило, это делается, чтобы изменить одно или несколько свойств антитела, такие как период полужизни в сыворотке, фиксация комплемента, связывание Fc рецептора и/или антиген-зависимая клеточная цитотоксичность. Кроме того, антитела настоящего изобретения можно модифицировать химически (например, к ним можно прикрепить одну или несколько химических групп). Это делается, чтобы изменить состояние их гликозилирования или также для изменения одного или нескольких их функциональных свойств. Каждое указанное антитело подробно описано далее. Нумерация остатков области Fc соответствует EU индексу Кабата (Kabat).
В соответствии с одним аспектом изобретения, область шарнира СН1 модифицируют так, чтобы изменить там количество остатков цистеина (например, увеличить его или уменьшить). Этот подход подробно описан в работе Bodmer et al, U.S. Patent No. 5,677,425. Число остатков цистеина в области шарнира СН1 изменяют, например, чтобы облегчить сборку легких и тяжелых цепей, или чтобы увеличить или уменьшить стабильность антитела.
В соответствии с другим аспектом, область шарнира Fc антитела мутируют так, чтобы уменьшить время биологического полураспада (полужизни) антитела. Конкретно, одну или несколько аминокислотных мутаций вводят в область интерфейса домена СН2-СН3 фрагмента Fc, так чтобы антитело хуже связывалось с протеином А стафилококка (SpA), по сравнению со связыванием нативного домена Fc-шарнира. Этот подход подробно описан в работе Ward et al. U.S. Patent No. 6,165,745.
В соответствии с другим аспектом изобретения, антитело модифицируют, чтобы увеличить время его биологической жизни. Возможны различные подходы. Например, можно ввести одну или несколько мутаций T252L, T254S, T256F, как описано в патенте U.S. No. 6,277,375 автором Ward. Альтернативно, чтобы увеличить время биологической жизни, можно внести изменения в областях антитела СН1 или CL, включив в него эпитоп, связывающий стабилизирующий рецептор и взятый из двух петель домена СН2 Fc-область IgG, как описано в патентах U.S. Nos. 5,869,046 и 6,121,022, чье авторство принадлежит Presta et al.
В соответствии с другими аспектами, область Fc изменяют, замещая один или несколько аминокислотных остатков на другие аминокислотные остатки, чтобы изменить эффекторную функцию (функции) антитела. Например, один или несколько аминокислотных остатков, выбранных из числа остатков 234, 235, 236, 237, 297, 318, 320 и 322, можно заменить на другие остатки, так чтобы антитело изменило сродство к эффекторному лиганду, но сохранило антиген-связывающую способность родительского антитела. Эффекторный лиганд, сродство к которому следует изменить, может, например, соответствовать Fc-рецептору или компоненту С1 комплемента. Этот подход подробно описан патентах U.S. Nos. 5,624,821 и 5,648,260, оба написаны Winter et al.
В соответствии с другим примером, один или несколько аминокислотных остатков, выбранных из числа 329, 331 и 322, можно заменить на другие остатки, так чтобы изменить у нового антитела связывание C1q и/или уменьшить или полностью устранить комплемент-зависимую цитотоксичность (CDC). Этот подход подробно описан в патенте U.S. №6,194,551 автора Idusogie et al.
В соответствии с еще одним примером, можно изменить один или несколько аминокислотных остатков в положениях 231 и 239, чтобы изменить способность антитела фиксировать комплемент. Этот подход более подробно описан Bodmer et al. в публикации РСТ Publication WO 94/2935.
В соответствии с еще одним примером, область Fc модифицируют, чтобы повысить способность антитела опосредовать зависящую от него клеточную цитотоксичность (ADCC) и/или чтобы повысить сродство антитела к рецептору Fcγ, модифицируя один или несколько аминокислотных остатков в положениях 238, 239, 248, 249, 252, 254, 255, 256, 258, 265, 267, 268, 269, 270, 272, 276, 278, 280, 283, 285, 286, 289, 290, 292, 293, 294, 295, 296, 298, 301, 303, 305, 307, 309, 312, 315, 320, 322, 324, 326, 327, 329, 330, 331, 333, 334, 335, 337, 338, 340, 360, 373, 376, 378, 382, 388, 389, 398, 414, 416, 419, 430, 434, 435, 437, 438 или 439. Этот подход подробно описан Presta в публикации РСТ Publication WO 00/42072. Более того, были картированы сайты связывания lgG1 человека с FcγRI, FcγRII, FcγRIII и FcRn, и были описаны варианты с улучшенным связыванием (см. Shields, R.L et al. (2001) J. Biol. Chem. 276:6591-6604). Показано, что специфические мутации в положениях 256, 290, 298, 333, 334 и 339 улучшают связывание с FcγRIII. Кроме того, связывание с FcγRIII улучшает следующая комбинация мутантов: T256A/S298A, S298A/E333A, S298A/K224A и S298A/E333A/K334A.
Еще одна модификация антител настоящего изобретения связана с явлением пегиляции. Антитело можно пегилировать, например, чтобы увеличить продолжительность ее биологической (например, в сыворотке) полужизни. Чтобы пегилировать антитело, проводят его (или его фрагмента) реакцию с полиэтилен гликолем (PEG), например, с его реактивным эфирным или альдегидным производным, в таких условиях, когда одна или несколько PEG групп связываются с антителом или его фрагментом. Предпочтительно, если пегиляция выполняется с помощью реакции ацилирования или алкилирования с реактивной молекулой PEG (или аналогичного реактивного водорастворимого полимера). В настоящей заявке термин "полиэтилен гликоль" охватывает все формы PEG, используемые для дериватизации других протеинов, такие как моно (С1-С10)алкокси- или арилокси-полиэтилен гликоль или полиэтилен гликоль-малеимид. В соответствии с некоторыми аспектами изобретения, антитело необходимо пегилировать в агликозилированное антитело. Методы пегилирования протеинов известны в соответствующей области и могут быть применены к антителам настоящего изобретения. См., например, написанный Nishimura et al. патент ЕР 0154316 и ЕР 0401384, написанный Ishikawa et al.
Методы конструирования антител
Как было описано выше, дефукозилированные анти-CD30 антитела настоящего изобретения, последовательности VH и Vk которых описаны в этом изобретении, можно использовать для создания новых анти-CD30 антител. Для этого модифицируют последовательности VH и/или Vk или связанные с ними постоянные области. Так, в соответствии с другим аспектом настоящего изобретения, структурные характеристики анти-CD30 антител изобретения, например, 5F11, 17G1 или 2Н9, позволяют создать структурно родственные анти-CD30 антитела, сохраняющие по меньшей мере одно функциональное свойство антител изобретения, такое как связывание с CD30 человека. Например, один или несколько CDR областей антител 5F11, 17G1 или 2Н9 или их мутаций можно рекомбинантно объединить с известными каркасными областями и/или другими CDR для создания новых рекомбинантно сконструированных анти-CD30 антител настоящего изобретения, как описано выше. Другой тип модификации включает описанные в предыдущем разделе. Исходным материалом для конструирования является одна или несколько описанных здесь последовательностей VH и/или Vk или один или несколько областей CDR. Для создания сконструированного антитела не обязательно фактически делать (то есть, экспрессировать в виде протеина) антитела с одной или несколькими описанными здесь VH и/или Vk последовательностями или одним или несколькими областями CDR. Достаточно только воспользоваться содержащейся в последовательностях информацией и создать на ее основе последовательности "второго поколения", а затем приготовить эти последовательности и экспрессировать их как протеин.
Таким образом, в соответствии с другим своим аспектом, изобретение направлено на метод получения анти-CD30 антител, включающий:
(a) получение: (i) последовательности вариабельной области тяжелой цепи антитела, содержащей последовательность CDR1, выбранную из группы SEQ ID NOs:7, 8 и 9, последовательность CDR2, выбранную из группы SEQ ID NOs:10, 11 и 12, и/или последовательность CDR3, выбранную из группы SEQ ID NOs:13, 14 и 15; и/или (ii) последовательности вариабельной области легкой цепи антитела, содержащей последовательность CDR1, выбранную из группы SEQ ID NOs:16, 17 и 18, последовательность CDR2, выбранную из группы SEQ ID NOs:19, 20 и 21, и/или последовательность CDR3, выбранную из группы SEQ ID NOs:22, 23 и 24; и/или
(b) изменение по меньшей мере одного аминокислотного остатка последовательности вариабельной области тяжелой цепи антитела и/или последовательности вариабельной области легкой цепи антитела для создания по меньшей мере одной измененной последовательности антитела; и
(c) экспрессия измененной последовательности антитела в виде протеина.
Получить и экспрессировать измененные последовательности антитела позволяют стандартные методы, известные в молекулярной биологии. Приготовленное таким способом измененное антитело можно дефукозилировать описанными здесь методами, получив дефукозилированное измененное анти-CD30 антитело.
Функциональные свойства измененных антител проверяют стандартными методами анализа, известными в соответствующей области и/или описанными здесь, такими как те, что излагаются в разделе Примеров (например, цитометрия в потоке, анализы связывания, анализ ADCC).
В соответствии с определенными аспектами методов конструирования антител настоящего изобретения, мутации можно вводить случайным образом или селективно во всей кодирующей последовательности анти-CD30 антитела или в ее части, а полученные модифицированные анти-CD30 антитела можно скринировать на способность к связыванию и/или другие описанные здесь функциональные свойства. Методы создания мутаций описаны в литературе. Например, в публикации РСТ WO 02/092780 автор Short описывает методы создания и скринирования мутаций антител с помощью насыщающего мутагенеза, монтажа синтетических сшивок или их комбинации. Кроме того, в публикации РСТ WO 03/074679 ее авторы Lazar et al. описывают использование методов компьютерного скрининга для оптимизации физико-химических свойств антител.
Молекулы нуклеиновых кислот, кодирующие антитела настоящего изобретения
Еще один аспект настоящего изобретения - молекулы нуклеиновых кислот, кодирующие антитела настоящего изобретения. Термин "молекула нуклеиновой кислоты" здесь означает молекулу РНК или ДНК. Молекулы нуклеиновых кислот могут быть двухцепочечными или одноцепочечными, но предпочтительно, чтобы это была двухцепочечная ДНК. Нуклеиновые кислоты могут содержаться в целых клетках, в клеточных лизатах, в частично очищенном или практически чистом виде. Нуклеиновая кислота называется "выделенной" или "практически чистой", если очищена от других клеточных компонентов или других загрязнителей, например, от других нуклеиновых кислот или протеинов, стандартными методами, включая обработку щелочью/SDS, расслоение с помощью CsCl, хроматографию на колонке, электрофорез в агарозном геле и другие методы, хорошо известные в данной области. См. F. Ausubel, et al., ed. (1987) Current Protocols in Molecular Biology, Greene Publishing и Wiley Interscience, New York. Нуклеиновая кислота настоящего изобретения может представлять собой, например, ДНК или РНК, и может содержать или не содержать интронные последовательности. В соответствии с предпочтительным аспектом, нуклеиновая кислота представляет собой молекулу кДНК.
Нуклеиновые кислоты настоящего изобретения можно получить стандартными методами молекулярной биологии. Если антитела экспрессируются в гибридомах (например, в гибридомах, полученных у трансгенной мыши с генами иммуноглобулина человека, подробно описанной ниже), то получаемые в гибридомах кДНК, кодирующие легкие и тяжелые цепи антитела, можно выделить стандартными методами ПЦР-амплификации или кДНК-клонирования. Если антитела получают из библиотеки генов иммуноглобулина (например, методами дисплея в фагах), кодирующие антитела нуклеиновые кислоты можно выделить из библиотеки.
Предпочтительные молекулы нуклеиновых кислот настоящего изобретения кодируют последовательности VH и VL моноклональных антител 5F11, 17G1 и 2Н9. Последовательность ДНК, кодирующая VH последовательность 5F11, показана как SEQ ID NO:30. Последовательность ДНК, кодирующая VL последовательность 5F11, показана как SEQ ID NO:33. Последовательность ДНК, кодирующая VH последовательность 17G1, показана как SEQ ID NO:31. Последовательность ДНК, кодирующая VL последовательность 17G1, показана как SEQ ID NO:34. Последовательность ДНК, кодирующая VH последовательность 2Н9, показана как SEQ ID NO:32. Последовательность ДНК, кодирующая VL последовательность 2Н9, показана как SEQ ID NO:35.
После получения фрагментов ДНК, кодирующих VH и VL, с этими фрагментами можно работать стандартными рекомбинантными методами работы с ДНК. Например, можно конвертировать гены вариабельной области в гены цепи антитела полной длины, в гены фрагмента Fab или в ген scFv. В соответствии с этими методами, VH или VL-кодирующий фрагмент ДНК оперативно связывают с другим фрагментом ДНК, кодирующим другой протеин, например, постоянную область антитела или гибкий линкер. Термин "оперативно связывают" в контексте настоящего изобретения означает, что два фрагмента ДНК объединяют так, чтобы кодируемые ими аминокислотные последовательности оставались внутри рамки.
Выделенную ДНК, кодирующую VH область, можно конвертировать в ген тяжелой цепи полной длины, оперативно связав VH-кодирующую последовательность ДНК с другой молекулой ДНК, кодирующей постоянные области тяжелой цепи (СН1, СН2 и СН3). Последовательности генов постоянных областей тяжелых цепей человека известны в литературе (см., например, Kabat, E.A., el al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health и Human Services, NIH Publication No.91-3242), и содержащие эти области фрагменты ДНК можно получить методом стандартной PCR-амплификации. Постоянная область тяжелой цепи может представлять собой постоянную область IgG1, IgG2, IgG3, IgG4, IgA, IgE, IgM или IgD, но наиболее предпочтительно, если это постоянная область IgG1 или IgG4. В случае гена тяжелой цепи фрагмента Fab, VH-кодирующую ДН К можно оперативно связать с другой молекулой ДНК, кодирующей только постоянную область тяжелой цепи СН1.
Выделенную молекулу ДНК, кодирующую VL область, можно конвертировать в ген легкой цепи полной длины (или в ген Fab легкой цепи), оперативно связав VL-кодирующую последовательность ДНК с другой молекулой ДНК, кодирующей постоянную область легкой цепи, CL. Последовательности генов постоянных областей легких цепей человека известны в литературе (см., например, Kabat, E.A., el al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health и Human Services, NIH Publication No. 91-3242), и содержащие эти области фрагменты ДНК можно получить методом стандартной PCR-амплификации. Постоянная область легкой цепи может представлять собой постоянную область каппа или лямбда, но наиболее предпочтительно, если это постоянная область каппа.
Для создания гена scFv VH- и VL-кодирующие фрагменты ДНК оперативно связывают с другим фрагментом, кодирующим гибкий линкер, например, аминокислотную последовательность (Gly4-Ser)3, так что VH и VL последовательности будут экспрессироваться в виде сплошного одноцепочечного протеина, VH и VL области которого будут соединены гибким линкером (см., например, Bird et al. (1988) Science 242:423-426; Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883; McCafferty et al., (1990) Nature 348:552-554).
Композиции нуклеиновых кислот настоящего изобретения часто бывают представлены в виде нативных последовательностей (за исключением модифицированных сайтов ограничения и тому подобное). Однако, геномные композиции, композиции, полученные из кДНК, и их смеси можно мутировать в соответствии со стандартными методами получения генных последовательностей. В случае кодирующих последовательностей эти мутации могут желательным образом влиять на последовательности аминокислот. В особенности, в область действия настоящего изобретения входят последовательности ДНК, в значительной степени гомологичные или производные от нативных V, D, J, константы, переключателей и других подобных последовательностей (слово "производные" означает, что последовательность идентична другой последовательности или представляет собой ее модификацию).
Получение моноклональных антител изобретения
Моноклональные антитела настоящего изобретения (mAbs) можно получить разнообразными методами, включая традиционные методы работы с моноклональными антителами, например, стандартный метод гибридизации соматических клеток, описанный в работе Kohler and Milstein (1975) Nature 256: 495. Хотя предпочтительными являются процедуры гибридизации соматических клеток, в принципе, можно использовать и другие методы получения моноклональных антител, например, вирусную или онкогенную трансформацию В-лимфоцитов.
Предпочтительной животной системой для получения гибридом является мышиная система. Получение гибридом в мышах представляет собой хорошо отработанную процедуру. В молекулярной биологии хорошо известны протоколы иммунизации и методы выделения иммунизированных спленоцитов для гибридизации. Описаны также партнеры гибридизации (например, клетки мышиной миеломы) и процедуры гибридизации.
В соответствии с различными аспектами, антитела могут быть, например, антителами мыши, гуманизированными антителами или химерными антителами.
Химерные или гуманизированные антитела настоящего изобретения можно получить на основании последовательности мышиного моноклонального антитела, приготовленного как описано выше. ДНК, кодирующие иммуноглобулины тяжелых и легких цепей, можно получить из интересующей гибридомы мыши и включить в них не мышиные (например, человеческие) последовательности иммуноглобулинов с помощью стандартных методов молекулярной биологии. Например, для создания химерного антитела вариабельные области мыши можно связать с постоянными областями человека с помощью хорошо известных методов (см., например, U.S. No. 4,816,567 автора Cabilly et al.). Для создания гуманизированного антитела можно мышиные области CDR включить в каркас человека с помощью хорошо известных методов (см., например, U.S. Patent No. 5,225,539 авторов Winter, и U.S. Patent Nos. 5,530,101; 5,585,089; 5,693,762 и 6,180,370 авторов Queen et al.). В литературе известно множество анти-CD30 антител мыши, с их помощью можно создавать химерные или гуманизированные анти-CD30 антитела, например, АС10, HeFi-1, Ber-H2, Ki-1, HRS-3, Irac, HRS-4, M44, М67 и Ber-H8.
В соответствии с предпочтительными аспектами, антитела настоящего изобретения представляют собой моноклональные антитела человека. Такие антитела, направленные против CD30, можно генерировать с помощью трансгенных или трансхромосомальных мышей, несущей части иммунной системы человека, а не мыши. Указанные трансгенные или трансхромосомальные мыши включают мышей, называемых здесь HuMAb и KМ, соответственно, их вместе называют в данной работе "мышами Ig человека".
Мышь HuMAb mouse® (Medarex, Inc.) содержит минилокус гена иммуноглобулина человека, который кодирует неперегруппированные последовательности тяжелых (µ и γ) и легких к цепей иммуноглобулина человека; совместно с направленными мутациями он инактивирует эндогенный локус цепей µ и κ (см. Lonberg, et al. (1994) Nature 368(6474): 856-859). Соответственно, мышь демонстрирует сниженную экспрессию IgM или к мыши, и, в ответ на иммунизацию, введенные трансгены тяжелых и легких цепей человека подвергаются переключению класса и соматической мутации с генерацией моноклонального IgGk человека высокого сродства (Lonberg, N. et al. (1994), supra; reviewed in Lonberg, N. (1994) Handbook of Experimental Pharmacology 113:49-101; Lonberg, N. и Huszar, D. (1995) Intern. Rev. Immunol. 13: 65-93, и Harding, F. and Lonberg, N. (1995) Ann. N.Y. Acad. Sci. 764:536-546). Получение и использование мыши HuMab, а также содержащиеся в ней геномные модификации подробнее описаны в работах Taylor, L et al. (1992) Nucleic Acids Research 20:6287-6295; Chen, J. et al. (1993) International Immunology 5: 647-656; Tuaillon et al. (1993) Proc. Natl. Acad. Sci. USA 90:3720-3724; Choi et al. (1993) Nature Genetics 4:117-123; Chen, J. et al. (1993) EMBO J. 12: 821-830; Tuaillon et al. (1994) J. Immunol. 152:2912-2920; Taylor, L et al. (1994) International Immunology 6: 579-591; и Fishwild, D. et al. (1996) Nature Biotechnology 14: 845-851, содержание всех указанных работ специально включено сюда по ссылке по всей своей полноте. См. также, U.S. Patent Nos. 5,545,806; 5,569,825; 5,625,126; 5,633,425; 5,789,650; 5,877,397; 5,661,016; 5,814,318; 5,874,299; и 5,770,429; все они написаны Lonberg и Kay; U.S. Patent No. 5,545,807 автора Surani et al.; PCT Publication Nos. WO 92/03918, WO 93/12227, WO 94/25585, WO 97/13852, WO 98/24884 и WO 99/45962, все написаны Lonberg и Kay; и PCT Publication No. WO 01/14424 автора Korman et al.
В соответствии с еще одним аспектом, антитела настоящего изобретения можно вырастить в мыши-носителе последовательностей иммуноглобулина человека на трансгенах и трансхромосомах, например, мышь может быть носителем трансгена тяжелой цепи человека и трансхромосомы легкой цепи человека. Такая мышь называется "мышь КМ", она подробно описана в публикации РСТ WO 02/43478 автора Ishida et al.
В литературе известны и альтернативные трансгенные системы животных, экспрессирующие гены иммуноглобулина человека и позволяющие вырастить анти-CD30 антитела настоящего изобретения. Например, одной альтернативной трансгенной системой является система ксеномышь 0 (Abgenix, Inc.); кроме того, такая мышь описана, например, в патентах U.S. No. 5,939,598; 6,075,181; 6,114,598; 6, 150,584 и 6,162,963 автора Kucherlapati et al.
Более того, в литературе известны и альтернативные трансхромосомальные системы животных, экспрессирующие гены иммуноглобулина человека и позволяющие вырастить анти-CD30 антитела настоящего изобретения. Например, для этой цели можно использовать мышь-носитель трансхромосомы тяжелой цепи человека и трансхромосомы легкой цепи человека, называемую также "мышь ТС", такая мышь описана в работе Tomizuka et al. (2000) Proc. Natl. Acad. Sci. USA 97:722-727. Описаны также коровы, являющиеся носителями трансхромосом тяжелой и легкой цепей человека (Kuroiwa et al. (2002) Nature Biotechnology 20:889-894), с их помощью также можно вырастить анти-CD30 антитела настоящего изобретения.
Человеческие моноклональные антитела настоящего изобретения можно приготовить также с помощью методов фагового дисплея, применяемых для скрининга библиотек генов иммуноглобулина человека. Применение таких методов фагового дисплея для выделения антител человека хорошо известно в молекулярной биологии. См., например, U.S. Patent Nos. 5,223,409; 5,403,484; и 5,571,698 Ladner et al.; U.S. Patent Nos. 5,427,908 и 5,580,717 Dower et al.; U.S. Patent Nos. 5,969,108 и 6,172,197 McCafferty et al.; и U.S. Patent Nos. 5,885,793; 6,521,404; 6,544,731; 6,555,313; 6,582,915 и 6,593,081 Griffiths et al.
Человеческие моноклональные антитела настоящего изобретения можно приготовить также с использованием мыши SCID, которой были привиты иммунные клетки человека, так что после иммунизации такой мыши можно генерировать ответ в виде антител человека. Подобная мышь описана, например, в работах U.S. Patent Nos. 5,476,996 и 5,698,767 Wilson et al.
Иммунизация мыши Ig человека
Если человеческие антитела настоящего изобретения выращивают в мыши Ig человека, то такую мышь можно иммунизировать очищенным или обогащенным препаратом антигена CD30 и/или рекомбинантным CD30, или слитым белком CD30, как описано в работах Lonberg, N. et al. (1994) Nature 368(6474): 856-859; Fishwild, D. et al. (1996) Nature Biotechnology 14: 845-851; и РСТ Publication WO 98/24884 и WO 01/14424. Предпочтительно, чтобы возраст мыши на момент первой инфузии составлял 6-16 недель. Например, для внутрибрюшинной иммунизации мыши Ig человека можно использовать очищенный или рекомбинантный препарат антигена CD30 (5-50 мкг).
Подробная процедура генерации полностью человеческих моноклональных антител к CD30 описана в публикации РСТ WO 03/059282. Обобщая имеющийся опыт работы с различными антигенами, можно сказать, что для реакции трансгенной мыши ее надо первоначально иммунизировать внутрибрюшинно (IP) антигеном в полном адьюванте Фрейнда, после чего каждую неделю (в течение вплоть до 6 недель) повторять иммунизации IP в неполном адьюванте Фрейнда. Однако, эффективными могут быть также и другие адьюванты, а не только Фрейнда. Кроме того, чрезвычайно иммуногенными оказались цельные клетки в отсутствие адьюванта. Для отслеживания иммунного ответа в ходе иммунизации образцы плазмы крови забирают с помощью ретроорбитальных кровопусканий. Плазму скринируют методом ELISA (как описано ниже), и мышь с достаточными титрами анти-CD30 иммуноглобулина человека может быть использована для дальнейшей работы. С этой целью мыши внутривенно вводят антиген в течение трех дней, после чего ее забивают и выделяют селезенку. Предполагается, что для каждой иммунизации необходимо выполнить две-три фузии. Обычно, каждым антигеном иммунизируют от 6 до 24 мышей. Как правило, при этом используют штаммы как НСо7, так и НСо12. Кроме того, оба трансгена НСо7 и НСо12 можно вырастить совместно в одной мыши с двумя различными трансгенами тяжелых цепей человека (НСо7/НСо12).
Генерация гибридом, продуцирующих человеческие моноклональные антитела настоящего изобретения
Для генерации гибридом, продуцирующих человеческие моноклональные антитела настоящего изобретения, спленоциты и/или клетки лимфоузлов иммунизированной мыши можно выделить и слить их с соответствующей иммортализованной клеточной линией, такой как клеточная линия миеломы мыши. Полученные гибридомы скринируют на генерацию антиген-специфических антител. Например, суспензии, содержащие только лимфоциты селезенки иммунизированной мыши, можно сплавить с одной шестой этого количества Р3Х63-Ag8.653 несекретирующих клеток миеломы мыши (АТСС, CRL 1580) с 50% PEG. Клетки переносят в плоскодонные планшеты для микротитрования в количестве, приблизительно, 2×105, а затем две недели инкубируют в селективной среде, содержащей 20% фетальную сыворотку Clone Serum, 18% среды "653" conditioned media, 5% оригена (IGEN), 4 mM L-глугамина, 1 mM пирувата натрия, 5mM HEPES, 0.055 mМ 2-меркаптоэтанола, 50 единиц/мл пенициллина, 50 мг/мл стрептомицина, 50 мг/мл гентамицина и 1Х HAT (Sigma; HAT добавляют через 24 часа после фузии). Приблизительно, спустя две недели клетки можно культурировать в среде, в которой HAT заменен на HT. Индивидуальные ячейки можно скринировать методом ELISA на наличие человеческих моноклональных антител IgM и IgG. Состояние среды анализируют, приблизительно, через 10-14 дней после начала экстенсивного роста гибридомы. Секретирующие антитела гибридомы можно перенести в другие планшеты, скринировать еще раз, и если ответ на человеческий IgG будет, по-прежнему, положительным, то моноклональные антитела можно субклонировать, по крайней мере, дважды при ограниченном разбавлении. Стабильные субклоны можно затем культурировать in vitro, чтобы генерировать небольшие количества антител в культуральной среде ткани для характеризации.
Для очистки моноклональных антител человека, выбранные гибридомы можно вырастить в двухлитровой колбе с мешалкой, предназначенной для очистки моноклональных антител. Супернатанты фильтруют и концентрируют, после чего применяют метод аффинной хроматографии с протеином A-сефарозой (Pharmacia, Piscataway, N.J.). Чистоту элюированного IgG проверяют гель электрофорезом и высоко-производительной жидкостной хроматографией. Буферный раствор можно заменить на PBS, а концентрацию определить с помощью прибора OD280 с коэффициентом экстинкции 1.43. Моноклональные антитела разаликвочивают и хранят при температуре -80°C.
Генерация трансфертом, продуцирующих человеческие моноклональные антитела настоящего изобретения
Антитела настоящего изобретения можно также продуцировать в трансфектомах клетки-хозяина с помощью, например, сочетания хорошо известных рекомбинантных методов работы с ДНК и методов трансфекции генов (например., Morrison, S. (1985) Science 229:1202).
Например, чтобы экспрессировать антитела или их фрагменты, ДНК, кодирующие частично или полностью тяжелые и легкие цепи, можно получить стандартными методами молекулярной биологии (например, PCR-амплификация или кДНК-клонирование с использованием гибридомы, которая экспрессирует интересующие антитела), после чего их встраивают в векторы экспрессии, так что гены оперативно связываются с последовательностями, контролирующими транскрипцию и трансляцию. В этом контексте термин "оперативно связываются" означает, что ген антитела встраивается в вектор, так что контролирующие транскрипцию и трансляцию последовательности выполняют предназначенные для них функции регуляции транскрипции и трансляции гена антитела. Вектор экспрессии и контролирующие экспрессию последовательности должны быть совместимы с используемой для экспрессии клеткой-хозяином. Гены легкой и тяжелой цепей антитела можно включить в разные вектора, или, что более распространено, оба гена можно встроить в один и тот же вектор экспрессии. Для встраивания генов антитела в вектор экспрессии используют стандартные методы (например, лигацию комплементарных ограничивающих сайтов на фрагмент гена антитела и на вектор, или, если ограничивающих сайтов нет, то лигацию по типу тупых концов. Описанные здесь вариабельные области тяжелой и легкой цепей антитела можно использовать для создания генов полной длины любого изотипа антитела. Для этого их включают в вектор экспрессии, уже кодирующий области констант тяжелой цепи и констант легкой цепи желаемого изотипа, так что сегмент VH оперативно связывается с сегментом СН вектора, сегмент Vk оперативно связывается с сегментом CL вектора. В дополнение или помимо этого, вектор рекомбинантной экспрессии может кодировать сигнальный пептид, облегчающий секрецию цепи антитела из клетки-хозяина. Ген цепи антитела можно клонировать в вектор, так чтобы сигнальный пептид связывался внутри каркаса с амино-концом гена цепи антитела. Сигнальный пептид может представлять собой сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (то есть, сигнальный пептид протеина, не являющегося иммуноглобулином).
Помимо генов цепей антитела, векторы регуляторной экспрессии настоящего изобретения содержат регуляторные последовательности, которые контролируют экспрессию генов цепей антитела в клетке-носителе. Термин "регуляторные последовательности" означает промоторы, усилители и другие контролирующие экспрессию элементы (например, сигналы полиаденилирования), которые контролируют экспрессию и трансляцию генов цепей антитела. Указанные регуляторные последовательности включают, например, Goeddel (Gene Expression Technology. Methods in Enzymology 185, Academic Press, San Diego, CA (1990)). Компетентные в молекулярной биологии специалисты понимают, что конструирование вектора экспрессии, включая выбор регуляторной последовательности, может зависеть от таких факторов, как трансформируемая клетка-хозяин, требуемый уровень экспрессии протеина и т.д. Предпочтительные регуляторные последовательности для экспрессии в клетках носителей млекопитающих включают вирусные элементы, определяющие высокий уровень экспрессии протеинов в клетках млекопитающих, например, это могут быть промоторы и/или усилители, производные от цитомегаловируса (CMV), вируса Simian Virus 40 (SV40), аденовируса (например, большой поздний промотор аденовируса (AdMLP) и полиомы. Можно также использовать и невирусные регуляторные последовательности, такие как промоторы убиквитин и бета-глобин. Более того, возможны регуляторные элементы, состоящие из последовательностей из различных источников, такие как промоторная система SRα, содержащая последовательности раннего промотора SV40 и длинного терминального повтора вируса типа I Т-клеток лейкемии человека (Takebe, Y. et al. (1988) Mol. Cell. Biol. 8:466-472).
Помимо генов цепей и регуляторных последовательностей антитела, векторы рекомбинантной экспрессии настоящего изобретения могут содержать дополнительные последовательности, например, регулирующие репликацию вектора в клетках-хозяевах(например, запускающие репликацию) и выбираемые маркерные гены (selectable marker genes). Выбираемые маркерные гены облегчают выбор клетки-хозяина, в которую был введен вектор (см., например, U.S. Pat. Nos. 4,399,216, 4,634,665 и 5,179,017, все написанные Axel et al.). Например, обычно, выбираемые маркерные гены передают в те клетки, в которые был введен вектор, резистентность к действию лекарств, таких как G418, гигромицин или метатрексат. Предпочтительные выбираемые маркерные гены включают ген дигидрофолат редуктазы (DHFR) (для использования в клетках-хозяевах с DHFR с селекцией/амплификацией метатрексатом) и ген neo (для селекции G418).
В случае экспрессии легких и тяжелых цепей, кодирующие эти цепи векторы экспрессии переносят в клетку-хозяин стандартными способами. Различные формы термина "трансфекция" охватывают огромное количество методов, обычно, применяемых для введения экзогенной ДНК в прокариотические или эукариотические клетки. Например, это может быть электропорация, кальций-фосфатпреципитация, DЕАЕ-декстрантрансфекция и т.д. Хотя теоретически возможно экспрессировать антитела настоящего изобретения либо в прокариотических, либо в эукариотических клетках, наиболее предпочитаема экспрессия в эукариотических клетках, и особенно, в клетках млекопитающих, поскольку именно эукариотические клетки, в особенности, клетки млекопитающих, с большей вероятностью, по сравнению с прокариотическими клетками, способны собрать и секретировать правильно "свернутое" иммунологически активное антитело. Сообщалось, что прокариотическая экспрессия генов антител неэффективна для достижения больших выходов активных антител (Boss, M.A. и Wood, С.R. (1985) Immunology Today 6:12-13).
Предпочтительные клетки-хозяева для экспрессии рекомбинантных антител настоящего изобретения включают клетки, изменяющие фукозилирование экспрессируемого антитела. Например, в клетке-хозяине может отсутствовать фермент фукозилтрансфераза, так что такая клетка будет продуцировать протеины, в состав углеводов которых не входит фукоза, или клетка-носитель может экспрессировать гликопротеин-модифицирующие гликозилтрансферазы, так что экспрессируемые в такой клетке антитела будут содержать увеличенное количество разветвляющихся структур GlcNac, не допускающих фукозилирования. Другие используемые для экспрессии рекомбинантных антител клетки-носители млекопитающих включают Chinese Hamster Ovary (клетки СНО) (включат dhfr-CHO описанные в работе Urlaub и Chasin, (1980) Proc. Natl. Acad. Sci. USA 77:4216-4220, используемые совместно с DHFR-выбираемым маркером, например, как описано в работе R. J. Kaufman и Р. A. Sharp (1982) Mol. Biol. 159:601-621), клетки миеломы NSO, клетки COS и клетки SP2. В частности, в случае клеток миеломы NSO, другой предпочтительной системой экспрессии является система экспрессии гена GS, рассмотренная в патентах WO 87/04462, WO 89/01036 и ЕР 338,841. Когда кодирующие гены антитела рекомбинантные векторы экспрессии вводят в клетку-хозяин млекопитающего, антитела вырабатываются клеткой в течение периода времени, достаточного, чтобы обеспечить экспрессию антитела в клетке или, более предпочтительно, секрецию антитела в культуральную среду, в которой эти клетки находятся. Для выделения антител из культуральной среды используют стандартные методы очистки протеинов.
Иммуноконъюгаты
В соответствии с другим аспектом, изобретение направлено на дефукозилированные анти-CD30 антитела или их фрагменты, конъюгированные с терапевтической группой, такой как цитотоксин, лекарством (например, иммуносуппрессантом) или радиотоксином. Такие конъюгаты называются здесь "иммуноконъюгатами". Иммуноконъюгаты, содержащие один или более цитотоксин, называются иммунотоксинами. Цитотоксин или цитотоксический агент представляет собой любой агент, разрушающий (например, убивающий) клетки. Примеры цитотоксинов включают таксол, цитокалазин В, грамицидин D, этидиум бромид, эмитин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидрокси антрацин дион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол, пуромицин и их аналоги и гомологи. Терапевтические агенты, включают, кроме того, например, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабарин, 5-фторурацил декарбазин), алкилирующие агенты (например, мехлорэтамин, тиоэпахлорамбуцил, малфалан, кармустин (BSNU) иломустин (CCNU), циклотосфамид, бисульфан, дибромоманитол, стрептозотоцин, митомицин С и цис-дихлордиаминплатина(II) (DDP) цисплатин), антрациклины (например, даунорубицин (ранее дауномицин) и доксорубицин), антибиотики (например, дактиномицин (ранее актиномицин), блеомицин, митрамицин и антрамицин(АМС)), а также анти-митотические агенты (например, винкристин и винбластин).
Другие предпочтительные примеры терапевтических цитотоксинов, которые можно конъюгировать с антителами настоящего изобретения, включают дуокармицины, калихеамицины, майтанзины иауристатины, а также их производные. Пример конъюгата антитела с калихеамицином в настоящее время доступен коммерчески (Mylotarg™; Wyeth-Ayerst).
Цитотоксины можно конъюгировать с антителами настоящего изобретения с помощью линкера, технологически доступного в этой отрасли. Примеры типов линкеров, используемых для конъюгации цитотоксина с антителом, включают, но не ограничиваются, гидразоны, тиоэфиры, сложные эфиры, дисульфиды и пептид-содержащие линкеры. Можно выбрать такой линкер, чтобы он, например, разрушался при низком pН в лизосомальном компартменте, или разрушался протеазами, такими как протеазы, предпочтительно экспрессирующиеся в опухолевых тканях, например, катепсинами (например, катепсинами В, С и D).
Более подробное описание типов цитотоксинов, линкеров и методов конъюгации терапевтических агентов с антителами содержится в работах Saito, G. et al. (2003) Adv. Drug Deliv. Rev. 55:199-215; Trail, P.A. et al. (2003) Cancer Immunol. Immunother. 52:328-337; Payne, G. (2003) Cancer Cell 3:207-212; Alien, T.M. (2002) Nat. Rev. Cancer 2:750-763; Pastan, I. and Kreitman, R.J. (2002) Curr. Opin. Investig. Drugs 3:1089-1091; Senter, P.D. and Springer, C.J. (2001) Adv. Drug Deliv. Rev. 53:247-264.
Антитела настоящего изобретения можно конъюгировать также с радиоактивными изотопами, получая цитотоксические радиофармацевтические препараты, называемые также радиоиммуноконъюгатами. Примеры радиоактивных изотопов, которые можно конъюгировать с антителами для терапевтического или диагностического применения, включают, но не ограничиваются, иод131, индий111, иттрий90 и лютеций177. Известны методы приготовления радиоиммуноконъюгатов. Примеры коммерчески доступных радиоиммуноконъюгатов включают Zevalin™ (IDEC Pharmaceuticals) и Bexxar™ (Corixa Pharmaceuticals), подобные методы позволяют получить радиоиммуноконъюгаты с антителами настоящего изобретения.
Конъюгаты антител настоящего изобретения могут использоваться, чтобы модифицировать данный биологический ответ, и лекарственную группу не следует ограничивать только классическими терапевтическими агентами. Например, лекарственная группа может представлять собой протеин или полипептид, обладающий желательной биологической активностью. Такие протеины могут включать, например, ферментативно активный токсин или его активный фрагмент, такой как абрин, рицин А, экзотоксин синегнойной палочки или токсин дифтерии; такой протеин, как фактор некроза опухолей или гамма-интерферон; или модификаторы биологического ответа, такие как, например, лимфокины, интерлейкин-1 ("IL-1"), интерлейкин-2 ("IL-2"), интерлейкин-6("IL-6"), фактор стимуляции колонии макрофагов гранулоцитов ("GM-CSF"), фактор стимуляции колонии гранулоцитов ("G-CSF"), или другие факторы роста.
Методы конъюгирования подобных терапевтических групп с антителами хорошо известны в соответствующей области. См., например, работы Arnon et al., "Monoclonal Антитела For Immunotargeting Of Drugs In Cancer Therapy", in Monoclonal Антитела и Cancer Therapy, Reisfeld et al. (eds.), pp.243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al., "Антитела For Drug Delivery", in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp.623-53 (Marcel Dekker, Inc. 1987); Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", in Monoclonal Антитела '84: Biological и Clinical Applications, Pinchera et al. (eds.), pp.475-506 (1985); "Analysis, Results, и Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", in Monoclonal Антитела For Cancer Detection и Therapy, Baldwin et al. (eds.), pp.303-16 (Academic Press 1985), и Thorpe et al., "The Preparation и Cytotoxic Properties Of Antibody-Toxin Conjugates", Immunol. Rev., 62:119-58 (1982).
Фармацевтические композиции
В соответствии с еще одним аспектом, настоящее изобретение направлено на композиции, например, на фармацевтические композиции, содержащие одно моноклональное антитело настоящего изобретения (или его антиген-связывающий фрагмент) или их комбинацию совместно с фармацевтически приемлемым носителем. Такие композиции могут включать одно или несколько (например, два или больше различных) антител или иммуноконъюгатов изобретения. Например, фармацевтическая композиция настоящего изобретения может содержать комбинацию антител (или иммуноконъюгатов), связывающихся с различными эпитопами антигена-мишени или обладающих комплементарной активностью.
Фармацевтические композиции настоящего изобретения можно также назначать в ходе совместной терапии, то есть, совместно с другими агентами. Например, совместная терапия может включать назначение дефукозилированного анти-CD30 антитела настоящего изобретения совместно, по меньшей мере, с одним антинеопластическим, противовоспалительным или подавляющим иммунитет агентом. Подобные терапевтические агенты включают, помимо прочего, стероидные и нестероидные противовоспалительные лекарства (NSAIDS), например, аспирин и другие салицилаты, такие как ибупрофен (Motrin, Advil), напроксен (Naprosyn), сулиндак (Clinoril), дихлофенак (Voltaren), пироксикам (Feldene), кетопрофен (Orudis), дифлунизал (Dolobid), набуметон (Relafen), этодолак (Lodine), оксапроизн (Daypro), индометацин (Indocin), и аспирин в высоких дозах. Другие примеры терапевтических агентов, которые могут использоваться в совместной терапии, подробно описаны далее в разделе, посвященном применению антител настоящего изобретения.
В контексте настоящего изобретения термин "фармацевтически приемлемый носитель" включает любой и все растворители, среды диспергирования, покрытия, противогрибковые и антибактериальные агенты, изотонические агенты, средства задержки абсорбции, а также подобные препараты, которые должны быть физиологически совместимы. Предпочтительно, чтобы носитель был приемлем для внутривенного, внутримышечного, подкожного, парентерального, спинального или эпидермального введения (например, инъекция или инфузия). В зависимости от маршрута введения, активное соединение, то есть, антитело или иммуноконъюгат, может быть защищено покрытием из вещества, защищающего соединение от действия кислот и других природных условий, которые способны его инактивировать.
Фармацевтические соединения настоящего изобретения могут содержать одну или больше фармацевтически приемлемых солей. "Фармацевтически приемлемой" называют соль, которая сохраняет требуемую биологическую активность родительского соединения и не вызывает нежелательных биологических эффектов (см., например, Berge, S.M., et al. (1977) J. Pharm. Sci. 66:1-19). Примеры таких солей включают соли присоединения кислот и оснований. Соли присоединения кислот получают из нетоксических неорганических кислот, таких как соляная, азотная, фосфорная, серная, бромоводородная, иодоводородная, фосфористая и подобные им, а также из нетоксических органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенил-замещенные алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты и подобные им. Соли присоединения оснований включают полученные из щелочных и щелочно-земельных металлов, таких как натрий, калий, магний, кальций и подобные им, а также из нетоксических органических аминов, таких как N,N'-дибензилэтилендиамин, N-метилглюкамин, хлоропрокаин, холин, диэтаноламин, этилендиамин, прокаин и подобные им.
Фармацевтические композиции настоящего изобретения могут содержать также фармацевтически приемлемый антиоксидант. Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, цистеин гидрохлорид, бисульфат и метабисульфат натрия, сульфит натрия и подобные им; (2) маслорастворимые антиоксиданты, такие как аскорбил пальмиат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, альфа-токоферол и подобные им; (3) хелаторы металлов, такие как лимонная кислота, этилендиамин тетрауксусная кислота (ЭДТА), сорбитол, винная кислота, фосфористая кислота и подобные им.
Примеры растворимых водных и неводных носителей, которые могут использоваться в фармацевтических композициях настоящего изобретения, включают воду, этанол, полиолы (такие как глицерин, пропилен гликоль, полиэтилен гликоль и подобные им) и их подходящие смеси, растительные масла, такие как оливковое масло, а также пригодные для инъекций органические сложные эфиры, такие как этил олеат. Для обеспечения требуемой текучести можно воспользоваться такими покрытиями, как лецитин, в случае использования дисперсий обеспечить требуемый размер частиц, а также использовать поверхностно-активные вещества.
Указанные композиции могут также содержать такие адьюванты, как консерванты, увлажнители, эмульсификаторы и диспергирующие агенты. Чтобы не допустить развития микроорганизмов, проводят стерилизацию, а также включат различные антибактериальные и противогрибковые агенты, например, парабен, хлоробутанол, фенол сорбиновая кислота и подобные им. Иногда бывает желательно включить также изотонические агенты, такие как сахара, хлорид натрия и подобные им. Кроме того, можно обеспечить продолжительную абсорбцию пригодных для инъекций фармацевтических форм, включив в композиции агенты, замедляющие абсорбцию, например, моностеарат алюминия и желатин.
Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии, а также стерильные порошки для немедленного приготовления стерильных водных растворов или дисперсий. Использование таких средств и агентов в фармацевтически приемлемых субстанциях хорошо известно в фармацевтике. Их применение в фармацевтических композициях настоящего изобретения входит в область действия изобретения, за исключением случаев, когда растворимые носитель или агент несовместим с активным соединением. В композицию можно включить также дополнительные активные компоненты.
Как правило, терапевтические композиции должны быть стерильны и стабильны в условиях их производства и хранения. Композиции можно составить в виде раствора, микроэмульсии, липосомы и других упорядоченных структур, подходящих для высоких концентраций лекарства. Носителем может быть растворитель или среда диспергирования, содержащая, например, воду, этанол, полиолы (например, глицерин, пропилен гликоль, жидкий полиэтилен гликоль и подобные им), а также их подходящие смеси. Для обеспечения требуемой текучести можно воспользоваться такими покрытиями, как лецитин, в случае использования дисперсий обеспечить требуемый размер частиц, а также использовать поверхностно-активные вещества. Часто бывает желательно включить также изотонические агенты, например, сахара, полиспирты, такие как манит, сорбит, или хлорид натрия. Кроме того, можно обеспечить продолжительную абсорбцию пригодных для инъекций композиций, включив в них агенты, замедляющие абсорбцию, например, соли моностеаратов и желатин.
Для приготовления стерильных растворов для инъекций требуемое количество активного соединения можно включить в соответствующий растворитель с одним или несколькими перечисленными выше ингредиентами. Если требуется, затем проводят стерилизацию микрофильтрацией. В общем случае, для приготовления дисперсий активное соединение включают в стерильный носитель, содержащий базовую среду для диспергирования и другие необходимы ингредиенты, перечисленные выше. Для получения стерильных порошков, используемых при приготовлении стерильных водных растворов для инъекций, предпочтительными методами является вакуумная сушка и вымораживание (лиофилизация); в результате получают порошок, состоящий из активного ингредиента, а также дополнительных ингредиентов, содержащихся в использованном для сушки профильтрованном стерильном растворе.
Количество активного ингредиента, который можно смешать с веществом носителя для получения формы единичной дозировки, зависит от субъекта, которого требуется лечить, и конкретного режима приема препарата. В общем случае, количество активного ингредиента, который можно смешать с веществом носителя для получения формы единичной дозировки, должно обеспечивать терапевтический эффект. В целом, это количество колеблется, приблизительно, от 0,01 до 99% активного ингредиента, предпочтительно, приблизительно, от 0,1 до 70%, более предпочтительно, от 1 до 30% активного ингредиента, смешанного с фармацевтически приемлемым носителем.
Режим дозирования подбирается так, чтобы обеспечить оптимальный требуемый эффект (например, терапевтический ответ). Например, можно назначить однократную дозу, можно разделить ее на несколько доз в течение определенного временного промежутка, либо дозу можно увеличивать или уменьшать, в зависимости от терапевтической ситуации. Полезно составить парентеральную композицию, соответствующую форме единичной дозировки, это облегчит введение и сделает дозировку универсальной. Форма единичной дозировки в контексте настоящего изобретения означает физически дискретную единицу, подходящую для унитарной дозировки субъектам лечения; каждая такая единица содержит заранее определенное количество активного соединения, рассчитанное так, чтобы произвести желаемый терапевтический эффект, совместно с требуемым фармацевтическим носителем. Спецификация формы единичной дозировки изобретения определяется и непосредственно зависит от (а) уникальных характеристик активного соединения и конкретного терапевтического эффекта, который необходимо получить; и (b) ограничений, связанных с индивидуальной чувствительностью субъектов.
Дозировка при введение антитела колеблется, приблизительно, от 0.0001 до 100 мг/кг, чаще от 0,01 до 5 мг/кг веса тела пациента. Например, доза может составлять 0,3 мг/кг веса тела, 1 мг/кг веса тела, 3 мг/кг веса тела, 5 мг/кг веса тела или 10 мг/кг веса тела, или находятся в диапазоне 1-10 мг/кг. Примеры режима лечения включают назначение один раз в неделю, один раз в две недели, раз в три недели, раз в четыре недели, раз в месяц, раз в три месяца или раз каждые три-шесть месяцев. Предпочтительные режимы дозировки дефукозилированных анти-CD30 антител изобретения включают внутривенное введение 1 мг/кг веса тела или 3 мг/кг веса тела, причем режим введения антител может быть следующим: (i) шесть введений каждые четыре недели, а затем каждые три месяца; (ii) каждые три недели; (iii) однократное введение 3 мг/кг веса тела, а затем по 1 мг/кг каждые три недели.
В соответствии с некоторыми методами настоящего изобретения, два или более моноклональных антитела с различными характеристиками связывания вводят одновременно, в этом случае дозировка каждого антитела находится в указанных границах. Обычно, антитела вводят по различным поводам. Интервалы между отдельными введениями могут составлять, например, неделю, месяц, три месяца или год. Интервалы могут также быть нерегулярными и определяться содержанием в крови пациента антитела к антигену-мишени. Иногда, дозировку подбирают так, чтобы добиться содержания антитела в плазме крови, приблизительно, 1-1000 мкг/мл или, в соответствии с некоторыми методами, приблизительно, 25-300 мкг/мл.
Альтернативно, антитела можно вводить в составе препарата, обеспечивающего замедленный режим высвобождения, в этом случае требуется назначать его менее часто. Дозировки и частота зависят от продолжительности полу-жизни антитела в организме пациента. В общем случае, дольше всего живут антитела человека, затем следуют гуманизированные антитела, химерные антитела и нечеловеческие антитела. Дозировка и частота введения может зависеть от того, является ли лечение профилактическим или терапевтическим. В профилактических целях назначают относительно низкую дозу достаточно редко, и лечение проводят в течение длительного времени. Некоторые пациенты продолжают принимать препарат всю свою жизнь. В терапевтических целях относительно высокие дозы назначают достаточно часто. Это делают до тех пор, пока развитие болезни не замедляется или не останавливается, предпочтительно, до тех пор, пока пациент не продемонстрирует частичное или полное прекращение симптомов болезни. После этого пациента можно перевести на профилактический режим.
Фактические дозировки активных ингредиентов фармацевтических композиций настоящего изобретения могут колебаться так, чтобы найти такое количество активного ингредиента, которое эффективно позволяет добиться требуемого терапевтического ответа у конкретного пациента, для конкретного состава и режима введения, и при этом будучи нетоксичным для пациента. Выбранная дозировка зависит от большого количества фармакокинетических факторов, включая активность конкретных используемых композиций настоящего изобретения, использования его в виде эфира, соли или амида, маршрута и времени введения, скорости экскреции (выведения) используемого соединения, продолжительности лечения, других лекарств, соединений и/или веществ, используемых совместно с конкретной композицией, возраста, пола, веса, состояния, общего состояния здоровья и истории болезни пациента, а также других факторов, хорошо известных в медицинской практике.
Терапевтически эффективная дозировка анти-CD30 антител настоящего изобретения, предпочтительно, приводит к снижению интенсивности симптомов болезни, увеличению частоты и продолжительности периодов без симптомов, или предотвращению нарушений или инвалидности, вызванных влиянием болезни. Например, в случае лечения злокачественных опухолей, "терапевтически эффективная дозировка", предпочтительно, ингибирует рост клеток или опухоли, по меньшей мере, на 20%, более предпочтительно, по меньшей мере на 40%, еще более предпочтительно, по меньшей мере на 60%, и еще более предпочтительно, по меньшей мере на 80%, по сравнению с субъектами, не получавшими такое лечение. Способность соединения ингибировать рост опухолей можно оценить на животной модельной системе, способной предсказать эффективность лечения опухолей человека. Альтернативно, для оценки этого свойства композиции можно определить способность соединения ингибировать развитие опухолевых клеток, опытные практикующие врачи знают такие анализы in vitro. Терапевтически эффективное количество терапевтического соединения может уменьшить размер опухоли или иначе ослабить симптомы у субъекта. Компетентный специалист может определить такое количество, основываясь на таких факторах, как размер субъекта, интенсивность симптомов, а также конкретная композиция или выбранный маршрут введения.
Композицию настоящего изобретения можно вводить одним или несколькими маршрутами, используя один или несколько известных методов. Как понимает опытный врач, маршрут и/или режим введения зависит от требуемых результатов. Предпочтительные маршруты введения для антител настоящего изобретения включают внутривенное, внутримышечное, интрадермальное, внутрибрюшинное, подкожное, спинальное или другие парентеральные маршруты введения, например, инъекции или инфузии. Фраза "парентеральное введение" означает в контексте настоящего изобретения режимы введения, которые отличаются от энтерального или топического, обычно, осуществляются методом инъекции, и включают, но не ограничиваются, внутривенное, внутримышечное, внутриартериальное, интратекальное, антракапсулярное, внутриорбитальное, в сердечную мышцу, интрадермальное, внутрибрюшинное, транстрахеальное, подкожное, интраартикулярное, субкапсулярное, субарахноидальное, субкутикулярное, интраспинальное, эпидуральное и интрастернальное введение методом инъекции или инфузии.
Альтернативно, дефукозилированные антитела настоящего изобретения можно вводить по не-парентеральному маршруту, такому как топический, эпидермальный или мукозальный маршруты введения, например, интраназальный, оральный, вагинальный, ректальный, сублингвальный или топический маршруты.
В состав активных соединений можно включить носители, защищающие его от быстрого высвобождения. В результате будут получены составы с контролируемым высвобождением, включая импланты, трансдермальные пластыри и микроинкапсулированные системы доставки. В них могут использоваться биодеградируемые, биосовместимые полимеры, такие как винилацетат этилена, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие методы приготовления таких составов запатентованы или широко известны специалистам. См., например, Sustained и Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
При введении терапевтических композиций можно использовать медицинские приспособления, известные в соответствующей области. Например, в соответствии с предпочтительным аспектом изобретения, терапевтическую композицию настоящего изобретения можно ввести с помощью безиголочного гиподермического устройства для инъекций, такого как описано в патентах U.S. Patent Nos. 5,399,163; 5,383,851; 5,312,335; 5,064,413; 4,941,880; 4,790,824 или 4,596,556. Примеры хорошо известных имплантов и модулей, полезных в практике настоящего изобретения, включают: U.S. No. 4,487,603, описывающий имплантируемую помпу для микроинфузии для введения препарата с контролируемой скоростью; U.S. Patent No. 4,486,194, описывающий терапевтическое приспособление для введения лекарств через кожу; U.S. No. 4,447,233, описывающий помпу для инфузии медикаментов, которая обеспечивает точную скорость инфузии; U.S. No. 4,447,224, описывающий имплантируемый аппарат для инфузии с переменной скоростью, который обеспечивает непрерывную доставку лекарства; U.S. Patent No. 4,439,196, описывающий осмотическую систему доставки лекарства, содержащую несколько отсеков; а также U.S. No. 4,475,196, в котором также раскрыта осмотическая система доставки лекарства. Эти патенты включены в данную заявку по ссылке. Компетентным специалистам известно много других имплантов, систем доставки и модулей.
В соответствии с определенными аспектами, дефукозилированные антитела настоящего изобретения можно включить в состав, обеспечивающий правильное распределение лекарства in vivo. Например, большое количество высоко-гидрофильных лекарств не проходит через гематоэнцефалический барьер (ГЭБ). Чтобы терапевтические соединения настоящего изобретения проходили через ГЭБ (если это требуется), их надо включить в состав, например, липосом. Методы изготовления липосом описаны, например, в работах U.S. Patents 4,522,811; 5,374,548; и 5,399,331. Липосомы могут содержать одну или несколько групп, селективно транспортируемых в специфические клетки или органы, что улучшает доставку лекарства (см., например, V.V. Ranade (1989) J. Clin. Pharmacol. 29:685). Примеры таких целевых групп включают фолат и биотин (см., например, U.S. Patent 5,416,016 to Low et al.); маннозиды (Umezawa et al., (1988) Biochem. Biophys. Res. Commun. 153:1038); антитела (P.G. Bloeman et al. (1995) FEBS Lett. 357:140; M. Owais et al. (1995) Antimicrob. Agents Chemother. 39:180); рецептор поверхностно активного протеина A (Briscoe et al. (1995) Am. J. Physiol. 1233:134); p120 (Schreier et al. (1994) J. Biol. Chem. 269:9090); см. также К. Keinanen; M.L Laukkanen (1994) FEBS Lett. 346:123; J.J. Killion; I.J. Fidler(1994) Immunomethods 4:273.
Применения и методы настоящего изобретения
Дефукозилированные антитела, их композиции и методы настоящего изобретения находят многочисленные диагностические и терапевтические применения in vivo и in vitro, включая диагностику и лечение расстройств, в которых участвует экспрессия CD30. Например, эти молекулы можно вводить клеткам в культуре, например, in vitro или ex vivo, или людям, например, in vivo, для лечения, профилактики или диагностики разнообразных заболеваний. Термин "субъект" здесь означает людей или других животных. К числу животных относятся все позвоночные, например, млекопитающие и не млекопитающие, такие как приматы, овцы, собаки, кошки, коровы, лошади, свиньи, цыплята, птицы, амфибии и рептилии. Предпочтительные субъекты - это люди, страдающие заболеваниями, которые характеризуются экспрессией CD30. Если антитела к CD30 вводят совместно с другим агентом, то их можно вводить в любом порядке или одновременно.
Подходящие маршруты введения композиций антител (например, антител или иммуноконъюгатов) настоящего изобретения in vivo и in vitro хорошо известны в соответствующей области и могут быть подобраны специалистом. Например, композиции антител можно вводить методом инъекции (например, внутривенно или подкожно). Дозировка зависит от возраста и веса субъекта и от концентрации и/или состава композиции антител.
В соответствии с одним аспектом, антитела настоящего изобретения можно первоначально тестировать на связывание, ассоциированное с терапевтическим или диагностическим применением in vitro. Например, композиции настоящего изобретения можно тестировать методом ELISA и потоковыми цитометрическими анализами. Более того, можно проверить также способность этих молекул участвовать в запуске по меньшей мере одной опосредованной эффекторами активности эффекторных клеток, включая ингибирование роста и/или уничтожение клеток, экспрессирующих CD30. Протоколы анализа опосредованной эффекторными клетками ADCC описаны в следующем далее разделе Примеров.
A. Методы детекции
В соответствии с одним аспектом, антитела настоящего изобретения можно использовать для детекции уровней CD30 или клеток с CD30 на поверхности своей мембраны, эти уровни можно затем связать с симптомами определенных заболеваний.
В соответствии с конкретным аспектом, изобретение направлено на методы детекции наличия антигена CD30 в образце или на измерение количества антигена CD30, включающие воздействие на образец или на контрольный образец дефукозилированного антитела или его антиген-связывающего фрагмента, которые специфически связываются с CD30, в условиях, позволяющих образоваться комплексу между CD30 и антителом или его фрагментом. После этого регистрируют образование комплекса, причем различие в образовании комплекса между образцом и контрольным образцом позволяет сделать вывод о наличии в образце антигена CD30. Например, совместно с композициями настоящего изобретения можно стандартные хорошо известные методы регистрации, такие как ELISA и потоковые цитометрические анализы.
Таким образом, в соответствии с одним своим аспектом, изобретение направлено на методы определения наличия CD30 (например, антигена CD30 человека) в образце или измерения количества CD30, включающие воздействие на образец или на контрольный образец дефукозилированного антитела или его антиген-связывающего фрагмента, которые специфически связываются с CD30, в условиях, позволяющих образоваться комплексу между CD30 и антителом или его фрагментом. После этого регистрируют образование комплекса, причем различие в образовании комплекса между образцом и контрольным образцом позволяет сделать вывод о наличии в образце антигена CD30.
Композиции настоящего изобретения можно также применять к клеткам-мишеням, экспрессирующим CD30, например, для мечения таких клеток. Для этого к молекуле необходимо прикрепить агент связывания, который может быть зарегистрирован. Таким образом, настоящее изобретение направлено на методы локализации экспрессирующих CD30 клеток ex vivo или in vitro. В качестве детектируемой метки можно использовать, например, радиоизотоп, флуоресцирующее соединение, фермент или его кофактор.
B. Ингибирование роста клеток CD30+
Антитела можно использовать для ингибирования или блокирования функции CD30, что, в свою очередь можно связать с профилактикой или ослаблением симптомов некоторых заболеваний, если предположить, что CD30 принимает участие в развитии болезни. Различия в экспрессии CD30 при заболевании, по сравнению со здоровыми субъектами, можно определить, воздействуя на тестовый образец, взятый у субъекта, страдающего от заболевания, и на контрольный образец анти-CD30 антителом в условиях, позволяющих образоваться комплексу между антителом и CD30. Любые комплексы, образующиеся между антителом и CD30, регистрируют, и сравнивают полученные данные для образца и контроля.
Например, антитела позволяют осуществить in vivo или in vitro одно или несколько следующих действий: ингибировать рост и/иди уничтожить экспрессирующие CD30 клетки; опосредовать фагоцитоз или ADCC экспрессирующих CD30 клеток в присутствии эффекторных клеток человека; ингибировать удаление растворенного CD30; блокировать связывание лиганда CD30 с самим CD30; ингибировать экспрессию IL-4 или опосредовать экспрессию фенотипа Th2, например, при низких дозах. Как описано в настоящей заявке, дефукозилированные антитела настоящего изобретения показывают усиленную активность ADCC, по сравнению с их фукозилированной формой.
Таким образом, в соответствии с еще одним своим аспектом, настоящее изобретение направлено на метод ингибирования роста клеток CD30+, включающий воздействие на указанные клетки анти-CD30 антител в условиях, достаточных для индукции зависящей от антител клеточной цитотоксичности (ADCC) указанных клеток. Клетки могут, например, представлять собой опухолевые клетки. В соответствии с предпочтительным аспектом, анти-CD30 антитела представляют собой антитела человека.
В соответствии с еще одним аспектом, антитела настоящего изобретения или их связывающие фрагменты могут использоваться для модуляции уровней CD30 клеток-мишеней, например, путем захвата или элиминации рецепторов на клеточной поверхности. Для этой цели также можно использовать смеси анти-Fc рецепторных антител.
Мишень-специфические эффекторные клетки, например, эффекторные клетки, связанные с композициями настоящего изобретения, могут также использоваться в качестве терапевтических агентов. Подходящие в качестве мишеней эффекторные клетки могут представлять собой лейкоциты человека, такие как макрофаги, нейтрофилы или моноциты. Другие клетки включают эозинофилы, природные клетки-киллеры и другие клетки, содержащие IgG-или IgA-рецепторы. Если необходимо, эффекторные клетки можно получить у субъекта, подлежащего лечению. Мишень-специфические эффекторные клетки можно вводить в виде суспензии клеток в физиологически приемлемом растворе. Количество вводимых клеток может быть порядка 108-109, но оно сильно зависит от терапевтической цели. В общем случае, количества должно быть достаточно, чтобы определить локализацию клетки-мишени, например, экспрессирующей CD30 опухолевой клетки, и повлиять на уничтожение клеток, например, на фагоцитоз. Также могут варьироваться маршруты введения.
Терапия мишень-специфическими эффекторными клетками может проводиться совместно с другими методами с целью удаления клеток мишени. Например, противоопухолевая терапия с использованием композиций настоящего изобретения и/или нацеленных на эти композиции эффекторных клеток может проводиться совместно с химиотерапией. В дополнение к этому, методами комбинационной иммунотерапии две различные популяции цитотоксических эффекторов можно нацелить на удаление опухолевых клеток.
C. Использование иммуноконъюгатов и комбинационной терапии
В соответствии с одним из аспектов, иммуноконъюгаты настоящего изобретения можно использовать для того, чтобы направить определенные соединения (например, терапевтические агенты, метки, цитотоксины, радиотоксины, иммуносуппрессанты и т.д.) на клетки с CD30 клеточными рецепторами на поверхности, связав такие соединения с антителами. Таким образом, изобретение также направлено на методы локализации ex vivo или in vitro клеток, экспрессирующих CD30 (например, с помощью регистрируемой метки, такой как радиоизотоп, флуоресцирующее соединение, фермент или его кофактор). Альтернативно, иммуноконъюгаты можно использовать для того, чтобы убивать клетки с CD30 клеточными рецепторами на поверхности, направляя цитотоксины и радиотоксины на CD30 (например, так можно убивать экспрессирующие CD30 опухолевые клетки) или на экспрессирующие CD30 антиген-представляющие клетки (например, в случае аутоиммунных заболеваний).
В соответствии с другими аспектами, субъекта можно дополнительно лечить агентом, который модулирует, например, усиливает или ингибирует, экспрессию или активность Fcγ или Fcγ рецепторов, например, воздействуя на субъект цитокинами. Цитокины, предпочтительные для введения при лечении, включают колониестимулирующий фактор гранулоцитов (G-CSF), включают колониестимулирующий фактор макрофагов гранулоцитов (GM-CSF), γ-интерферон (IFN-γ), и фактор некроза опухолей (TNF).
В соответствии с еще одним аспектом, субъекта можно дополнительно лечить препаратом из лимфокинов. Раковые клетки, не слишком сильно экспрессирующие CD30, можно заставить делать это с помощью препаратов из лимфокинов. Последние вызывают более гомогенную экспрессию CD30 в клетках опухолей, что может привести к более эффективной терапии. Подходящие для администрирования препараты из лимфокинов включают гамма-интерферон, фактор некроза опухолей и их комбинацию. Их можно вводить внутривенно. Подходящие дозировки лимфокинов составляют от 10000 до 1000000 единиц/пациента.
В соответствии с другим аспектом, пациентам, которых лечат композициями антител настоящего изобретения, можно дополнительно вводить (до, одновременно или после введения антител изобретения) другие терапевтические агенты, такие как цитотоксические или радиотоксические агенты, которые усиливают терапевтический эффект антител человека. Антитела можно связать с агентом (например, с иммунокомлексом), или их можно вводить отдельно от агента. В последнем случае (раздельная администрация) их можно вводить до, после или параллельно с агентом, или их можно назначать совместно с другими видами лечения, такими как противораковая терапия, например, лучевая терапия. Подобные терапевтические агенты включают, помимо прочего, антинеопластические агенты, такие какдоксорубицин (адриамицин), цисплатин блеомицин сульфат, кармустин, хлорамбуцил, а также циклофосфамид гидроксимочевина; сами по себе эти вещества эффективны при таких концентрациях, когда они становятся токсичными или субтоксичными для пациентов. Цисплатин назначают внутривенно в дозе 100 мг/мл раз в четыре недели, а адриамицин назначают внутривенно в дозе 60-75 мг/мл каждые 21 день. Совместное введение анти-CD30 антител или их антиген-связывающих фрагментов настоящего изобретения и химиотерапевтического агента позволяет получить два противораковых агента, действующих по различным механизмам и вызывающих цитотоксический эффект у человеческих опухолевых клеток. Такая совместная администрация позволяет решить проблемы, связанные с развитием резистентности к действию лекарств или изменением антигенных свойств опухолевых клеток, которые могут сделать их невосприимчивыми к действию антител.
D. Лечение аутоиммунных заболеваний
Композиции настоящего изобретения можно использовать in vitro или in vivo для лечения заболеваний, опосредованных или протекающих с участием CD30, например, заболеваний, характеризующихся экспрессией, как правило, сверхэкспрессией CD30. Это могут быть аутоиммунные заболевания, опосредуемые макрофагами, активированными нейтрофилами, дендритными или NK клетками, такие как отторжение трансплантированных органов или вторичная болезнь типа "трансплантат против хозяина" (GVHD). Растворимый в воде CD30 регулярно смывается с поверхности экспрессирующих CD30 клеток. Повышенное содержание SCD30 отмечалось в сыворотке пациентов, страдающих большим количеством опухолегенных и аутоиммунных заболеваний. Соответственно, еще одно применение антител настоящего изобретение заключается в профилактике или лечении заболеваний, вовлекающих блокаду или ингибирование вымывания sCD30.
При действии антитела на CD30 (например, при назначении антитела субъекту) способность последнего индуцировать такую активность ингибируется и, тем самым, связанное с этим заболевание вылечивается. Композицию антитела можно вводить отдельно или вместе с другим терапевтическим агентом, таким как иммуносуппрессант, действующий совместно или синергично с композицией антител для лечения или профилактики опосредованных CD30 заболеваний. Предпочтительные антитела связываются с эпитопами, специфичными по отношению к CD30, и, таким образом, преимущественно ингибируют индуцированную CD30 активность, но не влияют на активность структурно родственных антигенов поверхности. Композиции могут использоваться для лечения любых заболеваний, опосредованных клетками, экспрессирующими CD30, включая, но не ограничиваясь, аутоиммунную гемолитическую анемию (АIНА), ревматоидный артрит (RA), системную красную волчанку, системный склероз, атопический дерматит, болезнь Гравса, тироидит Хашимото, грануломатоз Вегнера, синдром Омена, хроническую почечную недостаточность, идиопатическую тромбоцитопеническую пурпуру (IТР), синдром воспаленного кишечника (IBD), включая болезнь Крона, язвенный колит и глютеновую болезнь, инсулин-зависимый сахарный диабет (IDDM), острый инфекционный мононуклеоз, HIV, связанные с герпесом заболевания, множественный склероз (MS), гемолитическую анемию, тироидит, синдром мышечной скованности, обыкновенная пузырчатка и миастения gravis (MG).
E. Лечение рака
В соответствии с другим своим аспектом, настоящее изобретение направлено на метод ингибирования роста опухолевых клеток CD30+ (то есть, опухолевых клеток, экспрессирующих CD30) у субъекта, при котором дефукозилированные анти-CD30 антитела настоящего изобретения назначают субъекту, так чтобы заингибировать рост опухолевых клеток CD30+. В случае человека, антитело, предпочтительно, представляет собой гуманизированное антитело или антитело человека. В соответствии с предпочтительным аспектом изобретения, опухолевые клетки представляют собой клетки опухоли болезни Ходжкинса. В соответствии с еще одним предпочтительным аспектом изобретения, опухолевые клетки представляют собой клетки опухоли анапластической крупно-клеточной лимфомы (ALCL). В соответствии с другими аспектами, клетки опухолей связаны с болезнями, выбранными из группы, включающей лимфому не Ходжкина, лимфому Буркитта, кожные T-клеточные лимфомы, узелковые мелкоклеточные лимфомы, лимфоцитарные лимфомы, периферические лимфомы T-клеток, лимфомы Леннерта, лимфомы иммунобластов, лейкемии/лимфомы T-клеток (ATLL), лимфома взрослых T-клеток (T-ALL), фолликулярные лимфомные опухоли энтеробластов/центроцитов (cb/cc), диффузные крупноклеточные лимфомы В-типа, Т-клеточная лимфому, похожую на ангиоиммунобластозную лимфаденопатию (AILD), лимфону взрослых R-клеток (ATL), HIV-ассоциированные лимфомы, связанные с полостью тела, эмбриональные карциномы, недифференцированные карциномы носоглотки (например, опухоль Шминке), болезнь Кастлмана, саркома Капоши и другие CD30+ Т-клеточные лимфомы и CD30+ B-клеточные лимфомы.
Метод включает введение субъекту композиции антител настоящего изобретения в количестве, эффективном для лечения или профилактики заболевания. Композицию антител можно вводить самостоятельно или совместно с другим терапевтическим агентом, таким как цитотоксический или радиотоксический агент, который действует вместе с или синергично с композицией антител, осуществляя лечение или профилактику заболеваний, связанных с экспрессией CD30.
Наборы
В область действия настоящего изобретения попадают также наборы, включающие антитела настоящего изобретения и инструкции по их применению. Наборы могут содержать также один или больше дополнительных реагентов, таких как иммуностимулирующий реагент, цитотоксический агент или радиотоксический агент, или одно или больше дополнительных антител настоящего изобретения (например, антител с комплементарной активностью, связывающихся с эпитопом антигена CD30, отличающимся от того, на который действует первое антитело). Наборы, как правило, содержат наклейку, на которой написано, для чего предназначено их содержание. Термин "наклейка" включает любой письменный материал, поставляемый совместно с набором или на наборе, или сопровождающий набор каким-либо иным способом.
Далее настоящее изобретение иллюстрируется следующими примерами, которые не ограничивают его область. Содержание всех рисунков, всех ссылок, патентов и опубликованных патентных заявок, процитированных в настоящей заявке, явным образом включено в нее по ссылке.
ПРИМЕРЫ
Пример 1. Приготовление и характеризация дефукозилированных анти-CD30 моноклональных антител
В этом примере полностью человеческие моноклональные анти-CD30 антитела экспрессируются в линии клеток, в которых отсутствует фермент фукозил трансфераза, так что углеводные цепи протеинов, продуцируемых клеточной линией, не содержат фукозы. Дефукозилированные антитела были протестированы в сравнении с фукозилированными анти-CD30 антителами (экспрессирующимися в другой клеточной линии, содержащей фермент фукозил трансферазу) с целью определить структурные и характеристические различия между антителами. При анализе использовались разнообразные методы химического анализа, включая капиллярный электрофорез, сравнение аминокислотных последовательностей, определение массовых различий методом масс-спектроскопии и разницы в зарядах методом капиллярной изоэлектрической фокусировки.
Анти-CD30 полностью человеческие моноклональные антитела 5F11 были первоначально описаны в публикации PСТ WO 03/059282. Аминокислотные и нуклеотидные последовательности тяжелой цепи 5F11 показаны на Фиг.1, а аминокислотные и нуклеотидные последовательности легкой цепи 5F11 показаны на Фиг.2. Вариабельные последовательности тяжелых и легких цепей 5F11 были субклонированы в вектор экспрессии. Вариабельную каппа область кДНК 5F11, включая ее сигнальную последовательность и оптимальную последовательность Козака, субклонировали в рамке совместно с постоянной каппа-областью человека. Вариабельную область кДНКтяжелой цепи 5F11, включая ее сигнальную последовательность и оптимальную последовательность Козака, субклонировали в рамке совместно с постоянной тяжелой областью человека γ1. Экспрессию тяжелых и легких цепей осуществляли с помощью промоторов убиквитина С человека (Nenoi, M. et al. Gene 175:179, 1996). Этот вектор экспрессии более подробно описан в американской патентной заявке No. 60/500,803, содержание которой явным образом включено сюда по ссылке.
Вектор экспрессии перенесли в FUT8-/- клеточную линию-носитель Ms704 с помощью электропорации ДНК. Линию Ms704 FUTS-/- создали направленным разрушением гена FUT8 в клетках CHO/DG44 с помощью двух замещающих векторов, что более подробно описано в американской патентной заявке U.S. 20040110704 авторами Amane et al., а также в работе Yamane-Ohnuki et al. (2004) Biotechnol Bioeng S7:614-22. Клетки Ms704 адаптировали для роста в культуре суспензии в среде роста EX-CELL™ 325 PF СНО среде (JRH #14335), в которой дополнительно растворили 100 мкМ гипоксантина и 16 мкМ тимидина (Invitrogen #11067-030), а также 6 мМ L-глутамина (Invitrogen #25030-OS1).
Используемый для электропорации вектор ДНК осадили этанолом и ресуспендировали в 10 мМ Tris 7,6, 1 мМ EDTA. 1,5, 10, 15 или 20 мкг ДНК использовали для двадцати электропорации, по четыре электропорации на каждую концентрацию ДНК. Клетки Ms704 приготовили для трансфекции, промыв клетки в буферном растворе с сахарозой (SBS) и ресуспендировав их в растворе SBS в концентрации 1×107 клеток/мл. 400 мкл суспензии клеток смешали с конструктом ДНК и электропорировали со следующими настройками прибора: напряжение 230 В, емкость 400 мкф и сопротивление 13 Ом (ВТХ Molecular Delivery Systems #600 клеточный электроманипулятор). Клетки извлекли из кювет для электропорации, после чего к ним добавили 20 мл среды роста. После этого их поместили в 96-луночные планшеты по 200 мкл клеток на лунку, приблизительно, 4×104 клеток на лунку. Через два дня после электропорации из каждой лунки извлекли по 150 мкл среды и заменили ее на 150 мкл среды селекции и среды роста, содержащей 400 мкг/мл G418(lnvitrogen #10131-035). Каждые три-семь дней по 150 мкл среды селекции на лунку заменяли свежей средой. Клетки-носители СНО DG44 (FUT 8+/+) электропорировали идентичным конструктом 5F11 с помощью такой же процедуры, так получили трансфектанты СНО DG44, экспрессирующие рекомбинантные антитела 5F11, которые содержали фукозилированные углеводы.
Наиболее продуктивные клоны Ms704 и СНО DG44 размножили, и рекомбинантные антитела 5F11 выделили из супернатантов клеточной культуры аффинной хроматографией с Протеином А.
Сравнительный анализ N-связанных олигосахаридов, полученных из образцов анти-CD30 моноклональных антител, которые были выделены из клеточных линий Ms704 и СНО DG44, выполнили методом капиллярного электрофореза с детекцией флуоресценции, индуцированной лазером (cLIF) (Chen и Evangelista (1998), Electrophoresis 15:1892)). N-связанные олигосахариды очищенных антител выделили, добавив пептид N-гликаназу (Prozyme) и инкубировав систему в течение ночи. Протеин осадили этанолом, а супернатант, содержащий углеводы, перенесли в новую пробирку и высушили с помощью приспособления Speedvac. Углеводы ресуспендировали и дериватизировали с помощью 8-аминопирен-1,3,6-трисульфоната (8-aminopyrene-l,3,6-trisulfonate (APTS)) в условиях мягкого восстановительного аминирования, при котором влияние дезаллилирования и отщепления остатков фукозы сведено к минимуму. Аддукты реакции анализировали методом капиллярного электрофореза с детекцией флуоресценции, индуцированной лазером (Beckman Coulter) (Ma и Nashabeh (1999) Anal. Chem. 71:5185). Между антителами, полученными из клеточной линии Ms704 и из клеточной линии СНО DG44, обнаружили различия в профиле олигосахаридов; эти различия хорошо согласовывались с отсутствием остатков фукозы у анти-CD30 антител, выделенных из линии Ms704.
Чтобы подтвердить отсутствие остатков фукозы у антител, экспрессированных в клетках Ms704, выполнили композиционный анализ моносахаридов. Результаты такого анализа представлены далее в Таблице 1:
Результаты анализа моносахаридов подтверждают, что у экспрессирующихся в клетках Ms704 антител отсутствуют остатки фукозы.
Если не считать различия в олигосахаридов, продемонстрированного методом капиллярного электрофореза и анализом моносахаридов, образцы протеинов анти-CD30 антител, полученных из клеток Ms704 и СНО DG44, были идентичны. Анализ N-терминальных последовательностей протеинов показал, что эти последовательности идентичны. Масс-спектроскопия легких цепей анти-CD30 антител, производных от Ms704 и СНО DG44 показала массы 23,740 и 23,742, соответственно, что укладывается в инструментальную ошибку. Оба антитела протестировали с помощью стандартного капиллярного изоэлектрического фокусирующего набора (Beckman Coulter), результаты анализа показывают, что оба образца антитела характеризуются идентичными изоэлектрическими точками со значением 8,6. Проведенные анализы позволяют заключить, что образцы антител из клеток Ms704 и СНО DG44 практически идентичны, за исключением дефукозилирования углеводного компонента антител из Ms704.
Пример 2. Анализ активности ADCC дефукозилированных анти-CD30 антител
Анти-CD30 моноклональные антитела 5F11 способны убивать CD30+клетки за счет популяции эффекторных клеток, что осуществляется с помощью зависящей от антител клеточной цитотоксичности (ADCC). В этом примере дефукозилированные 5F11 (defuc-5F11) моноклональные антитела проверили на способность убивать клетки CD30+ линий в присутствии эффекторных клеток. Эта проверка осуществлялась с помощью анализа цитотоксичности по высвобождению хрома.
Эффекторные клетки человека выделили из цельной крови следующим образом. Моноядерные клетки человеческой периферической крови выделили из гепаринизированной цельной крови стандартным методом разделения Ficoll-paque. Клетки ресуспендировали в среде RPMI1640, содержащей 10% FBS и 200 ед/мл IL-2 человека, а затем одну ночь инкубировали при температуре 37°C. На следующий день клетки собрали, однократно промыли культуральной средой и ресуспендировали в концентрации 1×107 клеток/мл. Два миллиона клеток CD30+ инкубировали с 200 µCi 51Cr в 1 мл общего объема в течение часа при 37°C. Затем клетки мишени промыли один раз, ресуспендировали в 1 мл среды и еще 30 минут инкубировали при 37°C. После заключительной инкубации клетки мишени промыли еще один раз и разбавили, получив 1×105 клеток/мл.
CD30+ клеточные линии L540 (лимфома Ходжкина человека; DSMZ Deposit No. ACC 72), L428 (лимфома Ходжкина человека; DSMZ Deposit No. АСС 197), L1236 (лимфома Ходжкина человека; DSMZ Deposit No. ACC 530) и Karpas (лимфома Т-клеток человека; DSMZ Deposit No. ACC 31) сначала проверили на связывание фукозилированных 5F11 (fuc-5F11) и defuc-5F11 стандартным анализом FACS. Все клеточные линии мишеней продемонстрировали сходные профили связывания в интервале концентраций антител для fuc-5F11 и defuc-5F11. Уровень экспрессии CD30, рассчитанный по средней интенсивности флуоресценции, был наибольшим для L540, за ним следовали Karpas, L428, наименьшая экспрессия CD30 отмечена для клеток L1236.
Клетки L540, L428, L1236 и Karpas протестировали в модифицированном использующим 51Cr анализе зависящей от антител клеточной цитотоксичности (ADCC). Это сделали следующим образом. Каждую линию клеток-мишеней (100 мкл меченых клеток CD30+) проинкубировали с 50 мкл эффекторных клеток и 50 мкл антител. В экспериментах использовали отношение мишень:эффектор, равное 1:50. Во всех экспериментах выполняли также следующие отрицательные контроли: а) клетки мишени и эффекторные клетки без антител; b) клетки мишени без эффекторных клеток; с) лунки, содержащие клетки мишени и эффекторные клетки в присутствие 1% Triton Х-100, и d) человеческий изотипный контроль IgG1. Через 4 часа инкубации при 37°C супернатанты собрали и перенесли в счетчик гамма-излучения (Cobra II производства Packard Instruments) с окном регистрации 240-400 кЭв. На графике изобразили счет за минуту как функцию концентрации антител, и проанализировали данные методом нелинейной регрессии с сигмоидальным доза-ответом (вариабельный наклон) с помощью программного обеспечения Prism (San Diego, CA). Кривые клеточной цитотоксичности для линий L540, L428, L1236 и Karpas и для различных концентраций fuc-5F11 и defuc-5F11 показаны на Фиг.7-10, соответственно. Процент лизиса определили по следующему уравнению:
% лизиса=(СРМ образца - СРМ без антител)/(СРМ TritonX - СРМ без антител)×100
% лизиса определяли для концентрации антитела 25 мкг/мл и отношению клеток мишени к эффекторным клеткам, равному 1:50. Для каждой линии клеток-мишеней рассчитали также значения EC50. Результаты приводятся в следующей далее Таблице 2.
ни
ни
В случае клеток defuc-5F11 процент лизиса был от 1,61 раз (для клеток L540) до 3,25 раз (для клеток L1236) больше, чем для антител линии fuc-5F11. Повышенная эффективность defuc-5F11 приводит к заметному лизису клеток в условиях, при которых fuc-5F11 не проявляет заметного эффекта. Например, в случае клеток L1236, характеризующихся низким уровнем экспрессии CD30, defuc-5F11 при концентрации 0,1 мкг/мл вызывает 10% специфический лизис, fuc-5F11 в той же концентрации не проявляет заметного эффекта (см. Фиг.9). ADCC активность defuc-5F11 была от 4,7 раз (клетки L540) до 27,1 раз (клетки L1236) более мощной, чем в случае антитела fuc-5F11, что видно по отношению из значений EC50.
Пример 3: Анализ активности ADCC анти-CD30 антител
В этом примере анти-CD30 моноклональные антитела протестировали на способность убивать клетки линии CD30+ в присутствии эффекторных клеток по механизму зависящей от антител клеточной цитотоксичности (ADCC). Исследование проводилось с помощью флуоресцентного анализа цитотоксичности. Человеческие эффекторные клетки приготовили, как описано выше, метод анализа ADCC также был описан ранее. Как видно из Фиг.13, при использовании дефукозилированных анти-CD30 антител ADCC-активность возрастала, по сравнению с аналогичным показателем родительского антитела. Кроме того, дефукозилированные анти-CD30 антитела оказались более активными, по сравнению с родительскими антителами, так как EC50 для них был меньше, чем в случае родительских анти-CD30 антител. Антитела оказались также более эффективными, поскольку максимальный процентлизиса для дефукозилированных анти-CD30 антител был выше. В случае любого антитела, анти-CD16 (3G8) антитела эффективно ингибировали ADCC, показывая, что этот лизис был опосредован CD16.
Пример 4: Усиление ADCC в присутствии человеческих эффекторных клеток
Анализы ADCC выполнялись, как описано выше. В этом эксперименте, однако, эффекторные клетки мыши сравнили с эффекторными клетками человека. Как видно из Фиг.14, при использовании мышиных эффекторных клеток между родительскими и дефукозилированными анти-CD30 антителами не наблюдалось различия в ADCC. В то же время, при использовании человеческих эффекторных клеток наблюдалось заметное повышение ADCC для дефукозилированных антител, по сравнению с родительскими анти-CD30 антителами.
Пример 5: Сравнение методом ADCC анализа родительских и дефукозилированных антител при использовании эффекторных клеток мартышек cynomolgus
У мартышек cynomolgus взяли цельную кровь. Периферическую кровь этих мартышек с лизированными красными кровяными клетками стимулировали 50 ед/мл rIL-2 и инкубировали в среде RPMI1640, содержащей 10% FBS, в течение ночи при 37°С. В день эксперимента клетки ресуспендировали в буфере анализа (RPMI1640, 10% FBS, 2,5 мМ пробенецида) до концентрации 1×107 клеток/мл. CD30-положительные клетки мишени, Karpas 299, пометили, трижды промыли промывочным буфером (PBS, 2,5 мМ пробенецида, 20 mM HEPES) и довели до концентрации 1×105 клеток/мл, чтобы добиться отношения их содержания к концентрации эффекторных клеток 1:50. ADCC анализ выполнили, как описано выше. Мы сравнили активность родительских анти-CD30 антител с дефукозилированными антителами, используя эффекторные клетки, выделенные из крови cynomolgus. В случае родительских антител наблюдалась умеренная активность (начиная от, приблизительно, 7-10% лизиса при концентрации 10 мкг/мл). Напротив, дефукозилированные антитела индуцировали значительно более высокий процент лизиса (начиная от, приблизительно, 10-30% лизиса при концентрации 10 мкг/мл), они характеризовались также сниженными значениями EC50 (см. Фиг.15).
Пример 6: Анализ Скэтчарда сродства связывания анти-CD30 моноклональных антител по отношению к клеткам L540, активированным клетками периферической крови человека и cynomolgus
Мы определили сродство связывания для родительских и дефукозилированных анти-CD30 антител. Мы сравнили сродство связывания двух этих антител с CD30-положительными клетками L540, а также с моноядерными клетками периферической крови человека и cynomolgus, активированными РHА/Соn А.
Клетки периферической крови человека и cynomolgus стимулировали 2 мкг/мл РНА, 10 мкг/мл Con А, и 50 ед/мл rIL-2, после чего 3 дня выдерживали в среде RPMI1640, содержащей 10% фетальной бычьей сыворотки (fetal bovine serum (FBS)), при концентрации 1×106 клеток/мл. В день эксперимента клетки промыли и довели до концентрации 2×107 клеток/мл в буфере связывания (RPMI1640+10% FBS). В качестве контроля использовали CD30-положительные клетки L450 (доведенные до концентрации 4-8×106 клеток/мл). Такой выбор контроля был сделан потому, что эти клетки экспрессируют большое количество антигена. Клетки хранили на льду до начала эксперимента. Планшеты со стекло-волоконным фильтром от Millipore (MAFBNOB50) покрыли 1% обезжиренным сухим молоком в воде и одну ночь хранили при температуре 4°С Планшеты трижды промыли 0,2 мл буфера связывания. Для определения максимального связывания в соответствующие ячейки добавили по 50 мкл одного буфера (общее связывание). В контрольные ячейки добавили по 25 мкл одного буфера. Во все ячейки добавили также различные концентрации антител 125I-анти-CD30 в объеме 25 мкл. В контрольные ячейки добавили различные концентрации немеченых антител при 300-400-кратном избытке в объеме 25 мкл (неспецифическое связывание), а во все остальные ячейки добавили по 25 мкл CD30-положительных клеток L540 или стимулированных клеток периферической крови человека и cynomolgus в буфере связывания. Планшеты 2 часа инкубировали на шейкере при скорости вращения 200 RPM и температуре 4°С По завершении инкубации планшеты Millipore дважды промыли 0,2 мл холодного промывочного буфера (RPMI1640, 10% FBS, 500 мМ NaCl). Фильтры извлекли, и измерили излучение на гамма-счетчике. Расчет равновесного связывания провели с использованием параметров связывания одного сайта программным обеспечением Prism (San Diego, CA).
На основании описанного выше анализа связывания Скэтчарда определили KD родительского анти-CD30 антитела по отношению к клеткам L540. Оно составило, приблизительно, 1,4 нМ. Для дефукозилированных антител KD составляет 1,9 нМ (Таблица 3). Это означает, что при удалении фукозы происходят незначительные изменения сродства. Эксперимент повторили с первичными клетками, а не клеточной линией. Определили также сродство клеток, экспрессирующих значительно меньшее количество рецепторов. Активированные клетки периферической крови человека подготовили, как описано выше. KD составляло 1,1 и 2,7 нМ для родительских и дефукозилированных анти-CD30 антител, соответственно.
Наконец, сравнили сродство связывания родительских и дефукозилированных антител с моноядерными клетками из периферической крови cynomolgus, активированными PHA, Con А и rIL-2. Для родительских и дефукозилированных анти-CD30 антител, соответственно, KD составило, приблизительно, 0,47 нМ и 0,83 нМ.
ные CD30
Эквиваленты
Компетентные в соответствующей области специалисты смогут придумать или установить, проведя рутинные эксперименты, множество эквивалентов описанных здесь конкретных аспектов изобретения. Эти эквиваленты входят в область действия следующей далее формулы изобретения.
зародышевые линии
зародышевые линии
зародышевые линии
зародышевые линии
| название | год | авторы | номер документа |
|---|---|---|---|
| ВЫДЕЛЕННОЕ АНТИТЕЛО ПРОТИВ СПЕЦИФИЧЕСКОГО МЕМБРАННОГО АНТИГЕНА ПРОСТАТЫ (PSMA) И СПОСОБ ИНГИБИРОВАНИЯ РОСТА КЛЕТОК, ЭКСПРЕССИРУЮЩИХ PSMA | 2006 |
|
RU2421466C2 |
| СПОСОБЫ РАЗРУШЕНИЯ КЛЕТОК С ИСПОЛЬЗОВАНИЕМ ЭФФЕКТОРНЫХ ФУНКЦИЙ АНТИ-EphA4 АНТИТЕЛ | 2007 |
|
RU2429246C2 |
| НОВЫЕ АНТИ-CLDN18.2 АНТИТЕЛА | 2020 |
|
RU2830887C2 |
| АНТИ-LRP6 АНТИТЕЛА | 2011 |
|
RU2587625C2 |
| АНТИ-ТАТ226 АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ | 2007 |
|
RU2448980C2 |
| АНТИ-ICOS АНТИТЕЛА | 2017 |
|
RU2764548C2 |
| АНТИ-CD40-АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2012 |
|
RU2609647C2 |
| Анти-LAG-3 антитела | 2016 |
|
RU2760582C2 |
| АНТИ-ГЛИПИКАН 3-АНТИТЕЛО, ИМЕЮЩЕЕ МОДИФИЦИРОВАННУЮ САХАРНУЮ ЦЕПЬ | 2005 |
|
RU2451030C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ЧЕЛОВЕКА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1 (PD-1) И СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТИ-PD-1-АНТИТЕЛ САМОСТОЯТЕЛЬНО ИЛИ В КОМБИНАЦИИ С ДРУГИМИ ИММУНОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ | 2006 |
|
RU2494107C2 |














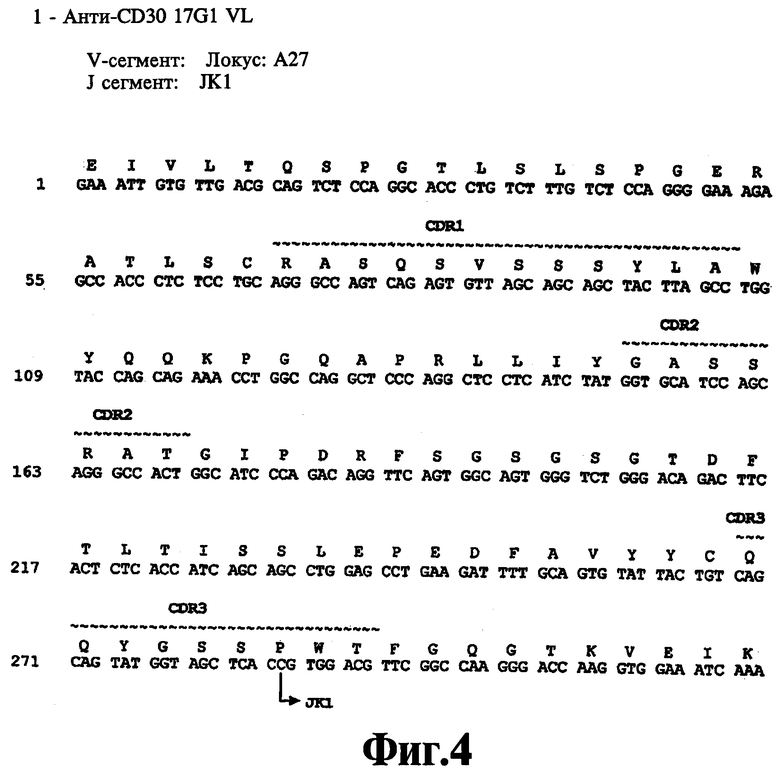
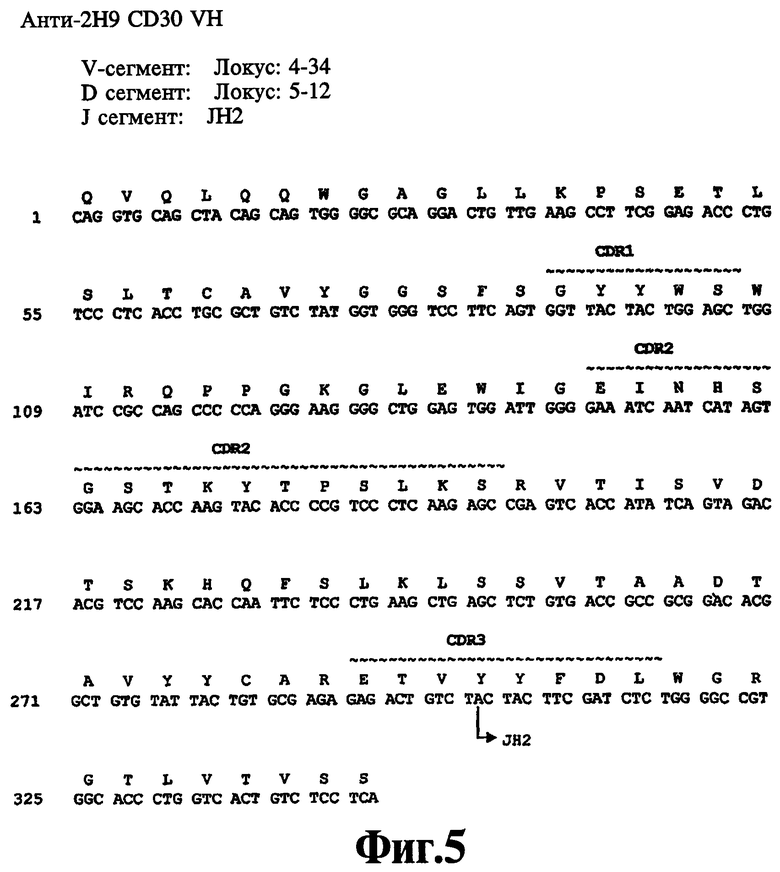
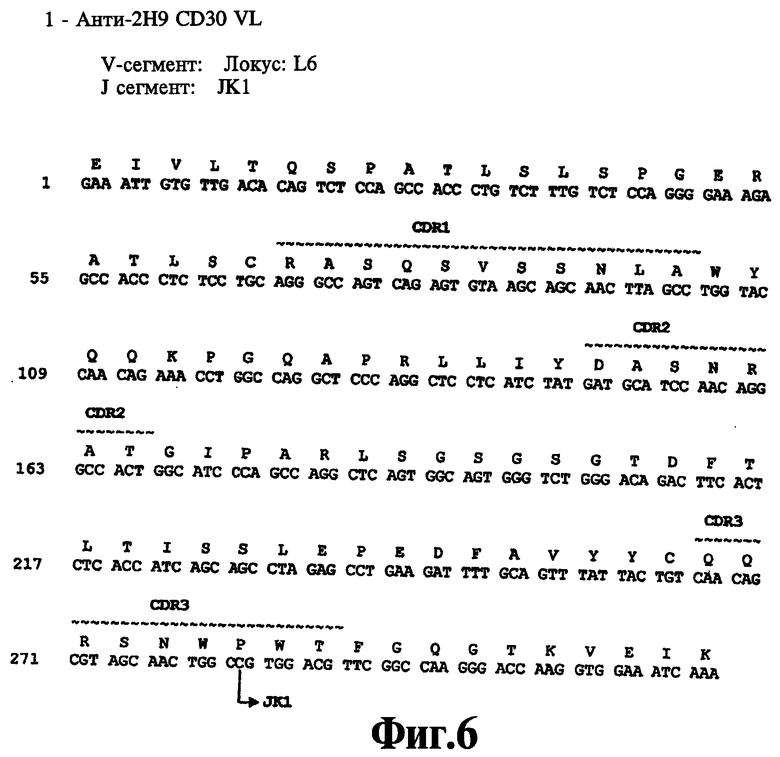
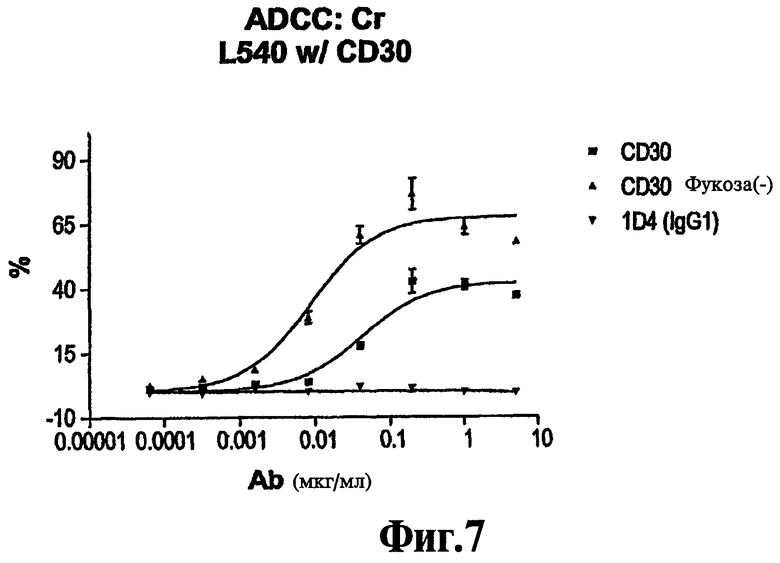
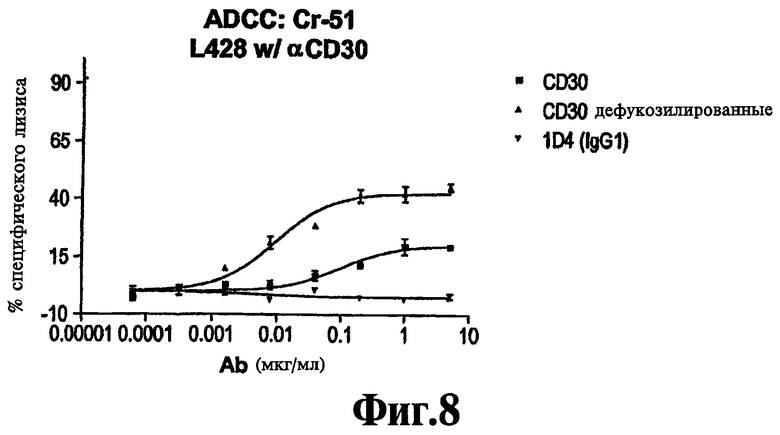
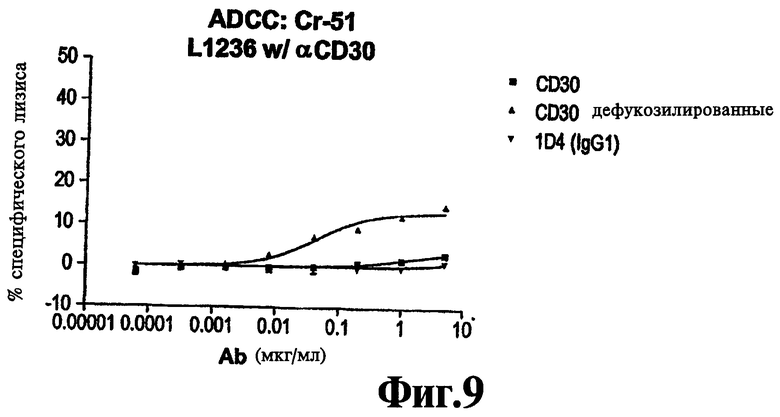
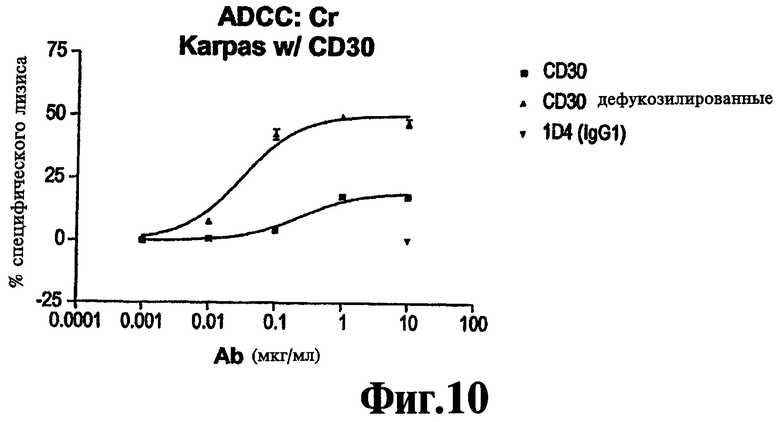


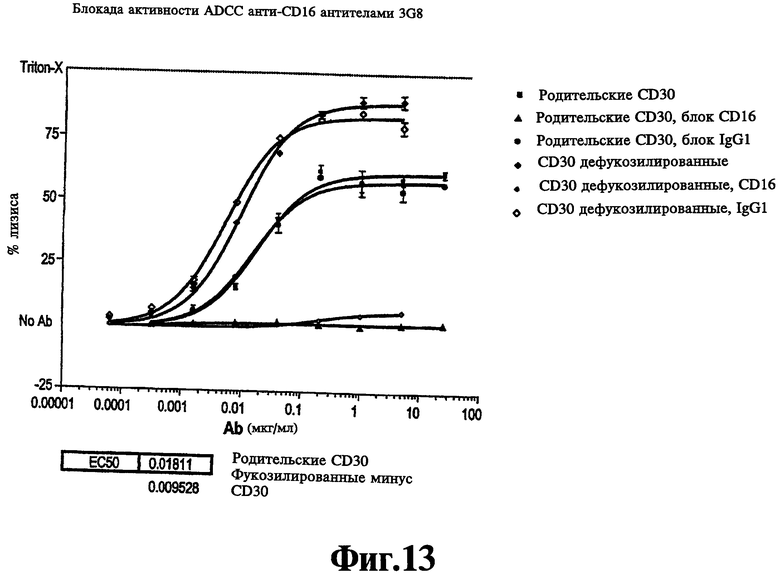

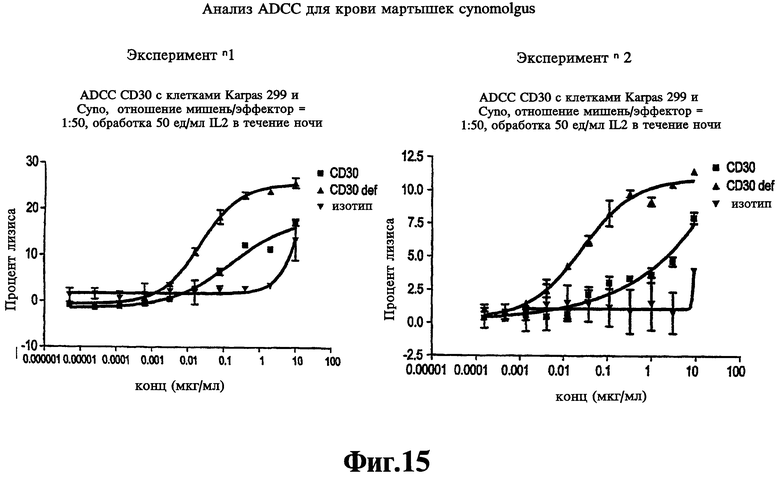
Настоящее изобретение относится к области иммунологии. Предложены варианты выделенного анти-CD30 антитела, по существу свободного от фукозильных остатков. Указанное антитело характеризуется тем, что содержит в одном варианте 3 CDR из тяжелой цепи и три CDR из легкой цепи, а в другом варианте характеризуется наличием вариабельной области тяжелой цепи и вариабельной области легкой цепи. Раскрыта хозяйская клетка, продуцирующая указанное антитело, по существу свободная от фукозилтрансферазы, описан способ ингибирования роста клеток CD30+ и способ ингибирования роста опухолевых клеток, экспрессирующих CD30, использующий антитело. Описаны варианты применения антител для получения химерного или гуманизированного варианта антитела. Антитела настоящего изобретения демонстрируют повышенную ADCC клеточную цитотоксичность, в отношении линий клеток ходжкинской лимформы человека: L428, L540, L1236 и линии T-клеточной лимформы человека: KARPAS, экспрессирующих CD30, которые не лизируются фукозилированной формой антител. 7 н. и 17 з.п. ф-лы, 15 ил., 4 табл., 6 пр.
1. Выделенное анти-CD30 антитело, по существу, свободное от остатков фукозы, включающее вариабельную область тяжелой цепи CDR1, представленную аминокислотной последовательностью SEQ ID NO:7, вариабельную область тяжелой цепи CDR2, представленную аминокислотной последовательностью SEQ ID NO:10, вариабельную область тяжелой цепи CDR3, представленную аминокислотной последовательностью SEQ ID NO:13, вариабельную область легкой цепи CDR1, представленную аминокислотной последовательностью SEQ ID NO:16, вариабельную область легкой цепи CDR2, представленную аминокислотной последовательностью SEQ ID NO:19, и вариабельную область легкой цепи CDR3, представленную аминокислотной последовательностью SEQ ID NO:22.
2. Антитело по п.1, которое представляет собой моноклональное антитело.
3. Антитело по п.1, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов VH 4-34 или VH 3-07 человека.
4. Антитело по п.1, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов Vk L15, А27 или L6 человека.
5. Антитело по п.1, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов VH 4-34 или Vk 3-07 человека, и вариабельную область тяжелой цепи, представляющую продукт или производное генов Vk L15, A27 или L6 человека.
6. Выделенное анти-CD30 антитело, по существу, свободное от остатков фукозы, включающее вариабельную область тяжелой цепи, представленную аминокислотной последовательностью SEQ ID NO:1, и вариабельную область легкой цепи, представленную аминокислотной последовательностью SEQ ID NO:4.
7. Антитело по п.6, которое представляет собой моноклональное антитело.
8. Антитело по п.6, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов VH 4-34 или VH 3-07 человека.
9. Антитело по п.6, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов Vk L15, A27 или L6 человека.
10. Антитело по п.6, которое содержит вариабельную область тяжелой цепи, представляющую продукт или производное генов VH 4-34 или VH 3-07 человека, и вариабельную область тяжелой цепи, представляющую продукт или производное генов Vk L15, А27 или L6 человека.
11. Хозяйская клетка, продуцирующая антитело по любому из пп.1-10, причем указанная клетка, по существу, свободна от фукозилтрансферазы, так что экспрессируемое указанной клеткой анти-CD30 антитело, по существу, свободно от остатков фукозы.
12. Клетка по п.11, которая экспрессирует анти-CD30 антитело, представляющее собой антитело человека.
13. Клетка по п.11, в которой фукозилтрансфераза представляет собой FUT8.
14. Клетка по п.11, которая представляет собой клетку CHO.
15. Способ ингибирования роста клеток CD30+, включающий контактирование указанных клеток с антителом по любому из пп.1-10.
16. Способ по п.15, в котором ингибируют рост опухолевых клеток.
17. Способ по п.15, в котором используют антитело, представляющее собой антитело человека.
18. Способ ингибирования роста экспрессирующих CD30 опухолевых клеток у субъекта, включающий введение субъекту антитела по любому из пп.1-10 в количестве, эффективном для ингибирования роста экспрессирующих CD30 опухолевых клеток у субъекта.
19. Способ по п.18, в котором используют антитело, представляющее собой антитело человека.
20. Способ по п.18, в котором ингибируют рост опухолевых клеток, представляющих собой опухолевые клетки, относящиеся к болезни Ходжкина.
21. Способ по п.18, в котором ингибируют рост опухолевых клеток, представляющих собой опухолевые клетки анапластической крупноклеточной лимфомы (ALCL).
22. Способ по п.18, в котором ингибируют рост опухолевых клеток связанных с болезнью, выбранной из группы, включающей лимфому не Ходжкина, лимфому Буркитта, кожные T-клеточные лимфомы, узелковые мелкоклеточные лимфомы, лимфоцитарные лимфомы, периферические лимфомы T-клеток, лимфомы Леннерта, лимфомы иммунобластов, лейкемии/лимфомы T-клеток (ATLL), лейкемию взрослых T-клеток (T-ALL), фолликулярные раковые лимфомы энтеробластов/центроцитов (cb/cc), диффузные крупноклеточные лимфомы B-типа, T-клеточную лимфому, подобную ангиоиммунобластозной лимфаденопатии (AILD), лимфому взрослых T-клеток (ATL), HIV-ассоциированные лимфомы, связанные с полостью тела, эмбриональные карциномы, недифференцированные карциномы носоглотки (например, опухоль Шминке), болезнь Кастлмана, саркому Капоши, CD30+ Т-клеточные лимфомы и CD30+ B-клеточные лимфомы.
23. Применение антитела по п.1 для получения химерного или гуманизированного варианта анти-CD30 антитела, по существу, свободного от остатков фукозы.
24. Применение антитела по п.6 для получения химерного или гуманизированного варианта анти-CD30 антитела, по существу, свободного от остатков фукозы.
| BORCHMANN et al., "The human anti-CD30 antibody 5F11 shows in vitro and in vivo activity against malignant lymphoma", Neoplasia, 2003, v.102, no.10, стр.3737-3742 | |||
| NIWA et.al., "Defucosylated chimeric anti-CC chemokine receptor 4 IgGl with Enhanced antibody-dependent cellular cytotoxicity shows potent therapeutic activity to cell leukemia and |
Авторы
Даты
2013-09-10—Публикация
2006-02-17—Подача