Текст описания приведен в факсимильном виде.
























































































































































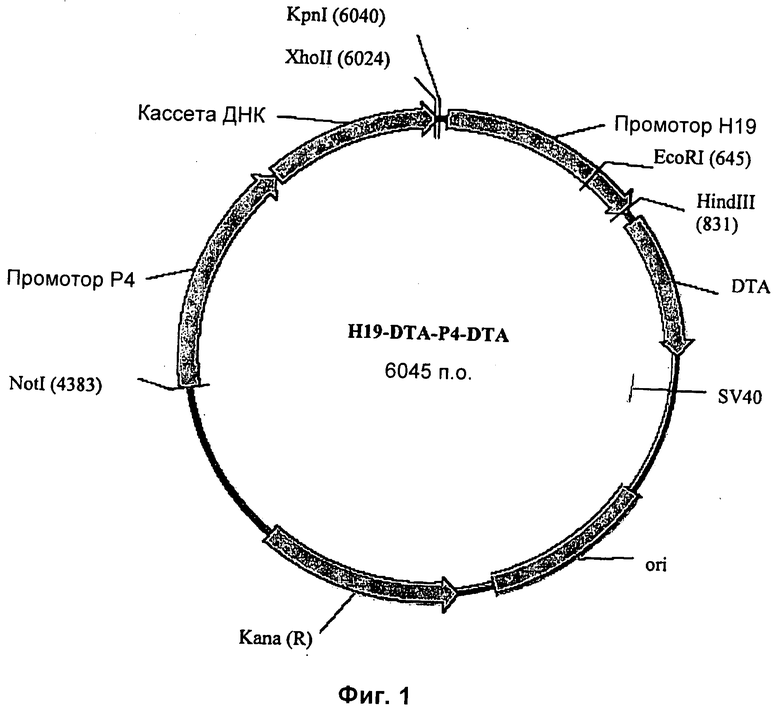
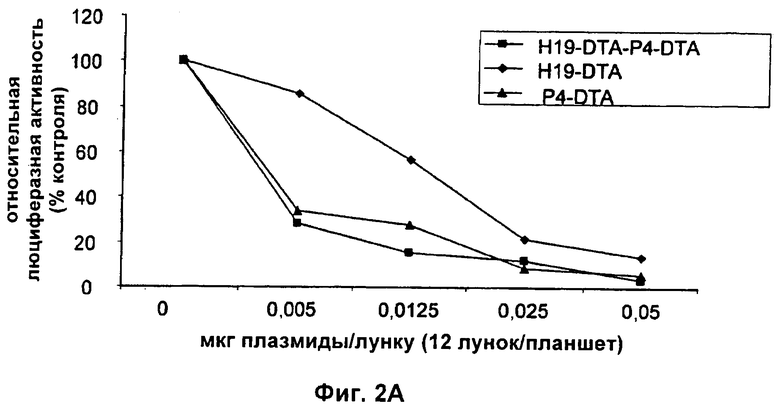
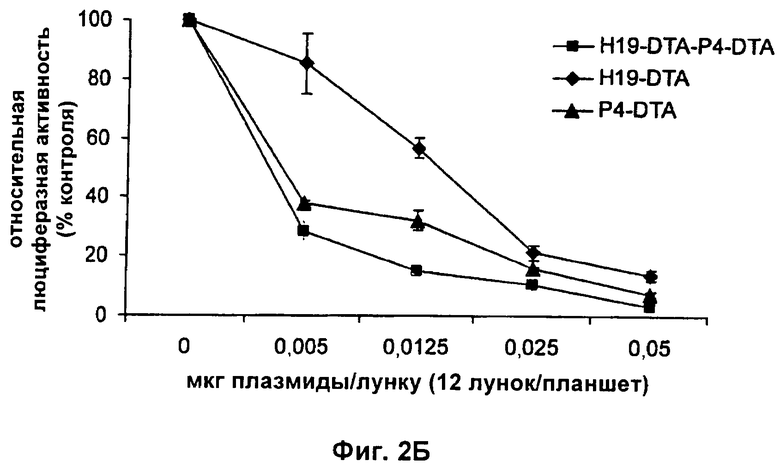
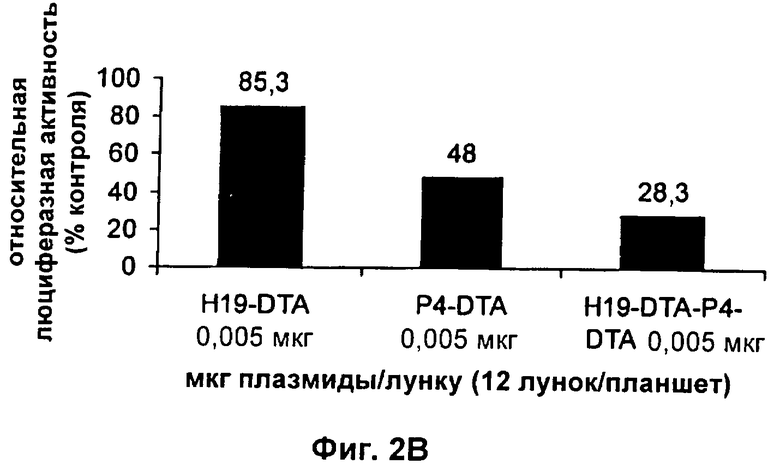
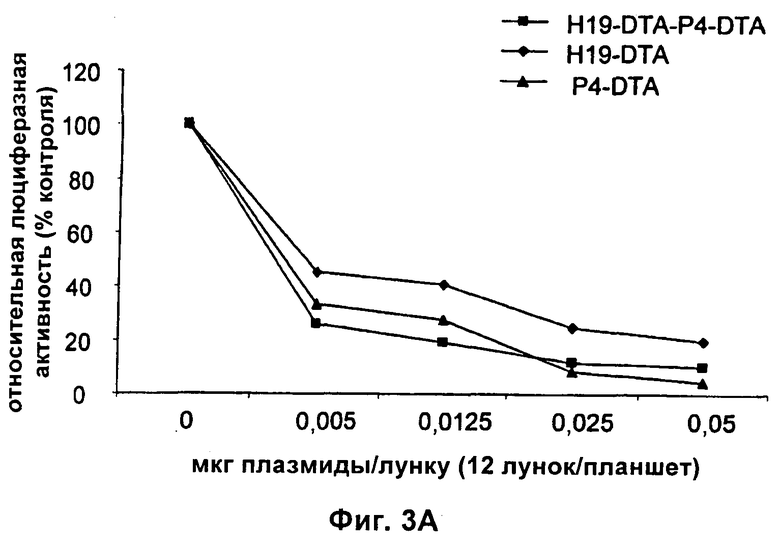
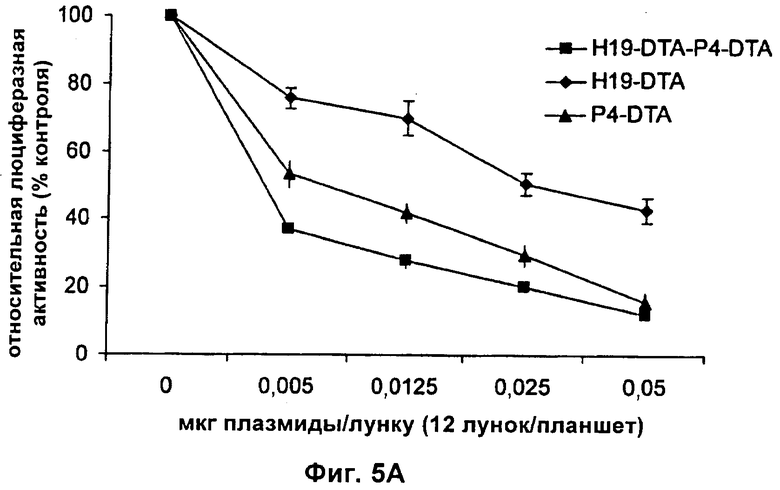
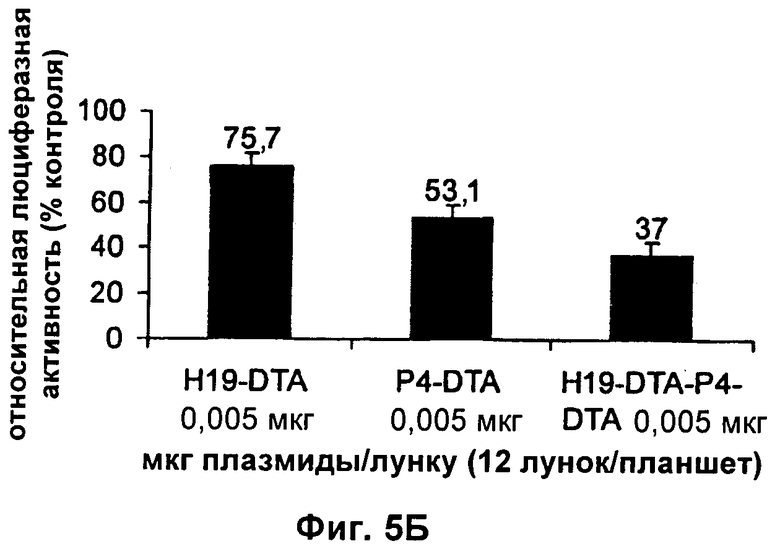
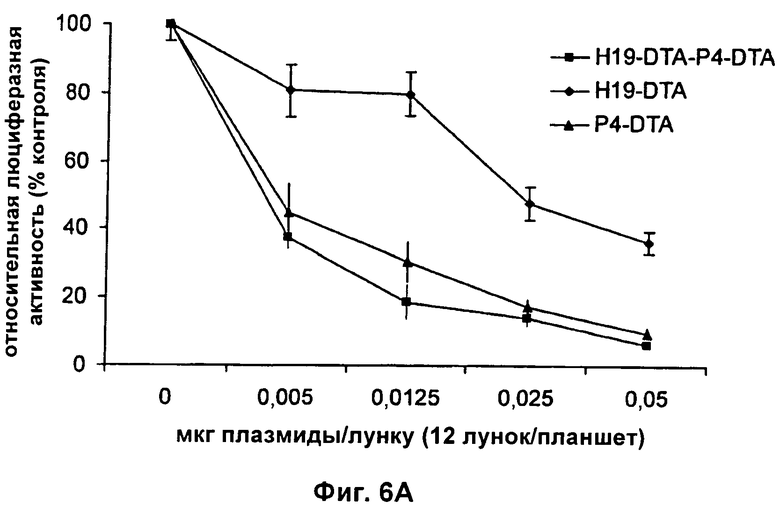
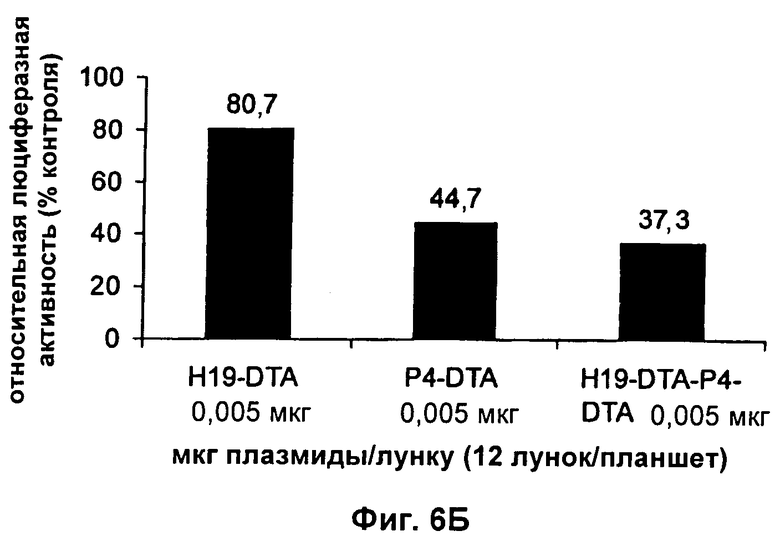
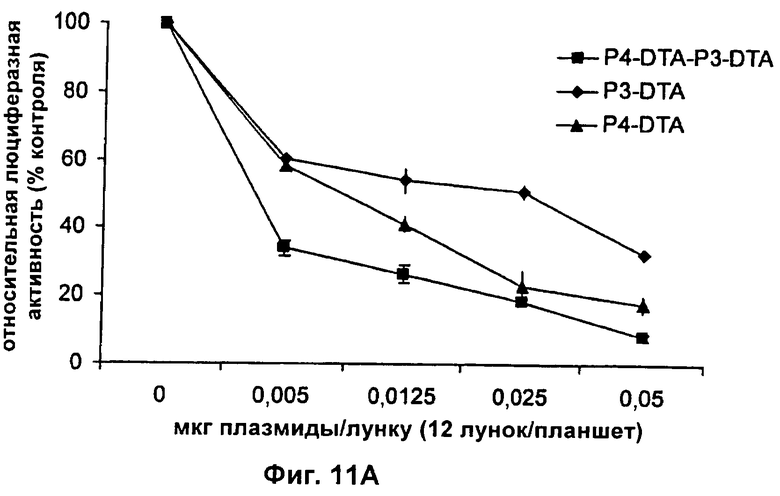
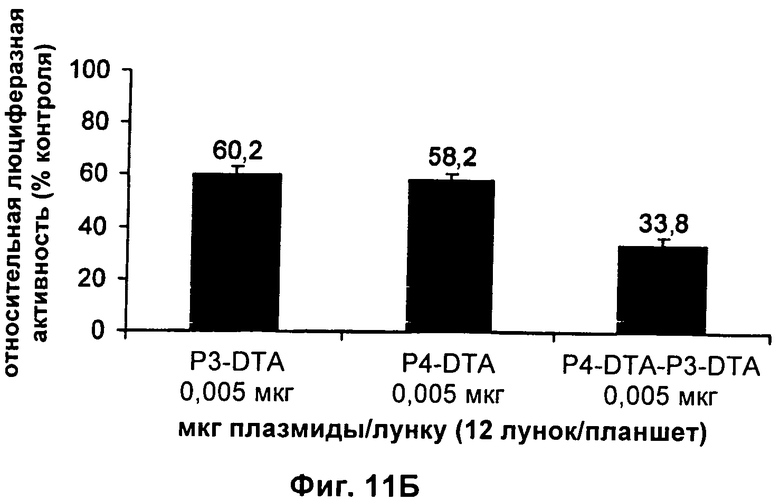
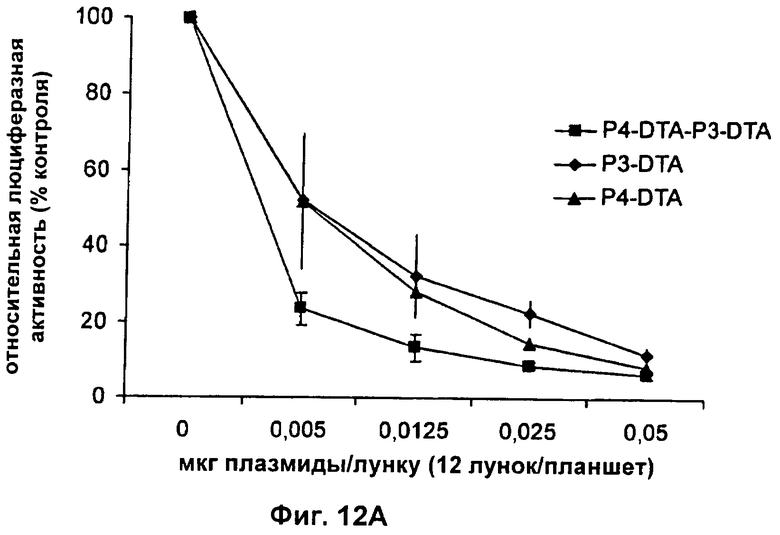
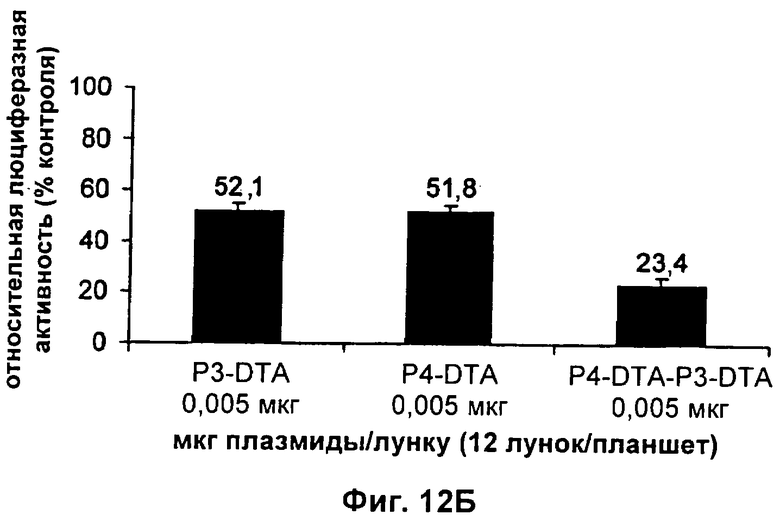
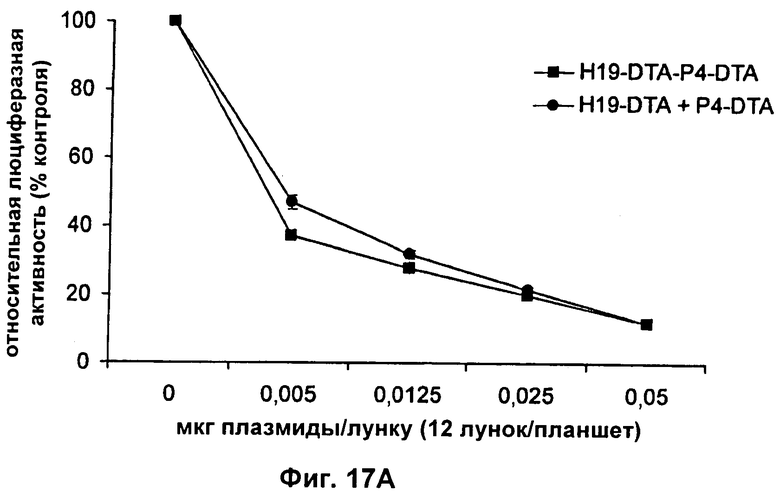
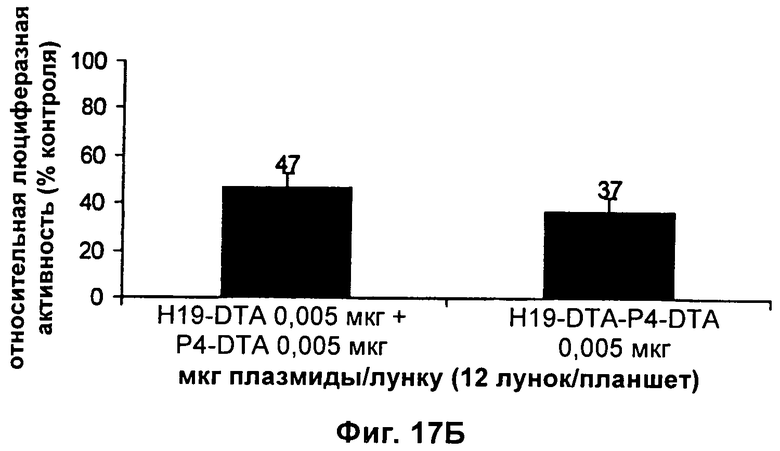
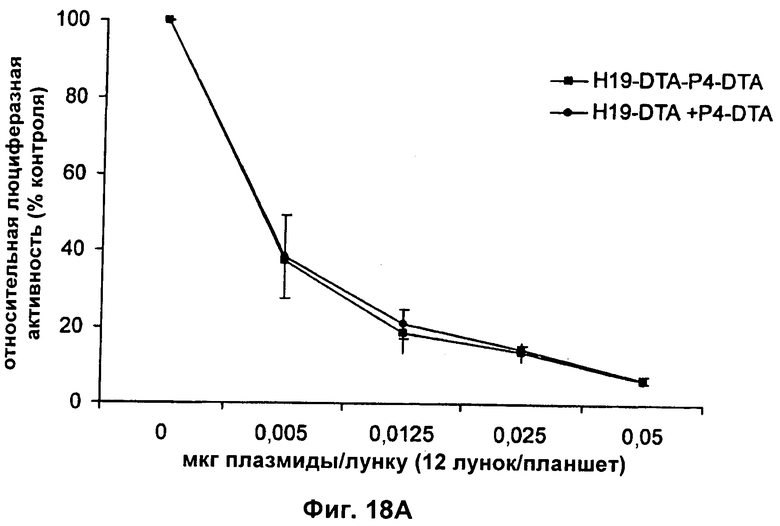
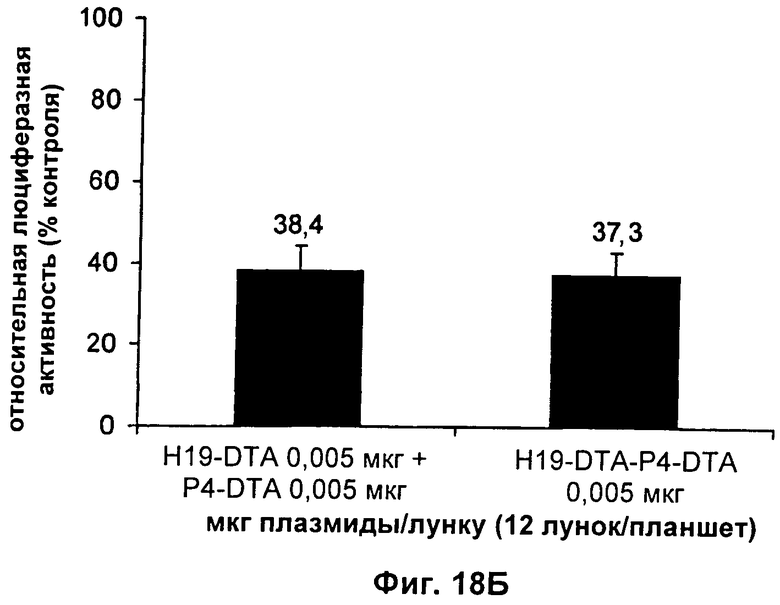
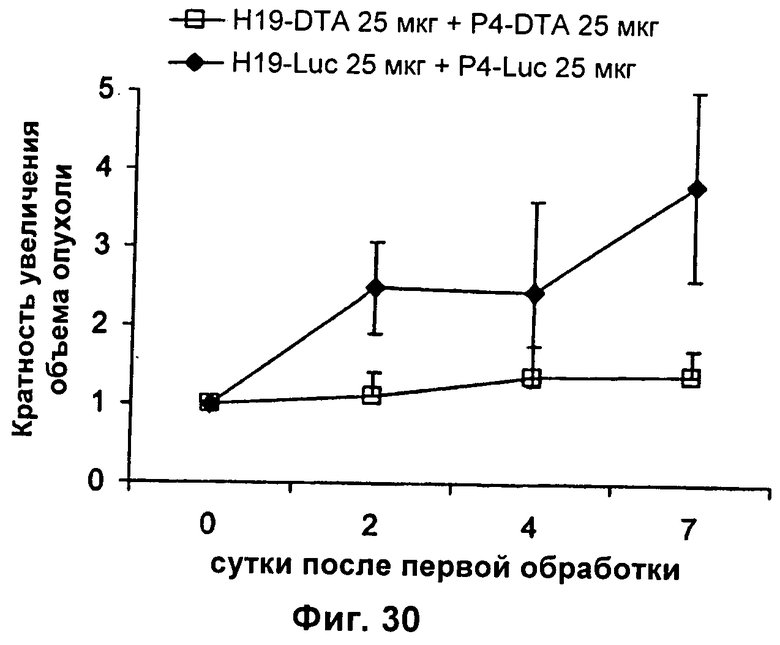
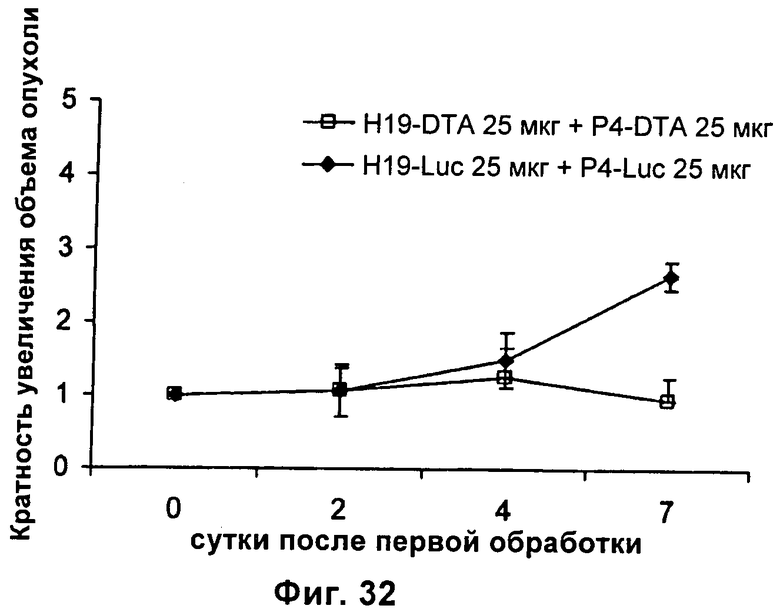
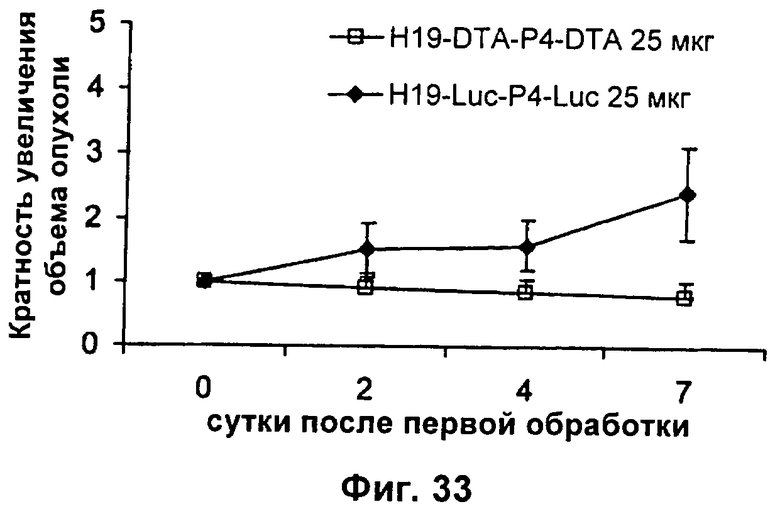
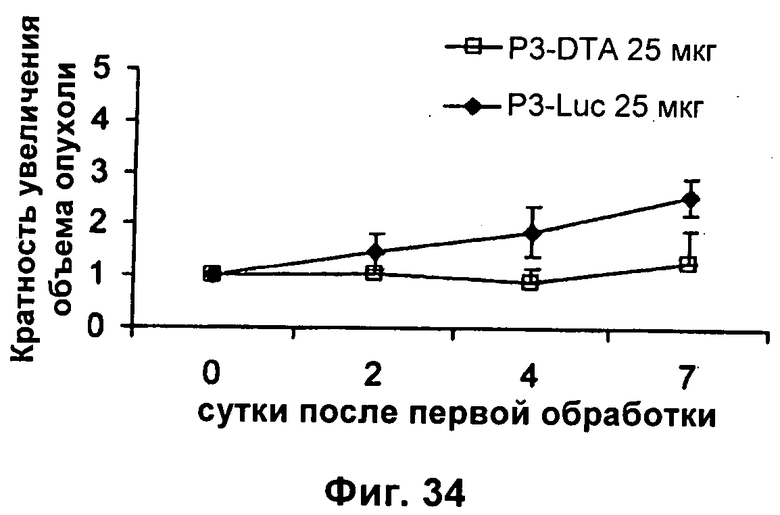
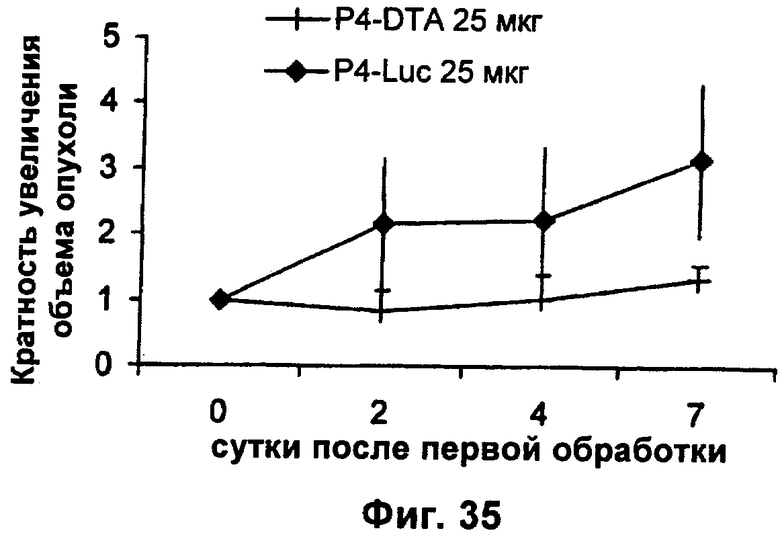
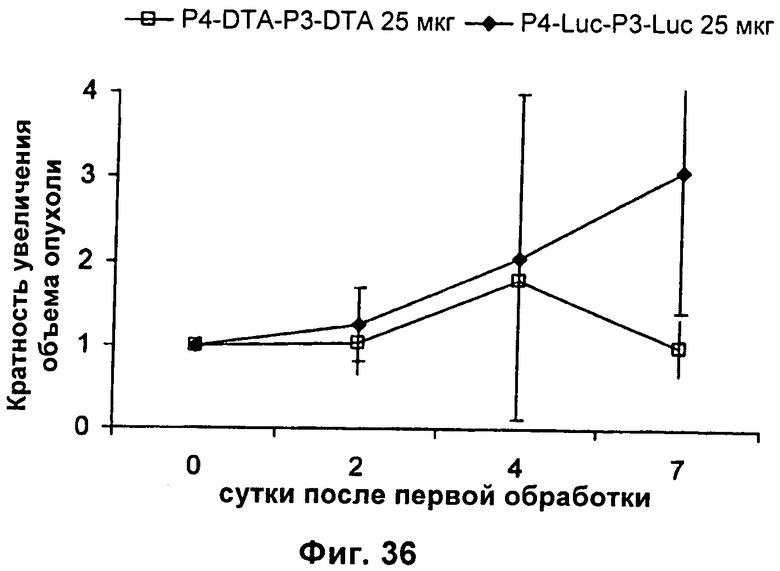
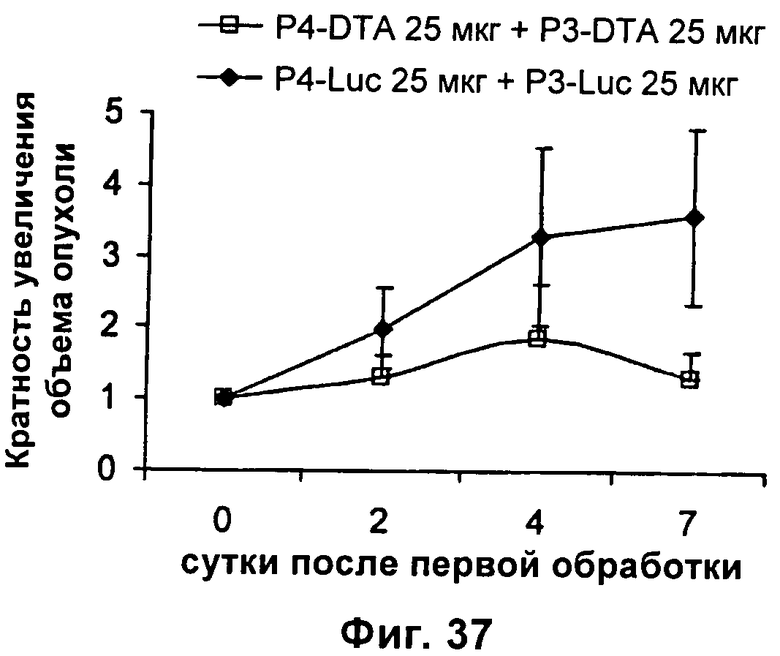
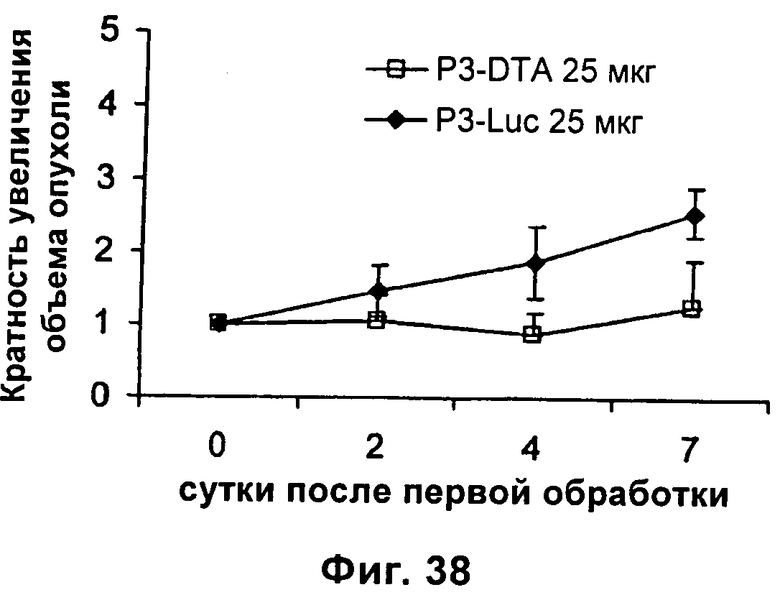
Настоящее изобретение относится к области генной терапии. Предложена конструкция нуклеиновой кислоты для лечения опухолей, содержащая по меньшей мере две открытые рамки считывания, включающие последовательности, кодирующие цитотоксический или цитостатический генный продукт, в частности дифтерийный токсин, функциональным образом связанные с различными опухоль-специфичными промоторами: Н19-специфичным промотором, промотором IGF-II Р3 или Р4. Рассмотрен эукариотический вектор экспрессии, содержащий указанную конструкцию нуклеиновой кислоты, а также способы лечения и ингибирования развития опухоли у субъекта-человека посредством введения конструкции нуклеиновой кислоты по изобретению. Настоящее изобретение может найти дальнейшее применение в терапии рака. 9 н. и 24 з.п. ф-лы, 12 пр., 40 ил.
1. Конструкция нуклеиновой кислоты, полезная для лечения опухолей, содержащая:
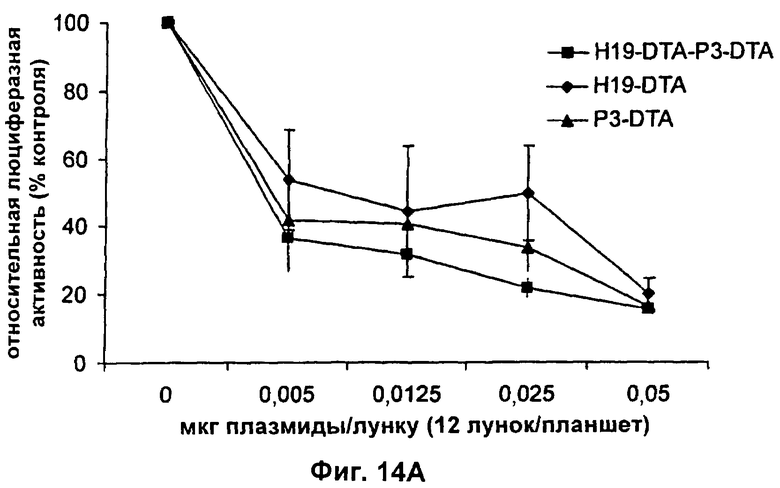
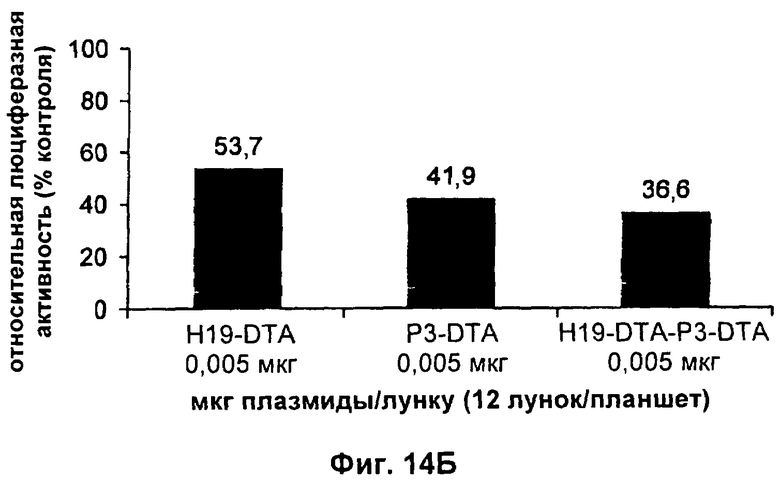
а) первую открытую рамку считывания, кодирующую дифтерийный токсин, причем данная первая открытая рамка считывания связана функциональным образом с Н19-специфичным промотором; и
б) вторую открытую рамку считывания, кодирующую дифтерийный токсин, причем данная вторая открытая рамка считывания связана функциональным образом с промотором IGF-II (инсулиноподобный фактор роста-II), выбранным из последовательностей IGF-II P4 и IGF-II Р3;
или содержащая:
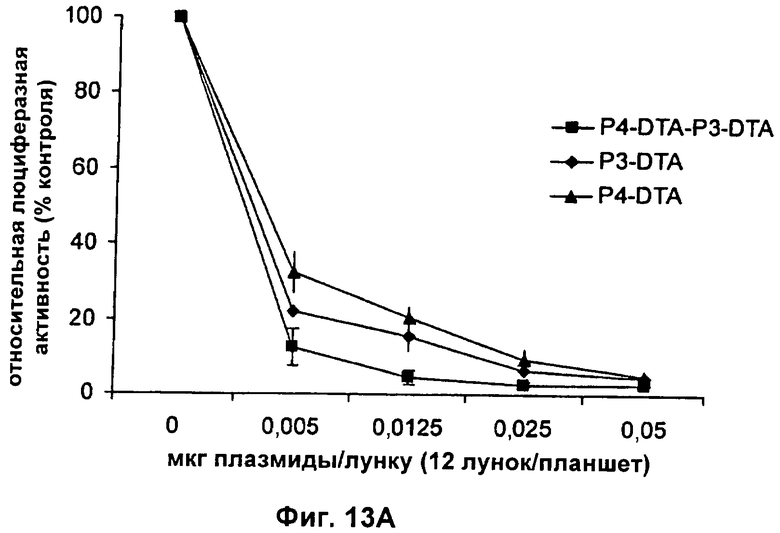
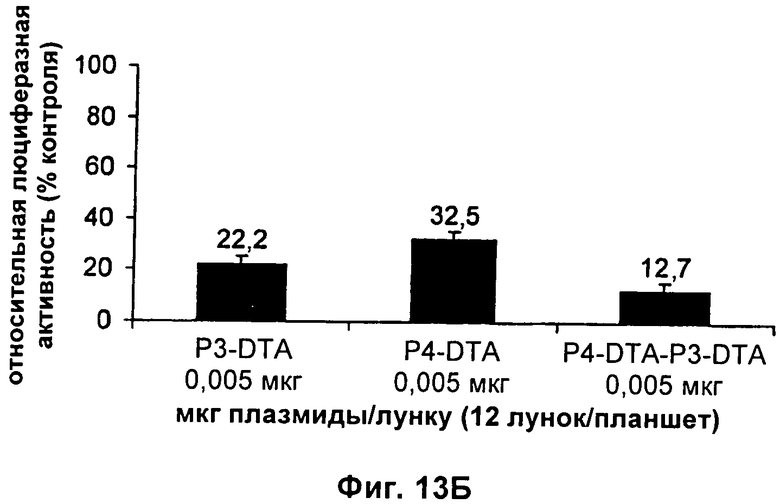
а) первую открытую рамку считывания, кодирующую дифтерийный токсин, причем указанная первая открытая рамка считывания связана функциональным образом с промотором IGF-II Р3; и
б) вторую открытую рамку считывания, кодирующую дифтерийный токсин, причем указанная вторая открытая рамка считывания связана функциональным образом с промотором IGF-II P4.
2. Конструкция нуклеиновой кислоты по п.1, где дифтерийный токсин представляет собой дифтерийный токсин A (DTA).
3. Конструкция нуклеиновой кислоты по п.1, где Н19-специфичный промотор содержит последовательность нуклеиновой кислоты, изложенную в любой из SEQ ID NO:1-2.
4. Конструкция нуклеиновой кислоты по п.1, где указанный промотор IGF-II Р4 содержит последовательность нуклеиновой кислоты, изложенную в SEQ ID NO:9.
5. Конструкция нуклеиновой кислоты по п.1, где указанный промотор IGF-II Р3 содержит последовательность нуклеиновой кислоты, как изложено в последовательности, выбранной из SEQ ID NO:8, SEQ ID NO:12 и SEQ ID NO:17.
6. Конструкция нуклеиновой кислоты по п.1, представляющая собой плазмиду.
7. Эукариотический вектор экспрессии, содержащий конструкцию нуклеиновой кислоты по п.1.
8. Конструкция нуклеиновой кислоты по п.2, где указанный дифтерийный токсин содержит последовательность, как изложено в SEQ ID NO:7.
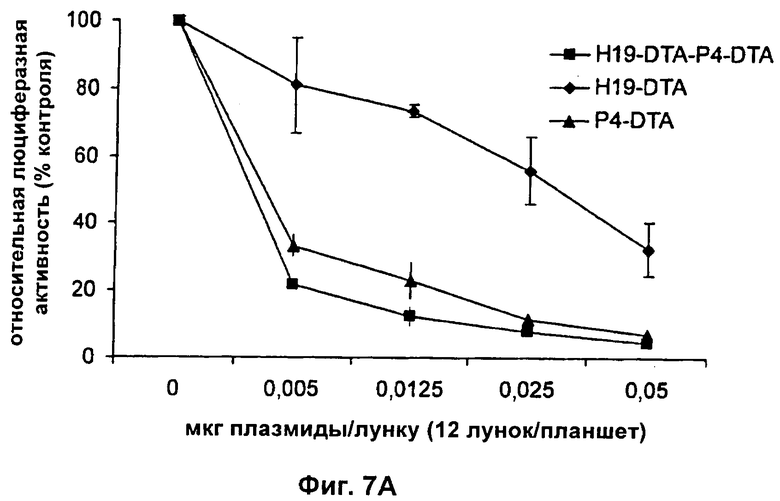
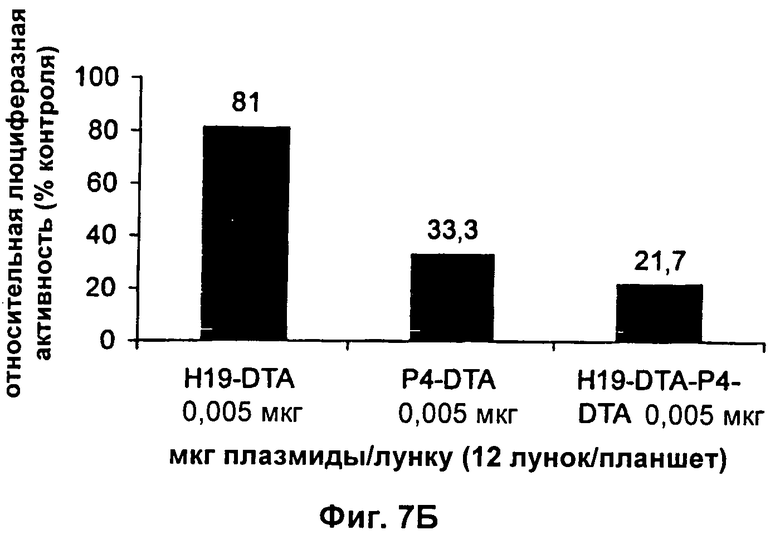
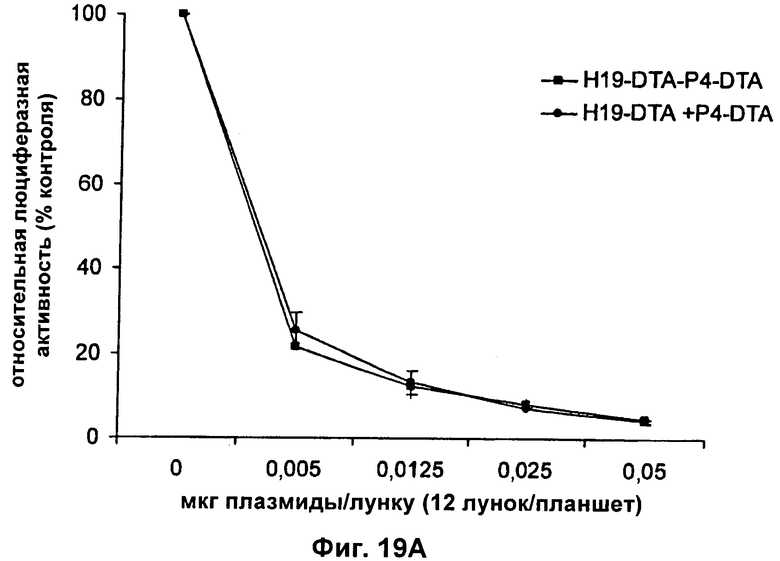
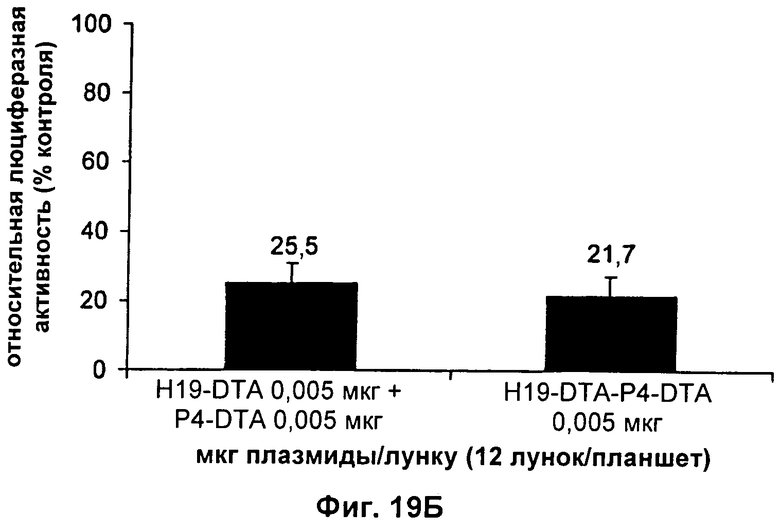
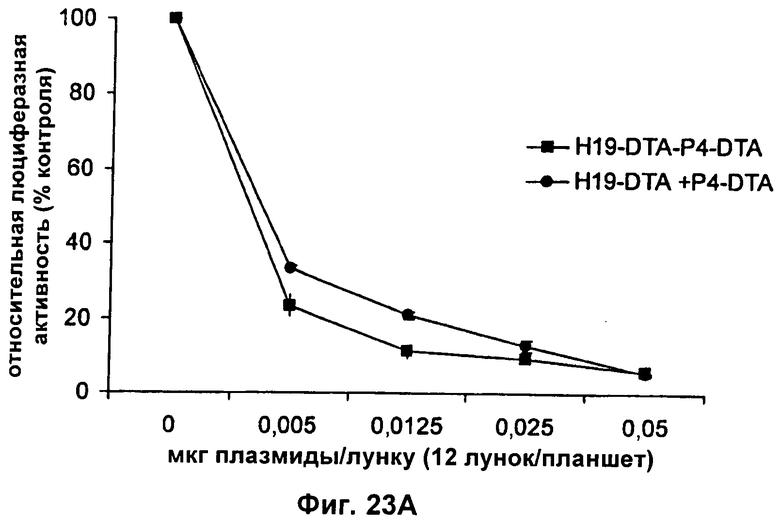
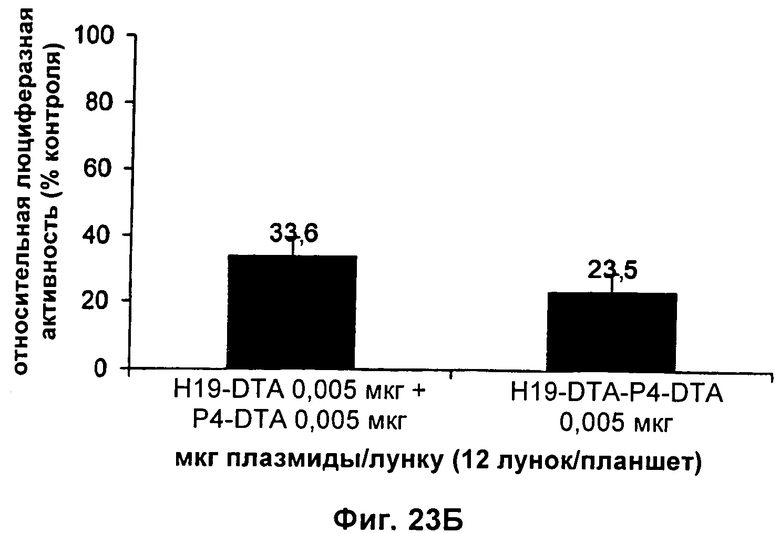
9. Конструкция нуклеиновой кислоты по п.1, где первая открытая рамка считывания связана функциональным образом с Н19-специфичным промотором, и вторая открытая рамка считывания связана функциональным образом с промотором IGF-II Р4.
10. Конструкция нуклеиновой кислоты по п.9, дополнительно содержащая третью открытую рамку считывания, кодирующую дифтерийный токсин, причем указанная третья открытая рамка считывания связана функциональным образом с промотором IGF-II Р3.
11. Конструкция нуклеиновой кислоты по п.1, где первая открытая рамка считывания связана функциональным образом с Н19-специфичным промотором, и вторая открытая рамка считывания связана функциональным образом с промотором IGF-II Р3.
12. Конструкция нуклеиновой кислоты по п.11, дополнительно содержащая третью открытую рамку считывания, кодирующую дифтерийный токсин, причем указанная третья открытая рамка считывания связана функциональным образом с промотором IGF-II Р4.
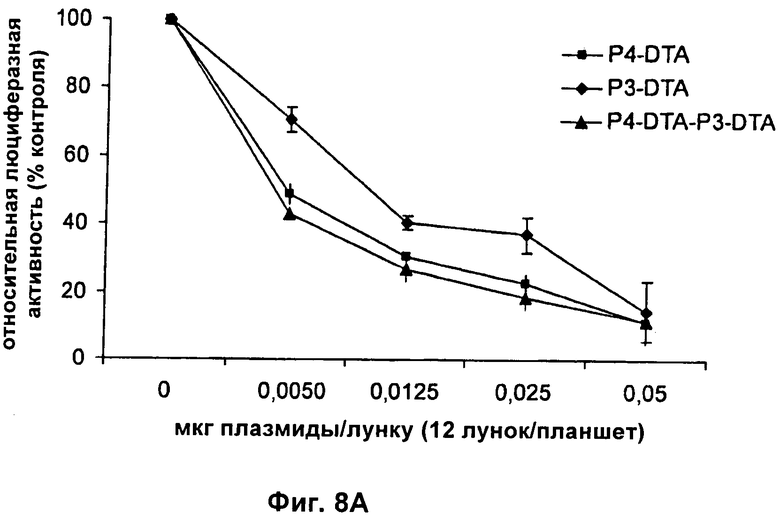
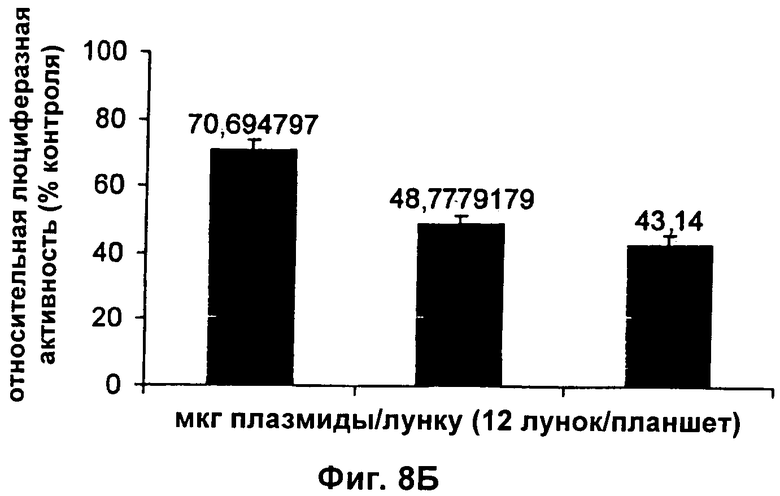
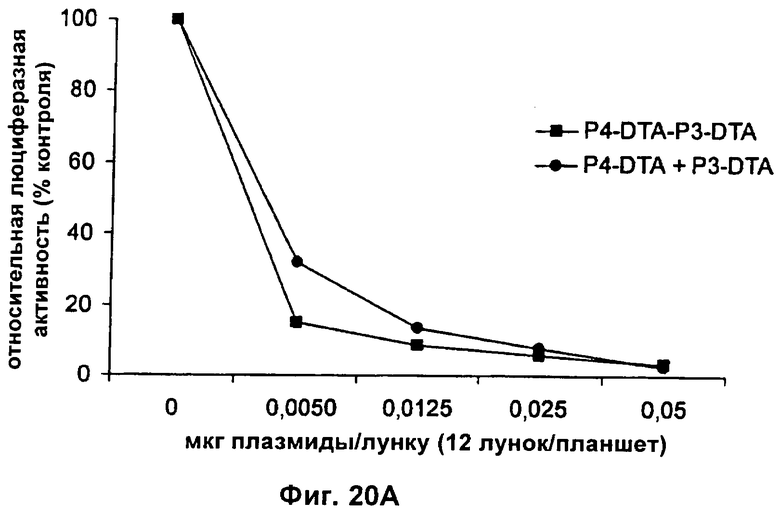
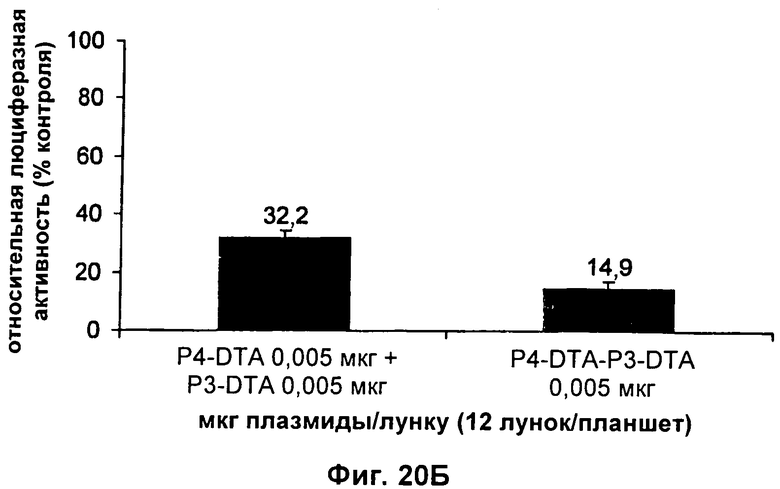
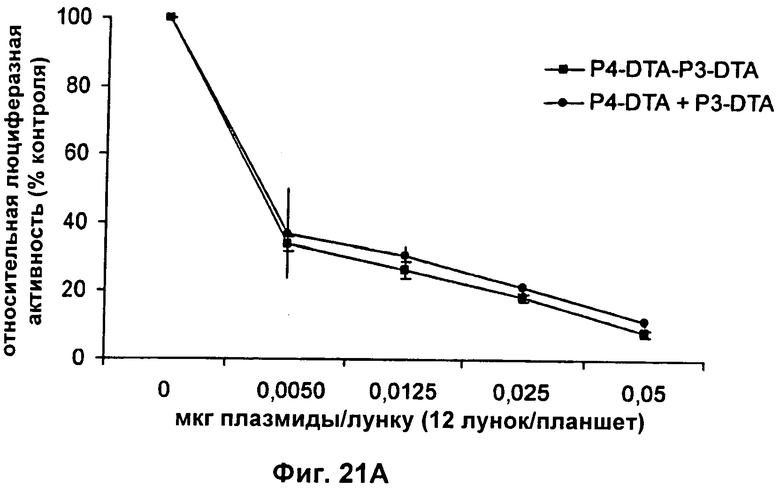
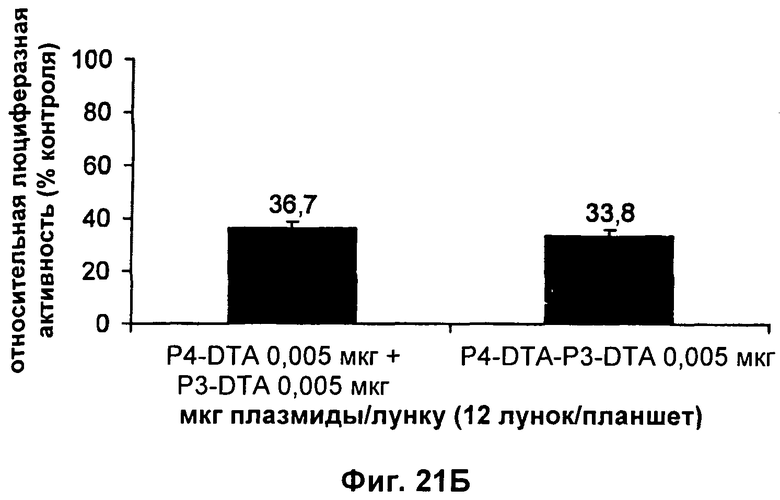
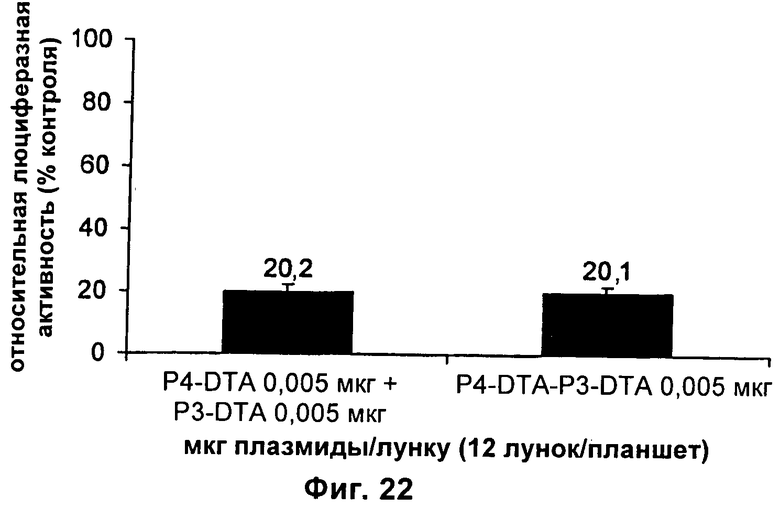
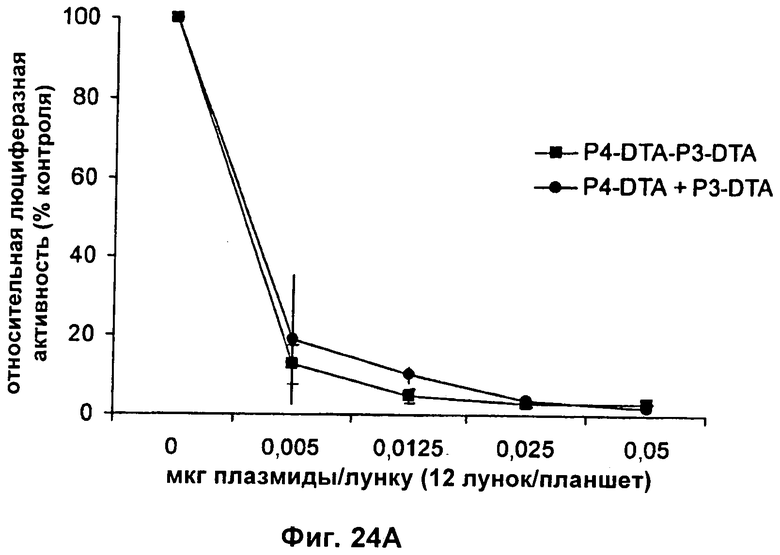
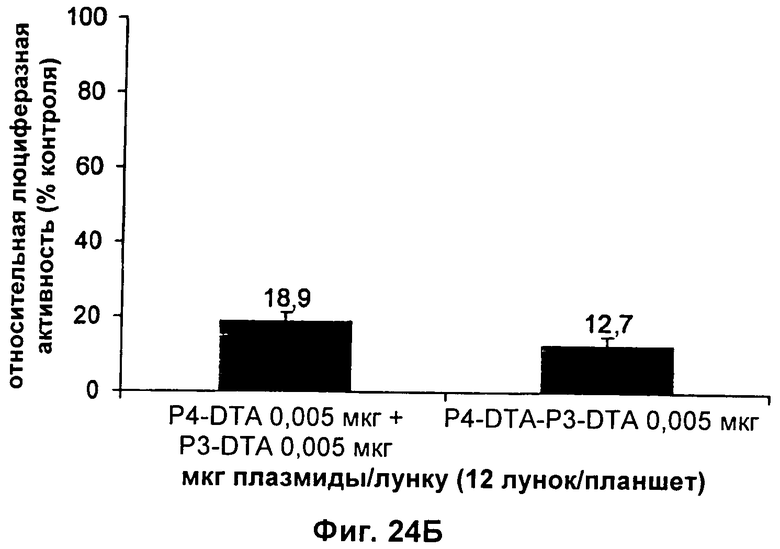
13. Конструкция нуклеиновой кислоты по п.1, где первая открытая рамка считывания связана функциональным образом с промотором IGF-II Р3, и вторая открытая рамка считывания связана функциональным образом с промотором IGF-II P4.
14. Способ лечения опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.1, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором H19, транскрипт, управляемый промотором IGF-II Р3, или транскрипт, управляемый промотором IGF-II P4, посредством чего лечат опухоль у субъекта-человека.
15. Способ по п.14, где указанная опухоль представляет собой карциному.
16. Способ по п.15, где указанная опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
17. Способ ингибирования развития опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.1, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором H19, транскрипт, управляемый промотором IGF-II P4, или транскрипт, управляемый промотором IGF-II Р3, посредством чего ингибируют развитие опухоли у субъекта-человека.
18. Способ по п.17, где указанная опухоль представляет собой карциному.
19. Способ по п.18, где указанная опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
20. Способ ингибирования метастаза опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.1, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором H19, транскрипт, управляемый промотором IGF-II P4, или транскрипт, управляемый промотором IGF-II Р3, посредством чего ингибируют развитие опухоли у субъекта-человека.
21. Способ по п.20, где указанная опухоль представляет собой карциному.
22. Способ по п.21, где указанная опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
23. Способ лечения опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.13, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором IGF-II Р3, или транскрипт, управляемый промотором IGF-II P4, посредством чего лечат опухоль у субъекта-человека.
24. Способ по п.23, где указанная опухоль представляет собой карциному.
25. Способ по п.24, где указанная, опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
26. Способ ингибирования развития опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.13, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором IGF-II Р3, или транскрипт, управляемый промотором IGF-II P4, посредством чего ингибируют развитие опухоли у субъекта-человека.
27. Способ по п.26, где указанная опухоль представляет собой карциному.
28. Способ по п.27, где указанная опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
29. Способ ингибирования метастаза опухоли у субъекта-человека, нуждающегося в этом, включающий введение указанному субъекту-человеку конструкции нуклеиновой кислоты по п.13, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором IGF-II Р3, или транскрипт, управляемый промотором IGF-II P4, посредством чего ингибируют развитие опухоли у субъекта-человека.
30. Способ по п.29, где указанная опухоль представляет собой карциному.
31. Способ по п.30, где указанная опухоль выбрана из группы, состоящей из карциномы мочевого пузыря, гепатокарциномы, карциномы яичника и карциномы поджелудочной железы.
32. Конструкция нуклеиновой кислоты, полезная для лечения опухолей, содержащая:
первую открытую рамку считывания, кодирующую цитотоксический или цитостатический генный продукт, причем данная первая открытая рамка считывания связана функциональным образом с первым промотором; и
вторую открытую рамку считывания, кодирующую указанный цитотоксический или цитостатический генный продукт, причем данная вторая открытая рамка считывания связана функциональным образом со вторым промотором;
где первый промотор и второй промотор выбраны из группы, состоящей из:
1) первого промотора, представляющего собой Н19-специфичный промотор, и второго промотора, представляющего собой промотор IGF-II P4;
2) первого промотора, представляющего собой промотор H19, и второго промотора, представляющего собой промотор IGF-II Р3; и
3) первого промотора, представляющего собой промотор IGF-II P4, и второго промотора, представляющего собой промотор IGF-II Р3.
33. Конструкция нуклеиновой кислоты по п.32 для лечения опухоли, ингибирования развития опухоли или ингибирования метастаза опухоли у субъекта-человека, нуждающегося в этом, где клетка указанной опухоли способна экспрессировать транскрипт, управляемый промотором H19.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| AYESH B | |||
| et al., "Inhibition of tumor growth by DT-A expressed under the control of IGF2 P3 and P4 promoter sequences." Mol Ther | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| OHANA P | |||
| et al., "Regulatory sequences of H19 and IGF2 genes in DNA-based therapy of colorectal rat liver metastases" | |||
| Journal of Gene | |||
Авторы
Даты
2013-07-10—Публикация
2008-10-23—Подача