Изобретение относится к биологии, токсикологической и аналитической химии, а именно к способам извлечения азатиоприна из биологических жидкостей, и может быть использовано в практике химико-токсикологических и клинических лабораторий для извлечения азатиоприна из биологических жидкостей с целью его последующего определения. Способ относится к числу массовых.
Известен способ извлечения производных пурина (кофеина) из биологической жидкости (раствора альбумина), состоящий в том, что анализируемую пробу обрабатывают раствором пепсина в растворе хлороводородной кислоты, доводят реакцию среды полученной смеси до рН 4, инкубируют при температуре 37°С в течение 1 часа, экстрагируют трижды хлороформом при соотношении объемов водной и органической фаз 1:1, экстракты объединяют, остаток растворяют в фосфатном буфере с рН 7,4, полученный раствор фильтруют и определяют количество извлеченного производного пурина по величине оптической плотности фильтрата, измеренной при длине волны 273 нм (Стрелова О.Ю., Чувина Н.А. Изолирование кофеина из крови с применением ферментативного гидролиза на примере модельного вещества // Судебно-медицинская экспертиза. - 2008. - Т.51, №4. - С.28-31).
Способ отличается трудоемкостью и относительно низкой степенью извлечения.
Известен способ извлечения производных пурина из биожидкостей (крови), заключающийся в том, что анализируемую пробу обрабатывают сульфатом аммония, выдерживают в течение 30 минут при перемешивании, раствор центрифугируют при 3000 оборотах в минуту, центрифугат отделяют, доводят его реакцию до рН 4,0-5,0, экстрагируют трижды хлороформом при соотношении водной и органической фаз на каждой стадии экстракции 1:1, экстракты объединяют, экстрагент испаряют, остаток растворяют в фосфатном буфере с рН 7,4, полученный раствор фильтруют и определяют количество извлеченного вещества по величине оптической плотности, измеренной при длине волны 273 нм (Стрелова О.Ю., Чувина Н.А. Оценка эффективности методов изолирования токсических веществ из крови // Судебно-медицинская экспертиза. - 2008. - Т.51, №4. - С.22-24).
Способ характеризуется недостаточно высокой степенью извлечения.
Наиболее близким является способ извлечения производных пурина (к которым относится и азатиоприн) из плазмы крови, состоящий в том, что анализируемую пробу обрабатывают осаждающим белки реагентом, в качестве которого используется хлорная кислота, извлечение отделяют от выпавшего осадка центрифугированием, центрифугат обрабатывают раствором гидроксида натрия, избыток щелочи нейтрализуют раствором хлороводородной кислоты, полученный раствор экстрагируют смесью органических растворителей хлороформ-пропанол-2, взятых в объемном отношении 1:1, органический экстракт отделяют центрифугированием, экстрагент испаряют до сухого остатка, остаток растворяют в подвижной фазе и определяют количество перешедшего в экстракт анализируемого соединения методом ВЭЖХ по площади хроматографического пика (Dobrocky P., Bennet P.N., Natarianny L.J. Rapid method for the routine determination of caffeini and its metabolites by high-performance liquid chromatography // J. Chromatogr. Biomed. AppL - 1994. - Vol.652, №1. - P.104-108).
Способ характеризуется недостаточно высокой степенью извлечения. Техническим результатом настоящего изобретения является повышение степени извлечения.
Технический результат достигается тем, что анализируемую пробу обрабатывают осаждающим белки реагентом, в качестве которого используется ацетон, извлечение отделяют от выпавшего осадка путем фильтрования, ацетон из фильтрата испаряют в токе воздуха при комнатной температуре, водный остаток разбавляют водой, образующийся раствор обрабатывают сульфатом аммония, экстрагируют 0,9 моль/дм3 раствором диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1 при соотношении водной и органической фаз 5:1 по объему, органический экстрагент отделяют, а количество перешедшего в экстракт анализируемого соединения определяют по величине оптической плотности экстракта, разбавленного в 10 раз 1,4-диоксаном, проводя измерения при длине волны 279 нм.
Способ осуществляется следующим образом: плазму крови, содержащую азатиоприн, обрабатывают осаждающим белки реагентом, в качестве которого используется ацетон, извлечение отделяют от выпавшего осадка путем фильтрования, ацетон из фильтрата испаряют в токе воздуха при комнатной температуре, водный остаток разбавляют водой, образующийся раствор обрабатывают сульфатом аммония, экстрагируют 0,9 моль/дм3 раствором диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1 при соотношении водной и органической фаз 5:1 по объему, органический экстрагент отделяют, а количество перешедшего в экстракт анализируемого соединения определяют по величине оптической плотности экстракта, разбавленного в 10 раз 1,4-диоксаном, проводя измерения при длине волны 279 нм.
Способ иллюстрируется следующими примерами.
Пример 1
Извлечение азатиоприна из плазмы крови
В 5 г плазмы крови человека вносят 1 мг азатиоприна в виде 0,5 см3 0,1% раствора, тщательно перемешивают биологическую жидкость с веществом. Полученную смесь обрабатывают 10 см3 осаждающего белки реагента, в качестве которого используют ацетон, и оставляют на 5 минут при перемешивании. По истечении указанного времени жидкое извлечение отделяют от выпавшего осадка путем фильтрования через бумажный фильтр. Фильтр и осадок на фильтре промывают 5 см3 ацетона. Порции фильтрата объединяют в выпарительной чашке и испаряют ацетон в токе воздуха при комнатной температуре. К водному остатку фильтрата добавляют 5 см воды, в образующийся раствор вводят сульфат аммония до получения насыщенного водно-солевого раствора, который экстрагируют 2 см3 0,9 моль/дм3 раствора диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1, на вибросмесителе в течение 8 минут, после чего раствор оставляют на 3-5 минут для расслаивания системы, органический экстракт отделяет 0,2 см экстракта вносят в мерную колбу вместимостью 10 см, доводят до метки 1,4-диоксаном и измеряют оптическую плотность полученного раствора на спектрофотометре СФ-2000 при длине волны 279 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По величине оптической плотности определяют количество азатиоприна, перешедшее в слой экстрагента, используя уравнение градуировочного графика. Рассчитывают степень извлечения азатиоприна как отношение количества вещества, перешедшего в слой экстрагента, в процентах к его количеству, внесенному в биологическую жидкость.
Построение градуировочного графика
В ряд мерных колб вместимостью 10 мл вносят 0,1, 0,2, 0,4, 1,0, 1,6, 2,0 см3 0,01% раствора азатиоприна в хлороформе, по 0,2 см3 0,9 моль/дм3 раствора диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1, и доводят 1,4-диоксаном до метки. Оптическую плотность образующихся растворов измеряют на спектрофотометре СФ-2000 при 279 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте.
По результатам измерения оптической плотности серии растворов с известными концентрациями азатиоприна строят график зависимости оптической плотности от концентрации определяемого вещества. График линеен в интервале концентраций 1,0 - 20,0 мкг/см3. Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
А=0,06285-С+0,00124,
где А - оптическая плотность; С - концентрация анализируемого вещества (мкг в 1 см3 фотометрируемого раствора).
Результаты извлечения азатиоприна из плазмы крови представлены в таблице 1.
Пример 2
Извлечение азатиоприна из мочи
В 5 г мочи человека вносят 1 мг азатиоприна в виде 0,5 см3 0,1% раствора, тщательно перемешивают биологическую жидкость с веществом. Полученную смесь обрабатывают 10 см осаждающего белки реагента, в качестве которого используют ацетон, и оставляют на 5 минут при перемешивании. По истечении указанного времени жидкое извлечение отделяют от выпавшего осадка путем фильтрования через бумажный фильтр. Фильтр и осадок на фильтре промывают 5 см3 ацетона. Порции фильтрата объединяют в выпарительной чашке и испаряют ацетон в токе воздуха при комнатой температуре. К водному остатку фильтрата добавляют 5 см3 воды, в образующийся раствор вводят сульфат аммония до получения насыщенного водно-солевого раствора, который экстрагируют 2 см3 0,9 моль/дм3 раствора диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1, на вибросмесителе в течение 8 минут, после чего раствор оставляют на 3-5 минут для расслаивания системы, органический экстракт отделяют, 0,2 см3 экстракта вносят в мерную колбу вместимостью 10 см3, доводят до метки 1,4-диоксаном и измеряют оптическую плотность полученного раствора на спектрофотометре СФ-2000 при длине волны 279 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора положенного в контрольном опыте. По величине оптической плотности определяют количество азатиоприна, перешедшее в слой экстрагента, используя уравнение градуировочного графика. Рассчитывают степень извлечения азатиоприна как отношение количества вещества, перешедшего в слой экстрагента, в процентах к его количеству, внесенному в биологическую жидкость.
Схема построения градуировочного графика для определения азатиоприна и уравнение этого графика представлены выше в примере 1.
Результаты извлечения азатиоприна из мочи представлены в таблице 2.
Предлагаемый способ по сравнению с прототипом на 7-8% повышает степень извлечения азатиоприна из биологических жидкостей.
Сравнительная характеристика предлагаемого и известного способов представлена в таблице 3.
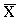
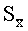
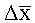
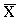
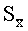
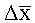
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОКАИНА В ПЛАЗМЕ КРОВИ | 2013 |
|
RU2537179C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ 1-АМИНО-2-НАФТОЛ-4-СУЛЬФОКИСЛОТЫ ИЗ ВОДНЫХ РАСТВОРОВ | 2004 |
|
RU2252934C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ НИТРОСОЕДИНЕНИЙ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1996 |
|
RU2100808C1 |
| Способ определения кофеина в биологическом материале | 2016 |
|
RU2638789C1 |
| Способ определения 2,6-бис-[бис-(бета-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале | 2016 |
|
RU2617176C1 |
| Способ определения алкил-динитрофенолов в биологическом материале | 1990 |
|
SU1786426A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ТЕОБРОМИНА ИЗ ВОДНЫХ РАСТВОРОВ | 2011 |
|
RU2486511C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-БИС-[БИС-(БЕТА-ОКСИЭТИЛ)-АМИНО]-4,8-ДИ-N-ПИПЕРИДИНО-ПИРИМИДО(5,4-D)ПИРИМИДИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2322674C1 |
| Способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале | 2018 |
|
RU2692127C1 |
| СПОСОБ ЭКСТРАКЦИОННОГО ИЗВЛЕЧЕНИЯ И КОНЦЕНТРИРОВАНИЯ НАФТОЛМОНОСУЛЬФОКИСЛОТ ИЗ ВОДНЫХ РАСТВОРОВ | 2004 |
|
RU2255083C1 |
Изобретение относится к токсикологической и аналитической химии, а именно к способу извлечения азатиоприна из биологических жидкостей, заключающийся в том, что анализируемую пробу обрабатывают осаждающим белки реагентом, в качестве которого используется ацетон, извлечение отделяют от выпавшего осадка путем фильтрования, ацетон из фильтрата испаряют в токе воздуха при комнатной температуре, водный остаток разбавляют водой, образующийся раствор обрабатывают сульфатом аммония, экстрагируют 0,9 моль/дм3 раствором диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном отношении 1:1 при соотношении водной и органической фаз 5:1 по объему, органический экстрагент отделяют, а количество перешедшего в экстракт анализируемого соединения определяют по величине оптической плотности экстракта, разбавленного в 10 раз 1,4-диоксаном, проводя измерения при длине волны 279 нм. Изобретение обеспечивает повышение степени извлечения азатиоприна из биологических жидкостей. 2 пр., 3 табл.
Способ извлечения азатиоприна из биологических жидкостей, заключающийся в том, что анализируемую пробу обрабатывают осаждающим белки реагентом, извлечение отделяют от выпавшего осадка, экстрагируют смесью органических растворителей и определяют количество перешедшего в экстракт анализируемого соединения, отличающийся тем, что в качестве осаждающего белки реагента используется ацетон, после отделения извлечения от выпавшего осадка ацетон испаряют в токе воздуха при комнатной температуре, водный остаток разбавляют водой, обрабатывают сульфатом аммония. экстрагируют 0,9 моль/дм3 раствором диметилфталата в смеси 1,4-диоксан-хлороформ, взятых в объемном соотношении 1:1 при соотношении водной и органической фаз 5:1 по объему, а количество перешедшего в экстракт анализируемого соединения определяют по величине оптической плотности экстракта, разбавленного в 10 раз 1.4-диоксаном, проводя измерения при длине волны 279 нм.
| Кривошеева О.А., Коренман Я.И., Мокшина Н.Я. | |||
| Солохин С.А | |||
| Экстракционно-спектрофотометрическое определение азатиоприна в водных средах// Современные проблемы химической науки и образования | |||
| Том II, 20.04.2012 | |||
| Коренман Я.И., Шорманов В.К., Мокшина Н.Я., Кривошеева О.А., Климанов Д.В | |||
| Экстракционное извлечение кофеина из плазмы крови / IV |
Авторы
Даты
2013-10-10—Публикация
2012-06-13—Подача