Изобретение относится к химической и фармацевтической отраслям промышленности и касается противомикробных средств и композиций на основе аминопроизводных фуллерена С60. Изобретение может найти применение в биомедицинских исследованиях и в производстве новых лекарственных препаратов, предназначенных для лечения и профилактики инфекционных заболеваний. Кроме того, изобретение может использоваться для создания дезинфекционных агентов, предназначенных для обеззараживания и стерилизации загрязненных микроорганизмами сред и поверхностей.
После открытия фуллеренов в 1985 г. [1 - W. Kroto, J.R. Heath, S.C. O'Brien, R.F. Curl, R.E. Smalley. С60: Buckminsterfullerene, Nature, 318, 162-163 (1985)], разработки метода их получения в макроколичествах путем электродугового испарения графита [2 - W. ICratchmer, L.D. Lamb, K. Fostiropoulos, D.R. Huffman. Сбо: a new form of carbon. Nature, 347, 354-358 (1990)] или при неполном сгорании углеводородов [3 - II. Murayama. S. Tomonoh, J.M. Alford, M.H. Karpuk. Fullerene production in tons and more: From science to industry. FuH. Nunotub Curbon Nanostruct., 12, 1-9 (2004)] и эффективных методов разделения фуллеренов [4 - К. Nagala. С. Dejima. Y. Kjkuchi, M. Hashiguchi. Kilogram-scale [60] fullerene separation from a fullerene mixture: Selective complexation of tullerenes with 1,8-diazabicyclo[5.4.0]undec-7-ene (DBU). Chem. Lett., 34, 178-179 (2005)] низший фуллерен С60 высокой чистоты стал доступен в килограммовых количествах по цене менее 15€/г [5 - http://www.neotechproduct.ru/str6.php?lang=rus].
Доступность фуллеренов для исследований позволила найти ряд областей практического использования этих соединений, в том числе в фармацевтической химии - в качестве новых лекарственных препаратов широкого спектра действия. При этом наиболее многообещающие результаты получены с использованием химически модифицированных фуллеренов С60 и С70, в основном содержащих ионогенные группы - аминные [6 - О. Troshina, P. Troshin, A. Peregudov, V. Kozlovski, R. Lyubovskaya. Photoaddition of N-Substituted Piperazines to Сбо: An Efficient Approach to the Synthesis of Water-Soluble Fullerene Derivatives. Chem. Eur Journal, 12, 5569-5577 (2006)] и карбоксильные [7 - M. Brettereich, A. Hirsch. A highly water-soluble dendro[60]fullerene. Tetrahedron Letters, 39, 2731-2734 (1998); 8 - 0. Troshina, P. Troshin, A. Peregudov, V. K-ozlovskiy, J. Balzarini, R. Lyubovskaya. Chlorofullerene С60Сl6: a precursor for straightforward preparation of highly water-soluble polycarboxylic fullerene derivatives active against HIV. Org. Biomol. Chem., 5. 2783-2791 (2007)].
Фуллерены и их производные проявляют выраженную противовирусную, противоопухолевую, нейропротекторную, антиамилоидную и другие активности [9 - Л.Б. Пиотровский, О.И. Киселев. Фуллерены в биологии. СПб, Росток, 2006]. Уникальное сочетание мембранотропных и амфифильных свойств функционализированных фуллеренов, определяющее их способность легко проходить через клеточные мембраны, благоприятствуют созданию эффективных лекарственных средств на основе этого класса соединений. Кроме того, фуллерены могут быть использованы в качестве средств доставки других лекарственных препаратов в живые ткани и клетки.
Важным направлением возможного использования фуллеренов является разработка на их основе противоинфекционных (то есть противовирусных, антибактериальных и противогрибковых) средств. В этом случае важной мишенью их действия является липидная мембрана патогена: благодаря высокому сродству к ее внутренней гидрофобной части фуллерены накапливаются в липидном бислое, обуславливая нарушения ассоциированных с мембранами метаболических процессов [10 - А.К. Сироткин, Л.Б. Пиотровский, Л.Н. Познякова, О.И. Киселев. Влияние комплексов фуллерена С60 с поливинилпирролидоном на морфологию вирусов гриппа. Вопр. биол. мед. фарм. химии, 2005, 3, 21-24; 11 - N. Tsao, T.Y. Luh, С.К. Chou, T.Y. Chang, J.J. Wu, C.C. Liu, H.Y. Lei. In vitro action of carboxyfullerene. J. Antimicrobial Chemother., 2002, 49, 641-649]. Противомикробное действие производных фуллеренов усиливается при одновременном облучении видимым или ультрафиолетовым светом, что обусловлено способностью фуллеренов генерировать под воздействием света активные формы кислорода, вызывающие пероксидное окисление липидов биологических мембран [12 - J. Lee, Y. Mackeyev, M. Cho, D. Li, J.-H. Kirn, L.J. Wilson, P. J.J. Alvarez. Photochemical and antimicrobial properties of novel С60 derivatives in aqueous systems. Environ. Sci. Technol., 43, 6604-6610 (2009)].
Задачей данного изобретения является разработка соединений фуллеренов и композиций на их основе, обладающих устойчивой и выраженной биологической активностью в отношении широкого круга патогенных и условно-патогенных микроорганизмов.
В настоящем изобретении эта задача решается применением пантааминопроизводных фуллерена С60 общей формулы 1:
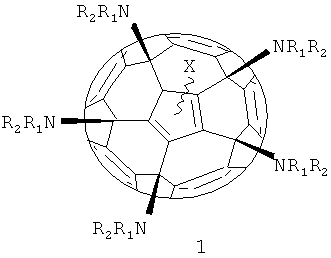
где в общей формуле 1 Х означает:
- отрицательный заряд («-»), локализованный на фуллереновом каркасе, или
- атом хлора (-Сl), присоединенный к углеродному каркасу, или
- атом водорода (-Н);
где в общей формуле 1 фрагмент NR1R2 описывается, но не ограничивается нижеследующими определениями:
- остаток амина, где R1 и R2 - атомы водорода или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmC2m+1; n=1-20);
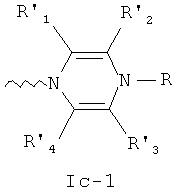
- остаток пиперазина общей формулы Ic-1
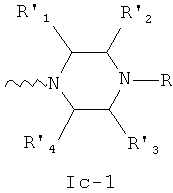
где R, R'1, R'2, R'3 и R'4 - это атомы водорода или линейные или разветвленные алкильные (CmC2m+1; n=1-20) радикалы, а также остатки алифатических спиртов -(CH2)nOH, простых эфиров -(CH2)nSH, кислот -(CH2)nCOOH, их сложных эфиров -(CH2)nCOOR'5 или амидов -(CH2)nCONR'5R'6, для которых n=0-20, а R'5 и R'6 - это атомы водорода или линейные алкильные (CmC2m+1; n=1-20) радикалы.
Структуры соединений общей формулы 1 и метод их синтеза были описаны нами ранее [13 - П.А. Трошин, А.Б. Корнев, Е.А. Хакина, В.Ф. Разумов «Аминофуллерены и способ их получения» Заявка на изобретение №2010127788 от 07072019, РФ и А.В. Komev, Е.A. Khakina, S.I. Troyanov, A.A. Kushch, D.G. Deryabin, A.S. Peregudov, A. Vasilchenko, V.M. Martynenko, P.A. Troshin, Facile preparation of amine and amino acid adducfs of [60] fullerene using chlorofullerene C60Cl6 as a precursor. Chem. Commun., 2012, 48, 5461-5463]. В данном изобретении раскрывается способ практического применения указанных соединений общей формулы 1 в качестве противомикробных препаратов в чистом виде и в составе композиций.
В соответствии с настоящим изобретением противомикробная композиция антибактериального действия на основе аминопроизводных фуллерена содержит по весу от 0.0001 до 100% соединений общей формулы 1, остальное - нейтральные компоненты или вещества, позитивно модифицирующие (усиливающие, пролонгирующие и т.д.) антимикробное действие композиции.
Наиболее близким известным аналогом изобретения является использование аминопроизводных фуллерена общей формулы 2 в качестве антибактериального и противоракового средства [18 - Т. Mashino. Antibacterial agent and anticancer agent. Патент ЕР 1611889 A1 от 04.01.2006]. Соединения формулы 2 представляют собой сложные смеси региоизомеров фуллереновых полиаддуктов и получаются лишь с очень небольшим выходом - порядка 9%, что затрудняет их практическое использование.
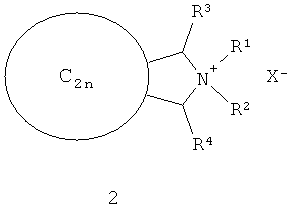
В отличие от описанных ранее соединений фуллеренов, проявляющих противомикробные свойства, производные фуллеренов, соответствующие общей формуле 1, отличаются простотой получения и низкой стоимостью, и поэтому могут быть легко синтезированы в больших количествах с целью практического использования. Кроме того, соединения в соответствии с формулой 1 являются амфифильными, так как имеют в своей структуре гидрофобные и гидрофильные фрагменты, что обеспечивает легкость их проникновения через клеточные мембраны. Это является важным преимуществом указанных производных по сравнению с большинством ранее описанных соединений (например, общей формулы 2), в которых каркас фуллерена равномерно покрыт заряженными группами.
Производные фуллеренов общей формулы 1, особенно содержащие положительно заряженные группы, например, аммонийные, обладают высокой ингибирующей активностью по отношению к различным грамположительным и грамотрицательным бактериям, что позволяет использовать их в качестве химиотерапевтических средств широкого спектра действия или дезинфектантов для обеззараживания загрязненных микроорганизмами сред и поверхностей. В основе противомикробного действия производных фуллеренов общей формулы 1 лежит их мембранотропная активность, то есть высокое сродство к мембранам микробных клеток, что было установлено с использованием метода атомно-силовой микроскопии (см. пример 1). Наиболее выраженной активностью при этом обладают катионные производные фуллеренов, поскольку они более эффективно связываются с отрицательно заряженными мембранами патогенных микроорганизмов за счет электростатического притяжения. Результатом же подобного взаимодействия является повреждение и гибель микробных клеток, что было установлено сочетанием бактериологического и биолюминесцентного методов.
Защищаемое применение соединений общей формулы 1 подразумевает, в том числе, их использование для лечения и профилактики инфекционных заболеваний. С этой целью производные фуллеренов могут вводиться в организм для обеспечения системного эффекта, а также применяться местно для воздействия на определенные области (например, в составе перевязочных материалов для обработки ран, при обработке операционного поля и т.д.). Соединения фуллеренов могут использоваться в виде твердых веществ, растворов или суспензий в воде или других растворителях, а также нанесенными на различные носители. Возможно также использование соединений общей формулы 1 в составе композиций с другими веществами, в том числе с противомикробными препаратами других классов (четвертичными аммониевыми соединениями и др.).
В состав патентуемого изобретения входит также применение производных фуллерена общей формулы 1 для дезинфекции микробиологически загрязненных сред и поверхностей. Для проведения дезинфекции жидких и газовых сред производные фуллеренов могут вводиться в указанные среды в виде растворов, суспензий или аэрозолей, а также применяться в процессах фильтрования в виде чистых веществ или иммобилизованными на различных носителях. С целью обеззараживания твердых поверхностей производные 1 могут наноситься на них в виде твердых частиц, растворов или суспензий. При этом для обеспечения длительной защиты от распространения микроорганизмов производное фуллерена может не удаляться из среды или с поверхности, подвергнутой дезинфицирующей обработке.
Антимикробное действие производных фуллеренов может быть усилено при одновременном воздействии ультрафиолетового или видимого света, что связано со способностью фуллеренов выступать в качестве фотосенсибилизаторов, переводящих содержащийся в среде кислород в его активные формы (например, синглетный кислород или супероксид-анион-радикал). Фотохимическая генерация активных форм кислорода, осуществляемая производными фуллерена в непосредственной близости к липидной мембране или молекулам нуклеиновых кислот, приводит к окислительному повреждению этих структур и в конечном итоге к потере жизнеспособности микробной клетки. Возможность усиления антимикробной активности производных фуллеренов общей формулы 1 под воздействием света иллюстрируется примером 2. Благодаря этому свойству соединения фуллеренов общей формулы 1 могут быть использованы в качестве средств для фотодинамической терапии инфекционных заболеваний, а также для фотохимической очистки загрязненных сред, в том числе поверхностей медицинского назначения и сточных вод.
Антимикробное действие производных фуллеренов может быть модифицировано (усилено или пролонгировано) при их использовании в композиции с иными исходно инертными или антимикробными веществами, в том числе также проявляющими тропность к мембранным структурам бактериальных клеток-мишеней. При этом в основе подобной активности, с одной стороны, лежит синергестический антимикробный эффект производного фуллерена и вещества-компаньона, а с другой - возможность образования между ними надмолекулярных комплексов, постепенное высвобождение действующих начал из которых ведет к пролонгации антимикробного эффекта. Возможность модификации антимикробной активности производных фуллеренов общей формулы 1 в их композиции с четвертичным аммониевым соединением иллюстрируется примером 3. Благодаря этому действие соединений фуллеренов общей формулы 1 в зависимости от их молярного соотношения с веществом-компаньоном может быть либо усилено, либо пролонгировано, что в зависимости от конкретной задачи является положительным эффектом при лечении и профилактике инфекционных заболеваний или очистке загрязненных микроорганизмами сред, в том числе поверхностей медицинского назначения и сточных вод.
Заявляемое изобретение иллюстрируется, но никак не ограничивается следующими примерами.
Пример 1. Оценка противомикробной активности производных фуллеренов В качестве примеров производных фуллеренов, соответствующих общей формуле 1, были использованы соединения 1а-в.
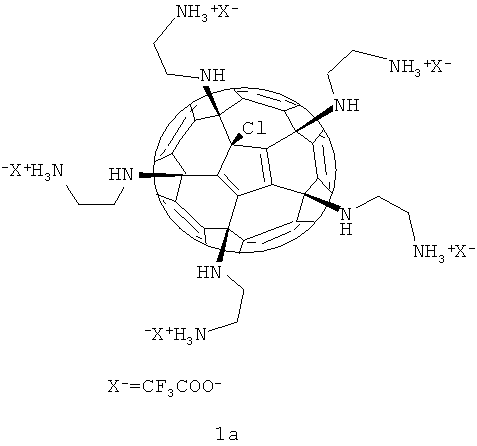
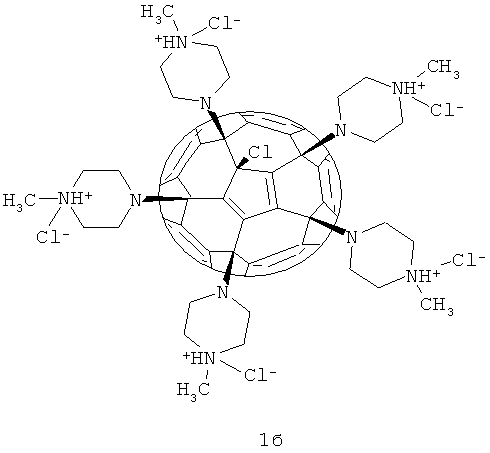
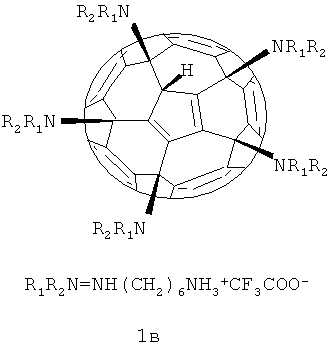
Определение антимикробной активности (концентрации LD50, вызывающей гибель 50% бактериальных клеток-мишеней после 60 минут контакта) проводилось на модельных грамотрицательном (Eschenchia coli) и грамположительном (Bacillus subtilis) микроорганизмах в бактериологических тестах высева на плотные питательные среды Одновременно исследовалось подавление производными фуллерена 1a-в свечения биолюминесцентных сенсорных систем на основе рекомбинантных штаммов Eschenchia coli К12 TG1 и Bacillus subtilis В-10548 с клонированными luxCD(AB)E-генами природного морского люминесцирующего микроорганизма Photobactenum leiognathi Характеристикой антимикробного действия в данном случае служила величина ЕС50 - концентрация исследованных производных фуллеренов, вызывающая подавление биолюминесценции к 60-й минуте контакта на 50% от контрольных значений
Результаты определения противомикробной активности приведены в таблице 1
Из приведенных значений активности видно, что катионные производные фуллерена С60 способны эффективно подавлять как грамположительные, так и грамотрицательные микроорганизмы в микромолярном диапазоне концентраций
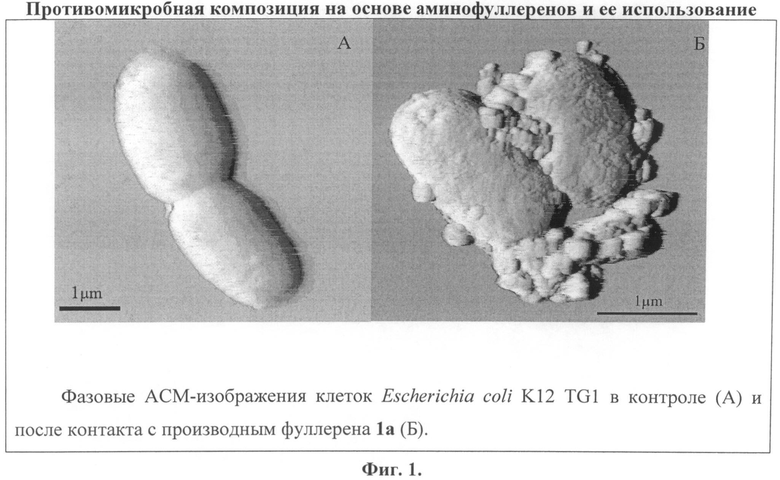
Прямое взаимодействие аминопроизводных фуллеренов с бактериальными клетками доказано с помощью атомно-силовой микроскопии Полученные изображения интактных бактериальных клеток, а также клеток после контакта с аминопроизводным фуллерена 1а приведены на Фиг 1 При этом после инкубации с аминопроизводным фуллерена 1а клетки Escherichia coli К 12 TG1 претерпевали существенные морфологические изменения: в тесной связи с ними фиксировались выпуклые образования неправильной формы размером от 47,3±3,11 нм до 276,0±14,9 нм, предположительно представляющие собой ассоциаты аминопроизводного фуллерена 1а, установившие контакт с бактериальной поверхностью.
Пример 2. Усиление противобактериальной активности производных фуллеренов под действием облучения
Фотосенсибилизирующие свойства производных фуллерена С60 были изучены с использованием сенсорного люминесцирующего штамма Escherichia coli К 12 TG1 с клонированными luxCDABE-гепами морского люминесцирующего микроорганизма Photobacterium leiognathi.
Суспензия клеток сенсорной бактериальной системы смешивалась с водным раствором производных фуллеренов 1а-в соответствующих концентраций, после чего проводилось их облучение светом ртутно-кварцевой лампы в течение 5, 10 или 15 минут. После дополнительного инкубирования в течение 15 минут измеряли уровень биолюминесценции исследуемых проб и рассчитывали значения ЕС50, характеризующие эффективные концентрации производных фуллеренов, вызывающие тушение биолюминесценции сенсорного микроорганизма на 50% по сравнению с контролем.
Результаты определения противомикробного действия производных фуллеренов в темноте и при облучении ультрафиолетовым светом представлены в таблице 2. Видно, что противобактериальное действие исследованных производных 1а-в значительно усиливается под воздействием УФ-облучения, что проявляется в значимом снижении регистрируемых значений ЕС50.
Пример 3. Модификация противобактериальной активности производных фуллеренов в композиции с четвертичным аммониевым соединением - дидедилдиметиламмония бромида клатратом (ДДАБ-К).
Модификация свойств аминопроизводного фуллерена 1а была изучена в тесте подавления биолюминесценции сенсорного штамма Escherichia coli К 12 TG1 с клонированными luxCDABE- генами морского люминесцирующего микроорганизма Photobacterium leiognathi.
Водные растворы фуллерена 1a c концентрациями от 0,0078 до 0,125 мМ в равных объемах смешивались с раствором дидедилдиметиламмония бромида клатрата (ДДАБ-К) в концентрациях от 0,0156 до 0,125 мМ и выдерживались в течение 10-30 мин. В полученные композиции вносили суспензии клеток сенсорной бактериальной системы, после чего в течение 60 мин динамически измеряли интенсивность биолюминесценции, отражающую развитие противобактериального эффекта. Результат модификации противобактериальной активности фуллерена 1а оценивали как «усиление эффекта» при более значимом подавлении уровня бактериальной биолюминесценции композицией по сравнению с изолированным действием эквимолярных количеств фуллерена и ДДАБ-К, а как «пролонгацию эффекта» - при увеличении времени полного подавления бактериальной биолюминесценции по сравнению с аналогичным действием эквимолярных количеств фуллерена и ДДАБ-К.
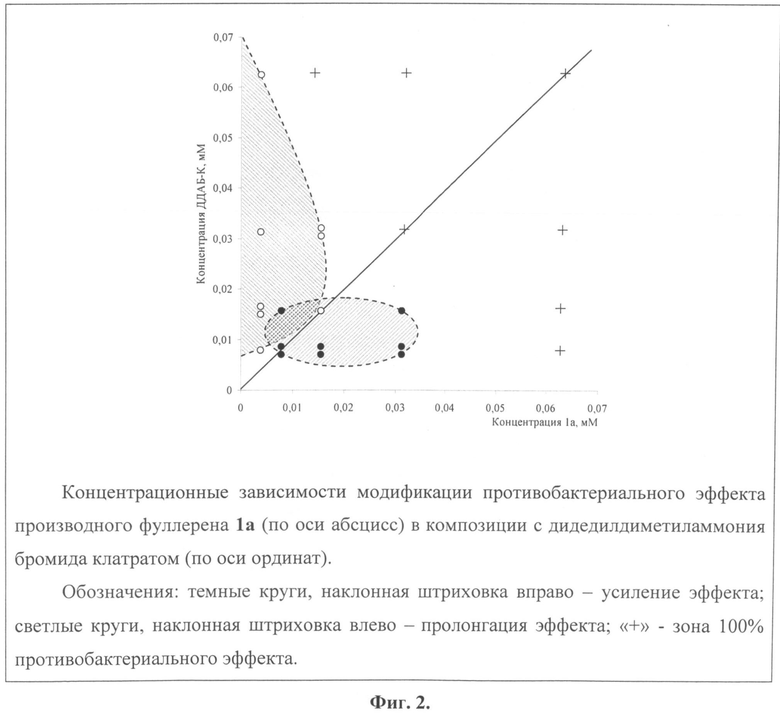
Результаты исследования характера модификации противомикробного эффекта производного фуллерена 1а в композиции с ДДАБ-К представлены на Фиг.2.
При молярном соотношении «фуллерен 1а: ДДАБ-К» больше 1 (справа от наклонной линии), в том числе в диапазоне концентраций фуллерена 1а от 0,0078 до 0,03125 мМ и ДДАБ-К от 0,0078 до 0,0156 мМ, каждая из которых самостоятельно обуславливает только частичное тушение бактериальной биолюминесценции, регистрируется усиление антибактериального эффекта сформированных композиций, потенциально определяемое синергетическим эффектом входящих в них веществ в отношении клеток сенсорной бактериальной системы.
В свою очередь при молярном соотношении «фуллерен 1а: ДДАБ-К» меньше 1 (слева от наклонной линии), в том числе в диапазоне концентраций фуллерена 1а от 0,0039 до 0,0156 мМ и ДДАБ-К от 0,0078 до 0,0625 мМ, регистрируется пролонгация эффекта, потенциально определяемая первичным формированием надмолекулярных комплексов из веществ-компаньонов с последующим постепенным высвобождением действующих начал и определяемой этим более плавной динамикой развития противобактериального эффекта.
Таким образом, в зависимости от молярного соотношения фуллерена 1a c ДДАБ-К противобактериальный эффект может быть либо усилен, либо пролонгирован, что в зависимости от конкретной задачи является положительным эффектом при лечении и профилактике инфекционных заболеваний или очистке загрязненных сред микроорганизмами, в том числе поверхностей медицинского назначения и сточных вод.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АМИННЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ С60 И С70 И КОМПОЗИЦИЙ НА ИХ ОСНОВЕ В КАЧЕСТВЕ ПРОТИВОМИКРОБНЫХ СРЕДСТВ | 2011 |
|
RU2522012C2 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ 1,3-ДИГИДРОКСИБЕНЗОЛА В КАЧЕСТВЕ СЕНСИБИЛИЗАТОРОВ БАКТЕРИАЛЬНЫХ КЛЕТОК К ПОВРЕЖДАЮЩЕМУ ВОЗДЕЙСТВИЮ НАНОСТРУКТУРИРОВАННЫХ СОЕДИНЕНИЙ УГЛЕРОДА | 2014 |
|
RU2598731C2 |
| ФОСФОРСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНА C И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2509083C2 |
| АРИЛИРОВАННЫЕ ПОЛИКАРБОКСИЛЬНЫЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ КОВАЛЕНТНЫЕ КОНЪЮГАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2567299C2 |
| НАНОАГРЕГАТЫ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИИ НА ОСНОВЕ НАНОАГРЕГАТОВ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ, ПРИМЕНЕНИЕ НАНОАГРЕГАТОВ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ И КОМПОЗИЦИЙ НА ИХ ОСНОВЕ В КАЧЕСТВЕ БИОЛОГИЧЕСКИ-АКТИВНЫХ СОЕДИНЕНИЙ, ДЛЯ ПОНИЖЕНИЯ ТОКСИЧНОСТИ И УСИЛЕНИЯ ТЕРАПЕВТИЧЕСКОГО ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, А ТАКЖЕ В КАЧЕСТВЕ ПРЕПАРАТОВ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2550030C2 |
| СЕРОСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2477273C2 |
| Применение водорастворимых производных фуллерена в качестве лекарственных препаратов нейропротекторного и противоопухолевого действия | 2017 |
|
RU2704483C2 |
| Способ получения продуктов с антибактериальной активностью из мицелия базидиомицетов | 2022 |
|
RU2800356C1 |
| Антиоксидантный препарат для животных на основе водного раствора фуллерена С, ресвератрола и альфа-липоевой кислоты | 2022 |
|
RU2807600C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДДУКТОВ ФУЛЛЕРЕНА | 2010 |
|
RU2462474C2 |
Изобретение относится к применению производных фуллерена общей формулы 1 в качестве противомикробных препаратов. В формуле 1 Х означает отрицательный заряд, локализованный на фуллереновом каркасе, атом хлора, присоединенный к углеродному каркасу, или атом водорода; фрагмент NR1R2 означает остаток амина, где R1 и R2 - атомы водорода, или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmH2m+1; n=1-20), или остаток пиперазина общей формулы Ic-1, где R, R'1, R'2 R'3 и R'4 - атомы водорода или линейные или разветвленные алкильные (CmH2m+1; n=l-20) радикалы, а также остатки алифатических спиртов -(СН2)nOH, простых эфиров -(CH2)nOR'5, тиолов -(CH2)nSH, кислот -(СН2)nCOOH, их сложных эфиров -(CH2)nCOOR'5 или амидов -(CH2)nCONR'5R'6, для которых n=0-20, R'5 и R'6 - атомы водорода или линейные алкильные (CmH2m+1; n=1-20) радикалы. Изобретение также относится к антибактериальной композиции, содержащей указанные соединения и компоненты, усиливающие или пролонгирующие антибактериальное действие. 2 н.п. ф-лы, 2 табл., 2 ил., 3 пр.

1. Применение производных фуллерена общей формулы 1 в качестве противомикробных препаратов

где в общей формуле 1 Х означает:
- отрицательный заряд («-»), локализованный на фуллереновом каркасе, или
- атом хлора (-Cl), присоединенный к углеродному каркасу, или
- атом водорода (-Н);
где в общей формуле 1 фрагмент NR1R2 описывается, но не ограничивается нижеследующими определениями:
- остаток амина, где R1 и R2 - атомы водорода или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmH2m+1; n=1-20);
- остаток пиперазина общей формулы Ic-1
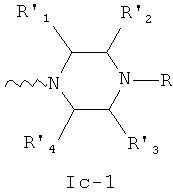
где R, R'1, R'2 R'3 и R'4 - это атомы водорода или линейные или разветвленные алкильные (CmH2m+1; n=1-20) радикалы, а также остатки алифатических спиртов -(СН2)nOH, простых эфиров -(CH2)nOR'5, тиолов -(CH2)nSH, кислот -(СН2)nCOOH, их сложных эфиров -(CH2)nCOOR'5 или амидов -(CH2)nCONR'5R'6, для которых n=0-20, a R'5 и R'6 - это атомы водорода или линейные алкильные (CmH2m+1; n=1-20) радикалы.
2. Антибактериальная композиция, содержащая эффективную концентрацию производных фуллерена общей формулы 1, а также инертный разбавитель и компоненты, усиливающие или пролонгирующие антибактериальное действие производного фуллерена общей формулы 1.
| Устройство для аэрации жидкости | 1988 |
|
SU1611889A1 |
| ВОДОРАСТВОРИМЫЕ АМИНОФУЛЛЕРЕНЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2358904C2 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ РЕПРОДУКЦИИ ОБОЛОЧЕННЫХ ВИРУСОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ВИРУСНЫХ ИНФЕКЦИЙ | 2003 |
|
RU2236852C1 |
| TROSHINA O.A | |||
| ET AL | |||
| "Reactions of chlorofullerene СС with N-substituted piperazines", Tetrahedron, 2006, v.62, pp.10147-10151 | |||
| Т | |||
| Mashino ET AL | |||
| "Antibacterial and Antiproliferative Activity of Cationic Fullerene Derivatives", Bioorganic & Medicinal Chemistry Letters, 13, 2003, 4395-4397. | |||
Авторы
Даты
2013-12-20—Публикация
2011-08-30—Подача