Изобретение относится к химической и фармацевтической отраслям промышленности и касается противомикробных средств и композиций на основе аминопроизводных фуллеренов. Изобретение может найти применение в биомедицинских исследованиях и в производстве новых лекарственных препаратов, предназначенных для лечения и профилактики инфекционных заболеваний. Кроме того, изобретение может использоваться для создания дезинфекционных агентов, предназначенных для обеззараживания и стерилизации загрязненных микроорганизмами сред и поверхностей.
После открытия фуллеренов в 1985 г. [1 - W. Kroto, J.R. Heath, S.C. O′Brien, R.F. Curl, R.E. Smalley. C60: Buckminsterfullerene, Nature, 318, 162-163 (1985)], разработки метода их получения в макроколичествах путем электродугового испарения графита [2 - W. Krätchmer, L.D. Lamb, K. Fostiropoulos, D.R. Huffman. С60: a new form of carbon. Nature, 347, 354-358 (1990)] или при неполном сгорании углеводородов [3 - Н. Murayama, S. Tomonoh, J.M. Alford, M.E. Karpuk. Fullerene production in tons and more: From science to industry. Full. Nanotub. Carbon Nanostruct., 12, 1-9 (2004)] и эффективных методов разделения фуллеренов [4 - K. Nagata, Е. Dejima, Y. Kikuchi, М. Hashiguchi. Kilogram-scale [60] fullerene separation from a fullerene mixture: Selective complexation of fullerenes with 1,8-diazabicyclo [5.4.0] undec-7-ene (DBU). Chem. Lett., 34, 178-179 (2005)] низший фуллерен C60 высокой чистоты стал доступен в килограммовых количествах по цене менее 15€/г [5 - http://www.neotechproduct.ru/str6.php?lang=rus].
Доступность фуллеренов для исследований позволила найти ряд областей практического использования этих соединений, в том числе в фармацевтической химии - в качестве новых лекарственных препаратов широкого спектра действия. При этом наиболее многообещающие результаты получены с использованием химически модифицированных фуллеренов C60 и C70, в основном содержащих ионогенные группы - аминные [6 - О. Troshina, P. Troshin, A. Peregudov, V. Kozlovski, R. Lyubovskaya. Photoaddition of N-Substituted Piperazines to C60: An Efficient Approach to the Synthesis of Water-Soluble Fullerene Derivatives. Chem. Eur. J., 12, 5569-5577 (2006)] и карбоксильные [7 - M. Brettereich, A. Hirsch. A highly water-soluble dendro [60] fullerene. Tetrahedron Lett.39, 2731-2734 (1998); 8 - O. Troshina, P. Troshin, A. Peregudov, V. Kozlovskiy, J. Balzarini, R. Lyubovskaya. Chlorofullerene C60Cl6: a precursor for straightforward preparation of highly water-soluble polycarboxylic fullerene derivatives active against HIV. Org. Biomol. Chem., 5, 2783-2791 (2007)].
Фуллерены и их производные проявляют выраженную противовирусную, противоопухолевую, нейропротекторную, антиамилоидную и другие активности [9 - Л.Б. Пиотровский, О.И. Киселев. Фуллерены в биологии. СПб, Росток, 2006]. Уникальное сочетание мембранотропных и амфифильных свойств функционализированных фуллеренов, определяющее их способность легко проходить через клеточные мембраны, благоприятствует созданию эффективных лекарственных средств на основе этого класса соединений. Кроме того, фуллерены могут быть использованы в качестве средств доставки других лекарственных препаратов в живые ткани и клетки.
Важным направлением возможного использования фуллеренов является разработка на их основе противоинфекционных (то есть противовирусных, антибактериальных и противогрибковых) средств. В этом случае важной мишенью их действия является липидная мембрана патогена: благодаря высокому сродству к ее внутренней гидрофобной части фуллерены накапливаются в липидном бислое, обуславливая нарушения ассоциированных с мембранами метаболических процессов [10 - А.К. Сироткин, Л.Б. Пиотровский, Л.Н. Познякова, О.И. Киселев. Влияние комплексов фуллерена C60 с поливинилпирролидоном на морфологию вирусов гриппа. Вопр. биол. мед. форм, химии, 2005, 3, 21 -24; 11 - N. Tsao, T.Y. Luh, С.К. Chou, T.Y. Chang, J.J. Wu, С.С.Liu, H.Y. Lei. In vitro action of carboxyfullerene. J. Antimicrobial Chemother., 2002, 49, 641-649]. Противомикробное действие производных фуллеренов усиливается при одновременном облучении видимым или ультрафиолетовым светом, что обусловлено способностью фуллеренов генерировать под воздействием света активные формы кислорода, вызывающие пероксидное окисление липидов биологических мембран [12 - J. Lee, Y. Mackeyev, М. Cho, D. Li, J.-H. Kim, L.J. Wilson, P.J.J. Alvarez. Photochemical and antimicrobial properties of novel С60 derivatives in aqueous systems. Environ. Sci. Technol., 43, 6604-6610 (2009)].
Несмотря на перспективность использования производных фуллеренов в качестве антимикробных терапевтических средств или дезинфектантов, ни одно из этих соединений пока не нашло практического применения в указанной области. Это может быть объяснено отсутствием соединений фуллеренов, обладающей устойчивой и выраженной биологической активностью в отношении широкого круга патогенных и условно-патогенных микроорганизмов.
Задачей данного изобретения является разработка высокоэффективных противомикробных средств на основе производных фуллеренов.
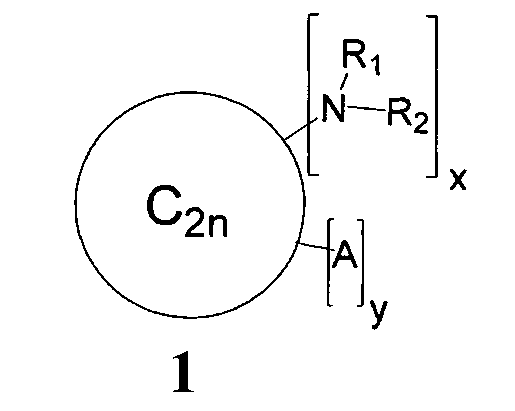
В настоящем изобретении эта задача решается путем применения аминопроизводных фуллеренов C60 и C70 общей формулы 1 в качестве действующего начала для создания противомикробных средств и композиций:

где в общей формуле 1 фрагмент C2n обозначает:
углеродный каркас фуллерена C60 (n=30), C70 (n=35) или углеродный наноматериал, называемый в научно-технической литературе «фуллереновый экстракт» и представляющий собой неразделенную смесь фуллеренов C60, C70 и высших фуллеренов (Cn>70);
где в общей формуле 1 «x» может принимать значения от 1-40, а «y» - от 0 до 30;
где в общей формуле 1 фрагмент А обозначает:
- одновалентный атом фтора или водорода, алкильный или арильный радикал, гидроксильную группу - OH, нитрогруппу - NO2, остаток азотистой кислоты - ONO;
трех-, четырех-, пяти- или шестичленный карбоциклический или гетероциклический фрагмент, аннелированный к фуллереновому каркасу;
- атом кислорода (-O-), присоединенный к фуллереновому каркасу в составе оксиранового фрагмента;
где в общей формуле 1 NR1R2 описывается нижеследующими определениями:
- остаток амина, где R1 и R2 - атомы водорода или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmH2m+1; n=1-20);
- остаток пиперазина общей формулы Ic-1,
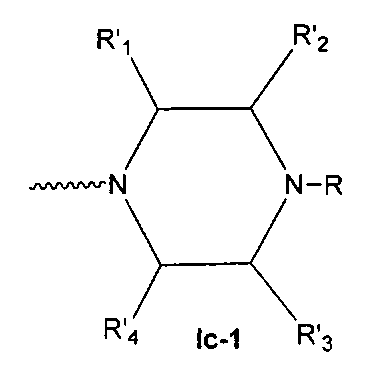
где R, R′1 R′2 R′3 и R′4 - это атомы водорода или линейные или разветвленные алкильные (CmH2m+1; n=1-20) радикалы, а также остатки алифатических спиртов - (СН2)nOH, простых эфиров - (CH2)nOR′5, тиолов - (CH2)nSH, кислот - (СН2)nCOOH, их сложных эфиров - (CH2)nCOOR′5 или амидов - (CH2)nCONR′5R′6, для которых n=0-20, а R′5 и R′6 - это атомы водорода или линейные алкильные (CmH2m+1; n=1-20) радикалы.
Способ получения аминопроизводных фуллеренов общей формулы 1 описан нами ранее в публикациях [13 - О.A. Troshina, P.A. Troshin, A.S. Peregudov, V.I. Kozlovskiy, R.N. Lyubovskaya, ″Photoaddition of N-substituted piperazines to С60: an efficient approach to synthesis of water-soluble fullerene derivatives″, Chem. Eur. J. 2006, 12, 5569; 14 - O.A. Troshina, P.A. Troshin, A.S. Peregudov, E.M. Balabaeva, V.I. Kozlovskiy, R.N. Lyubovskaya, ″Reactions of chlorofullerene C60Cl6 with N-substituted piperazines″, Tetrahedron 2006, 62, 10147-10151; 15 - P.A. Troshin, O.A. Troshina, S.M. Peregudova, E.I. Yudanova, A.G. Buyanovskaya, D.V. Konarev, A.S. Peregudov, A.N. Lapshin, R.N. Lyubovskaya, ″Chemical and electrochemical reduction of the highly chlorinated fullerenes C60Cl24 and C60Cl30″, Mendeleev Commun. 2006, 206-208; 16 - О.А. Трошина, П.A. Трошин, P.H. Любовская, Патент РФ «Водорастворимые аминофуллерены и способы их получения″, №2358904 от 25.12.2005; 17 - О.А. Трошина, диссертация на соискание ученой степени кандидата химических наук, Черноголовка, 2007, 18 - Н. Isobe, Т. Tanaka, W. Nakanishi, L. Lemiegre, E. Nakamura, Regioselective Oxygenative Tetraamination of [60] Fullerene. Fullerene-mediated Reduction of Molecular Oxygen by Amine via Ground State Single Electron Transfer in Dimethyl Sulfoxide. J. Org. Chem. 2005, 70, 4826-4832]. Предметом данного изобретения является применение указанных соединений общей формулы 1 в качестве противомикробных препаратов. Соединения общей формулы 1 могут использоваться индивидуально (в чистом виде) или в составе противомикробных композиций с эффективной концентрацией аминопроизводных фуллерена (от 0.0001 до 99.9%). Остальное - нейтральные компоненты или вещества, позитивно модифицирующие (усиливающие, пролонгирующие и т.д.) антимикробное действие композиции.
Состав нейтральных компонентов для лекарственных препаратов антибактериального действия известен из литературных источников. Так нейтральными компонентами для препаратов в форме порошков оптимальным является использование лактозы, сахарозы, сорбитола, маннитола, крахмала (картофельного и кукурузного), амилопектина, целлюлозы и ее производных, желатина, стеараты кальция и магния, воски на основе полиэтиленгликоля согласно ЕР 19840850211. В жидкой форме антибактериальный препарат может содержать в качестве разбавителя воду, а также глицерин, пропиленгликоль, этанол, сахара согласно ЕР 19840850211.
Разбавители и наполнители для антибактериальных препаратов дезинфецирующего действия известны из предшествующего уровня техники, например: Lange, ed., Handbook for Detergent Formulator s, Hanser-Gardner Publishers, Cincinnati, OH (1994); Sittig, Detergent Manufacture Including Zeolite Builders and Other New Materials, Noyes Publications, Park Ridge, NJ. (1979); Chemicals for the Detergent Industry, Business Communications, Inc., Norwalk, Conn. (1987); Cutler et al, Detergency: Theory and Technology, Dekker, New York (1987); Allured, ed., McCutcheon′s Functional Materials: International & North American Edition, MC Publishing Co., New Jersey (1995); Longman, The Analysis of Detergents and Detergent Products, Books on Demand, Ann Arbor, MI (1989).
Кроме того, антибактериальные препараты дезинфецирующего действия могут содержать нейтральные ароматизаторы, например содержащие гераниол, геранилацетат, линалол, линалилацетат, тетрагидролиналол, цитронеллол, цитронеллил ацетат, дигидромирценол, дигидромирценил ацетат, нопол ацетат, 2-фенилэтанол, 2-фенилэтилацетат, бензиловый спирт, бензилацетат, бензилсалицилат, бензилбензоат, стираллилацетат, амилсалицилат, диметилбензилкарбинол, изономил ацетат, ветиверилацетат, п-трет-бутилциклогексилацетат, ветиверол, альфа-н-амилциннальдегид, альфа-н-гексилциннальдегид, 2-метил-3-(п-трет-бутилфенил)пропаналь, 2-метил-3-(п-изопропилфенил)пропаналь, трициклодеценил ацетат, трициклодеценил пропионат, 4-(4-гидрокси-4-метилпентил)-3-циклогексенил карбальдегид, 4-ацетоки-3-пентилтетрагидропиран, метил дигидрожасмонат, 2-н-гептилциклогептанон, 3-метил-2-пентилциклопентанон, н-деканаль, н-додеканаль, 9-деценол-1, феноксиэтил изобутират, диметиловый ацеталь фенилацетальдегида, геранонитрил, цедрил ацетат, 3-изокамфилциклогексанол, аубепин, гелиотропин, кумарин, эвгенол, ванилин, дифениловый эфир, иононы, цис-3-гексенол и его сложные эфиры и др. согласно PCT/US 1996/016431.
Круг возможных промышленных ароматизаторов может включать LAVANDE (LAVENDER) PC 23696, CITRUS PC 23969, MIMOSA (JASMINE) PC 24309, ZESTY (GRAPEFRUIT) PC 24219, VIOLETTE (VIOLET) PC 27410, SPITZ PC 24736, POMME (APPLE) I PC 25003, CHYPRE PC 24447, GUM (BUBBLEGUM) II PC 27038, ZESTE (LEMON) PC 24449, ARDANTE PC 24448, V AN IL L AROME (VANILLA) PC 24217. PAOLA PC 24310, EUCALYPTUS PC 24583, NECTAR PE 24180, MUGUET PC 24311, GUM (BUBBLEGUM) I PC 24446, GRANY (GRANNY APPLE) PC 24453, CITRON (LIME)ELLE PC 24584, JASMIN PC 25512, CITRON (LIME)ADE PC 27039 согласно PCT/US 1996/016431.
Нейтральные компоненты могут представлять собой неионные поверхностно-активные вещества (ПАВ), такие как этиленоксилированные длинноцепочечные первичные спирты, содержащие от 12 до 18 углеродных атомов в алкильной группе и от 5 до 15 фрагментов этиленоксида (ЭО), этиленоксилированные алкилфеиолы, содержащие от 8 до 10 углеродных атомов в алкильной группе и от 5 до 8 фрагментов этиленоксида (ЭО), этиленоксилированные амиды жирных кислот, 12 до 18 углеродных атомов в остатке жирной кислоты и длинноцепочные аминооксиды, содержащие от 14 до 20 углеродных атомов. Предпочтительные примеры таких ПАВ включают нонилфенол этоксилат, нонилфенол конденсированный с этиленкосидом, нонилфениловый эфир полиэтиленгликоля согласно PCT/US 1996/016431.
Другие примеры нейтральных ПАВ известны из Myers, Surfactant Science and Technology, VCH Publishers, Inc., New York (1992); Rosen, Surfactants and Interfacial Phenomena, Wiley, New York (1984); Schick et al. Surfactant Science Series, Vols.1-22, Dekker, New York (1961-1987); Tadros, Surfactants, Academic Press, London (1984); патентов США №. 3,664,961 и 4,863,629.
Другими нейтральными компонентами могут быть гидрофильные материалы, такие как основы (пирофосфат калия), абразивы, красители, ингибиторы коррозии, защелачиватели мягчители, антистатические добавки, отбеливатели, загустители, водорастворимые полимеры, вододиспергируемые полимеры неорганические соли, стабилизаторы и органические растворители согласно PCT/US 1.996/016431.
Позитивно модифицирующие (усиливающие, пролонгирующие и т.д.) антимикробное действие добавки известны из предшествующего уровня техники и включают четвертичные аммонийные соли (например, дидецилдиметиламмоний бромид) и мочевину, известные, например, из патента РФ №2095086.
Наиболее близким известным аналогом изобретения является использование аминопроизводных фуллерена общей формулы 2 в качестве антибактериального и противоракового средства [18 - Т. Mashino. Antibacterial agent and anticancer agent. Патент EP 1611889 A1 от 04.01.2006]. Соединения формулы 2 представляют собой сложные смеси региоизомеров фуллереновых полиаддуктов и получаются лишь с очень небольшим выходом - порядка 9%, что затрудняет их практическое использование.

В отличие от описанных ранее соединений фуллеренов, проявляющих противомикробные свойства, производные фуллеренов, соответствующие общей формуле 1, отличаются простотой получения и низкой стоимостью и поэтому могут быть легко наработаны в больших количествах с целью практического использования. Кроме того, аминопроизводные фуллеренов формулы 1 являются амфифильными, так как имеют в своей структуре гидрофобные и гидрофильные фрагменты, что обеспечивает легкость их проникновения через клеточные мембраны. Это является важным преимуществом указанных производных по сравнению с большинством ранее описанных соединений (например, общей формулы 2), в которых каркас фуллерена равномерно покрыт заряженными группами.
Производные фуллеренов общей формулы 1, особенно те из них, которые содержат положительно заряженные группы, например аммонийные, обладают высокой ингибирующей активностью по отношению к различным грамположительным и грамотрицательным бактериям, что позволяет использовать их в качестве химиотерапевтических средств широкого спектра действия или дезинфектантов для обеззараживания загрязненных микроорганизмами сред и поверхностей. В основе противомикробного действия производных фуллеренов общей формулы 1 лежит их мембранотропная активность, то есть высокое сродство к мембранам микробных клеток, что было установлено с использованием метода атомно-силовой микроскопии (см. пример 1). Наиболее выраженной активностью при этом обладают катионные производные фуллеренов, поскольку они более эффективно связываются с отрицательно заряженными мембранами патогенных микроорганизмов за счет электростатического притяжения. Результатом же подобного взаимодействия является повреждение и гибель микробных клеток, что было установлено сочетанием бактериологического и биолюминесцентного методов.
Дополнительным фактором, обеспечивающим антибактериальную активность соединений общей формулы 1, является их способность повреждать ДНК микробных клеток. Повреждающее воздействие производных фуллерена на молекулы ДНК было установлено в экспериментах in vitro с помощью гель-электрофореза, а также in vivo с использованием репортерных генетических конструкций, отклик которых наблюдается в ответ на повреждения ДНК (см. пример 2).
Применение соединений общей формулы 1 в качестве компонентов противомикробных средств подразумевает, в том числе их использование для лечения и профилактики инфекционных заболеваний. С этой целью производные фуллеренов могут вводиться в организм для обеспечения системного эффекта, а также применяться местно для воздействия на определенные области (например, в составе перевязочных материалов для обработки ран, при обработке операционного поля и т.д.). Соединения фуллеренов могут использоваться в виде твердых веществ, растворов или суспензий в воде или других растворителях, а также нанесенными на различные носители. Возможно также использование соединений согласно формуле 1 в составе композиций с другими веществами, в том числе с противомикробными препаратами других классов.
В состав патентуемого изобретения входит также использование производных фуллерена общей формулы 1 для дезинфекции микробиологически загрязненных сред и поверхностей. Для проведения дезинфекции жидких и газовых сред производные фуллеренов могут вводиться в указанные среды в виде растворов, суспензий или аэрозолей, а также применяться в процессах фильтрования в виде чистых веществ или иммобилизованными на различных носителях. С целью обеззараживания твердых поверхностей аминофуллерены 1 могут наноситься на них в виде твердых частиц, растворов или суспензий. При этом для обеспечения длительной защиты от распространения микроорганизмов производное фуллерена может долгое время не удаляться из среды или с поверхности, подвергнутой дезинфекционной обработке.
Антимикробное действие производных фуллеренов может быть усилено при одновременном воздействии ультрафиолетового или видимого света, что связано со способностью фуллеренов выступать в качестве фотосенсибилизаторов, переводящих содержащийся в среде кислород в его активные формы (например, синглетный кислород или супероксид-анион-радикал). Фотохимическая генерация активных форм кислорода, осуществляемая производными фуллерена в непосредственной близости к липидной мембране или молекулам нуклеиновых кислот, приводит к окислительному повреждению этих структур и в конечном итоге к потере жизнеспособности микробной клетки. Возможность усиления антимикробной активности производных фуллеренов общей формулы 1 под воздействием света иллюстрируется примером 3. Благодаря этому свойству соединения фуллеренов согласно формуле 1 могут быть использованы в качестве средств для фотодинамической терапии инфекционных заболеваний, а также для фотохимической очистки загрязненных сред, в том числе поверхностей медицинского назначения и сточных вод.
Заявляемое изобретение иллюстрируется, но никак не ограничивается следующими примерами.
Пример 1. Оценка противомикробной активности производных фуллеренов
В качестве примеров аминопроизводных фуллеренов общей формулы 1 были использованы соединения 1а-в.
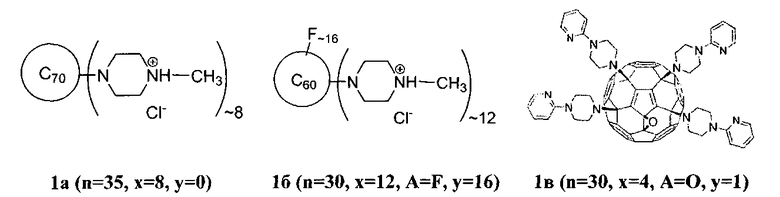

Определение антимикробной активности (концентрации LD50, вызывающей гибель 50% бактериальных клеток-мишеней после 60 минут контакта) проводилось на модельных грамотрицательном (Escherichia coli) и грамположительном (Bacillus subtilis) микроорганизмах в бактериологических тестах высева на плотные питательные среды. Одновременно исследовалось подавление производными фуллерена 1а-в свечения биолюминесцентных сенсорных систем на основе рекомбинантных штаммов Escherichia coli K12 TG1 и Bacillus subtilis B-10548 с клонированными luxCD(AB)E-генами природного морского люминесцирующего микроорганизма Photobacterium leiognathi. Характеристикой антимикробного действия в данном случае служила величина ЕС50 - концентрация исследованных производных фуллеренов, вызывающая подавление биолюминесценции к 60-й минуте контакта на 50% от контрольных значений.
Результаты определения противомикробной активности приведены в таблице 1.
Из приведенных значений активности видно, что катионные производные фуллерена C60 способны эффективно подавлять как грамположительные, так и грамотрицательные микроорганизмы в микромолярном диапазоне концентраций.
Для сравнения в таблице 1 приведены результаты определения антибактериальной активности немодифицированного фуллерена C60 и его поликарбоксильного производного, содержащего присоединенные остатки фенилуксусной кислоты. Видно, что указанные вещества совершенно не обладают противомикробной активностью. Поэтому именно использование аминопроизводных фуллеренов позволяет добиваться технически важного результата - высокой антимикробной активности.
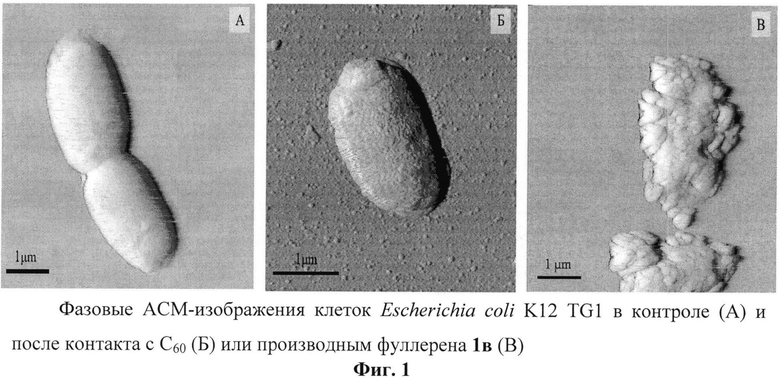
Прямое взаимодействие аминопроизводных фуллеренов с бактериальными клетками доказано с помощью атомно-силовой микроскопии. Полученные изображения интактных бактериальных клеток, а также клеток после контакта с фуллереном C60 и аминопроизводным фуллерена 1в приведены на Фиг.1.
После инкубации с аминопроизводным фуллерена 1в клетки Escherichia coli K12 TG1 претерпевали существенные морфологические изменения: происходило увеличение показателя шероховатости поверхности (с 2,34±0,67 нм до 14,98±7,56 нм), а также изменение геометрических размеров клеток, но без признаков высвобождения цитоплазматического содержимого во внешнюю среду. На поверхности бактерий наблюдалось образование гранул диаметром 33,6±24,0 нм, предположительно представляющих собой ассоциаты молекул производного фуллерена.
Пример 2. Генотоксическое воздействие производных фуллеренов на микроорганизмы
Доказательство возможности прямого повреждения ДНК in vitro было получено при исследовании плазмидной ДНК с помощью гель-электрофореза до и после контакта с аминопроизводными фуллеренов.
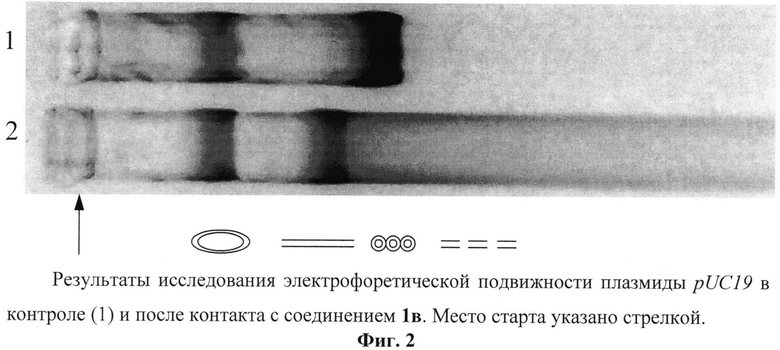
Плазмида pUC19 была инкубирована в течение 15 минут с производным 1в в концентрации 1 мкМ. При анализе электрофоретической подвижности было установлено, что исходно данная молекула ДНК существовала в двух основных конформациях: кольцевой суперскрученной и кольцевой релаксированной (дорожка 1 на Фиг.2). После контакта с производным 1в наблюдалось исчезновение суперскрученной конформации, переход значительного количества кольцевых молекул ДНК в линеаризованные с деградацией последних до более мелких фрагментов с формированием соответствующего «шмера» (дорожка 2 на Фиг.2). Таким образом, результатом воздействия производных фуллерена на молекулы ДНК является изменение конформации молекул биополимера и образование в них двуцепочечных разрывов.
Для изучения возможности повреждения ДНК бактериальных клеток in vivo была использована репортерная клеточная система на основе штамма Esherichia coli, несущего luxCDABE-гены Photorhabdus luminescence, клонированные под промотором гена recA, являющегося активатором SOS-ответа бактериальных клеток при воздействии физических и химических ДНК-повреждающих факторов. В результате запуск процесса репарации ДНК при ее повреждении закономерно сопровождается возникновением свечения данной репортерной системы, что позволяет с ее использованием оценивать качественные и количественные характеристики активности различных генотоксикантов.
После инкубации репортерного штамма Е. coli с соединением 1в наблюдалась двукратная индукция свечения генетической конструкции recA′::lux, что может интерпретироваться как индуцируемое данным аминопроизводным C60-фуллерена повреждение ДНК бактериальных клеток-мишеней.
Пример 3. Усиление противобактериальной активности производных фуллеренов под действием облучения
Фотосенсибилизирующие свойства производных фуллеренов были изучены с использованием сенсорного люминесцирующего штамма Escherichia coli K12 TG1 с клонированными luxCDABE-генами морского люминесцирующего микроорганизма Photobacterium leiognathi.
Суспензия клеток сенсорной бактериальной системы смешивалась с водным раствором производных фуллеренов 1а и 1в соответствующих концентраций, после чего проводилось их облучение светом ртутно-кварцевой лампы в течение 5, 10 или 15 минут. После дополнительного инкубирования в течение 15 минут измеряли уровень биолюминесценции исследуемых проб и рассчитывали значения EC50, характеризующие эффективные концентрации производных фуллеренов, вызывающие тушение биолюминесценции сенсорного микроорганизма на 50% по сравнению с контролем.
Результаты определения противомикробного действия производных фуллеренов в темноте и при облучении ультрафиолетовым светом представлены в таблице 2. Видно, что противобактериальное действие исследованных производных 1а и 1в значительно усиливается под воздействием УФ-облучения, что проявляется в значимом снижении регистрируемых значений EC50.
Пример 4. Композиция противобактериального действия на основе производного фуллерена 1в и АОБ
Была исследована антибактериальная композиция производного фуллерена 1в с 4-гексилбензол-1,3-диолом (гексилрезорцин). Алкилоксибензолы (АОБ) представляют собой химические аналоги одного из типов регуляторных молекул у микроорганизмов.

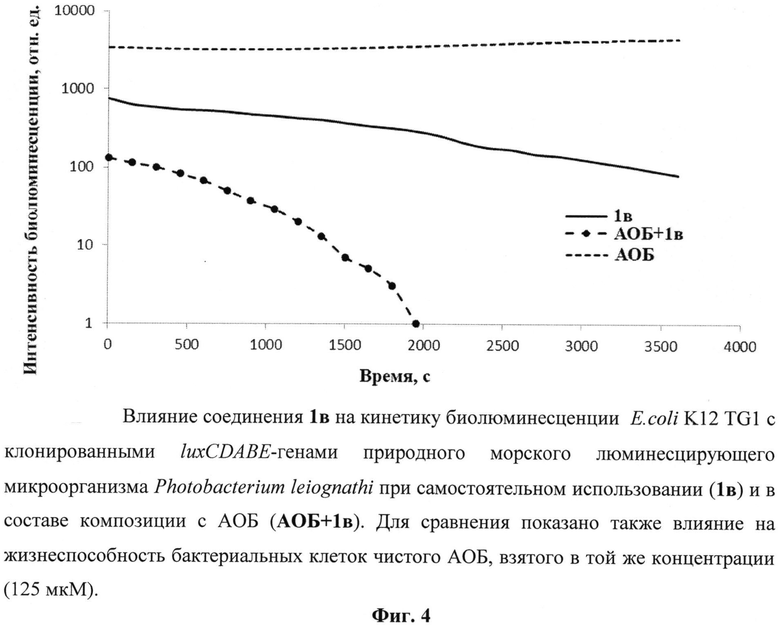
Производное фуллерена 1в обладает сравнительно слабой антибактериальной активностью и потому представляет интерес ее повышение при использовании композиций с АОБ. Исследовалось воздействие композиции на бактериальные клетки E.coli K12 TG1 с клонированными luxCDABE-генами природного морского люминесцирующего микроорганизма Photobacterium leiognathi. Показано, что АОБ в диапазоне концентраций 62,5-250 мкМ более чем в два раза снижает значения EC50, т.е. потенцирует антибактериальный эффект 1в (Фиг.3). Чистый АОБ в указанном диапазоне концентраций не влияет на биолюминесценцию и жизнеспособность бактериальных клеток на протяжении времени эксперимента (Фиг.4). Приведенный пример подтверждает возможность создания и использования композиций антибактериального действия на основе производных фуллерена общей формулы 1 и дополнительных компонентов, использование которых по такому назначению было раскрыто ранее (см. выше).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ ПЕНТААМИНОФУЛЛЕРЕНОВ В КАЧЕСТВЕ ПРОТИВОМИКРОБНЫХ СРЕДСТВ И ПРОТИВОМИКРОБНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2011 |
|
RU2501785C2 |
| ФОСФОРСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНА C И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2509083C2 |
| АРИЛИРОВАННЫЕ ПОЛИКАРБОКСИЛЬНЫЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ КОВАЛЕНТНЫЕ КОНЪЮГАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2567299C2 |
| Применение водорастворимых производных фуллерена в качестве лекарственных препаратов нейропротекторного и противоопухолевого действия | 2017 |
|
RU2704483C2 |
| СЕРОСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ФУЛЛЕРЕНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2477273C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОПРОПАНОВЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ, ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ В КАЧЕСТВЕ МАТЕРИАЛОВ ДЛЯ ЭЛЕКТРОННЫХ ПОЛУПРОВОДНИКОВЫХ УСТРОЙСТВ, ОРГАНИЧЕСКОГО ПОЛЕВОГО ТРАНЗИСТОРА, ОРГАНИЧЕСКОЙ ФОТОВОЛЬТАИЧЕСКОЙ ЯЧЕЙКИ, ОРГАНИЧЕСКИЙ ПОЛЕВОЙ ТРАНЗИСТОР И ОРГАНИЧЕСКАЯ ФОТОВОЛЬТАИЧЕСКАЯ ЯЧЕЙКА | 2011 |
|
RU2519782C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФУЛЛЕРЕНА С | 2010 |
|
RU2456233C2 |
| Применение пентааминокислотных производных фуллеренов в качестве антиоксидантов и антидиабетических средств | 2016 |
|
RU2669341C2 |
| НАНОАГРЕГАТЫ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИИ НА ОСНОВЕ НАНОАГРЕГАТОВ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ, ПРИМЕНЕНИЕ НАНОАГРЕГАТОВ ВОДОРАСТВОРИМЫХ ПРОИЗВОДНЫХ ФУЛЛЕРЕНОВ И КОМПОЗИЦИЙ НА ИХ ОСНОВЕ В КАЧЕСТВЕ БИОЛОГИЧЕСКИ-АКТИВНЫХ СОЕДИНЕНИЙ, ДЛЯ ПОНИЖЕНИЯ ТОКСИЧНОСТИ И УСИЛЕНИЯ ТЕРАПЕВТИЧЕСКОГО ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, А ТАКЖЕ В КАЧЕСТВЕ ПРЕПАРАТОВ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2550030C2 |
| Способ получения аддуктов легких фуллеренов с L-аминокислотами | 2024 |
|
RU2837394C1 |

Изобретение относится к химическо-фармацевтической промышленности и касается применения производных фуллеренов общей формулы 1
где в общей формуле 1 фрагмент C2n обозначает:
углеродный каркас фуллерена C60 (n=30), C70 (n=35);
где в общей формуле 1 «x» может принимать значения от 4 до 12, а «y» - от 0 до 16;
где в общей формуле 1 фрагмент А обозначает:
- одновалентный атом фтора или водорода;
- атом кислорода (-O-), присоединенный к фуллереновому каркасу в составе оксиранового фрагмента;
где в общей формуле 1 NR1R2 описывается нижеследующими определениями:
- остаток амина, где R1 и R2 - атомы водорода или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmH2m+1; m=1-20);
- остаток пиперазина общей формулы Ic-1,

где R, R′1, R′2 R′3 и R′4 - это атомы водорода или линейные или разветвленные алкильные (CmH2m+1 m=1-20) радикалы.
в качестве противомикробных средств, а также противомикробной композиции включающей производные фуллеренов. Изобретение может быть использовано в биомедицинских исследованиях и в производстве новых лекарственных препаратов, предназначенных для лечения и профилактики инфекционных заболеваний, а также для создания дезинфекционных агентов, предназначенных для обеззараживания и стерилизации загрязненных микроорганизмами сред и поверхностей. 2 н.п. ф-лы, 4 пр., 2 табл., 4 ил.
1. Применение производных фуллеренов общей формулы 1 в качестве противомикробных препаратов.

где в общей формуле 1 фрагмент C2n обозначает:
углеродный каркас фуллерена C60 (n=30), C70 (n=35);
где в общей формуле 1 «x» может принимать значения от 4 до 12, а «y» - от 0 до 16;
где в общей формуле 1 фрагмент А обозначает:
- одновалентный атом фтора или водорода;
- атом кислорода (-O-), присоединенный к фуллереновому каркасу в составе оксиранового фрагмента;
где в общей формуле 1 NR1R2 описывается нижеследующими определениями:
- остаток амина, где R1 и R2 - атомы водорода или замещенные протонированными (NH3 +) или непротонированными (NH2) аминогруппами линейные или разветвленные алкильные радикалы (CmH2m+1; m=1-20);
- остаток пиперазина общей формулы Ic-1,

где R, R′1, R′2 R′3 и R′4 - это атомы водорода или линейные или разветвленные алкильные (CmH2m+1 m=1-20) радикалы.
2. Противомикробная композиция, содержащая по весу от 0,0001 до 99.9% производного фуллерена общей формулы 1, остальное - инертные разбавители или компоненты, усиливающие противомикробное действие производного фуллерена общей формулы 1 или сами обладающие противомикробным действием.
| ВОДОРАСТВОРИМЫЕ АМИНОФУЛЛЕРЕНЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2358904C2 |
| Трошина А.О.: "Получение водорастворимых производных фуллеренов, исследование их физико-химических свойств и биологической активности"/автореферат, Черноголовка, 2007 | |||
| NINA TSAO ET AL.: "In vitro action of carboxyfullerene"/J | |||
| of Antimicrobal Chemotherapy, 2002, 49, 641, 649 | |||
| Семенов К.: "Нанолекарства от химиков | |||
Авторы
Даты
2014-07-10—Публикация
2011-08-30—Подача