Область техники
Изобретение относится к медицине и иммунологии, и представляет собой принципиально новый способ проведения диагностики, основанный на определении белковых молекул - антител - к специфичной и чувствительной комбинации опухоле-ассоциированных гликанов (сигнатуре) на фоне индивидуальных особенностей конкретного больного. Данное изобретение может найти применение в иммунологии и медицине для исследования и диагностики рака молочной железы.
Уровень техники
Рак молочной железы является одним из наиболее значимых заболеваний у женщин, характеризующийся высоким уровнем заболеваемости и являющийся ведущей онкологической патологией у женщин старше 40 лет. Раннее выявление рака молочной железы является социально значимой задачей современного здравоохранения.
На сегодняшний день диагностика рака молочной железы представляет собой комплексное обследование пациента, включающего в себя индивидуальный врачебный осмотр, а также инструментальные методы исследования: маммографию, ультразвуковое обследование, биопсия. К сожалению, в большинстве случаев заболевание диагностируется на довольно поздней стадии.
Важной составляющей диагностики является определение опухоль-ассоциированных антигенов в сыворотке крови пациента. Многочисленные исследования выявили множество антигенов, ассоциированных с раком молочной железы человека и характеризующих биологические особенности опухоли - пролиферативную активность, гормональную чувствительность, выраженность метастазирования. Однако до сих пор не найдено ни одного маркера, специфичного только для опухоли.
Например, СА15-3, широко используется при наблюдении за течением заболевания и возникновением рецидивов, зарекомендовавший себя как высокоспецифичный маркер отдаленных метастазов со специфичностью 96% (I. P. Tomlinson, A. Whyman, J. A. Barrett, J. K. Kremer. Tumour marker СА15-3: possible uses in the routine management of breast cancer Eur J Cancer. 1995 Jun; 31A(6): 899-902). Однако он не обладает достаточной чувствительностью и специфичностью для диагностики на ранней стадии рака (не более 60% (М.Л. Алексеева Е.В. Гусарова С.М. Муллабаева Т.С. Понкратова. Онкомаркеры, их характеристика и некоторые аспекты клинико-диагностического использования. Пробл. Репрод. 3, 65-79 (2005)). Группа онкофетальных антигенов - раковоэмбриональный антиген (РЭА) и тканевый полипептидный антиген (ТРА) - также не являются специфичными к опухолевым клеткам, их определение используют только для оценки прогноза и ранней диагностики отдаленных метастазов. Сочетанное определение уровня РЭА, ТРА и СА15-3 в крови больных раком молочной железы увеличивает чувствительность и специфичность оценки эффективности лечения и прогноза до 90% (A. Nicolini, С. Colombini, L. Luciani, A. Carpi, L.Giuliani. Evaluation of serum СА15-3 determination with CEA and ТРА in the postoperative follow-up of breast cancer patients. Br. J. Cancer. 64(1), 154-158 (1991)), но не диагностики.
В клинической практике довольно часто наблюдаются случаи, когда уровень онкомаркеров был в границах нормы, несмотря на наличие злокачественной опухоли у пациента. Такая ситуация нередка при начальных стадиях развития опухоли. В связи с этим, онкомаркеры обычно используются только при профилактических исследованиях пациентов, входящих в группы риска развития новообразований, а также при мониторинге установленного лечения.
Благодаря работе Хакомори (S. Hakomori Tumor-associated carbohydrate antigens. Annu Rev Immunol. 2, 103-126 (1984)), практический интерес онкологов вызывает класс гликановых антигенов, известных как опухоле-ассоциированные углеводные антигены (TACAs), присутствующие на поверхности клеток, компонентах тканей и в кровотоке. TACAs детектируются на всех злокачественных новообразованиях, являясь результатом онкологической трансформации и играя роль ключевых молекул при метастазировании. Не последнюю роль при онкотрансформации играют анти-гликановые антитела (Е.Р. Smorodin, О.А. Kurtenkov, B.L. Sergeyev, K.E. Kodar, V.I. Chuzmarov, V.P. Afanasyev. Postoperative change of anti-Thomsen-Friedenreich and Tn IgG level: the follow-up study of gastrointestinal cancer patients. World J. Gastroenterol. 14(27), 4352-4358 (2008), Schwartz-Albiez R. Naturally occurring antibodies directed against carbohydrate tumor antigens. Adv. Exp. Med. Biol. 750, 27-43 (2012)). Основным инструментом для изучения анти-гликановых антител является гликочип или гликановый эррей (O. Blixt, et al.. Printed covalent glycan array for ligand profiling of diverse glycan binding proteins Proc. Natl. Acad. Sci. USA. 101 (49), 17033-17038 (2004)). С помощью этого метода были исследованы профили антител здоровых доноров (М.Е. Huflejt, M. Vuskovic, D. Vasiliu, H. Xu, P. Obukhova, N. Shilova, A. Tuzikov, O. Galanina, B. Arun, K. Lu, N.V. Bovin. Anti-carbohydrate antibodies of normal sera: findings, surprises and challenges. Mol. Immunol. 46(15), 3037-3049 (2009)), а также больных раком, например, лимфомой Ходжкина (С.Н. Lawrie, Т. Marafloti, C.S. Hatton, S. Dimhofer, G. Roncador, P. Went, A. Tzankov, S.A. Pileri, K. Pulford, A.H. Banham. Cancer-associated carbohydrate identification in Hodgkin's lymphoma by carbohydrate array profiling. Int. J. Cancer. 118, 3161-3166 (2006)) и раком яичника (F. Jacob, D.R. Goldstein, N.V. Bovin, T. Pochechueva, M. Spengler, R. Caduff, D. Fink, M. Vuskovic, М.Е. Huflejt, V. Heinzelmann-Schwarz. Serum antiglycan antibody detection of nonmucinous ovarian cancers by using a printed glycan array. Int. J. Cancer. 130(1), 138-146 (2012)). [1]. Подход, описанный в статье [1] является ближайшим аналогом данного изобретения.
Согласно цитированной статье [1], поиск нового поколения маркеров немуцинозного рака яичника осуществляли с помощью гликанового эррея, содержащего 203 олигосахаридные структуры. В исследовании участвовали 24 здоровых донора и 33 больных раком яичника. Посредством кластерного анализа был выявлен паттерн антител к специфическим углеводным структурам, состоящий из 10 гликанов. Найденный паттерн позволил авторам [1] достоверно различить здоровых доноров и раковых больных (чувствительность и специфичность составили 79,2 и 84,8%, соответственно). Однако данный подход лишь незначительно улучшил характеристики классической тест-системы, основанной на параллельном определении опухолевого маркера СА125 (методом иммуноферментного анализа). Подобных работ в области рака молочной железы не проводилось.
Раскрытие изобретения
Задачей изобретения является создание специфичного и чувствительного способа проведения диагностики рака молочной железы.
Техническим результатом изобретения является специфичная и чувствительная комбинация опухоле-ассоциированных гликанов.
Технический результат достигается способом диагностики рака молочной железы, заключающимся в том, что в крови человека детектируют антитела, направленные к следующим гликанам: Manβ1-4GlcNAcβ, Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα, НОСН2(НОСН)4CH2NH2, GlcAβ, Galα, 6-O-Su-GlcNAcβ, GalNAcβ1-3Galβ, 6-O-Su-Galβ1-4(6-O-Su)Glcβ, GlcAβ1-3Galβ, Neu5Acα2-3Galβ1-4Glcβ, GlcNAcβ1-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ, Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ, Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ с помощью микрочипа с нанесенными на него указанными гликанами и, по наличию в крови уровня антител выше порогового одновременно ко всем указанным гликанам, диагностируют рак молочной железы.
Настоящим изобретением предлагается способ диагностики рака молочной железы, основанный на детектировании углевод-связывающих белковых молекул - антител к комбинации углеводных лигандов (гликанов) с помощью микрочипа. Данные антитела детектируются в исследуемых образцах сыворотки крови одновременно при помощи вторичных антител, содержащих флуоресцентную метку, или любой другой системой визуализации. Лиганды представляют собой олигосахариды, и/или полисахариды, и/или пептиды, и/или гликопептиды, и/или биотин. Один чип содержит множество индивидуальных лигандов. Часть из них служат в качестве положительного и отрицательного контролей работы микрочипа.
Эффективность использования комбинации маркеров была показана в работе (R. Radpour, Z. Barekati, C. Kohler, Q. Lv, N. Bürki, C. Diesch, J. Bitzer, H. Zheng, S. Schmid, X.Y. Zhong. Hypermethylation of tumor suppressor genes involved in critical regulatory pathways for developing a blood-based test in breast cancer. PLoS One. 6(1), el 6080. (2011)) при разработке эпигенетического теста на рак молочной железы в крови пациентов. Тест основан на фиксировании изменений в метилировании участков генов-супрессоров опухолевого роста при раке молочной железы. Авторы показали, что чувствительность и специфичность диагностики существенно возрастает, если использовать комбинацию из 8 генов вместо одного, можно увеличить чувствительность и специфичность до уровня более, чем 90%. Однако, как отмечают авторы (Van De Voorde L, Speeckaert R, Van Gestel D, Bracke M, De Neve W, Delanghe J, Speeckaert M. DNA methylation-based biomarkers in serum of patients with breast cancer. Mutat. Res. 751(2), 304-325 (2012)), следует с осторожностью относится к эпигенетическим маркерам, таким как метилирование ДНК, поскольку они достаточно сильно подвержены влиянию нормальных физиологических процессов, таких как, например, старение.
В настоящем изобретении тот же принцип объединения нескольких маркеров в диагностическую комбинацию лигандов (сигнатуру) приложен для диагностики рака молочной железы. По сравнению с указанным выше подходом [1] подобное объединение принципиально улучшило чувствительность и специфичность диагностики, поскольку существующие на сегодняшний день биомаркеры рекомендованы к использованию только с целью оценки эффективности лечения и профилактических исследований, но не для диагностики.
Далее, изобретение иллюстрируется ссылками на рисунки, а также примерами, которые приводятся исключительно с целью иллюстрации и пояснения сущности заявленного изобретения, но которые не предназначены для ограничения объема притязаний.
Список использованных сокращений
ROC-анализ - анализ взаимодействия чувствительности и представительности
AUC - площадь под ROC-кривой, показатель точности диагностического теста;
CMG - диглицил-Н-карбоксиметилглицин;
BovSlOG - Ser-Ala-Pro-Asp-Thr-Arg-Pro-Ala-Pro-Gly-NH2;
ИФБ - 0,1 М изотонический фосфатный буфер (0,01 М Na2HPO4, 0,01 М NaH2PO4, 0,138 М NaCl и 0,0027 М KCl, рН 7,4).
ИФБ - 1%, 0,1%, 0,05% - ИФБ, содержащий 1, 0,1 и и 0,05% Tween20, соответственно;
БСА - бычий сывороточный альбумин;
Ig(G+M+A) - иммуноглобулины классов G, M, A.
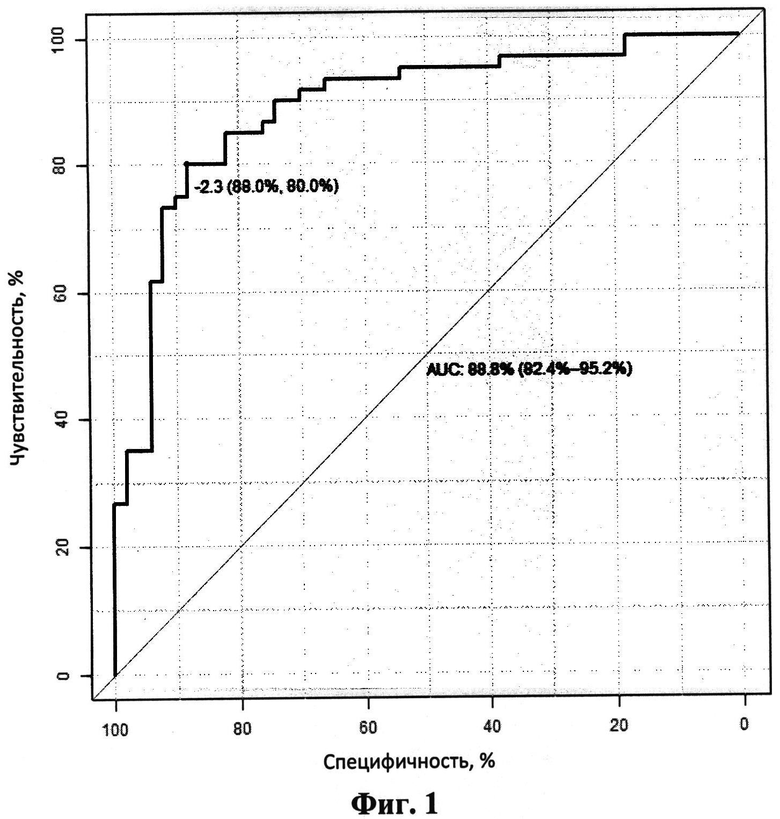
Фиг.1 демонстрирует результаты ROC-анализа эффективности диагностики рака молочной железы, основанной на использовании сигнатуры из 15 гликанов. Рядом с кривой приведена величина порогового значения с соответствующими показателями специфичности и чувствительности, а также величина AUC с доверительными интервалами.
Осуществление изобретения
Настоящее изобретение обеспечивает способ проведения диагностики рака молочной железы, основанный на определении белковых молекул - антител - к специфичной и чувствительной комбинации опухоле-ассоциированных гликанов (сигнатуре) на фоне индивидуальных особенностей конкретного больного.
Способ диагностики рака молочной железы по данному изобретению заключается в одновременном детектировании углевод-связывающих белковых молекул - антител D в исследуемых образцах сыворотки крови к сигнатуре из углеводных лигандов, специфичных для рака молочной железы, с использованием микрочипов. Антитела детектируются одновременно при помощи вторичных антител, содержащих флуоресцентную метку, либо любой другой системы визуализации антител.
В качестве лигандов микрочипа используются амино-спейсерированные олигосахариды, а также полисахариды (наличие спейсера у последних не обязательно), а также вещества неуглеводной природы, такие как биотин и пептиды. Лиганды, не входящие в сигнатуру, находятся на чипе в качестве положительного и отрицательного контролей.
Выбор гликанов, включаемых в сигнатуру, проводился на основании непараметрического теста Уилкоксона-Манна-Уитни (WMW) для дискриминации групп здоровых доноров и пациентов с раком молочной железы. На основании этого теста гликаны ранжировались, а затем последовательно суммировались в сигнатуру; при этом каждый последующий добавляемый гликан не должен был ухудшать точность теста.
При использовании в качестве маркера только одного гликана - Manβ1-4GlcNAcβ - точность теста была лишь средней (AUC=0,693), при объединении уже двух гликанов точность теста возрастала до 0,737, что уже является хорошим показателем. При использовании сигнатуры из 15 гликанов величина AUC составляла - 0,888, что соответствует очень хорошей точности теста.
Таким образом, предлагаемый способ позволяет диагностировать рак молочной железы с использованием сигнатуры из 15 гликанов с точностью 88,8% (доверительный интервал 82,4-95,2%) и показателями чувствительности и специфичности 80 и 88%, соответственно. Соответствующие результаты ROC-анализа приведены на фиг.1. Регистрируемая величина - «отклик сигнатуры» - рассчитывается как сумма сигналов с проявленного биочипа от перечисленных ниже 15 гликанов (знак суммирования приведен после каждого гликана), преобразованных как описано в Примере: 1. Manβ1-4GlcNAcβ (+), 2. Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα (+), 3. НОСН2(НОСН)4CH2NH2 (+), 4. GlcAβ (-), 5. Galα (+), 6. 6-O-Su-GlcNAcβ (-), 7. GalNAcβ1-3Galβ (-), 8. 6-O-Su-Galβ1-4(6-O-Su)Glcβ (+), 9. GlcAβ1-3Galβ (+), 10. Neu5Acα2-3Galβ1-4Glcβ (+), 11. GlcNAcβ1-3Galβ1-3GalNAcα (-), 12. Neu5Acα2-3Galβ1-3GalNAcα (-), 13. Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ (+), 14. Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ (+), 15. Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ (+).
Эффективность найденной сигнатуры протестировали на группе из 50 доноров («Заболевание отсутствует») и 60 пациентов с раком молочной железы («Заболевание присутствует»). Для всех пациентов диагноз был ранее подтвержден хирургическими методами. Полученные результаты приведены в Таблице. Как видно из Таблицы, часть результатов является ложноположительными (доноры, для которых тест показал положительный результат), а часть - ложноотрицательными (пациенты, для которых тест показал отрицательный результат), что, однако, не является критическим и соответствует очень хорошей точности разработанного диагностического теста.
Приведенный ниже пример предназначен не для ограничения притязаний, а исключительно для иллюстрации отдельных воплощений настоящего изобретения.
Пример. Использование микрочипа для диагностики рака молочной железы.
Для конструирования чипа использовались следующие гликаны и другие лиганды.
1. Спейсерированные олигосахариды: Manβ1-4GlcNAcβ, Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα, НОСН2(НОСН)4CH2NH2, GlcAβ, Galα, 6-O-Su-GlcNAcβ, GalNAcβ1-3Galβ, 6-O-Su-Galβ1-4(6-O-Su)Glcβ, GlcAβ1-3Galβ, Neu5Acα2-3Galβ1-4Glcβ, GlcNAcβ1-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ, Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ, Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ.
2. Гликопептид GlcNAcβ1-[НООС(СН3)СН]-3-O-GlcNAcβ-L-аланил-D-изоглутаминил-L-лизин.
3. Полисахариды: Escherichia coli 052, 058, 073.
4. Биотин в виде производного с 6-аминогексановым спейсером.
5. Пептиды BovS10G и CMG.
Спейсерированные гликаны или другие лиганды растворяли в 300 мМ фосфатном буфере, рН 8,0, содержащем 0.005% Tween 20, в концентрации 50 мкМ и наносили их на поверхность N-гидроксисукцинимид-активированных слайдов Н (Schott Nextenon, Германия) с помощью устройства для контактной печати OmniGrid II (Digilab, США), как описано в работе (Blixt О., et al., Printed covalent glycan array for ligand profiling of diverse glycan binding proteins, Proc. Natl. Acad. Sci. USA, 2004, v.101 (49), p.17033-17038). После последовательного нанесения всех лигандов, чип выдерживали в течение 1 ч при комнатной температуре и относительной влажности 80%, после чего блокировали оставшиеся непрореагировавшие активированные группы поверхности 100 мМ раствором борной кислоты (Хеликон, Россия), содержащим 25 мМ этаноламин (Merck, США) и 0,2% Tween-20, рН8,5. Заблокированные микрочипы промывали бидистиллированной водой и высушивали центрифугированием.
В исследовании участвовали 50 здоровых доноров и 60 пациентов с хирургически подтвержденным раком молочной железы.
Анализ сыворотки крови доноров и пациентов осуществляли следующим образом:
Чипы выдерживали в течение 15 мин в ИФБ, содержащем 0,1% Tween-20 (ИФБ - 0,1%), затем прибавляли 200 мкл исследуемой сыворотки крови донора или пациента, разбавленной в 15 раз с помощью ИФБ - 1%, содержащим 1% БСА и выдерживали на шейкере при относительной влажности 80% в течение 1 ч при 37°С. Затем чипы промывали ИФБ-0,05% и прибавляли 200 мкл раствора биотинилированных антител козы против человеческих иммуноглобулинов Ig(G+M+A) (ThermoSci, США), разведение 1:200 в ИФБ - 0,1%, содержащем 1% БСА. После инкубации на шейкере при относительной влажности 80% в течение 1 ч при 37°С чип промывали ИФБ - 0,05% и прибавляли раствор стрептавидина, меченого флуоресцентным красителем Alexa555, разведение 1:1000 в ИФБ - 0,1%. После инкубации чипов в течение 40 мин при комнатной температуре в отсутствие света, их промывали сначала ИФБ - 0,05%, затем бидистиллированной водой и высушивали центрифугированием. Изображения получали с помощью конфокального сканера ProScanArray Gx (PerkinElmer, США) с разрешением 5 мкм (мощность лазера 90%). Полученные файлы просматривали и обрабатывали с помощью программного обеспечения ScanArray Express 3.0 и Microsoft Excel.
Для расчета отклика сигнатуры полученные с чипов сигналы - относительные флуоресцентные единицы - сначала нормализовали по приведенным ниже формулам для линейной нормализации:
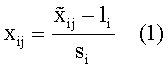
где 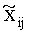
Параметры li и si определяли для каждого пациента (донора) независимо:
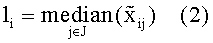
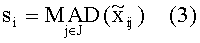
где J - набор индексов колонок, которые соответствуют гликанам, а также контрольным соединениям.
После чего данные подвергали процедуре нормализующего преобразования Бокса-Кокса (Box G.E.P., Сох D.R., An analysis of transformations. J R Stat Soc, 1964. В 26: p.211-252) с учетом отрицательных значений данных (согласно рекомендациям авторов (John J. A., Draper N. R., An alternative family of transformations. Appl Stat, 1980. 29: p.190-197)):
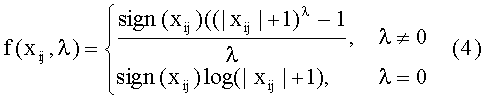
где λ - степень параметра преобразования, равная 0,2.
Отклик сигнатуры рассчитывали как сумму преобразованных сигналов от перечисленных ниже 15 гликанов (знак суммирования приведен после каждого гликана): 11. Manβ1-4GlcNAcβ (+), 2. Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα (+), 3. НОСН2(НОСН)4CH2NH2 (+), 4. GlcAβ (-), 5. Galα (+), 6. 6-O-Su-GlcNAcβ (-), 7. GalNAcβ1-3Galβ (-), 8. 6-O-Su-Galβ1-4(6-O-Su)Glcβ (+), 9. GlcAβ1-3Galβ (+), 10. Neu5Acα2-3Galβ1-4Glcβ (+), 11. GlcNAcβ1-3Galβ1-3GalNAcα (-), 12. Neu5Acα2-3Galβ1-3GalNAcα (-), 13. Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ (+), 14. Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ (+), 15. Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ (+).
Если полученная величина была выше порогового значения в -2,3, то результат анализа считали положительным (рак есть), если ниже - результат отрицательный (рака нет).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕЧАТИ БИОЛОГИЧЕСКИХ ЛИГАНДОВ В ПРОЦЕССЕ ИЗГОТОВЛЕНИЯ БИОЧИПОВ | 2012 |
|
RU2543145C2 |
| СПОСОБ ОБНАРУЖЕНИЯ САХАРНЫХ ЦЕПЕЙ С GlcNAc, СИНТЕЗИРОВАННЫХ GnT-V | 2006 |
|
RU2442989C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ, КОДИРУЮЩИЕ АНТИТЕЛА ПРОТИВ СИАЛИРОВАННОГО АНТИГЕНА ЛЬЮИСА ЧЕЛОВЕКА | 2014 |
|
RU2699289C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ, КОДИРУЮЩИЕ АНТИТЕЛА ПРОТИВ СИАЛИРОВАННОГО АНТИГЕНА ЛЬЮИСА ЧЕЛОВЕКА | 2014 |
|
RU2791967C2 |
| АДАПТАЦИЯ ВИРУСА ГРИППА Н5 К ЧЕЛОВЕКУ | 2014 |
|
RU2708447C2 |
| Гуманизированные антитела к антигену Томсена-Фриденрайха | 2015 |
|
RU2699717C2 |
| ТЕРАПЕВТИЧЕСКИЕ АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С БИАНТЕННАРНЫМИ АНТИГЕНАМИ ЛЬЮИСА B И ЛЬЮИСА Y | 2019 |
|
RU2803097C2 |
| Способ диагностики/скрининга колоректального рака, основанный на одновременном количественном определении онкомаркеров белковой природы, антител к гликанам, иммуноглобулинов G, А и М в крови человека на биологическом микрочипе | 2015 |
|
RU2625018C2 |
| КОМПОЗИЦИИ УГЛЕВОДНОЙ ВАКЦИНЫ ДЛЯ ИНДУКЦИИ ИММУННОГО ОТВЕТА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ РАКА | 2014 |
|
RU2666141C2 |
| СПОСОБЫ И РЕАГЕНТЫ ДЛЯ ПРЕДУПРЕЖДЕНИЯ И/ИЛИ ЛЕЧЕНИЯ ИНФЕКЦИИ | 2015 |
|
RU2698099C2 |
Изобретение относится к медицине и иммунологии и представляет собой новый способ проведения диагностики, основанный на определении белковых молекул - антител - к специфичной и чувствительной комбинации опухоле-ассоциированных гликанов на фоне индивидуальных особенностей конкретного больного. Данное изобретение может найти применение в иммунологии и медицине для исследования и диагностики рака молочной железы. В способе диагностики рака молочной железы детектируют в крови человека антитела, направленные к следующим гликанам: Manβ1-4GlcNAcβ, Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα, HOCH2(HOCH)4CH2NH2, GlcAβ, Galα, 6-O-Su-GlcNAcβ, GalNAcβ1-3Galβ, 6-O-Su-Galβ1-4(6-O-Su)Glcβ, GlcAβ1-3Galβ, Neu5Acα2-3Galβ1-4Glcβ, GlcNAcβ1-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ, Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ, Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ с помощью микрочипа с нанесенными на него указанными гликанами и, по наличию в крови уровня антител выше порогового одновременно ко всем указанным гликанам, диагностируют рак молочной железы. Предлагаемый способ позволяет улучшить чувствительность и специфичность диагностики рака молочной железы. 1 ил., 1 табл., 1 пр.
Способ диагностики рака молочной железы, заключающийся в том, что в крови человека детектируют антитела, направленные к следующим гликанам: Manβ1-4GlcNAcβ, Galβ1-4GlcNAcβ1-6(Galβ1-3)GalNAcα, НОСН2(НОСН)4CH2NH2, GlcAβ, Galα, 6-O-Su-GlcNAcβ, GalNAcβ1-3Galβ, 6-O-Su-Galβ1-4(6-O-Su)Glcβ, GlcAβ1-3Galβ, Neu5Acα2-3Galβ1-4Glcβ, GlcNAcβ1-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3GalNAcα, Neu5Acα2-3Galβ1-3(Fucα1-4)GlcNAcβ, Galβ1-4GlcNAcβ1-3(GlcNAcβ1-6)Galβ1-4GlcNAcβ, Neu5Acα2-6(Galβ1-3)GlcNAcβ1-3Galβ1-4Glcβ с помощью микрочипа с нанесенными на него указанными гликанами и по наличию в крови уровня антител выше порогового одновременно ко всем указанным гликанам диагностируют рак молочной железы.
| US 2010075344 А1, 25.03.2010 | |||
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ И ПРЕДСКАЗАНИЯ РАКА И МОНИТОРИНГ ТЕРАПИИ РАКОВЫХ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2395090C2 |
| US 2007059769 А1, 15.03.2007 | |||
| ZHAO Р et al | |||
| Proteomic identification of glycosylphosphatidylinositol anchor-dependent membrane proteins elevated inbreast carcinoma | |||
| J Biol Chem | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2014-01-20—Публикация
2012-11-23—Подача